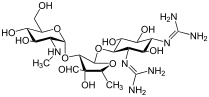
สเตรปโตมัยซิน
 | |
 | |
| ข้อมูลทางคลินิก | |
|---|---|
| AHFS/Drugs.com | โมโนกราฟ |
| ระดับความเสี่ยงต่อทารกในครรภ์ |
|
| ช่องทางการรับยา | ฉีดเข้ากล้ามเนื้อ, ฉีดเข้าหลอดเลือดดำ |
| รหัส ATC | |
| กฏหมาย | |
| สถานะตามกฏหมาย | |
| ข้อมูลเภสัชจลนศาสตร์ | |
| ชีวประสิทธิผล | 84% ถึง 88% ในกรณีฉีดเข้ากล้ามเนือ (ประมาณ)[1] 0% โดยการรับประทาน |
| ครึ่งชีวิตทางชีวภาพ | 5 ถึง 6 ชั่วโมง |
| การขับออก | ไต |
| ตัวบ่งชี้ | |
| |
| เลขทะเบียน CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| NIAID ChemDB | |
| PDB ligand | |
| ECHA InfoCard | 100.000.323 |
| ข้อมูลทางกายภาพและเคมี | |
| สูตร | C21H39N7O12 |
| มวลต่อโมล | 581.574 g/mol g·mol−1 |
| แบบจำลอง 3D (JSmol) | |
| จุดหลอมเหลว | 12 องศาเซลเซียส (54 องศาฟาเรนไฮต์) |
| |
| |
| | |
สเตรปโตมัยซิน (อังกฤษ: Streptomycin) เป็นยาปฏิชีวนะชนิดหนึ่งในกลุ่มอะมิโนไกลโคไซด์ ซึ่งมีข้อบ่งใช้สำหรับรักษาโรคที่เกิดจากการติดเชื้อแบคทีเรียหลายชนิด[2] รวมถึง วัณโรค, การติดเชื้อ Mycobacterium avium complex, เยื่อบุหัวใจอักเสบ, บรูเซลโลสิส, การติดเชื้อแบคทีเรียสกุลเบอโคเดอเรีย, กาฬโรค, ไข้กระต่าย, และไข้หนูกัด[2] กรณีวัณโรคระยะแสดงอาการนั้นมักจะใช้สเตรปโตมัยซินร่วมกับไอโซไนอะซิด, ไรแฟมพิซิน, และไพราซินาไมด์[3] ยานี้สามารถบริหารยาได้โดยการฉีดเข้าหลอดเลือดดำและการฉีดเข้ากล้ามเนื้อ[2]
สเตรปโตมัยซินจัดเป็นยาในกลุ่มอะมิโนไกลโคไซด์[2] ซึ่งออกฤทธิ์ที่หน่วยย่อย 30 เอสของไรโบโซมแบคทีเรีย ทำให้แบคทีเรียนั้นๆไม่สามารถสร้างโปรตีนที่จำเป็นต่อการดำรงชีวิตและเพิ่มจำนวนได้ ส่งผลให้แบคทีเรียเซลล์นั้นๆตายไปในที่สุด[2] อาการไม่พึงประสงค์ที่พบได้บ่อยจากการได้รับการรักษาด้วยสเตรปโตมัยซิน ได้แก่ อาการรู้สึกหมุน, อาเจียน, อาการชาบริเวณผิว, ไข้, และมีผื่นคัน[2] การใช้ยานี้ในหญิงตั้งครรภ์อาจทำให้ทารกหูหนวกแต่กำเนิดได้[2] แต่การใช้ยานี้ในหญิงที่กำลังให้นมบุตรนั้นพบว่าค่อนข้างมีความปลอดภัย[3] ทั้งนี้ ไม่แนะนำให้ใช้สเตรปโตมัยซินในผู้ป่วยที่มีโรคกล้ามเนื้ออ่อนแรงชนิดร้าย เนื่องจากอาจทำให้อาการของโรคแย่ลงได้[3]
สเตรปโตมัยซินถูกค้นพบใน ค.ศ. 1943 จากเชื้อแบคทีเรีย Streptomyces griseus[4][5] โดยยานี้ได้ถูกจัดเป็นหนึ่งในรายการยาจำเป็นขององค์การอนามัยโลก (World Health Organization's List of Essential Medicines) ซึ่งเป็นรายการยาที่มีประสิทธิภาพและความปลอดภัยสูง และมีความสำคัญเป็นลำดับแรกของระบบสุขภาพพื้นฐานของประชาชนในประเทศต่างๆ[6] ราคาสำหรับการขายส่งของสเตรปโตมัยซินในประเทศกำลังพัฒนามีมูลค่าระหว่าง 0.38 – 4.39 ดอลลาร์สหรัฐ ต่อขนาดยาที่ต้องใช้ในหนึ่งวัน[7] ส่วนในสหรัฐอเมริกานั้น เฉพาะค่าใช้จ่ายของยาสเตรปโตมัยซินในการรักษาหนึ่งรอบนั้นมีมูลค่ามากกว่า 200 ดอลลาร์สหรัฐ[8]
การใช้ประโยชน์[แก้]
การใช้ประโยชน์ทางการแพทย์[แก้]
- เยื่อบุหัวใจอักเสบติดเชื้อ ที่มีสาเหตุมาจากเชื้อแบคทีเรียสกุลเอนเทอโรคอคคัส ในกรณีที่ไม่ตอบสนองต่อการรักษาด้วยเจนตามัยซิน
- วัณโรค โดยใช้ร่วมกับยาปฏิชีวนะชนิดอื่น ในกรณีวัณโรคระยะแสดงอาการ มักใช้สเตรปโตมัยซินร่วมกับไอโซไนอะซิด, ไรแฟมพิซิน, และไพราซินาไมด์[3] อย่างไรก็ตาม สเตรปโตมัยซินไม่ได้จัดเป็นการรักษาทางเลือกแรกในข้อบ่งใช้นี้ โดยจะสงวนไว้ในกรณีวัณโรคดื้อต่อยาปฏิชีวนะทางเลือกแรก เนื่องจากมีค่าใช้จ่ายด้านยาในการรักษาค่อนข้างสูง
- กาฬโรค (การติดเชื้อแบคทีเรียเยอซิเนีย แพสทิซ) เคยมีการใช้สเตรปโตมัยซินเป็นทางเลือกแรกสำหรับข้อบ่งใช้นี้ อย่างไรก็ตาม ในปัจจุบันมีเฉพาะองค์การอาหารและยาของสหรัฐอเมริกาเท่านั้นที่ให้รับรับรองให้มีการใช้สเตรปโตมัยซินสำหรับข้อบ่งใช้ข้างต้น
- ในการปศุสัตว์ สเตรปโตมัยซินถือว่าเป็นยาปฏิชีวนะทางเลือกแรกในการรักษาโรคติดเชื้อแบคทีเรียแกรมลบในสัตว์ขนาดใหญ่ เช่น ม้า, วัว, แกะ, และอื่นๆ โดยมักใช้ร่วมกับโพรเคน เบนซิลเพนิซิลลิน โดยการฉีดเข้ากล้ามเนื้อ
- การติดเชื้อไข้กระต่าย โดยส่วนใหญ่มักได้รับการรักษาด้วยสเตรปโตมัยซิน
โดยส่วนใหญ่แล้ว การบริหารยาสเตรปโตมัยซินนั้นจะนิยมใช้วิธีการฉีดเข้ากล้ามเนื้อ เนื่องจากหลายประเทศมีการจดทะเบียนเพียงรูปแบบเภสัชภัณฑ์ประเภทนี้เท่านั้น แต่ในบางพื้นที่นั้นอาจพบเห็นการใช้ยาดังกล่าวในรูปแบบการฉีดเข้าหลอดเลือดดำได้บ้างประปราย[1]
สารกำจัดศัตรูพืชและสัตว์[แก้]
สเตรปโตมัยซินเป็นยาปฏิชีวนะอีกชนิดหนึ่งที่ถูกนำมาใช้ในการเกษตรเพื่อเป็นสารกำจัดศัตรูพืชและสัตว์ ทั้งนี้ เพื่อฆ่าเชื้อแบคทีเรียที่เป็นอันตรายในวัตถุดิบเหล่านั้นก่อนนำมาใช้เพื่อการบริโภคในมนุษย์ โดยมีการใช้สเตรปโตมัยซินในการควบคุมโรคที่อาจเกิดขึ้นกับผลไม้, ผัก, เมล็ดพันธุ์, และไม้ประดับ แต่ที่พบเห็นการใช้ได้บ่อยที่สุดคือ การใช้สเตรปโตมัยซินเพื่อควบคุมโรคไหม้ไฟในต้นแอปเปิลและไม้ผลสกุลไพรัส (เช่น สาลี่, ลูกแพร์) อย่างไรก็ตาม สำหรับในทางการแพทย์แล้ว การใช้ยาปฏิชีวนะในกรณีดังกล่าวที่มากเกินจำเป็นมีความสัมพันธ์กับการเกิดการดื้อต่อยาปฏิชีวนะของแบคทีเรียหลายสายพันธุ์ได้ นอกจากนี้ยังมีการนำสเตรปโตมัยซินมาใช้ในการควบคุมการเจริญเติบโตของสาหร่ายสีเขียวแกมน้ำเงินในสระที่ปลูกไม้ประดับและพิพิธภัณฑ์สัตว์น้ำ[9] อย่างไรก็ตาม เนื่องจากเป็นที่ทราบกันดีว่ายาปฏิชีวนะบางขนานสามารถออกฤทธิ์ยับยั้งการเจริญเติบโตหรือฆ่าเซลล์ยูแคริโอตบางชนิดได้ แต่ในกรณีของสเตรปโตมัยซิยกลับไม่ได้เป็นเช่นนั้น โดยเฉพาะอย่างยิ่งฤทธิ์ในการต้านเชื้อราของยานี้ ซึ่งพบว่ามีผลต่อการเจริญเติบโตของเชื้อราน้อยมาก[10]
การเพาะเลี้ยงเซลล์[แก้]
ในการการเพาะเลี้ยงเซลล์นั้น จะมีการนำสเตรปโตมัยซินร่วมกับเพนิซิลลินมาใช้เป็นสารละลายยาปฏิชีวนะมาตรฐานเพื่อป้องกันการติดเชื้อแบคทีเรียของเซลล์ที่ถูกเพาะเลี้ยง
การแยกโปรตีนให้บริสุทธิ์[แก้]
เมื่อมีการสกัดแยกโปรตีนออกจากสารสกัดชีวภาพ อาจมีการเติมสเตรปโตมัยซินลงไปในสารละลายเพื่อกำจัดกรดนิวคลีอิกออกไป โดยสเตรปโตไมซินจะเข้าจับกับไรโบโซมและเกิดการตกตะกอนออกจากสารละลาย โดยวิธีการนี้ถูกนำมาใช้ในการกำจัดอาร์อาร์เอ็นเอ, เอ็มอาร์เอ็นเอ, หรือแม้กระทั่งดีเอ็นเอ ออกจากเซลล์โพรแคริโอต
ขอบเขตการออกฤทธิ์[แก้]
สเตรปโตมัยซินถูกนำมาใช้ทางคลินิกเพื่อรักษาวัณโรค โดยใช้ร่วมกับยาปฏิชีวนะชนิดอื่นๆ รวมไปถึงการใช้รักษาโรคเยื่อบุหัวใจอักเสบติดเชื้อที่เกิดจากการติดเชื้อแบคทีเรียที่ยังตอบสนองต่อยานี้ โดยค่าความเข้มข้นของสเตรปโตมัยซินต่ำสุดที่สามารถยับยั้งการเจริญเติบโตของเชื้อแบคทีเรียบางสายพันธุ์ ดังแสดงต่อไปนี้:[11][12]
- Mycobacterium tuberculosis: 1 μg/ml - 2 μg/ml
- Staphylococcus aureus: 4 μg/ml
อาการไม่พึงประสงค์[แก้]
อาการไม่พึงประสงค์จากการได้รับสเตรปโตมัยซินที่ต้องเฝ้าระวังและติดตามอย่างใกล้ชิดนั้นมีความคล้ายคลึงกับที่พบในยากลุ่มอะมิโนไกลโคไซด์ชนิดอื่นๆ ได้แก่ การเกิดพิษต่อไต และความเป็นพิษต่อหู[13] ซึ่งอาจทำให้เกิดการสูญเสียการได้ยินชั่วคราวหรือถาวรได้ นอกจากนี้ การที่ยาส่งผลกระทบต่อระบบประสาท อาจทำให้ผู้ป่วยสูญเสียการทรงตัว จากความผิดปกติของการทำงานของระบบเวสติบูลาร์ ซึ่งเป็นผลมาจากการเกิดพยาธิสภาพที่เส้นประสาทสมองคู่ที่ 8 (vestibulocochlear nerve) ซึ่งผู้ป่วยจะมีอาการได้ยินเสียงผิดปกติในหู, อาการรู้สึกหมุน, และอาการเซ หรือภาวะกล้ามเนื้อเสียสหการ นอกจากนี้การเป็นพิษต่อไตของยานี้อาจส่งผลรบกวนการวินิจฉัยโรคไตวายได้[14] ส่วนอาการไม่พึงประสงค์อื่นที่พบได้ทั่วไป แต่ไม่มีความรุนแรงมาก ได้แก่ อาการรู้สึกหมุน, อาเจียน, ชาบริเวณใบหน้า, ไข้, และผื่น ทั้งนี้การเกิดไข้และผื่นจากยาอาจเกิดจากการได้รับยาบ่อยเกินไป[2]
ทั้งนี้ ไม่แนะนำให้ใช้ยานี้ในหญิงตั้งครรภ์ เนื่องจากยาอาจก่อให้เกิดพิษแก่ตัวอ่อนได้[2] แต่ในหญิงให้นมบุตรนั้น สามารถใช้ยานี้ได้ เนื่องจากสเตรปโตมัยซินสามารถถูกขับออกทางน้ำนมได้น้อยมาก[3] นอกจากนี้ ผู้ป่วยที่มีโรคกล้ามเนื้ออ่อนแรงชนิดร้ายเป็นโรคร่วมไม่ควรได้รับการรักษาด้วยสเตรปโตมัยซิน เนื่องจากจะทำให้อาการทางกล้ามเนื้อของผู้ป่วยแย่ลงได้[3]
กลไกการออกฤทธิ์[แก้]
สเตรปโตมัยซินเป็นยาปฏิชีวนะที่ออกฤทธิ์ยับยั้งการสังเคราะห์โปรตีนของเซลล์แบคทีเรีย โดยยานี้จะเข้าจับกับหน่วยย่อย 30 เอสของไรโบโซมแบคทีเรีย ซึ่งจะส่งผลรบกวนการเข้าจับกันระหว่างฟอร์มิล–เมไธโอนิล–ทีอาร์เอ็นเอ กับหน่วยย่อย 30 เอสดังกล่าว[15] ทำให้การอ่านข้อมูลจากโคดอนผิดพลาด จนนำไปสู่การยับยั้งการสร้างโปรตีนที่จำเป็นต่อการดำรงชีวิตและการเพิ่มจำนวนของเซลล์ ส่งผลให้เซลล์แบคทีเรียนั้นๆตายไปในที่สุด อย่างไรก็ตาม กลไกการออกฤทธิ์โดยละเอียดของสเตรปโตมัยซินนั้นยังไม่เป็นที่ทราบแน่ชัด แต่คาดว่ายานี้จะป้องกันการจับตัวกันเป็น 70 เอสไรโบโซมของหน่วยย่อย 30 เอสและหน่วยย่อย 50 เอส และทำให้การแปลรหัสพันธุกรรมจากเอ็มอาร์เอ็นเอนั้นเกิดการผิดพลาด จนทำให้โปรตีนที่สร้างขึ้นมาเกิดการกลายพันธุ์แบบเฟรมชิฟท์ (frameshift mutation) และเป็นโปรตีนที่ไม่สามารถทำงานได้ ส่งผลให้เซลล์นั้นๆตายไป[16] โดยไรโบโซมในเซลล์ของมนุษย์นั้นมีโครงสร้างที่แตกต่างไปจากไรโบโซมที่พบในแบคทีเรีย ทำให้สเตรปโตมัยซินไม่มีผลต่อเซลล์มนุษย์ หากใช้ยาในขนาดและระยะเวลาที่เหมาะสม ทั้งนี้ ณ ความเข้นข้นต่ำๆ สเตรปโตมัยซินจะออกฤทธิ์เพียงแค่ยับยั้งการจเริญเติบโตของแบคทีเรียเท่านั้น โดยเหนี่ยวนำให้ไรโบโซมแปรรหัสพันธุกรรมจากเอ็มอาร์เอ็นเอผิดพลาด[17] สเตรปโตมัยซินเป็นยาปฏิชีวนะที่ออกฤทธิ์ครอบคลุมทั้งเชื้อแบคทีเรียแกรมบวกและแกรมลบ[18] จึงจัดได้ว่ายานี้เป็นยาปฏิชีวนะที่ออกฤทธิ์กว้างอีกชนิดหนึ่งที่มีประโยชน์อย่างมากในการรักษาโรคติดเชื้อแบคทีเรียชนิดต่างๆ
ประวัติการค้นพบ[แก้]
สเตรปโตมัยซินถูกค้นพบครั้งแรกเมื่อวันที่ 19 ตุลาคม ค.ศ. 1943 ในห้องปฏิบัติการของมหาวิทยาลัยรัทเกอร์ส โดยอัลเบิร์ต ชาตซ์ (Albert Schatz) นักศึกษาปริญญาเอกชาวอเมริกัน ซึ่งเป็นศิษย์ของเซลมัน แวกส์มัน ในโครงการวิจัยที่ได้รับงบประมาณสนับสนุนจากบริษัทเมอร์ค[19][20] ในการศึกษาวิจัยครั้งนี้ แวกส์มันและเจ้าหน้าที่ประจำห้องปฏิบัติการของเขาได้ค้นพบยาปฏิชีวนะหลายนิด ได้แก่ แอคติโนมัยซิน , คลาวาซิน, สเตรปโตธริซิน, กริซีอิน, ฟราดิซิน, นีโอมัยซิน, แคนดิซิดิน, และแคนดิดิน ในจำนวนนี้มีเพียงสเตรปโตมัยซินและนีโอมัยซินเท่านั้นที่พบว่ามีประสิทธิภาพในการรักษาโรคที่เกิดจากการติดเชื้อแบคทีเรียได้หลายชนิด โดยสเตรปโตมัยซินถือเป็นยาปฏิชีวนะชนิดแรกที่สามารถใช้รักษาวัณโรคให้หายขาดได้ และทำให้แวกส์มันได้รับรางวัลโนเบลสาขาสรีรวิทยาหรือการแพทย์ ในปี ค.ศ. 1952 ในฐานะที่เป็นผู้ค้นพบสเตรปโตมัยซิน ซึ่งถือเป็นยาปฏิชีวนะชนิดแรกที่ใช้ในการรักษาวัณโรคระยะแสดงอาการ[21] ต่อมาแวกส์มันได้รับการกล่าวโทษจาก อัลเบิร์ต ชาตซ์ ซึ่งเป็นนักศึกษาที่ทำโครงการดังกล่าวภายใต้การควบคุมดูแลของเขา ว่าตนควรมีส่วนร่วมกับสิ่งที่แวกส์มันได้จากการค้นพบสเตรปโตมัยซินในครั้งนี้[22][23][24][25]
ในช่วงหลังสิ้นสุดสงครามโลกครั้งที่ 2 กองทัพบกสหรัฐได้ทำการทดลองเกี่ยวกับการใช้สเตรปโตมัยซินในการรักษาโรคติดเชื้อแบคทีเรียที่รุนแรงจนเสี่ยงอันตรายแก่ชีวิตในโรงพยาบาลทหารที่เมืองแบตเทิลครีก, รัฐมิชิแกน ผู้ป่วยรายแรกที่ได้รับการรักษาด้วยสเตรปโตมัยซินนั้นได้เสียชีวิตลง ส่วนผู้ป่วยรายที่สองรอดชีวิตแต่ตาบอดจากอาการไม่พึงประสงค์ของสเตรปโตมัยซิน ในเดือนมีนาคม ค.ศ. 1946 ผู้ป่วยรายที่ 3 —โรเบิร์ต เจ. โดล ซึ่งได้รับบาดเจ็บอย่างสาหัสจากการสู้รบในสงครามโลกครั้งที่ 2 ที่เมืองคาสเติลดายาโน[26] หลังจากล้มเหลวจากการรักษาภาวะติดเชื้อด้วยเพนิซิลลิน เขาได้รับการรักษาต่อด้วยสเตรปโตมัยซิน และสามารถหายเป็นปกติได้ภายในระยะเวลาอันรวดเร็ว ซึ่งต่อมาเขาได้เป็นผู้ดำรงตำแหน่งประธานวุฒิสภาสหรัฐ และเป็นหนึ่งในผู้ท้าชิงตำแหน่งประธานาธิบดีสหรัฐปี ค.ศ. 1996 [27][28]
จากนั้นได้มีการทำการศึกษาแบบสุ่มแรกของสเตรปโตมัยซินซึ่งใช้ในการรักษาวัณโรคปอด ซึ่งดำเนินการศึกษาในช่วง ค.ศ. 1946 ถึง 1948 โดยสภาวิจัยทางการแพทย์ (Medical Research Council) ของสหราชอาณาจักร ภายใต้การควบคุมของ Geoffrey Marshall (1887–1982) โดยการศึกษานี้เป็นแบบการทดลองแบบสุ่มและมีกลุ่มควบคุมและมีการปกปิดทั้งสองด้าน[29] โดยผลการศึกษาพบว่า สเตรปโตมัยซินมีประสิทธิภาพในการต้านวัณโรค แม้ว่าจะมีอาการไม่พึงประสงค์เกิดขึ้นแต่ก็มีเพียงเล็กน้อย และพบปัญหาการดื้อต่อสเตรปโตมัยซินบ้างในสัดส่วนที่น้อย[30]
เนื่องจากสเตรปโตมัยซินนั้นแยกได้จากเชื้อจุลินทรีย์ในตัวอย่างดินที่ได้มาจากรัฐนิวเจอร์ซีย์ ทำให้ S. griseus ซึ่งเป็นแบคทีเรียที่มาของสเตรปโตมัยซิน ได้รับการเสนอให้เป็นเชื้อจุลินทรีย์สัญลักษณ์ของรัฐนิวเจอร์ซีย์อย่างเป็นทางการ โดยร่างกฎหมายนี้ได้รับการส่งเข้าวาระการประชุมโดยวุฒิสภา แซม ธอมพ์สัน (Senator Sam Thompson) (R-12) ในเดือนพฤษภาคม ค.ศ. 2017 ในวาระการประชุมที่ S3190 และสมาชิกสภาผู้แทนราษฎร แอนเนตต์ ควิจาโน (Annette Quijano) (D-20) ในเดือนมิถุนายน ค.ศ. 2017 ในวาระการประชุมที่ A31900.[31][32]
อ้างอิง[แก้]
- ↑ 1.0 1.1 Zhu M, Burman WJ, Jaresko GS, Berning SE, Jelliffe RW, Peloquin CA (October 2001). "Population pharmacokinetics of intravenous and intramuscular streptomycin in patients with tuberculosis". Pharmacother. 21 (9): 1037–1045. doi:10.1592/phco.21.13.1037.34625. PMID 11560193. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-10-05. สืบค้นเมื่อ 2010-05-25.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 2.7 2.8 "Streptomycin Sulfate". The American Society of Health-System Pharmacists. เก็บจากแหล่งเดิมเมื่อ 20 December 2016. สืบค้นเมื่อ 8 December 2016.
- ↑ 3.0 3.1 3.2 3.3 3.4 3.5 WHO Model Formulary 2008 (PDF). World Health Organization. 2009. pp. 136, 144, 609. ISBN 9789241547659. เก็บ (PDF)จากแหล่งเดิมเมื่อ 13 December 2016. สืบค้นเมื่อ 8 December 2016.
- ↑ Torok, Estee; Moran, Ed; Cooke, Fiona (2009). Oxford Handbook of Infectious Diseases and Microbiology (ภาษาอังกฤษ). OUP Oxford. p. Chapter 2. ISBN 9780191039621. เก็บจากแหล่งเดิมเมื่อ 2017-09-08.
- ↑ Renneberg, Reinhard; Demain, Arnold L. (2008). Biotechnology for Beginners (ภาษาอังกฤษ). Elsevier. p. 103. ISBN 9780123735812. เก็บจากแหล่งเดิมเมื่อ 2017-09-10.
- ↑ "WHO Model List of Essential Medicines (19th List)" (PDF). World Health Organization. April 2015. เก็บ (PDF)จากแหล่งเดิมเมื่อ 13 December 2016. สืบค้นเมื่อ 8 December 2016.
- ↑ "Streptomycin Sulfate". International Drug Price Indicator Guide. สืบค้นเมื่อ 8 December 2016.[ลิงก์เสีย]
- ↑ Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. p. 36. ISBN 9781284057560.
- ↑ Qian, H., Li, J., Pan, X., Sun, Z., Ye, C., Jin, G., & Fu, Z. (2012). "Effects of streptomycin on growth of algae Chlorella vulgaris and Microcystis aeruginosa". Environmental Toxicology. 27 (4): 229–237.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Reilly, H. C., Schatz, A., & Waksman, S. A. (1945). "Antifungal properties of antibiotic substances". Journal of Bacteriology,. 49 (6): 585–594. เก็บจากแหล่งเดิมเมื่อ 2017-09-10.
{{cite journal}}: CS1 maint: extra punctuation (ลิงก์) CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Archived copy". เก็บจากแหล่งเดิมเมื่อ 2014-03-03. สืบค้นเมื่อ 2014-03-03.
{{cite web}}: CS1 maint: archived copy as title (ลิงก์) - ↑ http://www.toku-e.com/Assets/MIC/Streptomycin%20sulfate.pdf
- ↑ "Archived copy". เก็บจากแหล่งเดิมเมื่อ 2017-01-06. สืบค้นเมื่อ 2017-01-05.
{{cite web}}: CS1 maint: archived copy as title (ลิงก์) - ↑ Syal K, Srinivasan A, Banerjee D (2013). "Streptomycin interference in Jaffe reaction — Possible false positive creatinine estimation in excessive dose exposure". Clinical Biochemistry. 46: 177–179.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Sharma D, Cukras AR, Rogers EJ, Southworth DR, Green R (7 December 2007). "Mutational analysis of S12 protein and implications for the accuracy of decoding by the ribosome". Journal of Molecular Biology. 374 (4): 1065–76. doi:10.1016/j.jmb.2007.10.003. PMC 2200631. PMID 17967466.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Raymon, Lionel P. (2011). COMLEX Level 1 Pharmacology Lecture Notes. Miami, FL: Kaplan, Inc. p. 181. CM4024K.
- ↑ Voet, Donald & Voet, Judith G. (2004). Biochemistry (3rd ed.). John Wiley & Sons. p. 1341. ISBN 0-471-19350-X.
- ↑ Jan-Thorsten Schantz; Kee-Woei Ng (2004). A manual for primary human cell culture. World Scientific. p. 89.
- ↑ Comroe JH Jr (1978). "Pay dirt: the story of streptomycin. Part I: from Waksman to Waksman". American Review of Respiratory Disease. 117 (4): 773–781. PMID 417651.
- ↑ Kingston W (July 2004). "Streptomycin, Schatz v. Waksman, and the balance of credit for discovery". J Hist Med Allied Sci. 59 (3): 441–62. doi:10.1093/jhmas/jrh091. PMID 15270337.
- ↑ Official list of Nobel Prize Laureates in Medicine เก็บถาวร 2017-06-09 ที่ เวย์แบ็กแมชชีน
- ↑ Wainwright, M. (1990). Miracle Cure: The Story of Penicillin and the Golden Age of Antibiotics. Blackwell. ISBN 9780631164920. เก็บจากแหล่งเดิมเมื่อ 2017-09-10. สืบค้นเมื่อ 2014-12-29.
- ↑ Wainwright, M. (1991). "Streptomycin: discovery and resultant controversy". Journal of the History and Philosophy of the Life Sciences. 13: 97–124.
- ↑ Kingston, William (2004-07-01). "Streptomycin, Schatz v. Waksman, and the balance of credit for discovery". Journal of the History of Medicine and Allied Sciences. 59 (3): 441–462. doi:10.1093/jhmas/jrh091. ISSN 0022-5045. PMID 15270337.
- ↑ Pringle, Peter (2012). Experiment Eleven: Dark Secrets Behind the Discovery of a Wonder Drug. New York: Walker & Company. ISBN 978-1620401989.
- ↑ ""Losing the War" by Lee Sandlin". Leesandlin.com. สืบค้นเมื่อ 2010-06-17.
- ↑ Dole, B. One Soldier's Story, pp. 202–04.
- ↑ Cramer, Richard Ben, What It Takes (New York, 1992), pp. 110-11.
- ↑ Metcalfe NH (February 2011). "Sir Geoffrey Marshall (1887-1982) : respiratory physician, catalyst for anaesthesia development, doctor to both Prime Minister and King, and World War I Barge Commander". J Med Biogr. 19 (1): 10–4. doi:10.1258/jmb.2010.010019. PMID 21350072.
- ↑ D'Arcy Hart P (August 1999). "A change in scientific approach: from alternation to randomised allocation in clinical trials in the 1940s". British Medical Journal. 319 (7209): 572–3. doi:10.1136/bmj.319.7209.572. PMC 1116443. PMID 10463905.
- ↑ "New Jersey S3190 | 2016-2017 | Regular Session". LegiScan (ภาษาอังกฤษ). สืบค้นเมื่อ 2017-11-29.
- ↑ "New Jersey A4900 | 2016-2017 | Regular Session". LegiScan (ภาษาอังกฤษ). สืบค้นเมื่อ 2017-11-29.
แหล่งข้อมูลอื่น[แก้]
- "Notebooks Shed Light on an Antibiotic's Contested Discovery," New York Times, June 12, 2012, by Peter Pringle
- Streptomycin bound to proteins ใน ธนาคารข้อมูลโปรตีน
- Kingston, William (2004). "Streptomycin, Schatz v. Waksman, and the Balance of Credit for Discovery". Journal of the History of Medicine and Allied Sciences. 59 (3): 441–462. doi:10.1093/jhmas/jrh091. PMID 15270337.
- Mistiaen, Veronique (2 November 2002). "Time, and the great healer". The Guardian.. The history behind the discovery of streptomycin.
- EPA R.E.D. Facts sheet on use of streptomycin as a pesticide.
