นีโอมัยซิน
 | |
 | |
| ข้อมูลทางคลินิก | |
|---|---|
| ชื่อทางการค้า | Neo-rx, Neocin, Myneocin |
| AHFS/Drugs.com | Neomycin (Systemic) |
| MedlinePlus | a682274 |
| ระดับความเสี่ยงต่อทารกในครรภ์ |
|
| ช่องทางการรับยา | ยาใช้ภายนอก, รับประทาน |
| รหัส ATC | |
| กฏหมาย | |
| สถานะตามกฏหมาย |
|
| ข้อมูลเภสัชจลนศาสตร์ | |
| ชีวประสิทธิผล | ไม่มี |
| การจับกับโปรตีน | N/A |
| การเปลี่ยนแปลงยา | N/A |
| ครึ่งชีวิตทางชีวภาพ | 2–3 ชั่วโมง |
| ตัวบ่งชี้ | |
| |
| เลขทะเบียน CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| ECHA InfoCard | 100.014.333 |
| ข้อมูลทางกายภาพและเคมี | |
| สูตร | C23H46N6O13 |
| มวลต่อโมล | 614.650 g·mol−1 |
| แบบจำลอง 3D (JSmol) | |
| |
| |
| | |
นีโอมัยซิน (อังกฤษ: Neomycin) เป็นยาปฏิชีวนะกลุ่มอะมิโนไกลโคไซด์ มีจำหน่ายในท้องตลาดในหลายรูปแบบเภสัชภัณฑ์ เช่น ยารับประทาน ครีม ขี้ผึ้งและยาหยอดยา นีโอมัยซินถูกค้นพบในปี ค.ศ. 1949 ในห้องปฏิบัติการของเซลมัน แวกส์มัน โดยถูกจัดให้เป็นยาปฏิชีวนะที่อยู่ในกลุ่มอะมิโนไกลโคไซด์ ซึ่งมีโครงสร้างที่มีลักษณะเป็นน้ำตาลอะมิโน (Amino sugars) อย่างน้อย 2 โมเลกุลเชื่อมต่อกันด้วยพันธะไกลโคไซด์ (glycosidic bond)
การใช้ประโยชน์ทางการแพทย์[แก้]
โดยส่วนใหญ่แล้วนีโอมัยซินจะถูกนำมาใช้ในรูปแบบยาใช้ภายนอก เช่น นีโอสปอริน อย่างไรก็ตาม ยานี้สามารถบริหารยาโดยการรับประทานได้ แต่จำเป็นต้องใช้ร่วมกับยาปฏิชีวนะอื่น นีโอมัยซินเป็นยาปฏิชีวนะที่ไม่ถูกดูดซึมในระบบทางเดินอาหาร และถูกนำมาใช้เพื่อเป็นการป้องกันโรคสมองจากตับ (hepatic encephalopathy) และภาวะสารไขมันสูงในเลือด (hypercholesterolemia) เนื่องจากการที่นีโอมัยซินออกฤทธิ์ฆ่าเชื้อแบคทีเรียในทางเดินอาหาร จะส่งผลให้ระดับแอมโมเนียในร่างกายต่ำลง จึงช่วยป้องกันการเกิดโรคสมองจากตับได้ โดยเฉพาะการให้ยาก่อนการผ่าตัดอวัยวะทางเดินอาหาร นอกจากนี้แล้ว นีโอมัยซินยังออกฤทธิ์ครอบคลุมเชื้อแบคทีเรียที่ดื้อต่อสเตรปโตมัยซิน ซึ่งเป็นยาหลักอีกชนิดหนึ่งที่ใช้ในการรักษาวัณโรค[1] และเคยมีการใช้นีโอมัยซินในการรักษาภาวะที่เชื้อแบคทีเรียในลำไส้เล็กมีการเจริญเติบโตมากเกินไป (small intestinal bacterial overgrowth) ทั้งนี้ นีโอมัยซินไม่มีในรูปแบบยาที่ใช้สำหรับการฉีดเข้าหลอดเลือดดำ เนื่องจากตัวยามีพิษต่อไตสูงเป็นอย่างมาก เมื่อเทียบกับสารกลุ่มอะมิโนไกลโคไซด์อื่น ๆ อย่างไรก็ตาม ปัจจุบันมีการผสมนีโอมัยซินปริมาณเล็กน้อยในวัคซีนชนิดฉีดบางชนิด เพื่อจุดประสงค์ในการเป็นสารกันเสีย โดยขนาดยาที่ผู้ฉีดวัคซีนจะได้รับในกรณีนี้อยู่ที่ประมาณ 25 μg ต่อการฉีดวัคซีนนั้นหนึ่งครั้ง[2]
อณูชีววิทยา[แก้]
การดื้อต่อยานีโอมัยซินของแบคทีเรียนั้นจะเกิดผ่านยีนที่ควบคุมการสร้างเอนไซม์อะมิโนไกลโคไซด์ฟอสโฟทรานส์เฟอเรส (aminoglycoside phosphotransferase หรือ Kanamycin kinase) จำนวน 1 – 2 ยีน[3] ในปัจจุบัน ยีนที่มีชื่อว่า neo ซึ่งส่วนใหญ่จะถูกใส่เข้าไปอยู่ในพลาสมิด (Plasmid) ซึ่งเป็นสารพันธุกรรมที่อยู่นอกโครโมโซม (extrachromosomal DNA) มักถูกใช้โดยนักอณูชีววิทยาเพื่อเพาะเลี้ยงเซลล์สายพันธุ์ของสัตว์เลี้ยงลูกด้วยน้ำนมที่คงทนต่อยาปฏิชีวนะเพื่อจุดประสงค์ในการทดลองสร้างสารโปรตีนบางชนิด พลาสมิดที่ถูกผลิตขึ้นเพื่อสร้างโปรตีนเชิงการค้าในปัจจุบันมีหลายชนิดที่มียีน neo เป็นยีนบ่งชี้ (selectable marker) โดยเซลล์ที่ไม่มีส่วนประกอบของยีนนี้ (Non-transfected cells) จะตายในการเพาะเลี้ยงเมื่อสัมผัสกับนีโอมัยซินหรือยาปฏิชีวนะอื่นที่เทียบเคียงกันได้ โดยนีโอมัยซินหรือกานามัยซินจะถูกใช้ในการเพาะเลี้ยงเซลล์กลุ่มโพรแคริโอต ส่วนเซลล์ยูแคริโอตนั้นจะใช้จีนีติซิน (G418)
นีโอมัยซินออกฤทธิ์โดยจับกับหน่วยย่อย 30 เอสของไรโบโซม ซึ่งจะส่งผลยับยั้งการแปรรหัสของเอ็มอาร์เอ็นเอ[4] นอกจากนี้นีโอมัยซินยังมีความจำเพาะในการจับกับ phosphatidylinositol 4,5-bisphosphate (PIP2) สูงมาก ซึ่งสารฟอสโฟลิพิดดังกล่าวเป็นส่วนประกอบที่สำคัญของเยื่อหุ้มเซลล์[5]
ชีวสังเคราะห์[แก้]
นีโฮมัยซินถูกแยกจากเชื้อแบคทีเรีย Streptomyces fradiae และ Streptomyces albogriseus ได้เป็นครั้งแรกในปี ค.ศ. 1949 (NBRC 12773)[6] โดยเป็นยาที่เป็นส่วนผสมของนีโอมัยซินบี (neomycin B หรือ framycetin) และอิพิเมอร์ (Epimers) ของมัน คือ นีโอมัยซินซี ซึ่งมีอยู่ประมาณร้อยละ 5 – 15 ของมวลทั้งหมด โดยทั้งสองสารเป็นสารสำคัญในสารผสมนีโอมัยซินที่ออกฤทธิ์ได้ดีในสภาวะที่เป็นด่าง[7] นีโอมัยซินละลายน้ำได้ดีแต่ไม่ละลายในตัวทำละลายอินทรีย์[8] ทั้งนี้ นีโอมัยซินออกฤทธิ์ต้านเชื้อแบคทีเรียได้ทั้งแกรมบวกและแกรมลบ แต่ด้วยการเกิดพิษต่อระบบการได้ยินที่เกิดได้ในอัตราที่สูงมาก จึงทำให้มีการจำกัดการใช้ยานี้ในรูปแบบยาใช้ภายนอกและยาที่ใช้สำหรับฆ่าเชื้อแบคทีเรียในช่องปากและทางเดินอาหารเท่านั้น[9]
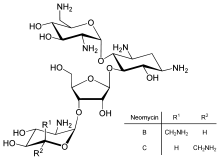
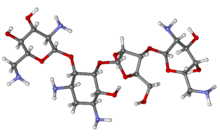
นีโอมัยซินบี (Neomycin B) มีโครงสร้างที่ประกอบด้วย 4 ส่วนเชื่อมต่อกันด้วยพันธะไกลโคไซด์ (glycosidic bond) ได้แก่ D-neosamine, 2-deoxystreptamine (2-DOS), D-ribose และ L-neosamine
นีโอมัยซินเอ หรือเรียกอีกชื่อหนึ่งว่า นีเอมีน (neamine) ซึ่งมีส่วนประกอบของวง D-neosamine และ 2-deoxystreptamine ถูกสร้างจากยีนจำนวน 6 ยีน คือ ยีน DOIS (btrC, neo7) ; ยีน L-glutamine:DOI aminotransferase (btrS, neo6) ; ยีน putative glycosyltransferase (btrM, neo8) ; ยีน putative aminotransferase (btrB, neo18) ซึ่งควบคุมการสร้างเอนไซม์ glutamate-1-semialdehyde 2,1- aminomutase ด้วย; ยีน putative alcohol dehydrogenase (btrE, neo5) ; และยีน putative dehydrogenase อื่น ๆ (btrQ, neo11) ซึ่งทำหน้าที่ควบคุมการสร้างเอนไซม์ Choline dehydrogenase และฟลาโวโปรตีนที่เกี่ยวข้องด้วย[10] ส่วนเอนไซม์ที่ทำหน้าที่ในควบคุมการเกิดปฏิกิริยาดีแอซิติลเลชัน (deacetylation) เพื่อนำหมู่อะซิติลออกจาก N-acetylglucosamine ของยากลุ่มอะมิโนไกลโคไซด์ นั้น (Neo16) ยังไม่ทราบแน่ชัด (ลำดับพันธุกรรมคล้ายคลึงกับ BtrD)[11]
ส่วนการเข้าจับของน้ำตาล D-ribose ระหว่างการเกิดปฏิกิริยาไรโบซิเลชัน (ribosylation) ของนีเอมีนนั้น จะใช้ 5-phosphoribosyl-1-diphosphate (PRPP) เป็นตัวให้หมู่ไรโบซิล (BtrL, BtrP) ;[12] ซึ่งควบคุมกระบวนการนี้โดยยีน glycosyltransferase (potential homologues RibF, LivF, Parf) (Neo15)[13]
นีโอซามีนบี (Neosamine B หรือ L-neosamine B) ซึ่งมีโครงสร้างที่คล้ายคลึงกับนีโอซามีนซี (neosamine C หรือ D-niosamine) เป็นอย่างมาก แต่กระบวนการสังเคราะห์นั้นจำเป็นที่จะต้องมีปฏิกิริยาการเกิดอิพิเมอร์ (epimerization) เพิ่มขึ้นมาอีก 1 ขั้นตอน เพื่อสร้างนีโอซามีนบีที่เป็นอิพิเมอร์กับนีโอมัยซินบี[14]
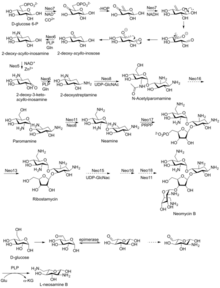
นีโอมัยซินซีสามารถสังเคราะห์ได้จากการผลิตไรบอสตามัยซิน[15]
ขอบเขตการออฤทธิ์[แก้]
ขอบเขตการออกฤทธิ์ของนีโอมัยซินนั้นมีความคล้าบคลึงกันกับยาปฏิชีวนะในกลุ่มอะมิโนไกลโคไซด์ ซึ่งออกฤทธิ์ต้านเชื้อแบคทีเรียแกรมลบได้เป็นอย่างดีอื่น ๆ นอกจากนี้ยังสามารถออกฤทธิ์ต่อแบคทีเรียแกรมบวกได้บางสายพันธุ์ ยานี้มีความสัมพันธ์กับการเกิดอาการพิษในมนุษย์ โดยมีรายงานการเกิดปฏิกิริยาการแพ้ยาอยู่บ่อยครั้ง[16] ในบางครั้งแพทย์จึงไม่ใช้ยาปฏิชีวนะรูปแบบครีมที่มีส่วนผสมของนีโอมัยซิน เช่น พอลีสปอรีน ซึ่งเป็นสูตรผสมระหว่างบาซิตราซิน และพอลีมัยซินบี และ/หรือเจนตามัยซิน หรือกรามิซิดีน[17] เชื้อแบคทีเรียแกรมลบสำคัญทางการแพทย์ที่ตอบสนองต่อการรักษาด้วยนีโอมัยซินได้ดี ได้แก่ Enterobacter cloacae, Escherichia coli และ Proteus vulgaris ซึ่งมีค่าความเข้มข้นของยาในระดับต่ำสุด (ในหลอดทดลอง) ที่สามารถยับยั้งการเจริญเติบโตของเชื้อแบคทีเรียได้ (Minimum Inhibitory Concentration; MIC) คือ >16 μg/ml, 1 μg/ml, และ 0.25 μg/ml ตามลำดับ[18]
ส่วนประกอบ[แก้]
นีโอมัยซินสูตรที่ได้มาตรฐานนั้นจะประกอบไปด้วยสารประกอบที่เกี่ยวเนื่องหลายชนิด ได้แก่ นีโอมัยซินเอ (หรือนีเอมีน – Neamine), นีโอมัยซินบี (หรือฟรามัยซีติน – framycetin), นีโอมันซินซี, และสารประกอบอื่นอีกหลายชนิดในสัดส่วนที่ค่อนข้างน้อย โดยในสารประกอบทั้งหมดที่เป็นส่วนผสมของนีโอมัยซินนี้พบว่า นีโอมัยซินบี เป็นสารที่มีปริมาณมากที่สุด รองลงมาคือ นีโอมัยซินเอ โดยนีโอมัยซินเอเป็นสารที่ไม่ออกฤทธิ์ที่เกิดจากการเสื่อมสลาย (inactive degradation product) ของนีโอมัยซินซี และบีไอโซเมอร์[19] จำนวนและสัดส่วนของสารที่เป็นส่วนประกอบของนีโอมัยซินจะมีความแตกต่างกันในแต่ละรอบของการผลิตขึ้นอยู่กับผู้ผลิตและกระบวนการที่ใช้ในการผลิต[20]
ความปลอดภัย[แก้]
ในปี ค.ศ. 2005 – 2006 นีโอมัยซินเป็นยาลำดับที่ 5 ที่ก่อให้เกิดปฏิกิริยาการแพ้ได้มากที่สุดในการทำแพ็ทเทสต์ (ร้อยละ 10.0)[21] อาการไม่พึงประสงค์อื่นของนีโอมัยซินอาจเกิดขึ้นได้นั้นไม่แตกต่างไปจากยาปฏิชีวนะชนิดอื่นที่อยู่ในกลุ่มอะมิโนไกลโคไซด์ โดยนีโอมัยซินสามารถก่อให้เกิดพิษต่อระบบการได้ยิน (ototoxicity) ทำให้เกิดเสียงดังในหูที่ผิดปกติ (tinnitus), สูญเสียการได้ยิน, และเกิดความผิดปกติของ Vestibular system แต่อาการไม่พึงประสงค์ดังข้างต้นที่กล่าวมานั้นเกิดได้ค่อนข้างน้อย ผู้ป่วยที่มีเสียงดังในหูผิดปกติ หรือมีภาวะประสาทหูเสื่อม (sensorineural hearing loss) อยู่ก่อนแล้ว ควรแจ้งแพทย์ให้ทราบก่อนการใช้ยานี้
ประวัติการค้นพบ[แก้]
นีโอมัยซินถูกค้นพบในปี ค.ศ. 1949 โดยนักชีวเคมีและนักจุลชีววิทยาชาวอเมริกันเชื้อสายยิวชื่อ เซลมัน แวกส์มัน และ ฮิวเบิร์ต เลเชอวาลิเออร์ (Hubert Lechevalier) ในห้องปฏิบัติการของมหาวิทยาลัยรัทเกอร์ (Rutgers University) ทั้งนี้ นีโอมัยซินนั้นถูกสร้างขึ้นได้ตามธรรมชาติโดยเชื้อแบคทีเรีย Streptomyces fradiae[22] โดยกระบวนการการสังเคราะห์จำเป็นอาศัยอาหารเพาะเลี้ยงเชื้อที่จำเพาะและในอยู่สภาวะไร้ออกซิเจน[23]
กลไกการออกฤทธิ์[แก้]
เป็นที่รู้กันดีว่ายาปฏิชีวนะในกลุ่มอะมิโนไกลโคไซด์อย่างนีโอมัยซินนั้นมีความสามารถจับกับอาร์เอ็นเอสายคู่ได้ด้วยความจำเพาะที่ค่อนข้างสูง[24] โดยค่าคงที่การแตกตัว (dissociation constant, Kd) ของนีโอมัยซินต่อตำแหน่ง A-site บนอาร์เอ็นเออยู่ที่ช่วงประมาณ 109 M−1[25] อย่างไรก็ตาม ตั้งแต่มีการค้นพบนีโอมัยซินมาเป็นระยะเวลามากกว่า 50 ปี กลไกการจับกับดีเอ็นเอของนีโอมัยซินนั้นก็ยังไม่สามารถทราบได้แน่ชัดเท่าใดนัก โดยพบว่านีโอมัยซินนั้นมีผลเพิ่มการคงสภาพทางความร้อนของ Triple-stranded DNA โดยไม่มีผลหรือมีผลบ้างเล็กน้อยต่อการคงสภาพของ B-DNA duplex[26] นอกจากนี้นีโอมัยซินยังมีความสามารถจับกับโครงสร้างอื่นที่คล้ายกับโครงสร้าง A-DNA ได้ ซึ่ง triplex DNA ก็เป็นหนึ่งในโครงสร้างเหล่านั้น ยิ่งไปกว่านั้น นีโอมัยซินยังสามารถเข้าจับเป็นสารประกอบเชิงซ้อนกับสารพันธุกรรมระหว่างการก่อตัวสายผสมสามสายของ DNA และ RNA (DNA:RNA hybrid triplex formation) ได้[27]
อ้างอิง[แก้]
- ↑ Hellman, L. M. "Neomycin, a New Antibiotic Active Against Streptomycin-Resistant Bacteria, Including Tuberculosis Organisms." American Journal of Obstetrics and Gynecology 58.6 (1949) : 1224. CrossRef. Web.
- ↑ Heidary, Noushin; Cohen, David E. (2005). "Hypersensitivity reactions to vaccine components". Dermatitis. 16 (3): 115–20. doi:10.1097/01206501-200509000-00004. PMID 16242081.
- ↑ "G418/neomycin-cross resistance?". สืบค้นเมื่อ 2008-10-19.
- ↑ Mehta, Roopal; Champney, W. Scott (2003). "Neomycin and Paromomycin Inhibit 30S Ribosomal Subunit Assembly in Staphylococcus aureus". Current Microbiology. 47 (3): 237–43. doi:10.1007/s00284-002-3945-9. PMID 14570276.
- ↑ Gabev, Eugene, et al. "Binding of Neomycin to Phosphatidylinositol 4,5-Biphosphate (PIP 2)." BBA − Biomembranes 979.1 (1989) : 105-12. CrossRef. Web.
- ↑ Waksman, Selman A.; Lechevalier, Hubert A.; Harris, Dale A. (1949). "Neomycin—Production and Antibiotic Properties 123". Journal of Clinical Investigation. 28 (5 Pt 1): 934–9. doi:10.1172/JCI102182. PMC 438928. PMID 16695766.
- ↑ Hellman, L. M. "Neomycin, a New Antibiotic Active Against Streptomycin-Resistant Bacteria, Including Tuberculosis Organisms." American Journal of Obstetrics and Gynecology 58.6 (1949) : 1224. CrossRef. Web.
- ↑ Hellman, L. M. "Neomycin, a New Antibiotic Active Against Streptomycin-Resistant Bacteria, Including Tuberculosis Organisms." American Journal of Obstetrics and Gynecology 58.6 (1949) : 1224. CrossRef. Web.
- ↑ Dewick, Paul M. (March 2009). Medicinal Natural Products: A Biosynthetic Approach (3rd ed.). Chichester, United Kingdom: John Wiley and Sons. pp. 508, 510, 511. ISBN 978-0-470-74168-9.
- ↑ Kudo, Fumitaka; Yamamoto, Yasuhito; Yokoyama, Kenichi; Eguchi, Tadashi; Kakinuma, Katsumi (2005). "Biosynthesis of 2-Deoxystreptamine by Three Crucial Enzymes in Streptomyces fradiae NBRC 12773". The Journal of Antibiotics. 58 (12): 766–74. doi:10.1038/ja.2005.104. PMID 16506694.
- ↑ Park, Je Won; Park, Sung Ryeol; Nepal, Keshav Kumar; Han, Ah Reum; Ban, Yeon Hee; Yoo, Young Ji; Kim, Eun Ji; Kim, Eui Min; Kim, Dooil; Sohng, Jae Kyung; Yoon, Yeo Joon (2011). "Discovery of parallel pathways of kanamycin biosynthesis allows antibiotic manipulation". Nature Chemical Biology. 7 (11): 843–52. doi:10.1038/nchembio.671. PMID 21983602.
- ↑ Kudo, Fumitaka; Fujii, Takuya; Kinoshita, Shunsuke; Eguchi, Tadashi (2007). "Unique O-ribosylation in the biosynthesis of butirosin". Bioorganic & Medicinal Chemistry. 15 (13): 4360–8. doi:10.1016/j.bmc.2007.04.040. PMID 17482823.
- ↑ Fan, Qingzhi; Huang, Fanglu; Leadlay, Peter F.; Spencer, Jonathan B. (2008). "The neomycin biosynthetic gene cluster of Streptomyces fradiae NCIMB 8233: Genetic and biochemical evidence for the roles of two glycosyltransferases and a deacetylase". Organic & Biomolecular Chemistry. 6 (18): 3306–14. doi:10.1039/B808734B. PMID 18802637.
- ↑ Llewellyn, Nicholas M.; Spencer, Jonathan B. (2006). "Biosynthesis of 2-deoxystreptamine-containing aminoglycoside antibiotics". Natural Product Reports. 23 (6): 864–74. doi:10.1039/B604709M. PMID 17119636.
- ↑ Kudo, Fumitaka, et al. "Enzymatic Preparation of Neomycin C from Ribostamycin." The Journal of Antibiotics 62.11 (2009) : 643-6. MEDLINE. Web.
- ↑ Vanessa Ngan (2002). "Allergy to neomycin". DermNet (ภาษาอังกฤษ). สืบค้นเมื่อ 2018-01-08.
- ↑ "Your Medicine Cabinet". DERMAdoctor.com, Inc. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2009-07-09. สืบค้นเมื่อ 2008-10-19.
- ↑ "Neomycin sulfate, EP Susceptibility and Minimum Inhibitory Concentration (MIC) Data" (PDF). TOKU-E.
- ↑ Cammack, R. Attwood, T. K. Campbell, P. N. Parish, J. H. Smith, A. D. Stirling, J. L. Vella, F. (2006). "Oxford Dictionary of Biochemistry and Molecular Biology (2nd Edition) – neomycin." Oxford University Press. (2006) : 453. Knovel.com. Web. 18 Nov. 2014.
- ↑ Tsuji, K; Robertson, J. H.; Baas, R; McInnis, D. J. (1969). "Comparative study of responses to neomycins B and C by microbiological and gas-liquid chromatographic assay methods". Applied microbiology. 18 (3): 396–8. PMC 377991. PMID 4907002.
- ↑ Zug, K. A.; Warshaw, E. M.; Fowler Jr, J. F.; Maibach, H. I.; Belsito, D. L.; Pratt, M. D.; Sasseville, D; Storrs, F. J.; Taylor, J. S.; Mathias, C. G.; Deleo, V. A.; Rietschel, R. L.; Marks, J (2009). "Patch-test results of the North American Contact Dermatitis Group 2005-2006". Dermatitis. 20 (3): 149–60. PMID 19470301.[ลิงก์เสีย]
- ↑ "The Nobel Prize in Physiology or Medicine 1952". Nobel Foundation. สืบค้นเมื่อ 2008-10-29.
- ↑ "Neomycin." Pharmaceutical Manufacturing Encyclopedia (3rd edition) Volume 3. (2007) : 2415–2416. Knovel.com. Web. 18 Nov. 2014.
- ↑ Jin, Yi; Watkins, Derrick; Degtyareva, Natalya N.; Green, Keith D.; Spano, Meredith N.; Garneau-Tsodikova, Sylvie; Arya, Dev P. (2016). "Arginine-Linked Neomycin B Dimers: Synthesis, rRNA Binding, and Resistance Enzyme Activity". MedChemComm. 7 (1): 164–169. doi:10.1039/C5MD00427F.
- ↑ Kaul, Malvika; Pilch, Daniel S. (2002). "Thermodynamics of Aminoglycoside−rRNA Recognition: The Binding of Neomycin-Class Aminoglycosides to the A Site of 16S rRNA". Biochemistry. 41 (24): 7695–706. doi:10.1021/bi020130f. PMID 12056901.
- ↑ Arya, Dev P; Coffee, R.Lane (2000). "DNA Triple Helix Stabilization by Aminoglycoside Antibiotics". Bioorganic & Medicinal Chemistry Letters. 10 (17): 1897–9. doi:10.1016/S0960-894X(00)00372-3. PMID 10987412.
- ↑ Arya, Dev P.; Coffee, R. Lane; Charles, I. (2001). "Neomycin-Induced Hybrid Triplex Formation". Journal of the American Chemical Society. 123 (44): 11093–4. doi:10.1021/ja016481j. PMID 11686727.
