แบคทีเรียดื้อยา

จุลชีพดื้อยา (อังกฤษ: Antimicrobial resistance; AMR) เป็นคำที่ใช้สื่อถึงจุลชีพที่มีความสามารถในการปรับตัวให้ทนต่อฤทธิ์ของยาต้านจุลชีพที่มีประสิทธิภาพในการรักษาโรคที่เกิดจากการติดเชื้อจุลชีพนั้น ๆ ในอดีต[2][3][4] โดยคำนี้สื่อความรวมถึง "แบคทีเรียดื้อยา" หรือ "แบคทีเรียดื้อต่อยาปฏิชีวนะ" (antibiotic resistance) ด้วย ซึ่งเป็นจุลชีพที่พบการดื้อยามากที่สุด[3] โดยการรักษาโรคที่เกิดจากการติดเชื้อจุลชีพที่ดื้อต่อยานั้นทำได้ค่อนข้างยาก จึงจำเป็นต้องมีการใช้ยาต้านจุลชีพในขนาดที่สูงกว่าปกติในการรักษา หรือต้องปรับเปลี่ยนแบบแผนการรักษาโดยใช้ยาทางเลือกรอง ซึ่งทำให้มีค่าใช้จ่ายในการรักษาที่สูงกว่าปกติ และมีความเสี่ยงที่อาจเกิดอาการไม่พึงประสงค์หรือการเกิดพิษได้มากกว่าการรักษาด้วยสูตรการรักษามาตรฐาน นอกจากนี้แล้ว การรักษาโรคที่เกิดจากการติดเชื้อจุลชีพดื้อยาดังกล่าวจะยิ่งทวีความยากลำบากในการรักษามากขึ้นหากเชื้อสาเหตุนั้นเกิดการดื้อยาต้านจุลชีพหลายชนิด (multiple drug resistance; MDR หรือ ซุปเปอร์บั๊ก)[5] ทั้งนี้ กลไกการดื้อยาของจุลชีพนั้นสามารถเกิดขึ้นได้ผ่าน 3 กลไกหลัก คือ การดื้อยาโดยธรรมชาติของจุลชีพสายพันธุ์นั้น ๆ, การกลายพันธุ์ หรือ การได้รับยีนดื้อยาจากสายพันธุ์หรือสเตรนอื่น[6] โดยจุลชีพสายพันธุ์ต่าง ๆ นั้นสามารถเกิดการกลายพันธุ์ได้ทั้งหมด ได้แก่ เชื้อราจะเกิดการดื้อต่อยาต้านเชื้อรา ไวรัสจะเกิดการดื้อต่อยาต้านไวรัส โพรโทซัวสามารถเกิดการต่อยาต้านโพรโทซัว และแบคทีเรียจะเกิดการดื้อต่อยาปฏิชีวนะ และการดื้อยานี้อาจเกิดขึ้นได้เองโดยธรรมชาติของจุลชีพซึ่งเป็นผลมาจากการกลายพันธุ์แบบสุ่ม[7]
การป้องกันการดื้อยาของแบคทีเรียนั้นสามารถกระทำได้หลายช่องทาง ได้แก่ ใช้ยาปฏิชีวนะเมื่อมีข้อบ่งใช้ที่เหมาะสม หยุดการใช้ยาปฏิชีวนะหรือยาต้านจุลชีพอื่นในทางที่ผิด[8][9] หากเป็นไปได้ให้พิจารณาใช้ยาปฏิชีวนะชนิดออกฤทธิ์แคบ (Narrow-spectrum antibiotics) แทนยาปฏิชีวนะชนิดออกฤทธิ์กว้าง (Board-spectrum antibiotics) เนื่องจากการใช้ยาปฏิชีวนะชนิดออกฤทธิ์แคบจะมีความจำเพาะต่อเชื้อสาเหตุและมีประสิทธิภาพมากกว่า ซึ่งจะช่วยลดความเสี่ยงของการเกิดการดื้อยาของจุลชีพได้[10] ในกรณีที่ต้องรับประทานยาเองที่บ้าน ผู้ใช้ยาควรมีความตระหนักรู้ถึงวิธีการใช้ยาที่เหมาะสม และความเสี่ยงที่อาจเกิดขึ้นได้จากการใช้ยาดังกล่าวนอกเหนือจากคำแนะนำของบุคลการทางการแพทย์ นอกจากนี้ บุคลากรทางการแพทย์ซึ่งมีโอกาสสัมผัสกับเชื้อจุลชีพต่าง ๆ ในการทำงานก็ถือเป็นภาคส่วนที่สำคัญที่จะช่วยลดการแพร่กระจายของแบคทีเรียดื้อยาได้ โดยการรักษาสุขอนามัยและการมีระบบการสุขาภิบาลที่ดีในสถานพยาบาล ซึ่งรวมไปถึงการล้างมือและการทำให้ปราศจากเชื้อ (disinfecting) ในระหว่างการสัมผัสผู้ป่วยแต่ละราย รวมไปถึงการให้ความรู้เพื่อกระตุ้นความตระหนักรู้ในประเด็นดังกล่าวแก่ผู้ป่วย ญาติผู้ป่วย หรือบุคคลอื่นในสถานพยาบาล[11]
การเพิ่มขึ้นของแบคทีเรียดื้อยาในปัจจุบันนั้นมีสาเหตุหลักมาจกาการใช้ยาปฏิชีวนะในมนุษย์และสัตว์อื่น รวมไปถึงการแพร่กระจายของแบคทีเรียดื้อยาระหว่างมนุษย์กับสัตว์เหล่านั้น[8] นอกจากนี้ การดื้อยาของแบคทีเรียนี้ยังทำให้เกิดการคัดเลือกจากแรงกดดัน (selection pressure) ในกลุ่มประชากรของแบคทีเรีย ส่งผลให้แบคทีเรียที่ไวต่อยาต้านจุลชีพตาย และแบคทีเรียที่ดื้อยาต้านจุลชีพซึ่งเดิมมีอยู่ในสัดส่วนที่น้อยนั้น มีจำนวนที่เพิ่มมากขึ้น การที่แบคทีเรียที่ดื้อยากลับกลายมาเป็นประชากรกลุ่มใหญ่ในสายพันธุ์นั้น ๆ ทำให้การรักษาโรคที่เกิดจากการติดเชื้อดังกล่าวต้องได้รับการปรับเปลี่ยนไปใช้การรักษาด้วยยาทางเลือกรอง รวมถึงทำให้เกิดการขาดแคลนยาปฏิชีวนะที่ใช้ในการรักษาจนทำให้ต้องการเร่งรัดการคิดค้นพัฒนายาปฏิชีวนะชนิดใหม่ที่รวบรัดขั้นตอนตามมาตรฐานการพัฒนายาใหม่ที่เคยมีมา อย่างไรก็ตาม ถึงแม้จะมีการเร่งรัดพัฒนายาปฏิชีวนะชนิดใหม่ขึ้นมาเพื่อจัดการกับภาวะฉุกเฉินที่เกี่ยวเนื่องกับแบคทีเรียดื้อยาดังข้างต้น แต่ยาปฏิชีวนะชนิดใหม่ที่ถูกผลิตออกสู่ตลาดยานั้นก็ยังคงมีจำนวนไม่มากพอที่จะบรรเทาปัญหาดังกล่าวลงได้[12]
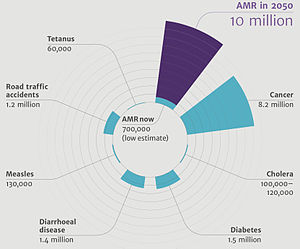
การเพิ่มขึ้นของการดื้อยาของแบคทีเรียนี้ ทำให้มีผู้เสียชีวิตจากการเจ็บป่วยด้วยโรคติดเชื้อดื้อยาอย่างรุนแรงประมาณปีละ 700,000 – 1,000,000 คนต่อปี[13][14] เฉพาะในสหรัฐอเมริกา ในแต่ละปีจะมีผู้ที่เจ็บป่วยด้วยโรคติดเชื้อแบคทีเรียดื้อยาอย่างน้อย 2,000,000 คน และในจำนวนนี้มีผู้ที่ประสบความล้มเหลวในการรักษาและนำไปสู่การเสียชีวิตมากถึง 23,000 คนต่อปี[15] ด้วยความรุนแรงแรงของปัญหาการดื้อยาของแบคทีเรียนี้ ทำให้มีการเรียกร้องให้ประชาคมโลกกำหนดมาตรการการดำเนินการร่วมกันเพื่อจัดการกับภัยคุกคามดังกล่าว จนได้เป็นข้อเสนอสำหรับสนธิสัญญาระหว่างประเทศเรื่องการดื้อต่อยาของจุลชีพ[16] แต่การดำเนินงานดังกล่าวนั้นไม่อาจกระทำได้ในทุกประเทศทั่วโลก เนื่องจากบางประเทศที่มีฐานะยากจนและมีระบบการสาธารณสุขที่อ่อนแอนั้นไม่อาจดำเนินการตามเจตนารมณ์ดังกล่าวได้เต็มที่ ทำให้กลุ่มประเทศดังกล่าวมีอุบัติการณ์การเกิดการดื้อยาของจุลชีพที่ค่อนข้างสูง[9]
คำจำกัดความ[แก้]
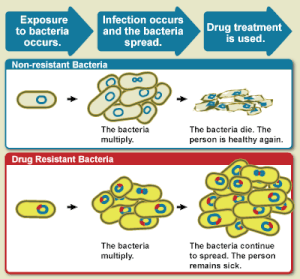
องค์การอนามัยโลกได้ให้คำนิยามของ จุลชีพดื้อยา ว่าเป็น จุลชีพที่ทนต่อยาต้านจุลชีพที่เคยมีประสิทธิภาพดีในการรักษาโรคที่เกิดจากการติดเชื้อจุลชีพดังกล่าว[3] ทั้งนี้การดื้อต่อยาปฏิชีวนะนี้เกิดขึ้นในจุลชีพเท่านั้น คนหรืออวัยวะที่เกิดการติดเชื้อจุลชีพนั้นไม่อาจก่อให้เกิดการดื้อยาปฏิชีวนะได้[18] ในปี ค.ศ. 2014 ด้วยความรุนแรงของการดื้อยาของจุลชีพทำให้องค์การอนามัยโลก (World Health Organization) ประกาศให้ปัญหาการดื้อยาของเชื้อแบคทีเรียเป็น "ปัญหาสำคัญเร่งด่วนที่สุดที่เกิดขึ้นในทุกภูมิภาคทั่วโลกและทุกคนล้วนจะต้องได้รับผลกระทบจากปัญหานี้ ไม่ว่าวัยใด หรือประเทศใดก็ตาม – การดื้อยานี้ทำให้แบคทีเรียเปลี่ยนแปลงไปจากเดิม ดังนั้น ยาปฏิชีวนะที่เคยใช้ได้ผลจะไม่สามารถใช้งานได้กับคนที่ต้องการการรักษาโรคที่เกิดติดเชื้อนี้ - นี่จึงถือเป็นภัยคุกคามหลักต่อการสาธารณสุขในปัจจุบัน"[19][20]
สาเหตุ[แก้]

ถึงแม้ว่าการดื้อต่อยาปฏิชีวนะของแบคทีเรียนั้นมีมาก่อนที่จะมีการใช้ยาดังกล่าวในมนุษย์[21][22] แต่การใช้ยาปฏิชีวนะโดยมนุษย์กันอย่างแพร่หลายในปัจจุบันนี้ทำให้การดื้อยาปฏิชีวนะของแบคทีเรียเพิ่มมากขึ้นกว่าปกติผ่านกระบวนการการกดดันทางวิวัฒนาการ (evolutionary pressure)[23][24] ทั้งนี้ สาเหตุหลักที่ทำให้การใช้ยาปฏิชีวนะในมนุษย์ได้รับความนิยมเป็นอย่างมาก โดยเป็นผลมาจากความสามารถในการผลิตยาปฏิชีวนะในระดับอุตสาหกรรมเพิ่มขึ้นทั่วโลกตลอดทุกช่วงเวลาตั้งแต่ปี 1950 ทำให้ปริมาณยาปฏิชีวนะที่ผลิตขึ้นมีจำนวนมากพอที่จะจำหน่ายแก่ประชาชนได้อย่างกว้างขวาง ประกอบกับการที่รัฐไม่สามารถควบคุมการขายได้ โดยเฉพาะในกลุ่มประเทศรายได้น้อยและรายได้ปานกลางหลายประเทศ ซึ่งสามารถซื้อยาดังกล่าวได้โดยไม่ต้องใช้ใบสั่งยาจากแพทย์ และการซื้อยาใช้เองในกรณีดังกล่าว ส่วนใหญ่มักเป็นการใช้ยาปฏิชีวนะที่ไม่ตรงข้อบ่งใช้ ซึ่งจะส่งผลให้ความเสี่ยงที่อาจเกิดการดื้อยาปฏิชีวนะของแบคทีเรียสูงขึ้นได้ในทุก ๆ สายพันธุ์ที่มีอยู่ในปัจจุบัน[25]
เหตุผลอื่น ๆ ที่ทำให้เกิดการดื้อยาของจุลชีพในปัจจุบัน ได้แก่:
- การใช้ยาปฏิชีวนะในการปศุสัตว์ โดยมีการรับรองให้มีการใช้ยาปฏิชีวนะในขนาดต่ำแก่ปศุสัตว์เพื่อเสริมการเจริญเติบโตของสัตว์ดังกล่าวในประเทศอุตสาหกรรมหลายประเทศ ซึ่งเป็นที่ทราบกันดีว่าการใช้ยาปฏิชีวนะในกรณีนี้สามารถนำไปสู่การเพิ่มขึ้นของการดื้อยาปฏิชีวนะของแบคทีเรียได้[26][27]
- การปล่อยของเสียที่มีส่วนผสมของยาปฏิชีวนะอยู่ในปริมาณสูงสู่สิ่งแวดล้อมของโรงงานผลิตยา เนื่องจากไม่มีระบบการบำบัดน้ำเสีย (wastewater treatment) ที่ดีมากพอ ทำให้ความเสี่ยงที่จะเกิดการดื้อยาของแบคทีเรียในสิ่งแวดล้อมเพิ่มสูงมากขึ้น และแพร่กระจายได้มากขึ้น[28][29]
- ถึงแม้จะยังไม่ทราบแน่ชัดว่าสารต้านแบคทีเรียในสบู่และผลิตภัณฑ์สุขภาพอื่นนั้นมีส่วนช่วยในการดื้อยาของแบคทีเรียหรือไม่ แต่อย่างไรก็ตาม องค์การอาหารและยาของสหรัฐอเมริกาได้ห้ามให้มีการใช้สารต้านแบคทีเรียจำนวน 19 ชนิดในผลิตภัณฑ์สบู่ต้านแบคทีเรียเมื่อวันที่ 2 กันยายน ค.ศ. 2016 ด้วยให้เหตุผลประกอบว่า "ไม่มีข้อมูลที่แสดงให้เห็นได้เด่นชัดว่าสบู่ที่มีส่วนผสมของสารต้านแบคทีเรียนั้นมีประสิทธิภาพดีกว่าการล้างทำความสะอาดด้วยน้ำเปล่าและสบู่ทั่วไปในการป้องกันภาวะความเจ็บป่วยจากแบคทีเรีย"[30][31][32]
การดื้อยาจากการใช้ยาปฏิชีวนะในมนุษย์[แก้]
การเพิ่มขึ้นของการดื้อยาปฏิชีวนะของแบคทีเรียนั้นมีความสัมพันธ์กับปริมาณการสั่งใช้ยาหรือการใช้ยาดังกล่าว รวมไปถึงการรับประทานยาปฏิชีวนะไม่ครบตามที่ได้ควรได้รับ[33] โดยการสั่งยาใช้ปฏิชีวนะที่ไม่เหมาะสมนี้มีสาเหตุมาจากหลายประการ ทั้งจากการที่ผู้ป่วยยืนยันที่จะให้แพทย์สั่งใช้ยาปฏิชีวนะแก่ตน ถึงแม้จะไม่มีข้อบ่งชี้ที่จำเป็นต้องใช้ยาดังกล่าว และแพทย์บางรายก็อาจสั่งจ่ายยาปฏิชีวนะให้แก่ผู้ป่วยของตนตามที่ร้องขอ เนื่องจากไม่มีเวลามากพอที่จะอธิบายให้ผู้ป่วยตระหนักรู้ได้ถึงเหตุผลที่ไม่ควรใช้ยาปฏิชีวนะในการรักษาการเจ็บป่วยครั้งนั้น ๆ และในบางกรณี แพทย์ผู้สั่งใช้ยาเองก็ไม่ทราบแน่ชัดว่าเมื่อใดที่จำเป็นต้องใช้ยาปฏิชีวนะหรือมีความระมัดระวังมากเกินไปในการสั่งใช้ยาเนื่องมาจากเหตุผลทางการแพทย์ รวมไปถึงเหตุผลทางกฎหมาย[34] นอกจากนี้แล้ว การที่มีระดับความเข้มข้นของยาปฏิชีวนะในร่างกายต่ำมากเกินไปก็อาจก่อให้เกิดการดื้อยาของแบคทีเรียได้ผ่านกระบวนการการเหนี่ยวนำให้เกิดการกลายพันธุ์ของแบคทีเรียนั้น ๆ ส่งผลให้แบคทีเรียดังกล่าวสามารถเจริญเติบโตอยู่ได้ตามปกติถึงแม้จะมีการรักษาด้วยยาปฏิชีวนะชนิดเดิมที่ให้ความเข้มข้นของยาในกระแสเลือดมากขึ้นกว่าเดิมก็ตาม ยกตัวอย่างเช่น การดื้อยาของแบคทีเรีย Pseudomonas aeruginosa และ Bacteroides fragilis ที่ถูกเหนี่ยวนำให้เกิดการกลายพันธุ์จากการได้รับยาปฏิชีวนะในขนาดที่ให้ความเข้มข้นของยาดังกล่าวในร่างกายต่ำกว่าความเข้มข้นต่ำสุดที่สามารถยับยั้งการเจริญของแบคทีเรียดังกล่าว (subinhibitory concentration)[35]
ดังที่กล่าวไปในข้างต้นว่า การใช้ยาปฏิชีวนะที่ไม่เหมาะสมและไม่จำเป็นเพื่อการรักษาความเจ็บป่วยของมนุษย์ในปัจจุบันนั้นเป็นสาเหตุหลักที่ก่อให้เกิดภาวะฉุกเฉินด้านการดื้อยาของแบคทีเรีย โดยมากกว่าร้อยละ 50 ของการใช้ยาปฏิชีวนะในมนุษย์พบว่าเป็นการใช้ยาที่ไม่เหมาะสมและไม่ตรงตามข้อบ่งใช้[8] ยกตัวอย่างเช่น คน 1 ใน 3 คน ยังคงมีความเชื่อว่ายาปฏิชีวนะมีประสิทธิภาพในการรักษาโรคไข้หวัด[36] โดยพบว่าการสั่งจ่ายยาปฏิชีวนะเพื่อรักษาโรคไข้หวัดนั้นพบเห็นได้มากที่สุดในประเด็นของการสั่งใช้ยาปฏิชีวนะที่ไม่ตรงตามข้อบ่งใช้ ถึงแม้จะเป็นที่ทราบกันดีของบุคลากรทางการแพทย์ว่ายาดังกล่าวไม่มีประสิทธิภาพในการต้านไวรัสที่เป็นสาเหตุของโรคไข้หวัด[37] นอกจากนี้การใช้ยาปฏิชีวนะแม้เพียงครั้งเดียว ถึงแม้จะเป็นการใช้ในผู้ที่มีข้อบ่งใช้ที่จำเป็นต้องได้รับยาดังกล่าว ก็สามารถเพิ่มความเสี่ยงที่อาจก่อให้เกิดการดื้อยาปฏิชีวนะของแบคทีเรียได้ โดยความเสี่ยงที่เพิ่มขึ้นดังกล่าวจะคงอยู่ได้นานประมาณ 1 เดือน ถึง 1 ปี ตั้งแต่เริ่มมีการใช้ยาดังกล่าว[38][39]
ความเสี่ยงที่จะเกิดการดื้อยาปฏิชีวนะของแบคทีเรียนั้นจะเพิ่มขึ้นตามระยะเวลาที่ใช้ยาปฏิชีวนะในการรักษา ดังนั้น ตราบใดที่ยังมีการใช้ยาปฏิชีวนะในจำนวนที่น้อยที่สุดที่ให้ประสิทธิภาพดีในการรักษา และใช้ยาดังกล่าวเป็นระยะเวลาที่สั้นที่สุดเท่าที่เป็นได้จะช่วยลดความเสี่ยงต่อการเกิดการดื้อยาของแบคทีเรีย ช่วยลดภาระค่าใช้จ่าย ให้ผลลัพธิ์การรักษาที่ดีกว่าและมีภาวะแทรกซ้อนน้อย[10] .ทำให้ในปัจจุบันมีการใช้สูตรการรักษาด้วยยาปฏิชีวนะระยะสั้นในผู้ที่เจ็บป่วยด้วยโรคติดเชื้อแบคทีเรียหลายชนิด ได้แก่ โรคปอดอักเสบชุมชน (community-acquired pneumonia; CAP),[40] เยื่อบุช่องท้องอักเสบเองจากแบคทีเรีย (spontaneous bacterial peritonitis; SBP),[41] ผู้ป่วยหนักในหน่วยอภิบาลที่คาดว่าอาจมีการติดเชื้อแบคทีเรียในปอด,[42] กลุ่มอาการที่เข้าได้กับอาการปวดท้องเฉียบพลัน (acute abdominal),[43] หูชั้นกลางอักเสบ, โพรงอากาศอักเสบ และการติดเชอื้แบคทีเรียในช่องคอ (throat infection),[44] และการเจ็บป่วยจากการทะลุของลำไส้[45][46] ในบางกรณี การรักษาด้วยยาปฏิชีวนะสูตรระยะสั้นอาจไม่สามารถรรักษาภาวะการติดเชื้อนั้น ๆ ได้ เช่นเดียวกันกับการรักษาด้วยยาปฏิชีวนะสูตรระยะยาว[47] การศึกษาทางคลินิกที่ได้รับการตีพิมพ์ในวารสารทางการแพทย์ของสมาคมการแพทย์อังกฤษ (British Medical Association) พบว่า หากอาการและอาการแสดงของการติดเชื้อแบคทีเรียถูกกำจัดออกไปด้วยการรักษาด้วยยาปฏิชีวนะแล้ว ควรหยุดการบริหารยาดังกล่าว ณ 72 ชั่วโมงหลังอาการดีขึ้น[48] ทั้งนี้ ส่วนใหญ่ผู้ป่วยมักมีอาการดีขึ้นก่อนที่เชื้อก่อโรคจะถูกกำจัดออกไปหมด ดังนั้นแพทย์ควรให้คำแนะนำแก่ผู้ป่วยทุกคนที่ได้รับการรักษาด้วยยาปฏิชีวนะให้ตระหนักรู้ถึงการได้รับการรักษาด้วยยาดังกล่าวจนถึงระยะเวลาที่แนะนำในแนวทางการรักษามาตรฐาน นักวิจัยบางคนสนับสนุนให้แพทย์ใช้หลักสูตรยาปฏิชีวนะที่สั้นมากในการรักษา และประเมินผู้ป่วยหลังจากนั้น 2–3 วันและหยุดการรักษาหากไม่มีอาการทางคลินิกที่บ่งบอกถึงการติดเชื้อแบคทีเรีย[49]
นอกจากนี้ การใช้ยาปฏิชีวนะในกลุ่มที่แตกต่างกันพบว่ามีความสัมพันธ์กับการเกิดการดื้อยาหรือการแพร่กระจายของเชื้อบางสายพันธ์ที่มากกว่าการใช้ยาปฏิชีวนะในกลุ่มอื่น อาทิ อัตราการติดเชื้อสแตปฟิโลคอคคัส ออเรียสที่ดื้อต่อยาเมทิซิลลิน (Methicillin-resistant Staphylococcus aureus; MRSA) จะสูงขึ้นเมื่อมีการใช้ยาปฏิชีวนะกลุ่มไกลโคเปปไทด์ (Glycopeptide antibiotics), เซฟาโลสปอริน, และควิโนโลน[50][51] เซฟาโลสปอริน และโดยเฉพาะควิโนโลนและคลินดามัยซินนั้นมีสามารถเหนี่ยวนำให้เกิดการเพิ่มจำนวนที่มากเกินปกติของแบคทีเรีย Clostridium difficile ในทางเดินอาหารได้[52][53]
นอกเหนือจากปัจจัยดังข้างต้นแล้ว ปัจจัยบางประการที่จำเป็นต่อการรักษาผู้ป่วยในหน่วยอภิบาล (intensive care unit; ICU) อย่างการใส่เครื่องช่วยหายใจ (mechanical ventilation) และการมีโรคร่วมหลายโรค ก็เป็นปัจจัยเสริมที่เพิ่มความเสี่ยงต่อการติดเชื้อแบคทีเรียดื้อยาได้เช่นกัน[54] รวมถึงการล้างมือและการทำให้ปราศจากเชื้อ (disinfecting) ที่ไม่ดีพอระหว่างการสัมผัสผู้ป่วยแต่ละคนของบุคลากรทางการแพทย์และเจ้าหน้าที่หอผู้ป่วยนั้นก็มีความสัมพันธ์กับการแพร่กระจายของจุลชีพดื้อยาเช่นกัน[55]
การดื้อยาจากการใช้ยาปฏิชีวนะในสัตว์[แก้]

ในช่วงหลายทศวรรษที่ผ่านมา เป็นที่สงสัยถึงความสัมพันธ์ระหว่างการใช้ยาปฏิชีวนะในการปศุสัตว์กับการเกิดการดื้อยาปฏิชีวนะของแบคทีเรีย จนกระทั่งองค์การอนามัยโลกได้ให้ข้อสรุปในประเด็นดังกล่าวว่า "การใช้ยาปฏิชีวนะที่ไม่เหมาะสมในการเลี้ยงสัตว์เป็นปัจจัยที่ส่งเสริมให้เกิดและการแพร่กระจายของเชื้อโรคที่ทนต่อยาปฏิชีวนะและควรห้ามไม่ให้มีการใช้ยาปฏิชีวนะเป็นตัวกระตุ้นการเจริญเติบโตในอาหารสัตว์"[56] องค์การอนามัยโลกได้เพิ่มหลักเกณฑ์ด้านสุขอนามัยสัตว์บกเพื่อเป็นแนวทางในการให้คำแนะนำแก่สมาชิกขององค์กรในการสร้างและประสานการตรวจสอบและติดตามเฝ้าระวังการดื้อยาต้านจุลชีพระดับประเทศ,[57] ติดตามตรวจสอบปริมาณยาปฏิชีวนะที่ใช้ในการเลี้ยงสัตว์,[58] และให้คำแนะนำแก่องค์กรหรือหน่วยงานอื่น ๆ เพื่อให้มั่นใจว่ามีการใช้ยาปฏิชีวนะอย่างเหมาะสมและรอบคอบ ส่วนอีกแนวทางหนึ่งคือ การใช้วิธีการที่จะช่วยในการตรวจหาปัจจัยเสี่ยงที่เกี่ยวข้องกับการดื้อยา และประเมินความเสี่ยงนั้น ๆ ต่อการดื้อยาปฏิชีวนะของแบคทีเรีย[59]
การดื้อยาโดยธรรมชาติ[แก้]
การดื้อยาปฏิชีวนะของแบคทีเรียนั้นสามารถเกิดขึ้นได้เองทั่วไปในธรรมชาติ[60] โดยมีการค้นพบยีนที่มีมาแต่โบราณซึ่งเป็นยีนทำให้แบคทีเรียเหล่านั้นดื้อต่อยาปฏิชีวนะ โดยยาปฏิชีวนะนั้นอาจเป็นยาที่ถูกผลิตขึ้นมาโดยแบคทีเรียนั้น ๆ[61][62] ซึ่งยีนที่ทำให้เกิดการดื้อยาดังกล่าวเป็นที่รู้จักกันดีว่าเป็นรีซิสโตม (resistome) ที่พบการเกิดขึ้นได้เองในธรรมชาติ[60] โดยยีนเหล่านั้นอาจถูกถ่ายทอดจากแบคทีเรียที่ไม่ก่อโรคไปยังแบคทีเรียอื่นที่ก่อโรคและทำให้แบคทีเรียที่ได้รับยีนนี้เข้าไปสามารถทนต่อยาปฏิชีวนะได้เช่นกัน[60]
ใน ค.ศ. 1952 มีการค้นพบการดื้อยาเพนิซิลลินในแบคทีเรียบางสายพันธุ์ ซึ่งเป็นช่วงเวลาก่อนที่จะมีการนำยาดังกล่าวมาใช้ในทางคลินิก[63] นอกจากนี้ยังมีการค้นพบว่ามีการดื้อยาสเตรปโตมัยซินของแบคทีเรียบางชนิดในช่วงเวลาก่อนหน้านั้นอีกด้วย[64] ต่อมาใน ปี ค.ศ. 1962 ได้มีการตรวจพบเอนไซม์เพนิซิลิเนสในเอนโดสปอร์ของแบคทีเรีย Bacillus licheniformis ซึ่งเอนไซม์ดังกล่าวเป็นเอนไซม์ที่ทำลายโครงสร้างหลักของยากลุ่มเพนิซิลลิน จากดินแห้งบนรากพืชที่ถูกเก็บไว้ในพิพิธภัณฑ์บริติชตั้งแต่ปี ค.ศ. 1689[65][66][67] นอกจากนั้น การศึกษาจุลชีพในทางเดินอาหารของวิลเลียม เบรน (William Braine) และจอห์น ฮาร์ทเนลล์ (John Hartnell) ซึ่งเป็นลูกเรือที่เสียชีวิตในการเดินสำรวจมหาสมุทรอาร์กติกของจอห์น แฟรงคลิน (Franklin's lost expedition) พบแบคทีเรียสกุล Clostridium จำนวน 6 สเตรนที่ดื้อต่อเซโฟซิตินและคลินดามัยซิน[68]
ทั้งนี้ การสร้างเอนไซม์เพนิซิลิเนสของแบคทีเรียนั้นอาจขึ้นอยู่กับบางสถานการณ์และสิ่งแวดล้อมด้วย โดยการหลั่งเอนไซม์นี้อาจเป็นผลมาจากการสร้างกลไกการป้องกันตนเองของแบคทีเรีนนั้น ๆ จากสภาพแวดล้อมในแหล่งที่อยู่ของตนที่เป็นอันตราย ยกตัวอย่างเช่น Staphylococcus aureus จะมีการสร้างเอนไซม์เพนิซิลิเนสออกมาเป็นจำนวนมากเมื่อต้องอาศัยอยู่ในแหล่งที่มีราตระกูลสกุลทริโคไฟตอนที่ผลิตเพนิซิลลิน ซึ่งส่งผลให้แบคทีเรียเกิดการดื้อต่อยาเพนิซิลลินได้[67] Search for a penicillinase ancestor has focused on the class of proteins that must be a priori capable of specific combination with penicillin.[69] แต่ในทางกลับกัน การดื้อยาของแบคทีเรียที่พบในทางเดินอาหารของวิลเลียม เบรน และจอห์น ฮาร์ทเนลล์ ดังที่ได้กล่าวไว้ในข้างต้น อาจเป็นผลมาจากการที่ทั้งสองคนได้รับเชื้อแบคทีเรียที่สามารถสร้างเอนไซม์หรือเกิดการกลายพันธุ์แบบสุ่มของโครโมโซมได้เองตามธรรมชาติจนทำให้ทนต่อยาปฏิชีวนะดังกล่าวก็เป็นได้[68]
นอกจากนี้ยังมีหลักฐานเชิงประจักษ์ที่บ่งชี้ได้ว่าโลหะหนัก และสารก่อมลพิษอื่น ๆ อาจมีส่วนในการทำให้เกิดการแพร่กระจายของแบคทีเรียดื้อยาได้โดยโลหะหนักและสารพิษเหล่านั้นจะทำให้แบคทีเรียที่ไม่ดื้อยาไม่สามารถดำรงชีวิตอยู่ได้ แต่ในทางตรงกันข้าม แบคทีเรียที่ดื้อยาจะไม่ได้รับผลกระทบดังกล่าวและจะมีการเพิ่มจำนวนมากขึ้นเพื่อทดแทนแบคทีเรียไม่ดื้อยาที่ลดจำนวนลงไป[70]
การดื้อยาจากมลภาวะในสิ่งแวดล้อม[แก้]
ปัญหาการดื้อต่อยาปฏิชีวนะของแบคทีเรียในปัจจุบันได้ทวีความรุนแรงมากขึ้นจนเป็นภัยคุกคามต่อสุขภาพทั้งมนุษย์และสัตว์ต่าง ๆ ไม่ว่าจะมีแหล่งอาศัยอยู่บนบกหรือในน้ำ โดยปัจจัยสำคัญอีกประการหนึ่งที่มีส่วนหนุนให้ปัญหาดังกล่าวแพร่กระจายจนส่งผลกระทบในวงกว้างก็คือ การปนเปื้อนและการแพร่กระจายของยาปฏิชีวนะหรือสารที่ออกฤทธิ์เป็นยาปฏิชีวนะในสิ่งแวดล้อม โดยเฉพาะอย่างยิ่ง น้ำเสียจากโรงพยาบาลและน้ำเสียจากชุมชนเมืองที่ถูกปล่อยออกสู่ธรรมชาติโดยไม่ได้รับการบำบัดหรือมีระบบการบำบัดที่ไม่รัดกุม ถือเป็นสาเหตุหลักที่ทำให้เกิดการปนเปื้อนดังกล่าว[71][72] ยาปฏิชีวนะได้ก่อให้เกิดมลพิษต่อสิ่งแวดล้อมนับตั้งแต่มีการนำมาใช้ในมนุษย์ (ยา, การเกษตร) ผ่านทางของเสียต่าง ๆ ที่ถูกขับออกจากร่างกายกมนุษย์ สัตว์เลี้ยง และของเสียจากอุตสาหกรรมยา[73] การที่ของเสียที่มีการปนเปื้อนของยาปฏิชีวนะถูกปล่อยสู่สิ่งแวดล้อมโดยไม่ได้รับการบำบัดหรือได้รับการบำบัดที่ไม่ดีมาก จะเป็นปัจจัยเสริมให้เกิดการดื้อยาปฏิชีวนะของแบคทีเรียได้มากขึ้น และเกิดการปนเปื้อนและแพร่กระจายของแบคทีเรียดื้อยาดังกล่าวในสิ่งแวดล้อมนั้นอีกด้วย ในปี ค.ศ. 2011 การทำแผนที่ของตัวอย่างน้ำทิ้งและน้ำประปาในนิวเดลี ประเทศอินเดีย ซึ่งเป็นที่ทราบกันดีว่ามีจำนวนการใช้ยาปฏิชีวนะของประชาชนบริเวณนั้นในสัดส่วนที่สูง ผลการตรวจพบว่ามีการปนเปื้อนแบคทีเรียอยู่เป็นจำนวนมากและยังส่งผลให้เกิดการติดเชื้อแบคทีเรียในทางเดินอาหารในชุมชนที่อุปโภคบริโภคน้ำจากแหล่งดังกล่าวอย่างเป็นวงกว้างและยากแก่การควบคุมโรค โดยพบว่าเชื้อก่อโรคดังกล่าวส่วนใหญ่มักมีผลตรวจเอนไซม์ NDM-1 เป็นบวก ซึ่งเป็นเอนไซม์ดังกล่าวจะส่งผลให้แบคทีเรียนั้น ๆ เกิดการดื้อต่อยาที่มีโครงสร้างหลักเป็นวงบีตา-แลคแตมได้หลายชนิด[74] ซึ่งโดยทั่วไปแล้ว ร้อยละ 70–80 ของผู้ปวยที่มีอาการท้องร่วงมักมีสาเหตุมาจากการติดเชื้อไวรัส ซึ่งไม่สามารถรักษาได้โดยการใช้ยาปฏิชีวนะ แต่ในการข้อมูลจากการศึกษากลับพบว่าราวร้อยละ 40 ของผู้ป่วยที่มีอาการข้างต้นยังคงพยายามที่จะรักษาอาการท้องร่วงนั้นด้วยยาปฏิชีวนะ[75] ในบางพื้นที่ผู้ที่รักษาอาการท้องร่วงอย่างไม่เหมาะสมด้วยยาปฏิชีวนะนั้นมีสัดส่วนที่มากถึงร้อยละ 80[75]
เนื่องจากแบคทีเรียเป็นสิ่งมีชีวิตที่สามารถแบ่งเซลล์เพื่อเพิ่มจำนวนได้อย่างรวดเร็ว ทำให้แบคทีเรียดื้อยาที่แพร่กระจายลงสู่สิ่งแวดล้อมนั้นสามารถเจริญเติบโตและแพร่จำนวนได้มากภายในระยะเวลาอันสั้น ยิ่งไปกว่านั้น แบคทีเรียที่ดื้อยาเหล่านี้ยังสามารถถ่ายทอดยีนดื้อยาไปยังแบคทีเรียสายพันธุ์หรือสเตรนอื่น ๆ ได้ผ่านกระบวนการที่เรียกว่า การถ่ายทอดยีนในแนวราบ (horizontal gene transfer; HGT) ดังนั้น ถึงแม้ว่ายาปฏิชีวนะที่แบคทีเรียดังกล่าวดื้อยาจะไม่ถูกปล่อยลงสู่ธรรมชาติเพิ่มเติมในอนาคต ยีนที่ดื้อยาปฏิชีวนะดังกล่าวก็จะยังคงพบเห็นอยู่ในแบคทีเรียธรรมชาติทั่วไป เนื่องจากแบคทีเรียดังกล่าวจะมีการแบ่งตัวและถ่ายทอดยีนดื้อยาให้กันจากรุ่นสู่รุ่น[73] นอกจากนี้ยังพบว่า มีการแพร่กระจายเป็นวงกว้างของแบคทีเรียดื้อยาในสัตว์ทะเลที่มีกระดูกสันหลัง ซึ่งเป็นที่คาดการณ์กันว่าแบคทีเรียดื้อยาที่พบเหล่านี้อาจเป็นแหล่งสำคัญที่จะทำให้เกิดการแพร่กระจายของเชื้อดื้อยาในสิ่งแวดล้อมทางทะเล[76]
การป้องกัน[แก้]

ในปัจจุบัน มีการเรียกร้องให้มีมาตรการจัดการกับปัญหาการดื้อยาปฏิชีวนะของแบคทีเรียที่มีอุบัติการณ์และความรุนแรงเพิ่มมากขึ้น ซึ่งรวมไปถึงการร่างสนธิสัญญาระหว่างประเทศเพื่อแก้ปัญหาด้านการดื้อยาของจุลชีพ อย่างไรก็ตาม การดำเนินงานนี้จำเป็นต้องมีรายละเอียดและได้รับความสนใจจากภาคส่วนต่าง ๆ มากขึ้นเพื่อที่จะประมาณการและวัดแนวโน้มความรุนแรงของปัญหาดังกล่าวในระดับนานาชาติ โดยที่ผ่านมามีแนวคิดที่จะนำระบบการติดตามและประเมินผลการรักษา (tracking system) มาใช้จัดการกับปัญหานี้ แต่การใช้งานจริงนั้นยังไม่อาจเกิดขึ้นได้มากเท่าใดนัก ซึ่งระบบในลักษณะนี้จะให้ข้อมูลเชิงลึกแก่พื้นที่ที่มีการดื้อยาสูง รวมถึงข้อมูลที่จำเป็นสำหรับการประเมินการดำเนินงานและการเปลี่ยนแปลงอื่น ๆ ที่ทำขึ้นเพื่อต่อสู้หรือจัดการกับปัญหาการทนต่อยาปฏิชีวนะของแบคทีเรีย โดยกลยุทธิ์สำคัญ 5 ประการที่จำเป็นสำหรับการลดการเกิดการดื้อยาของแบคทีเรีย ได้แก่[78]
- มีการเฝ้าระวังการใช้ยาปฏิชีวนะ เพื่อสงวนยาปฏิชีวนะที่มีอยู่ในปัจจุบันและที่อาจค้นพบใหม่ในอนาคตให้มีประสิทธิภาพในการรักษาโรคติดเชื้อแบคทีเรียต่าง ๆ ได้ดีเหมือนที่ผ่านมา
- มีการกำหนดกรอบเวลาที่จำเป็นต้องมีการสั่งจ่ายยาปฏิชีวนะที่มีประสิทธิภาพและเจาะจงกับเชื้อสาเหตุให้เร็วที่สุดเท่าที่เป็นไปได้
- พัฒนาและรับรองยาปฏิชีวนะชนิดใหม่ให้ได้ 10 ชนิดภายในปี ค.ศ. 2020
- พัฒนาวิธีการศึกษาพันธุศาสตร์ระดับโมเลกุลเพื่อตรวจหายีนของแบคทีเรียที่ก่อให้เกิดการดื้อยาปฏิชีวนะ
- ไม่ก่อให้เกิดความล่าช้าในขั้นตอนการกระจายงบประมาณเพื่อกองทุนนวัตกรรมต้านการดื้อยาของแบคทีเรียมูลค่า 2 พันล้านเหรียญสหรัฐ
ระยะเวลาการใช้ยาปฏิชีวนะ[แก้]
ระยะเวลาที่ใช้สำหรับการรักษาโรคติดเชื้อแบคทีเรียด้วยยาปฏิชีวนะนั้นจะขึ้นอยู่กับชนิดของโรคและปัญหาด้านสุขภาพอื่น ๆ ของผู้ป่วยแต่ละราย[10] การหยุดการรักษาด้วยยาปฏิชีวนะหลังจากผู้ป่วยมีอาการดีขึ้นโดยที่ไม่ได้รับยาปฏิชีวนะครบตามกรอบระยะเวลาที่กำหนดในแบบแผนการรักษานั้น มีหลักฐานเชิงประจักษ์บางแหล่งที่พบว่า การเกิดการดื้อยาปฏิชีวนะของแบคทีเรียจะเกิดขึ้นได้มากกว่าปกติในกรณีดังกล่าว[10] แต่ข้อมูลบางแหล่งก็ระบุไปในอีกทิศทางหนึ่งว่า การหยุดการรักษาด้วยยาปฏิชีวนะเร็วกว่าปกตินั้นอาจเป็นการกระทำที่สมเหตุสมผลได้ในผู้ป่วยบางราย[10] แต่ผู้ป่วยโรคติดเชื้อบางชนิดจำเป็นที่จะต้องได้รับการรักษาด้วยยาปฏิชีวนะเป็นระยะเวลานาน การพิจารณาหยุดการใช้ยาในผู้ป่วยดังกล่าวไม่ได้ขึ้นอยู่กับว่าผู้ป่วยจะมีอาการดีขึ้นหรือไม่ก็ตาม[10]
การติดตามและวางผังงาน[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การจำกัดการใช้ยาปฏิชีวนะ[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ระดับโรงพยาบาล[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ระดับบุคลากร[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ระดับประชาชน[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
สุขาภิบาลและการอนามัย[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การจัดการการใช้ยาปฏิชีวนะในสัตว์[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ยุโรป[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
สหรัฐอเมริกา[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การวางแผนปฏิบัติงานและสร้างความตระหนักในระดับนานาชาติ[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
“สัปดาห์รู้รักษ์ ตระหนักใช้ยาปฏิชีวนะ[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
กลไกการดื้อยา[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ประวัติ และประเด็นด้านสังคมและวัฒนธรรม[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การศึกษาวิจัย[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
สถานการณ์แบคทีเรียดื้อยาในประเทศไทย[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ดูเพิ่ม[แก้]
อ้างอิง[แก้]
- ↑ Kirby-Bauer Disk Diffusion Susceptibility Test Protocol เก็บถาวร 2011-06-26 ที่ เวย์แบ็กแมชชีน, Jan Hudzicki, ASM
- ↑ "Review on Antimicrobial Resistance". amr-review.org. สืบค้นเมื่อ 20 May 2016.
- ↑ 3.0 3.1 3.2 "Antimicrobial resistance Fact sheet N°194". who.int. April 2014. สืบค้นเมื่อ 7 March 2015.
- ↑ "About Antimicrobial Resistance - Antibiotic/Antimicrobial Resistance - CDC". www.cdc.gov. 19 September 2017.
- ↑ "Antibiotic Resistance Questions & Answers". Get Smart: Know When Antibiotics Work. Centers for Disease Control and Prevention, USA. 30 June 2009. สืบค้นเมื่อ 20 March 2013.
- ↑ "General Background: About Antibiotic Resistance". www.tufts.edu. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2015-10-23. สืบค้นเมื่อ 2015-10-30.
- ↑ Berkeley.edu. "Mutations are random". University of California Museum of Paleontology. สืบค้นเมื่อ February 19, 2018.
- ↑ 8.0 8.1 8.2 "About Antimicrobial Resistance". www.cdc.gov. สืบค้นเมื่อ 2015-10-30.
- ↑ 9.0 9.1 Swedish work on containment of antibiotic resistance – Tools, methods and experiences (PDF). Stockholm: Public Health Agency of Sweden. 2014. pp. 16–17, 121–128. ISBN 978-91-7603-011-0. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2015-07-23. สืบค้นเมื่อ 2018-02-19.
- ↑ 10.0 10.1 10.2 10.3 10.4 10.5 "Duration of antibiotic therapy and resistance". NPS Medicinewise. National Prescribing Service Limited trading, Australia. 13 June 2013. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2015-07-23. สืบค้นเมื่อ 22 July 2015.
- ↑ "CDC Features – Mission Critical: Preventing Antibiotic Resistance". www.cdc.gov. สืบค้นเมื่อ 2015-07-22.
- ↑ Cassir, N; Rolain, JM; Brouqui, P (2014). "A new strategy to fight antimicrobial resistance: the revival of old antibiotics". Frontiers in Microbiology. 5: 551. doi:10.3389/fmicb.2014.00551. PMC 4202707. PMID 25368610.
- ↑ WHO (April 2014). "Antimicrobial resistance: global report on surveillance 2014". WHO. WHO. สืบค้นเมื่อ May 9, 2015.
- ↑ 14.0 14.1 O'neill, Jim (May 2016). "TACKLING DRUG-RESISTANT INFECTIONS GLOBALLY: FINAL REPORT AND RECOMMENDATIONS" (PDF). amr-review.org/. สืบค้นเมื่อ November 10, 2017.
- ↑ "Antibiotic / Antimicrobial Resistance - CDC". www.cdc.gov. 18 August 2017.
- ↑ Hoffman S.J.; Outterson K.; Røttingen J-A.; Cars O.; Clift C.; Rizvi Z.; Rotberg F.; Tomson G.; Zorzet A. (Feb 2015). "An International Legal Framework to Address Antimicrobial Resistance". Bulletin of the World Health Organization. 93 (2): 66. doi:10.2471/BLT.15.152710. PMC 4339972. PMID 25883395.
- ↑ "What is Drug Resistance?". www.niaid.nih.gov. สืบค้นเมื่อ 2015-07-26.
- ↑ "CDC: Get Smart: Know When Antibiotics Work". Cdc.gov. สืบค้นเมื่อ 2013-06-12.
- ↑ "Antimicrobial resistance: global report on surveillance" (PDF). The World Health Organization. April 2014. ISBN 978 92 4 156474 8. สืบค้นเมื่อ 13 June 2016.
- ↑ "WHO's first global report on antibiotic resistance reveals serious, worldwide threat to public health" Retrieved 2014-05-02
- ↑ D'Costa VM, King CE, Kalan L, Morar M, Sung WW, Schwarz C, Froese D, Zazula G, Calmels F, Debruyne R, Golding GB, Poinar HN, Wright GD (2011). "Antibiotic resistance is ancient". Nature. 477 (7365): 457–461. Bibcode:2011Natur.477..457D. doi:10.1038/nature10388. PMID 21881561.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Caldwell & Lindberg 2011.
- ↑ Hawkey & Jones 2009, pp. i3–i10.
- ↑ Goossens H, Ferech M, Vander Stichele R, Elseviers M (2005). "Outpatient antibiotic use in Europe and association with resistance: a cross-national database study". Lancet. 365 (9459): 579–87. doi:10.1016/S0140-6736(05)17907-0. PMID 15708101.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Laxminarayan R, Duse A, Wattal C, Zaidi AK, Wertheim HF, Sumpradit N, Vlieghe E, Hara GL, Gould IM, Goossens H, Greko C, So AD, Bigdeli M, Tomson G, Woodhouse W, Ombaka E, Peralta AQ, Qamar FN, Mir F, Kariuki S, Bhutta ZA, Coates A, Bergstrom R, Wright GD, Brown ED, Cars O (2013). "Antibiotic resistance-the need for global solutions". Lancet Infect Dis. 13 (12): 1057–98. doi:10.1016/S1473-3099(13)70318-9. PMID 24252483.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) As PDF. - ↑ Ferber D (4 January 2002). "Livestock Feed Ban Preserves Drugs' Power". Science. 295 (5552): 27–28. doi:10.1126/science.295.5552.27a. PMID 11778017.(ต้องรับบริการ)
- ↑ Mathew AG, Cissell R, Liamthong S (2007). "Antibiotic resistance in bacteria associated with food animals: a United States perspective of livestock production". Foodborne Pathog. Dis. 4 (2): 115–33. doi:10.1089/fpd.2006.0066. PMID 17600481.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ "Pharmaceuticals Sold In Sweden Cause Serious Environmental Harm In India, Research Shows". ScienceDaily. ScienceDaily, LLC. 7 February 2009. สืบค้นเมื่อ 29 January 2015.
We estimated that the[water] treatment plant released 45 kilograms of the antibiotic ciprofloxacin in one day, which is equivalent to five times the daily consumption of Sweden,”
- ↑ Larsson DG, Fick J (Jan 2009). "Transparency throughout the production chain – a way to reduce pollution from the manufacturing of pharmaceuticals?". Regul Toxicol Pharmacol. 53 (3): 161–3. doi:10.1016/j.yrtph.2009.01.008. PMID 19545507.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ CDC. "Antibiotic Resistance Questions and Answers" [Are antibacterial-containing products (soaps, household cleaners, etc.) better for preventing the spread of infection? Does their use add to the problem of resistance?]. Atlanta, Georgia, USA.: Centers for Disease Control and Prevention. สืบค้นเมื่อ February 25, 2015.
- ↑ Allison E. Aiello; Elaine L. Larson; Stuart B. Levy (2007). "Consumer Antibacterial Soaps: Effective or Just Risky?". Clinical Infectious Diseases. 45 (Supplement 2): S137-47. doi:10.1086/519255. PMID 17683018.
- ↑ Kodjak A (2 September 2016). "FDA Bans 19 Chemicals Used In Antibacterial Soaps". NPR. สืบค้นเมื่อ 24 October 2017.
- ↑ Pechère JC (September 2001). "Patients' interviews and misuse of antibiotics". Clin. Infect. Dis. 33 Suppl 3: S170–3. doi:10.1086/321844. PMID 11524715.
Noncompliance may have an impact on antibiotic resistance ... Type A consists in shorter than prescribed courses. By reducing the antibiotic pressure, provided that the daily doses are otherwise respected, one may see a theoretical advantage ... Type B noncompliance reduces the number of daily doses ... indicate that such underdosing may promote the selection of resistance
- ↑ Arnold SR, Straus SE (2005). Arnold, Sandra R (บ.ก.). "Interventions to improve antibiotic prescribing practices in ambulatory care". Cochrane Database of Systematic Reviews (4): CD003539. doi:10.1002/14651858.CD003539.pub2. PMID 16235325.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Ventola, C. Lee. "The antibiotic resistance crisis: part 1: causes and threats." Pharmacy and Therapeutics 40.4 (2015): 277.
- ↑ McNulty CA, Boyle P, Nichols T, Clappison P, Davey P (August 2007). "The public's attitudes to and compliance with antibiotics". J. Antimicrob. Chemother. 60 Suppl 1: i63–8. doi:10.1093/jac/dkm161. PMID 17656386.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Ronald Eccles; Olaf Weber, บ.ก. (2009). Common cold (Online-Ausg. ed.). Basel: Birkhäuser. p. 234. ISBN 978-3-7643-9894-1.
- ↑ Costelloe C, Metcalfe C, Lovering A, Mant D, Hay AD (2010). "Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis". British Medical Journal. 340: c2096. doi:10.1136/bmj.c2096. PMID 20483949.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Antimicrobial Resistance: Tackling a Crises for the Health and Welfare of Nations: 2014. Jim O'Neill Gibbs Building, 215 Euston Road, London, NW1 2BE. 11 December 2014.(ต้องรับบริการ)
- ↑ Li JZ, Winston LG, Moore DH, Bent S (September 2007). "Efficacy of short-course antibiotic regimens for community-acquired pneumonia: a meta-analysis". Am. J. Med. 120 (9): 783–90. doi:10.1016/j.amjmed.2007.04.023. PMID 17765048.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Runyon BA, McHutchison JG, Antillon MR, Akriviadis EA, Montano AA (June 1991). "Short-course versus long-course antibiotic treatment of spontaneous bacterial peritonitis. A randomized controlled study of 100 patients". Gastroenterology. 100 (6): 1737–42. PMID 2019378.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Singh N, Rogers P, Atwood CW, Wagener MM, Yu VL (1 August 2000). "Short-course Empiric Antibiotic Therapy for Patients with Pulmonary Infiltrates in the Intensive Care Unit A Proposed Solution for Indiscriminate Antibiotic Prescription". Am. J. Respir. Crit. Care Med. 162 (2): 505–511. doi:10.1164/ajrccm.162.2.9909095. PMID 10934078.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Gleisner AL, Argenta R, Pimentel M, Simon TK, Jungblut CF, Petteffi L, de Souza RM, Sauerssig M, Kruel CD, Machado AR (30 April 2004). "Infective complications according to duration of antibiotic treatment in acute abdomen". International Journal of Infectious Diseases. 8 (3): 155–162. doi:10.1016/j.ijid.2003.06.003. PMID 15109590.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Pichichero ME, Cohen R (1997). "Shortened course of antibiotic therapy for acute otitis media, sinusitis and tonsillopharyngitis". The Pediatric Infectious Disease Journal. 16 (7): 680–95. doi:10.1097/00006454-199707000-00011. PMID 9239773.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Dellinger EP, Wertz MJ, Lennard ES, Oreskovich MR (1986). "Efficacy of Short-Course Antibiotic Prophylaxis After Penetrating Intestinal Injury". Archives of Surgery. 121 (1): 23–30. doi:10.1001/archsurg.1986.01400010029002. PMID 3942496.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Perez-Gorricho B, Ripoll M (2003). "Does short-course antibiotic therapy better meet patient expectations?". International Journal of Antimicrobial Agents. 21 (3): 222–8. doi:10.1016/S0924-8579(02)00360-6. PMID 12636982.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Keren R, Chan E (2002). "A Meta-analysis of Randomized, Controlled Trials Comparing Short- and Long-Course Antibiotic Therapy for Urinary Tract Infections in Children". Pediatrics. 109 (5): E70–0. doi:10.1542/peds.109.5.e70. PMID 11986476.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ McCormack J, Allan GM (2012). "A prescription for improving antibiotic prescribing in primary care". British Medical Journal. 344: d7955. doi:10.1136/bmj.d7955. PMID 22302779.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Marc Bonten, MD; Eijkman-Winkler Institute for Medical Microbiology, Utrecht, the Netherland | Infectious Diseases, and Inflammation เก็บถาวร 17 พฤษภาคม 2013 ที่ เวย์แบ็กแมชชีน
- ↑ Tacconelli E, De Angelis G, Cataldo MA, Pozzi E, Cauda R (January 2008). "Does antibiotic exposure increase the risk of methicillin-resistant Staphylococcus aureus (MRSA) isolation? A systematic review and meta-analysis". J. Antimicrob. Chemother. 61 (1): 26–38. doi:10.1093/jac/dkm416. PMID 17986491.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Muto CA, Jernigan JA, Ostrowsky BE, Richet HM, Jarvis WR, Boyce JM, Farr BM (May 2003). "SHEA guideline for preventing nosocomial transmission of multidrug-resistant strains of Staphylococcus aureus and enterococcus" (PDF). Infect Control Hosp Epidemiol. 24 (5): 362–86. doi:10.1086/502213. PMID 12785411. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2016-04-18. สืบค้นเมื่อ 2018-02-20.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Vonberg, Dr Ralf-Peter. "Clostridium difficile: a challenge for hospitals". European Center for Disease Prevention and Control. Institute for Medical Microbiology and Hospital Epidemiology: IHE. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 11 June 2009. สืบค้นเมื่อ 27 July 2009.
- ↑ Kuijper EJ, van Dissel JT, Wilcox MH (Aug 2007). "Clostridium difficile: changing epidemiology and new treatment options". Current Opinion in Infectious Diseases. 20 (4): 376–83. doi:10.1097/QCO.0b013e32818be71d. PMID 17609596.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Thomas JK, Forrest A, Bhavnani SM, Hyatt JM, Cheng A, Ballow CH, Schentag JJ (March 1998). "Pharmacodynamic Evaluation of Factors Associated with the Development of Bacterial Resistance in Acutely Ill Patients during Therapy". Antimicrob. Agents Chemother. 42 (3): 521–7. PMC 105492. PMID 9517926.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ Girou E, Legrand P, Soing-Altrach S, Lemire A, Poulain C, Allaire A, Tkoub-Scheirlinck L, Chai SH, Dupeyron C, Loche CM (October 2006). "Association between hand hygiene compliance and methicillin-resistant Staphylococcus aureus prevalence in a French rehabilitation hospital". Infect Control Hosp Epidemiol. 27 (10): 1128–30. doi:10.1086/507967. PMID 17006822.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)(ต้องรับบริการ) - ↑ "Antibiotic resistance". World Health Organization.
- ↑ "1.6.7". Access online: OIE - World Organisation for Animal Health. www.oie.int. สืบค้นเมื่อ 2015-11-14.
- ↑ "1.6.8". Access online: OIE - World Organisation for Animal Health. www.oie.int. สืบค้นเมื่อ 2015-11-14.
- ↑ "1.6.9". Access online: OIE - World Organisation for Animal Health. www.oie.int. สืบค้นเมื่อ 2015-11-14.
- ↑ 60.0 60.1 60.2 Wright GD (October 2010). "Antibiotic resistance in the environment: a link to the clinic?". Current Opinion in Microbiology. 13 (5): 589–94. doi:10.1016/j.mib.2010.08.005. PMID 20850375.(ต้องรับบริการ)
- ↑ D'Costa, Vanessa; King, Christine; Kalan, Lindsay; Morar, Mariya; Sung, Wilson; Schwarz, Carsten; Froese, Duane; Zazula, Grant; Calmels, Fabrice; Debruyne, Regis; Golding, G. Brian; Poinar, Hendrik N.; Wright, Gerard D. (September 2011). "Antibiotic resistance is ancient". Nature. 477 (7365): 457–461. Bibcode:2011Natur.477..457D. doi:10.1038/nature10388. PMID 21881561.
- ↑ Pawlowski, Andrew C; Wang, Wenliang; Koteva, Kalinka; Barton, Hazel; McArthur, Andrew G; Wright, Gerard D (December 2016). "A diverse intrinsic antibiotic resistome from a cave bacterium". Nature Communications. 7: 1–10. Bibcode:2016NatCo...713803P. doi:10.1038/ncomms13803. PMID 27929110.
- ↑ "Mutations are random". University of California. สืบค้นเมื่อ Aug 14, 2011.
- ↑ Richard William Nelson. Darwin, Then and Now: The Most Amazing Story in the History of Science, i Universe, 2009, p. 294
- ↑ Kiser, J.S.; Gale, G.O.; Kemp, G.A. (1970). "3.2 Resistance to Antimicrobial Agents: Evolution of Drug Resistance". Advances in Applied Microbiology. Vol. 11. Academic Press. p. 80. ISBN 978-0-08-056425-8.
- ↑ Pollock MR (1967). "Origin and function of penicillinase: a problem in biochemical evolution". British Medical Journal. 4 (5571): 71–7. doi:10.1136/bmj.4.5571.71. PMC 1748446. PMID 4963324.(ต้องรับบริการ)
- ↑ 67.0 67.1 "Some bacteria choose to live in a pool of penicillin". New Scientist. 54 (799): 546. 8 June 1972.
- ↑ 68.0 68.1 Siddal, R. (11 February 1989). "Ancient bacteria resitent to some antibiotics". New Scientist. 121 (1651): 34. Bibcode:1989NewSc.121...34H.
- ↑ Pollock, p. 77
- ↑ Sieler, Claudia; Berendonk, Thomas U (December 14, 2012). "Heavy metal driven co-selection of antibiotic resistance in soil and water bodies impacted by agriculture and aquaculture". Frontiers in Microbiology. 3: 399. doi:10.3389/fmicb.2012.00399. PMC 3522115. PMID 23248620.
- ↑ Levy, Stuart B. (2002-01-01). "Factors impacting on the problem of antibiotic resistance". Journal of Antimicrobial Chemotherapy. 49 (1): 25–30. doi:10.1093/jac/49.1.25. ISSN 0305-7453. PMID 11751763.
- ↑ Marti, Elisabet; Variatza, Eleni; Balcazar, Jose Luis (2014-01-01). "The role of aquatic ecosystems as reservoirs of antibiotic resistance". Trends in Microbiology. 22 (1): 36–41. doi:10.1016/j.tim.2013.11.001. ISSN 0966-842X. PMID 24289955.
- ↑ 73.0 73.1 Martinez, J. L., & Olivares, J. (2012). Envrionmental Pollution By Antibiotic Resistance Genes. In P. L. Keen, & M. H. Montforts, Antimicrobial Resistance in the Environment (pp. 151- 171). Hoboken, N.J.: John Wiley & Sons.
- ↑ Walsh, Timothy R; Weeks, Janis; Livermore, David M; Toleman, Mark A. "Dissemination of NDM-1 positive bacteria in the New Delhi environment and its implications for human health: an environmental point prevalence study". The Lancet Infectious Diseases. 11 (5): 355–362. doi:10.1016/s1473-3099(11)70059-7.
- ↑ 75.0 75.1 Araya P (May 2016). "The Impact of Water and Sanitation on Diarrhoeal Disease Burden and Over-Consumption of Anitbiotics" (PDF). เก็บ (PDF)จากแหล่งเดิมเมื่อ 1 October 2017. สืบค้นเมื่อ 12 November 2017.
- ↑ Rose JM, Gast RJ, Bogomolni A, Ellis JC, Lentell BJ, Touhey K, Moore M (2009). "Occurrence and patterns of antibiotic resistance in vertebrates off the Northeastern United States coast". FEMS Microbiol. Ecol. 67 (3): 421–31. doi:10.1111/j.1574-6941.2009.00648.x. PMID 19187217.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Centers for Disease Control and Prevention (2015). "Healthy Living". สืบค้นเมื่อ July 23, 2015.
- ↑ Lee, J. H.; Park, K. S.; Karim, A. M.; Lee, C.-R.; Lee, S. H. (2016). "How to minimise antibiotic resistance". Lancet Infect. Dis. (ภาษาอังกฤษ). 16 (1): 17–18. doi:10.1016/S1473-3099(15)00467-3. PMID 26738826.
บรรณานุกรม[แก้]
หนังสือ[แก้]
- Caldwell R, Lindberg D, บ.ก. (2011). "Understanding Evolution" [Mutations are random]. University of California Museum of Paleontology.
- Reynolds LA, Tansey EM, บ.ก. (2008). Superbugs and superdrugs : a history of MRSA : the transcript of a Witness Seminar held by the Wellcome Trust Centre for the History of Medicine at UCL, London, on 11 July 2006. London: Wellcome Trust Centre for the History of Medicine at UCL. ISBN 978-0-85484-114-1.
- Stemming the Superbug Tide: Just A Few Dollars More. OECD Health Policy Studies. Paris: OECD Publishing. 2018. doi:10.1787/9789264307599-en. ISBN 9789264307582. S2CID 239804815.
วารสาร[แก้]
- Arias CA, Murray BE (January 2009). "Antibiotic-resistant bugs in the 21st century--a clinical super-challenge". The New England Journal of Medicine. 360 (5): 439–43. doi:10.1056/NEJMp0804651. PMID 19179312. S2CID 205104375.
- "Special Issue: Ethics and Antimicrobial Resistance". Bioethics. 365 (33). 2019.
- Goossens H, Ferech M, Vander Stichele R, Elseviers M (2005). Esac Project. "Outpatient antibiotic use in Europe and association with resistance: a cross-national database study". Lancet. Group Esac Project. 365 (9459): 579–87. doi:10.1016/S0140-6736(05)17907-0. PMID 15708101. S2CID 23782228.
- Hawkey PM, Jones AM (September 2009). "The changing epidemiology of resistance" (PDF). The Journal of Antimicrobial Chemotherapy. 64 (Suppl 1): i3-10. doi:10.1093/jac/dkp256. PMID 19675017.
- Soulsby EJ (November 2005). "Resistance to antimicrobials in humans and animals". BMJ. 331 (7527): 1219–20. doi:10.1136/bmj.331.7527.1219. PMC 1289307. PMID 16308360.
- "Alternatives to Antibiotics Reduce Animal Disease". Commonwealth Scientific and Industrial Research Organization. 9 January 2006.
- Cooke P, Rees-Roberts D (2017). CATCH. 16-minute film about a post-antibiotic world. Review: Sansom C (March 2017). "Media Watch: An intimate family story in a world without antibiotics". Lancet Infect Dis. 17 (3): 274. doi:10.1016/S1473-3099(17)30067-1.
แหล่งข้อมูลอื่น[แก้]
- แบคทีเรียดื้อยา ที่เว็บไซต์ Curlie (ภาษาอังกฤษ)
- แอนิเมชันเกี่ยวกับจุลชีพดื้อยา (ภาษาอังกฤษ)
- "แนวทางการจัดการโรคที่เกิดจากการติดเชื้อจุลชีพดื้อยาหลายขนานในสถานพยาบาล 2006" ของศูนย์ควบคุมและป้องกันโรค ประเทศสหรัฐอเมริกา (ภาษาอังกฤษ)
- โครงการการเฝ้าระวังการใช้ยาต้านจุลชีพ, ศูนย์วิจัยและนโยบายด้านโรคติดต่อ (Center for Infectious Disease Research and Policy; CIDRAP), มหาวิทยาลัยมินนิโซตา (ภาษาอังกฤษ)
- พันธมิตรอุตสาหกรรมด้านการดื้อยาของจุลชีพ (AMR Industry Alliance), ประกอบด้วยสมาชิกจากบริษัทขนาดใหญ่ที่ดำเนินกิจการด้านการวิจัยและพัฒนายา โรงงานยา บริษัทด้านเทคโนโลยีชีวภาพ และบริษัที่เกี่ยวเนื่องกับงานด้านการวินิจฉัยโรคติดเชื้อ (ภาษาอังกฤษ)
