การตรวจโรคติดเชื้อไวรัสโคโรนา 2019

การตรวจทางห้องปฏิบัติการเพื่อหาโรคติดเชื้อโคโรนาไวรัส 2019 (COVID-19) และหาเชื้ออันเป็นสาเหตุโรคคือไวรัสโคโรนาสายพันธุ์ใหม่ (SARS-CoV-2) มีอยู่หลายวิธี รวมทั้งวิธีตรวจเชื้อไวรัสโดยตรง (เช่น RT-PCR, INAA และแอนติเจน) และวิธีตรวจสารภูมิต้านทานที่ร่างกายสร้างตอบสนองต่อการติดเชื้อไวรัส มีประโยชน์ทั้งเพื่อตรวจวินิจฉัยและรักษา และเพื่อสอดส่องการติดโรคของประชากร ทั้งสามารถแสดงจำนวนคนติดเชื้อแล้วแม้ในผู้มีอาการน้อยหรือไม่มีอาการเลย จึงสามารถใช้วัดอัตราตาย (mortality rate) และระดับภูมิคุ้มกันหมู่ในกลุ่มประชากรได้ แต่ระยะเวลาและประสิทธิภาพของภูมิคุ้มกันที่ว่านี้ก็ยังไม่ชัดเจน[1] และอัตราผลบวกลวงและผลลบลวงก็ต้องพิจารณาด้วย
การตรวจเหล่านี้ยังจำกัดมาก จนถึงเดือนมีนาคม 2020 ก็ยังไม่มีประเทศใดซึ่งมีข้อมูลที่เชื่อถือได้เกี่ยวกับความชุกโรคในกลุ่มประชากรของตน ๆ[2] จนถึงวันที่ 29 เมษายน ประเทศที่เผยแพร่ข้อมูลได้ตรวจโรคในอัตราเพียงแค่ร้อยละ 1.4 ของประชากรทั้งประเทศ ไม่มีประเทศใดที่สุ่มตัวอย่างเกินร้อยละ 14 ของประชากรทั้งประเทศ[3] ประเทศต่าง ๆ ได้ตรวจมากน้อยไม่เท่ากัน[4] ความผันแปรเช่นนี้คงส่งผลต่ออัตราป่วยตาย (CFR) ของโรค ซึ่งน่าจะประเมินเกินในประเทศต่าง ๆ เนื่องกับอคติในการสุ่มตัวอย่าง[5][6][7]
ในวันที่ 2 พฤษภาคม ประเทศไทยได้ตรวจคน 72,745 คนโดยมีผู้ติดโรคในประเทศ 2,966 คนและมีผู้เสียชีวิตแล้ว 54 คน[8]
วิธีการตรวจ
[แก้]วิธีการตรวจสามารถแยกเป็นสองหมวดใหญ่ ๆ เพราะมีประโยชน์แตกต่างกัน วิธีตรวจบางอย่างสืบหาตัวไวรัสโดยตรง เช่น RT-PCR เป็นต้น ส่วนวิธีอื่นตรวจสารภูมิต้านทานที่ร่างกายสร้างตอบสนองต่อการติดเชื้อไวรัส ทางเลือกอีกอย่างก็คือตรวจดูความเสียหายของปอดด้วยเอกซ์เรย์คอมพิวเตอร์หรือการตรวจว่าได้ออกซิเจนน้อย เพราะเมื่อตรวจด้วย RT-PCR ไวรัสจะต้องมีมากพอสมควร จึงมีผลลบลวงบ้างโดยเฉพาะโรคระยะต้น ๆ (เพราะไวรัสยังมีไม่มากพอ)
โรคที่กำลังเป็น
[แก้]ปฏิกิริยาลูกโซ่พอลิเมอเรส
[แก้]ปฏิกิริยาลูกโซ่พอลิเมอเรส (PCR) เป็นกระบวนการถ่ายแบบส่วนเฉพาะเล็ก ๆ ของดีเอ็นเอให้เพิ่มจำนวนเป็นแสนเท่า ๆ จึงทำให้มีพอในการตรวจจับหรือวิเคราะห์ได้ แต่ไวรัสต่าง ๆ รวมทั้ง SARS-CoV-2 ก็ไม่มีดีเอ็นเอ มีแต่อาร์เอ็นเอ[9] ตัวอย่างที่ได้จากทางลมหายใจของคนไข้จะนำมาทำปฏิกิริยากับสารเคมีบางอย่าง[10][9] ซึ่งกำจัดสารส่วนเกินอื่น ๆ และชักเอาแต่อาร์เอ็นเอมาจากตัวอย่าง ส่วนปฏิกิริยาลูกโซ่พอลิเมอเรสแบบย้อนกลับ (RT-PCR) เป็นเทคนิคที่เบื้องต้นใช้เอนไซม์รีเวิร์สแทรนสคริปเทสเปลี่ยนอาร์เอ็นเอให้เป็นดีเอ็นเอ แล้วใช้ PCR เพื่อถ่ายแบบดีเอ็นเอให้มีประมาณพอตรวจดูว่าเป็นยีนของไวรัสหรือไม่[9] ส่วนปฏิกิริยาลูกโซ่พอลิเมอเรสในเวลาจริง (Real-time PCR หรือ qPCR)[11] เป็นเทคนิคที่เร่งระยะ PCR ของกระบวนการเช่นนี้ เป็นปฏิบัติการอัตโนมัติที่ทำได้ไวและผิดพลาดน้อยกว่า จึงกลายเป็นวิธีที่มักเลือกทำ[12][13] เทคนิคเหล่านี้รวม ๆ กันอาจเรียกในภาษาอังกฤษว่า real-time RT-PCR (ปฏิกิริยาลูกโซ่พอลิเมอเรสแบบย้อนกลับในเวลาจริง)[14] หรือ quantitative RT-PCR[15] จึงบางครั้งย่อเป็น qRT-PCR[16] หรือเป็น rRT-PCR[17] หรือเป็น RT-qPCR[18] แม้บางครั้งก็อาจใช้คำย่อว่า RT-PCR หรือ PCR เฉย ๆ
ตัวอย่างที่ใช้ตรวจจะมาจากทางเดินหายใจที่ได้โดยวิธีต่าง ๆ รวมทั้งการป้ายกวาดทางจมูกร่วมคอหอย (nasopharyngeal swab) หรือจากเสมหะ[19] หรือจากน้ำลาย[20] ผลจะได้ภายในไม่กี่ ชม. จนถึง 2 วัน[21]
เมื่อตรวจผู้ที่ติดโรค โอกาสพบไวรัสจะขึ้นอยู่กับเวลาที่ผ่านไปหลังติดเชื้อ การตรวจการป้ายกวาดจากคอด้วยวิธีนี้ จะเชื่อถือได้ก็ภายใน 1 อาทิตย์แรกหลังติดโรคเท่านั้น เพราะต่อจากนั้นตัวไวรัสจะไม่มีในคอแต่ก็ยังเพิ่มพูนในปอด สำหรับคนที่เป็นโรคในอาทิตย์ที่สอง สามารถเอาตัวอย่างจากทางเดินหายใจส่วนลึกด้วยการดูดด้วยหลอดสวน หรือเสมหะที่ไอขึ้นมาก็ใช้ได้[22] ในงานศึกษาหนึ่ง การตรวจได้ผลบวกสูงสุดสำหรับคนติดโรคในอาทิตย์แรก คือ 100% ตามด้วย 89.3%, 66.1%, 32.1%, 5.4% และ 0% ในอาทิตย์ที่ 2-3-4-5-6 ตามลำดับ[23][24]
น้ำลายได้แสดงแล้วว่า เป็นสื่อนำไวรัสที่สามัญแต่ชั่วคราว[25] และผลที่รายงานไปยังองค์การอาหารและยาสหรัฐแสดงว่า มันอาจมีประสิทธิผลเท่ากับการป้ายกวาดจากจมูกหรือคอ[20] เมื่อกลางเดือนเมษายน องค์การอาหารและยาสหรัฐได้อนุมัติผ่านมาตรการฉุกเฉินให้ใช้การตรวจน้ำลายแทนการป้ายกวาดทางจมูก[26] เชื่อว่า นี่จะลดความเสี่ยงต่อแพทย์พยาบาล[27] สบายต่อคนไข้มากกว่า[26] และทำให้ผู้ที่กักตัวสามารถเก็บตัวอย่างของตัวเองได้อย่างมีประสิทธิภาพกว่า[27]
แต่ตามผู้เชี่ยวชาญบางท่าน ยังมีข้อมูลเกี่ยวกับการตรวจน้ำลายน้อยเกินไป ไม่ชัดเจนว่ามันไวโรคเท่ากับการตรวจด้วยการป้ายกวาดคอและจมูกหรือไม่[28][25] มีงานศึกษาบางงานที่ชี้ว่า ประโยชน์ในการวินิจฉัยโรคของน้ำลายขึ้นอยู่กับว่าได้มาจากที่ไหน (เช่น คอส่วนลึก ช่องปาก หรือจากต่อมน้ำลาย)[25] งานศึกษาหนึ่งที่คณะสาธารณสุขของมหาวิทยาลัยเยลพบว่า น้ำลายช่วยให้ตรวจโรคได้ไวและสม่ำเสมอกว่าในช่วงติดโรคทั้งหมดเมื่อเทียบกับตัวอย่างที่ได้จากการป้ายกวาดจมูกและคอ[29][30]
-
การป้ายกวาดทางจมูกร่วมคอหอยเพื่อตรวจโรค
-
การป้ายกวาดที่คอเพื่อตรวจโรค
-
เครื่อง PCR
Isothermal amplification assays
[แก้]มีวิธีการตรวจด้วย isothermal nucleic acid amplification หลายอย่างที่มีหลักคล้ายกับปฏิกิริยาลูกโซ่พอลิเมอเรส (PCR) คือถ่ายแบบส่วนจีโนมของไวรัส แต่เร็วกว่าเพราะไม่ต้องมีวงจรเพิ่มความร้อนและลดความร้อนที่ต้องทำซ้ำ ๆ กับตัวอย่างที่ได้
แอนติเจน
[แก้]วันที่ 9 พฤษภาคม 2020 สหรัฐได้อนุมัติให้ใช้ชุดตรวจแอนติเจนโรคโควิดเป็นชุดแรก[31] ซึ่งแม้จะไม่แม่นยำเท่ากับ RT-PCR เมื่อแสดงผลลบ แต่ก็ให้ผลได้เร็วกว่าและราคาถูกกว่า[31] และถ้าให้ผลบวกก็มักจะถูกต้อง[31]
แอนติเจนเป็นส่วนของจุลชีพก่อโรคที่ร่างกายตอบสนองทางภูมิคุ้มกัน เทียบกับการตรวจด้วย RT-PCR ที่สืบหาอาร์เอ็นเอของไวรัส กับการตรวจแอนติบอดีที่ตรวจสารภูมิต้านทานมนุษย์ซึ่งร่างกายสร้างตอบสนองต่อไวรัส (สืบหาได้หลังจากติดโรคเป็นวัน ๆ หรือเป็นอาทิตย์ ๆ) การตรวจแอนติเจนจะสืบหาโปรตีนที่ผิวของไวรัส ในกรณีโคโรนาไวรัส ปกติจะเป็นโปรตีนที่ปรากฏเป็นเดือยที่ผิวของไวรัส และจะใช้การป้ายกวาดจมูกเพื่อเก็บตัวอย่างจากช่องจมูก[32] ปัญหาอย่างหนึ่งก็คือการหาโปรตีนที่เฉพาะต่อ SARS-CoV-2[33] เช่น มีโคโรนาไวรัสที่เป็นญาติกันซึ่งก่อหวัดธรรมดา[34]
คนพวกหนึ่งเชื่อว่า นี่เป็นวิธีเดียวที่ให้ตรวจคนที่กำลังเป็นโรคจำนวนมาก ๆ ได้[32] เพราะการตรวจด้วย INAA เช่น ที่จำหน่ายโดยบริษัทแอบบอตต์ สามารถตรวจตัวอย่างทีละตัวอย่างต่อเครื่องเท่านั้น และการตรวจด้วย RT-PCR แม้แม่นยำก็ใช้เวลาและพลังงานมากบวกกับบุคลากรที่ต้องฝึกเพื่อปฏิบัติการ[32]
ตัวอย่างที่ได้จากจมูกของคนไข้จะใช้ป้ายริ้วกระดาษที่มีสารภูมิต้านทานเทียมซึ่งออกแบบให้จับกับแอนติเจนของไวรัส ดังนั้น แอนติเจนที่มีในตัวอย่างจะจับกับริ้วกระดาษแล้วแสดงผลให้เห็น โดยทำได้ภายใน 30 นาที ให้ผลในที่ที่ตรวจ ไม่ต้องใช้อุปกรณ์ราคาแพงและไม่ต้องฝึกบุคลากร[32] ปัญหาสำหรับไวรัสที่ก่อโรคระบบหายใจก็คือมักไม่มีแอนติเจนในตัวอย่างเพียงพอให้ตรวจจับได้[33] ซึ่งเป็นจริงอย่างยิ่งสำหรับผู้ที่ไร้อาการและมีน้ำมูกไหลน้อยมาก ไม่เหมือนกับการตรวจด้วย RT-PCR ซึ่งถ่ายแบบยีนจำนวนน้อย ๆ ให้กลายเป็นจำนวนมากเพื่อให้ตรวจจับได้ การตรวจทางแอนติเจนไม่ขยายจำนวนโปรตีนของไวรัส[32][35]
ตามข้อมูลขององค์การอนามัยโลก ความไวของชุดตรวจแอนติเจนคล้าย ๆ กันสำหรับโรคระบบหายใจอื่น ๆ เช่น ไข้หวัดใหญ่ อยู่ที่ระหว่างอัตราร้อยละ 34-80 องค์กรจึงแถลงการณ์ว่า "ตามข้อมูลนี้ การตรวจเช่นนี้จะพลาดไม่พบคนไข้ผู้ติดโรคโควิด-19 ครึ่งหนึ่งหรือยิ่งกว่า โดยขึ้นอยู่กับกลุ่มคนไข้" นักวิทยาศาสตร์จำนวนมากตั้งข้อสงสัยว่า จะสามารถพัฒนาการตรวจแอนติเจนที่เชื่อถือได้เพียงพอให้ทันเป็นประโยชน์ในเหตุการณ์โรคระบาดทั่วหรือไม่[35] แต่ตามองค์การอาหารและยาสหรัฐ ผลบวกจากการตรวจแอนติเจนแม่นยำมาก แต่ก็มีโอกาสได้ผลลบลวงมากกว่า ดังนั้น การได้ผลลบจึงไม่ได้ชี้ว่า ไม่ติดโรค[36]
การสร้างภาพ
[แก้]เอกซเรย์คอมพิวเตอร์ที่หน้าอก (CT scan) ไม่แนะนำสำหรับการตรวจคัดกรองโรคทั่วไป เพราะสิ่งที่แสดงไม่เฉพาะเจาะจงต่อโรคโควิด[37][38] ลักษณะทั่วไปเบื้องต้นที่มักพบของโรครวมภาพคล้ายกับกระจกฝ้า (ground glass opacity) กระจายไปที่พูหลายพูในปอดทั้งสอง โดยกระจายไปแบบรอบ ๆ (peripheral) หรือที่ด้านหลัง (posterior)[38] และต่อไปอาจเกิดลักษณะต่าง ๆ เช่น ลักษณะมีรอยโรคเด่นที่เนื้อปอดด้านนอกใต้เยื่อหุ้มปอด (subpleural dominance), ผนังกั้นกลีบปอดย่อยหนาตัวพร้อมกับมีสารน้ำเติมเต็มถุงลมเห็นเป็นลักษณะคล้ายกระเบื้องปูพื้นถนน (crazy-paving pattern), และเนื้อปอดทึบ (consolidation)[A][38][40]
-
ภาพเอกซเรย์คอมพิวเตอร์ทั่วไปของโรคโควิด
-
ภาพเอกซเรย์คอมพิวเตอร์ในช่วงที่โรคลุกลามอย่างรวดเร็ว
การติดเชื้อในอดีต
[แก้]การตรวจเลือด (ทางวิทยาเซรุ่ม) ทำกับเลือดที่ดูดออก ไม่ใช่การป้ายกวาดตัวอย่างที่จมูกหรือคอ และสามารถระบุบุคคลที่ติดเชื้อแล้วฟื้นสภาพจากโรคโควิด รวมทั้งผู้ที่ไม่รู้ว่าตนติดโรค[41] การพัฒนาการตรวจทางวิทยาเซรุ่มโดยมากอยู่ในระยะวิจัย[42]
ร่างกายตอบสนองทางภูมิต้านทานต่อการติดเชื้อส่วนหนึ่งโดยสร้างสารภูมิต้านทาน (แอนติบอดี) เช่น แบบ IgM และ IgG ตามองค์การอาหารและยาสหรัฐ แบบ IgM ที่เนื่องกับเชื้อ SARS-CoV-2 ทั่วไปสามารถตรวจพบในเลือดหลังจากติดเชื้อแล้วหลายวัน แม้ระดับต่าง ๆ ในช่วงติดโรคยังไม่ชัดเจน[43] ส่วนแบบ IgG ปกติจะตรวจจับได้หลังจากติดเชื้อ 10-14 วันแต่ก็อาจพบก่อนหน้านั้น และปกติจะถึงระดับสูงสุดราว 28 วันหลังติดเชื้อ[44][45] เพราะสารภูมิต้านทานเกิดช้า จึงไม่สามารถบ่งการติดเชื้อซึ่งกำลังเป็นได้ดีที่สุด แต่เพราะอาจคงยืนในเลือดเป็นเวลาหลายปี จึงดีเพื่อตรวจประวัติการติดเชื้อ[32]
การรตรวจสารภูมิต้านทางสามารถใช้กำหนดอัตราประชากรที่ได้ติดโรค และสมมุติว่ามีภูมิคุ้มกันแล้ว แต่ก็ยังไม่ชัดเจนว่า ภูมิคุ้มกันที่ว่านี่แข็งแรงแค่ไหนและมีผลนานเท่าไร[1][46] ในเดือนเมษายน 2020 "ประเทศหลายประเทศกำลังพิจารณาการออกเอกสารที่เรียกว่าพาสปอร์ตภูมิคุ้มกันหรือใบรับรองว่าไม่เสี่ยงโรคสำหรับผู้ที่มีสารภูมิต้านทานต่อต้านโควิด-19 เพื่ออนุญาตให้เดินทางได้ หรือกลับไปทำงาน โดยสมมุติว่า ไม่เสี่ยงติดเชื้ออีก"[47] แต่ในวันที่ 24 เมษายน 2020 องค์การอนามัยโลกก็แจ้งว่า "ปัจจุบันยังไม่มีหลักฐานว่า ผู้ที่ฟื้นจากโรค COVID-19 แล้วและมีสารภูมิต้านทานจะปลอดภัยจากการติดเชื้อเป็นครั้งที่สอง"[48] เหตุผลของความไม่แน่นอนอย่างหนึ่งก็คือ การตรวจสารภูมิต้านทานที่ทำอย่างกว้างขวางโดยมากตรวจจับสารภูมิต้านทานที่เข้ายึด (binding) กับแอนติเจน ไม่ใช้สารภูมิต้านทานกำจัดฤทธิ์เชื้อ (neutralizing)[49][50][51][52] สารภูมิต้านทานที่กำจัดฤทธิ์ของเชื้อ (neutralizing antibody ตัวย่อ NAb) เป็นสารภูมิต้านทานที่ป้องกันเซลล์จากจุลชีพก่อโรคหรือเชื้อแบบอนุภาคโดยกำจัดฤทธิ์ทางชีวภาพของมัน[53] ในขณะที่สารภูมิต้านทานที่เข้ายึดกับเชื้อ (binding antibody) จะยึดกับเชื้อโดยไม่กำจัดฤทธิ์ของมัน แต่ยึดเพื่อระบุให้ระบบภูมิต้านทานทำลายเชื้อนี้[54] โดบอาจเพิ่มฤทธิ์ของเชื้อเนื่องกับปฏิกิริยากับหน่วยรับบนผิวของมาโครฟาจ (macrophage)[B][56] เพราะการตรวจโรคโดยมากจะให้ผลบวกเมื่อเจอสารภูมิต้านทานแบบเข้ายึด ดังนั้น การตรวจเช่นนี้จึงไม่สามารถระบุได้ว่า บุคคลนั้นได้สร้างภูมิต้านทานแบบกำจัดฤทธิ์เชื้อซึ่งจะทำให้ไม่ติดโรคอีกหรือไม่[50][52]
อย่างไรก็ดี ปกติก็คาดกันว่า ถ้ามีสารภูมิต้านทานแบบเข้ายึด ก็จะมีสารภูมิต้านทานแบบกำจัดฤทธิ์เชื้อด้วย[52] และในบรรดาโรคไวรัสต่าง ๆ การตอบสนองทางภูมิต้านทางรวม ๆ กันทั้งหมดก็จะมีสหสัมพันธ์กับการตอบสนองด้วยสารภูมิต้านทานแบบกำจัดฤทธิ์เชื้อ[57] แต่นี่ยังไม่ชัดเจนสำหรับโควิด และถ้าสมมุติได้ว่า เมื่อติดโรคแล้ว โอกาสการติดเชื้อเป็นครั้งที่สองภายใน 2-3 เดือนต่อมาจะน้อย ภูมิป้องกันเช่นนี้จะอยู่นานเท่าไรก็ยังไม่รู้[50] งานศึกษาในประเทศจีนกับคนไข้ 175 คนที่ฟื้นตัวจากโรคและมีอาการน้อยรายงานว่า คน 10 คนไม่มีสารภูมิต้านทานที่กำจัดฤทธิ์เชื้อในระดับที่ตรวจจับได้เมื่อออกจาก รพ. และก็ไม่มีในกาลต่อ ๆ มาด้วย คนไข้เหล่านี้ฟื้นตัวโดยไม่มีสารภูมิต้านทานกำจัดฤทธิ์เชื้อได้อย่างไร และเสี่ยงติดโรคอีกหรือไม่ ยังต้องตรวจสอบกันอีกต่อไป[50][58] อนึ่ง แม้จะมีสารภูมิต้านทานกำจัดฤทธิ์เชื้อ แต่โรคไวรัสหลายอย่าง เช่น เอชไอวี ก็ได้วิวัฒนาการกลไกหลีกเลี่ยงการตอบสนองทางภูมิต้านทานเช่นนี้ อย่างไรก็ดี แม้ยังต้องตรวจดูในเรื่องโควิด แต่ประสบการณ์การติดเชื้อไวรัสในอดีตก็ได้แสดงว่า ระดับสารภูมิต้านทานกำจัดฤทธิ์เชื้อในคนไข้ที่ฟื้นสภาพเป็นตัวบ่งที่ดีว่ามีภูมิคุ้มกันโรค[49]
ปกติจะสมมุติว่า เมื่อติดโรคแล้ว การติดโรคเป็นครั้งที่สอง 2-3 เดือนหลังจากนั้นมีโอกาสน้อย แต่ภูมิต้านทานเช่นนี้จะคงยืนยาวนานแค่ไหนก็ไม่ชัดเจน[50] งานศึกษาหนึ่งแสดงว่า ในลิงวอกที่ติดเชื้อ SARS-CoV-2 ลิงจะไม่ติดอีกที่ 29 วันหลังติดเชื้อ[59] งานศึกษาหลายงานได้แสดงว่า สารภูมิต้านทานกำจัดฤทธิ์ของเชื้อ (NAb) ไวรัสโรคซาร์ส (ซึ่งเป็นบรรพบุรุษของเชื้อ SARS-CoV-2) จะคงยืนในมนุษย์ส่วนมากเป็นเวลา 2 ปี[60] แล้วจะหายไปหลังจาก 6 ปี[61] แต่ memory cell รวมทั้ง Memory B cell ซึ่งผลิตสารภูมิต้านทาน และ Memory T cell ซึ่งกำจัดเชื้อโรคอาจคงยืนนานกว่ามาก และอาจทำให้การติดโรคอีกรุนแรงลดลง[61]
-
การตรวจโรคในที่ที่ตรวจคนไข้ (PoCT) ในประเทศเปรูโดยใช้ปิเปตต์/หลอดแก้วเก็บตัวอย่างเลือด
-
แล้วป้ายเลือดลงที่อุปกรณ์ตรวจวินิจฉัยโรคแบบเร็ว (RDT)
-
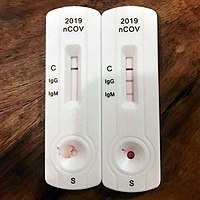
อุปกรณ์ตรวจวินิจฉัยโรคแบบเร็ว (RDT) สำหรับ COVID-19 แสดงการตอบสนองของสารภูมิต้านทานแบบ IgG และ IgM (ซ้าย) ไม่พบโรค (ขวา) พบสารภูมิต้านทานทั้งสองแบบ
ระยะที่สามารถตรวจจับไวรัสได้หรือระยะที่คนไข้มีไวรัสที่ทำให้ติดเชื้อ
[แก้]ศูนย์ควบคุมและป้องกันโรคสหรัฐ (CDC) ได้ให้ข้อมูลและคำแนะนำนี้ในวันที่ 3 พฤษภาคม[62] ศูนย์แจ้งว่า ณ ปัจจุบัน ยังมีข้อมูลจำกัดว่า คนไข้จะปล่อยอาร์เอ็นเอ SARV-CoV-2 ที่ทำให้คนอื่นติดโรคได้นานเท่าไรหลังติดเชื้อ ประเด็นสำคัญ ๆ สรุปไว้ดังต่อไปนี้
- ไวรัสในตัวอย่างจากทางลมหายใจส่วนบนจะลดลงหลังเริ่มป่วย[63]
- ณ ปัจจุบัน ไวรัสที่ถ่ายแบบตนเองได้ยังไม่สามารถเพาะได้หลังจาก 9 วันจากเริ่มป่วย ประเมินทางสถิติว่าโอกาสได้ไวรัสที่ถ่ายแบบตนเองได้จะเข้าสู่ศูนย์ในวันที่ 10[64]
- ในขณะที่การแยกไวรัสที่ถ่ายแบบตนเองได้มีโอกาสลดลง สารภูมิต้านทานต้าน SARS-CoV-2 คือ IgM และ IgG ก็จะตรวจจับได้ในบุคคลที่ฟื้นสภาพจากการติดเชื้อ โดยจำนวนบุคคลได้เพิ่มขึ้นเรื่อย ๆ ๆ[65]
- การเพาะไวรัสจากตัวอย่างทางเดินลมหายใจส่วนบนโดยมากไม่สำเร็จถ้าไวรัสมีน้อยแต่ยังสามารถตรวจจับได้ (คือ Ct values สูงกว่า 33-35)[62]
- หลังจากฟื้นสภาพจากอาการความเจ็บป่วย คนไข้จำนวนมากจะไม่มีอาร์เอ็นไวรัสที่ตรวจจับได้ในตัวอย่างที่ได้จากทางเดินหายใจส่วนบน ในบรรดาผู้ที่ยังคงมีอาร์เอ็นเอนที่ตรวจจับได้ ความเข้มข้นของอาร์เอ็นเอที่ตรวจจับได้หลังจากฟื้นสภาพทั่วไปจะอยู่ในพิสัยที่ CDC ไม่สามารถแยกไวรัสที่ถ่ายแบบตนเองได้เป็นเอกเทศอย่างเชื่อถือได้[66]
- ยังไม่พบสหสัมพันธ์ที่ชัดเจนระหว่างระยะที่ป่วยกับระยะหลังฟื้นสภาพที่คนไข้มีอาร์เอ็นเอของไวรัสในตัวอย่างทางเดินหายใจส่วนบน[67]
- ไวรัสที่ทำให้ติดเชื้อได้ยังไม่สามารถเพาะได้เลยจากปัสสาวะ และยังไม่สามารถเพาะอย่างเชื่อถือได้จากอุจจาระ[68] แหล่งไวรัสเหล่านี้มีความเสี่ยงทำให้ติดโรคน้อยหรือไม่มีเลย โดยที่ถ้าเสี่ยง ก็สามารถบรรเทาได้อย่างเพียงพอด้วยการรักษาความสะอาดมือ
สำหรับจุลชีพก่อโรคที่อุบัติใหม่เช่น SARS-CoV-2 รูปแบบและระยะของความเจ็บป่วยและการติดเชื้อได้ยังไม่ชัดเจน แต่ข้อมูลที่มีแสดงว่า การมีอาร์เอ็นเอของ SARS-CoV-2 ในตัวอย่างที่ได้จากทางเดินลมหายใจบนจะลดลงหลังการเกิดอาการ ในวันที่ 10 หลังเกิดเจ็บป่วย การได้ไวรัสที่ถ่ายแบบตนเองได้จากการเพาะไวรัส (โดยเป็นตัวแทนว่ามีไวรัสที่ทำให้ติดเชื้อ) จะลดลงและเข้าสู่ศูนย์ แม้บุคคลอาจจะมีตัวอย่างที่แสดงผลบวกด้วย PCR จนถึงอาทิตย์ที่ 6[69] แต่ก็ยังไม่ชัดเจนว่า ตัวอย่างที่ให้ผลบวกทาง PCR เช่นนี้หมายถึงการยังมีไวรัสที่แพร่โรคหรือไม่ เมื่อฟื้นสภาพหมดอาการแล้ว คนไข้จำนวนมากจะไม่ปล่อยอาร์เอ็นเอของไวรัส SARS-CoV-2 อีกต่อไป ในบรรดาคนไข้ที่ฟื้นสภาพโดยมีอาร์เอ็นเอในตัวอย่างทางเดินลมหายใจส่วนบนที่ตรวจจับได้ ความเข้มข้นของอาร์เอ็นเอหลัง 3 วันปกติจะอยู่ในพิสัยที่ CDC ไม่สามารถเพาะไวรัสอย่างเชื่อถือได้ ข้อมูลเช่นนี้ได้จากผู้ใหญ่ในกลุ่มอายุต่าง ๆ และเจ็บป่วยหนักเบาไม่เท่ากัน ส่วนข้อมูลจากเด็กและทารกปัจจุบันยังไม่มี[62]
การตรวจอย่างน้อยที่สุดและจำเป็น
[แก้]ตามนักวิทยาการระบาด เพราะกำลังผ่อนมาตรการล็อกดาวน์ การควบคุมโรคระบาดทั่วที่ได้ประสิทธิผลในสหรัฐจะเป็นไปไม่ได้จนกว่าคนที่ติดเชื้อแล้วทั้งหมดจะสามารถระบุและแยกตัวได้ก่อนทำให้คนอื่นติดโรค ซึ่งหมายความว่าต้องตรวจคนอย่างแพร่หลายแม้ก่อนปรากฏอาการ[70] การติดต่อได้ของโรคระบุได้โดยค่าสืบพันธุ์พื้นฐาน (R0) ค่า R0 (อ่านว่า อาร์น็อต)[71] ของเชื้อ SARS-CoV-2 ทั่วไปเชื่อว่าอยู่ระหว่าง 2.2-2.5[72] ซึ่งหมายความว่า ในกลุ่มประชากรที่คนทั้งหมดมีโอกาสเสี่ยงติดโรค คนที่ติดเชื้อคนหนึ่งคาดหวังว่าจะทำให้คนอื่น 2.2-2.5 คนติดเชื้อ[73] แต่นี่ก็สามารถต่าง ๆ กันในภูมิประเทศต่าง ๆ ได้[74] ในรัฐนิวยอร์ก R0 อยู่ระหว่าง 3.4-3.8[75] ความยากลำบากอย่างหนึ่งในการระงับไม่ให้โรคระบาดก็คือ โดยเฉลี่ยแล้ว ผู้ติดเชื้อจะแสดงอาการ 5 วันหลังติดเชื้อ (คือ มีระยะฟักตัวเฉลี่ย 5 วัน) และเริ่มทำให้คนอื่นติดโรค 2-3 วันก่อนปรากฏอาการ[72][76] ตามงานศึกษางานหนึ่ง ประเมินว่า การติดเชื้อไวรัสร้อยละ 44 เกิดภายในระยะ 2-3 วันที่ว่านี้[72][77] อนึ่ง คนที่ติดเชื้อจำนวนสำคัญไม่แสดงอาการเลยแต่ก็ยังทำให้คนอื่นติดโรค[77] ดังนั้น ถ้าจะระงับการแพร่เชื้อได้ ต้องตรวจและแยกตัวผู้ติดเชื้อก่อนปรากฏอาการ
ตามสถาบันสุขภาพของมหาวิทยาลัยฮาร์วาร์ด สหรัฐทั้งประเทศควรจะตรวจตัวอย่างมากว่า 900,000 ตัวอย่างต่อวัน[78][79] องค์กรอื่น ๆ ได้ให้ค่าประเมินอื่น ๆ มากจนถึง 23 ล้านตัวอย่างต่อวัน[80][81][82][83] ในสัปดาห์ซึ่งสุดวันที่ 7 พค. สหรัฐตรวจตัวอย่างโดยเฉลี่ย 248,000 รายการต่อวัน[79][84] ตามองค์การอนามัยโลก ถ้าตัวอย่างที่ตรวจพบว่ามีผลบวกเกิน 10% ก็ยังจัดว่า ตรวจคนจำนวนยังไม่พอ[85]
ตามนักวิทยาการระบาด การเพิ่มการตรวจเป็นจำนวนมหาศาลเยี่ยงนี้หมายความว่า รัฐจะต้องขยายสร้างโครงสร้างพื้นฐานเพื่อตรวจโรคเป็นอย่างมาก ซึ่งต้องรวมโปรแกรมการตรวจเคลื่อนที่ การตรวจในพื้นที่ ให้ความใส่ใจเป็นพิเศษกับกลุ่มเสี่ยง เช่น ในสถานพยาบาลระยะยาว คนจรจัด และเจ้าหน้าที่ของบริการให้สถานที่อยู่กับคนจรจัด ผู้ว่าจ้างในที่ทำงานแออัด และทุกคนที่เข้าใกล้คนไข้โควิดแล้ว บุคคลเช่นนี้ต้องตรวจทุก ๆ 5 วัน[70]
การตรวจ
[แก้]


หลังจากปัญหาเรื่องความแม่นยำและจำนวนที่ตรวจโรคได้ในช่วงเดือนมกราคมและกุมภาพันธ์ สหรัฐตรวจคน 300,000 คนทุกวันในวันที่ 9 พฤษภาคม[84][87] ประเทศยุโรปสามประเทศมุ่งตรวจโรค 100,000 รายการต่อวัน เยอรมนีตั้งแต่กลางเมษายน สหราชอาณาจักรตั้งแต่ปลายเมษายน และฝรั่งเศสตั้งแต่ปลายมิถุนายน เยอรมนีมีอุตสาหกรรมวินิจฉัยโรคทางการแพทย์ขนาดใหญ่ มีแล็บตรวจเกิน 100 แห่งซึ่งเป็นทั้งแหล่งเทคโนโลยีและเป็นโครงสร้างพื้นฐาน จึงอาจเพิ่มการตรวจอย่างรวดเร็ว ส่วนสหราชอาณาจักรมุ่งใช้บริษัทวิทยาศาสตร์ชีวภาพเพื่อตรวจวินิจฉัยและเพิ่มจำนวนการตรวจ[88]
ในเยอรมนี สมาคมแพทย์ประกันสุขภาพบังคับตามกฎหมาย (NASHIP) กล่าวในวันที่ 2 มีนาคมว่า กลุ่มสามารถตรวจสอบโรค 12,000 รายการต่อวันสำหรับผู้ป่วยนอกโดยได้ตรวจ 10,700 รายการในสัปดาห์ก่อน ประกันสุขภาพเป็นผู้จ่ายเมื่อแพทย์สั่งตรวจ[89] ตามประธานสถาบันโรเบิร์ตค็อก (Robert Koch Institute) เยอรมนีมีสมรรถภาพการตรวจทั้งหมด 160,000 รายการต่ออาทิตย์[90] ในวันที่ 19 มีนาคม มีจุดจอดรถตรวจในเมืองใหญ่ ๆ หลายแห่ง[91] ในวันที่ 26 มีนาคม จำนวนการตรวจทั้งหมดในประเทศไม่ชัดเจน เพราะรายงานแต่ผลบวก รัฐมนตรีกระทรวงสารธารณสุขเจนส์ สแปน ประเมินว่ามีการตรวจ 200,000 รายต่อสัปดาห์[92] การสำรวจแล็บงานแรกในปลายเดือนมีนาคมพบว่า มีการตรวจอย่างน้อย 483,295 รายโดยมีตัวอย่างที่มีโรค 33,491 รายคือ 6.9%[93]
ต้นเดือนเมษายน สหราชอาณาจักรสามารถตรวจโดยกวาดป้าย 10,000 รายการต่ออาทิตย์ มีเป้าหมายตรวจ 100,000 รายการต่อวันเมื่อถึงปลายเดือนเมษายน และจะตรวจให้ได้ถึง 250,000 รายการต่อวัน[88] กระทรวงสาธารณสุขอังกฤษ (NHS) ประกาศว่า กำลังเริ่มตรวจกรณีสงสัยโดยทำที่บ้าน ซึ่งจะกำจัดความเสี่ยงทำให้คนอื่นติดโรคเมื่อเทียบกับไป รพ. หรือเมื่อต้องฆ่าเชื้อในรถพยาบาล[94]
เมื่อจอดรถตรวจในกรณีที่สงสัย เจ้าหน้าที่จะใช้อุปกรณ์ป้องกันโรค[95][96] ศูนย์จอดรถตรวจทำให้เกาหลีใต้สามารถตรวจโรคได้เร็วที่สุดและกว้างขวางที่สุดในบรรดาประเทศทั้งหมด[97] ส่วนฮ่องกงใช้แผนให้คนไข้อยู่บ้าน โดยแผนกฉุกเฉินจะส่งหลอดตัวอย่างไปให้เพื่อถ่มน้ำลาย แล้วส่งหลอดกลับโดยจะได้ผลต่อมา[98]
ในอิสราเอล นักวิจัยที่สถาบันเทคโนโลยีเทคเนียนและโรงพยาบาลแรมแบมได้พัฒนาและทดสอบวิธีการตรวจตัวอย่างจากคนไข้ 64 คนพร้อม ๆ กัน โดยรวมตัวอย่างเข้าด้วยกันและตรวจสอบยิ่งขึ้นถ้าตัวอย่างรวมปรากฏว่ามีเชื้อ[99][100][101] แต่นั้น วิธีนี้ก็ได้ใช้ในอิสราเอล เยอรมนี เกาหลีใต้[102] รัฐเนแบรสกา[103] รัฐอุตตรประเทศ[104] รัฐเบงกอลตะวันตก[105] รัฐปัญจาบ[106] รัฐฉัตตีสครห์[107] และรัฐมหาราษฏระ[108]
ในเมืองอู่ฮั่น บริษัทบีจีไอกรุ๊ปได้สร้างแล็บตรวจโรคฉุกเฉินชั่วคราวใหญ่ขนาด 2,000 ตารางเมตรชื่อว่า "หัวแหย่น" (จีน: 火眼 แปลว่า ตาไฟ) โดยเปิดวันที่ 5 กุมภาพันธ์[109][110] และสามารถตรวจตัวอย่างได้ 10,000 ตัวอย่างต่อวัน[111][110] ผู้ตั้งบริษัทได้ควบคุมดูแลการก่อสร้างซึ่งใช้เวลา 5 วัน[112] แบบจำลองได้แสดงว่า กรณีคนติดโรคในมณฑลหูเป่ย์อาจจะสูงกว่าถึง 47% และค่าใช้จ่ายเพื่อควบคุมการกักบริเวณจะสูงขึ้นถึงสองเท่าถ้าสมรรถภาพในการตรวจเช่นนี้ไม่มี[ต้องการอ้างอิง] ต่อจากนั้นบริษัทจึงได้สร้างแล็บในเมือง 12 เมืองทั่วประเทศจีนรวมทั้งเชินเจิ้น เทียนจิน ปักกิ่ง และเซี่ยงไฮ้ วันที่ 4 มีนาคม 2020 สมรรถภาพการตรวจของบริษัทอยู่ที่ 50,000 รายการต่อวัน[113]
บริษัทออริกามิแอสเซส์ได้เผยแพร่แบบของชุดทดสอบโอเพนซอร์ซซึ่งสามารถตรวจตัวอย่าง 1,122 รายการโดยใช้ชุดทดสอบเพียง 93 ชุด[114] ซึ่งสามารถทำในแล็บขนาดเล็กโดยไม่ต้องใช้หุ่นยนต์ที่จัดการของเหลว
ในเดือนมีนาคม ความขาดแคลนสารกระทำปฏิกิริยา (reagent) เป็นจุดคอคอดที่จำกัดจำนวนการตรวจโรคในสหภาพยุโรป สหราชอาณาจักร[115] และสหรัฐ[116][117] นักวิชาการบางท่านจึงได้ตรวจดูการเตรียมตัวอย่างที่ให้ความร้อนจนถึง 98 องศาเซลเซียส เป็นเวลา 5 นาทีเพื่อให้ปล่อยจีโนมอาร์เอ็นเอแล้วนำมาตรวจสอบต่อไป[118][119]
ในวันที่ 31 มีนาคม สหรัฐอาหรับเอมิเรตส์ได้ตรวจไวรัสโคโรนาในกลุ่มประชากรต่อหัวมากกว่าประเทศอื่น ๆ ทั้งหมด โดยเป็นไปตามแผนเพื่อเพิ่มตรวจประชาชนให้ได้เป็นจำนวนมาก[120] ซึ่งทำโดยตรวจจอดรถ และซื้อแล็บที่มีสมรรถภาพในการตรวจจนถึงระดับประชากรจากบริษัทกรุ๊ป 42 และบีจีไอกรุ๊ป (ตามแล็บฉุกเฉินหัวแหย่นในประเทศจีน) แล็บสร้างเพียงแค่ 14 วัน และสามารถตรวจด้วยวิธี RT-PCR เป็นหมื่น ๆ รายการต่อวัน เป็นแล็บขนาดใหญ่ระดับนี้แห่งแรกที่ปฏิบัติการนอกประเทศจีน[121]
วันที่ 8 เมษายน 2020 ศาลสูงสุดของอินเดียตัดสินว่า แล็บเอกชนควรได้ค่าชดใช้เมื่อตรวจโรคโควิด[122] แต่แล็บเอกชนก็ระบุว่า ไม่สามารถขยายตรวจเพิ่มขึ้นได้เพราะถูกจำกัดราคา ต้องจ่ายเงินล่วงหน้าสำหรับวัสดุที่ต้องใช้ แต่กลับได้ค่าชดใช้ล่าช้าจาก รพ.[123]
การผลิตและปริมาณ
[แก้]
ประเทศต่าง ๆ รวมทั้งจีน ฝรั่งเศส เยอรมนี ฮ่องกง ญี่ปุ่น สหราชอาณาจักร และสหรัฐ ได้สร้างชุดตรวจที่เล็งส่วนต่าง ๆ ของยีนไวรัส องค์การอนามัยโลกได้ใช้แบบของเยอรมนีเพื่อผลิตชุดทดสอบและส่งไปยังประเทศรายได้น้อยซึ่งไม่มีทรัพยากรเพื่อพัฒนาชุดทดสอบของตนเอง สูตรชุดทดสอบเยอรมันได้เผยแพร่ตั้งแต่วันที่ 17 มกราคม 2020 ส่วนของศูนย์ควบคุมและป้องกันโรคสหรัฐไม่ได้เผยแพร่จนถึงวันที่ 28 มกราคม การผลิตชุดทดสอบจึงล่าช้า[125]
จีน[126] และสหรัฐ[127] มีปัญหาเรื่องความเชื่อถือได้ของชุดการตรวจเมื่อโรคระบาดใหม่ ๆ สองประเทศเหล่านี้บวกกับออสเตรเลีย[128] ไม่อาจผลิตชุดการตรวจเพียงพอแก่ความต้องการหรือตามที่ผู้เชี่ยวชาญทางสาธารณสุขแนะนำได้ เมื่อเปรียบเทียบกัน เกาหลีใต้สามารถตรวจโรคได้อย่างกว้างขวาง จึงช่วยลดการระบาดของโรค รัฐบาลเกาหลีใต้ได้สร้างสมรรถภาพการตรวจสอบในแล็บเอกชนเป็นเวลาหลายปีแล้ว[129] วันที่ 16 มีนาคม องค์การอนามัยโลกได้สนับสนุนให้เพิ่มสมรรถภาพการตรวจสอบว่าเป็นวิธีที่ดีสุดเพื่อชลอการระบาดของโควิด[130][131]
เพราะตัวอย่างที่ต้องตรวจมีมากเหตุโรคระบาด และเพราะไม้พันสำลีและสารกระทำปฏิกิริยา (reagent) ขาดแคลน แล็บเอกชนสหรัฐจึงล่าช้าในการตรวจ[132]
การตรวจที่มี
[แก้]PCR
[แก้]เมื่อนักวิทยาศาสตร์จีนได้เผยแพร่ข้อมูลจีโนมของไวรัสโควิดในวันที่ 11 มกราคม 2020 สถาบันวิจัยทางการแพทย์มาเลเซีย (IMR) ในกัวลาลัมเปอร์ได้สร้างตัว primer และ probe ที่เฉพาะเจาะจงต่อไวรัสในวันเดียวกัน แล็บของสถาบันเตรียมการล่วงหน้าคือค้นหาสารกระทำปฏิกิริยา (reagent) เพื่อตรวจจับไวรัสโคโรนาด้วยวิธี rt-PCR[133] ลำดับตัวทำปฏิกิริยาขององค์การอนามัยโลก (คือ primer และ probe) ที่เผยแพร่ต่อมาหลายวันก็คล้ายกับของแล็บมาก แบบที่แล็บค้นพบก็ได้ใช้วินิจฉัยคนไข้มาเลเซียคนแรกที่ติดโควิดในวันที่ 24 มกราคม[134]
กระทรวงสาธารณสุขอังกฤษพัฒนาชุดการตรวจตั้งแต่วันที่ 10 มกราคม[135] โดยใช้การวิเคราะห์ตัวอย่างที่ได้กวาดป้ายแบบปฏิกิริยาลูกโซ่พอลิเมอเรสแบบย้อนกลับตามเวลาจริง (rRT-PCR)[136] ซึ่งตรวจว่ามีไวรัสโคโรนาชนิดไร ๆ ก็ได้รวมทั้ง SARS-CoV-2 และได้ส่งให้ใช้ในแล็บต่าง ๆ 12 แห่งทั่วสหราชอาณาจักรในวันที่ 10 กุมภาพันธ์[137]
ชารีเทในเมืองเบอร์ลินซึ่งเป็นโรงพยาบาลมหาวิทยาลัยในยุโรป ได้ร่วมงานกับบุคลากรต่าง ๆ ในยุโรปและฮ่องกงเพื่อพัฒนาการตรวจแบบ PCR แล้วเผยแพร่ผลที่ได้ในวันที่ 23 มกราคม ชุดตรวจใช้ rRT-PCR และเป็นชุดตรวจ 250,000 ชุดที่องค์การอนามัยโลกได้แจกจ่าย[138] ส่วนบริษัทเกาหลีใต้ Kogenebiotech ได้พัฒนาชุดตรวจอาศัย PCR (เรียกว่า PowerChek Coronavirus) ซึ่งได้รับอนุมัติจากศูนย์ควบคุมและป้องกันโรคเกาหลีในวันที่ 4 กุมภาพันธ์[139] ชุดตรวจสืบหายีน "E" ที่ ไวรัสโคโรนาบีตาทุกชนิดมี และยีน RdRp ที่เฉพาะเจาะจงต่อ SARS-CoV-2[140]
ในประเทศจีน บีจีไอกรุ๊ปเป็นบริษัทแรก ๆ ที่ได้รับอนุมัติฉุกเฉินโดยองค์การบริหารเวชภัณฑ์แห่งชาติประเทศจีน (NMPA) สำหรับชุดตรวจที่ใช้เทคโนโลยี PCR[141]
ในสหรัฐ ศูนย์ควบคุมและป้องกันโรคสหรัฐได้แจกจ่ายชุดตรวจโรคไปให้กับแล็บสาธารณสุขของรัฐผ่านเว็บไซต์ International Reagent Resource[142] เพราะการตรวจทางยีนหนึ่งอย่างใน 3 อย่างในชุดตรวจต้น ๆ มีผลคลุมเครือเพราะสารทำปฏิกิริยา (reagent) บกพร่อง และเพราะศูนย์ควบคุมและป้องกันโรคสหรัฐในเมืองแอตแลนตาเป็นจุดคอคอดในการตรวจ จึงทำให้สามารถตรวจตัวอย่างเพียงแค่ 100 ตัวอย่างต่อวันในสหรัฐตลอดเดือนกุมภาพันธ์ แต่การตรวจที่ตรวจยีนแค่ 2 ส่วนก็ระบุว่าไม่น่าเชื่อถือจนกระทั่งถึงวันที่ 28 กุมภาพันธ์ และแล็บของรัฐต่าง ๆ และแล็บเฉพาะพื้นที่ ๆ ก็ไม่ได้รับอนุญาตให้ใช้ตรวจ[143] การอนุมัติต่อมาเป็นการอนุญาตในการฉุกเฉิน[ต้องการอ้างอิง] ส่วนแล็บเอกชนในสหรัฐเริ่มตรวจโรคเริ่มตั้งแต่ต้นเดือนมีนาคม ในวันที่ 5 มีนาคม บริษัทแล็บคอร์ปประกาศขายชุดตรวจโรคที่ใช้เทคโนโลยี RT-PCR ทั่วประเทศ[144] ส่วนบริษัทเควสต์ไดแอ็กนอสติกส์ได้ประกาศเช่นเดียวกันโดยเริ่มขายตั้งแต่วันที่ 9 มีนาคม[145]
ในรัสเซีย สถาบันเว็กเตอร์ได้พัฒนาและผลิตชุดตรวจแรกซึ่งเริ่มผลิตในวันที่ 24 มกราคม[146] วันที่ 11 กุมภาพันธ์ ชุดตรวจได้รับอนุมัติจากองค์กรของรัฐที่ควบคุมดูแลระบบสาธารณสุข[147]
วันที่ 12 มีนาคม คลินิกมาโยซึ่งเป็น รพ. ที่จัดว่าดีที่สุดในสหรัฐรายงานว่าได้พัฒนาชุดตรวจโรค[148] ในวันที่ 18 มีนาคม องค์การอาหารและยาสหรัฐให้อนุญาตฉุกเฉินแก่บริษัทแอบบอทต์แล็บ[149] สำหรับอุปกรณ์ของบริษัท องค์กรได้ให้อนุมัติเช่นกันกับบริษัทโฮโลจิกเมื่อวันที่ 16 มีนาคม[150] กับบริษัทแล็บคอร์ปในวันเดียวกัน[149] และกับบริษัทเทอร์โมฟิเช่อร์ไซเอ็นทิฟิกในวันที่ 19 มีนาคม[151] วันที่ 21 มีนาคม บริษัทเซฟิดก็ได้รับอนุมัติเช่นเดียวกัน เป็นชุดตรวจที่ใช้เวลา 45 นาทีและใช้กับเครื่องของบริษัท[152][153] ที่ปกติใช้ตรวจวัณโรคและการแพ้ยาปฏิชีวนะได้อย่างรวดเร็ว
วันที่ 13 เมษายน กระทรวงสาธารสุขแคนาดาอนุมัติชุดตรวจจากบริษัทสปาร์ตันไบโอไซเอ็นซ์ ซึ่งสถาบันต่าง ๆ สามารถตรวจคนไข้ได้ด้วยเครื่องวิเคราะห์ดีเอ็นเอมือถือแล้วรับผลโดยไม่ต้องส่งตัวอย่างไปที่ศูนย์[154][155]
Isothermal nucleic amplification
[แก้]
วันที่ 27 มีนาคม 2020 องค์การอาหารและยาสหรัฐอนุมัติผ่านมาตรการฉุกเฉินให้ใช้การทดสอบทางเคมีชีวภาพอัตโนมัติ (automated assay) ของบริษัทแอบบอตต์ที่ใช้วิธี isothermal nucleic acid amplification (มีชื่อว่า ID NOW COVID-19) แทน PCR[156] เป็นวิธีที่ถ่ายแบบยีนส่วนพิเศษของไวรัสคือ RdRp แล้วตรวจหาแบบที่ถ่ายด้วยวิธี fluorescently-labeled molecular beacons คือปล่อยโมเลกุลเรืองแสง (fluorophore) ให้เข้าจับกับส่วนที่ว่าของไวรัส[157] ชุดตรวจใช้กับเครื่องตรวจขนาดประมาณ "เครื่องปิ้งขนมปัง" ซึ่งมีราคาระหว่าง 12,000-15,000 ดอลลาร์สหรัฐ (ประมาณ 377,000-471,000 บาท)[158] จึงสามารถทำในแล็บหรือในสถานที่ตรวจผู้ป่วยโดยให้ผลภายใน 13 นาทีหรือน้อยกว่า[157] มีเครื่องปฏิบัติการเช่นนี้ได้ 18,000 เครื่องในสหรัฐ และบริษัทคาดว่าจะสามารถผลิตชุดตรวจได้ถึง 50,000 ชุดต่อวัน[159] เพราะวิธีนี้ไม่จำเป็นต้องผ่านวงจรหมุนเวียนอุณหภูมิ (ดังที่ PCR ปกติต้องใช้) จึงสามารถแสดงผลบวกได้เร็วถึง 5 นาทีและผลลบเร็วถึง 13 นาที
ผู้เข้าพบประธานาธิบดีสหรัฐคือดอนัลด์ ทรัมป์ปัจจุบันจะต้องตรวจด้วยวิธีนี้ที่ทำเนียบขาว[160]
ในงานศึกษาที่คลินิกคลีฟแลนด์ ชุดตรวจที่ว่าในปัจจุบันสามารถตรวจพบไวรัสในตัวอย่างที่มีเชื้อในอัตราเพียงร้อยละ 85.2 และตามผู้อำนวยการของงานศึกษานี้ ชุดตรวจหนึ่ง ๆ ควรจะชื่อถือได้อย่างน้อยร้อยละ 95 ส่วนบริษัทแก้ว่า ปัญหาอาจมาจากการใส่ตัวอย่างลงในน้ำยาพิเศษแทนที่จะใส่เข้าเครื่องโดยตรง[161]
การตรวจแอนติเจน
[แก้]วันที่ 8 พฤษภาคม 2020 องค์การอาหารและยาสหรัฐได้อนุญาตตามมาตรการฉุกเฉินให้ใช้การตรวจโรคโควิดทางแอนติเจนที่เรียกว่า Sofia 2 SARS Antigen FIA ของบริษัทควิเด็ล[162][36] เป็นชุดตรวจแบบ lateral flow test[C] ที่ใช้สารภูมิต้านทานแบบโมโนโคลน (monoclonal antibodies) คือผลิตจากเซลล์ภูมิคุ้มกันที่มีบรรพบุรุษเดียวกันเพื่อตรวจจับโปรตีน nucleocapsid (N)[D] ของไวรัส[168] แล้วใช้เครื่องอ่านผลของบริษัทที่เรียกว่า Sofia 2 โดยใช้เทคโนโลยี immunofluorescence คือใช้สีย้อมเรืองแสงที่เข้าจับกับโปรตีนไวรัสประกอบกับสารภูมิต้านทาน[168] วิธีการตรวจนี้ ง่ายกว่า ราคาถูกกว่า แต่แม่นยำน้อยกว่าการตรวจด้วย PCR สามารถใช้ในแล็บหรือในสถานที่ตรวจคนไข้ และให้ผลภายใน 15 นาที[162] อาจให้ผลลบถ้าระดับแอนติเจนของไวรัสในตัวอย่างต่ำกว่าขีดจำกัดของชุดตรวจ[169] ผลลบควรยืนยันด้วยการตรวจแบบ RT-PCR[168]
การตรวจทางวิทยาการเซรุ่ม
[แก้]จนถึงวันที่ 4 พฤษภาคม มีวิธีการตรวจ 11 แบบที่ได้รับอนุมัติให้ใช้ในสหรัฐตามมาตรการฉุกเฉิน[170] โดยทำเป็นรายการมีคำอธิบายอยู่ที่ Johns Hopkins Center for Health Security เก็บถาวร 2020-06-09 ที่ เวย์แบ็กแมชชีน ส่วนประเทศอื่น ๆ ก็ได้อนุมัติวิธีการตรวจอื่น ๆ[171]
ในสหรัฐ จนถึงวัน 28 เมษายน บริษัทเควสต์ไดแอ็กนอสติกส์ได้ให้บริการตรวจสารภูมิต้านทานของเชื้อโควิดแก่สาธารณชนทั่วไปผ่านบริการเควสต์ไดเร็กต์ มีค่าใช้จ่ายประมาณ 130 ดอลลาร์สหรัฐ (ประมาณ 4,085 บาท) คนตรวจต้องไปเจาะเลือด ณ ที่รับตรวจ โดยจะให้ผลเป็นวัน ๆ ต่อจากนั้น[172]
ประเทศจำนวนหนึ่งเริ่มสำรวจการติดโรคของประชากรอย่างกว้างขวางโดยใช้ชุดตรวจเช่นที่ว่า[173][174] งานศึกษาในรัฐแคลิฟอร์เนียที่ตรวจสารภูมิต้านทานในประชากรเทศมณฑลหนึ่งประเมินว่า อัตราคนติดเชื้ออยู่ระหว่างร้อยละ 2.5-4.2 ของประชากรทั้งหมด ซึ่งเป็น 50-85 เท่าของจำนวนกรณีที่ยืนยันโรคแล้ว[175][176]
รายการชุดตรวจขององค์การอนามัยโลก
[แก้]| วันติด รายการ |
ชื่อผลิตภัณฑ์ | ผู้ผลิต |
|---|---|---|
| 3 เมษา | ชุด Cobas SARS-CoV-2 qualitative assay ใช้กับเครื่อง cobas 6800/8800 Systems | Roche Molecular Systems |
| 7 เมษา | Coronavirus (COVID-19) genesig rtPCR assay | Primerdesign |
| 9 เมษา | Abbott Realtime SARS-CoV-2[177] | บริษัทแอบบอตต์ |
| 24 เมษา | PerkinElmer SARS-CoV-2 Real-time RT-PCR Assay[177] | SYM-BIO LiveScience |
จนถึงวันที่ 7 เมษายน องค์การอนามัยโลกได้อนุมัติการสั่งซื้อชุดตรวจโรค 2 อย่างเพื่อใช้เป็นการฉุกเฉินในระหว่างโรคระบาดทั่วโควิด เพื่อให้มีการตรวจโรคที่รับรองคุณภาพและแม่นยำ[178] การอนุมัติหมายความว่า องค์การอนามัยโลกและองค์กรจัดหาสินค้าที่เกี่ยวข้องกันอื่น ๆ สามารถส่งชุดตรวจได้ตามจำเป็น
ความแม่นยำ
[แก้]ในเดือนมีนาคม 2020 จีน[126] ได้รายงานปัญหาความแม่นยำของชุดตรวจที่ใช้
ส่วนในสหรัฐ ชุดตรวจที่ศูนย์ควบคุมและป้องกันโรคสหรัฐได้พัฒนาก็มีปัญหาด้วย จนรัฐบาลต้องยกเลิกระเบียบราชการจุกจิกซึ่งกันไม่ให้แล็บเอกชนสามารถตรวจโรคได้[127]
ประเทศสเปนได้ซื้อชุดตรวจจากบริษัทจีนคือเชินเจิ้นไบโออี้ซี่ไบโอเทคโนโลยี แต่ก็พบว่าผลไม่แม่นยำ แต่บริษัทอธิบายว่า อาจเป็นเพราะได้ตัวอย่างที่ไม่ดีหรือใช้ชุดตรวจอย่างไม่ถูกต้อง กระทรวงสาธารณสุขสเปนแจ้งว่า จะเปลี่ยนชุดตรวจที่ไม่แม่นยำกับชุดตรวจอื่นที่บริษัทส่งให้[179]
ชุดตรวจ 80% ที่ประเทศเช็กเกียซื้อจากจีนให้ผลไม่ถูกต้อง[180][181]
ประเทศสโลวาเกียซื้อชุดตรวจ 1.2 ล้านชุดจากจีนแต่ก็พบว่าไม่แม่นยำ ซึ่งนายกรัฐมนตรีใหม่ของประเทศผู้ไม่ถูกกับรัฐบาลเก่า แนะนำให้ทิ้งลงในแม่น้ำดานูบ[182]
แพทย์โรคระบาดของกระทรวงสาธารสุขตุรกีกล่าวว่า ชุดตรวจที่ได้ซื้อจากจีนมี "อัตราความผิดพลาดสูง" และกระทรวงจึง "ไม่ได้ใช้พวกมัน"[183][184]
สหราชอาณาจักรได้ซื้อชุดตรวจ 3.5 ล้านชุดจากจีนในต้นเดือนเมษายน 2020 แต่ก็ประกาศว่าใช้ไม่ได้[185][186]
วันที่ 21 เมษายน หลังจากรัฐรัฐหนึ่งได้ร้องเรียน คณะกรรมการการวิจัยทางการแพทย์อินเดีย (ICMR) ก็ได้แนะนำให้รัฐต่าง ๆ เลิกใช้ชุดตรวจสารภูมิต้านทานที่ให้ผลเร็วซึ่งซื้อมาจากประเทศจีน รัฐมนตรีสาธารณสุขของรัฐราชสถานได้กล่าวในวันที่ 21 เมษายนว่า ชุดตรวจแม่นยำเพียงแค่ 5.4% เทียบกับที่หวังว่าจะแม่นยำถึง 90%[187]
การตรวจยืนยัน
[แก้]องค์การอนามัยโลกแนะนำว่า ประเทศที่ไม่มีสมรรถภาพในการตรวจ หรือแล็บระดับชาติที่มีประสบการณ์น้อยกับโควิด ให้ส่งผลบวกที่ได้แรก 5 ตัวอย่างและผลลบที่ได้แรก 10 ตัวอย่าง ไปยังแล็บมาตรฐานขององค์การ 16 แห่งเพื่อยืนยันผล[188][189] แล็บมาตรฐาน 7 แห่งอยู่ในเอเชีย, 5 แห่งในยุโรป, 2 แห่งในแอฟริกา, 1 แห่งในอเมริกาเหนือ และแห่งหนึ่งในออสเตรเลีย[190]
ประสิทธิผลทางคลินิก
[แก้]ถ้าตรวจแล้ว มีการกักบริเวณคนไข้ที่พบผลบวก แล้วติดตามคนที่สัมพันธ์ติดต่อกับคนไข้ พบว่ามีผลดี[ต้องการอ้างอิง]
อิตาลี
[แก้]นักวิจัยในเมืองอิตาลีคือโฟ ซึ่งเป็นเมืองแรกในอิตาลีที่มีคนเสียชีวิตเหตุโควิด ได้ทดสอบประชากรทั้งหมดของเมือง 3,400 คน 2 รอบโดยห่างกัน 10 วัน คนครึ่งหนึ่งตรวจได้ผลบวกโดยไม่มีอาการ และที่พบทั้งหมดถูกกักบริเวณไม่ให้ไปยังที่ชุมชน ซึ่งกำจัดการแพร่เชื้อได้โดยสิ้นเชิง[191]
สิงคโปร์
[แก้]เพราะติดตามผู้ได้สัมผัสกับโรคอย่างทั่วถึง เพราะระงับการเดินทางเข้าประเทศ ตรวจโรค และกักกันบริเวณ การระบาดของโรคในสิงคโปร์จึงช้ากว่าประเทศพัฒนาแล้วอื่น ๆ โดยไม่ได้บังคับให้ปิดร้านอาหารหรือร้านค้า งานต่าง ๆ หลายงานถูกยกเลิก และรัฐก็เริ่มแนะนำให้ประชาชนอยู่บ้านเริ่มตั้งแต่ 28 มีนาคมแต่ก็เปิด รร. อีกตามกำหนดหลังจากวันหยุดปกติเมื่อวันที่ 23 มีนาคม[192] แม้ต่อมาวันที่ 8 เมษายนก็ได้ปิด รร. โดยให้นักเรียนนักศึกษาเรียนต่อที่บ้าน[193]
เรือบรรทุกเครื่องบินสหรัฐธีโอดอร์โรสเวลต์
[แก้]การตรวจลูกเรือร้อยละ 94 ในเรือบรรทุกเครื่องบินสหรัฐธีโอดอร์โรสเวลต์จาก 4,800 นายได้พบว่า ในบรรดาลูกเรือ 600 คนที่พบผลบวก ร้อยละ 60 ไม่มีอาการอะไร ๆ[194]
รัสเซีย
[แก้]ในวันที่ 27 เมษายน รัสเซียได้ตรวจตัวอย่างแล้ว 3 ล้านรายการ มีคนไข้ 183,000 คนในการดูแลของแพทย์เพราะสงสัยว่าติดเชื้อไวรัสโควิด[195] 87,147 คนตรวจไวรัสได้ผลบวก และมีคนตายที่ยืนยันโรคแล้ว 794 คน[196] ในวันที่ 28 เมษายน องค์กรสอดส่องดูแลสาธารณสุขของรัฐบาลกลาง (Roszdravnadzor) ได้แจ้งโดยเป็นส่วนการรายงานอัปเดตของประธานาธิบดีว่า ประเทศมีแล็บ 506 แห่งที่กำลังตรวจโรค คนร้อยละ 45 ที่ตรวจได้ผลบวกไม่มีอาการ ร้อยละ 20 มีอาการปอดบวม และร้อยละ 5 มีโรครุนแรง ร้อยละ 40 ติดเชื้อมาจากสมาชิกครอบครัว ประชาชนรายงานความเจ็บป่วยเร็วขึ้นคือรายงานหลังจากติดเชื้อ 6 วันกลายเป็นรายงานวันที่พบอาการ หมอเมืองมอสโก 3,200 คนได้ตรวจสารภูมิต้านทานโดยร้อยละ 20 มีภูมิต้านทานโรค[197]
ประเทศอื่น ๆ
[แก้]ประเทศหลายประเทศอื่น ๆ เช่น ไอซ์แลนด์[198] และเกาหลีใต้[199] ได้รับมือกับโรคโดยติดตามผู้สัมผัสกับโรคอย่างทั่วถึง ระงับการเดินทางเข้าประเทศ ตรวจโรค และกักบริเวณคนติด แต่ก็ไม่ได้ปิดประเทศ (lock-down) มากเท่าประเทศอื่น ๆ งานศึกษาทางสถิติงานหนึ่งพบว่า ประเทศที่ตรวจโรคมากกว่าเทียบกับจำนวนผู้เสียชีวิต จะมีอัตราป่วยตายต่ำกว่ามาก อาจเป็นเพราะสามารถตรวจผู้ที่มีอาการน้อยหรือไม่มีอาการ[5] งานศึกษาที่ตามมาอีกงานหนึ่งพบว่า ประเทศที่ตรวจคนได้มากกว่าจะมีกรณีคนไข้ที่กระจายไปยังคนอายุน้อยกว่า เทียบกับประชากรทั้งหมด[200]
การวิจัยและพัฒนา
[แก้]การตรวจโดยใช้สารภูมิต้านทานโมโนโคลน (monoclonal antibody) ซึ่งเข้าจับกับผิวเคลือบอนุภาคไวรัส (คือ nucleocapsid protein หรือ N protein) ของ SARS-CoV-2 กำลังพัฒนาขึ้นในไต้หวัน โดยหวังว่า มันจะช่วยให้รู้ผลการตรวจโรคภายใน 15-20 นาทีเหมือนอย่างชุดการทดสอบวินิจฉัยโรคไข้หวัดใหญ่อย่างรวดเร็ว (RIDT)[201] แต่ในวันที่ 8 เมษายน องค์การอนามัยโลกก็แสดงความเป็นห่วงว่า วิธีการตรวจนี้ต้องตรวจสอบความน่าเชื่อถือได้สำหรับโควิด และยังอยู่ในระยะวิจัยเท่านั้น[202] ส่วนองค์การอาหารและยาสหรัฐได้อนุมัติการตรวจสารภูมิต้านทานในวันที่ 2 เมษายน[203] แต่นักวิจัยบางส่วนเตือนว่า การตรวจเช่นนี้ไม่ควรมีผลต่อการตัดสินใจทางสาธารณสุขต่อจนกว่าจะรู้อัตราคนรอดชีวิตผู้ผลิตสารภูมิต้านทานกำจัดฤทธิ์โรค[46]
สถิติการตรวจไวรัสในประเทศต่าง ๆ
[แก้]ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
เชิงอรรถ
[แก้]- ↑ pulmonary consolidation เป็นบริเวณเนื้อเยื่อปอด (ปกติบีบอัดได้) ที่มีน้ำเต็ม ซึ่งทำให้เนื้อเยื่อปอดบวมหรือแข็งตัว ต่างกับปอดปกติที่เมื่อหายใจเข้าจะนิ่ม ๆ เป็นอาการทางรังสีวิทยาอย่างหนึ่ง[39]
- ↑ มาโครฟาจ (อังกฤษ: macrophage จากคำภาษากรีกซึ่งแปลว่า ตัวกินใหญ่) เป็นเซลล์เม็ดเลือดขาวประเภทหนึ่งที่เข้าหุ้มแล้วย่อยสลายเศษเหลือของเซลล์, วัสดุแปลกปลอม, จุลินทรีย์, เซลล์มะเร็ง และสิ่งอื่น ๆ ที่ไม่มีโปรตีนบนผิวซึ่งแสดงอย่างจำเพาะเจาะจงว่าเป็นเซลล์ปกติ[55] เป็นกระบวนการที่เรียกว่าฟาโกไซโทซิส
- ↑ lateral flow test[163] หรือ lateral flow immunochromatographic assay เป็นอุปกรณ์ง่าย ๆ ที่ใช้ตรวจการมี (หรือไม่มี) สารเคมีที่เป็นเป้าหมายอย่างหนึ่งในตัวอย่างโดยไม่ต้องใช้อุปกรณ์ราคาแพง แม้จะมีการประยุกต์ใช้วิธีเดียวกันในแล็บที่ต้องใช้อุปกรณ์อ่านผล[164] ปกติแล้ว เครื่องมือเช่นนี้ใช้ตรวจที่บ้าน ที่ที่ตรวจคนไข้ หรือในแล็บ ตัวอย่างการประยุกต์ที่ใช้อย่างกว้างขวางก็คืออุปกรณ์ตรวจการตั้งครรภ์ เทคโนโลยีอาศัยชั้นที่ทำเป็นรูเล็ก ๆ ต่อ ๆ กัน เช่น กระดาษพรุน[165] พอลิเมอร์ที่มีโครงสร้างเล็ก ๆ[166][167] หรือโพลีเมอร์พรุน (sintered polymer) วัสดุที่ว่ามาทั้งหมดมีสมรรถภาพในการให้ของเหลว (เช่น ปัสสาวะ) ซึมผ่าน
- ↑ nucleocapsid ก็คือกรดนิวคลีอิกและโปรตีนที่หุ้มรอบ ๆ ไวรัส
อ้างอิง
[แก้]- ↑ 1.0 1.1 Abbasi, Jennifer (2020-04-17). "The Promise and Peril of Antibody Testing for COVID-19". JAMA. JAMA Network. doi:10.1001/jama.2020.6170. PMID 32301958. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-26. สืบค้นเมื่อ 2020-04-20.
- ↑ Ioannidis, John P.A. (2020-03-17). "A fiasco in the making? As the coronavirus pandemic takes hold, we are making decisions without reliable data". STAT. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-29. สืบค้นเมื่อ 2020-03-22.
- ↑ "Total tests for COVID-19 per 1,000 people". Our World in Data. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-16.
- ↑ "Iceland has tested more of its population for coronavirus than anywhere else. Here's what it learned". USA Today. 2020-04-11. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-20. สืบค้นเมื่อ 2020-04-16.
- ↑ 5.0 5.1 Ward, D. (April 2020). "Sampling Bias: Explaining Wide Variations in COVID-19 Case Fatality Rates". doi:10.13140/RG.2.2.24953.62564/1.
- ↑ Henriques, Martha. "Coronavirus: Why death and mortality rates differ". bbc.com (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-19. สืบค้นเมื่อ 2020-04-08.
- ↑ Michaels, Jonathan A.; Stevenson, Matt D. (2020). "Explaining national differences in the mortality of Covid-19: Individual patient simulation model to investigate the effects of testing policy and other factors on apparent mortality" (PDF). doi:10.1101/2020.04.02.20050633. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-04-18.
- ↑ "โรคติดเชื้อไวรัสโคโรนา 2019 (COVID-19)". กรมควบคุมโรค. 2020-05-02. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-03.
- ↑ 9.0 9.1 9.2 "How is the COVID-19 Virus Detected using Real Time RT-PCR?". IAEA. 2020-03-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-26. สืบค้นเมื่อ 2020-05-05.
- ↑ "RNA Extraction". AssayGenie. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-06. สืบค้นเมื่อ 2020-05-07.
- ↑ Bustin, Stephen A.; Benes, Vladimir; Garson, Jeremy A.; Hellemans, Jan; Huggett, Jim; Kubista, Mikael; Mueller, Reinhold; Nolan, Tania; Pfaffl, Michael W.; Shipley, Gregory L.; Vandesompele, Jo; Wittwer, Carl T. (2009-04-01). "The MIQE Guidelines: Minimum Information for Publication of Quantitative Real-Time PCR Experiments". Clinical Chemistry (ภาษาอังกฤษ). pp. 611–622. doi:10.1373/clinchem.2008.112797. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27.
- ↑ "Real-time reverse transcription PCR (qRT-PCR) and its potential use in clinical diagnosis" (PDF). Clinical Science. 2005-09-23. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2018-07-21. สืบค้นเมื่อ 2020-05-05.
- ↑ "The Basics: RT-PCR". ThermoFisher Scientific. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14. สืบค้นเมื่อ 2020-05-05.
- ↑ Kang, XP; Jiang, T; Li, YQ (2010). "A duplex real-time RT-PCR assay for detecting H5N1 avian influenza virus and pandemic H1N1 influenza virus". Virol. J. 7: 113. doi:10.1186/1743-422X-7-113. PMC 2892456. PMID 20515509.
- ↑ Joyce, C (2002). Quantitative RT-PCR. A review of current methodologies. Methods Mol. Biol. Vol. 193. pp. 83–92. doi:10.1385/1-59259-283-X:083. ISBN 978-1-59259-283-8. PMID 12325527.
- ↑ Varkonyi-Gasic, E; Hellens, RP (2010). "qRT-PCR of Small RNAs". Plant Epigenetics. Methods in Molecular Biology. Vol. 631. pp. 109–22. doi:10.1007/978-1-60761-646-7_10. ISBN 978-1-60761-645-0. PMID 20204872.
- ↑ "ACCELERATED EMERGENCY USE AUTHORIZATION (EUA) SUMMARY COVID-19 RT-PCR TEST (LABORATORY CORPORATION OF AMERICA)". FDA. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-23. สืบค้นเมื่อ 2020-04-03.
- ↑ Taylor, S; Wakem, M; Dijkman, G; Alsarraj, M; Nguyen, M (April 2010). "A practical approach to RT-qPCR-Publishing data that conform to the MIQE guidelines". Methods. 50 (4): S1-5. doi:10.1016/j.ymeth.2010.01.005. PMID 20215014.
- ↑ "Real-Time RT-PCR Panel for Detection 2019-nCoV". Centers for Disease Control and Prevention. 2020-01-29. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-01-30. สืบค้นเมื่อ 2020-02-01.
- ↑ 20.0 20.1 "Here's where things stand on COVID-19 tests in the U.S." ScienceNews. 2020-04-17. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-19. สืบค้นเมื่อ 2020-05-06.
- ↑ "Curetis Group Company Ares Genetics and BGI Group Collaborate to Offer Next-Generation Sequencing and PCR-based Coronavirus (2019-nCoV) Testing in Europe". GlobeNewswire News Room. 2020-01-30. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-01-31. สืบค้นเมื่อ 2020-02-01.
- ↑ Drosten, Christian (2020-03-26). "Coronavirus-Update Folge 22" (PDF). NDR. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-03-31. สืบค้นเมื่อ 2020-04-02.
- ↑ "Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19". Centers for Disease Control and Prevention (ภาษาอังกฤษแบบอเมริกัน). 2020-04-30. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-04.
- ↑ "Profile of RT-PCR for SARS-CoV-2: a preliminary study from 56 COVID-19 patients". Clinical Infectious Diseases (ภาษาอังกฤษ). 2020-04-19. doi:10.1093/cid/ciaa460/5822175. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-07. สืบค้นเมื่อ 2020-05-08.
- ↑ 25.0 25.1 25.2 "Saliva: potential diagnostic value and transmission of 2019-nCoV". Nature. 2020-04-17. สืบค้นเมื่อ 2020-05-06.
- ↑ 26.0 26.1 "FDA authorizes Covid-19 saliva test for emergency use". CNN. 2020-04-14. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14. สืบค้นเมื่อ 2020-05-01.
- ↑ 27.0 27.1 "New Rutgers Saliva Test for Coronavirus Gets FDA Approval". Rutgers.edu. 2020-04-13. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-13. สืบค้นเมื่อ 2020-05-01.
- ↑ "COVID-19 saliva tests: What is the benefit?". Mayo Clinic. 2020-04-16. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-01. สืบค้นเมื่อ 2020-05-06.
- ↑ "Yale University School of Public Health finds saliva samples promising alternative to nasopharyngeal swab". Merck Manual. 2020-04-29. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-28.
- ↑
Wyllie, Anne Louise; Fournier, John; Casanovas-Massana, Arnau; Campbell, Melissa; Tokuyama, Maria; Vijayakumar, Pavithra; Geng, Bertie; Muenker, M. Catherine; Moore, Adam J.; Vogels, Chantal B. F.; Petrone, Mary E.; Ott, Isabel M.; Lu, Peiwen; Lu-Culligan, Alice; Klein, Jonathan; Venkataraman, Arvind; Earnest, Rebecca; Simonov, Michael; Datta, Rupak; Handoko, Ryan; Naushad, Nida; Sewanan, Lorenzo R.; Valdez, Jordan; White, Elizabeth B.; Lapidus, Sarah; Kalinich, Chaney C.; Jiang, Xiaodong; Kim, Daniel J.; Kudo, Eriko; และคณะ (2020-04-22). "Saliva is more sensitive for SARS-CoV-2 detection in COVID-19 patients than nasopharyngeal swabs". medRxiv. doi:10.1101/2020.04.16.20067835. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-05.
{{cite journal}}: Cite journal ต้องการ|journal=(help) - ↑ 31.0 31.1 31.2 "Coronavirus (COVID-19) Update: FDA Authorizes First Antigen Test to Help in the Rapid Detection of the Virus that Causes COVID-19 in Patients". FDA (ภาษาอังกฤษ). 2020-05-09. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-11.
- ↑ 32.0 32.1 32.2 32.3 32.4 32.5 "Developing Antibodies and Antigens for COVID-19 Diagnostics". Technology Networks. 2020-04-06. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14. สืบค้นเมื่อ 2020-04-30.
- ↑ 33.0 33.1 "NIH launches competition to speed COVID-19 diagnostics". AAAS. 2020-04-29. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-29. สืบค้นเมื่อ 2020-05-01.
- ↑ "Coronaviruses and Acute Respiratory Syndromes (COVID-19, MERS, and SARS)". Merck. 2020-04-01. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-24. สืบค้นเมื่อ 2020-05-01.
- ↑ 35.0 35.1 "What to know about the three main types of coronavirus tests". CNN. 2020-04-29. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-30.
- ↑ 36.0 36.1 "Coronavirus (COVID-19) Update: FDA Authorizes First Antigen Test to Help in the Rapid Detection of the Virus that Causes COVID-19 in Patients". FDA (ภาษาอังกฤษ). 2020-05-09. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27.
- ↑ "ACR Recommendations for the use of Chest Radiography and Computed Tomography (CT) for Suspected COVID-19 Infection". American College of Radiology. 2020-03-22. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-07.
- ↑ 38.0 38.1 38.2 Salehi, Sana; Abedi, Aidin; Balakrishnan, Sudheer; Gholamrezanezhad, Ali (2020-03-14). "Coronavirus Disease 2019 (COVID-19): A Systematic Review of Imaging Findings in 919 Patients". American Journal of Roentgenology (ภาษาอังกฤษ): 1–7. doi:10.2214/AJR.20.23034. ISSN 0361-803X. PMID 32174129.
Known features of COVID-19 on initial CT include bilateral multilobar ground-glass opacification (GGO) with a peripheral or posterior distribution, mainly in the lower lobes and less frequently within the right middle lobe.
- ↑ "Consolidation - Definition". Merriam-Webster. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-02. สืบค้นเมื่อ 2009-01-16.
- ↑ Lee, Elaine Y. P.; Ng, Ming-Yen; Khong, Pek-Lan (2020-02-24). "COVID-19 pneumonia: what has CT taught us?". The Lancet Infectious Diseases (ภาษาอังกฤษ). 0 (4): 384–385. doi:10.1016/S1473-3099(20)30134-1. ISSN 1473-3099. PMC 7128449. PMID 32105641. สืบค้นเมื่อ 2020-03-13.
- ↑ "The next frontier in coronavirus testing: Identifying the full scope of the pandemic, not just individual infections". STAT. 2020-03-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-27. สืบค้นเมื่อ 2020-04-30.
- ↑ "Tests that have been approved for research or surveillance purposes only". Johns Hopkins. 2020-04-30. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-12. สืบค้นเมื่อ 2020-05-01.
- ↑ "Cellex Emergency Use Authorization". FDA. 2020-04-01. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-10.
- ↑ "Will an Antibody Test Allow Us to Go Back to School or Work?". New York Times. 2020-04-10. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-10. สืบค้นเมื่อ 2020-04-15.
- ↑ "Mount Sinai Emergency Use Authorization". FDA. 2020-04-15. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-25. สืบค้นเมื่อ 2020-04-18.
- ↑ 46.0 46.1 "What Immunity to COVID-19 Really Means". Scientific American. 2020-04-10. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28.
- ↑ Lovelace Jr., Berkeley (2020-04-27). "WHO warns about coronavirus antibody tests as some nations consider issuing 'immunity passports' to recovered patients". CNBC. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27.
- ↑ ""Immunity passports" in the context of COVID-19". World Health Organization. 2020-04-24. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-29. สืบค้นเมื่อ 2020-04-28.
There is currently no evidence that people who have recovered from COVID-19 and have antibodies are protected from a second infection.
- ↑ 49.0 49.1 "A SARS-CoV-2 surrogate virus neutralization test (sVNT) based on antibody-mediated blockage of ACE2-spike (RBD) protein-protein interaction". Research Square. 2020-04-23. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-24. สืบค้นเมื่อ 2020-04-28.
- ↑ 50.0 50.1 50.2 50.3 50.4 "Will antibody tests for the coronavirus really change everything?". Nature. 2020-04-18. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-04-20.
- ↑ "A SARS-CoV-2 surrogate virus neutralization test (sVNT) based on antibody-mediated blockage of ACE2-spike (RBD) protein-protein interaction". Researchsquare.com. 2020-04-23. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-24. สืบค้นเมื่อ 2020-04-28.
- ↑ 52.0 52.1 52.2 "Q&A on COVID-19 Antibody Tests". factcheck.org. 2020-04-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27. สืบค้นเมื่อ 2020-04-28.
- ↑ "Neutralising antibody". Biology-Online. 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2010-06-16. สืบค้นเมื่อ 2009-07-04.
- ↑ Schmaljohn, AL (July 2013). "Protective antiviral antibodies that lack neutralizing activity: precedents and evolution of concepts". Current HIV Research. 11 (5): 345–53. doi:10.2174/1570162x113116660057. PMID 24191933.
- ↑ "Macrophages". Duquesne University. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2019-10-22.
- ↑ "Virus neutralization by antibodies". Virology Blog. 2009-07-24. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2009-07-28. สืบค้นเมื่อ 2020-04-29.
- ↑ "expert reaction to announcement by Roche of its new serology test for COVID-19 antibodies". Science Media Centre. 2020-04-17. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-30. สืบค้นเมื่อ 2020-04-28.
- ↑ "Neutralizing antibody responses to SARS-CoV-2 in a COVID-19 recovered patient cohort and their implications". Medrxiv. 2020-04-20. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-28.
- ↑ "COVID-19 Reinfection Not a Concern, Monkey Study Suggests". Genetic Engineering & Biotechnology News. 2020-03-23. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-27. สืบค้นเมื่อ 2020-04-29.
- ↑ "Disappearance of Antibodies to SARS-Associated Coronavirus after Recovery". NEJM. 2007-09-13. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-01. สืบค้นเมื่อ 2020-05-01.
- ↑ 61.0 61.1 "Lack of Peripheral Memory B Cell Responses in Recovered Patients with Severe Acute Respiratory Syndrome: A Six-Year Follow-Up Study" (PDF). Journal of Immunology. 2011-04-19. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-05-03. สืบค้นเมื่อ 2020-05-01.
- ↑ 62.0 62.1 62.2 "Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19". CDC. 2020-05-03. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-04.
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020) อ้างอิง
- ข้อมูลที่ยังไม่ตีพิมพ์ของ CDC
- Midgley, CM; Kujawski, SA; Wong, KK; Collins, J; Epstein, undefined; Killerby, ME; al., et (April 2020). "Clinical and virologic characteristics of the first 12 patients with coronavirus disease 2019 (COVID-19) in the United States". Nat. Med. doi:10.1038/s41591-020-0877-5. PMID 32327757.
- Young, Barnaby Edward; Ong, Sean Wei Xiang; Kalimuddin, Shirin; Low, Jenny G.; Tan, Seow Yen; Loh, Jiashen; Ng, Oon-Tek; Marimuthu, Kalisvar; Ang, Li Wei; Mak, Tze Minn; Lau, Sok Kiang; Anderson, Danielle E.; Chan, Kian Sing; Tan, Thean Yen; Ng, Tong Yong; Cui, Lin; Said, Zubaidah; Kurupatham, Lalitha; Chen, Mark I-Cheng; Chan, Monica; Vasoo, Shawn; Wang, Lin-Fa; Tan, Boon Huan; Lin, Raymond Tzer Pin; Lee, Vernon Jian Ming; Leo, Yee-Sin; Lye, David Chien (2020). "Epidemiologic Features and Clinical Course of Patients Infected With SARS-CoV-2 in Singapore". JAMA. 323 (15): 1488. doi:10.1001/jama.2020.3204. ISSN 0098-7484.
- Zou, Lirong; Ruan, Feng; Huang, Mingxing; Liang, Lijun; Huang, Huitao; Hong, Zhongsi; Yu, Jianxiang; Kang, Min; Song, Yingchao; Xia, Jinyu; Guo, Qianfang; Song, Tie; He, Jianfeng; Yen, Hui-Ling; Peiris, Malik; Wu, Jie (2020). "SARS-CoV-2 Viral Load in Upper Respiratory Specimens of Infected Patients". New England Journal of Medicine. 382 (12): 1177–1179. doi:10.1056/NEJMc2001737. ISSN 0028-4793.
- Wölfel, Roman; Corman, Victor M.; Guggemos, Wolfgang; Seilmaier, Michael; Zange, Sabine; Müller, Marcel A.; Niemeyer, Daniela; Jones, Terry C.; Vollmar, Patrick; Rothe, Camilla; Hoelscher, Michael; Bleicker, Tobias; Brünink, Sebastian; Schneider, Julia; Ehmann, Rosina; Zwirglmaier, Katrin; Drosten, Christian; Wendtner, Clemens (2020). "Virological assessment of hospitalized patients with COVID-2019". Nature. doi:10.1038/s41586-020-2196-x. ISSN 0028-0836.
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020)
อ้างอิง
- ข้อมูลที่ยังไม่ตีพิมพ์ของ CDC
- Wölfel et al. (2020)
- Arons, Melissa M.; Hatfield, Kelly M.; Reddy, Sujan C.; Kimball, Anne; James, Allison; Jacobs, Jesica R.; Taylor, Joanne; Spicer, Kevin; Bardossy, Ana C.; Oakley, Lisa P.; Tanwar, Sukarma; Dyal, Jonathan W.; Harney, Josh; Chisty, Zeshan; Bell, Jeneita M.; Methner, Mark; Paul, Prabasaj; Carlson, Christina M.; McLaughlin, Heather P.; Thornburg, Natalie; Tong, Suxiang; Tamin, Azaibi; Tao, Ying; Uehara, Anna; Harcourt, Jennifer; Clark, Shauna; Brostrom-Smith, Claire; Page, Libby C.; Kay, Meagan; Lewis, James; Montgomery, Patty; Stone, Nimalie D.; Clark, Thomas A.; Honein, Margaret A.; Duchin, Jeffrey S.; Jernigan, John A. (2020). "Presymptomatic SARS-CoV-2 Infections and Transmission in a Skilled Nursing Facility". New England Journal of Medicine. doi:10.1056/NEJMoa2008457. ISSN 0028-4793.
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020) "As the likelihood of isolating replication-competent virus decreases, anti-SARS-CoV-2 IgM and IgG can be detected in an increasing number of persons recovering from infection." อ้างอิง Wölfel et al. (2020)
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020) "Among those who continue to have detectable RNA, concentrations of detectable RNA 3 days following recovery are generally in the range at which replication-competent virus has not been reliably isolated by CDC." อ้างอิง
- ข้อมูลที่ยังไม่ตีพิมพ์ของ CDC
- Young et al. (2020)
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020) "No clear correlation has been described between length of illness and duration of post-recovery shedding of detectable viral RNA in upper respiratory specimens." อ้างอิง
- ข้อมูลที่ยังไม่ตีพิมพ์ของ CDC
- Midgley et al. (2020)
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020) "Infectious virus has not been cultured from urine or reliably cultured from feces" อ้างอิง
- ข้อมูลที่ยังไม่ตีพิมพ์ของ CDC
- Midgley et al. (2020)
- Wölfel et al. (2020)
- ↑ Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19 (2020) อ้างอิง Zhang, Sheng; Tong, Yi Xin; Xiao, Ai Tang (2020). "Profile of RT-PCR for SARS-CoV-2: a preliminary study from 56 COVID-19 patients". Clinical Infectious Diseases. doi:10.1093/cid/ciaa460. ISSN 1058-4838.
- ↑ 70.0 70.1 Soe-Lin, Shan; Hecht, Robert (2020-04-26). "Most Americans Who Carry the Coronavirus Don't Know It". The New York Times. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-15. สืบค้นเมื่อ 2020-05-11.
- ↑ "What Is R0? Gauging Contagious Infections". Healthline (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-26.
pronounced 'R naught'
- ↑ 72.0 72.1 72.2 He, Xi; Lau, Eric H. Y.; Wu, Peng; Deng, Xilong; Wang, Jian; Hao, Xinxin; Lau, Yiu Chung; Wong, Jessica Y.; Guan, Yujuan; Tan, Xinghua; Mo, Xiaoneng; Chen, Yanqing; Liao, Baolin; Chen, Weilie; Hu, Fengyu; Zhang, Qing; Zhong, Mingqiu; Wu, Yanrong; Zhao, Lingzhai; Zhang, Fuchun; Cowling, Benjamin J.; Li, Fang; Leung, Gabriel M. (May 2020). "Temporal dynamics in viral shedding and transmissibility of COVID-19". Nature Medicine (ภาษาอังกฤษ). pp. 672–675. doi:10.1038/s41591-020-0869-5. สืบค้นเมื่อ 2020-05-11.
- ↑ Fraser, Christophe; Donnelly, Christl A; Cauchemez, Simon และคณะ (2009-06-19). "Pandemic Potential of a Strain of Influenza A (H1N1): Early Findings". Science. 324 (5934): 1557–1561. Bibcode:2009Sci...324.1557F. doi:10.1126/science.1176062. PMC 3735127. PMID 19433588.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) Free text - ↑ "COVID-19 Infections Tracker". COVID-19 Projections Using Machine Learning. สืบค้นเมื่อ 2020-05-11.
- ↑ "About covid19-projections.com". COVID-19 Projections Using Machine Learning. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-26. สืบค้นเมื่อ 2020-05-11.
- ↑ "People with COVID-19 may be infectious days before symptoms: study". medicalxpress.com (ภาษาอังกฤษ). 2020-04-15. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-10. สืบค้นเมื่อ 2020-05-11.
- ↑ 77.0 77.1 "50 Percent of People with COVID-19 Aren't Aware They Have Virus". Healthline (ภาษาอังกฤษ). 2020-04-24. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-23. สืบค้นเมื่อ 2020-05-11.
- ↑ "HGHI and NPR publish new state testing targets - Pandemics Explained". globalepidemics.org. 2020-05-07. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-26. สืบค้นเมื่อ 2020-05-11.
- ↑ 79.0 79.1 "U.S. Coronavirus Testing Still Falls Short. How's Your State Doing?". NPR.org (ภาษาอังกฤษ). 2020-05-07. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-11.
- ↑ "What Testing Capacity Do We Need?". The Henry J. Kaiser Family Foundation. 2020-04-17. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-11.
- ↑ Romer, Paul. "Roadmap to responsibly reopen America" (PDF). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-05-28. สืบค้นเมื่อ 2020-05-11.
- ↑ "Roadmap to pandemic resilience" (PDF). EDMOND J. SAFRA CENTER FOR ETHICS AT HARVARD UNIVERSITY. 2020-04-20. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-11.
- ↑ "National Covid-19 Testing Action Plan". The Rockefeller Foundation. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-23. สืบค้นเมื่อ 2020-05-11.
- ↑ 84.0 84.1 "US Historical Data". The COVID Tracking Project (ภาษาอังกฤษ).
- ↑ "Which States Are Doing Enough Testing? This Benchmark Helps Settle The Debate". NPR.org (ภาษาอังกฤษ). 2020-04-22. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-11.
- ↑ Roser, Max; Ritchie, Hannah; Ortiz-Ospina, Esteban (2020-03-04). "Coronavirus Disease (COVID-19) - Statistics and Research". Our World in Data – โดยทาง ourworldindata.org.
- ↑ "COVID-19: Tests per day". Our World in Data. สืบค้นเมื่อ 2020-04-15.
- ↑ 88.0 88.1 "Coronavirus (COVID-19): Scaling up our testing programmes" (PDF). Department of Health and Social Care. 2020-04-04. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-04-09.
- ↑ "Coronavirus und Covid-19: So testet Deutschland". Der Spiegel (ภาษาเยอรมัน). 2020-03-05. สืบค้นเมื่อ 2020-03-23.
- ↑ Oltermann, Philip (2020-03-22). "Germany's low coronavirus mortality rate intrigues experts". The Guardian (ภาษาอังกฤษแบบบริติช). ISSN 0261-3077. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-30. สืบค้นเมื่อ 2020-03-24.
- ↑ "Covid-19 - Tests auf das Coronavirus: Wann, wo und wie?". Deutschlandfunk (ภาษาเยอรมัน). 2020-03-19. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-24.
- ↑ Charisius, Hanno (2020-03-26). "Covid-19: Wie gut testet Deutschland?" (ภาษาเยอรมัน). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-23. สืบค้นเมื่อ 2020-03-26.
- ↑ "Coronavirus Disease 2019 Daily Situation Report of the Robert Koch Institute". Robert Koch Institute. 2020-03-26. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-03-27. สืบค้นเมื่อ 2020-04-28.
- ↑ "NHS pilots home testing for coronavirus". MobiHealthNews. 2020-02-24. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-02-25.
- ↑ "Mayo Clinic starts drive-thru testing for COVID-19". PostBulletin.com (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-13.
- ↑ Hawkins, Andrew J. (2020-03-11). "Some states are offering drive-thru coronavirus testing". The Verge (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-22. สืบค้นเมื่อ 2020-03-13.
- ↑ "South Korea's Drive-Through Testing For Coronavirus Is Fast - And Free". npr (ภาษาอังกฤษ). 2020-03-11. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-16.
- ↑ "In Age of COVID-19, Hong Kong Innovates To Test And Quarantine Thousands". NPR.org (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ "Pooling method allows dozens of COVID-19 tests to run simultaneously". medicalxpress.com (ภาษาอังกฤษแบบอเมริกัน). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-22. สืบค้นเมื่อ 2020-03-24.
- ↑ "Israeli team has coronavirus test kit to test dozens of people at once". The Jerusalem Post | JPost.com. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-19. สืบค้นเมื่อ 2020-03-24.
- ↑ Israel21c Staff (2020-03-19). "Israelis introduce method for accelerated COVID-19 testing". Israel21c. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-22. สืบค้นเมื่อ 2020-03-24.
- ↑ "[Coronavirus] Verified 'sample pooling' introduced to prevent herd infection in S. Korea". www.ajudaily.com (ภาษาอังกฤษ). 2020-04-09. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-30. สืบค้นเมื่อ 2020-04-19.
- ↑ "Gov. Ricketts provides update on coronavirus testing". KMTV (ภาษาอังกฤษ). 2020-03-24. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-20. สืบค้นเมื่อ 2020-04-19.
- ↑ "Latest coronavirus update: UP to begin 'pool testing' of Covid suspects". Free Press Journal (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-17. สืบค้นเมื่อ 2020-04-19.
- ↑ "West Bengal to start pool testing of samples in low-risk zones". The Times of India (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-22. สืบค้นเมื่อ 2020-04-19.
- ↑ "Punjab launches pool testing". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-20. สืบค้นเมื่อ 2020-04-19.
- ↑ "'Chhattisgarh to adopt pool sample testing': Health minister TS Singh Deo on Covid-19". Hindustan Times (ภาษาอังกฤษ). 2020-04-15. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-15. สืบค้นเมื่อ 2020-04-19.
- ↑ "Maharashtra to go for pool testing to defeat coronavirus". Deccan Herald (ภาษาอังกฤษ). 2020-04-12. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-15. สืบค้นเมื่อ 2020-04-19.
- ↑ "Wuhan Test Lab Opens; CDC Ships Diagnostic Kits: Virus Update". Bloomberg. 2020-02-05. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-02-05. สืบค้นเมื่อ 2020-02-07.
- ↑ 110.0 110.1 "China virus crisis deepens as whistleblower doctor dies". AFP.com (ภาษาอังกฤษ). 2012-02-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27. สืบค้นเมื่อ 2020-02-07.
- ↑ 日检测量达万份的"火眼"实验室连夜试运行. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-02-06.
- ↑ "BGI's Coronavirus Response? Build a Lab in Wuhan". GEN - Genetic Engineering and Biotechnology News (ภาษาอังกฤษแบบอเมริกัน). 2020-02-12. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-07. สืบค้นเมื่อ 2020-03-27.
- ↑ "COVID-19 Local Laboratory Solution". BGI - Global (ภาษาอังกฤษแบบบริติช). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14. สืบค้นเมื่อ 2020-03-27.
- ↑ "Origami Assays". Origami Assays. 2020-04-02. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14. สืบค้นเมื่อ 2020-04-07.
- ↑ "Coronavirus disease 2019 (COVID-19) pandemic: increased transmission in the EU/EEA and the UK -seventh update" (PDF). European Centre for Disease Prevention and Control. 2020-03-25. pp. 15–16. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-04-27. สืบค้นเมื่อ 2020-03-29.
the current shortages of laboratory consumables and reagents affect diagnostic capacity and hamper the epidemic response at the national and local levels. The laboratories have experienced delayed or missing deliveries of swabbing material, plastic consumables, RNA extraction and RT-PCR reagents, and PPE. This is affecting laboratories in all EU/EEA countries.
- ↑
Baird, Robert P. (2020-03-24). "Why Widespread Coronavirus Testing Isn't Coming Anytime Soon". The New Yorker (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-28. สืบค้นเมื่อ 2020-03-29.
South Dakota, said that her state’s public-health laboratory—the only lab doing COVID-19 testing in the state—had so much trouble securing reagents that it was forced to temporarily stop testing altogether. also noted critical shortages of extraction kits, reagents, and test kits
- ↑
Ossola, Alexandra (2020-03-25). "Here are the coronavirus testing materials that are in short supply in the US". Quartz (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-26. สืบค้นเมื่อ 2020-03-29.
extract the virus’s genetic material—in this case, RNA—using a set of chemicals that usually come in pre-assembled kits. “The big shortage is extraction kits” There are no easy replacements here: “These reagents that are used in extraction are fairly complex chemicals. They have to be very pure, and they have to be in pure solution”
- ↑
Fomsgaard, Anders (2020-03-27). "Statens Serum Institut (SSI) solves essential COVID-19 testing deficiency problem". en.ssi.dk (ภาษาอังกฤษ). Statens Serum Institut. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-29.
several countries are in lack of the chemical reagents necessary to test their citizens for the disease.
- ↑ "Danish researchers behind simple coronavirus test method". cphpost.dk. The Copenhagen Post. 2020-03-28. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-28.
- ↑ Sullivan, Helen; Rawlinson, Kevin; Gayle, Damien; Topping, Alexandra; Mohdin, and Aamna; Willsher, Kim; Wintour, Patrick; Wearden, Graeme; Greenfield, Patrick (2020-03-31). "Global confirmed virus death toll passes 40,000 - as it happened". The Guardian (ภาษาอังกฤษแบบบริติช). ISSN 0261-3077. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-07. สืบค้นเมื่อ 2020-04-01.
- ↑ "VIDEO: UAE sets up COVID-19 detection lab in just 14 days". Gulf Today. 2020-03-31. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ "Private Labs Should Be Reimbursed At Appropriate Time For COVID-19 Tests, Says AIIMS RDA General Secretary". BW BUSINESSWORLD. 2020-04-30. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-30.
- ↑ "Covid-19: Private laboratories struggle with price caps, do only 17% tests". The Economic Times. 2020-04-23. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27.
- ↑ Lee, Timothy B. (2020-04-02). "America's COVID-19 testing has stalled, and that's a big problem". Ars Technica. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-24.
- ↑ "PolitiFact - Biden falsely says Trump administration rejected WHO coronavirus test kits (that were never offered)". @politifact. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-19.
- ↑ 126.0 126.1 "Heartbreak in the Streets of Wuhan". Bloomberg Businessweek. 2020-03-12. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ 127.0 127.1 "State figures on testing raise questions about efforts to contain outbreak". The BostonGlobe.com. 2020-03-14. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
flaws with the testing kits first distributed by the federal government and bureaucratic hurdles that held up testing by private labs at hospitals, universities and testing chains
- ↑ Davey, Melissa (2020-03-14). "Australian stocks of coronavirus testing kits 'rapidly deteriorating', says chief medical officer". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-12 – โดยทาง www.theguardian.com.
- ↑ "Experts Credit South Korea's Extensive Testing For Curbing Coronavirus Spread". NPR.org. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27.
- ↑ "'Test, Test, Test': WHO Chief's Coronavirus Message to World". The New York Times. 2020-03-16. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-20. สืบค้นเมื่อ 2020-03-16.
- ↑ Reuters, Source (2020-03-16). "'Test, test, test': WHO calls for more coronavirus testing - video". The Guardian. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-15. สืบค้นเมื่อ 2020-03-16.
- ↑ "Coronavirus Testing Backlogs Continue As Laboratories Struggle To Keep Up With Demand". NPR.org. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28.
- ↑ "Laboratory Readiness for Detecting the 2019 novel coronavirus (2019-nCoV) infection in Malaysia". Director-General of Health, Malaysia. 2020-02-09. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-02.
- ↑ "Malaysia must ramp up testing". The Star Malaysia. 2020-03-26. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-30.
- ↑ "UK defends coronavirus response after Reuters investigation". Reuters (ภาษาอังกฤษ). 2020-04-09. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-24. สืบค้นเมื่อ 2020-04-12.
After developing a test for the new virus by Jan. 10
- ↑ "COVID-19 virus testing in NHS laboratories" (PDF). NHS England and NHS Improvement. 2020-03-16. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-04-12.
- ↑
- "PHE novel coronavirus diagnostic test rolled out across UK". GOV.UK (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-11. สืบค้นเมื่อ 2020-03-30
- "'Increased likelihood' of China virus reaching UK". BBC News (ภาษาอังกฤษแบบบริติช). 2020-01-23. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-15. สืบค้นเมื่อ 2020-03-30
- "PHE tells patients with suspected coronavirus to call GP or NHS 111" (ภาษาอังกฤษ). The Pharmaceutical Journal. 2020-01-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-30.
- ↑ Sheridan, Cormac (2020-02-19). "Coronavirus and the race to distribute reliable diagnostics". Nature Biotechnology (ภาษาอังกฤษ). 38 (4): 382–384. doi:10.1038/d41587-020-00002-2. PMID 32265548. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-25.
- ↑ Jeong, Sei-im (2020-02-28). "Korea approves 2 more COVID-19 detection kits for urgent use". koreabiomed.com (ภาษาเกาหลี). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-12.
- ↑ "[NEW PRODUCT] COVID-19 KIT". kogene.co.kr. 2020-02-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-23.
- ↑ "BGI Sequencer, Coronavirus Molecular Assays Granted Emergency Use Approval in China". GenomeWeb. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-09.
- ↑ "About IRR". internationalreagentresource.org. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-20.
- ↑ "Transcript for the CDC Telebriefing Update on COVID-19". CDC. 2020-02-28. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14.
- ↑ "LabCorp Launches Test for Coronavirus Disease 2019 (COVID-19)". Laboratory Corporation of America Holdings. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-19.
- ↑ "Covid19 : COVID-19". questdiagnostics.com. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28.
- ↑ Совещание по вопросам развития ситуации с коронавирусной инфекцией и мерам по её профилактике
- ↑ "В России зарегистрирована отечественная тест-система для определения коронавируса" [Russia has registered a domestic test system for determining coronavirus]. Interfax-Russia.ru. 2020-02-14. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ Plumbo, Ginger (2020-03-12). "Mayo Clinic develops test to detect COVID-19 infection". Mayo Clinic (ภาษาอังกฤษแบบอเมริกัน). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-01. สืบค้นเมื่อ 2020-03-13.
- ↑ 149.0 149.1 "Emergency Use Authorization". FDA. 2020-04-30. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-29.
- ↑ "Hologic's Molecular Test for the Novel Coronavirus, SARS-CoV-2, Receives FDA Emergency Use Authorization". Hologic. 2020-03-16. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-13.
- ↑ "FDA Approves Abbott Laboratories Coronavirus Test, Company To Ship 150,000 Kits". IBTimes.com. 2020-03-19. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-03-20.
- ↑ "Sunnyvale company wins FDA approval for first rapid coronavirus test with 45-minute detection time". EastBayTimes.com. 2020-03-21. เก็บจากแหล่งเดิมเมื่อ 2020-03-22. สืบค้นเมื่อ 2020-05-03.
- ↑ "Xpert® Xpress SARS-CoV-2 has received FDA Emergency Use Authorization". www.cepheid.com (ภาษาอังกฤษแบบอเมริกัน). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-22. สืบค้นเมื่อ 2020-04-13.
- ↑ "Health Canada approves new rapid COVID-testing kits". The Globe and Mail Inc. 2020-04-13. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ "The power of DNA testing for everyone". Spartan Bioscience. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-22. สืบค้นเมื่อ 2020-04-14.
- ↑ "Letter from FDA". FDA. 2020-03-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27. สืบค้นเมื่อ 2020-04-02.
- ↑ 157.0 157.1 "ID NOW COVID-19, Instruction for Use". FDA. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-21.
- ↑ "The scramble for the rapid coronavirus tests everybody wants". Washington Post. 2020-04-01. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-01.
- ↑ "'A game changer': FDA authorizes Abbott Labs' portable, 5-minute coronavirus test the size of a toaster". USA Today. 2020-03-28. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-20.
- ↑ "To protect Trump, White House among first to use rapid coronavirus tests sought by communities". Washington Post. 2020-04-07. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-08.
- ↑ "Study Raises Questions About False Negatives From Quick COVID-19 Test". NPR. 2020-04-21. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-05-01.
- ↑ 162.0 162.1 "FDA issues emergency approval of new antigen test that is cheaper, faster and simpler". Washington Post. 2020-05-09.
- ↑ "Concurrent Engineering for Lateral-Flow Diagnostics (IVDT archive, Nov 99)". Nov 1999. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2010-12-28.
- ↑ "Paper-based microfluidic point-of-care diagnostic devices". 2013. doi:10.1039/C3LC50169H.
{{cite journal}}: Cite journal ต้องการ|journal=(help) - ↑ "LATERAL FLOW". BioDot Inc. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2012-07-28.
- ↑
"Synthetic microfluidic paper: high surface area and high porosity polymer micropillar arrays". 2016. doi:10.1039/C5LC01318F.
{{cite journal}}: Cite journal ต้องการ|journal=(help) - ↑
Guo, Weijin; Hansson, Jonas; van der Wijngaart, Wouter (2016). "Viscosity Independent Paper Microfluidic Imbibition" (PDF). MicroTAS. Dublin, Ireland. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2018-07-30.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 168.0 168.1 168.2 "Sofia 2 SARS Antigen FIA Instructions for Use". FDA. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-28.
- ↑ "Sofia 2 package insert" (PDF). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-05-28. สืบค้นเมื่อ 2020-05-12.
- ↑ "Emergency Use Authorizations". FDA. 2020-05-01. สืบค้นเมื่อ 2020-05-01.
- ↑ "Tests that have been approved for diagnostic use in other countries". Johns Hopkins. 2020-04-30. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-06-09. สืบค้นเมื่อ 2020-05-01.
- ↑ "Quest Diagnostics Launches Consumer-Initiated COVID-19 Antibody Test Through QuestDirect™". Quest Diagnosics. 2020-04-28. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-26.
- ↑ "NIH Begins Study to Quantify Undetected Cases of Coronavirus Infection | NIH: National Institute of Allergy and Infectious Diseases". niaid.nih.gov. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-26. สืบค้นเมื่อ 2020-04-11.
- ↑ Mandavilli, Apoorva; Thomas, Katie (2020-04-10). "Will an Antibody Test Allow Us to Go Back to School or Work?". The New York Times. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-27. สืบค้นเมื่อ 2020-04-11.
- ↑ Yadlowsky, Steve; Shah, Nigam; Steinhardt, Jacob (2020-03-27). "Estimation of SARS-CoV-2 Infection Prevalence in Santa Clara County". Medrxiv. medrxiv.org. doi:10.1101/2020.03.24.20043067. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-16. สืบค้นเมื่อ 2020-04-17.
- ↑ "Antibody tests suggest that coronavirus infections vastly exceed official counts". Nature. 2020-04-19. สืบค้นเมื่อ 2020-04-20.
- ↑ 177.0 177.1 "WHO Emergency Use Listing for SARS‐CoV‐2 in vitro diagnostic products" (PDF). องค์การอนามัยโลก. สืบค้นเมื่อ 2020-05-04.
- ↑ "WHO lists two COVID-19 tests for emergency use". World Health Organization. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-14. สืบค้นเมื่อ 2020-04-10.
- ↑ "Chinese firm to replace exported coronavirus test kits deemed defective by Spain". 2020-03-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-24 – โดยทาง www.reuters.com.
- ↑ Morning, Prague (2020-03-26). "80% of Rapid COVID-19 Tests the Czech Republic Bought From China are Wrong". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-25.
- ↑
VOJTĚCH BLAŽEK (2020-03-23). "Úřad dopředu psal, kdy mohou rychlotesty selhat. I tak je stát nasadil" [The office wrote in advance when rapid tests could fail. Even so, the state deployed them]. Zeznam Zprávy (ภาษาเช็ก). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-07. สืบค้นเมื่อ 2020-04-07.
Indeed, the rapid tests that arrived from China a few days ago do not really reliably detect the infection at an early stage
- ↑ "Europe turned to China for coronavirus testing help. Why some are now regretting it". Fortune. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-19.
- ↑ "Coronavirus test kits purchased from China are unreliable, says Science Committee member". www.duvarenglish.com. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ "Coronavirus: Turkey rejects Chinese testing kits over inaccurate results". Middle East Eye. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28.
- ↑
Reporter, Chris Smyth, Whitehall Editor | Dominic Kennedy, Investigations Editor | Billy Kenber, Investigations. "Britain has millions of coronavirus antibody tests, but they don't work". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27 – โดยทาง www.thetimes.co.uk.
{{cite web}}:|first=มีชื่อเรียกทั่วไป (help) - ↑ "Government's testing chief admits none of 3.5m coronavirus antibody kits work sufficiently". The Independent. 2020-04-06. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-12.
- ↑ "ICMR asks states not to use rapid test kits for two days". The Telegraph. 2020-04-21. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28.
- ↑ "National laboratories". who.int (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-30.
- ↑
"PHE novel coronavirus diagnostic test rolled out across UK". GOV.UK (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-11. สืบค้นเมื่อ 2020-04-12.
In addition to processing samples from suspected cases in this country, PHE is now working as a reference laboratory for WHO, testing samples from countries that do not have assured testing capabilities.
- ↑ "Specimen referral for COVID-19 - operational details of WHO reference laboratories providing confirmatory testing for COVID-19" (PDF). World Health Organization. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-04-11. สืบค้นเมื่อ 2020-03-29.
- ↑ "How an experiment helped one Italian town find 'submerged infections,' cut new COVID-19 cases to zero". National Post. 2020-03-19.
- ↑ "COVID-19 outbreak: Petition to close schools in Singapore garners 7,700 signatures to date". msn.com. 2020-03-24. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18.
- ↑ "Coronavirus: Most workplaces to close, schools will move to full home-based learning from next week, says PM Lee". The Straits Times. 2020-04-03. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-23.
- ↑ "Coronavirus clue? Most cases aboard U.S. aircraft carrier are symptom-free". Reuters. 2020-04-16. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-11.
- ↑ "Over 3 mln COVID-19 tests conducted in Russia". TASS. 2020-04-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-11. สืบค้นเมื่อ 2020-04-29.
- ↑ "О подтвержденных случаях новой коронавирусной инфекции COVID-2019 в России". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-28.
- ↑ "Попова заявила, что взрывной рост заболеваемости не допущен из-за принимаемых мер" [Popova said explosive growth in incidence was not allowed due to measures taken]. TASS. 2020-04-28. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-12. สืบค้นเมื่อ 2020-04-29.
- ↑ "COVID-19: First results of the voluntary screening in Iceland". Nordic Life Science - the leading Nordic life science news service (ภาษาอังกฤษแบบอเมริกัน). 2020-03-27. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-27. สืบค้นเมื่อ 2020-04-05.
- ↑ Normile, Dennis (2020-03-17). "Coronavirus cases have dropped sharply in South Korea. What's the secret to its success?". Science (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-05-01. สืบค้นเมื่อ 2020-04-05.
- ↑ Ward, Dan (May 2020) "Sampling Bias: Explaining Variations in Age Distributions of COVID-19 Cases". Technical Report. WardEnvironment. doi: 10.13140/RG.2.2.27321.19047/2
- ↑ "Catching Virus Fast! Academia Sinica discovered useful antibodies for developing rapid immune based test kit of SARS-CoV-2 coronavirus". sinica.edu.tw. Academia Sinica. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-18. สืบค้นเมื่อ 2020-03-12.
- ↑ "Advice on the use of point-of-care immunodiagnostic tests for COVID-19". who.int (ภาษาอังกฤษ). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-28. สืบค้นเมื่อ 2020-04-11.
- ↑ "Fauci once dismissed concerns about 'silent carriers' of coronavirus. Not anymore". Yahoo News. 2020-04-07. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-04-29.
แหล่งข้อมูลอื่น
[แก้]![]() บทความนี้รวมเอางานสาธารณสมบัติจากเว็บไซต์หรือเอกสารของ ศูนย์ควบคุมและป้องกันโรคสหรัฐ (CDC) "Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19" (สืบค้นเมื่อ 2020-05-05)
บทความนี้รวมเอางานสาธารณสมบัติจากเว็บไซต์หรือเอกสารของ ศูนย์ควบคุมและป้องกันโรคสหรัฐ (CDC) "Symptom-Based Strategy to Discontinue Isolation for Persons with COVID-19" (สืบค้นเมื่อ 2020-05-05)
- Data on COVID-19 testing at Our World in Data (31 March 2020)
- COVID-19 Testing (at least) - now Free for all? (CDC; US Congress; CSPAN video/6:00; March 12, 2020)
- Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR; NCBI-PMC, DOI (23 January 2020)
- "EUA Authorized Serology Test Performance". U.S. Food and Drug Administration (FDA).
- CS1 maint: uses authors parameter
- บทความที่ขาดแหล่งอ้างอิงเฉพาะส่วนตั้งแต่April 2020
- บทความที่ขาดแหล่งอ้างอิงเฉพาะส่วนตั้งแต่March 2020
- Wikipedia articles incorporating text from the Centers for Disease Control and Prevention
- Infectious disease blood tests
- โรคติดเชื้อ
- การตรวจเลือด
- COVID-19
- Medical responses to the 2019-20 coronavirus pandemic
- บทความเกี่ยวกับ การแพทย์ ที่ยังไม่สมบูรณ์