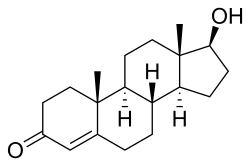
เทสโทสเตอโรน
| |

| |
| ชื่อ | |
|---|---|
| IUPAC name
(8R,9S,10R,13S,14S,17S)-17-hydroxy-10,13-dimethyl-1,2,6,7,8,9,11,12,14,15,16,17-dodecahydrocyclopenta[a]phenanthren-3-one
| |
| ชื่ออื่น
Androst-4-en-17β-ol-3-one
| |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ดรักแบงก์ | |
| ECHA InfoCard | 100.000.336 |
| KEGG | |
ผับเคม CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| C19H28O2 | |
| มวลโมเลกุล | 288.42 g/mol |
| จุดหลอมเหลว | 155 |
| เภสัชวิทยา | |
| G03BA03 (WHO) | |
| ผ่านผิวหนัง (เจล, ครีม, ยาทา, แผ่นแปะผิวหนัง), ทางปาก (testosterone undecanoate), กระพุ้งแก้มในปาก, สูดทางจมูก, ฉีดในกล้ามเนื้อ (Testosterone esters), ฝังใต้ผิวหนัง | |
| เภสัชจลนศาสตร์: | |
| ทางปาก - ต่ำมาก (เนื่องจากต้องผ่านการย่อยอาหาร) | |
| 97.0-99.5% (กับ sex hormone-binding globulin และ human serum albumin)[1] | |
| ตับ (โดย reduction และ conjugation) | |
| 2-4 ชม.[ต้องการอ้างอิง] | |
| ปัสสาวะ (90%), อุจจาระ (6%) | |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
เทสโทสเตอโรน (อังกฤษ: Testosterone) เป็นฮอร์โมนหลักในกลุ่มฮอร์โมนเพศชายและสเตอรอยด์การสร้าง (anabolic steroid) ประเภทหนึ่งที่พบในสัตว์มีกระดูกสันหลังโดยมาก มีบทบาทสำคัญในพัฒนาการของเนื้อเยื่อในระบบสืบพันธุ์ชาย เช่น อัณฑะและต่อมลูกหมาก ตลอดจนส่งเสริมลักษณะเฉพาะทางเพศทุติยภูมิ เช่น การเจริญเติบโตของกล้ามเนื้อกับกระดูก และการเกิดขนตัว[2] นอกจากนั้นแล้ว ฮอร์โมนยังเป็นสิ่งที่ขาดไม่ได้ต่อสุขภาพและความอยู่เป็นสุข[3] ตลอดจนป้องกันโรคกระดูกพรุน[4] ระดับฮอร์โมนที่ไม่พอในชาย อาจทำให้เกิดความผิดปกติต่าง ๆ เช่น ความอ่อนแอและการเสียกระดูก ฮอร์โมนอาจใช้เพื่อรักษาอวัยวะเพศชายทำงานไม่พอ (male hypogonadism) และมะเร็งเต้านมบางชนิด[5] เนื่องจากระดับฮอร์โมนจะลดลงเรื่อย ๆ ตามอายุ แพทย์บางครั้งจะให้ฮอร์โมนสังเคราะห์กับชายสูงอายุเพื่อแก้ปัญหาการขาด เทสโทสเตอโรนเป็นสเตอรอยด์ในกลุ่ม androstane ที่มีกลุ่มคีโทนและไฮดรอกซิลที่ตำแหน่ง 3 และ 17 ตามลำดับ ซึ่งสามารถสังเคราะห์จากคอเลสเตอรอลในหลายขั้นตอน และตับจะเปลี่ยนมันเป็นเมแทบอไลต์ที่ไม่มีฤทธิ์[6] ฮอร์โมนสามารถเข้ายึดและออกฤทธิ์ต่อตัวรับแอนโดรเจน (androgen receptor) ในนิวเคลียสของเซลล์[6]
ในมนุษย์และสัตว์มีกระดูกสันหลังโดยมาก อัณฑะเป็นอวัยวะที่หลั่งฮอร์โมนในชาย และรังไข่ในหญิงแม้ในระดับที่ต่ำกว่า ต่อมหมวกไตก็หลั่งฮอร์โมนแม้เล็กน้อยด้วย โดยเฉลี่ย ในชายผู้ใหญ่ ระดับเทสโทสเตอโรนจะอยู่ที่ 7-8 เท่าของหญิงผู้ใหญ่[7] เพราะฮอร์โมนมีเมแทบอลิซึมที่สูงกว่าในชาย การผลิตแต่ละวันจะมากกว่าหญิงประมาณ 20 เท่า[8][9] หญิงยังไวต่อฮอร์โมนมากกว่าชายอีกด้วย[10]
ผลทางสรีรภาพ[แก้]
โดยทั่วไปแล้ว ฮอร์โมนแอนโดรเจน เช่น เทสโทสเตอโรน จะสนับสนุนการสังเคราะห์โปรตีนและดังนั้น การเจริญเติบโตของเนื้อเยื่อที่มีตัวรับแอนโดรเจน (androgen receptor)[11] ฮอร์โมนยังเรียกได้ว่ามีผลสร้างบุรุษภาพและทำให้โต[12]
- ผลทำให้โต (Anabolic effects) รวมทั้งการเพิ่มขนาดและความแข็งแรงของกล้ามเนื้อ เพิ่มความหนาแน่นและความแข็งแรงของกระดูก และกระตุ้นให้สูงขึ้นและให้กระดูกเจริญเต็มที่เป็นผู้ใหญ่
- ผลสร้างบุรุษภาพ (Androgenic effects) รวมทั้งการทำให้อวัยวะเพศเจริญเติบโตเต็มวัย โดยเฉพาะองคชาตและถุงอัณฑะในทารก และภายหลังคลอด (ปกติในช่วงวัยเริ่มเจริญพันธุ์) เสียงแตก ขนที่ใบหน้า (เช่นหนวดเครา) และขนรักแร้
ซึ่งผลหลายอย่างเหล่านี้เป็นลักษณะเฉพาะเพศชายทุติยภูมิ ผลของเทสโทสเตอโรนยังสามารถจัดตามอายุที่ปกติเกิดขึ้น หลังจากคลอดในทั้งหญิงชาย ผลโดยมากจะเป็นไปตามระดับและระยะที่มีเทสโทสเตอโรนอิสระเวียนในเลือด
ก่อนเกิด[แก้]
ผลก่อนเกิดแบ่งออกเป็นสองกลุ่ม โดยจัดตามระยะพัฒนาการ ระยะแรกเกิดขึ้นระหว่าง 4-6 อาทิตย์ในครรภ์ ตัวอย่างรวมทั้งการสร้างอวัยวะเพศ รวมทั้ง midline fusion, การสร้างท่อปัสสาวะในองคชาต, การทำถุงอัณฑะให้บางและมีรอยย่น, การเพิ่มขนาดองคชาต, ตลอดจนพัฒนาการของต่อมลูกหมากและถุงพักน้ำอสุจิ (seminal vesicle) ด้วย แม้ว่าบทบาทของเทสโทสเตอโรนจะน้อยกว่าของ dihydrotestosterone มาก
ในไตรมาสที่สอง ระดับแอนโดรเจนจะขึ้นอยู่กับเพศ[13] ไตรมาสนี้มีผลต่อการสร้างบุรุษภาพและสตรีสภาพของทารก และเป็นตัวพยากรณ์พฤติกรรมเพศหญิงหรือชาย ได้ดียิ่งกว่าระดับฮอร์โมนแม้ในตัวเองเมื่อเป็นผู้ใหญ่ เช่น ระดับเทสโทสเตอโรนของมารดาระหว่างมีครรภ์จะมีสหสัมพันธ์กับพฤติกรรมตามเพศของลูกสาว ที่มีกำลังยิ่งกว่าระดับฮอร์โมนของตัวลูกสาวเองเมื่อเป็นผู้ใหญ่[14]
ทารกวัยต้น[แก้]
ผลของแอนโดรเจนต่อทารกวัยต้นเป็นเรื่องที่เข้าใจน้อยที่สุด ในอาทิตย์แรกของทารกชาย ระดับเทสโทสเตอโรนจะสูงขึ้น ระดับจะอยู่ในพิสัยที่มีในช่วงวัยรุ่นเป็นเวลา 2-3 เดือน แต่ปกติจะลดลงถึงระดับเด็กที่แทบตรวจจับไม่ได้โดยอายุ 4-6 เดือน[15][16]
หน้าที่ของระดับฮอร์โมนที่สูงขึ้นในมนุษย์ยังไม่ชัดเจน มีการคาดว่า เป็นการสร้างบุรุษภาพในสมอง เนื่องจากว่าอวัยวะอื่น ๆ ไม่เปลี่ยนแปลงอย่างสำคัญ[17] สมองเพศชายจะเกิดบุรุษภาพอาศัยกระบวนการ aromatization ที่เปลี่ยนเทสโทสเตอโรนให้เป็นเอสโทรเจน ซึ่งสามารถข้ามส่วนกั้นระหว่างเลือด-สมอง (blood-brain barrier) เข้าไปในสมอง เทียบกับทารกหญิงที่จะมีโปรตีน α-fetoprotein เข้ายึดกับเอสโทรเจน ทำให้สมองของหญิงไม่เปลี่ยนแปลง[18]
ก่อนวัยเริ่มเจริญพันธุ์[แก้]
แอนโดรเจนจะเพิ่มขึ้นอย่างมีผลก่อนวัยเริ่มเจริญพันธุ์ทั้งในหญิงชาย ผลรวมทั้งกลิ่นตัวเหมือนผู้ใหญ่ ผิวหนังและผมมัน สิว การเกิดของขนหัวหน่าว ขนรักแร้ การเจริญเติบโตอย่างรวดเร็ว การเจริญเติบโตของกระดูกเป็นผู้ใหญ่ และขนที่ใบหน้า[19]
วัยเริ่มเจริญพันธุ์[แก้]
ผลในวัยเริ่มเจริญพันธุ์จะเกิดเมื่อระดับแอนโดรเจนสูงกว่าระดับในหญิงผู้ใหญ่เป็นเวลาหลายเดือนหรือหลายปี ในชาย นี้มักจะเกิดในช่วงหลัง ๆ และจะเกิดในหญิงหลังจากมีระดับเทสโทสเตอโรนอิสระในเลือดสูงเป็นระยะเวลานาน ผลรวมทั้ง[19][20]
การเจริญของเนื้อเยื่อที่ผลิตตัวอสุจิในอัณฑะ ภาวะเจริญพันธุ์ของชาย การขยายขนาดขององคชาตหรือปุ่มกระสัน การเพิ่มอารมณ์ทางเพศ และการแข็งตัวขององคชาตหรือการมีเลือดคั่งคัดในปุ่มกระสัน การเติบโตของขากรรไกร หน้าผาก คาง จมูก และการเปลี่ยนรูปของกระดูกใบหน้า โดยทำงานสัมพันธ์กับ human growth hormone[21] การเจริญเติบโตของกระดูกจนถึงขนาดผู้ใหญ่และการหยุดโต ซึ่งเกิดโดยอ้อมผ่านเมแทบอไลต์ของ estradiol (ซึ่งเป็นฮอร์โมนหญิงหลัก) และดังนั้น จะเกิดอย่างค่อย ๆ เป็นค่อย ๆ ไปในชายเทียบกับหญิง กล้ามเนื้อจะเพิ่มขนาดและความแข็งแรง ไหล่จะใหญ่ขึ้นและซี่โครงขยายใหญ่ขึ้น เสียงแตก และลูกกระเดือกโตขึ้น ต่อมไขมัน (sebaceous glands) จะขยายใหญ่ขึ้น ซึ่งอาจทำให้เกิดสิว ไขมันใต้ผิวหนังบนใบหน้าจะลดลง ขนหัวหน่าวจะขยายไปถึงต้นขาและไปทางสะดือ ขนใบหน้าจะเกิด (เช่น จอนผม หนวด เครา) ผมจะบาง (androgenetic alopecia) ขนหน้าอก ขนรอบหัวนม ขนรอบทวารหนัก ขนขา และขนรักแร้ จะเพิ่ม
ผู้ใหญ่[แก้]
ผลของเทสโทสเตอโรนในผู้ใหญ่เห็นได้ชัดในชายมากกว่าหญิง แต่น่าจะสำคัญต่อทั้งสองเพศ ผลอาจลดลงเมื่อระดับเทสโทสเตอโรนลดลงตามอายุ[22]

หน้าที่ทางชีวภาพ[แก้]
เทสโทสเตอโรนจำเป็นในการสร้างตัวอสุจิโดยปกติ เพราะมันออกฤทธิ์ต่อ Sertoli cell ซึ่งกระตุ้นให้เซลล์ต้นกำเนิดตัวอสุจิ (spermatogonia) ซึ่งเป็นเซลล์สืบพันธุ์ที่ยังไม่แตกต่างให้เกิดความแตกต่าง และเป็นตัวควบคุมการตอบสนองแบบฉับพลันของเขตสมองคือแกนไฮโปทาลามัส-พิทูอิทารี-อะดรีนัล (HPA) เมื่อมีการแข่งสถานะทางสังคม[23] แอนโดรเจนรวมทั้งเทสโทสเตอโรนจะเพิ่มการเจริญเติบโตของกล้ามเนื้อ เทสโทสเตอโรนยังควบคุมการมีตัวรับ thromboxane A2 ของเซลล์ megakaryocyte ซึ่งอยู่ในไขกระดูกและทำหน้าที่ผลิตเกล็ดเลือด และควบคุมตัวเกล็ดเลือดเอง ดังนั้น จึงควบคุมการแข็งตัวของเลือดในมนุษย์ด้วย[24][25]
ความเสี่ยงต่อสุขภาพ[แก้]
เทสโทสเตอโรนดูจะไม่เพิ่มความเสี่ยงมะเร็งต่อมลูกหมาก แต่ว่า สำหรับคนไข้มะเร็งต่อมลูกหมากที่ผ่านการรักษา testosterone deprivation therapy ซึ่งใช้ยาเพื่อไม่ให้ผลิตแอนโดรเจน การมีระดับเทสโทสเตอโรนที่สูงกว่าระดับที่ถูกตอนมีหลักฐานว่า เพิ่มอัตราการกระจายตัวของมะเร็งต่อมลูกหมากที่มี[26][27][28]
ผลงานวิจัยขัดแย้งกันเรื่องความสำคัญของเทสโทสเตอโรนต่อสุขภาพของหลอดเลือดและหัวใจ[29][30] อย่างไรก็ดี การธำรงระดับปกติในชายสูงอายุมีหลักฐานว่า ช่วยปรับปรุงด้าน ๆ ต่างที่เชื่อว่า ลดความเสี่ยงโรคหลอดเลือดและหัวใจ เช่น มีดัชนีมวลกายที่ดีกว่า ลดไขมันรอบพุง ลดระดับคอเลสเตอรอล และมีเมแทบอลิซึมของน้ำตาลที่ดีกว่า[31]
ในหญิง ระดับแอนโรเจนที่สูงสัมพันธ์กับการมีประจำเดือนไม่สม่ำเสมอทั้งในกลุ่มคนไข้และกลุ่มประชากรปกติ[32]
อารมณ์เพศ[แก้]
เมื่อน้ำอสุจิที่ประกอบด้วยเทสโทสเตอโรนและเอ็นดอร์ฟินหลั่งออกไปกระทบกับผนังคอมดลูกหลังจากมีเพศสัมพันธ์ หญิงจะได้รับเทสโทสเตอโรน เอ็นดอร์ฟิน และออกซิโทซินเพิ่ม เป็นการปรับปรุงสิ่งแวดล้อมทางสรีรภาพของอวัยวะเพศภายในของหญิงให้ดียิ่งขึ้นเพื่อการตั้งครรภ์ และต่อจากนั้น เพื่อบำรุงรักษาทารกในครรภ์ในช่วงก่อนเป็นตัวอ่อน (pre-embryonic stage) ส่วนชายเมื่อถึงจุดสุดยอดจะได้เอ็นดอร์ฟินและออกซิโทซินเพิ่ม ทำให้รู้สึกรักใคร่และรู้สึกเหมือนพ่อ ซึ่งเป็นช่วงเวลาเดียวที่ชายมีออกซิโทซินในระดับที่แข่งกับหญิงได้[33] ระดับเทสโทสเตอโรนในกายจะเป็นไปตามจังหวะรอบวันที่ถึงจุดสูงสุดแต่ละวัน ไม่ว่าจะมีกิจกรรมทางเพศหรือไม่[34]
ความเสียวสุดยอดทางเพศของหญิงที่รู้สึกผ่อนคลายเป็นหลักมีสหสัมพันธ์กับระดับเทสโทสเตอโรน แต่ว่า ความเสียวสุดยอดของชายไม่มีสหสัมพันธ์กับระดับเทสโทสเตอโรน และก็ไม่มีสหสัมพันธ์ระหว่างระดับเทสโทสเตอโรนกับ sexual assertiveness ทั้งในชายหญิง[35]
ในหญิง อารมณ์ทางเพศและการสำเร็จความใคร่ด้วยตนเองจะเพิ่มความเข้มข้นของเทสโทสเตอโรนเล็กน้อย[36] เทียบกับชาย ที่ระดับสเตอรอยด์ต่าง ๆ ในเลือดรวมทั้งระดับเทสโทสเตอโรน จะสูงขึ้นอย่างสำคัญ[37]
สัตว์เลี้ยงลูกด้วยนม[แก้]
งานศึกษาแสดงว่า ระดับอารมณ์เพศในหนูไวต่อการลดระดับเทสโทสเตอโรน เมื่อหนูที่ขาดเทสโทสเตอโรนได้ฮอร์โมนในระดับกลาง ๆ พฤติกรรมทางเพศ (การร่วมเพศ เพื่อนที่ชอบ เป็นต้น) ก็จะกลับมาเหมือนเดิม แต่จะไม่เป็นเช่นนี้ถ้าได้ในระดับน้อย ๆ ดังนั้น สัตว์เลี้ยงลูกด้วยนมเช่นนี้อาจเป็นแบบจำลองเพื่อศึกษาประชากรคนไข้มนุษย์ที่ขาดอารมณ์ทางเพศ เช่น hypoactive sexual desire disorder[38]
ในสัตว์เลี้ยงลูกด้วยนมทุกชนิดที่ตรวจสอบ ระดับเทสโทสเตอโรนของตัวผู้จะสูงขึ้นเมื่อเจอตัวเมีย "ใหม่" การเพิ่มฮอร์โมนเป็นรีเฟล็กซ์ในหนูหริ่งตัวผู้ สัมพันธ์กับระดับอารมณ์เพศที่มีในเบื้องต้น[39]
ในสัตว์อันดับวานรที่ไม่ใช่มนุษย์ เทสโทสเตอโรนในวัยเริ่มเจริญพันธุ์อาจกระตุ้นให้มีอารมณ์เพศ ซึ่งทำให้ลิงหาประสบการณ์ทางเพศกับตัวเมียมากขึ้น และดังนั้น ก็จะทำให้ชอบใจในตัวเมีย[40] งานวิจัยยังแสดงด้วยว่า ถ้ากำจัดเทสโทสเตอโรนออกจากระบบของชายผู้ใหญ่ หรือวานรตัวผู้ที่โตแล้ว ความต้องการทางเพศจะลดลง แต่จะไม่ลดสมรรถภาพในกิจกรรมทางเพศ (รวมทั้งขึ้นขี่ หลั่งน้ำอสุจิ เป็นต้น)[40]
งานศึกษาแสดงว่าระดับเทสโทสเตอโรนของหนูตัวผู้จะเพิ่มขึ้นตอบสนองต่อสิ่งเร้าที่เคยเป็นกลางมาก่อนหลังจากฝึก (conditioned) ให้ตอบสนองทางเพศ[41] โดยทำให้เกิดรีเฟล็กซ์ที่องคชาต (เช่น การแข็งตัวและการหลั่งอสุจิ) ซึ่งทฤษฎีการแข่งขันของตัวอสุจิ (Sperm competition theory) อธิบายว่า ช่วยผลิตตัวอสุจิที่มีโอกาสชนะสูงขึ้น ทำให้มีโอกาสสูงขึ้นในการสืบพันธุ์ ในเมื่อหนูตัวผู้มากกว่าหนึ่งตัวผสมพันธุ์กับตัวเมีย
ชาย[แก้]
ในชาย ระดับเทสโทสเตอโรนที่สูงขึ้นสัมพันธ์กับกิจกรรมทางเพศ[42] ในชายรักต่างเพศ ฮอร์โมนก็จะสูงขึ้นด้วยแม้เพียงแค่คุยกับผู้หญิงระยะสั้น ๆ และระดับเทสโทสเตอโรนที่สูงขึ้นในชายก็จะสัมพันธ์กับระดับที่ผู้หญิงรู้สึกว่าผู้ชายกำลังพยายามทำให้เธอประทับใจ[43]
ชายที่ดูหนังโป๊จะมีระดับเทสโทสเตอโรนสูงขึ้นโดยเฉลี่ย 35% โดยถึงขีดสูงสุดที่ 60-90 นาทีหลังจากหนังจบลง แต่ปรากฏการณ์นี้ไม่พบในชายที่ดูหนังที่ไม่มีเรื่องเซ็กซ์[44] นอกจากนั้นแล้ว ชายที่ดูหนังโป๊ยังรายงานว่า มีกำลังใจเพิ่มขึ้น ต้องการแข่งขันเพิ่มขึ้น และหมดแรงน้อยลง[45] ความผ่อนคลายที่เกิดหลังอารมณ์เพศก็สัมพันธ์กับระดับเทสโทสเตอโรนด้วย[46]
ระดับเทสโทสเตอโรนซึ่งเป็นฮอร์โมนที่มีผลต่อพฤติกรรมทางเพศของชาย จะขึ้นอยู่ว่าได้กลิ่นหญิงที่ตกไข่หรือหญิงที่ไม่ตกไข่ ชายที่ได้กลิ่นหญิงผู้กำลังตกไข่จะธำรงระดับเทสโทสเตอโรนสม่ำเสมอในระดับที่สูงกว่าชายที่ได้กลิ่นหญิงที่ไม่ตกไข่ ดังนั้น ทั้งระดับเทสโทสเตอโรนและอารมณ์เพศของชาย จะขึ้นอยู่กับวงจรทางฮอร์โมนของหญิง[47]
นี่เป็นเรื่องที่อาจสัมพันธ์กับสมมติฐานการเปลี่ยนแปลงเหตุการตกไข่ (ovulatory shift hypothesis)[48] ที่อ้างว่า ผู้ชายปรับตัวให้ตอบสนองต่อวงจรการตกไข่ของหญิงโดยจะรู้ว่า เมื่อไรหญิงเจริญพันธุ์มากที่สุด และผู้หญิงจะสืบหาผู้ชายที่ชอบใจเมื่อถึงจุดที่เจริญพันธุ์มากที่สุด ซึ่งฮอร์โมนอาจเป็นตัวขับเคลื่อนพฤติกรรมของทั้งสอง ชายที่มีขีดเริ่มเปลี่ยนอารมณ์เพศต่ำกว่ามีโอกาสใส่ใจในเรื่องเพศสูงกว่า และเทสโทสเตอโรนอาจทำงานโดยเพิ่มความใส่ใจในสิ่งเร้าที่อยู่ในประเด็น[49]
หญิง[แก้]
แอนโดรเจนอาจจะคุมลักษณะทางกายภาพของเนื้อเยื่อในช่องคลอด และมีส่วนในความตื่นตัวทางเพศของอวัยวะเพศหญิง[50] ระดับเทสโทสเตอโรนของหญิงจะสูงกว่าเมื่อวัดก่อนมีเพศสัมพันธ์เทียบกับก่อนนอนกอดกัน และเมื่อวัดหลังมีเพศสัมพันธ์เทียบกับหลังจากนอนกอดกัน[51] แต่หลังจากให้เทสโทสเตอโรน จะใช้เวลาบ้างก่อนอวัยวะเพศจะตื่นตัว นอกจากนั้นแล้ว อวัยวะเพศที่ตื่นตัวอาจรู้สึกไวกว่าและทำให้มีพฤติกรรมทางเพศมากกว่า[52]
ถ้าหญิงมีระดับพื้นฐาน (baseline) ของเทสโทสเตอโรนที่สูงกว่า ก็จะมีความตื่นตัวทางเพศมากกว่า แต่ก็มีระดับเทสโทสเตอโรนที่เพิ่มขึ้นน้อยกว่า ซึ่งแสดงว่า อาจจะมีขีดสูงสุดที่เทสโทสเตอโรนจะมีผลในหญิง การคิดเรื่องเพศยังเปลี่ยนระดับเทสโทสเตอโรนในหญิงด้วย แต่ไม่เปลี่ยนระดับคอร์ติซอล (ฮอร์โมนเครียด) ดังนั้น ยาคุมกำเนิดโดยฮอร์โมนอาจมีผลต่อระดับเทสโทสเตอโรนที่เป็นการตอบสนองต่อความคิดทางเพศ[53]
เทสโทสเตอโรนอาจมีประสิทธิผลต่อโรคความตื่นตัวทางเพศของหญิง (female sexual arousal disorder)[54] โดยมียาแบบแผ่นแปะผิวหนัง แม้จะไม่มีสูตรยาแอนโดรเจนที่องค์การอาหารและยาสหรัฐ (FDA) อนุมัติให้ใช้รักษาการขาดแอนโดรเจน แต่ว่า แพทย์ก็ยังสามารถสั่งยานอกป้ายเพื่อรักษาการมีอารมณ์เพศต่ำ หรืออวัยวะเพศไม่ทำงานในหญิงสูงอายุ และการให้เทสโทสเตอโรนรักษาหญิงวัยทองก็ใช้ได้ตราบที่ได้เอสโทรเจนไปด้วย[54]
ความสัมพันธ์กับคู่[แก้]
ความรักจะลดระดับเทสโทสเตอโรนในชายในขณะที่เพิ่มระดับในหญิง ซึ่งคาดว่า เป็นความเปลี่ยนแปลงชั่วคราวเพื่อลดความแตกต่างทางพฤติกรรมระหว่างเพศ[33] แต่ว่า ก็มีการเสนอว่า หลังจากระยะฮันนีมูนประมาณ 1-3 ปี ในความสัมพันธ์ ระดับเทสโทสเตอโรนที่เปลี่ยนไปจะกลับคืนสู่สภาพเดิม[33]
ชายที่ผลิตเทสโทสเตอโรนน้อยกว่า มีโอกาสมีความสัมพันธ์กับคู่รักสูงกว่า[55] และ/หรือแต่งงาน[56] และชายที่ผลิตเทสโทสเตอโรนมากกว่ามีโอกาสหย่าสูงกว่า[56] แต่ว่า อะไรเป็นเหตุยังไม่สามารถกำหนดได้จากค่าสหสัมพันธ์ที่ปรากฏเช่นนี้
การแต่งงานหรือความสัมพันธ์แบบผูกขาดสามารถลดระดับเทสโทสเตอโรนได้ด้วย[57] ชายโสดที่ไม่มีประสบการณ์ด้านความสัมพันธ์มีระดับเทสโทสเตอโรนที่ต่ำกว่าชายที่มีประสบการณ์แล้ว ซึ่งเสนอว่า ชายที่มีประสบการณ์จะมีสภาพการแข่งขันที่สูงกว่าผู้ไม่มีประสบการณ์[58]
ชายที่มีคู่แล้วที่ทำกิจรักษาความสัมพันธ์เช่นใช้เวลาร่วมกับคู่หรือกับลูก มีระดับเทสโทสเตอโรนที่ไม่แตกต่างจากเวลาที่ไม่ทำกิจกรรมเช่นนี้ รวม ๆ กันแล้ว ผลแสดงว่า การมีกิจกรรมที่ต้องแข่งขันกัน ไม่ใช่กิจกรรมรักษาความสัมพันธ์ ที่สัมพันธ์กับความเปลี่ยนแปลงของระดับเทสโทสเตอโรน[59]
ชายที่ผลิตเทสโทสเตอโรนมากกว่ามีโอกาสมีชู้มากกว่า[56] ระดับเทสโทสเตอโรนไม่ได้ขึ้นอยู่กับว่าคู่จะอยู่ใกล้ ๆ หรือไม่ (ไม่ว่าจะอยู่ในเมืองเดียวกันหรือต่างเมืองกัน) เพราะว่า ทั้งสองมีระดับเทสโทสเตอโรนไม่ต่างกัน[55] ส่วนในหญิง การมีคู่อยู่ใกล้ ๆ อาจจำเป็นในปฏิสัมพันธ์ระหว่างเทสโทสเตอโรน-คู่ คือ หญิงที่มีคู่อยู่ในเมืองเดียวกันมีระดับเทสโทสเตอโรนที่ต่ำกว่าหญิงที่มีคู่อยู่ต่างเมือง[60]
ความเป็นพ่อ[แก้]
ความเป็นพ่อยังลดระดับเทสโทสเตอโรนในชาย ซึ่งเแสดงว่าความเปลี่ยนแปลงทางอารมณ์และพฤติกรรมที่เกิดช่วยทำให้ดูแลลูก[61] เมื่อเด็กเป็นทุกข์ ความเปลี่ยนแปลงของระดับเทสโทสเตอโรนจะเป็นตัวบอกลักษณะของพ่อ ถ้าระดับลดลง พ่อจะเห็นใจลูกมากกว่าพ่อที่ระดับเพิ่ม[62]
พฤติกรรมและบุคลิกภาพ[แก้]
ระดับเทสโทสเตอโรนยังมีบทบาทสำคัญในการเสี่ยงเมื่อต้องตัดสินใจเรื่องการเงิน[63][64]
ความดุและพฤติกรรมอาชญากรรม[แก้]
งานศึกษาโดยมากสนับสนุนความสัมพันธ์ระหว่างพฤติกรรมอาชญากรรมกับระดับเทสโทสเตอโรน แม้ว่าความสัมพันธ์จะจำกัดถ้าตรวจสอบแต่ละเพศต่างหาก ๆ งานโดยมากพบว่า ระดับเทสโทสเตอโรนสัมพันธ์กับพฤติกรรมหรือลักษณะบุคลิกภาพที่สัมพันธ์กับอาชญากรรม เช่น พฤติกรรมต่อต้านสังคมและการติดเหล้า งานจำนวนมากตรวจสอบความสัมพันธ์ระหว่างพฤติกรรมหรือความรู้สึกดุเทียบกับเทสโทสเตอโรน โดยงานครึ่งหนึ่งพบว่า มีความสัมพันธ์ แต่อีกครึ่งก็ไม่พบ งานศึกษาเกือบทั้งหมดพบว่า พฤติกรรมอาชญากรรมของเด็กไม่สัมพันธ์กับระดับเทสโทสเตอโรน[65]
เทสโทสเตอโรนเป็นปัจจัยเพียงอย่างเดียวในหลาย ๆ ปัจจัยที่มีอิทธิพลต่อความดุ และประสบการณ์ในอดีตหรือสิ่งเร้าในสิ่งแวดล้อมก็มีค่าสหสัมพันธ์ที่มีกำลังกว่า งานศึกษา 2-3 งานพบว่า สารอนุพันธุ์ของเทสโทสเตอโรน คือ estradiol (ซึ่งเป็นเอสโทรเจนชนิดหนึ่ง) อาจมีบทบาทสำคัญในความดุของชาย[65][66][67][68] ยังมีงานศึกษาที่พบว่า เทสโทสเตอโรนอำนวยความดุโดยควบคุมตัวรับ vasopressin ในเขตสมองไฮโปทาลามัส[69]
ฮอร์โมนทางเพศบางกรณีอาจสนับสนุนให้ประพฤติอย่างยุติธรรม งานศึกษาปี 2553 ให้ผู้ร่วมการทดลองหญิงต่อรองแบ่งเงินที่มีจริง ๆ โดยเป็นเกมการทดลองทางเศรษฐศาสตร์ที่เรียกว่า Ultimatum (ข้อเสนอขาด) ที่ให้ฝ่ายหนึ่งเสนอแบ่งเงิน โดยทำได้ทั้งแบบยุติธรรมและไม่ยุติธรรมโดยเป็นข้อเสนอขาด ซึ่งอีกฝ่ายหนึ่งอาจจะยอมรับหรือปฏิเสธก็ได้ ยิ่งเสนอแบ่งให้ยุติธรรมเท่าไร ก็มีโอกาสน้อยลงที่อีกฝ่ายหนึ่งจะปฏิเสธเท่านั้น ถ้าอีกฝ่ายหนึ่งปฏิเสธข้อเสนอ ทั้งสองฝ่ายก็จะไม่ได้อะไร ผู้ร่วมการทดลองที่เสริมระดับเทสโทสเตอโรนให้สูงขึ้นโดยทั่วไปเสนอการแบ่งที่ดีกว่า ยุติธรรมกว่า ผู้ที่ได้ยาหลอก และดังนั้น ลดความเสี่ยงการถูกปฏิเสธจนน้อยที่สุด[70] งานศึกษาต่อมาที่ใช้เกมการทดลองอีกอย่างหนึ่ง (public goods game) ยืนยันผลเช่นนี้สำหรับหญิงในระดับหนึ่ง[71]
แต่งานปี 2552 ที่ศึกษาใช้เกมเดียวกันกลับพบว่า ชายที่มีเทสโทสเตอโรนสูงใจดีน้อยกว่า 27% และชายที่มีเทสโทสเตอโรนต่ำสุดใจดีกว่า 560%[72] งานวิจัยปี 2547 พบว่าวัยรุ่นที่ใช้สเตอรอยด์เพื่อสร้างกล้ามเนื้อ (anabolic steroid) ซึ่งเพิ่มระดับเทสโทสเตอโรน สัมพันธ์กับความรุนแรงที่เพิ่มขึ้น[73] งานศึกษาอื่นยังพบว่า การให้เทสโทสเตอโรนเพิ่มความก้าวร้าวทางคำพูดและความโกรธแก่ผู้ร่วมการทดลองบางคน[74]
เทสโทสเตอโรนมีสหสัมพันธ์อย่างสำคัญกับความดุและพฤติกรรมแข่งขัน โดยมีทฤษฎี 2 อย่างที่อธิบายเรื่องนี้[75]
ทฤษฎีแรกคือสมมติฐานการท้าทาย (challenge hypothesis) ซึ่งอ้างว่า เทสโทสเตอโรนจะเพิ่มขึ้นในวัยเริ่มเจริญพันธุ์ เพื่ออำนวยพฤติกรรมการสืบพันธุ์และการแข่งขัน ซึ่งรวมความดุด้วย[75] ดังนั้น จึงเป็นการแข่งขันท้าทายในสัตว์ตัวผู้ที่อำนวยให้เกิดความดุและความรุนแรง[75] งานศึกษายังพบสหสัมพันธ์โดยตรงระหว่างระดับเทสโทสเตอโรนกับสถานะทางสังคม โดยเฉพาะในกลุ่มอาชญากรรุนแรงที่สุดในคุกผู้มีระดับเทสโทสเตอโรนสูงสุด[75] งานเดียวกันยังพบว่า พ่อ (ที่ไม่อยู่ในการแข่งขันแล้ว) มีระดับเทสโทสเตอโรนต่ำสุดเทียบกับชายอื่น ๆ[75]
ทฤษฎีที่สอง คือ "evolutionary neuroandrogenic (ENA) theory of male aggression"[76][77] อ้างว่า เทสโทสเตอโรนและฮอร์โมนแอนโดรเจนอื่น ๆ มีวิวัฒนาการเพื่อสร้างบุรุษภาพในสมองเพื่อให้มีลักษณะช่างแข่งขัน แม้ถึงกระทั่งเสี่ยงความบาดเจ็บต่อตนเองและผู้อื่น ดังนั้น บุคคลที่มีภาวะสมองเช่นนั้นโดยเป็นผลของระดับเทสโทสเตอโรนและแอนโดรเจนทั้งก่อนคลอดและเมื่อเป็นผู้ใหญ่ จะสามารถหาทรัพยากรได้เพิ่มขึ้น และดึงดูดความสนใจและผสมพันธุ์กับคู่ให้มากที่สุดเท่าที่จะเป็นไปได้[76] การปรับสภาพสมองเช่นนี้ไม่ใช่อำนวยโดยระดับเทสโทสเตอโรนเมื่อเป็นผู้ใหญ่เท่านั้น แต่รวมการได้รับเทสโทสเตอโรนเมื่อเป็นทารกในครรภ์ด้วย
ระดับเทสโทสเตอโรนที่ได้ก่อนคลอดซึ่งระบุโดยอัตราส่วนความยาวระหว่างนิ้วชี้กับนิ้วนางที่ต่ำ และที่ได้เมื่อเป็นผู้ใหญ่ เพิ่มความเสี่ยงการทำฟาวล์หรือมีพฤติกรรมดุสำหรับนักฟุตบอลชาย[78] ยังมีงานศึกษาอื่นอีกที่พบว่าการได้เทสโทสเตอโรนระดับสูง หรือมีอัตราส่วนความยาวนิ้วที่น้อยกว่า มีสหสัมพันธ์กับความดุมากกว่าในชาย[79][80][81][82][83]
ระดับเทสโทสเตอโรนที่สูงขึ้นในการแข่งขันเป็นตัวพยากรณ์ความดุในชาย แต่ไม่เป็นในหญิง[84] ผู้ร่วมการทดลองที่มีปฏิสัมพันธ์กับปืนสั้นและเกมทดลองอย่างหนึ่ง มีระดับเทสโทสเตอโรนและความดุที่สูงขึ้น[85] การคัดเลือกโดยธรรมชาติอาจวิวัฒนาการให้ชายไวต่อสถานการณ์แข่งขันหรือที่ท้าทายสถานะทางสังคมมากกว่า และการทำงานของเทสโทสเตอโรนเป็นองค์ประกอบสำคัญในพฤติกรรมดุในสถานการณ์เหล่านั้น[86]
เทสโทสเตอโรนทำให้ดุโดยออกฤทธิ์ให้เขตใต้เปลือกสมอง (subcortical) ทำงาน ซึ่งอาจจะมีการยับยั้งภายใต้สถานการณ์ทางสังคมหรือทางครอบครัว และปรากฏในระดับต่าง ๆ ผ่านความคิด ความโกรธ ความดุร้ายทางวาจา การแข่งขัน การแข่งสถานะทางสังคม และความรุนแรงทางกาย[87] เทสโทสเตอโรนอำนวยให้ใส่ใจในเรื่องโหดร้ายและรุนแรง เช่น สนับสนุนให้ดูสิ่งเร้าที่รุนแรงนานขึ้น[88] ลักษณะปรากฏ (phenotype) ในโครงสร้างสมองที่เกี่ยวกับเทสโทสเตอโรนโดยเฉพาะ สามารถพยากรณ์พฤติกรรมดุในบุคคลตั้งแต่เด็กจนถึงผู้ใหญ่[89]
estradiol มีสหสัมพันธ์กับความดุของหนูหริ่งตัวผู้[90] นอกจากนั้นแล้ว การเปลี่ยนเทสโทสเตอโรนไปเป็น estradiol ยังควบคุมความดุของนกกระจอกตัวผู้ในฤดูผสมพันธุ์[91] หนูที่ได้สเตอรอย์อะนาบอลิค (anabolic) ซึ่งเพิ่มระดับเทสโทสเตอโรนยังดุมากกว่าเมื่อล่อ เพราะ "ไวต่อการคุกคาม"[92]
สมอง[แก้]
การแบ่งเพศมีผลต่อสมองด้วย[13] เพราะว่า เอนไซม์ aromatase จะเปลี่ยนเทสโทสเตอโรนเป็น estradiol ซึ่งมีหน้าที่สร้างบุรุษภาพในสมองของหนูหริ่งตัวผู้ ในมนุษย์ การสร้างบุรุษภาพต่อสมองของทารกสัมพันธ์กับการมีตัวรับแอนโดรเจนที่ใช้งานได้ ตามงานศึกษาที่สังเกตความชอบใจทางเพศของคนไข้ที่ผิดปกติแต่กำเนิดในด้านการสร้างแอนโดรเจนหรือด้านการทำงานของตัวรับแอนโดรเจน[93]
สมองของชายไม่เหมือนหญิง (อาจเพราะมีระดับเทสโทสเตอโรนที่ต่างกัน) อย่างหนึ่งก็คือขนาด คือสมองของชายโดยเฉลี่ยจะใหญ่กว่า[94] ชายปรากฏว่ามีใยประสาทที่มีปลอกหุ้มยาวถึง 176,000 กม. เมื่ออายุ 20 ปี เทียบกับของหญิงที่ยาว 149,000 กม. (น้อยกว่าประมาณ 15%)[95]
การให้เทสโทสเตอโรนในขนาดที่มากกว่าร่างกายผลิต ไม่มีผลระยะสั้นโดยตรงต่อพื้นอารมณ์หรือพฤติกรรม ของชายที่สุขภาพดี 43 คนเป็นเวลา 10 อาทิตย์[96] ระดับเทสโทสเตอโรนมีสหสัมพันธ์กับความกล้าเสี่ยงในการเลือกอาชีพของผู้หญิง[63][97]
ความใส่ใจ ความจำ และสมรรถภาพด้านพื้นที่และทิศทาง (spatial ability) เป็นหน้าที่ทางการรู้คิดที่สำคัญที่เทสโทสเตอโรนมีอิทธิพลในมนุษย์ หลักฐานเบื้องต้นแสดงว่า ระดับเทสโทสเตอโรนที่ต่ำอาจเป็นปัจจัยเสี่ยงต่อความเสื่อมการรู้คิด และในที่สุดต่อภาวะสมองเสื่อมคล้ายกับโรคอัลไซเมอร์[98][99][100][101] ซึ่งเป็นหลักฐานหลักในการแพทย์ยืดชีวิต ที่จะใช้เทสโทสเตอโรนเพื่อชะลออายุ หลักฐานโดยมากแสดงว่า มีความสัมพันธ์ระหว่างสมรรถภาพในเรื่องพื้นที่/ทิศทางกับระดับเทสโทสเตอโรนที่เวียนอยู่ในเลือด โดยเป็นฟังก์ชันเส้นโค้งหรือกำลังสอง[102] ที่การผลิตแอนโดรเจนทั้งเกินหรือขาด มีผลลบต่อระบบการรู้คิด

ชีวเคมี[แก้]
ชีวสังเคราะห์[แก้]
เหมือนกับฮอร์โมนแบบสเตอรอยด์อื่น ๆ เทสโทสเตอโรนสังเคราะห์มาจากคอเลสเตอรอล (ดูรูป)[104] ขั้นแรกในกระบวนการชีวสังเคราะห์ก็คือการแยก (ผ่านกระบวนการออกซิเดชัน) โซ่ข้างคอเลสเตอรอลด้วย cholesterol side-chain cleavage enzyme (P450scc, CYP11A1) ซึ่งเป็นเอนไซม์ cytochrome P450 oxidase ของไมโทคอนเดรีย โดยคอเลสเตอรอลจะเสียอะตอมคาร์บอน 6 อะตอมกลายเป็น pregnenolone ขั้นต่อไป เอนไซม์ CYP17A1 (17α-hydroxylase/17,20-lyase) ในร่างแหเอนโดพลาซึมจะดึงเอาคาร์บอนอีก 2 อะตอมออก กลายเป็นสเตอรอยด์แบบ C19 หลายอย่าง[105] ต่อจากนั้น เอนไซม์ 3β-hydroxysteroid dehydrogenase จะเป็นตัวออกซิไดส์เปลี่ยนกลุ่ม 3β-hydroxyl ให้เป็น androstenedione และในขั้นสุดท้ายที่เป็นตัวจำกัดอัตราการเปลี่ยน เอนไซม์ 17β-hydroxysteroid dehydrogenase จะเป็นตัวรีดิวซ์ androstenedione ซึ่งอยู่ในกลุ่ม C17 keto ให้เป็นเทสโทสเตอโรน
ในชาย เทสโทสเตอโรนโดยมาก (>95%) จะผลิตในอัณฑะ[2] และต่อมหมวกไตผลิตที่เหลือโดยมาก ในหญิงซึ่งผลิตน้อยกว่ามาก เทสโทสเตอโรนจะสังเคราะห์โดยต่อมหมวกไต, thecal cells ของรังไข่, และรกระหว่างการตั้งครรภ์[106]
ส่วน Leydig cell ในอัณฑะเป็นตัวผลิตฮอร์โมนโดยเฉพาะ[107] อ้ณฑะยังมี Sertoli cell ที่จำเป็นต้องได้เทสโทสเตอโรนเพื่อการสร้างสเปิร์ม เหมือนกับฮอร์โมนโดยมาก เทสโทสเตอโรนจะส่งไปที่ที่ต้องการผ่านเลือด และส่งโดยยึดกับโปรตีนโดยเฉพาะในเลือด คือ sex hormone-binding globulin (SHBG)

การควบคุม[แก้]
ในชาย เทสโทสเตอโรนโดยมากสังเคราะห์ใน Leydig cell ซึ่งจำนวนของเซลล์จะควบคุมโดยฮอร์โมน (ดูรูป) luteinizing hormone (LH) และ follicle-stimulating hormone (FSH) นอกจากนั้นแล้ว ปริมาณเทสโทสเตอโรนที่ Leydig cell ผลิตจะอยู่ใต้การควบคุมของ LH ซึ่งควบคุมการแสดงออกของยีน 17β-hydroxysteroid dehydrogenase[108]
ส่วนปริมาณเทสโทสเตอโรนที่ผลิตจะควบคุมโดย hypothalamic-pituitary-testicular axis (ดูรูป)[109] คือ เมื่อระดับเทสโทสเตอโรนต่ำ ไฮโปทาลามัสจะหลั่งฮอร์โมน gonadotropin-releasing hormone (GnRH) ซึ่งจกระตุ้นต่อมใต้สมองให้หลั่ง FSH และ LH ซึ่งก็จะกระตุ้นให้อัณฑะสังเคราะห์เทสโทสเตอโรน และในที่สุด ระดับเทสโทสเตอโรนที่สูงขึ้นก็จะเป็นวงวนป้อนกลับแบบลบที่ออกฤทธิ์ให้ไฮโปทาลามัสและต่อมใต้สมองยับยั้งการหลั่ง GnRH แล้วก็ FSH/LH ตามลำดับ
ปัจจัยที่มีผลต่อระดับเทสโทสเตอโรนอาจรวมทั้ง
- อายุ - ระดับเทสโทสเตอโรนของชายจะค่อย ๆ ลดลงเมื่ออายุมากขึ้น[110][111] ปรากฏการณ์นี้บางครั้งเรียกว่า andropause (วัยทอง) หรืออวัยวะเพศทำงานน้อยเกินตั้งต้นเมื่อปลายชีวิต (late-onset hypogonadism)[112]
- การออกกำลังกาย ที่เพิ่มความแข็งแรงและกล้ามเนื้อ (Resistance training) จะเพิ่มระดับเทสโทสเตอโรน[113] แต่ว่า ในชายสูงอายุ ภาวะเช่นนี้สามารถหลีกเลี่ยงโดยการบริโภคโปรตีน[114] ส่วนการออกกำลังกายที่ทำให้อึด (Endurance training) อาจทำให้ระดับเทสโทสเตอโรนลดลง[115]
- สารอาหาร - การขาดวิตามินเออาจทำให้ระดับเทสโทสเตอโรนลดลงในเลือด[116] และการทานวิตามินดี (ซึ่งเป็น secosteroid) ในระดับ 400-1,000 IU/วัน (10-25 µg/วัน) จะเพิ่มระดับเทสโทสเตอโรน[117] การขาดธาตุสังกะสีจะลดระดับเทสโทสเตอโรน[118] แต่การทานเกินจะไม่มีผลต่อระดับเทสโทสเตอโรน[119]
- น้ำหนักลด อาจทำให้ระดับเทสโทสเตอโรนเพิ่มขึ้น เพราะเซลล์ไขมัน (Fat cell) จะสังเคราะห์เอนไซม์ aromatase ซึ่งเปลี่ยนเทสโทสเตอโรน (ฮอร์โมนเพศชาย) เป็น estradiol (ฮอร์โมนเพศหญิง)[120] แต่ว่า ก็ไม่มีความสัมพันธ์ที่ชัดเจนระหว่างดัชนีมวลกายกับระดับเทสโทสเตอโรน[121]
- การนอนหลับ - การหลับระยะตาเคลื่อนไหวอย่างรวดเร็ว (REM sleep) จะเพิ่มระดับเทสโทสเตอโรนตอนกลางคืน[122]
- พฤติกรรม - การแข่งขันทางสังคมในบางกรณีจะกระตุ้นให้ชายหลั่งเทสโทสเตอโรน[123]
- ยา - ยาต้านแอนโดรเจนทั้งแบบธรรมชาติและสังเคราะห์ เช่นชาที่ทำจากมินต์พันธุ์ Mentha spicata จะลดระดับเทสโทสเตอโรน[124][125][126] ชะเอมเทศสามารถลดการผลิตเทสโทสเตอโรนโดยมีผลมากกว่าในหญิง[127]
การกระจายตัว[แก้]
ในเลือด เทสโทสเตอโรน 98% จะยึดอยู่กับโปรตีน โดย 65% ยึดกับ sex hormone-binding globulin (SHBG) และ 33% ยึดอย่างอ่อน ๆ กับ human serum albumin[128] ระดับเทสโทสเตอโรนของชายผู้ใหญ่ (ที่เป็นอิสระหรือยึด) จะอยู่ที่ 10.4-24.3 nmol/L[ต้องการอ้างอิง] เทียบกับในหญิงที่ 30-70 ng/dL
เมแทบอลิซึม[แก้]
ทั้งเทสโทสเตอโรน และ 5α-DHT (Dihydrotestosterone) จะมีเมแทบอลิซึมโดยหลักในตับ[1][129] เทสโทสเตอโรนประมาณ 50% จะมีเมแทบอลิซึมแบบสังยุค (conjugation) ผ่านเอนไซม์ glucuronosyltransferase เป็น testosterone glucuronide และผ่าน sulfotransferase เป็น testosterone sulfate แม้ในระดับที่น้อยกว่า[1] เทสโทสเตอโรนอีก 40% จะผ่านเมแทบอลิซึมกับเอนไซม์ 5α-reductase, 5β-reductase, 3α-hydroxysteroid dehydrogenase และ 17β-HSD ตามลำดับกลายเป็น 17-ketosteroid คือ androsterone และ etiocholanolone ประมาณเท่า ๆ กัน[1][129][130] ซึ่งทั้งสองก็จะผ่านกระบวนการ glucuronidation และ (แม้จะน้อยกว่า) sulfation คล้ายกับของเทสโทสเตอโรน (ที่เรียกรวม ๆ ว่า กระบวนการ conjugation) ต่อไป[1][129]
เทสโทสเตอโรนสังยุคและเมทาบอไลต์ก็จะหลั่งออกจากตับเข้าสู่ระบบหัวใจหลอดเลือด แล้วขับออกทางปัสสาวะและน้ำดี[1][129][130] มีเทสโทสเตอโรนแค่ 2% ที่ขับออกทางปัสสาวะโดยไม่เปลี่ยนแปลง[129]
ในวิถีเมแทบอลิซึมของ 17-ketosteroid ในตับ เทสโทสเตอโรนจะเปลี่ยนด้วย 5α-reductase และ 5β-reductase เป็น Dihydrotestosterone คือ 5α-DHT และ 5β-DHT ที่ไม่มีฤทธิ์ตามลำดับ[1][129] แล้ว 3α-HSD ก็จะเปลี่ยน 5α-DHT และ 5β-DHT ไปเป็น 3α,5α-androstanediol และ 3α,5β-androstanediol ตามลำดับ[1][129] ต่อจากนั้น 17β-HSD ก็จะเปลี่ยน 3α,5α-androstanediol และ 3α,5β-androstanediol เป็น androsterone และ etiocholanolone ซึ่งก็จะผ่านกระบวนการ conjugation เป็นต้นเหมือนกับที่กล่าวด้านบน และขับออกจากร่างกาย[1][129]
3β,5α-Androstanediol (epiandrosterone) และ 3β,5β-androstanediol (epietiocholanolone) ก็สามารถเกิดในวิถีเมแทบอลิซึมนี้ด้วยเมื่อ 3β-HSD (แทน 3α-HSD) ออกฤทธิ์ต่อ 5α-DHT และ 5β-DHT แล้วเปลี่ยนเป็น epiandrosterone และ epietiocholanolone ตามลำดับ[131][132]
เทสโทสเตอโรนประมาณ 3% ในตับจะเปลี่ยนด้วย 17β-HSD ไปเป็น 4-androstenedione อย่างผันกลับได้[130]
นอกจากกระบวนการ conjugation และ วิถีเมแทบอลิซึม 17-ketosteroid แล้ว เทสโทสเตอโรนยังสามารถผ่านกระบวนการ hydroxylation และ oxidation โดยใช้เอนไซม์ cytochrome P450 ในตับ รวมทั้ง CYP3A4, CYP3A5, CYP2C9, CYP2C19, และ CYP2D6[133] โดยมี 6β-Hydroxylation และ (แม้น้อยกว่า) 16β-hydroxylation เป็นกระบวนการเปลี่ยนรูปหลัก[133] กระบวนการ 6β-hydroxylation ของเทสโทสเตอโรนมีเอนไซม์หลักเป็น CYP3A4 และ (แม้น้อยกว่า) CYP3A5 โดยเป็นกระบวนการเมแทบอลิซึมของเทสโทสเตอโรนในระบบ cytochrome P450 ถึง 75-80%[133]
นอกเหนือไปจาก 6β-hydroxytestosterone และ 16β-hydroxytestosterone เมแทบอไลต์ย่อยอื่น ๆ ที่ได้รวมทั้ง 1β-hydroxytestosterone, 2α/β-hydroxytestosterone, 11β-hydroxytestosterone, และ 15β-hydroxytestosterone[133][134] เอนไซม์ cytochrome P450 บางอย่างเช่น CYP2C9 และ CYP2C19 ยังสามารถเติมออกซิเจนให้กับเทสโทสเตอโรนที่ตำแหน่ง C17 เพื่อสร้าง androstenedione[133] เมแทบอไลต์โดยตรงจากเทสโทสเตอโรน คือ 5α-DHT และ estradiol มีฤทธิ์สำคัญทางชีวภาพ และสามารถสร้างทั้งในตับและนอกตับ[129]
5α-reductase จะเปลี่ยนเทสโทสเตอโรนประมาณ 5-7% ไปเป็น 5α-DHT โดยมีความเข้มข้นในเลือดที่ 10% ของเทสโทสเตอโรน และ aromatase จะเปลี่ยนเทสโทสเตอโรนประมาณ 0.3% เป็น estradiol[2][129][135][136] 5α-Reductase มีการแสดงออกมากในระบบสืบพันธุ์ของชาย รวมทั้งที่ต่อมลูกหมาก ถุงพักน้ำอสุจิ (seminal vesicle) และที่หลอดเก็บอสุจิ (epididymides)[137] ตลอดจนถึงผิวหนัง ปุ่มรากผม (hair follicle) และสมอง[138] ส่วน aromatase จะแสดงออกมากในเซลล์ไขมัน กระดูก และสมอง[139][140]
เทสโทสเตอโรนถึง 90% เปลี่ยนเป็น 5α-DHT ในเนื้อเยื่อ "androgenic" ที่มีระดับการแสดงออกของ 5α-reductase สูง[130] และเนื่องจาก 5α-DHT เป็นตัวทำการของตัวรับแอนโดรเจน (AR agonist) ที่มีฤทธิ์แรงกว่าเทสโทสเตอโรนเป็นหลายเท่า[141] จึงมีการประเมินว่า ผลของเทสโทสเตอโรนจะขยายเป็น 2-3 เท่าในเนื้อเยื่อเช่นนี้[142]
กลไกการออกฤทธิ์[แก้]
เทสโทสเตอโรนในมนุษย์และสัตว์มีกระดูกสันหลังอื่น ๆ ออกฤทธิ์ผ่านกลไกหลายอย่าง คือ ออกฤทธิ์ต่อตัวรับแอนโดรเจน (androgen receptor ตัวย่อ AR โดยตรงหรือโดยเป็น DHT) ซึ่งเป็นตัวรับในนิวเคลียส (nuclear receptor) และการแปรเป็น estradiol แล้วออกฤทธิ์ต่อตัวรับเอสโทรเจนบางอย่างทั้งในนิวเคลียสและบนเยื่อหุ้มเซลล์[143][144] แอนโดรเจนเช่นเทสโทสเตอโรนยังยึดและออกฤทธิ์ต่อ membrane androgen receptor ซึ่งเป็นตัวรับที่เยื่อหุ้มเซลล์ อีกด้วย[145][146][147]
เทสโทสเตอโรนที่เป็นอิสระ (T) จะส่งเข้าไปยังไซโทพลาซึมของเซลล์เป้าหมาย ที่มันสามารถเข้ายึดกับ AR แล้วรีดิวซ์เป็น 5α-dihydrotestosterone (DHT) โดยเอนไซม์ในไซโทพลาสซึมคือ 5α-reductase และเพราะ DHT จะเข้ายึดกับ AR เดียวกันแรงยิ่งกว่าเทสโทสเตอโรน ดังนั้น จึงมีฤทธิ์ทางแอนโดรเจนมากกว่าถึง 5 เท่า ของ T[148] ตัวรับเทสโทสเตอโรนหรือคอมเพล็กซ์รับ DHT จะเปลี่ยนรูป ทำให้มันสามารถเข้าไปในนิวเคลียสของเซลล์ และเข้ายึดกับลำดับนิวคลีโอไทด์โดยเฉพาะ ๆ บนโครโมโซมของดีเอ็นเอ จุดที่เข้ายึดเรียกว่า hormone response element (HREs) และมีอิทธิพลต่อการถอดรหัสยีนบางอย่าง ซึ่งเป็นผลที่ปรากฏของแอนโดรเจน
AR เกิดในระบบต่าง ๆ มากมายในร่างกายของสัตว์มีกระดูกสันหลัง และทั้งชายหญิงตอบสนองเช่นเดียวกันที่ฮอร์โมนระดับเดียวกัน ปริมาณเทสโทสเตอโรนที่ต่าง ๆ กันมากในช่วงก่อนคลอด ช่วงวัยเริ่มเจริญพันธุ์ และตลอดชีวิต สามารถอธิบายความแตกต่างระหว่างเพศของหญิงชาย กระดูกและสมองเป็นเนื้อเยื่อสำคัญสองอย่างในมนุษย์ที่ผลหลักของเทสโทสเตอโรนจะเกิดผ่านกระบวนการ aromatization แล้วเปลี่ยนเป็น estradiol โดยในกระดูก estradiol จะเร่งให้กระดูกอ่อนเปลี่ยนเป็นกระดูกแข็ง ทำให้ epiphysis ปิดและถึงจุดอวสานของการเจริญเติบโตของกระดูก
ในระบบประสาทกลาง เทสโทสเตอโรนก็จะผ่านกระบวนการ aromatization แล้วเปลี่ยนเป็น estradiol เหมือนกัน ซึ่ง (ไม่ใช่เทสโทสเตอโรน) ทำหน้าที่เป็นสัญญาณป้อนกลับที่สำคัญที่สุดต่อไฮโปทาลามัส (โดยเฉพาะในการหลั่งฮอร์โมน luteinizing hormone)[149] ในสัตว์เลี้ยงลูกด้วยนมมากมาย เอสโทรเจนที่ทำจากเทสโทสเตอโรนจะเป็นตัวทำบุรุษภาพของส่วนสมองที่ต่างกันระหว่างเพศ ทั้งในช่วงก่อนคลอดและใกล้ ๆ คลอด จึงเป็นตัวกำหนดพฤติกรรมทางเพศของชายต่อมา[150]
ทางการแพทย์[แก้]
แพทย์ใช้เทสโทสเตอโรนเป็นยารักษาชายที่ผลิตเทสโทสเตอโรนน้อยเกินไปหรือไม่ผลิตเลย และโรคมะเร็งเต้านมบางอย่าง[5] ซึ่งเรียกว่า hormone replacement therapy (HRT) หรือ testosterone replacement therapy (TRT) และธำรงระดับเทสโทสเตอโรนในเลือดให้อยู่ในพิสัยปกติ ส่วนปัญหาการผลิตเทสโทสเตอโรนที่น้อยลงตามอายุทำให้เกิดความสนใจใน androgen replacement therapy (การบำบัดโดยการแทนที่แอนโดรเจน)[151] แต่ก็ยังไม่ชัดเจนว่า การใช้เทสโทสเตอโรนในระดับต่ำเนื่องจากอายุจะมีผลดีหรือผลเสีย[152]
เทสโทสเตอโรนอยู่ในรายการยาที่จำเป็นขององค์การอนามัยโลก ซึ่งเป็นยาที่สำคัญที่สุดในระบบสาธารณสุขพื้นฐาน[153] เป็นยาที่ผลิตได้ทั่วไปโดยไม่มีสิทธิบัตร[5] โดยราคาจะขึ้นอยู่กับรูปแบบของยา[154] ซึ่งสามารถใช้เป็นครีมทา แผ่นแปะผิวหนัง ฉีดเข้าในกล้ามเนื้อ ยาทาที่แก้ม หรือยาทาน[5] ผลข้างเคียงสามัญของเทสโทสเตอโรนรวมทั้งมีสิว บวม และเต้านมโตในชาย[5]
ผลข้างเคียงรุนแรงที่อาจมีรวมการเป็นพิษต่อตับ โรคหัวใจ และความเปลี่ยนแปลงทางพฤติกรรม[5] หญิงหรือเด็กที่ได้ยา (โดยตั้งใจหรือบังเอิญ) อาจเกิดบุรุษภาพ[5] ไม่แนะนำให้บุคคลที่มีมะเร็งต่อมลูกหมากใช้ยา[5] และยาอาจมีผลเสียในช่วงการตั้งครรภ์หรือการให้นมลูก[5]
สัตว์อื่น ๆ[แก้]
สัตว์มีกระดูกสันหลังโดยมากมีเทสโทสเตอโรน เทสโทสเตอโรนและตัวรับแอนโดรเจนซึ่งอยู่ในนิวเคลียสของเซลล์ปรากฏเริ่มแรกในสัตว์มีกระดูกสันหลังมีขากรรไกใน Infraphylum คือ "Gnathostomata" (jawed vertebrates)[155] ส่วนสัตว์มีกระดูกสันหลังไม่มีขากรรไก (Agnathan) เช่น ปลาแลมป์เพรย์ทะเลไม่ผลิตเทสโทสเตอโรน แต่ใช้ 4-androstenedione เป็นฮอร์โมนเพศชาย[156]
ส่วนปลาผลิตฮอร์โมนที่ต่างกันเล็กน้อยที่เรียกว่า 11-ketotestosterone[157] ส่วนสิ่งที่คล้ายกันในแมลงก็คือ ecdysone[158]
การมีสเตอรอยด์ดาษดื่นอย่างนี้ในสัตว์ต่าง ๆ แสดงว่า ฮอร์โมนเพศมีประวัติทางวิวัฒนาการที่ยาวนาน[159]

ประวัติ[แก้]
องค์ประกอบในเลือดได้ปรากฏว่ามีฤทธิ์ต่อการทำงานของอัณฑะ เป็นองค์ประกอบที่ปัจจุบันเข้าใจว่าเป็นกลุ่มฮอร์โมนเพศชาย (androgenic hormone) เนื่องจากงานเกี่ยวกับการตอนและการปลูกถ่ายอัณฑะในเป็ดไก่ของ นพ. Arnold Adolph Berthold (พ.ศ. 2346-2404)[160] งานเกี่ยวกับฤทธิ์ของเทสโทสเตอโรนได้แรงสนับสนุนในปี 2432 เมื่อศาสตราจารย์แห่งมหาวิทยาลัยฮาร์วาร์ด Charles-Édouard Brown-Séquard (พ.ศ. 2360-2437) ฉีดตัวเองใต้ผิวหนังด้วย "ยาอายุวัฒนะ" (rejuvenating elixir) ซึ่งกลั่นมาจากอัณฑะของสุนัขและหนูตะเภา เขารายงานในวารสารการแพทย์ The Lancet ว่า เขากลับรู้สึกกระฉับกระเฉงและอยู่เป็นสุขอีก แต่ว่าผลอยู่เพียงชั่วคราว[161] ดังนั้น ความหวังของเขากับยาที่ว่าจึงหมดไป เมื่อถูกเยาะเย้ยโดยเพื่อนร่วมอาชีพ เขาจึงทิ้งงานในเรื่องกลไกและผลของแอนโดรเจนในมนุษย์
ในปี 2470 ศาสตราจารย์แผนกเคมีทางสรีรภาพแห่งมหาวิทยาลัยชิคาโก Fred C. Koch ได้แหล่งอัณฑะวัวแหล่งใหญ่ คือ คอกปศุสัตว์แห่งชิคาโก แล้วรับสมัครนักเรียนที่สามารถอดทนทำงานที่น่าเบื่อในการสกัดสารจากมัน ในปีนั้น ศ. กับนักศึกษาคนหนึ่งคือ Lemuel McGee สกัดสาร 20 มก. จากอัณฑะวัวรวมกันหนัก 40 ปอนด์ ที่เมื่อฉีดให้กับไก่แจ้ หมู และหนูที่ถูกตอน กลับสร้างบุรุษภาพในพวกมันอีก[162] มีอีกกลุ่มหนึ่งที่มหาวิทยาลัยอัมสเตอร์ดัมที่สกัดเทสโทสเตอโรนที่บริสุทธิ์ขึ้นจากอัณฑะวัวโดยวิธีคล้าย ๆ กันในปี 2477 แต่ว่า การสกัดฮอร์โมนจากเนื้อเยื่อสัตว์ที่มีขนาดพอจะศึกษาในมนุษย์ ก็เป็นไปไม่ได้จนกระทั่งบริษัทยายักษ์ในยุโรป คือ เชริ่ง (เบอร์ลิน ประเทศเยอรมนี) Organon (Oss ประเทศเนเธอร์แลนด์) และ Ciba (ปัจจุบันโนวาร์ติส, บาเซิล ประเทศสวิตเซอร์แลนด์) เริ่มโปรแกรมการวิจัยและพัฒนาสเตอรอยด์อย่างเต็มพิกัดในคริสต์ทศวรรษ 1930
กลุ่มนักวิจัยในบริษัท Organon เป็นพวกแรกที่สกัดฮอร์โมนได้โดยเฉพาะ ซึ่งเรียกในสิ่งตีพิมพ์เดือนพฤษภาคม 2478 มีชื่อเรื่องว่า On Crystalline Male Hormone from Testicles (Testosterone) [เกี่ยวกับฮอร์โมนเพศชายแบบผลึกจากอัณฑะ (เทสโทสเตอโรน)][163] โดยตั้งชื่อฮอร์โมนว่า "เทสโทสเตอโรน" จากรากศัพท์ของคำว่า testicle (อัณฑะ) กับ sterol และจากคำต่อท้ายของคำว่า คีโทน ส่วนโครงสร้างของฮอร์โมนเป็นผลงานของ ศ. ดร. อดอล์ฟ บูเทนันต์ แห่ง Gdańsk University of Technology ในเมืองกดัญสก์ ประเทศโปแลนด์ โดยได้รับอุปถัมภ์จาก บ. เชริ่ง[164][165]
การสังเคราะห์เทสโทสเตอโรนทางเคมีจากคอเลสเตอรอล ก็เริ่มทำได้ในปีเดียวกันเดือนสิงหาคมโดย ศ. บูเทนันต์ และเพื่อนร่วมงาน[166] ต่อมาอีกอาทิตย์เดียว กลุ่มของ Ciba นำโดย ศ. ดร. เลโอโปลด์ รูซิคกา (พ.ศ. 2430-2519) และเพื่อนร่วมงาน ก็พิมพ์ผลงานถึงวิธีการสังเคราะห์เทสโทสเตอโรนของตน[167] ต่อมาปี 2482 ศ. บูเทนันต์ และ ศ.รูซิคกา ร่วมรับรางวัลโนเบลสาขาเคมี สำหรับวิธีการสังเคราะห์เทสโทสเตอโรนที่ทำสำเร็จต่างหาก ๆ เริ่มจากคอเลสเตอรอล[165][168]
ต่อมา จึงมีการระบุเทสโทสเตอโรนว่าเป็น 17β-hydroxyandrost-4-en-3-one (C19H28O2) คือเป็นแอลกอฮอล์แบบ solid polycyclic โดยมีกลุ่มไฮดรอกซิลที่คาร์บอนตำแหน่งที่ 17 จึงชัดเจนว่า สามารถแต่งเติมเทสโทสเตอโรนสังเคราะห์โดยวิธีการต่าง ๆ เช่น esterification (ปฏิกิริยาระหว่างแอลกอฮอล์กับกรดกลายเป็นเอสเทอร์) และ alkylation (การย้ายกลุ่ม alkyl จากโมเลกุลหนึ่งไปยังอีกโมเลกุลหนึ่ง) การสังเคราะห์เอสเทอร์ต่าง ๆ ของเทสโทสเตอโรนที่มีฤทธิ์เป็นปริมาณมาก ๆ ในช่วงคริสต์ทศวรรษ 1930 ทำให้สามารถกำหนดผลของฮอร์โมน โดยงานวิจัยในสุนัขปี 2479 แสดงว่า เทสโทสเตอโรนยกระดับการคงไนโตรเจน (nitrogen retention) ไว้ได้ ซึ่งเป็นกลไกสำคัญของแอแนบอลิซึม ส่วนงานวิจัยปี 2483 ได้แสดงผลทั้ง anabolic และ androgenic ของ testosterone propionate ต่อชายบัณเฑาะก์ เด็กผู้ชาย และหญิง[169]
ดังนั้นระยะช่วงต้นคริสต์ทศวรรษ 1930 จนถึงทศวรรษ 1950 จึงเรียกว่า "ยุคทองของเคมีสเตอรอยด์"[170] และเกิดผลงานมากมายในช่วงนี้ งานวิจัยในช่วงนี้พิสูจน์ว่า สารประกอบที่สังเคราะห์ขึ้นได้ใหม่นี้ (เทสโทสเตอโรน) หรือกลุ่มสารประกอบ (เพราะมีสารอนุพันธ์มากมายที่พัฒนาขึ้นในช่วงคริสต์ทศวรรษ 1940-1960) มีฤทธิ์แรงในการสร้างกล้ามเนื้อ ความแข็งแรง และความรู้สึกอยู่เป็นสุข[171]
ดูเพิ่ม[แก้]
เชิงอรรถและอ้างอิง[แก้]
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 1.8 Melmed, Shlomo; Polonsky, Kenneth S.; Larsen, P. Reed; Kronenberg, Henry M. (30 November 2015). Williams Textbook of Endocrinology. Elsevier Health Sciences. pp. 711-. ISBN 978-0-323-29738-7.
- ↑ 2.0 2.1 2.2 Mooradian AD, Morley JE, Korenman SG (Feb 1987). "Biological actions of androgens". Endocrine Reviews. 8 (1): 1–28. doi:10.1210/edrv-8-1-1. PMID 3549275.
- ↑ Bassil N, Alkaade S, Morley JE (Jun 2009). "The benefits and risks of testosterone replacement therapy: a review". Therapeutics and Clinical Risk Management. 5 (3): 427–48. doi:10.2147/tcrm.s3025. PMC 2701485. PMID 19707253.
- ↑ Tuck SP, Francis RM (2009). "Testosterone, bone and osteoporosis". Advances in the Management of Testosterone Deficiency. Frontiers of Hormone Research. Vol. 37. pp. 123–32. doi:10.1159/000176049. ISBN 978-3-8055-8622-1. PMID 19011293.
- ↑ 5.0 5.1 5.2 5.3 5.4 5.5 5.6 5.7 5.8 "Testosterone". Drugs.com. American Society of Health-System Pharmacists. 4 December 2015. สืบค้นเมื่อ 3 September 2016.
- ↑ 6.0 6.1 Luetjens CM, Weinbauer GF (2012). "Chapter 2: Testosterone: Biosynthesis, transport, metabolism and (non-genomic) actions". ใน Nieschlag E, Behre HM, Nieschlag S (บ.ก.). Testosterone: Action, Deficiency, Substitution (4th ed.). Cambridge: Cambridge University Press. pp. 15–32. ISBN 978-1-107-01290-5.
- ↑ Torjesen PA, Sandnes L (Mar 2004). "Serum testosterone in women as measured by an automated immunoassay and a RIA". Clinical Chemistry. 50 (3): 678, author reply 678–9. doi:10.1373/clinchem.2003.027565. PMID 14981046.
- ↑ Southren AL, Gordon GG, Tochimoto S, Pinzon G, Lane DR, Stypulkowski W (May 1967). "Mean plasma concentration, metabolic clearance and basal plasma production rates of testosterone in normal young men and women using a constant infusion procedure: effect of time of day and plasma concentration on the metabolic clearance rate of testosterone". The Journal of Clinical Endocrinology & Metabolism. 27 (5): 686–94. doi:10.1210/jcem-27-5-686. PMID 6025472.
- ↑ Southren AL, Tochimoto S, Carmody NC, Isurugi K (Nov 1965). "Plasma production rates of testosterone in normal adult men and women and in patients with the syndrome of feminizing testes". The Journal of Clinical Endocrinology & Metabolism. 25 (11): 1441–50. doi:10.1210/jcem-25-11-1441. PMID 5843701.
- ↑ Dabbs M, Dabbs JM (2000). Heroes, rogues, and lovers: testosterone and behavior. New York: McGraw-Hill. ISBN 978-0-07-135739-5.
- ↑ Sheffield-Moore, M (2000). "Androgens and the control of skeletal muscle protein synthesis". Annals of Medicine. 32 (3): 181–6. doi:10.3109/07853890008998825. PMID 10821325.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Handelsman, David J (January 2013). "Androgen Physiology, Pharmacology and Abuse". Endotext [Internet]. WWW.ENDOTEXT.ORG. MDText.com, Inc.
- ↑ 13.0 13.1 Swaab, DF; Garcia-Falgueras, A (2009). "Sexual differentiation of the human brain in relation to gender identity and sexual orientation". Functional Neurology. 24 (1): 17–28. PMID 19403051.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Browne, KR (2002). Biology at work: rethinking sexual equality. New Brunswick, NJ: Rutgers University Press. p. 112. ISBN 0-8135-3053-9.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Forest, MG; Cathiard, AM; Bertrand, JA (July 1973). "Evidence of testicular activity in early infancy". The Journal of Clinical Endocrinology and Metabolism. 37 (1): 148–51. doi:10.1210/jcem-37-1-148. PMID 4715291.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Corbier, P; Edwards, DA; Roffi, J (1992). "The neonatal testosterone surge: a comparative study". Archives Internationales de Physiologie, de Biochimie et de Biophysique. 100 (2): 127–31. doi:10.3109/13813459209035274. PMID 1379488.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Dakin, CL; Wilson, CA; Kalló, I; Coen, CW; Davies, DC (May 2008). "Neonatal stimulation of 5-HT(2) receptors reduces androgen receptor expression in the rat anteroventral periventricular nucleus and sexually dimorphic preoptic area". The European Journal of Neuroscience. 27 (9): 2473–80. doi:10.1111/j.1460-9568.2008.06216.x. PMID 18445234.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Kalat, JW (2009). "Reproductive behaviors". Biological psychology. Belmont, Calif: Wadsworth, Cengage Learning. p. 321. ISBN 0-495-60300-7.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 19.0 19.1 Pinyerd, B; Zipf, WB (2005). "Puberty-timing is everything!". Journal of Pediatric Nursing. 20 (2): 75–82. doi:10.1016/j.pedn.2004.12.011. PMID 15815567.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Ganong (2012). Ganong's Review of Medical Physiology (24 ed.). TATA McGRAW Hill. pp. 423–25. ISBN 978-1-25-902753-6.
- ↑ Raggatt, LJ; Partridge, NC (2010). "Cellular and molecular mechanisms of bone remodeling". The Journal of Biological Chemistry. 285 (33): 25103–8. doi:10.1074/jbc.R109.041087. PMC 2919071. PMID 20501658.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Kelsey, TW; Li, LQ; Mitchell, RT; Whelan, A; Anderson, RA; Wallace, WH (8 October 2014). "A validated age-related normative model for male total testosterone shows increasing variance but no decline after age 40 years". PloS One. 9 (10): e109346. Bibcode:2014PLoSO...9j9346K. doi:10.1371/journal.pone.0109346. PMC 4190174. PMID 25295520.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Mehta, PH; Jones, AC; Josephs, RA (June 2008). "The social endocrinology of dominance: basal testosterone predicts cortisol changes and behavior following victory and defeat" (PDF). Journal of Personality and Social Psychology. 94 (6): 1078–93. doi:10.1037/0022-3514.94.6.1078. PMID 18505319. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 19 April 2009. สืบค้นเมื่อ 22 February 2017.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Ajayi, AA; Halushka, PV (May 2005). "Castration reduces platelet thromboxane A2 receptor density and aggregability". Qjm. 98 (5): 349–56. doi:10.1093/qjmed/hci054. PMID 15820970.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Ajayi, AA; Mathur, R; Halushka, PV (June 1995). "Testosterone increases human platelet thromboxane A2 receptor density and aggregation responses". Circulation. 91 (11): 2742–7. doi:10.1161/01.CIR.91.11.2742. PMID 7758179.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Morgentaler, A; Schulman, C (2009). "Testosterone and prostate safety". Frontiers of Hormone Research. Frontiers of Hormone Research. 37: 197–203. doi:10.1159/000176054. ISBN 978-3-8055-8622-1. PMID 19011298.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Rhoden, EL; Averbeck, MA; Teloken, PE (September 2008). "Androgen replacement in men undergoing treatment for prostate cancer". The Journal of Sexual Medicine. 5 (9): 2202–08. doi:10.1111/j.1743-6109.2008.00925.x. PMID 18638000.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Morgentaler, A; Traish, AM (February 2009). "Shifting the paradigm of testosterone and prostate cancer: the saturation model and the limits of androgen-dependent growth". European Urology. 55 (2): 310–20. doi:10.1016/j.eururo.2008.09.024. PMID 18838208.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Haddad, RM; Kennedy, CC; Caples, SM; Tracz, MJ; Boloña, ER; Sideras, K; Uraga, MV; Erwin, PJ; Montori, VM (January 2007). "Testosterone and cardiovascular risk in men: a systematic review and meta-analysis of randomized placebo-controlled trials". Mayo Clinic Proceedings. 82 (1): 29–39. doi:10.4065/82.1.29. PMID 17285783.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Jones, TH; Saad, F (December 2009). "The effects of testosterone on risk factors for, and the mediators of, the atherosclerotic process". Atherosclerosis. 207 (2): 318–27. doi:10.1016/j.atherosclerosis.2009.04.016. PMID 19464009.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Stanworth, RD; Jones, TH (2008). "Testosterone for the aging male; current evidence and recommended practice". Clinical Interventions in Aging. 3 (1): 25–44. PMC 2544367. PMID 18488876.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Van Anders, SM; Watson, NV (2006). "Menstrual cycle irregularities are associated with testosterone levels in healthy premenopausal women". American Journal of Human Biology. 18 (6): 841–44. doi:10.1002/ajhb.20555. PMID 17039468.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 33.0 33.1 33.2 Marazziti, D; Canale, D (August 2004). "Hormonal changes when falling in love". Psychoneuroendocrinology. 29 (7): 931–36. doi:10.1016/j.psyneuen.2003.08.006. PMID 15177709.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Fox, CA; Ismail, AA; Love, DN; Kirkham, KE; Loraine, JA (January 1972). "Studies on the relationship between plasma testosterone levels and human sexual activity". The Journal of Endocrinology. 52 (1): 51–8. doi:10.1677/joe.0.0520051. PMID 5061159.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ van Anders, SM; Dunn, EJ (August 2009). "Are gonadal steroids linked with orgasm perceptions and sexual assertiveness in women and men?". Hormones and Behavior. 56 (2): 206–13. doi:10.1016/j.yhbeh.2009.04.007. PMID 19409392.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Exton, MS; Bindert, A; Krüger, T; Scheller, F; Hartmann, U; Schedlowski, M (1999). "Cardiovascular and endocrine alterations after masturbation-induced orgasm in women". Psychosomatic Medicine. 61 (3): 280–89. doi:10.1097/00006842-199905000-00005. PMID 10367606.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Purvis, K; Landgren, BM; Cekan, Z; Diczfalusy, E (September 1976). "Endocrine effects of masturbation in men". The Journal of Endocrinology. 70 (3): 439–44. doi:10.1677/joe.0.0700439. PMID 135817.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Harding, SM; Velotta, JP (May 2011). "Comparing the relative amount of testosterone required to restore sexual arousal, motivation, and performance in male rats". Hormones and Behavior. 59 (5): 666–73. doi:10.1016/j.yhbeh.2010.09.009. PMID 20920505.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ James, PJ; Nyby, JG; Saviolakis, GA (September 2006). "Sexually stimulated testosterone release in male mice (Mus musculus) : roles of genotype and sexual arousal". Hormones and Behavior. 50 (3): 424–31. doi:10.1016/j.yhbeh.2006.05.004. PMID 16828762.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 40.0 40.1 Wallen, K (September 2001). "Sex and context: hormones and primate sexual motivation". Hormones and Behavior. 40 (2): 339–57. doi:10.1006/hbeh.2001.1696. PMID 11534996.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Hart, BL (December 1983). "Role of testosterone secretion and penile reflexes in sexual behavior and sperm competition in male rats: a theoretical contribution". Physiology & Behavior. 31 (6): 823–27. doi:10.1016/0031-9384(83)90279-2. PMID 6665072.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Kraemer, HC; Becker, HB; Brodie, HK; Doering, CH; Moos, RH; Hamburg, DA (March 1976). "Orgasmic frequency and plasma testosterone levels in normal human males". Archives of Sexual Behavior. 5 (2): 125–32. doi:10.1007/BF01541869. PMID 1275688.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Roney, JR; Mahler, SV; Maestripieri, D (2003). "Behavioral and hormonal responses of men to brief interactions with women". Evolution and Human Behavior. 24 (6): 365–75. doi:10.1016/S1090-5138(03)00053-9.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Pirke, KM; Kockott, G; Dittmar, F (November 1974). "Psychosexual stimulation and plasma testosterone in man". Archives of Sexual Behavior. 3 (6): 577–84. doi:10.1007/BF01541140. PMID 4429441.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Hellhammer, DH; Hubert, W; Schürmeyer, T (1985). "Changes in saliva testosterone after psychological stimulation in men". Psychoneuroendocrinology. 10 (1): 77–81. doi:10.1016/0306-4530(85)90041-1. PMID 4001279.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Rowland, DL; Heiman, JR; Gladue, BA; Hatch, JP; Doering, CH; Weiler, SJ (1987). "Endocrine, psychological and genital response to sexual arousal in men". Psychoneuroendocrinology. 12 (2): 149–58. doi:10.1016/0306-4530(87)90045-X. PMID 3602262.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Miller, SL; Maner, JK (February 2010). "Scent of a woman: men's testosterone responses to olfactory ovulation cues". Psychological Science. 21 (2): 276–83. doi:10.1177/0956797609357733. PMID 20424057.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Gangestead, SW; Thornhill, R; Garver-Apgar, CE (2005). "Adaptations to Ovulation: Implications for Sexual and Social Behavior". Current Directions in Psychological Science. 14 (6): 312–16. doi:10.1111/j.0963-7214.2005.00388.x.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Alexander, GM; Sherwin, BB (September 1991). "The association between testosterone, sexual arousal, and selective attention for erotic stimuli in men". Hormones and Behavior. 25 (3): 367–81. doi:10.1016/0018-506X(91)90008-6. PMID 1937428.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Traish, AM; Kim, N; Min, K; Munarriz, R; Goldstein, I (April 2002). "Role of androgens in female genital sexual arousal: receptor expression, structure, and function". Fertility and Sterility. 77 Suppl 4: S11-8. doi:10.1016/s0015-0282(02)02978-3. PMID 12007897.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ van Anders, SM; Hamilton, LD; Schmidt, N; Watson, NV (April 2007). "Associations between testosterone secretion and sexual activity in women". Hormones and Behavior. 51 (4): 477–82. doi:10.1016/j.yhbeh.2007.01.003. PMID 17320881.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Tuiten, A; Van Honk, J; Koppeschaar, H; Bernaards, C; Thijssen, J; Verbaten, R (February 2000). "Time course of effects of testosterone administration on sexual arousal in women". Archives of General Psychiatry. 57 (2): 149–53, discussion 155-6. doi:10.1001/archpsyc.57.2.149. PMID 10665617.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Goldey, KL; van Anders, SM (May 2011). "Sexy thoughts: effects of sexual cognitions on testosterone, cortisol, and arousal in women". Hormones and Behavior. 59 (5): 754–64. doi:10.1016/j.yhbeh.2010.12.005. PMID 21185838.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 54.0 54.1 Bolour, S; Braunstein, G (2005). "Testosterone therapy in women: a review". International Journal of Impotence Research. 17 (5): 399–408. doi:10.1038/sj.ijir.3901334. PMID 15889125.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 55.0 55.1 van Anders, SM; Watson, NV (July 2006). "Relationship status and testosterone in North American heterosexual and non-heterosexual men and women: cross-sectional and longitudinal data". Psychoneuroendocrinology. 31 (6): 715–23. doi:10.1016/j.psyneuen.2006.01.008. PMID 16621328.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 56.0 56.1 56.2 Booth, A; Dabbs, JM (1993). "Testosterone and Men's Marriages". Social Forces. 72 (2): 463–77. doi:10.1093/sf/72.2.463.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Mazur, A; Michalek, J (1998). "Marriage, Divorce, and Male Testosterone". Social Forces. 77 (1): 315–30. doi:10.1093/sf/77.1.315.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Gray, PB; Chapman, JF; Burnham, TC; McIntyre, MH; Lipson, SF; Ellison, PT (June 2004). "Human male pair bonding and testosterone". Human Nature. 15 (2): 119–31. doi:10.1007/s12110-004-1016-6. PMID 26190409.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Gray, PB; Campbell, BC; Marlowe, FW; Lipson, SF; Ellison, PT (October 2004). "Social variables predict between-subject but not day-to-day variation in the testosterone of US men". Psychoneuroendocrinology. 29 (9): 1153–62. doi:10.1016/j.psyneuen.2004.01.008. PMID 15219639.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ van Anders, SM; Watson, NV (February 2007). "Testosterone levels in women and men who are single, in long-distance relationships, or same-city relationships". Hormones and Behavior. 51 (2): 286–91. doi:10.1016/j.yhbeh.2006.11.005. PMID 17196592.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Berg, SJ; Wynne-Edwards, KE (June 2001). "Changes in testosterone, cortisol, and estradiol levels in men becoming fathers". Mayo Clinic Proceedings. 76 (6): 582–92. doi:10.4065/76.6.582. PMID 11393496.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ "Parenting Skills Influenced by Testosterone Levels, Empathy". Psych Central.com. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 31 October 2015. สืบค้นเมื่อ 2 November 2015.
- ↑ 63.0 63.1
Sapienza, P; Zingales, L; Maestripieri, D (September 2009). "Gender differences in financial risk aversion and career choices are affected by testosterone". Proceedings of the National Academy of Sciences of the United States of America. 106 (36): 15268–73. Bibcode:2009PNAS..10615268S. doi:10.1073/pnas.0907352106. PMC 2741240. PMID 19706398.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Apicella, CL; Dreber, A; Campbell, B; Gray, PB; Hoffman, M; Little, AC (November 2008). "Testosterone and financial risk preferences". Evolution and Human Behavior. 29 (6): 384–90. doi:10.1016/j.evolhumbehav.2008.07.001.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 65.0 65.1 Wright J, Ellis L, Beaver K (2009). Handbook of crime correlates. San Diego: Academic Press. pp. 208–10. ISBN 978-0-12-373612-3.
- ↑
Goldman, D; Lappalainen, J; Ozaki, N. "Direct analysis of candidate genes in impulsive disorders".
{{cite journal}}: Cite journal ต้องการ|journal=(help) อ้างอิงใน Bock, G; Goode, J, บ.ก. (1996). Genetics of Criminal and Antisocial Behaviour. Ciba Foundation Symposium 194. Chichester: John Wiley & Sons. - ↑ Coccaro E (1996). "Neurotransmitter correlates of impulsive aggression in humans. In: Ferris C, Grisso T, eds. Understanding Aggressive Behaviour inn Children". Annals of the New York Academy of Sciences. 794 (1): 82–89. Bibcode:1996NYASA.794...82C. doi:10.1111/j.1749-6632.1996.tb32511.x. PMID 8853594. S2CID 33226665.
- ↑ Finkelstein JW, Susman EJ, Chinchilli VM, Kunselman SJ, D'Arcangelo MR, Schwab J, Demers LM, Liben LS, Lookingbill G, Kulin HE (1997). "Estrogen or testosterone increases self-reported aggressive behaviors in hypogonadal adolescents". The Journal of Clinical Endocrinology & Metabolism. 82 (8): 2433–38. doi:10.1210/jcem.82.8.4165. PMID 9253313.
- ↑ Delville Y, Mansour KM, Ferris CF (July 1996). "Testosterone facilitates aggression by modulating vasopressin receptors in the hypothalamus". Physiology & Behavior. 60 (1): 25–9. doi:10.1016/0031-9384(95)02246-5. PMID 8804638. S2CID 23870320.
- ↑ Eisenegger C, Naef M, Snozzi R, Heinrichs M, Fehr E (2010). "Prejudice and truth about the effect of testosterone on human bargaining behaviour". Nature. 463 (7279): 356–59. Bibcode:2010Natur.463..356E. doi:10.1038/nature08711. PMID 19997098. S2CID 1305527.
- ↑ van Honk J, Montoya ER, Bos PA, van Vugt M, Terburg D (May 2012). "New evidence on testosterone and cooperation". Nature. 485 (7399): E4–5, discussion E5–6. Bibcode:2012Natur.485E...4V. doi:10.1038/nature11136. PMID 22622587. S2CID 4383859.
- ↑ Zak PJ, Kurzban R, Ahmadi S, Swerdloff RS, Park J, Efremidze L, Redwine K, Morgan K, Matzner W (2009-01-01). "Testosterone administration decreases generosity in the ultimatum game". PLOS ONE. 4 (12): e8330. Bibcode:2009PLoSO...4.8330Z. doi:10.1371/journal.pone.0008330. PMC 2789942. PMID 20016825.
- ↑ McGinnis MY (Dec 2004). "Anabolic androgenic steroids and aggression: studies using animal models". Annals of the New York Academy of Sciences. 1036 (1): 399–415. Bibcode:2004NYASA1036..399M. doi:10.1196/annals.1330.024. PMID 15817752. S2CID 36368056.
- ↑ von der PB, Sarkola T, Seppa K, Eriksson CJ (Sep 2002). "Testosterone, 5 alpha-dihydrotestosterone and cortisol in men with and without alcohol-related aggression". Journal of Studies on Alcohol. 63 (5): 518–26. doi:10.15288/jsa.2002.63.518. PMID 12380846.
- ↑ 75.0 75.1 75.2 75.3 75.4 Archer J (2006). "Testosterone and human aggression: an evaluation of the challenge hypothesis" (PDF). Neuroscience and Biobehavioral Reviews. 30 (3): 319–345. doi:10.1016/j.neubiorev.2004.12.007. PMID 16483890. S2CID 26405251. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ January 9, 2016.
- ↑ 76.0 76.1 Ellis L, Hoskin AW (2015). "The evolutionary neuroandrogenic theory of criminal behavior expanded". Aggression and Violent Behavior. 24: 61–74. doi:10.1016/j.avb.2015.05.002.
- ↑ Hoskin AW, Ellis L (2015). "Fetal Testosterone and Criminality: Test of Evolutionary Neuroandrogenic Theory". Criminology. 53 (1): 54–73. doi:10.1111/1745-9125.12056.
- ↑ Perciavalle V, Di Corrado D, Petralia MC, Gurrisi L, Massimino S, Coco M (Jun 2013). "The second-to-fourth digit ratio correlates with aggressive behavior in professional soccer players". Molecular Medicine Reports. 7 (6): 1733–1738. doi:10.3892/mmr.2013.1426. PMC 3694562. PMID 23588344.
- ↑ Bailey AA, Hurd PL (Mar 2005). "Finger length ratio (2D:4D) correlates with physical aggression in men but not in women". Biological Psychology. 68 (3): 215–222. doi:10.1016/j.biopsycho.2004.05.001. PMID 15620791. S2CID 16606349.
Lay summary: "Finger Length Predicts Aggression in Men". LiveScience. 2 March 2005. - ↑ Benderlioglu Z, Nelson RJ (Dec 2004). "Digit length ratios predict reactive aggression in women, but not in men". Hormones and Behavior. 46 (5): 558–564. doi:10.1016/j.yhbeh.2004.06.004. PMID 15555497. S2CID 17464657.
- ↑ Liu J, Portnoy J, Raine A (August 2012). "Association between a marker for prenatal testosterone exposure and externalizing behavior problems in children". Development and Psychopathology. 24 (3): 771–782. doi:10.1017/S0954579412000363. PMC 4247331. PMID 22781854.
- ↑ Butovskaya M, Burkova V, Karelin D, Fink B (1 October 2015). "Digit ratio (2D:4D), aggression, and dominance in the Hadza and the Datoga of Tanzania". American Journal of Human Biology. 27 (5): 620–627. doi:10.1002/ajhb.22718. PMID 25824265. S2CID 205303673.
- ↑ Joyce CW, Kelly JC, Chan JC, Colgan G, O'Briain D, Mc Cabe JP, Curtin W (Nov 2013). "Second to fourth digit ratio confirms aggressive tendencies in patients with boxers fractures". Injury. 44 (11): 1636–1639. doi:10.1016/j.injury.2013.07.018. PMID 23972912.
- ↑ Carré JM, Olmstead NA (Feb 2015). "Social neuroendocrinology of human aggression: examining the role of competition-induced testosterone dynamics" (PDF). Neuroscience. 286: 171–186. doi:10.1016/j.neuroscience.2014.11.029. PMID 25463514. S2CID 32112035. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ January 26, 2016. สืบค้นเมื่อ December 30, 2015.
- ↑ Klinesmith J, Kasser T, McAndrew FT (July 2006). "Guns, testosterone, and aggression: an experimental test of a mediational hypothesis". Psychological Science. 17 (7): 568–571. doi:10.1111/j.1467-9280.2006.01745.x. PMID 16866740. S2CID 33952211.
- ↑ Mcandrew FT (2009). "The Interacting Roles of Testosterone and Challenges to Status in Human Male Aggression" (PDF). Aggression and Violent Behavior. 14 (5): 330–335. doi:10.1016/j.avb.2009.04.006.
- ↑ Batrinos, ML (2012-01-01). "Testosterone and aggressive behavior in man". International Journal of Endocrinology and Metabolism. 10 (3): 563–68. doi:10.5812/ijem.3661. PMC 3693622. PMID 23843821.
- ↑ Weierstall R, Moran J, Giebel G, Elbert T (1 May 2014). "Testosterone reactivity and identification with a perpetrator or a victim in a story are associated with attraction to violence-related cues". International Journal of Law and Psychiatry. 37 (3): 304–312. doi:10.1016/j.ijlp.2013.11.016. PMID 24367977.
- ↑ Nguyen TV, McCracken JT, Albaugh MD, Botteron KN, Hudziak JJ, Ducharme S (Jan 2016). "A testosterone-related structural brain phenotype predicts aggressive behavior from childhood to adulthood". Psychoneuroendocrinology. 63: 109–118. doi:10.1016/j.psyneuen.2015.09.021. PMC 4695305. PMID 26431805.
- ↑ Soma KK, Scotti MA, Newman AE, Charlier TD, Demas GE (Oct 2008). "Novel mechanisms for neuroendocrine regulation of aggression". Frontiers in Neuroendocrinology. 29 (4): 476–89. doi:10.1016/j.yfrne.2007.12.003. PMID 18280561. S2CID 32650274.
- ↑ Soma KK, Sullivan KA, Tramontin AD, Saldanha CJ, Schlinger BA, Wingfield JC (2000). "Acute and chronic effects of an aromatase inhibitor on territorial aggression in breeding and nonbreeding male song sparrows". Journal of Comparative Physiology A. 186 (7–8): 759–69. doi:10.1007/s003590000129. PMID 11016791. S2CID 23990605.
- ↑ McGinnis MY, Lumia AR, Breuer ME, Possidente B (Feb 2002). "Physical provocation potentiates aggression in male rats receiving anabolic androgenic steroids". Hormones and Behavior. 41 (1): 101–10. doi:10.1006/hbeh.2001.1742. PMID 11863388. S2CID 29969145.
- ↑ Wilson, JD (September 2001). "Androgens, androgen receptors, and male gender role behavior". Hormones and Behavior. 40 (2): 358–66. doi:10.1006/hbeh.2001.1684. PMID 11534997.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Cosgrove, KP; Mazure, CM; Staley, JK (October 2007). "Evolving knowledge of sex differences in brain structure, function, and chemistry". Biological Psychiatry. 62 (8): 847–55. doi:10.1016/j.biopsych.2007.03.001. PMC 2711771. PMID 17544382.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Marner, L; Nyengaard, JR; Tang, Y; Pakkenberg, B (July 2003). "Marked loss of myelinated nerve fibers in the human brain with age". The Journal of Comparative Neurology. 462 (2): 144–52. doi:10.1002/cne.10714. PMID 12794739.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Bhasin, S; Storer, TW; Berman, N; Callegari, C; Clevenger, B; Phillips, J; Bunnell, TJ; Tricker, R; Shirazi, A; Casaburi, R (July 1996). "The effects of supraphysiologic doses of testosterone on muscle size and strength in normal men". The New England Journal of Medicine. 335 (1): 1–7. doi:10.1056/NEJM199607043350101. PMID 8637535.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ "Testosterone Affects Some Women's Career Choices". NPR. 28 August 2009.
- ↑
Pike, CJ; Rosario, ER; Nguyen, TV (April 2006). "Androgens, aging, and Alzheimer's disease". Endocrine. 29 (2): 233–41. doi:10.1385/ENDO:29:2:233. PMID 16785599.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Rosario, ER; Chang, L; Stanczyk, FZ; Pike, CJ (September 2004). "Age-related testosterone depletion and the development of Alzheimer disease". JAMA. 292 (12): 1431–32. doi:10.1001/jama.292.12.1431-b. PMID 15383512.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Hogervorst, E; Bandelow, S; Combrinck, M; Smith, AD (2004). "Low free testosterone is an independent risk factor for Alzheimer's disease". Experimental Gerontology. 39 (11–12): 1633–39. doi:10.1016/j.exger.2004.06.019. PMID 15582279.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Moffat, SD; Zonderman, AB; Metter, EJ; Kawas, C; Blackman, MR; Harman, SM; Resnick, SM (January 2004). "Free testosterone and risk for Alzheimer disease in older men". Neurology. 62 (2): 188–93. doi:10.1212/WNL.62.2.188. PMID 14745052.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Moffat, SD; Hampson, E (April 1996). "A curvilinear relationship between testosterone and spatial cognition in humans: possible influence of hand preference". Psychoneuroendocrinology. 21 (3): 323–37. doi:10.1016/0306-4530(95)00051-8. PMID 8817730.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Häggström, Mikael; Richfield, David (2014). "Diagram of the pathways of human steroidogenesis". WikiJournal of Medicine. 1 (1). doi:10.15347/wjm/2014.005. ISSN 2002-4436.
- ↑ Waterman, MR; Keeney, DS (1992). "Genes involved in androgen biosynthesis and the male phenotype". Hormone Research. 38 (5–6): 217–21. doi:10.1159/000182546. PMID 1307739.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Zuber, MX; Simpson, ER; Waterman, MR (December 1986). "Expression of bovine 17 alpha-hydroxylase cytochrome P-450 cDNA in nonsteroidogenic (COS 1) cells". Science. 234 (4781): 1258–61. Bibcode:1986Sci...234.1258Z. doi:10.1126/science.3535074. PMID 3535074.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Zouboulis, CC; Degitz, K (2004). "Androgen action on human skin -- from basic research to clinical significance". Experimental Dermatology. 13 Suppl 4 (s4): 5–10. doi:10.1111/j.1600-0625.2004.00255.x. PMID 15507105.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Brooks, RV (November 1975). "Androgens". Clinics in Endocrinology and Metabolism. 4 (3): 503–20. doi:10.1016/S0300-595X(75)80045-4. PMID 58744.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Payne AH, O'Shaughnessy P (1996). "Structure, function, and regulation of steroidogenic enzymes in the Leydig cell". ใน Payne AH, Hardy MP, Russell LD (บ.ก.). Leydig Cell. Vienna [Il]: Cache River Press. pp. 260–85. ISBN 978-0-9627422-7-9.
- ↑ Swerdloff RS, Wang C, Bhasin S (Apr 1992). "Developments in the control of testicular function". Baillière's Clinical Endocrinology and Metabolism. 6 (2): 451–83. doi:10.1016/S0950-351X(05)80158-2. PMID 1377467.
- ↑ Liverman CT, Blazer DG, และคณะ (Institute of Medicine (US) Committee on Assessing the Need for Clinical Trials of Testosterone Replacement Therapy) (January 1, 2004). "Introduction". Testosterone and Aging: Clinical Research Directions. National Academies Press (US). doi:10.17226/10852. ISBN 978-0-309-09063-6. PMID 25009850 – โดยทาง www.ncbi.nlm.nih.gov.
- ↑ Huhtaniemi I (2014). "Late-onset hypogonadism: current concepts and controversies of pathogenesis, diagnosis and treatment". Asian Journal of Andrology. 16 (2): 192–202. doi:10.4103/1008-682X.122336. PMC 3955328. PMID 24407185.
- ↑ Huhtaniemi IT (2014). "Andropause--lessons from the European Male Ageing Study". Annales d'Endocrinologie. 75 (2): 128–31. doi:10.1016/j.ando.2014.03.005. PMID 24793989.
- ↑ Vingren JL, Kraemer WJ, Ratamess NA, Anderson JM, Volek JS, Maresh CM (2010). "Testosterone physiology in resistance exercise and training: the up-stream regulatory elements". Sports Medicine. 40 (12): 1037–53. doi:10.2165/11536910-000000000-00000. PMID 21058750. S2CID 11683565.
- ↑ Hulmi JJ, Ahtiainen JP, Selänne H, Volek JS, Häkkinen K, Kovanen V, Mero AA (May 2008). "Androgen receptors and testosterone in men—effects of protein ingestion, resistance exercise and fiber type". The Journal of Steroid Biochemistry and Molecular Biology. 110 (1–2): 130–37. doi:10.1016/j.jsbmb.2008.03.030. PMID 18455389. S2CID 26280370.
- ↑ Hackney AC, Moore AW, Brownlee KK (2005). "Testosterone and endurance exercise: development of the "exercise-hypogonadal male condition"". Acta Physiologica Hungarica. 92 (2): 121–37. doi:10.1556/APhysiol.92.2005.2.3. PMID 16268050.
- ↑ Livera G, Rouiller-Fabre V, Pairault C, Levacher C, Habert R (August 2002). "Regulation and perturbation of testicular functions by vitamin A". Reproduction. 124 (2): 173–180. doi:10.1530/rep.0.1240173. PMID 12141930.
- ↑ Pilz S, Frisch S, Koertke H, Kuhn J, Dreier J, Obermayer-Pietsch B, และคณะ (March 2011). "Effect of vitamin D supplementation on testosterone levels in men". Hormone and Metabolic Research. 43 (3): 223–225. doi:10.1055/s-0030-1269854. PMID 21154195. S2CID 206315145.
- ↑ Prasad AS, Mantzoros CS, Beck FW, Hess JW, Brewer GJ (May 1996). "Zinc status and serum testosterone levels of healthy adults". Nutrition. 12 (5): 344–348. CiteSeerX 10.1.1.551.4971. doi:10.1016/S0899-9007(96)80058-X. PMID 8875519.
- ↑ Koehler K, Parr MK, Geyer H, Mester J, Schänzer W (January 2009). "Serum testosterone and urinary excretion of steroid hormone metabolites after administration of a high-dose zinc supplement". European Journal of Clinical Nutrition. 63 (1): 65–70. doi:10.1038/sj.ejcn.1602899. PMID 17882141.
- ↑ Håkonsen LB, Thulstrup AM, Aggerholm AS, Olsen J, Bonde JP, Andersen CY, Bungum M, Ernst EH, Hansen ML, Ernst EH, Ramlau-Hansen CH (2011). "Does weight loss improve semen quality and reproductive hormones? Results from a cohort of severely obese men". Reproductive Health. 8 (1): 24. doi:10.1186/1742-4755-8-24. PMC 3177768. PMID 21849026.
- ↑ MacDonald AA, Herbison GP, Showell M, Farquhar CM (2010). "The impact of body mass index on semen parameters and reproductive hormones in human males: a systematic review with meta-analysis". Human Reproduction Update. 16 (3): 293–311. doi:10.1093/humupd/dmp047. PMID 19889752.
- ↑ Andersen ML, Tufik S (Oct 2008). "The effects of testosterone on sleep and sleep-disordered breathing in men: its bidirectional interaction with erectile function". Sleep Medicine Reviews. 12 (5): 365–79. doi:10.1016/j.smrv.2007.12.003. PMID 18519168.
- ↑ Schultheiss OC, Campbell KL, McClelland DC (Dec 1999). "Implicit power motivation moderates men's testosterone responses to imagined and real dominance success". Hormones and Behavior. 36 (3): 234–41. doi:10.1006/hbeh.1999.1542. PMID 10603287. S2CID 6002474.
- ↑ Akdoğan M, Tamer MN, Cüre E, Cüre MC, Köroğlu BK, Delibaş N (May 2007). "Effect of spearmint (Mentha spicata Labiatae) teas on androgen levels in women with hirsutism". Phytotherapy Research. 21 (5): 444–47. doi:10.1002/ptr.2074. PMID 17310494. S2CID 21961390.
- ↑ Kumar V, Kural MR, Pereira BM, Roy P (Dec 2008). "Spearmint induced hypothalamic oxidative stress and testicular anti-androgenicity in male rats - altered levels of gene expression, enzymes and hormones". Food and Chemical Toxicology. 46 (12): 3563–70. doi:10.1016/j.fct.2008.08.027. PMID 18804513.
- ↑ Grant P (Feb 2010). "Spearmint herbal tea has significant anti-androgen effects in polycystic ovarian syndrome. A randomized controlled trial". Phytotherapy Research. 24 (2): 186–88. doi:10.1002/ptr.2900. PMID 19585478. S2CID 206425734.
- ↑ Armanini D, Fiore C, Mattarello MJ, Bielenberg J, Palermo M (Sep 2002). "History of the endocrine effects of licorice". Experimental and Clinical Endocrinology & Diabetes. 110 (6): 257–61. doi:10.1055/s-2002-34587. PMID 12373628.
- ↑ Cumming, DC; Wall, SR (November 1985). "Non-sex hormone-binding globulin-bound testosterone as a marker for hyperandrogenism". The Journal of Clinical Endocrinology and Metabolism. 61 (5): 873–6. doi:10.1210/jcem-61-5-873. PMID 4044776.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 129.00 129.01 129.02 129.03 129.04 129.05 129.06 129.07 129.08 129.09 Becker, Kenneth L. (2001). Principles and Practice of Endocrinology and Metabolism. Lippincott Williams & Wilkins. pp. 1116, 1119, 1183. ISBN 978-0-7817-1750-2.
- ↑ 130.0 130.1 130.2 130.3 Wecker, Lynn; Watts, Stephanie; Faingold, Carl; Dunaway, George; Crespo, Lynn (1 April 2009). Brody's Human Pharmacology. Elsevier Health Sciences. pp. 468–469. ISBN 0-323-07575-4.
- ↑
Penning, TM (2010). "New frontiers in androgen biosynthesis and metabolism". Curr Opin Endocrinol Diabetes Obes. 17 (3): 233–9. doi:10.1097/MED.0b013e3283381a31. PMC 3206266. PMID 20186052.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Horsky, J.; Presl, J. (6 December 2012). Ovarian Function and its Disorders: Diagnosis and Therapy. Springer Science & Business Media. pp. 107-. ISBN 978-94-009-8195-9.
- ↑ 133.0 133.1 133.2 133.3 133.4 Zhou, Shufeng (6 April 2016). Cytochrome P450 2D6: Structure, Function, Regulation and Polymorphism. CRC Press. pp. 242-. ISBN 978-1-4665-9788-4.
- ↑ Trager, L (1977). Steroidhormone: Biosynthese, Stoffwechsel, Wirkung (ภาษาเยอรมัน). Springer-Verlag. p. 349. ISBN 0-387-08012-0.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Randall, VA (April 1994). "Role of 5 alpha-reductase in health and disease". Baillière's Clinical Endocrinology and Metabolism. 8 (2): 405–31. doi:10.1016/S0950-351X(05)80259-9. PMID 8092979.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Meinhardt, U; Mullis, PE (August 2002). "The essential role of the aromatase/p450arom". Seminars in Reproductive Medicine. 20 (3): 277–84. doi:10.1055/s-2002-35374. PMID 12428207.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Noakes, David E. (23 April 2009). Arthur's Veterinary Reproduction and Obstetrics. Elsevier Health Sciences UK. pp. 695-. ISBN 978-0-7020-3990-4.
- ↑ Nieschlag, E; Behre, HM (1 April 2004). Testosterone: Action, Deficiency, Substitution. Cambridge University Press. pp. 626-. ISBN 978-1-139-45221-2.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Parl, Fritz F. (2000). Estrogens, Estrogen Receptor and Breast Cancer. IOS Press. pp. 25-. ISBN 978-0-9673355-4-4.
- ↑ Norman, Anthony W.; Henry, Helen L. (30 July 2014). Hormones. Academic Press. pp. 261-. ISBN 978-0-08-091906-5.
- ↑ Mozayani, Ashram; Raymon, Lionel (18 September 2011). Handbook of Drug Interactions: A Clinical and Forensic Guide. Springer Science & Business Media. pp. 656-. ISBN 978-1-61779-222-9.
- ↑ Sundaram, K; Kumar, N; Monder, C; Bardin, CW (1995). "Different patterns of metabolism determine the relative anabolic activity of 19-norandrogens". J. Steroid Biochem. Mol. Biol. 53 (1–6): 253–7. doi:10.1016/0960-0760(95)00056-6. PMID 7626464.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Hiipakka, RA; Liao, S (October 1998). "Molecular mechanism of androgen action". Trends in Endocrinology and Metabolism. 9 (8): 317–24. doi:10.1016/S1043-2760(98)00081-2. PMID 18406296.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ McPhaul, MJ; Young, M (September 2001). "Complexities of androgen action". Journal of the American Academy of Dermatology. 45 (3 Suppl): S87-94. doi:10.1067/mjd.2001.117429. PMID 11511858.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Bennett, NC; Gardiner, RA; Hooper, JD; Johnson, DW; Gobe, GC (2010). "Molecular cell biology of androgen receptor signalling". Int. J. Biochem. Cell Biol. 42 (6): 813–27. doi:10.1016/j.biocel.2009.11.013. PMID 19931639.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Wang, C; Liu, Y; Cao, JM (2014). "G protein-coupled receptors: extranuclear mediators for the non-genomic actions of steroids". Int J Mol Sci. 15 (9): 15412–25. doi:10.3390/ijms150915412. PMC 4200746. PMID 25257522.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Lang, F; Alevizopoulos, K; Stournaras, C (2013). "Targeting membrane androgen receptors in tumors". Expert Opin. Ther. Targets. 17 (8): 951–63. doi:10.1517/14728222.2013.806491. PMID 23746222.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Breiner, M; Romalo, G; Schweikert, HU (August 1986). "Inhibition of androgen receptor binding by natural and synthetic steroids in cultured human genital skin fibroblasts". Klinische Wochenschrift. 64 (16): 732–37. doi:10.1007/BF01734339. PMID 3762019.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Kelly, MJ; Qiu, J; Rønnekleiv, OK (2005-01-01). "Estrogen signaling in the hypothalamus". Vitamins and Hormones. 71: 123–45. doi:10.1016/S0083-6729(05)71005-0. PMID 16112267.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ McCarthy, MM (2008). "Estradiol and the developing brain". Physiological Reviews. 88 (1): 91–124. doi:10.1152/physrev.00010.2007. PMC 2754262. PMID 18195084.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Myers, JB; Meacham, RB (2003). "Androgen replacement therapy in the aging male". Reviews in Urology. 5 (4): 216–26. PMC 1508369. PMID 16985841.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Staff (3 March 2015). "Testosterone Products: Drug Safety Communication - FDA Cautions About Using Testosterone Products for Low Testosterone Due to Aging; Requires Labeling Change to Inform of Possible Increased Risk of Heart Attack And Stroke". FDA. สืบค้นเมื่อ 5 March 2015.
- ↑ "19th WHO Model List of Essential Medicines (April 2015)" (PDF). WHO. April 2015. สืบค้นเมื่อ 10 May 2015.
- ↑ Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. p. 197. ISBN 978-1-284-05756-0.
- ↑ Guerriero, G (2009). "Vertebrate sex steroid receptors: evolution, ligands, and neurodistribution". Annals of the New York Academy of Sciences. 1163: 154–68. doi:10.1111/j.1749-6632.2009.04460.x. PMID 19456336.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Bryan, MB; Scott, AP; Li, W (2008). "Sex steroids and their receptors in lampreys". Steroids. 73 (1): 1–12. doi:10.1016/j.steroids.2007.08.011. PMID 17931674.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Nelson, RF (2005). An introduction to behavioral endocrinology. Sunderland, Mass: Sinauer Associates. p. 143. ISBN 0-87893-617-3.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ De Loof, A (October 2006). "Ecdysteroids: the overlooked sex steroids of insects? Males: the black box". Insect Science. 13 (5): 325–338. doi:10.1111/j.1744-7917.2006.00101.x.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Mechoulam, R; Brueggemeier, RW; Denlinger, DL (September 1984). "Estrogens in insects". Journal Cellular and Molecular Life Sciences. 40 (9): 942–44. doi:10.1007/BF01946450.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Berthold, AA (1849). "Transplantation der Hoden" [Transplantation of testis]. Arch. Anat. Physiol. Wiss. (ภาษาเยอรมัน). 16: 42–6.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Brown-Sequard, CE (1889). "The effects produced on man by subcutaneous injections of liquid obtained from the testicles of animals". Lancet. 2 (3438): 105–07. doi:10.1016/S0140-6736(00)64118-1.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Gallagher, TF; Koch, FC (November 1929). "The testicular hormone". J. Biol. Chem. 84 (2): 495–500.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ David, KG; Dingemanse, E; Freud, JL (May 1935). "Über krystallinisches mannliches Hormon aus Hoden (Testosteron) wirksamer als aus harn oder aus Cholesterin bereitetes Androsteron" [On crystalline male hormone from testicles (testosterone) effective as from urine or from cholesterol]. Hoppe Seylers Z Physiol Chem (ภาษาเยอรมัน). 233 (5–6): 281–83. doi:10.1515/bchm2.1935.233.5-6.281.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Butenandt, A; Hanisch, G (1935). "Umwandlung des Dehydroandrosterons in Androstendiol und Testosterone; ein Weg zur Darstellung des Testosterons aus Cholestrin" [About Testosterone. Conversion of Dehydro-androsterons into androstendiol and testosterone; a way for the structure assignment of testosterone from cholestrol]. Hoppe Seylers Z Physiol Chem (ภาษาเยอรมัน). 237 (2): 89–97. doi:10.1515/bchm2.1935.237.1-3.89.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 165.0 165.1
Freeman, ER; Bloom, DA; McGuire, EJ (February 2001). "A brief history of testosterone". The Journal of Urology. 165 (2): 371–73. doi:10.1097/00005392-200102000-00004. PMID 11176375.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Butenandt, A; Hanisch, G (1935). "Uber die Umwandlung des Dehydroandrosterons in Androstenol-(17) -one-(3) (Testosterone) ; um Weg zur Darstellung des Testosterons auf Cholesterin (Vorlauf Mitteilung). [The conversion of dehydroandrosterone into androstenol-(17) -one-3 (testosterone) ; a method for the production of testosterone from cholesterol (preliminary communication)]". Chemische Berichte (ภาษาเยอรมัน). 68 (9): 1859–62. doi:10.1002/cber.19350680937.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Ruzicka, L; Wettstein, A (1935). "Uber die kristallinische Herstellung des Testikelhormons, Testosteron (Androsten-3-ol-17-ol) [The crystalline production of the testicle hormone, testosterone (Androsten-3-ol-17-ol)]". Helvetica Chimica Acta (ภาษาเยอรมัน). 18: 1264–75. doi:10.1002/hlca.193501801176.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Hoberman, JM; Yesalis, CE (February 1995). "The history of synthetic testosterone". Scientific American. 272 (2): 76–81. doi:10.1038/scientificamerican0295-76. PMID 7817189.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Kenyon, AT; Knowlton, K; Sandiford, I; Koch, FC; Lotwin; G (February 1940). "A comparative study of the metabolic effects of testosterone propionate in normal men and women and in eunuchoidism". Endocrinology. 26 (1): 26–45. doi:10.1210/Endo-26-1-26.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Schwarz, S; Onken, D; Schubert, A (July 1999). "The steroid story of Jenapharm: from the late 1940s to the early 1970s". Steroids. 64 (7): 439–45. doi:10.1016/S0039-128X(99)00003-3. PMID 10443899.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ de Kruif, P (1945). The Male Hormone. New York: Harcourt, Brace.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์)
แหล่งข้อมูลอื่น[แก้]
- Fargo KN, Pak TR, Foecking EM, Jones KJ (2010). "Molecular Biology of Androgen Action: Perspectives on Neuroprotective and Neurotherapeutic Effects.". ใน Pfaff DW, Etgen AM (บ.ก.). Molecular Mechanisms of Hormone Actions on Behavior. Elsevier Inc. pp. 1219–1246. doi:10.1016/B978-008088783-8.00036-X. ISBN 978-0-12-374939-0.
- Dowd NE (2013). "Sperm, testosterone, masculinities and fatherhood". Nevada Law Journal. 13 (2): 8.
- Celec P, Ostatníková D, Hodosy J (February 2015). "On the effects of testosterone on brain behavioral functions". Frontiers in Neuroscience. 9: 12. doi:10.3389/fnins.2015.00012. PMC 4330791. PMID 25741229.
- CS1 maint: uses authors parameter
- บทความที่ไม่มีแหล่งที่มาของ InChI
- บทความที่ขาดแหล่งอ้างอิงเฉพาะส่วนตั้งแต่October 2016
- บทความที่ขาดแหล่งอ้างอิงเฉพาะส่วนตั้งแต่November 2016
- Androgens and anabolic steroids
- แอนโดรเจนและสเตอรอยด์อะนาบอลิค
- บุรุษเวชศาสตร์
- ฮอร์โมนเพศ
- ฮอร์โมน
- ฮอร์โมนของอัฒฑะ
- ฮอร์โมนของรังไข่
- ฮอร์โมนมนุษย์
- เทสโทสเตอโรน
