นิวคลีโอไทด์

นิวคลีโอไทด์ (อังกฤษ: nucleotide) เป็นโครงสร้างพื้นฐานของกรดนิวคลีอิก ซึ่งประกอบด้วย นิวคลีโอไซด์ (neucleoside) กับหมู่ฟอสเฟต โดยนิวคลีโอไซด์ประกอบด้วยไนโตรจีนัสเบส (nitrogenous base; เรียกสั้นๆว่าเบส) กับน้ำตาลเพนโทส (มีคาร์บอน 5 โมเลกุล) ทั้งนี้เบสแบ่งตามโครงสร้างได้เป็นสองกลุ่มคือ ไพริมิดีน (โครงสร้างมี 1 วง) ได้แก่ ไซโตซีน (C) ไทมีน (T) และยูราซิล (U) และเบสไพรีน (โครงสร้างมี 2 วง) ได้แก่ อะดีนีน (A) กวานีน (G)
ในการรวมตัวเป็นนิวคลีโอไทด์ เบสจะต่อกับคาร์บอนตัวที่ 1 ของน้ำตาลเพนโทส และฟอสเฟตต่อกับน้ำตาลตัวที่ 5 ของเพนโทส น้ำตาลเพนโทสที่พบในนิวคลีโอไทด์มีสองชนิดคือน้ำตาลไรโบสกับน้ำตาลดีออกซีไรโบส
การสังเคราะห์[แก้]
นิวคลีโอไทด์ สามารถสังเคราะห์ได้ทั้ง ในห้องทดลอง อิน วิโทร (in vitro) และ ในสิ่งมีชีวิต อิน วิโว (in vivo) ในสิ่งมีชีวิต นิวคลีโอไทด์สามารถสังเคราะห์ จากการสร้างใหม่ (อังกฤษ :de novo) หรือ ใช้วิธีรีไซเคิลผ่าน salvage pathways[1] นิวคลีโอไทด์ มีโครงสร้างที่อดทนต่อการแตกตัวซึ่งเป็นประโยชน์ในการสามารถนำมาใช้ได้ใหม่ ในการสังเคราะห์ นิวคลีโอไทด์ตัวใหม่ การสังเคราะห์ในห้องทดลอง กลุ่มป้องกันอาจถูกนำมาใช้ nucleoside บริสุทธิ์ ถูกป้องกันเพื่อสร้าง phosphoramidite ซึ่งสามารถทดแทนสิ่งที่หาไม่ได้ในธรรมชาติ หรือ เพื่อ การสังเคราะห์ oligonucleotide
Pyrimidine ribonucleotides[แก้]
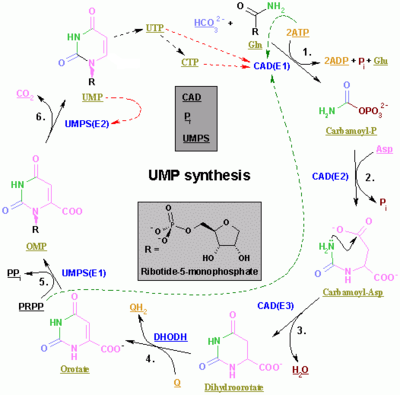
การสังเคราห์ Pyrimidine nucleotide เริ่มด้วยการสร้าง carbamoyl phosphate จาก glutamine และ CO2. ปฏิกิริยา cyclisation ระหว่าง carbamoyl phosphate ทำปฏิกิริยากับ aspartate ให้ orotate ในขั้นตอนย่อยๆ Orotate ทำปฏิกิริยากับ 5-phosphoribosyl α-diphosphate (PRPP) ให้ orotidine monophosphate (OMP) ซึ่งก็คือ decarboxylated เพื่อใช้สร้าง uridine monophosphate (UMP) ซึ่งมาจาก UMP ที่ pyrimidine nucleotide ตัวอื่นๆส่งต่อมา UMP เป็นตัว phosphorylated สำหรับ uridine triphosphate (UTP) ทำโดยผ่านปฏิกิริยากับ ATP 2 ขั้นตอน Cytidine monophosphate (CMP) ซึ่งได้รับมาจากการเปลี่ยน UTP ไปเป็น cytidine triphosphate (CTP) ด้วยปฏิกิริยาย่อยที่ทำให้เสีย 2 ฟอสเฟต[2][3]
Purine ribonucleotides[แก้]
อะตอมที่ใช้สร้าง purine nucleotides ได้มาจากหลายๆแหล่ง
 |
เป็นรูปแบบตั้งต้น biosynthetic ของ purine ring อะตอม N1 เกิดมาจาก amine group ของ Asp C2 และ C8 ได้รับมาจาก formate N3 และ N9 ได้รับมาจาก amide group ของ Gln C4 C5 และ N7 ได้รับมาจาก Gly C6 มาจาก HCO3- (CO2) |
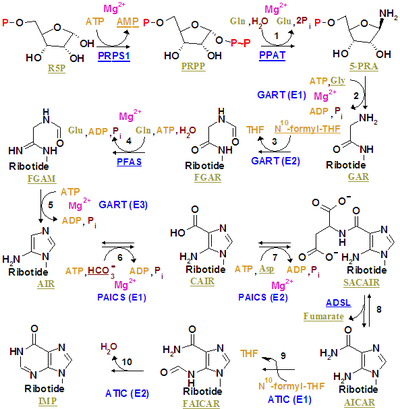
กระบวนการสังเคราะห์ใหม่ (อังกฤษ :de novo synthesis) ของ purine nucleotides ที่แสดงในรูปนี้ แสดงให้เห็น กระบวนการสร้าง purine ring กระทำโดย pathway 10 ขั้นตอน เพื่อเสริมกิ่งของ ผลิตภัณฑ์ระหว่างกลาง (intermediate) คือ IMP ซึ่งเป็น nucleotide ที่มีพื้นฐานจาก hypoxanthine สำหรับ AMP และ GMP เป็นกระบวนการย่อยของการสังเคราะห์ จากผลิตภัณฑ์ระหว่างกลาง ผ่าน pathway 2 ขั้นตอน ที่แยกออกจากกัน ดังนั้น purine moieties เป็นผลิตภัณฑ์ขั้นต้นส่วนหนึ่งของ ribonucleotides นอกเหนือจาก free bases
เอ็นไซม์ 6 ชนิดที่เป็นส่วนหนึ่งของการสังเคราะห์ IMP synthesis 3 ตัวในจำนวนนี้มีการทำงานได้หลายแบบ
ปฏิกิริยาที่ 1. เส้นทางเริ่มที่การสร้าง PRPP ซึ่ง PRPS1 คือ เอ็นไซม์ ที่พร้อมทำปฏิกิริยา R5P ซึ่งมีการจัดเรียงตัวเบื้องต้น โดย pentose phosphate pathway ไปเป็น PRPP โดยทำปฏิกิริยาซ้ำกับ ATP ปฏิกิริยานี้ไม่ปกติตรงที่ กลุ่ม pyrophosphoryl ซึ่งได้ส่งต่อมาจาก ATP ไปยัง C1 ใน R5P และทำให้เกิดผลิตภัณฑ์ที่มี α configuration ใน C1 ในปฏิกิริยานี้ยังได้ใช้ร่วมกับ pathways สำหรับการสังเคราะห์ Trp His และ pyrimidine nucleotides โดยเหมือนกับเป็น metabolic crossroad หลักที่ต้องการพลังงานจำนวนมากในการทำปฏิกิริยาซ้ำ
ปฏิกิริยาที่ 2. ในปฏิกิริยาแรกมีจุดเด่นตรงที่เกี่ยวข้องกับ purine nucleotide biosynthesis ตัวเร่งปฏิกรยา PPAT ซึ่งทำการเปลี่ยนตำแหน่ง pyrophosphate group (PPi) ใน PRPP โดย amide nitrogen ใน Gln ปฏิกิริยาเกิดขึ้น โดยการย้อน configuration ของ ribose C1 ซึ่งทำได้โดยการสร้าง β-5-phosphorybosylamine (5-PRA) และ การจัดวาง anomeric เตรียมไว้สำหรับการสร้าง nucleotide ในอนาคต ปฏิกิริยานี้ขับเคลื่อนให้เสร็จสมบูรณ์ได้โดย การ hydrolysis ตามลำดับของการปลดปล่อย PPi ซึ่งเป็นเส้นทางขั้นตอนการสร้าง flux และใช้เป็นเหตุผลในการควบคุมกระบวนการด้วย
การรวมตัวเป็นโพลีเมอร์[แก้]
ในการรวมตัวกันเป็นกรดนิวคลีอิก นิวคลีโอไทด์แต่ละตัวจะต่อกันด้วยพันธะฟอสโฟไดเอสเทอร์โดยหมู่ฟอสเฟต ที่คาร์บอนตัวที่ห้าของเพนโทสของนิวคลีโอไทด์ตัวหลังจะต่อกับหมู่ไฮดรอกซิล (-OH) ที่คาร์บอนตัวที่สามของเพนโทสของนิวคลีโอไทด์ตัวหน้า และจะต่อเช่นนี้ไปเรื่อยๆ สายของกรดนิวคลีอิกมีสองปลาย ปลายที่หมู่ฟอสเฟตเป็นอิสระเรียก ปลาย 5’ ส่วนปลายที่หมู่ไฮดรอกซิลเป็นอิสระเรียกว่าปลาย 3’
เนื่องจากส่วนของฟอสเฟตและน้ำตาลของนิวคลีโอไทด์เป็นส่วนที่คล้ายคลึงกัน แต่จุดที่ทำให้นิวคลีโอไทด์แต่ละตัวต่างกันอยู่ที่เบส ดังนั้นชนิดของเบสจึงเป็นตัวกำหนดคุณสมบัติของนิวคลีโอไทด์ ซึ่งเบสสามารถเข้าคู่กันด้วยพันธะไฮโดรเจนเป็นคู่ๆได้ เบสที่เข้าคู่กันได้นี้เรียกว่าเบสคู่สม เบสคู่สมมีสองคู่คือ A กับ T (หรือ U) และ G กับ C
อ้างอิง[แก้]
- Lehninger, A.L., Nelson, D.L., and Cox, M.M. 1993. Principle of Biochemistry. 2nd ed. New York.: Worth
- ↑ Zaharevitz DW, Anderson LW, Malinowski NM, Hyman R, Strong JM, Cysyk RL (November 1992). "Contribution of de-novo and salvage synthesis to the uracil nucleotide pool in mouse tissues and tumors in vivo". European Journal of Biochemistry. 210 (1): 293–6. doi:10.1111/j.1432-1033.1992.tb17420.x. PMID 1446677.
- ↑ Jones ME (1980). "Pyrimidine nucleotide biosynthesis in animals: genes, enzymes, and regulation of UMP biosynthesis". Annual Review of Biochemistry. 49 (1): 253–79. doi:10.1146/annurev.bi.49.070180.001345. PMID 6105839.
- ↑ McMurry JE, Begley TP (2005). The organic chemistry of biological pathways. Roberts & Company. ISBN 978-0-9747077-1-6.
