โรคอัลไซเมอร์
| โรคอัลไซเมอร์ (Alzheimer's disease) | |
|---|---|
 | |
| แผนภาพเปรียบเทียบระหว่างสมองของผู้สูงอายุปกติ (ซ้าย) และสมองผู้ป่วยโรคอัลไซเมอร์ (ขวา) มีการชี้แสดงลักษณะที่แยกระหว่างทั้งสอง | |
| สาขาวิชา | ประสาทวิทยา |
| อาการ | จำเหตุการณ์ปัจจุบันได้ยาก มีปัญหาด้านภาษา งุนงงสับสน อารมณ์แกว่ง[1][2] |
| การตั้งต้น | 65 ปีขึ้นไป[3] |
| ระยะดำเนินโรค | ระยะยาว[2] |
| สาเหตุ | ยังเข้าใจไม่มากนัก[1] |
| ปัจจัยเสี่ยง | พันธุกรรม ได้รับบาดเจ็บที่ศีรษะ โรคซึมเศร้า ความดันโลหิตสูง[1][4] |
| วิธีวินิจฉัย | ยึดอาการและการทดสอบการรู้หลังแยกสาเหตุอื่นที่เป็นไปได้[5] |
| โรคอื่นที่คล้ายกัน | การเปลี่ยนตามวัยปกติ[1] |
| ยา | สารยับยั้งอะเซทิลโคลีนเอสเตอเรส, สารต้านตัวรับเอ็นเอ็มดีเอ (มีประโยชน์เล็กน้อย)[6] |
| พยากรณ์โรค | อายุคาดหมายคงชีพ 3–9 ปี[7] |
| ความชุก | 29.8 ล้านคน (ปี 2558)[2][8] |
| การเสียชีวิต | 1.9 ล้านคน (ปี 2558)[9] |
โรคอัลซไฮเมอร์[10] หรือ โรคอัลไซเมอร์[11] (อังกฤษ: Alzheimer's disease หรือ AD) เป็นโรคการเสื่อมของระบบประสาทเรื้อรังที่ปกติเริ่มต้นช้า ๆ และค่อย ๆ มีอาการหนักขึ้นตามเวลา[1][2] เป็นภาวะสมองเสื่อมที่พบได้บ่อยที่สุดคือประมาณ 60–70% อาการเริ่มแรกที่พบบ่อยที่สุดได้แก่ การจำเหตุการณ์ปัจจุบันไม่ค่อยได้[1] เมื่อโรคลุกลามมากขึ้น อาการอาจมีปัญหาเรื่องการใช้ภาษา ความงุนงงสับสน (รวมทั้งหลงทางง่าย) อารมณ์แกว่ง เสียแรงจูงใจ ไม่ดูแลตนเองและมีปัญหาพฤติกรรม[1][2] เมื่ออาการของบุคคลเสื่อมลง ผู้ป่วยมักปลีกตัวออกจากครอบครัวและสังคม การทำงานของร่างกายจะค่อย ๆ เสื่อมลงจนนำไปสู่การเสียชีวิตในที่สุด[12] แม้การลุกลามของโรคอาจมีความเร็วแตกต่างกันได้ แต่อายุคาดหมายการคงชีพตรงแบบหลังวินิจฉัยแล้วอยู่ที่ 3 ถึง 9 ปี[7][13]
ยังไม่ค่อยเข้าใจสาเหตุของโรคอัลไซเมอร์ดีนัก[1] ความเสี่ยงประมาณ 70% เชื่อว่าได้รับมาจากบิดามารดาของผู้ป่วยโดยปกติเกี่ยวข้องกับหลายยีน[4] ปัจจัยเสี่ยงอื่นได้แก่ประวัติได้รับบาดเจ็บที่ศีรษะ โรคซึมเศร้าและความดันโลหิตสูง[1] กระบวนการของโรคสัมพันธ์กับพลาก (plaque) และนิวโรไฟบริลลารีแทงเกิล (neurofibrillary tangle) ในสมอง[4] การวินิจฉัยที่เป็นไปได้อาศัยประวัติความเจ็บป่วยและการทดสอบการรู้ กับการถ่ายภาพทางการแพทย์และการตรวจเลือดเพื่อแยกสาเหตุที่เป็นไปได้อย่างอื่น[5] อาการเริ่มแรกมักเข้าใจผิดว่าเป็นการเปลี่ยนตามวัยปกติ[1] การวินิจฉัยแน่ชัดจำเป็นต้องตรวจเนื้อเยื่อสมอง[4] การออกกำลังกายและการฝึกสมอง ตลอดจนการเลี่ยงโรคอ้วนอาจลดความเสี่ยงของโรคอัลไซเมอร์ อย่างไรก็ดี หลักฐานสนับสนุนข้อแนะนำเหล่านี้ยังอ่อนอยู่[4][14] ไม่มียาหรืออาหารเสริมที่แสดงว่าลดความเสี่ยงของโรค[15]
ไม่มีการรักษาใดหยุดหรือชะลอการลุกลามของโรค แม้การรักษาบางอย่างอาจลดอาการได้ชั่วคราว[2] ผู้ป่วยจำเป็นต้องพึ่งพาขอความช่วยเหลือผู้ป่วยมากขึ้นเรื่อย ๆ และมักเป็นภาระแก่ผู้ดูแล[16] ความกดดันนี้อาจรวมถึงส่วนสังคม จิตวิทยา กายภาพและเศรษฐกิจ[16] โปรแกรมออกกำลังกายอาจเป็นประโยชน์เกี่ยวกับความสามารถในการประกอบกิจวัตรประจำวันและอาจสามารถปรับปรุงผลลัพธ์ของโรคได้[17] ปัญหาพฤติกรรมหรือโรคจิตเนื่องจากภาวะสมองเสื่อมมักรักษาด้วยยารักษาโรคจิต แต่ปกติไม่แนะนำ เพราะมีประโยชน์น้อยและเพิ่มความเสี่ยงต่อการเสียชีวิตก่อนวัย[18][19]
ในปี 2558 มีผู้ป่วยโรคอัลไซเมอร์ประมาณ 29.8 ล้านคนทั่วโลก[2][8] มักเริ่มในผู้มีอายุตั้งแต่ 65 ปีขึ้นไป แม้ผู้ป่วย 4–5% เป็นโรคอัลไซเมอร์เป็นเร็ว (early-onset Alzheimer's)[3] โรคนี้เกิดในผู้มีอายุตั้งแต่ 65 ปีขึ้นไปประมาณ 6% ในปี 2558 โรคอัลไซเมอร์เป็นสาเหตุของการเสียชีวิต 1.9 ล้านครั้ง[9] จิตแพทย์และนักพยาธิวิทยาชาวเยอรมัน อาลัวส์ อัลซ์ไฮเมอร์ เป็นผู้ค้นพบโรคดังกล่าวในปี 2449 และโรคนี้ได้ชื่อตามเขา ในประเทศพัฒนาแล้ว โรคอัลไซเมอร์เป็นโรคที่มีมูลค่าทางการเงินสูงสุดโรคหนึ่ง[20][21]
อาการ[แก้]
- ผลของการเปลี่ยนตามวัยต่อความจำ (ไม่ใช่ AD)
- หลงลืมบ้างเป็นครั้งคราว
- วางสิ่งของผิดที่บางครั้ง
- เสียความจำระยะสั้นเล็กน้อย
- จำรายละเอียดแน่ชัดไม่ได้
- อัลไซเมอร์ระยะแรก
- จำไม่ได้ว่าลืมเป็นคราว ๆ
- ลืมชื่อของครอบครัวหรือมิตรสหาย
- เพื่อนหรือญาติใกล้ชิตอาจสังเกตการเปลี่ยนแปลงได้
- สับสนบ้างในสถานการณ์ที่ไม่ค่อยคุ้นเคย
- อัลไซเมอร์ระยะกลาง
- จำสารสนเทศที่เพิ่งเรียนรู้ยากยิ่งขึ้น
- สับสนเพิ่มขึ้นในหลายสถานการณ์
- มีปัญหาการหลับ
- มีปัญหาในการระบุตำแหน่งของตนเอง
- อัลไซเมอร์ระยะท้าย
- มีความสามารถในการคิดต่ำ
- พูดลำบาก
- สนทนาแบบเดิมซ้ำ
- ก้าวร้าว กระวนกระวายหรือหวาดระแวงมากขึ้น
การดำเนินโรคอัลไซเมอร์แบ่งออกเป็น 4 ระยะ โดยมีแบบรูปความเสื่อมของการรู้และหน้าที่แบบลุกลาม
ระยะก่อนสมองเสื่อม[แก้]
อาการแรกสุดมักเข้าใจผิดว่าเกิดขึ้นเองจากการเปลี่ยนตามวัย หรือเกิดจากภาวะเครียด[23] การทดสอบทางจิตประสาทวิทยาอย่างละเอียดอาจแสดงความบกพร่องทางการรู้เล็กน้อย ซึ่งอาจพบได้ 8 ปีก่อนผู้ป่วยครบตามเกณฑ์ทางคลินิกสำหรับการวินิจฉัยโรคอัลไซเมอร์[24] อาการเริ่มแรกจะมีผลกระทบต่อความสามารถในกิจวัตรประจำวันที่ซับซ้อนส่วนใหญ่[25] ความบกพร่องที่เห็นชัดมากที่สุดคือการเสียความจำระยะสั้น ซึ่งปรากฏเป็นการจำข้อเท็จจริงที่เพิ่งรู้มาหมาด ๆ ได้ยาก และไม่สามารถรับสารสนเทศใหม่ได้[26][27]
ปัญหาที่ตรวจจับได้ยากเกี่ยวกับหน้าที่การบริหารจัดการ อาทิความใส่ใจ, การวางแผน, ความยืดหยุ่น และความคิดเชิงนามธรรม หรือความบกพร่องของความจำเชิงอรรถศาสตร์ (การจำความหมายและความสัมพันธ์เชิงแนวคิด) อาจปรากฏอาการได้ในโรคอัลไซเมอร์ระยะแรก[28][29] อาจพบภาวะไร้อารมณ์ได้ในระยะนี้และจะเป็นอาการทางจิตประสาทที่คงอยู่มากที่สุดตลอดระยะการดำเนินโรค[30][31][32] อาการโรคซึมเศร้า ความหงุดหงิดและการรับรู้ความลำบากในการจำที่ตรวจจับได้ยากก็พบได้บ่อย ระยะก่อนคลินิกของโรคยังเรียกอีกอย่างว่า "ความบกพร่องทางการรู้เล็กน้อย" (MCI)[33] ซักมักพบว่าเป็นระยะเปลี่ยนผ่านระหว่างการเปลี่ยนตามวัยปกติกับภาวะสมองเสื่อม MCI อาจปรากฏอาการได้หลากหลาย และเมื่อการเสียความจำเป็นอาการเด่น จึงเรียกว่า "MCI ความจำเสื่อม" และมักพบว่าเป็นระยะบอกล่วงหน้าโรคอัลไซเมอร์[34]
สมองเสื่อมระยะแรก[แก้]
ผู้ป่วยโรคอัลไซเมอร์จะมีความบกพร่องของความจำและการเรียนรู้มากขึ้นเรื่อย ๆ จนสามารถวินิจฉัยอย่างแน่นอนได้ ผู้ป่วยจำนวนน้อยมีอาการบกพร่องทางภาษา หน้าที่การบริหาร การกำหนดรู้ (ภาวะเสียการระลึกรู้) หรือภาวะเสียการรู้ปฏิบัติเด่นกว่าปัญหาด้านความจำ[35] โรคอัลไซเมอร์ไม่มีผลกระทบต่อความสามารถด้านความจำทั้งหมดเท่า ๆ กัน โดยความทรงจำระยะยาวของชีวิตผู้ป่วย (ความจำเชิงเหตุการณ์) ข้อเท็จจริงที่เรียนมา (ความจำเชิงอรรถศาสตร์) และความจำโดยปริยาย (implicit memory) คือ ความจำของร่างกายว่าทำสิ่งต่าง ๆ อย่างไร เช่น การใช้ช้อนส้อมรับประทานอาหาร) ล้วนได้รับผลกระทบน้อยกว่าความจำหรือความรู้ใหม่[36][37]
ปัญหาทางภาษามีลักษณะเด่นคือการรวบคำให้สั้นและพูดหรือใช้ศัพท์ไม่ฉะฉานเหมือนเดิม ซึ่งทำให้ใช้ภาษาพูดหรือเขียนน้อยลง ในระยะนี้ปกติผู้ป่วยโรคอัลไซเมอร์ยังสามารถสื่อสารความคิดพื้นฐานได้เพียงพอ[38][39][40] เมื่อผู้ป่วยมีการกล้ามเนื้อมัดเล็ก เช่น การเขียน วาดภาพ หรือแต่งกาย อาจพบความบกพร่องของการประสานการเคลื่อนไหวและการวางแผน (ภาวะเสียการรู้ปฏิบัติ) บ้าง แต่โดยทั่วไปยังจับไม่ได้[41] เมื่อโรคดำเนินต่อไปผู้ป่วยโรคอัลไซเมอร์มักสามารถทำงานหลายอย่างได้ด้วยตัวเองแต่อาจต้องได้รับการช่วยเหลือหรือการกำกับสำหรับกิจกรรมที่ต้องอาศัยกระบวนการรู้อย่างมาก[35]
สมองเสื่อมระยะปานกลาง[แก้]
ในระยะนี้สมองจะเสื่อมลงเรื่อย ๆ จนสุดท้ายไม่สามารถพึ่งตนเองได้ โดยไม่สามารถประกอบกิจวัตรประจำวันส่วนใหญ่ได้[35] อาการพูดลำบากจะชัดเจนเพราะไม่สามารถนึกคำศัพท์ได้ ทำให้ใช้ศัพท์ผิดหรือใช้คำอื่นมาแทน (paraphasia) บ่อย ผู้ป่วยค่อย ๆ เสียทักษะการอ่านและการเขียนมากขึ้น[38][42] ลำดับการเคลื่อนไหวที่ซับซ้อนจะมีการประสานงานลดลงเรื่อย ๆ ตามการลุกลามของโรคอัลไซเมอร์ ทำให้ความเสี่ยงต่อการหกล้มเพิ่มขึ้นไปด้วย[43] ในระยะนี้ปัญหาความจำของผู้ป่วยจะเลวลง และผู้ป่วยอาจจำไม่ได้แม้แต่ญาติสนิทของตนเอง[44] ความทรงจำระยะยาวซึ่งแต่เดิมยังปกติอยู่ ก็บกพร่อง[45]
การเปลี่ยนแปลงพฤติกรรมและจิตประสาทวิทยาพบมากขึ้น อาการแสดงทั่วไปได้แก่ การหนีออกจากบ้าน ความหงุดหงิดและไม่ล่องตัว ทำให้ร้องไห้ มีความก้าวร้าวอย่างไม่คาดคิดฉับพลัน หรือดื้อกับผู้ดูแล อาการสับสนหรือเห็นภาพหลอนในเวลากลางคืน (sundowning) ก็มีได้[46] ผู้ป่วยโรคอัลไซเมอร์ประมาณ 30% มีอาการเชื่อว่าบุคคล สิ่งของ หรือสถานที่เปลี่ยนแปลงไป (เรียกว่า Delusional misidentification syndrome) และอาจมีอาการหลงผิดอย่างอื่น[47] ผู้ป่วยอาจเสียวิจารณญาณต่อกระบวนการและข้อจำกัดของโรค (ภาวะเสียสำนึกความพิการ) อาจกลั้นปัสสาวะไม่ได้[48] อาการเหล่านี้ทำให้เกิดความเครียดต่อผู้ดูแลและญาติ ซึ่งอาจลดความเครียดดังกล่าวโดยการย้ายผู้ป่วยจากบ้านไปยังถานดูแลระยะยาวอื่น[35][49]
สมองเสื่อมระยะสุดท้าย[แก้]
ในระยะสุดท้าย ผู้ป่วยต้องพึ่งพาผู้ดูแลตลอดเวลา ทักษะทางภาษาของผู้ป่วยลดลงเหลือวลีง่าย ๆ หรือคำเดี่ยว ๆ จนสุดท้ายไม่สามารถพูดได้โดยสิ้นเชิง[38] แม้ว่าผู้ป่วยเสียความสามารถด้านภาษาพูด แต่ยังมักเข้าใจและตอบสนองกลับมาด้วยการแสดงอารมณ์[50] แม้ผู้ป่วยยังมีลักษณะก้าวร้าว แต่ภาวะไร้อารมณ์สุดขั้วและอ่อนเพลียเป็นอาการที่พบมากกว่า[35] ในที่สุดผู้ป่วยจะไม่สามารถทำกิจกรรมใดได้เลยแม้เป็นกิจกรรมง่ายที่สุดหากขาดผู้ช่วยเหลือ มวลกล้ามเนื้อและการเคลื่อนไหวร่างกายลดลงจนผู้ป่วยติดเตียง[51] และไม่สามารถป้อนอาหารด้วยตนเองได้[52] ปกติสาเหตุการเสียชีวิตเป็นปัจจัยภายนอก เช่น แผลกดทับติดเชื้อหรือโรคปอดบวม ไม่ใช่เสียชีวิตจากโรคอัลไซเมอร์โดยตรง[53][54]
สาเหตุ[แก้]
ยังไม่ทราบสาเหตุของผู้ป่วยโรคอัลไซเมอร์ส่วนใหญ่ ยกเว้นผู้ป่วย 1% ถึง 5% ที่สามารถระบุข้อแตกต่างทางพันธุกรรมได้[55][56] มีสมมติฐานหลายอย่างเพื่อพยายามอธิบายสาเหตุของโรค
พันธุศาสตร์[แก้]
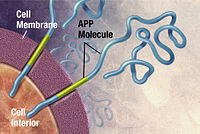
โรคอัลไซเมอร์ (และส่วนประกอบความจำจากโรค) ถ่ายทอดทางพันธุกรรมได้ในช่วง 49% ถึง 79%[57] โดยอาศัยการทบทวนการศึกษาฝาแฝดและครอบครัว ผู้ป่วยประมาณ 0.1% มีรูปแบบทายกรรมลักษณะเด่นในวงศ์ตระกูล ซึ่งมีอายุเริ่มต้นก่อนอายุ 65 ปี[58] โรคอัลไซเมอร์แบบนี้เรียก โรคอัลไซเมอร์ในวงศ์ตระกูลเกิดเร็ว โรคอัลไซเมอร์เกิดเร็วส่วนใหญ่ระบุสาเหตุได้ว่าเกิดจากการกลายพันธุ์ยีนตัวหนึ่งในบรรดาสามตัว คือ ยีนเข้ารหัสโปรตีนสารตั้งต้นแอมีลอยด์ (APP) และพรีเซนิลิน 1 และ 2[59] การกลายพันธุ์ของยีน APP และพรีเซนิลินเพิ่มการผลิตโปรตีนขนาดเล็ก ชื่อ เอบีตา42 (Aβ42) ซึ่งเป็นองค์ประกอบหลักในซีไนล์พลาก (senile plaque)[60] การกลายพันธุ์บางอย่างเพียงแต่เปลี่ยนแปลงอัตราส่วนระหว่าง Aβ42 และโปรตีนแบบสำคัญอย่างอื่น โดยเฉพาะเอบีตา40 (Aβ40) เท่านั้นโดยไม่เพิ่มระดับ Aβ42[61] อีกสองยีนที่สัมพันธ์กับโรคอัลไซเมอร์ทายกรรมลักษณะเด่น ได้แก่ ABCA7 และ SORL1[62]
ผู้ป่วยโรคอัลไซเมอร์ส่วนใหญ่ไม่ได้แสดงทายกรรมลักษณะเด่น และเรียกว่า อัลไซเมอร์เกิดห่าง ๆ (sporadic AD) ซึ่งความแตกต่างทางสิ่งแวดล้อมและพันธุกรรมอาจเป็นปัจจัยเสี่ยง ปัจจัยเสี่ยงทางพันธุกรรมที่ทราบดีที่สุด คือ ทายกรรมแอลลีลเอปไซลอน4 ของอะโปไลโปโปรตีนอี (APOE)[63][64] ผู้ป่วยโรคอัลไซเมอร์ระหว่าง 40 ถึง 80% มีแอลลีล APOEε4 อย่างน้อยหนึ่งแอลลีล[64] แอลลีล APOEε เพิ่มความเสี่ยงของโรคสามเท่าในเฮเทอโรไซโกต และ 15 เท่าในโฮโมไซโกต[58] ผลของสิ่งแวดล้อมและตัวดัดแปรพันธุกรรมทำให้เกิดเพเนแทรนซ์ไม่สมบูรณ์ซึ่งเหมือนกับโรคในมนุษย์หลายชนิด ตัวอย่างเช่น ประชากรไนจีเรียมไแสดงความสัมพันธ์ระหว่างปริมาณ APOEε4 กับอุบัติการณ์หรืออายุเริ่มเป็นโรคอัลไซเมอร์ดังที่เห็นได้ในกลุ่มประชากรอื่น[65][66] ความพยายามแรก ๆ ในการคัดกรองยีนที่อาจเป็นสาเหตุ 400 ยีนเพื่อหาความสัมพันธ์กับ AD เกิดห่าง ๆ และเกิดช้า (LOAD) ได้ผลลัพธ์เล็กน้อย[58][59] การศึกษาความสัมพันธ์ทั้งจีโนมล่าสุดพบว่ามียีน 19 บริเวณที่ดูมีผลต่อความเสี่ยง[67] ยีนเหล่านี้ได้แก่ CASS4, CELF1, FERMT2, HLA-DRB5, INPP5D, MEF2C, NME8, PTK2B, SORL1, ZCWPW1, SlC24A4, CLU, PICALM, CR1, BIN1, MS4A, ABCA7, EPHA1, และ CD2AP[67]
แอลลีลในยีน TREM2 สัมพันธ์กับความเสี่ยงเกิดโรคอัลไซเมอร์ 3 ถึง 5 เท่า[68][69] กลไกการออกฤทธิ์ที่มีการเสนอคือการผันแปรบางอย่างของ TREM2 ในเซลล์เม็ดเลือดขาวในสมองไม่สามารถควบคุมปริมาณของบีตาแอมีลอยด์ได้ SNP จำนวนมากมีความสัมพันธ์กับการศึกษาในปี 2561 ที่เติม SNP 30 ชนิดเพื่อแยก AD ออกเป็น 6 หมวด ได้แก่ ความจำ ภาษา ภาพและปริภูมิ และหน้าที่บริหาร[70]
สมมติฐานโคลิเนอร์จิก[แก้]
สมมติฐานเก่าที่สุดซึ่งการรักษาด้วยยาปัจจุบันพบมากที่สุดยึดเป็นพื้นฐาน ได้แก่ สมมติฐานโคลิเนอร์จิก (cholinergic hypothesis) ซึ่งเสนอว่าโรคอัลไซเมอร์เกิดจากการสังเคราะห์สารสื่อประสาทชนิดแอซิทิลโคลีน (acetylcholine) ลดลง สมมติฐานดังกล่าวปัจจุบันไม่ได้รับการสนับสนุนอย่างกว้างขวางแล้ว เนื่องจากการให้ยาเพื่อรักษาการขาดแอซิทิลโคลีนโดยตรงไม่มีประสิทธิภาพในการรักษาโรคอัลไซเมอร์มากนัก[71]
สมมติฐานแอมีลอยด์[แก้]
ในปี 2534 มีการตั้งสมมติฐานแอมีลอยด์ (amyloid hypothesis) ซึ่งมีมูลบทว่าการสะสมของแอมีลอยด์บีตา (amyloid beta; Aβ) เป็นสาเหตุหลักของโรคอัลไซเมอร์[72][73] ข้อสนับสนุนมูลบทนี้มาากตำแหน่งของยีนสำหรับโปรตีนสารตั้งต้นแอมีลอยด์ (APP) บนโครโมโซมคู่ที่ 21 ร่วมกับข้อเท็จจริงว่าบุคคลที่มีแฝดสามของโครโมโซม 21 (กลุ่มอาการดาวน์) ซึ่งมีสำเนายีนเกินมาแทบทุกคนอย่างน้อยมีอาการแรกเริ่มของ AD เมื่ออายุย่าง 40 ปี[74][75] นอกจากนี้ ไอโซฟอร์มจำเพาะหนึ่งของแอโพไลโปโปรตีน APOE4 เป็นปัจจัยเสี่ยงทางพันธุกรรมสำคัญหนึ่งของ AD แม้แอโพไลโปโปรตีนช่วยเสริมการสลายแอมีลอยด์บีตา แต่บางไอโซฟอร์มไม่ค่อยมีประสิทธิภาพในการทำหน้าที่ดังก่าว (เช่น APOE4) นำไปสู่การสะสมแอมีลอยด์ส่วนเกินในสมอง[76] หลักฐานเพิ่มเติมมาจากข้อค้นพบว่าหนูดัดแปลงพันธุกรรมแสดงรูปกลายพันธุ์ของยีน APP ของมนุษย์ก่อให้เกิดพลากแอมีลอยด์แบบสั่นและพยาธิสภาพสมองแบบคล้ายอัลไซเมอร์โดยมีความบกพร่องของการเรียนรู้เชิงปริภูมิ[77]
พบว่าวัคซีนขั้นทดลองชนิดหนึ่งสามารถชำระพลากแอมีลอยด์ในการทดลองในมนุษย์ขั้นต้น แต่ไม่มีผลอย่างมีนัยสำคัญใด ๆ ต่อภาวะสมองเสื่อม นักวิจัยจึงสงสัยว่าโอลิโกเมอร์ Aβ ที่มิใช่พลากเป็น Aβ รูปก่อโรคมากที่สุด โอลิโกเมอร์พิษเหล่านี้ ซึ่งเรียกว่า ไลแกนด์ฤทธิ์สั้นที่ได้จากแอมีลอยด์ (amyloid-derived diffusible ligands) จับกับตัวรับบนผิวเซลล์ประสาทและเปลี่ยนโครงสร้างของจุดประสานประสาท จึงรบกวนการสื่อสารของเซลล์ประสาท ตัวรับโอลิโกเมอร์ Aβ ตัวหนึ่งอาจเป็นโปรตีนพรีออน ซึ่งเป็นเดียวกับโปรตีนที่มีความเชื่อมโยงกับโรควัวบ้าและโรคในมนุษย์ที่เกี่ยวข้อง โรคครอยตส์เฟลดต์-จาค็อบ ฉะนั้นจึงอาจเป็นการเชื่อมโยงกลไกพื้นเดิมของโรคการเสื่อมของระบบประสาทเหล่านี้กับโรคอัลไซเมอร์[78]
ในปี 2552 มีการปรับทฤษฎี โดยเสนอว่าโปรตีนที่สัมพันธ์ใกล้ชิดกับโปรตีนบีตา-แอมีลอยด์ ซึ่งไม่จำเป็นต้องเป็นบีตา-แอมีลอยด์เอง อาจเป็นสาเหตุสำคัญของโรคอัลไซเมอร์ ทฤษฎีนี้เชื่อว่ากลไกที่สัมพันธ์กับแอมีลอยด์ซึ่งตัดการประสานของเซลล์ประสาทในสมองในระยะเติบโตเร็วในปฐมวัยอาจเกิดจากกระบวนการที่สัมพันธ์กับการเปลี่ยนตามวัยในชีวิตภายหลัง ทำให้เกิดความเสื่อมของเซลล์ประสาทในโรคอัลไซเมอร์[79] N-APP ซึ่งเป็นชิ้นส่วนหนึ่งจากปลายเอ็น (N-terminus) ของ APP อยู่ติดกับแอมีลอยด์บีตา และหนึ่งในเอ็นไซม์ชนิดเดียวกันนี้ตัดออกจาก APP; N-APP กระตุ้นวิถีการทำลายตัวเองโดยการจับกับตัวรับของเซลล์ประสาทเรียก ตัวรับมรณะ 6 (DR 6 หรือ TNFRSF21);[79] DR6 มีการแสดงออกสูงในบริเวณสมองของมนุษย์ที่ได้รับผลจากโรคอัลไซเมอร์มากที่สุด ฉะนั้นเป็นไปได้ที่วิถี N-APP/DR6 อาจถูกควบคุมในสมองวัยชราทำให้เกิดความเสียหาย ในแบบจำลองนี้ แอมีลอยด์บีตามีบทบาทส่งเสริมโดยการกดการทำหน้าที่ของจุดประสานประสาท
ต้นปี 2560 การทดลองเวอรูเบเซสแตด (verubecestat) ซึ่งยับยั้งโปรตีนบีตา-ซีครีเตส (beta-secretase) อันเป็นสาเหตุของการสร้างโปรตีนแอมีลอยด์บีตา ถูกระงับเนื่องจากคณะกรรมการอิสระพบว่า "แทบไม่มีโอกาสใด ๆ ในการค้นพบฤทธิ์ทางคลินิกเชิงบวก"[80] ในปี 2561 และ 2562 การทดลองอื่น รวมทั้งอะดูแคนูแมบซึ่ลดความเข้มข้นของแอมีลอยด์บีตาล้มเหลว ทำให้บางคนตั้งคำถามว่าสมมติฐานแอมีลอยด์ยังสมเหตุสมผลอยู่หรือไม่[81][82]
สมมติฐานเทา[แก้]

สมมติฐานเทาเสนอว่าความผิดปกติของโปรตีนเป็นการเริ่มลำดับของโรค[73] ในแบบจำลองนี้ เทาที่มีการเติมหมู่ฟอสเฟตมากเกิน (hyperphosphorylated tau) เริ่มจับคู่กับเทาสายอื่น จนสุดท้ายก่อเป็นนิวโรไฟบริลลารีแทงเกิล (neurofibrillary tangle) ภายในตัวเซลล์ประสาท[83] ไมโครทิวบูลจะสลายตัว เกิดการทำลายโครงสร้างไซโทสเกเลตอนของเซลล์แล้วทำให้ระบบขนส่งของเซลล์ประสาทไม่ทำงานด้วย[84] การไม่ทำงานของระบบขนส่งนี้อาจทำให้การสื่อสารทางชีวเคมีระหว่างเซลล์ประสททำหน้าที่ผิดปกติก่อน แล้วทำให้เซลล์ตายตามมา[85]
สมมติฐานอื่น[แก้]
มีการเสนอสมมติฐานระบบประสาทและหลอดเลือดซึ่งระบุว่าอาจเกี่ยวข้องกับการทำหน้าที่อย่างเลวของตัวกั้นระหว่างเลือดกับสมอง[86] นอกจากนี้ การติดเชื้อแบคทีเรียรูปเกลียว (spirochete) ยังมีความเชื่อมโยงกับภาวะสมองเสื่อม[87][88]
ภาวะธำรงดุลของโลหะชีวภาพอย่างไอออนทองแดง เหล็กและสังกะสีใน AD เสียไป แม้ยังไม่ชัดเจนว่าภาวะดังกล่าวเป็นเหตุหรือผลของการเปลี่ยนแปลงโปรตีน ไอออนเหล่านี้ทั้งมีผลกระทบต่อและได้รับผลกระทบจากเทา APP และ APOE[89] และการเสียการกำกับโปรตีนเหล่านี้อาจก่อให้เกิดความเครียดออกซิเจนซึ่งอาจส่งเสริมให้เกิดพยาธิสภาพ[90][91][92][93][94] คุณภาพของการศึกษาเหล่านี้บางครั้งตกเป็นที่วิจารณ์[95][96] และความเชื่อมโยงนี้ยังเป็นที่ถกเถียงกันอยู่[97] นักวิจัยส่วนใหญ่ไม่สนับสนุนความสัมพันธ์เชิงเหตุผลกับอะลูมิเนียม[96]
การสูบบุหรี่เป็นปัจจัยเสี่ยงที่สำคัญของ AD[98] มาร์กเกอร์ทั่วกายสำหรับระบบภูมิคุ้มกันสืบทอดเป็นปัจจัยเสี่ยงของ AD ที่เกิดช้า[99] มีหลักฐานเบื้อต้นว่าการสัมผัสกับมลภาวะทางอากาศอาจเป็นปัจจัยส่งเสริมต่อการเกิดโรคอัลไซเมอร์[100]
สมมติฐานหนึ่งว่าการเสียหน้าที่ของโอลิโกเดนโดรไซต์และไมอีลีนที่สัมพันธ์กับพวกมันระหว่างการเปลี่ยนตามวัยเอื้อต่อความเสียหายต่อแกนประสาทนำเข้า ซึ่งจะทำให้เกิการผลิตแอมีลอยด์และการเติมหมู่ฟอสเฟตมากเกินของเทาเป็นผลข้างเคียง[101][102]
รีโทรเจนะซิส (retrogenesis) เป็นสมมติฐานเกี่ยวกับการพัฒนาและการลุกลามของโรคอัลไซเมอร์ที่แบร์รี ไรซ์เบิร์ก (Barry Reisberg) เป็นผู้เสนอในคริสต์ทศวรรษ 1980[103] สมมติฐานคือขณะที่ทารกในครรภ์ผ่านกระบวนการเจริญของประสาทนิวรูเลชัน (neurulation) แล้วสิ้นสุดด้วยไมอีลินเนชัน (myelination) สมองของผู้ป่วย AD ผ่านกระบวนการเสื่อมของประสาทแบบย้อนกลับเริ่มต้นจากการสลายไมอีลีนและการตายของแกนประสาทนำเข้า (เนื้อขาว) จนสิ้นสุดด้วยการตายของเนื้อเทา[104] สมมติฐานยังว่า ทารกผ่านขั้นพัฒนาการของการรู้ ผู้ป่วย AD ผ่านกระบวนการย้อนกลับการเสื่อมของการรู้แบบก้าวหน้า[103] ไรซ์เบิร์กพัฒนาเครื่องมือการประเมินการดูแลที่เรียก "FAST" (เครื่องมือการจัดระยะการประเมินเชิงหน้าที่) ซึ่งเขาว่าทำให้ผู้ดูแลผู้ปว่ย AD สามารถบอกระยะการลุกลามของโรคและให้คำแนะนำเกี่ยวกับการดูแลชนิดที่จำเป็นในแต่ละระยะได้[103][105]
พยาธิสรีรวิทยา[แก้]

ประสาทพยาธิสภาพ[แก้]
ลักษณะที่พบในโรคอัลไซเมอร์คือการสูญเสียเซลล์ประสาทและจุดประสานประสาทภายในเปลือกสมองและบริเวณใต้เปลือกสมอง ทำให้เกิดการฝ่อที่เห็นได้ของสมองบริเวณที่เป็นโรค ซึ่งรวมถึงการเสื่อมของสมองกลีบขมับ (temporal lobe) และสมองกลีบข้าง (parietal lobe) และส่วนหนึ่งของสมองกลีบหน้า (frontal cortex) และรอยนูนซิงกูเลต (cingulate gyrus) ของสมอง[106] นอกจากนี้ยังปรากฏความเสื่อมในนิวเคลียสก้านสมอง เช่น โลคัสซีรูเลียส (locus coeruleus)[107] การศึกษาโดยใช้เอ็มอาร์ไอและเพ็ตบันทึกการลดขนาดของสมองบางบริเวณในผู้ป่วยโรคอัลไซเมอร์เมื่อผู้ป่วยมีการลุกลามจากการบกพร่องของการู้เล็กน้อยจนถึงโรคอัลไซเมอร์ เมื่อเทียบกับภาพคล้ายกันจากผู้ใหญ่สูงอายุกว่าที่มีสุขภาพดี[108][109]
พลากแอมีลอยด์และนิวโรไฟบริลลารีแทงเกิล (neurofibrillary tangle) เห็นได้ชัดเจนด้วยกล้องจุลทรรศน์ในสมองผู้ป่วยโรคอัลไซเมอร์[110] พลากมีลักษณะเป็นการสะสมของเพพไทด์แอมีลอยด์บีตาและสารองค์ประกอบของเซลล์ที่หนาแน่นและมักเป็นตะกอนอยู่ภายนอกและรอบ ๆ เซลล์ประสาท ส่วนนิวโรไฟบริลลารีแทงเกิลเกิดจากการรวมกลุ่มสะสมของโปรตีนที่เกี่ยวข้องกับไมโครทิวบูล ชื่อว่า โปรตีนเทา (tau protein) ซึ่งมีการเติมหมู่ฟอสเฟตมากผิดปกติ และสะสมอยู่ภายในเซลล์ประสาท แม้ว่าสมองของผู้สูงอายุหลายคนอาจพบพลากและแทงเกิลในสมองได้บ้างเนื่องจากความชราแต่สมองของผู้ป่วยโรคอัลไซเมอร์จะพบปริมาณคราบดังกล่าวมากกว่าในสมองบางบริเวณ เช่น บริเวณสมองกลีบขมับ[111] ส่วนลิวอีบอดี (Lewy body) ก็พบได้ไม่น้อยในสมองผู้ป่วยโรคอัลไซเมอร์[112]
ชีวเคมี[แก้]
โรคอัลไซเมอร์จัดเป็นโรคโปรตีนม้วนพับผิดปกติ (protein misfolding disease) ที่เกิดจากการะสะสมพลากของโปรตีนแอมีลอยด์บีตาและโปรตีนเทาที่ม้วนพับผิดปกติในสมอง[113] พลากเกิดจากเพปไทด์ขนาดเล็กยาวประมาณ 39–43 กรดอะมิโน ชื่อว่าแอมีลอยด์บีตา (Aβ) โดย Aβ เป็นชิ้นส่วนหนึ่งของโปรตีนสารตั้งต้นแอมีลอยด์ (APP) โปรตีนนี้เป็นทรานสเมมเบรนโปรตีน (transmembrane protein) ที่แทรกทะลุผ่านเยื่อหุ้มเซลล์ประสาท APP มีความจำเป็นต่อการเจริญเติบโต การดำรงชีวิต และการซ่อมแซมหลังได้รับบาดเจ็บของเซลล์ประสาท[114][115] ในโรคอัลไซเมอร์ แกมมาซีครีเตสและบีตาซีครีเตสทำงานร่วมกันในกระบวนการการสลายโปรตีนซึ่งตัดแบ่ง APP ออกเป็นชิ้นส่วนเล็ก ๆ[116] ชิ้นส่วนชิ้นหนึ่งที่เกิดขึ้นจะกลายเป็นเส้นใยแอมีลอยด์บีตา ซึ่งจับตัวเป็นก้อนตกตะกอนหนาแน่นอยู่นอกเซลล์ประสาท เรียกว่า ซีไนล์พลาก (senile plaque)[110][117]
โรคอัลไซเมอร์ยังถือว่าเป็นความผิดปกติของโปรตีนเทา (tauopathy) เนื่องจากการสะสมโปรตีนเทาอย่างผิดปกติ เซลล์ประสาททุกเซลล์จะมีโครงร่างของเซลล์ (cytoskeleton) ซึ่งบางส่วนเกิดจากโครงสร้างที่เรียก ไมโครทิวบูล (microtubule) ไมโครทิวบูลนี้ทำหน้าที่เสมือนรางรถไฟคือเป็นเส้นทางลำเลียงสารอาหารและโมเลกุลจากตัวเซลล์ไปยังปลายแกนประสาทนำออก (axon) และนำกลับ โปรตีนที่ชื่อว่า เทา (tau; Τ) ทำหน้าที่ช่วยให้ไมโครทิวบูลเสถียรหลังเกิดปฏิกิริยาฟอสโฟรีเลชัน จึงเรียกโปรตีนเทาว่าเป็น โปรตีนที่สัมพันธ์กับไมโครทิวบูล (MAP) ในผู้ป่วยอัลไซเมอร์ โปรตีนเทาจะเกิดการเปลี่ยนแปลงทางเคมี คือมีปฏิกิริยาฟอสโฟรีเลชั่นมากกว่าปกติ ทำให้โปรตีนจับคู่กันเกิดเป็น นิวโรไฟบริลลารีแทงเกิล (neurofibrillary tangle) และรบกวนระบบการขนส่งของเซลล์ประสาท[118] โปรตีนเทาที่มีพยาธิสภาพสามารถทำให้เซลล์ประสาทตายได้จากการเสียการกำกับแทรนส์โพเซเบิลเอลิมันต์ (transposable element)[119]
กลไกการเกิดโรค[แก้]
ยังไม่ทราบว่าการผลิตและการสะสมเพปไทด์แอมีลอยด์ทำให้เกิดพยาธิสภาพของโรคอัลไซเมอร์ได้อย่างไรแน่ชัด[120] สมมติฐานแอมีลอยด์แต่เดิมชี้ว่าการสะสมเพปไทด์แอมีลอยด์เป็นเหตุการณ์ศูนย์กลางที่กระตุ้นให้เกิดความเสื่อมของเซลล์ประสาท การสะสมของกลุ่มเส้นใยแอมีลอยด์ซึ่งเชื่อว่าแอมิลอยด์แบบเป็นพิษที่ทำให้รบกวนภาวะธำรงดุลของไอออนแคลเซียมของเซลล์ ชักนำให้เกิดการตายของเซลล์ที่ตั้งโปรแกรมไว้หรืออะพอพโทซิส (apoptosis)[121] นอกจากนี้ยังเป็นที่ทราบกันว่า Aβ เกิดขึ้นอย่างจำเพาะภายในไมโทคอนเดรียในเซลล์ที่เป็นโรคอัลไซเมอร์ ซึ่งไปยับยั้งการทำงานของเอนไซม์บางตัวและการใช้กลูโคสของเซลล์ประสาท[122]
กระบวนการอักเสบและไซโตไคน์ต่าง ๆ อาจมีบทบาทในพยาธิสภาพของโรคอัลไซเมอร์ด้วย การอักเสบเป็นสารส่อทั่วไปของความเสียหายต่อเนื้อเยื่อในโรคต่าง ๆ และอาจเป็นผลจากความเสียหายต่อเนื้อเยื่อในโรคอัลไซเมอร์หรือเป็นสารส่อของการตอบสนองทางภูมิคุ้มกัน[123] มีหลักฐานอันตรกิริยาอย่างเข้มระหว่างเซลล์ประสาทกับกลไกภูมิคุ้มกันในสมองเพิ่มขึ้น โรคอ้วนและการอักเสบทั่วร่างอาจรบกวนกระบวนการภูมิคุ้มกันซึ่งส่งเสริมการลุกลามของอัลไซเมอร์[124]
นอกจากนี้ยังมีการอธิบายการเปลี่ยนแปลงการกระจายของแฟกเตอร์บำรุงสมองต่าง ๆ และการแสดงตัวรับของแฟกเตอร์เหล่านี้อย่าง brain-derived neurotrophic factor (BDNF) ในโรคอัลไซเมอร์ด้วย[125][126]
การวินิจฉัย[แก้]

การวินิจฉัยโรคอัลไซเมอร์อาศัยประวัติของผู้ป่วย ประวัติที่ได้จากญาติ และการสังเกตพฤติกรรม หากมีลักษณเฉพาะทางประสาทวิทยาและจิตประสาทวิทยาและคัดภาวะอื่นออกไปแล้วเป็นการสนับสนุนการวินิจฉัย[127][128] การศึกษาจากภาพทางรังสีวิทยาเพิ่มเติมด้วยการถ่ายภาพรังสีส่วนตัดอาศัยคอมพิวเตอร์ (ซีที) หรือการสร้างภาพด้วยเรโซแนนซ์แม่เหล็ก (เอ็มอาร์ไอ) ร่วมกับเครื่องถ่ายภาพรังสีชนิดแกมมาหลายระนาบ (SPECT) หรือการถ่ายภาพรังสีระนาบด้วยการปล่อยโพซิตรอน (เพท) อาจช่วยในการคัดพยาธิสภาพทางสมองหรือชนิดย่อยของสมองเสื่อมอื่น ๆ ออกได้[129] ยิ่งไปกว่านั้น อาจช่วยพยากรณ์การเปลี่ยนจากขั้นบอกล่วงหน้าโรค (ความบกพร่องทางการรู้เล็กน้อย) เป็นโรคอัลไซเมอร์ได้[130]
การประเมินสติปัญญา เช่น การทดสอบความจำสามารถจำแนกระยะของโรคอัลไซเมอร์ได้[23] มีหน่วยงานทางการแพทย์หลายสถาบันสร้างเกณฑ์การวินิจฉัยสำหรับแพทย์เพื่อให้การวินิจฉัยโรคอัลไซเมอร์ได้ง่ายและเป็นมาตรฐานมากขึ้น บางครั้งสามารถยืนยันการวินิจฉัยหลังผู้ป่วยเสียชีวิตได้อย่างแม่นยำจากการศึกษาชิ้นส่วนสมองด้วยวิธีการศึกษาเนื้อเยื่อด้วยกล้องจุลทรรศน์[131]
เกณฑ์การวินิจฉัย[แก้]
สถาบันโรคทางประสาทและการสื่อสารและโรคหลอดเลือดสมองแห่งชาติ (National Institute of Neurological and Communicative Disorders and Stroke) และสมาคมโรคอัลไซเมอร์ (Alzheimer's Association)[a] ของสหรัฐสร้างเกณฑ์การวินิจฉัยโรคอัลไซเมอร์ที่เป็นที่นิยมใช้กันมากที่สุด คือ NINCDS-ADRDA Alzheimer's Criteria ในปี 2527[131] และมีการปรับปรุงอย่างกว้างขวางในปี 2550[132] เกณฑ์การวินิจฉัยดังกล่าวกำหนดให้ผู้ป่วยปรากฏความบกพร่องในการรู้และสงสัยเป็นกลุ่มอาการภาวะสมองเสื่อมต้องได้รับการตรวจยืนยันโดยการประเมินทางจิตประสาทวิทยาเพื่อวินิจฉัยทางคลินิกว่ามีโอกาส (possible) หรืออาจ (probable) เป็นโรคอัลไซเมอร์ ส่วนการวินิจฉัยแน่นอนได้แก่การตรวจยืนยันทางจุลพยาธิวิทยา คือการตรวจเนื้อเยื่อสมองทางจุลทรรศน์ พบว่าเกณฑ์การวินิจฉัยดังกล่าวมีความเชื่อถือได้และความสมเหตุสมผลดีเมื่อเทียบกับการวินิจฉัยยืนยันทางจุลพยาธิวิทยา[133] ในผู้ป่วยโรคอัลไซเมอร์มักพบความบกพร่องของในการรู้ 8 รูปแบบ ได้แก่ ด้านความจำ, ภาษา, ทักษะด้านความรู้สึก, ความใส่ใจ, ทักษะกล้ามเนื้อ, การรู้กาลเทศะและบุคคล, การแก้ปัญหา และความสามารถเชิงหน้าที่ รูปแบบการรู้ที่บกพร่องดังกล่าวเทียบเท่ากับเกณฑ์การวินิจฉัย NINCDS-ADRDA Alzheimer's Criteria ดังที่ระบุในเกณฑ์การวินิจฉัยโรคทางจิตเวช คู่มือการวินิจฉัยและสถิติสำหรับความผิดปกติทางจิต (DSM-IV-TR) ซึ่งตีพิมพ์โดยสมาคมจิตเวชศาสตร์อเมริกา[134][135]
เครื่องมือในการวินิจฉัย[แก้]

มีการใช้การทดสอบทางจิตประสาทวิทยาต่าง ๆ เช่น การตรวจสุขภาวะทางจิตแบบย่อ (mini-mental state examination; MMSE) อย่างกว้างขวางเพื่อประเมินความบกพร่องในการรู้เพื่อใช้วินิจฉัยโรค ส่วนชุดแบบทดสอบที่ละเอียดและครอบคลุมกว่านี้มีความจำเป็นสำหรับผลลัพธ์ที่มีความน่าเชื่อถือสูง โดยเฉพะาอย่างยิ่งในระยะแรก ๆ ของโรคอัลไซเมอร์[136][137] การตรวจทางประสาทวิทยาในผู้ป่วยโรคอัลไซเมอร์ระยะแรกโดยทั่วไปให้ผลปกติ ยกเว้นสำหรับการรู้เสื่อมอย่างชัดเจนเท่านั้น ซึ่งไม่ได้ต่างจากผลที่เกิดจากกระบวนการของโรคอื่น รวมทั้งภาวะความจำเสื่อมจากสาเหตุอื่น
การตรวจทางประสาทวิทยาเพิ่มเติมมีความสำคัญในการวินิจฉัยแยกโรคโรคอัลไซเมอร์และโรคอื่น ๆ[23] การซักประวัติจากสมาชิกในครอบครัวอาจช่วยในการประเมินโรค ผู้ดูแลผู้ป่วยอาจให้ข้อมูลที่สำคัญเกี่ยวกับความสามารถในการประกอบกิจวัตรชีวิตประจำวันของผู้ป่วย รวมทั้งความถดถอยของหน้าที่ทางจิตของผู้ป่วยตามเวลา[138] ความเห็นหรือมุมมองของผู้ดูแลมักมีความสำคัญในการวินิจฉัยหากผู้ป่วยโรคอัลไซเมอร์นั้นปกติไม่รับรู้ความเจ็บป่วยของตนเอง[139] หลายครั้งครอบครัวอาจพบอาการของภาวะสมองเสื่อมระยะแรกได้ยากตั้งแต่แรกและอาจสื่อสารข้อมูลที่ไม่ถูกต้องแม่นยำแก่แพทย์[140]
การทดสอบเพิ่มเติมให้ข้อมูลเพิ่มในบางลักษณะของโรคหรือใช้เพื่อคัดการวินิจฉัยอื่นออก การตรวจเลือดสามารถช่วยระบุสาเหตุอื่นของภาวะความจำเสื่อมที่ไม่ใช่โรคอัลไซเมอร์ได้[23] ซึ่งสาเหตุเหล่านี้มักพบได้น้อยแต่หายขาดได้[141] แพทย์ปกติตรวจการทำงานของไทรอยด์ ประเมินระดับวิตามินบี12 แยกโรคซิฟิลิส แยกปัญหาเมแทบอลิก (รวมทั้งการทดสอบการทำงานของไต ระดับอิเล็กโทรไลต์ และโรคเบาหวาน) ประเมินระดับโลหะหนัก (เช่น ตะกั่ว ปรอท) และภาวะโลหิตจาง และอาจจำเป็นต้องแยกอาการเพ้อ
การทดสอบทางจิตวิทยาสำหรับโรคซึมเศร้าอาจช่วยในการวินิจฉัยเพราะโรคซึมเศร้าสามารถเกิดร่วมกับโรคอัลไซเมอร์ หรือเป็นสาเหตุของความบกพร่องในการรู้[142][143]
ไม่แนะนำให้ใช้ C-PIB-PET สแกนเป็นเครื่องมือวินิจฉัยระยะแรกหรือใช้พยากรณ์การพัฒนาโรคอัลไซเมอร์เมื่อบุคคลปรากฏอาการแสดงของความบกพร่องทางการรู้เล็กน้อย (MCI)[144] เพราะมีความแม่นยำต่ำ หลักฐานไม่รองรับการใช้ ¹⁸F-FDG PET สแกนเป็นการทดสอบเดี่ยว ๆ เพื่อใช้ระบุบุคคลที่อาจเป็นโรคอัลไซเมอร์เช่นกัน[145]
การป้องกัน[แก้]

ไม่มีหลักฐานชี้ชัดสนับสนุนว่ามีวิธีหนึ่งวิธีใดที่สามารถป้องกันโรคอัลไซเมอร์ได้อย่างมีผล การศึกษาทั่วโลกว่าด้วยมาตรการป้องกันหรือชะลอการเกิดโรคอัลไซเมอร์มักให้ผลขัดแย้งกัน การศึกษาทางวิทยาการระบาดเสนอว่ามีความสัมพันธ์ระหว่างปัจจัยที่สามารถแก้ไขได้อย่างอย่าง เช่น อาหาร ความเสี่ยงของโรคหัวใจและหลอดเลือด ผลิตภัณฑ์เภสัชกรรม หรือกิจกรรมทางสติปัญญา เป็นต้น กับโอกาสเกิดโรคอัลไซเมอร์ในประชากร แต่ยังต้องมีการวิจัยตลอดจนการทดลองทางคลินิกเพิ่มเติมเพื่อหาคำตอบว่าปัจจัยเหล่านี้สามารถช่วยลดโรคอัลไซเมอร์ได้หรือไม่[15]
อาหาร[แก้]
บุคคลที่รับประทานอาหารสุขภาพดี หรืออาหารญี่ปุ่น หรืออาหารเมดิเตอร์เรเนียนมีควมเสี่ยงเกิดโรคอัลไซเมอร์ลดลง[146] อาหารเมดิเตอร์เรเนียนอาจช่วยปรับปรุงผลลัพธ์ของผู้ป่วยได้[147] ส่วนุคลที่รับประทานอาหารที่มีไขมันอิ่มตัวสูงและคาร์โบไฮเดรตอย่างง่าย (มอโนหรือไดแซ็กคาไรด์) มีความเสี่ยงสูงกว่า[148] มีการเสนอว่าประโยชน์ต่อระบบหัวใจและหลอดเลือดของอาหารเมดิเตอร์เรเนียนเป็นกลไกการออกฤทธิ์ลดโรคอัลไซเมอร์[149]
บางทีข้อสรุปต่อส่วนประกอบอาหารทำให้แน่ใจได้ยากเพราะผลแตกต่างกันระหว่างการศึกษาจากประชากรกับการทดลองแบบสุ่มที่มีการควบคุม มีหลักานจำกัดว่าการใช้แอลกอฮอล์ปริมาณน้อยถึงปานกลาง โดยเฉพาะอย่างยิ่งไวน์แดง มีความสัมพันธ์กับความเสี่ยงต่อโรคอัลไซเมอร์ที่ลดลง[146] มีหลักฐานเบื้องต้นว่าคาเฟอีนอาจช่วยป้องกัน[150] อาหารที่มีฟลาโวนอยด์สูงจำนวนหนึ่ง เช่น โกโก้ ไวน์แดงและชา อาจลดความเสี่ยงของโรคอัลไซเมอร์[151][152]
บทปฏิทัศน์เรื่องการใช้วิตามินและเกลือแร่ไม่พบว่ามีหลักฐานสอดคล้องกันในการแนะนำให้รับประทานวิตามินและเกลือแร่ ซึ่งรวมทั้งวิตามินเอ[153][154] ซี[155][156] รูปแอลฟาโทโคฟีรอลของวิตามินอี[157] เซเลเนียม[158] สังกะสี[159][160] และกรดโฟลิกทั้งที่มีหรือไม่มีวิตามินบี12[161] หลักฐานจากการศึกษาแบบสุ่มที่มีการควบคุมครั้งหนึ่งบ่งชี้ว่ารูปแอลฟาโทโคฟีรอลของวิตามินอีอาจชะลอการเสื่อมของการรู้ แต่มีการตัดสินว่าหลักฐานนี้มีคุณภาพ "ปานกลาง"[157] การทดลองที่พิจารณากรดโฟลิก (บี9) กับวิตามินบีอื่นไม่พบความสัมพันธ์อย่างมีนัยสำคัญกับการเสื่อมของการรู้ใด ๆ[162] อาหารเสริมกรดไขมันโอเมกา-3 จากพืชแสัตว์ และกรดโดโคซาเฮ็กซาอีโนอิก (DHA) ไม่ปรากฏว่ามีประโยชน์ในโรคอัลไซเมอร์ระดับอ่อนถึงปานกลาง[163][164]
สารเคอร์คิวมิน (curcumin) จากขมิ้นไม่พบประโยชน์ในมนุษย์แม้มีหลักฐานเบื้องต้นในสัตว์[165] ไม่มีหลักฐานสอดล้องกันและน่าเชื่อได้ว่าแปะก๊วยมีผลดีในการป้องกันความบกพร่องของการรู้และภาวะสมองเสื่อม[166] จนถึงปี 2551 ไม่มีหลักฐานรูปธรรมว่าแคนนาบินอยด์ (cannabinoids) มีผลช่วยลดอาการของโรคอัลไซเมอร์หรือภาวะสมองเสื่อม[167] อย่างไรก็ดี การวิจัยบางส่วนต่อเอ็นโดแคนนาบินอยด์ (endocannabinoids) ดูมีหวัง[168]
ยา[แก้]
แม้ว่าปัจจัยเสี่ยงด้านโรคหลอดเลือดหัวใจ เช่น ภาวะเลือดมีคอเลสเทอรอลมาก ความดันโลหิตสูง เบาหวาน และการสูบบุหรี่ จะเกี่ยวข้องกับโอกาสเสี่ยงเกิดที่สูงขึ้นและระยะเวลาการดำเนินโรคอัลไซเมอร์[169][170] แต่การใช้ยากลุ่มสแตตินซึ่งเป็นยาลดคอเลสเทอรอลไม่มีประสิทธิผลในการป้องกันหรือช่วยทำให้การดำเนินโรคอัลไซเมอร์ดีขึ้น[171][172]
ในปี 2550 คาดกันว่าการใช้ยากลุ่มยาแก้อักเสบชนิดไม่ใช่สเตรอยด์ (NSAIDs) เช่น แอสไพริน ไอบูโปรเฟน ในระยะยาวช่วยลดโอกาสเกิดโรคอัลไซเมอร์ได้บ้าง[173] หลักฐานเสนอว่า NSAIDs อาจลดการอักเสบที่เกี่ยวข้องกับแอมีลอยด์พลาก แต่การทดลองถูกระงับเพราะมีผลเสียสูง[15] ไม่มีการทดลองเพื่อป้องกันโรคใดสำเร็จเลย[15] จนถึงปี 2554 มีการเสนอยาบางชนิดเป็นสารป้องกันก่อนเกิดอาการ แต่ดูมีประโยชน์ไม่เท่ากับการรักษา[174] ฮอร์โมนทดแทนในสตรีหมดประจำเดือนซึ่งเคยใช้กันแต่เดิม อาจเพิ่มความเสี่ยงภาวะสมองเสื่อมด้วยซ้ำ[175][176]
วิถีชีวิต[แก้]
บุคคลที่ดำเนินกิจกรรมที่ต้องใช้ทักษะทางสติปัญญาเช่นอ่านหนังสือ เล่นหมากกระดาน เล่นปริศนาอักษรไขว้ เล่นดนตรี หรือมีปฏิสัมพันธ์ทางสังคมเป็นประจำมีความเสี่ยงการเกิดโรคอัลไซเมอร์ลดลง[177][178] ซึ่งสอดคล้องกับทฤษฎีการสงวนการรู้ (cognitive reserve theory) ที่ระบุว่า ประสบการณ์ชีวิตบางอย่างส่งผลให้การทำหน้าที่ของประสาทมีประสิทธิภาพมากยิ่งขึ้นทำให้ปัจเจกบุคคลมีการสงวนการรู้ซึ่งชะลอการเกิดอาการแสดงของภาวะสมองเสื่อม การศึกษาชะลอการเกิดกลุ่มอาการโรคอัลไซเมอร์แต่ไม่เปลี่ยนระยะเวลาของโรค[179] การเรียนภาษาที่สองแม้มีอายุมากแล้วดูเหมือนช่วยชะลอการเกิดโรคอัลไซเมอร์[180] กิจกรรมทางกายก็มีความสัมพันธ์กับโอกาสการเกิดโรคอัลไซเมอร์ลดลงเช่นกัน[179] การออกกำลังกายสัมพันธ์กับอัตราภาวะสมองเสื่อมที่ลดลง[181] และยังมีประสิทธิภาพในการลดความรุนแรงของอาการในผู้ป่วยโรคอัลไซเมอร์[182]
การบำบัดและการจัดการ[แก้]
ปัจจุบันยังไม่มีการรักษาโรคอัลไซเมอร์ให้หาย การรักษาที่มีในปัจจุบันให้ผลดีเล็กน้อยต่ออาการแต่โดยสภาพแล้วเป็นเพื่อการประทังเท่านั้น การรักษาในปัจจุบันแบ่งออกเป็น 3 รูปแบบ คือ การรักษาด้วยยา การรักษาทางจิตสังคม และการให้การดูแลผู้ป่วย
การรักษาด้วยยา[แก้]


ปัจจุบันมียาหรือเภสัชภัณฑ์ 5 ชนิดที่ใช้เพื่อรักษาอาการทางการรับรู้ในโรคอัลไซเมอร์ ประกอบด้วย 4 ชนิดเป็นแอนติโคลีนเอสเทอเรส (anticholinesterase) คือ tacrine, rivastigmine, galantamine และ donepezil และอีก 1 ชนิด คือเมแมนทีน (memantine) ซึ่งเป็นสารต้านตัวรับเอ็นเอ็มดีเอ (NMDA receptor antagonist) ประโยชน์ของการใช้ยาเหล่านี้มีน้อย[6][183][184] ไม่มียาใดที่แสดงให้เห็นชัดเจนว่าชะลอหรือหยุดการดำเนินโรคอย่างแท้จริง
ลักษณะของโรคอัลไซเมอร์ที่เป็นทราบกันดี คือ กัมมันตภาพของเซลล์ประสาทโคลิเนอร์จิก (cholinergic) มีลดลง[185] มีการใช้แอนติโคลีนเอสเทอเรสเพื่อลดอัตราการสลายแอซิทิลโคลีน (acetylcholine; ACh) ทำให้เพิ่มปริมาณความเข้มข้นของ ACh ในสมองเพื่อชดเชย ACh ที่มีปริมาณลดลงอันเนื่องจากการตายของเซลล์ประสาทโคลิเนอร์จิก[186] มีหลักฐานประสิทธิผลของยาเหล่านี้ในโรคอัลไซเมอร์ขั้นเบาถึงปานกลาง[187][184][183] และมีหลักฐานบ้างสำหรับการใช้ในระยะรุนแรง[183] การใช้ยาเหล่านี้ในความบกพร่องทางการรู้เล็กน้อยไม่แสดงว่ามีผลชะลอการเกิดโรคอัลไซเมอร์แม้แต่น้อย[188] ผลข้างเคียงที่พบบ่อยที่สุด ได้แก่ คลื่นไส้อาเจียน ซึ่งอาการทั้งสองเชื่อมโยงกับปริมาณโคลิเนอร์จิกที่มากเกิน ผลข้างเคียงเหล่านี้พบได้ในประมาณ 10–20% ของผู้ใช้ยา และมีความรุนแรงระดับเบาถึงปานกลาง และสามารถจัดการได้โดยปรับขนาดยาช้า ๆ[189] ผลที่พบน้อยลงมา เช่น ตะคริว หัวใจเต้นช้า เบื่ออาหาร น้ำหนักลด และเพิ่มการสร้างกรดกระเพาะ[187]
กลูตาเมตเป็นสารสื่อประสาทชนิดกระตุ้นในระบบประสาท แต่หากมีปริมาณมากเกินในสมองอาจทำให้เซลล์ตายได้จากกระบวนการชื่อว่า ภาวะเอ็กไซโททอกซิก (excitotoxicity) อันเกิดจากการกระตุ้นอย่างมากเกินของตัวรับกลูตาเมต ภาวะเอ็กไซโททอกซิกไม่ได้เกิดเฉพาะในโรคอัลไซเมอร์ แต่ยังพบในโรคทางระบบประสาทอื่น เช่น โรคพาร์กินสันและโรคปลอกประสาทเสื่อมแข็ง (multiple sclerosis)[190] เมแมนทีน (Memantine)[191] เป็นสารต้านตัวรับเอ็นเอ็มดีเอชนิดไม่แข่งขัน (noncompetitive) ซึ่งใช้ครั้งแรกเป็นสารต้านไข้หวัดใหญ่ สารนี้จะทำงานในระบบกลูตาเมเทอร์จิกโดยขัดขวางตัวรับเอ็นเอ็มดีเอและยับยั้งการกระตุ้นมากเกินของกลูตาเมต[190] เมแมนทีนมีประสิทธิภาพเล็กน้อยในการรักษาโรคอัลไซเมอร์ชนิดปานกลางและรุนแรง [192] ผลข้างเคียงของเมแมนทีนยังรายงานพบไม่บ่อยและไม่รุนแรง เช่น ประสาทหลอน สับสน เวียนศีรษะ ปวดศีรษะ และล้า[193] การใช้ยาเมแมนทีนและโดเนเพซิลร่วมกันให้ประสิทธิผลอย่างมีนัยสำคัญทางสถิติ แต่มีประสิทธิผลเพียงเล็กน้อยในทางคลินิก[194]
ยารักษาโรคจิตนอกแบบ (atypical antipsychotics) มีประโยชน์ในการลดความก้าวร้าวและโรคจิตในผู้ป่วยโรคอัลไซเมอร์อยู่บ้าง แต่ประโยชน์นั้นอาจมีน้อยกว่าผลข้างเคียงที่รุนแรง เช่น โรคหลอดเลือดสมอง ปัญหาการเคลื่อนไหวหรือการรู้ลดลง[195][196] และการใช้ระยะยาวมีการแสดงว่าสัมพันธ์กับอัตราตายที่เพิ่มขึ้น[196] การหยุดใช้ยาต้านโรคจิตในผู้ป่วยโรคอัลไซเมอร์ดูปลอดภัย[197]
แม้ว่ายาฮูเปอร์ซีนเอ (Huperzine A) จะดูมีหวัง แต่ยังต้องมีหลักฐานเพิ่มเติมก่อนแนะนำให้ใช้[198]
การรักษาทางจิตสังคม[แก้]

มีการนำการรักษาทางจิตสังคมมาใช้เสริมกับการรักษาด้วยยา แบ่งออกเป็นวิธีมุ่งเน้นด้านพฤติกรรม (behaviour-oriented), อารมณ์ (emotion-oriented), การรู้ (cognition-oriented) หรือการกระตุ้น (stimulation-oriented) ส่วนงานวิจัยว่าด้วยประสิทธิผลนั้นยังหาไม่พบและไม่จำเพาะต่อโรคอัลไซเมอร์ แต่มุ่งเน้นไปยังภาวะสมองเสื่อมโดยรวมแทน[199]
การแก้ไขพฤติกรรมคือการพยายามระบุและลดสิ่งที่เกิดขึ้นก่อนและผลที่ตามมาของพฤติกรรมปัญหา วิธีดังกล่าวยังไม่แสดงผลสำเร็จในการทำให้หน้าที่โดยรวมดีขึ้น[200] แต่สามารถช่วยลดปัญหาพฤติกรรมบางอย่างได้ เช่น การกลั้นปัสสาวะไม่ได้[201] ปัจจุบันยังขาดข้อมูลคุณภาพสูงเกี่ยวกับประสิทธิผลของเทคนิคดังกล่าวในการรักษาปัญหาพฤติกรรมอื่น ๆ เช่น การหนีออกจากบ้าน[202][203] ดนตรีบำบัดมีประสิทธิภาพลดอาการทางพฤติกรรมและจิต[204]
การรักษาที่มุ่งเน้นด้านอารมณ์ได้แก่ การบำบัดด้วยความทรงจำ (reminiscence therapy; RT), การบำบัดด้วยการให้เหตุผล (validation therapy), จิตบำบัดแบบประคับประคอง (supportive psychotherapy), การบูรณาการการรับความรู้สึก (sensory integration) หรือที่เรียกว่า สโนซีเลน (snoezelen) และการบำบัดด้วยการจำลองการมีอยู่ (simulated presence therapy; SPT) บทปฏิทัศน์คอคแครนไม่พบหลักฐานว่าการรักษาดังกล่าวมีประสิทธิภาพ[205] จิตบำบัดแบบประคับประคองมีการศึกษาทางวิทยาศาสตร์รูปนัยน้อยหรือไม่มีเลย แต่แพทย์บางคนพบว่าวิธีดังกล่าวช่วยให้บุคคลที่มีการรู้บกพร่องเล็กน้อยปรับตัวเข้ากับความเจ็บป่วยของตนได้[199] การบำบัดด้วยความทรงจำเกี่ยวข้องกับการอภิปรายประสบการณ์ในอดีตเป็นกลุ่มหรือแยกเดี่ยว ซึ่งมีการใช้ภาพถ่าย สิ่งของในบ้าน บันทึกดนตรีและเสียง หรือสิ่งของที่คุ้นเคยอย่างอื่นในอดีตมาช่วย บทปฏิทัศน์ปี 2561 ของ RT พบว่าผลลัพธ์ไม่เป็นไปในทิศทางเดียวกัน การทดลองมีขนาดเล็กและนัยสำคัญทางคลินิกที่น่าสงสัย และมีสถานที่แตกต่างกัน[206] การบำบัดด้วยการจำลองการมีอยู่ตั้งอยู่บนทฤษฎีการยึดติด (attachment) และมีการเล่นบันทึกเสียงของญาติสนิทที่สุดของผู้ป่วยโรคอัลไซเมอร์ มีหลักฐานบ้างว่า SPT อาจลดพฤติกรรมท้าทาย[207][208] ท้ายที่สุด การบำบัดด้วยการให้เหตุผลอาศัยพื้นฐานของการยอมรับความเป็นจริงและความจริงส่วนบุคคลของประสบการณ์ผู้อื่น ต่างจากการบูรณาการการรับความรู้สึก (sensory integration) ที่อาศัยการออกกำลังกายเพื่อกระตุ้นประสาทสัมผัสเป็นพื้นฐาน ทั้งนี้ ไม่มีหลักฐานสนับสนุนประโยชน์ของการบำบัดสองวิธีนี้[209][210]
เป้าหมายของการรักษาที่มุ่งเน้นการรู้คือการลดความบกพร่องในการรู้ (cognitive deficit) ซึ่งได้แก่การรับรู้ความเป็นจริงและการฟื้นฟูการรู้ การรับรู้ความเป็นจริง (reality orientation) ประกอบด้วยการรับรู้ข้อมูลเกี่ยวกับเวลา สถานที่ หรือบุคคลเพื่อช่วยให้เข้าใจตัวตนเกี่ยวกับสภาวะแวดล้อมและสถานที่ที่เขาอยู่ ในขณะที่การฟื้นฟูการรู้ (cognitive retraining) มุ่งพัฒนาความสามารถที่บกพร่องโดยการบริหารจิต ทั้งสองวิธีการแสดงประสิทธิผลบางส่วนในการทำให้ความสามารถด้านการรู้ดีขึ้น[211][212] แม้ในบางการศึกษาผลดังกล่าวเกิดขึ้นเพียงชั่วคราวและมีรายงานว่าเกิดผลเสียต่อผู้ป่วย เช่น ความคับข้องใจ[199]
การรักษาที่มุ่งเน้นการกระตุ้น เช่น ศิลปะบำบัด ดนตรีบำบัด การบำบัดโดยอาศัยสัตว์เลี้ยง กายภาพบำบัด และนันทนาการบำบัดชนิดอื่น การกระตุ้นมีการสนับสนุนอยู่บ้างเพื่อพัฒนาพฤติกรรม อารมณ์ และหน้าที่ อย่างไรก็ตาม การรักษาเหล่านี้นอกจากจะให้ผลดีในด้านการรักษาแล้วประโยชน์หลักยังช่วยพัฒนาทักษะในชีวิตประจำวันด้วย[199] ประสิทธิผลของการกระตุ้นสมองที่ไม่รุกล้ำและการกระตุ้นสมองแบบรุกล้ำในผู้ป่วยโรคอัลไซเมอร์ยังไม่แน่ชัด[213]
การดูแลผู้ป่วย[แก้]
เหตุที่โรคอัลไซเมอร์ยังไม่สามารถรักษาหายขาดได้ และผู้ป่วยไม่สามารถตอบสนองความต้องการของตัวเองมากขึ้นเรื่อย ๆ ผู้ดูแลจึงมีความสำคัญในการรักษาและต้องช่วยจัดการดูแลอย่างระมัดระวังตลอดการดำเนินโรค
ในผู้ป่วยระยะแรกและระยะปานกลาง การปรับเปลี่ยนสิ่งแวดล้อมที่อยู่อาศัยและวิถีชีวิตช่วยให้ผู้ป่วยมีความปลอดภัยมากขึ้นและลดภาระต่อผู้ดูแลได้[214][215] ตัวอย่างเช่นการปรับเปลี่ยนสภาพแวดล้อมให้ผู้ป่วยใช้ชีวิตประจำวันง่ายขึ้น การล็อกบ้านและรั้ว การติดป้ายหรือฉลากบนเครื่องใช้ภายในบ้านเพื่อบอกหรือเตือนผู้ป่วย หรือการใช้อุปกรณ์ชีวิตประจำวันที่มีการดัดแปลง[199][216][217] ถ้าผู้ป่วยเริ่มมีปัญหาการรับประทาน อาจเตรียมอาหารเป็นชิ้นเล็ก ๆ หรือปั่น[218] ถ้าผู้ป่วยเริ่มมีอาการกลืนลำบากอาจต้องใช้สายให้อาหาร (feeding tube) ในกรณีดังกล่าวผู้ดูแลและสมาชิกในครอบครัวควรคำนึงถึงประสิทธิผลและจริยธรรมของการให้อาหารทางสายยางต่อเนื่อง[219][220] ไม่มีข้อบ่งชี้ให้ทำการยึดยั้งผู้ป่วยอยู่กับที่ในทุกระยะของโรค แต่มีบางสถานการณ์จำเป็นต้องใช้วิธีดังกล่าวเพื่อป้องกันไม่ให้ผู้ป่วยเกิดอันตรายหรือทำอันตรายต่อผู้ดูแล[199]
เมื่อโรคดำเนินไป อาจเกิดปัญหาทางการแพทย์อื่น ๆ ตามมา เช่น โรคในช่องปากและฟัน แผลกดทับ ขาดสารอาหาร ปัญหาสุขอนามัย หรือการติดเชื้อในทางเดินหายใจ ผิวหนังหรือตา การดูแลอย่างระมัดระวังช่วยป้องกันภาวะดังกล่าว และหากเกิดปัญหาดังกล่าวตามมาแล้วต้องรับการรักษาโดยผู้เชี่ยวชาญ[54][221] ในระยะสุดท้ายของโรค การรักษาจะมุ่งเน้นการบรรเทาความรู้สึกไม่สะดวกสบายไปจนกระทั่งผู้ป่วยเสียชีวิต โดยมักอาศัยความช่วยเหลือของฮอสพิส (hospice)[222]
การพยากรณ์โรค[แก้]

การวินิจฉัยโรคอัลไซเมอร์ในระยะแรกทำได้ยาก การวินิจฉัยแน่นอนมักต้องปรากฏความบกพร่องในการรู้ที่เป็นอันตรายต่อกิจวัตรประจำวันแม้ว่าผู้ป่วยจะยังสามารถอยู่โดยไม่พึ่งพาผู้อื่นได้ โรคจะดำเนินต่อไปจากปัญหาการรู้เล็กน้อยเช่นความจำเสื่อม ไปเป็นระยะที่รบกวนการรู้และอื่น ๆ จนไม่อาจดำรงชีวิตอยู่ด้วยตัวเองได้ โดยเฉพาะในระยะท้ายของโรค[35]
ผู้ป่วยโรคอัลไซเมอร์มีการคาดหมายคงชีพน้อยกว่าประชากรปกติ[223] อายุคาดหมายคงชีพหลังวินิจฉัยตรงแบบมีพิสัยระหว่าง 3 ถึง 10 ปี[223] ผู้ป่วยน้อยกว่า 3% ดำรงชีวิตอยู่เกิน 14 ปีหลังได้รับการวินิจฉัย[224] ลักษณะที่สำคัญของโรคนี้อันสัมพันธ์กับอัตรารอดชีพที่ลดลง คือ การเพิ่มความรุนแรงของความบกพร่องทางการรู้, การลดระดับการทำหน้าที่, ประวัติการล้ม, และการรบกวนการทดสอบทางประสาทวิทยา โรคอื่น ๆ ที่อาจเกิดร่วม เช่น โรคหัวใจ เบาหวาน หรือประวัติการติดสุราก็เกี่ยวข้องกับการรอดชีพที่ลดลง[225][226] แม้ว่าผู้ป่วยยิ่งเกิดโรคอัลไซเมอร์เร็วเท่าใดก็ยิ่งมีปีรอดชีพรวมนานขึ้น แต่การคาดหมายคงชีพจะลดลงเป็นพิเศษเมื่อเทียบกับประชากรสุขภาพดีในกลุ่มที่มีอายุน้อย[227] ชายมีแนวโน้มพยากรณ์รอดชีพน้อยกว่าหญิง[224][228]
ปอดบวมและภาวะขาดน้ำเป็นสาเหตุสุดท้ายของการตายที่พบบ่อยที่สุด ส่วนมะเร็งเป็นสาเหตุการเสียชีวิตที่พบน้อยกว่าประชากรทั่วไป[228]
วิทยาการระบาด[แก้]
| อายุ | ผู้ป่วยใหม่ต่อ พันคน–ปี |
|---|---|
| 65–69 | 3 |
| 70–74 | 6 |
| 75–79 | 9 |
| 80–84 | 23 |
| 85–89 | 40 |
| 90– | 69 |
การศึกษาทางวิทยาการระบาดอาศัยการวัดหลัก 2 ชนิด คือ อุบัติการณ์และความชุกของโรค อุบัติการณ์คือจำนวนผู้ป่วยรายใหม่ต่อหน่วยคน–เวลาที่เสี่ยงรับโรค (มักใช้จำนวนผู้ป่วยใหม่ต่อพันคน–ปี) ในขณะที่ความชุกของโรคคือจำนวนผู้ป่วยทั้งหมดที่เป็นโรคในประชากรทั้งหมดในเวลาหนึ่ง
เมื่อพิจารณาอุบัติการณ์ การศึกษาตามแผน (cohort study) ติดตามประชากรที่ยังไม่มีโรคอัลไซเมอร์ในระยะเวลาหลายปี พบว่ามีอัตราเกิดภาวะสมองเสื่อมระหว่าง 10–15 ต่อพันคน–ปี และอัตราเป็นโรคอัลไซเมอร์ 5–8 ต่อพันคน–ปี[229][230] ซึ่งหมายความว่าในจำนวนผู้ป่วยสมองเสื่อมใหม่ในแต่ละปีมีครึ่งหนึ่งเป็นโรคอัลไซเมอร์ การมีอายุมากขึ้นเป็นปัจจัยเสี่ยงหลักของโรคนี้ และอัตราอุบัติการณ์โรคในแต่ละช่วงวัยก็ไม่เท่ากันกล่าวคือหลังจากอายุ 65 ปีขึ้นไป ทุกๆ 5 ปีหลังจากนั้นความเสี่ยงที่จะเกิดโรคอัลไซเมอร์จะเพิ่มขึ้นเป็นสองเท่า คือเพิ่มตั้งแต่ 3 จนถึง 69 ต่อพันคน–ปี[229][230] นอกจากนี้อัตราอุบัติการณ์ยังแตกต่างกันระหว่างเพศ เพศหญิงจะมีความเสี่ยงมากกว่าที่จะเป็นโรคอัลไซเมอร์โดยเฉพาะอย่างยิ่งในประชากรที่มีอายุมากกว่า 85 ปี[230][231] ในสหรัฐ ความเสี่ยงการเสียชีวิตจากโรคอัลไซเมอร์ในประชากรขาวที่มิใช่ฮิสแปนิกสูงกว่าประชากรดำที่มิใช่ฮิสแปนิก 26% ขณะที่ประชากรฮิสแปนิกมีความเสี่ยงต่ำกว่าประชากรขาวที่มิใช่ฮิสแปนิก 30%[232]
ความชุกของโรคอัลไซเมอร์ในประชากรขึ้นกับปัจจัยต่าง ๆ เช่น อุบัติการณ์และอัตรารอด เนื่องจากอุบัติการณ์ของโรคอัลไซเมอร์เพิ่มขึ้นตามอายุ การวิเคราะห์จึงจำเป็นต้องอาศัยอายุเฉลี่ยของประชากรที่สนใจด้วย มีการประมาณความชุกของโรคอัลไซเมอร์ในสหรัฐที่ประมาณ 1.6% ในปี 2543 ทั้งในประชากรทั้งหมดและในกลุ่มอายุ 65–74 ปี และมีอัตราเพิ่มขึ้นเป็น 19% ในกลุ่มอายุ 75–84 ปี และ 42% ในกลุ่มอายุมากกว่า 84 ปี[233] อัตราความชุกในประเทศกำลังพัฒนาน้อยกว่าในประเทศพัฒนาแล้ว[234] องค์การอนามัยโลกประมาณว่าในปี 2548 ประชากรทั่วโลก 0.379% มีภาวะสมองเสื่อม และอุบัติการณ์จะเพิ่มขึ้นเป็น 0.441% ในปี 2558 และเป็น 0.556% ในปี 2573[235] การศึกษาอื่นๆ ก็ให้ข้อสรุปที่ใกล้เคียงกัน[234] การสึกษาอื่นให้ข้อสรุปคล้ายกัน ในการศึกษาครั้งหนึ่งประมาณว่าในปี 2549 ประชากรโลก 0.40% (พิสัย 0.17–0.89%; จำนวนสัมบูรณ์ 26.6 ล้านคน; พิสัย 11.4–59.4 ล้านคน) ป่วยเป็นโรคอัลไซเมอร์ และอัตราความชุกจะเพิ่มเป็น 3 เท่า และจำนวนสัมบูรณ์จะเพิ่มเป็น 4 เท่าในปี 2593[236]
ประวัติศาสตร์[แก้]

นักปรัชญาและแพทย์ในยุคกรีกโบราณและโรมันเชื่อมโยงวัยสูงอายุกับภาวะสมองเสื่อมที่เพิ่มขึ้น[237] แต่ย่างเข้าปี 2444 กว่าที่จิตแพทย์ชาวเยอรมันชื่อ อาลอยซ์ อัลซไฮเมอร์ (Alois Alzheimer) สามารถระบุผู้ป่วยคนแรกด้วยโรคที่ต่อมาได้ชื่อว่า โรคอัลไซเมอร์ ในผู้ป่วยหญิงอายุ 55 ปีชื่อ ออกุสต์ เด. เขาติดตามผู้ป่วยรายนี้จนเสียชีวิตในปี 2449 และได้รายงานต่อสาธารณชนเป็นครั้งแรกในปีนั้น[238] จากนั้นเป็นเวลา 5 ปี มีรายงานผู้ป่วยที่มีอาการเดียวกัน 11 รายในเอกสารทางการแพทย์ รายงานบางส่วนเริ่มใช้คำว่า "โรคอัลไซเมอร์" แล้ว[237] เอมิล เครเพลิน (Emil Kraepelin) อธิบายโรคนี้เป็นโรคใหม่เป็นครั้งแรกหลังระงับลักษณะทางคลินิก (หลงผิดและประสาทหลอน) และลักษณะทางพยาธิวิทยา (พลากหลอดเลือดแดงแข็ง) ที่อยู่ในรายงานต้นฉบับของออกุสต์ เด. เขาใส่ โรคอัลไซเมอร์ หรือที่เครเพลินเรียกว่า ภาวะสมองเสื่อมก่อนวัยชรา (presenile dementia) เข้าเป็นชนิดย่อยของ ภาวะสมองเสื่อมในวัยชรา ใน ตำราจิตเวชศาสตร์ ฉบับพิมพ์ครั้งที่ 8 ซึ่งตีพิมพ์ปี 2453[239]
สำหรับช่วงเวลาส่วนใหญ่ของคริสต์ศตวรรษที่ 20 การวินิจฉัยโรคอัลไซเมอร์สงวนไว้สำหรับปัจเจกอายุระหว่าง 45 ถึง 65 ปีซึ่งมีอาการภาวะสมองเสื่อม ศัพทวิทยาเปลี่ยนหลังปี 2520 เมื่อการประชุมเรื่อง AD สรุปว่าการแสดงออกทางคลินิกและพยาธิวิทยาของภาวะสมองเสื่อมก่อนวัยชราและวัยชราแทบไม่ต่างกัน[240] แม้ผู้ประพันธ์เสริมว่าทั้งนี้ยังมีความเป็นไปได้ว่าอาจมีสาเหตุอย่างอื่น สุดท้ายทำให้การวินิจฉัยโรคอัลไซเมอร์ไม่ขึ้นกับอายุ[241] มีการใช้คำว่า ภาวะสมองเสื่อมวัยชราชนิดอัลไซเมอร์ (SDAT) อยู่ช่วงหนึ่งเพื่ออธิบายโรคอัลไซเมอร์ในบุคคลอายุเกิน 65 ปี และคำว่า "โรคอัลไซเมอร์คลาสสิก" ใช้อธิบายบุคคลที่อายุน้อยกว่า 65 ปี สุดท้าย มีการเห็นชอบอย่าเป็นทาการให้ใช้โรคอัลไซเมอร์ในการตั้งชื่อทางการแพทย์เพื่ออธิบายบุคคลอายุเท่าใดก็ได้ที่มีรูปแบบอาการทั่วไป การดำเนินโรคและประสาทพยาธิวิทยาอันเป็นลักษณะของโรคอัลไซเมอร์[242]
สังคมและวัฒนธรรม[แก้]
ค่าใช้จ่ายทางสังคม[แก้]
ภาวะสมองเสื่อม และโดยเฉพาะอย่างยิ่งโรคอัลไซเมอร์ อาจถือได้เป็นโรคที่เสียค่าใช้จ่ายสูงเป็นอันดับต้น ๆ สำหรับสังคมในทวีปยุโรปและสหรัฐ[20][21] ขณะที่ค่าใช้จ่ายในประเทศอื่นอย่างอาร์เจนตินา[243] และเกาหลีใต้[244] ก็สูงและกำลังเพิ่มขึ้นเช่นกัน ราคาของโรคอาจเพิ่มขึ้นจากสังคมที่มีผู้สูงอายุมากขึ้น และกลายเป็นปัญหาสังคมที่สำคัญ ค่าใช้จ่ายที่เกี่ยวข้องกับ AD มีทั้งค่าใช้จ่ายทางการแพทย์โดยตรง เช่น การบริบาลในสถานบริบาล ค่าใช้จ่ายที่มิใช่ทางการแพทย์โดยตรง เช่น การบริบาลเวลากลางวันในบ้าน (in-home day care) และค่าใช้จ่ายโดยอ้อม เช่น ผลิตภาพที่เสียไปของทั้งผู้ป่วยและผู้ดูแล[21] มูลค่านี้แตกต่างกันไปตามการศึกษาต่าง ๆ แต่มูลค่าสำหรับภาวะสมองเสื่อมทั่วโลกคำนวณไว้ประมาณ 160,000 ล้านดอลลาร์สหรัฐ[245] ส่วนมูลค่าของโรคอัลไซเมอร์ในสหรัฐอาจถึง 100,000 ล้านดอลลาร์สหรัฐต่อปี[21]
ค่าใช้จ่ายสำหรับสังคมมีที่มาจากการบริบาลระยะยาวโดยวิชาชีพสาธารณสุขมากที่สุด โดยเฉพาะอย่างยิ่งการรับรักษาในสถานพยาบาลซึ่งคิดเป็นสองในสามของค่าใช้จ่ายทั้งหมดของสังคม[20] ค่าใช้จ่ายของการอาศัยที่บ้านก็สูงมากเช่นกัน โดยเฉพาะเมื่อนำค่าใช้จ่ายโดยอ้อมสำหรับครอบครัว เช่น เวลาการให้การดูแลและรายได้ที่เสียไปของผู้ดูแล มาพิจารณาด้วย[246]
ค่าใช้จ่ายเพิ่มขึ้นตามความรุนแรงของภาวะสมองเสื่อมและการมีพฤติกรรมเปลี่ยนแปลง[247] และมีความสัมพันธ์กับเวลาที่ต้องให้การดูแลที่จำเป็นสำรับการบริบาลทางกายภาพ[246] ฉะนั้น การรักษาใด ๆ ที่ชะลอการเสื่อมของการรู้ ชะลอการรับรักษาในสถานพยาบาล หรือลดชั่วโมงของผู้ดูแลจะมีประโยชน์ทางเศรษฐกิจ การประเมินการรักษาปัจจุบันทางเศรษฐกิจแสดงผลลัพธ์ทางบวก[21]
ภาระของผู้ดูแล[แก้]
ผู้ดูแลหลักมักเป็นคู่สมรสหรือญาติสนิท[248] ทราบกันว่าโรคอัลไซเมอร์เป็นภาระใหญ่หวงต่อผู้ดูแลซึ่งมีทั้งแง่มุมทางสังคม จิตวิทยา กายภาพหรือเศรษฐกิจ[16][249][250] ปกติผู้ป่วย AD และครอบครัวมักนิยมการบริบาลที่บ้าน[251] ตัวเลือกนี้ยังชะลอหรือกำจัดความจำเป็นต้องได้รับากรบริบาลระดับที่เป็นวิชาชีพมากขึ้นและเสียค่าใช้จ่ายมากขึ้น[251][252] กระนั้น ผู้อยู่อาศัยในสถานบริบาลสองในสามมีภาวะสมองเสื่อม[199]
ผู้ดูแลผู้ป่วยสมองเสื่อมมีอัตราโรคทางกายและจิตใจสูง[253] ปัจจัยที่สัมพันธ์กับปัญหาทางจิตสังคมที่เพิ่มขึ้นของผู้ดูแลหลัก ได้แก่ การมีผู้ป่วยที่บ้าน ผู้ดูแลเป็นคู่สมรส พฤติกรรมที่ต้องใช้ความพยายามอย่างยิ่งของผู้ป่วย เช่น โรคซึมเศร้า พฤติกรรมเปลี่ยน ประสาทหลอน ปัญหาการหลับหรือปัญหาการเดิน และการแยกตัวจากสังคม[254][255] สำหรับปัญหาเศรษฐกิจ ผู้ดูแลครอบครัวมักต้องสละเวลางานเพื่อใช้เวลา 47 ชั่วโมงต่อสัปดาห์โดยเฉลี่ยกับผู้ป่วย AD ขณะที่มีค่าใช้จ่ายการบริบาลผู้ป่วยสูง ค่าใช้จ่ายโดยตรงและโดยอ้อมของการบริบาลผู้ป่วยโรคอัลไซเมอร์โดยเฉี่ยอยู่ระหว่าง 18,000 ถึง 77,500 ดอลลาร์สหรัฐต่อปีในสหรัฐ ขึ้นอยู่กับการศึกษา[246][248]
การบำบัดทางความคิดและพฤติกรรมและการสอนยุทธศาสตร์การรับมือไม่ว่าแบบเดี่ยวหรือเป็นกลุ่มปรากฏว่ามีประสิทธิผลในการเพิ่มสุขภาพจิตของผู้ดูแล[16][256]
สื่อ[แก้]
มีการพรรณนา AD ในภาพยนตร์อย่าง ไอริส (ปี 2544) ซึ่งยึดบันทึกความทรงจำของไอริส เมอร์ด็อค ภรรยาของจอห์น เบย์ลีย์;[257] เดอะโน้ตบุ๊ก (ปี 2547) ซึ่งอิงนวนิยายชื่อเดียวกันโดยนิโคลัส สปากส์ในปี 2539;[258] เมมโมรีส์ออฟทูมอร์โรว์ (ปี 2549) ซึ่งอิงนวนิยายชื่อเดียวกันโดยฮิโรชิ โอกิวาระ;[259] อะเวย์ฟรอมเฮอร์ (ปี 2549) ซึ่งอิงตามนิยายสั้น เดอะแบร์เคมโอเวอร์เดอะเมาน์เทน ของอลิซ มันโร;[260] อลิซ...ไม่ลืม (Still Alice, ปี 2557) มีเนื้อหาว่าด้วยศาสตราจารย์มหาวิทยาลัยโคลัมเบียซึ่งป่วยเป็นโรคอัลไซเมอร์ระยะแรก โดยอิงตามนวนิยายชื่อเดียวกันเมื่อปี 2550 โดยลิซา จีโนวา สารคดีว่าด้วยโรคอัลไซเมอร์ ได้แก่ มัลคอล์มแอนด์บาร์บารา: อะเลิฟสตอรี (ปี 2542) และ มัลคอล์มแอนด์บาร์บารา: เลิฟส์แฟร์เวล (ปี 2550) ซึ่งมีมัลคอล์ม พอยต์ตันนำแสดงทั้งสองเรื่อง[261][262][263]
ทิศทางการวิจัย[แก้]
ยา[แก้]
ในรอบทศวรรษปี 2545–2555 มีการประเมินสารประกอบ 244 ชนิดในการทดลองทางคลินิกระยะที่ 1, 2 และ 3 และมีสารประกอบชนิดเดียว (เมแมนทีน) ที่ได้รับอนุมัติจากคณะกรรมการอาหารและยาสหรัฐ[264] โซเลนซูแมบ (solanezumab) และอะดูคานูแมบ (aducanumab) ไม่แสดงว่ามีประสิทธิภาพในผู้ที่มีอาการของโรคอัลไซเมอร์แล้ว[265]
พื้นที่การวิจัยหนึ่งมุ่งเน้นการรักษาพยาธิภาพโรคพื้นเดิม การลดระดับบีตาแอมีลอยด์เป็นเป้าหมายทั่วไปของสารประกอบที่กำลังอยู่ระหว่างการสืบสวน (เช่น อะโปมอร์ฟีน)[266] การบำบัดด้วยภูมิคุ้มกันหรือการให้วัคซีนสำหรับโปรตีนแอมีลอยด์เป็นวิธีการรักษาหนึ่งที่อยู่ระหว่างการศึกษา[267] จะใช้การบำบัดแบบสันนิษฐาน (putative therapy) เพื่อรักษาผู้ที่ได้รับการวินิจฉัยแล้ว ซึ่งต่างจากการให้วัคซีนเพื่อป้องกัน ทั้งนี้ ตั้งอยู่บนมโนทัศน์ของการฝึกระบบภูมิคุ้มกันให้รับรู้ โจมตีและย้อนกลับซึ่งการสะสมแอมีอยด์เพื่อเปลี่ยนแปลงการดำเนินโรค[268] ตัวอย่างของวัคซีนป้องกันที่กำลังอยู่ระหว่างการสืบสวนได้แก่ ACC-001[269][270] แม้มีการระงับการทดลองในปี 2551[271] สารที่คล้ายกันอีกสารหนึ่ง ได้แก่ บาพินิวซูแมบ (bapineuzumab) ซึ่งเป็นแอนติบอดีที่ได้รับการออกแบบมาให้เหมือนกับแอนติบอดีต่อแอมีลอยด์ที่เหนี่ยวนำตามธรรมชาติ[272] อย่างไรก็ดี พบว่าสารภูมิคุ้มกันบำบัดก่อให้เกิดอาการไม่พึงประสงค์จากการใช้ยาที่น่ากังวลบางอย่าง เช่น ความผิดปกติของการสร้างภาพที่เกี่ยวข้องกับแอมีลอยด์ (amyloid-related imaging abnormalities)[273] แนวทางการพัฒนายาอย่างอื่นคือสารที่ช่วยป้องกันระบบประสาท เช่น AL-108[274] และสารการลดอันตรกิริยาโลหะกับโปรตีน (metal-protein interaction attenuation agent) เช่น PBT2[275] ด้านโปรตีนรวมตัวที่ขัดขวางตัวรับทีเอ็นเอฟแอลฟา (TNFα receptor-blocking fusion protein) อีแทเนอร์เซปต์ (etanercept) ซึ่งให้ผลลัพธ์ที่ให้ความเชื่อมั่น[276]
ในปี 2551 มีการทดลองทางคลินิกแยกกันสองการทดลองแสดงผลลัพธ์เชิงบวกในการเปลี่ยนการดำเนินโรคใน AD ขั้นเบาและปานกางด้วยเมทิลไทโอนิเนียมคลอไรด์ ซึ่งเป็นยายับยั้งการสะสมโปรตีนเทา[277][278] และไดมีบอน สารต้านฮิสตามีน[279] แต่การทดลองระยะที่ 3 ของไดมีบอนไม่มีผลเชิงบวกในจุดสิ้นสุดปฐมภูมิและทุติยภูมิ[280][281][282] งานวิจัยเมทิลไทโอนิเนียมคลอไรด์แสดงว่าชีวปริมาณออกฤทธิ์ของเมทิลไทโอนิเนียมจากทางเดินอาหารได้รับผลกระทบจากการได้รับอาหารและความเป็นกรดของกระเพาะอาหาร ทำให้ขนาดยาแปรปรวนอย่างไม่คาดคิด[283] สูตรที่มีการปรับให้เสถียรแล้วตัวใหม่ เช่น โปรดรัก LMTX อยู่ในการทดลองระยะที่ 3 (ในปี 2557)[284]
การป้องกันเชิงพฤติกรรม[แก้]
การวิจัยเรื่องผลของการทำสมาธิต่อการสงวนความจำและการทำหน้าที่เชิงการรู้ยังอยู่ในขั้นแรกเริ่ม[285] บทปฏิทัศน์ในปี 2558 เสนอว่าการรักษาที่เน้นสติอาจป้องกันหรือชะลอการเกิดความบกพร่องทางการรู้เล็กน้อยและโรคอัลไซเมอร์ได้[286]
การติดเชื้อและการส่งผ่าน[แก้]
พบว่าไวรัสเริม HSV-1 อยู่ในบริเวณเดียวกับแอมีลอยด์พลาก[287] ซึ่งมีการเสนอว่ามีความเป็นไปได้ที่สามารถรักษาหรือป้องกัน AD ด้วยยาต้านไวรัส[287][288] การศึกษายาต้านไวรัสในการเพาะเซลล์ให้ผลลัพธ์ที่น่าพึงพอใจ[289]
มีการอธิบายการติดเชื้อราของสมองผู้ป่วย AD[290] มีการเสนอสมมติฐานโดยนักจุลชีววิทยา แอล. คาร์ราสโค เมื่อกลุ่มของเขาพบสหสัมพันธ์ทางสถิติระหว่างการติดเชื้อราทั่วร่างกับ AD[291] งานวิจัยเพิ่มเติมเปิดเผยว่ามีการติดเชื้อราในบริเวณต่าง ๆ ของสมองผู้ป่วย AD แต่ไม่พบในปัจเจกควบคุม[292] [293] การติดเชื้อราอธิบายอาการที่สังเกตได้ในผู้ป่วย AD การดำเนินโรคอย่างช้าของ AD สมกับสภาพเรื้อรังของการติดเชื้อราทั่วกายบางชนิด ซึ่งอาจไม่มีอาการ ฉะนั้นจึงไม่ผิดสังเกตและไม่ได้รับการรักษา[292] สมมติฐานเชื้อรายังเข้าได้กับสมมติฐาน AD อื่นที่มีอยู่แล้วอื่น เช่น สมมติฐานแอมีลอยด์ ซึ่งสามารถอธิบายได้ว่าเป็นการตอบสนองของระบบภูมิคุ้มกันต่อการติดเชื้อในระบบประสาทส่วนกลาง[294][295][296] ดังที่ อาร์. มัวร์และ อาร์. แทนซีในแบบจำลอง AD ของหนูและหนอน
นอกจากนี้ กำลังมีการศึกษาการส่งผ่านระหว่างบุคคลที่เป็นไปได้ในผู้ป่วยหายาก[297] เช่น ในผู้ป่วยโกรทฮอร์โมน[298]
การสร้างภาพ[แก้]
ในบรรดาเทคนิคการสร้างภาพทางการแพทย์ เครื่องถ่ายภาพรังสีชนิดแกมมาหลายระนาบ (single photon emission computed tomography) ดูเหมือนดีที่สุดในการแยกโรคอัลไซเมอร์จากภาวะสมองเสื่อมชนิดอื่น และมีการแสดงว่าระดับความแม่นยำสูงกว่าเมื่อเทียบกับการทดสอบทางจิตวิทยาและการวิเคราะห์ประวัติทางการแพทย์[299] ความก้าวหน้าดังกล่าวนำให้มีการเสนอให้เป็นเกณฑ์การวินิจฉัยใหม่[23][132]
การถ่ายภาพรังสีระนาบด้วยการปล่อยโพซิตรอน (เพท) ด้วยพิตต์สเบิร์กคอมพาวน์บี (PiB) ยังใช้สืบสวนโรคได้อยู่ แต่เภสัชรังสีเพทสแกนคล้ายกัน ชื่อ ฟอร์เบตาพีร์ (florbetapir) ซึ่งมีฟลูออรีน-18 นิวไคลด์กัมมันตรังสีที่อยู่ได้นานกว่า เป็นเครื่องมือวินิจฉัยในโรคอัลไซเมอร์[300][301]
การสร้างภาพแอมีลอยด์น่าจะใช้ร่วมกับมาร์กเกอร์อื่นมากกว่าใช้เป็นทางเลือกเดี่ยว ๆ[302] เอ็มอาร์ไอเชิงปริมาตรสามารถตรวจจับการเปลี่ยนแปลงขนาดบริเวณต่าง ๆ ของสมองได้ การวัดบริเวณเห่านี้ว่าการฝ่อระหว่างการดำเนินโรคอัลไซเมอร์มีการแสดงผลลัพธ์ที่มีหวังว่าจะเป็นตัวบ่งชี้เพื่อวินิจฉัยในอนาคต และอาจมีราคาถูกกว่าวิธีสร้างภาพแบบอื่นที่กำลังศึกษาอยู่ในปัจจุบัน[303]
ในปี 2554 คณะกรรมการองค์การอาหารและยาสหรัฐออกเสียงเป็นเอกฉันท์แนะนำการอนุมัติฟอร์เบตาพีร์[304] สารที่ใช้สร้างภาพดังกล่าวสามารถช่วยตรวจจับพลากสมองของโรคอัไซเมอร์ได้[305] ผลสแกนเป็นลบบ่งชี้ว่ามีพลากกระจัดกระจายหรือไม่มีพลาก ซึ่งไม่สอดคล้องกับการวินิจฉัย AD[306]
การวินิจฉัย[แก้]
มีการเน้นการวิจัยโรคอัลไซเมอร์ในด้านการวินิจฉัยโรคดังกล่าวก่อนเริ่มปรากฏอาการ[307] มีการพัฒนาการทดสอบทางชีวเคมีหลายอย่างเพื่อให้ตรวจพบได้เร็วยิ่งขึ้น การทดสอบดังกล่าวบางอย่างเกี่ยวข้องกับการวิเคราะห์น้ำหล่อสมองไขสันหลังเพื่อหาบีตาแอมีลอยด์ ความเข้มข้นของโปรตีนเทารวม และโปรตีนเทา181พีที่เติมหมู่ฟอสเฟต[308] การเจาะน้ำหล่อสมองไขสันหลังทำให้เจ็บปวดจึงควรเลี่ยงการเจาะซ้ำ ๆ การตรวจเลือดเพื่อหาไมโครอาร์เอ็นเอในระบบไหลเวียนและไบโอมาร์กเกอร์การอักเสบเป็นตัวบ่งชี้ทางเลือกที่อาจเป็นไปได้[308]
เชิงอรรถ[แก้]
- ↑ เดิมคือ สมาคมโรคอัลไซเมอร์และความผิดปกติที่เกี่ยวข้อง (Alzheimer's Disease and Related Disorders Association)
อ้างอิง[แก้]
- ↑ 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 Burns A, Iliffe S (February 2009). "Alzheimer's disease". BMJ. 338: b158. doi:10.1136/bmj.b158. PMID 19196745.
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 "Dementia Fact sheet". World Health Organization. 12 December 2017.
- ↑ 3.0 3.1 Mendez MF (November 2012). "Early-onset Alzheimer's disease: nonamnestic subtypes and type 2 AD". Archives of Medical Research. 43 (8): 677–85. doi:10.1016/j.arcmed.2012.11.009. PMC 3532551. PMID 23178565.
- ↑ 4.0 4.1 4.2 4.3 4.4 Ballard C, Gauthier S, Corbett A, Brayne C, Aarsland D, Jones E (March 2011). "Alzheimer's disease". Lancet. 377 (9770): 1019–31. doi:10.1016/S0140-6736(10)61349-9. PMID 21371747.
- ↑ 5.0 5.1 "Dementia diagnosis and assessment" (PDF). National Institute for Health and Care Excellence (NICE). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 5 December 2014. สืบค้นเมื่อ 30 November 2014.
- ↑ 6.0 6.1 Commission de la transparence (June 2012). "Drugs for Alzheimer's disease: best avoided. No therapeutic advantage" [Drugs for Alzheimer's disease: best avoided. No therapeutic advantage]. Prescrire International. 21 (128): 150. PMID 22822592.
- ↑ 7.0 7.1 Querfurth HW, LaFerla FM (January 2010). "Alzheimer's disease". The New England Journal of Medicine. 362 (4): 329–44. doi:10.1056/NEJMra0909142. PMID 20107219.
- ↑ 8.0 8.1 "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1545–1602. October 2016. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577. PMID 27733282.
- ↑ 9.0 9.1 "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053): 1459–1544. October 2016. doi:10.1016/S0140-6736(16)31012-1. PMC 5388903. PMID 27733281.
- ↑ ศัพท์บัญญัติราชบัณฑิตยสถาน เก็บถาวร 2017-07-15 ที่ เวย์แบ็กแมชชีน ข้อมูลปรับปรุงวันที่ 6 สิงหาคม พ.ศ. 2544 เรียกดูเมื่อ 11 เมษายน พ.ศ. 2552
- ↑ บัญชีจำแนกโรคระหว่างประเทศ ฉบับประเทศไทย (อังกฤษ-ไทย) ฉบับปี 2009. สำนักนโยบายและยุทธศาสตร์ สำนักงานปลัดกระทรวงสาธารณสุข, 2552.
- ↑ "About Alzheimer's Disease: Symptoms". National Institute on Aging. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 15 January 2012. สืบค้นเมื่อ 28 December 2011.
- ↑ Todd S, Barr S, Roberts M, Passmore AP (November 2013). "Survival in dementia and predictors of mortality: a review". International Journal of Geriatric Psychiatry. 28 (11): 1109–24. doi:10.1002/gps.3946. PMID 23526458.
- ↑ "So, What Can You Do?". National Institute on Aging. 29 July 2016. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 3 April 2017.
- ↑ 15.0 15.1 15.2 15.3 Hsu D, Marshall GA (2017). "Primary and Secondary Prevention Trials in Alzheimer Disease: Looking Back, Moving Forward". Current Alzheimer Research. 14 (4): 426–40. doi:10.2174/1567205013666160930112125. PMC 5329133. PMID 27697063.
- ↑ 16.0 16.1 16.2 16.3 Thompson CA, Spilsbury K, Hall J, Birks Y, Barnes C, Adamson J (July 2007). "Systematic review of information and support interventions for caregivers of people with dementia". BMC Geriatrics. 7: 18. doi:10.1186/1471-2318-7-18. PMC 1951962. PMID 17662119.
- ↑ Forbes D, Forbes SC, Blake CM, Thiessen EJ, Forbes S (April 2015). "Exercise programs for people with dementia". The Cochrane Database of Systematic Reviews (Submitted manuscript). 132 (4): CD006489. doi:10.1002/14651858.CD006489.pub4. PMID 25874613.
- ↑ National Institute for Health and Clinical Excellence. "Low-dose antipsychotics in people with dementia". National Institute for Health and Care Excellence (NICE). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 5 December 2014. สืบค้นเมื่อ 29 November 2014.
- ↑ "Information for Healthcare Professionals: Conventional Antipsychotics". US Food and Drug Administration. 16 June 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 29 November 2014. สืบค้นเมื่อ 29 November 2014.
- ↑ 20.0 20.1 20.2 Bonin-Guillaume S, Zekry D, Giacobini E, Gold G, Michel JP (January 2005). "[The economical impact of dementia]". Presse Médicale (ภาษาฝรั่งเศส). 34 (1): 35–41. doi:10.1016/s0755-4982(05)83882-5. PMID 15685097.
- ↑ 21.0 21.1 21.2 21.3 21.4 Meek PD, McKeithan K, Schumock GT (1998). "Economic considerations in Alzheimer's disease". Pharmacotherapy. 18 (2 Pt 2): 68–73, discussion 79–82. doi:10.1002/j.1875-9114.1998.tb03880.x (inactive 2019-07-19). PMID 9543467.
{{cite journal}}: CS1 maint: DOI inactive as of กรกฎาคม 2019 (ลิงก์) - ↑ "Evaluating Prescription Drugs Used to Treat: Alzheimer's Disease Comparing Effectiveness, Safety, and Price" (PDF). Consumer Reports Drug Effectiveness Review Project. Consumer Reports. พฤษภาคม 2012. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 5 กันยายน 2012. สืบค้นเมื่อ 1 พฤษภาคม 2013.
- ↑ 23.0 23.1 23.2 23.3 23.4 Waldemar G, Dubois B, Emre M, Georges J, McKeith IG, Rossor M, Scheltens P, Tariska P, Winblad B (January 2007). "Recommendations for the diagnosis and management of Alzheimer's disease and other disorders associated with dementia: EFNS guideline". European Journal of Neurology. 14 (1): e1–26. doi:10.1111/j.1468-1331.2006.01605.x. PMID 17222085.
- ↑ Bäckman L, Jones S, Berger AK, Laukka EJ, Small BJ (September 2004). "Multiple cognitive deficits during the transition to Alzheimer's disease". Journal of Internal Medicine. 256 (3): 195–204. doi:10.1111/j.1365-2796.2004.01386.x. PMID 15324363.
- ↑ Perneczky R, Pohl C, Sorg C, Hartmann J, Komossa K, Alexopoulos P, Wagenpfeil S, Kurz A (2006). "Complex activities of daily living in mild cognitive impairment: conceptual and diagnostic issues". Age Ageing. 35 (3): 240–245. doi:10.1093/ageing/afj054. PMID 16513677.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Arnáiz E, Almkvist O (2003). "Neuropsychological features of mild cognitive impairment and preclinical Alzheimer's disease". Acta Neurol. Scand., Suppl. 179: 34–41. doi:10.1034/j.1600-0404.107.s179.7.x. PMID 12603249.
- ↑ Kazui H, Matsuda A, Hirono N; และคณะ (2005). "Everyday memory impairment of patients with mild cognitive impairment". Dement Geriatr Cogn Disord. 19 (5–6): 331–7. doi:10.1159/000084559. PMID 15785034. สืบค้นเมื่อ 2008-06-12.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Rapp MA, Reischies FM (2005). "Attention and executive control predict Alzheimer disease in late life: results from the Berlin Aging Study (BASE)". American Journal of Geriatric Psychiatry. 13 (2): 134–141. doi:10.1176/appi.ajgp.13.2.134. PMID 15703322.
- ↑
Spaan PE, Raaijmakers JG, Jonker C (2003). "Alzheimer's disease versus normal ageing: a review of the efficiency of clinical and experimental memory measures". Journal of Clinical Experimental Neuropsychology. 25 (2): 216–233. doi:10.1076/jcen.25.2.216.13638. PMID 12754679.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Craig D, Mirakhur A, Hart DJ, McIlroy SP, Passmore AP (2005). "A cross-sectional study of neuropsychiatric symptoms in 435 patients with Alzheimer's disease". American Journal of Geriatric Psychiatry. 13 (6): 460–468. doi:10.1176/appi.ajgp.13.6.460. PMID 15956265.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Robert PH, Berr C, Volteau M, Bertogliati C, Benoit M, Sarazin M, Legrain S, Dubois B (2006). "Apathy in patients with mild cognitive impairment and the risk of developing dementia of Alzheimer's disease: a one-year follow-up study". Clin Neurol Neurosurg. 108 (8): 733–736. doi:10.1016/j.clineuro.2006.02.003. PMID 16567037.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑
Palmer K, Berger AK, Monastero R, Winblad B, Bäckman L, Fratiglioni L (2007). "Predictors of progression from mild cognitive impairment to Alzheimer disease". Neurology. 68 (19): 1596–1602. doi:10.1212/01.wnl.0000260968.92345.3f. PMID 17485646.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑
Small BJ, Gagnon E, Robinson B (April 2007). "Early identification of cognitive deficits: preclinical Alzheimer's disease and mild cognitive impairment". Geriatrics. 62 (4): 19–23. PMID 17408315.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Grundman M, Petersen RC, Ferris SH, Thomas RG, Aisen PS, Bennett DA, และคณะ (January 2004). "Mild cognitive impairment can be distinguished from Alzheimer disease and normal aging for clinical trials". Archives of Neurology. 61 (1): 59–66. doi:10.1001/archneur.61.1.59. PMID 14732621.
- ↑ 35.0 35.1 35.2 35.3 35.4 35.5 Förstl H, Kurz A (1999). "Clinical features of Alzheimer's disease". European Archives of Psychiatry and Clinical Neuroscience. 249 (6): 288–290. doi:10.1007/s004060050101. PMID 10653284.
- ↑ Carlesimo GA, Oscar-Berman M (June 1992). "Memory deficits in Alzheimer's patients: a comprehensive review". Neuropsychol Rev. 3 (2): 119–69. doi:10.1007/BF01108841. PMID 1300219.
- ↑
Jelicic M, Bonebakker AE, Bonke B (1995). "Implicit memory performance of patients with Alzheimer's disease: a brief review". International Psychogeriatrics. 7 (3): 385–392. doi:10.1017/S1041610295002134. PMID 8821346.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 38.0 38.1 38.2 Frank EM (September 1994). "Effect of Alzheimer's disease on communication function". J S C Med Assoc. 90 (9): 417–23. PMID 7967534.
- ↑ Becker JT, Overman AA (2002). "[The semantic memory deficit in Alzheimer's disease]". Rev Neurol (ภาษาสเปน). 35 (8): 777–83. PMID 12402233.
- ↑ Hodges JR, Patterson K (April 1995). "Is semantic memory consistently impaired early in the course of Alzheimer's disease? Neuroanatomical and diagnostic implications". Neuropsychologia. 33 (4): 441–59. doi:10.1016/0028-3932(94)00127-B. PMID 7617154.
- ↑ Benke T (December 1993). "Two forms of apraxia in Alzheimer's disease". Cortex. 29 (4): 715–25. PMID 8124945.
- ↑
Forbes KE, Shanks MF, Venneri A (March 2004). "The evolution of dysgraphia in Alzheimer's disease". Brain Res. Bull. 63 (1): 19–24. doi:10.1016/j.brainresbull.2003.11.005. PMID 15121235.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑
Galasko D, Schmitt F, Thomas R, Jin S, Bennett D (2005). "Detailed assessment of activities of daily living in moderate to severe Alzheimer's disease". Journal of the International Neuropsychology Society. 11 (4): 446–453. PMID 16209425.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑
Galasko D, Schmitt F, Thomas R, Jin S, Bennett D (July 2005). "Detailed assessment of activities of daily living in moderate to severe Alzheimer's disease". J Int Neuropsychol Soc. 11 (4): 446–53. PMID 16209425.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Sartori G, Snitz BE, Sorcinelli L, Daum I (September 2004). "Remote memory in advanced Alzheimer's disease". Arch Clin Neuropsychol. 19 (6): 779–89. doi:10.1016/j.acn.2003.09.007. PMID 15288331.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Volicer L, Harper DG, Manning BC, Goldstein R, Satlin A (May 2001). "Sundowning and circadian rhythms in Alzheimer's disease". Am J Psychiatry. 158 (5): 704–11. doi:10.1176/appi.ajp.158.5.704. PMID 11329390. สืบค้นเมื่อ 2008-08-27.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ อาการทางประสาทจิตเวช:
- Scarmeas N, Brandt J, Blacker D; และคณะ (December 2007). "Disruptive behavior as a predictor in Alzheimer disease". Arch. Neurol. 64 (12): 1755–61. doi:10.1001/archneur.64.12.1755. PMID 18071039.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - Tatsch MF, Bottino CM, Azevedo D; และคณะ (May 2006). "Neuropsychiatric symptoms in Alzheimer disease and cognitively impaired, nondemented elderly from a community-based sample in Brazil: prevalence and relationship with dementia severity". Am J Geriatr Psychiatry. 14 (5): 438–45. doi:10.1097/01.JGP.0000218218.47279.db. PMID 16670248.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - Volicer L, Bass EA, Luther SL (October 2007). "Agitation and resistiveness to care are two separate behavioral syndromes of dementia". J Am Med Dir Assoc. 8 (8): 527–32. doi:10.1016/j.jamda.2007.05.005. PMID 17931577.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- Scarmeas N, Brandt J, Blacker D; และคณะ (December 2007). "Disruptive behavior as a predictor in Alzheimer disease". Arch. Neurol. 64 (12): 1755–61. doi:10.1001/archneur.64.12.1755. PMID 18071039.
- ↑ Honig LS, Mayeux R (June 2001). "Natural history of Alzheimer's disease". Aging (Milano). 13 (3): 171–82. PMID 11442300.
- ↑ Gold DP, Reis MF, Markiewicz D, Andres D (January 1995). "When home caregiving ends: a longitudinal study of outcomes for caregivers of relatives with dementia". J Am Geriatr Soc. 43 (1): 10–6. PMID 7806732.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bär M, Kruse A, Re S (December 2003). "[Situations of emotional significance in residents suffering from dementia]". Z Gerontol Geriatr (ภาษาเยอรมัน). 36 (6): 454–62. doi:10.1007/s00391-003-0191-0. PMID 14685735.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Souren LE, Franssen EH, Reisberg B (June 1995). "Contractures and loss of function in patients with Alzheimer's disease". J Am Geriatr Soc. 43 (6): 650–5. PMID 7775724.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Berkhout AM, Cools HJ, van Houwelingen HC (September 1998). "The relationship between difficulties in feeding oneself and loss of weight in nursing-home patients with dementia". Age Ageing. 27 (5): 637–41. doi:10.1093/ageing/27.5.637. PMID 12675103.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Wada H, Nakajoh K, Satoh-Nakagawa T; และคณะ (2001). "Risk factors of aspiration pneumonia in Alzheimer's disease patients". Gerontology. 47 (5): 271–6. doi:10.1159/000052811. PMID 11490146.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 54.0 54.1 Gambassi G, Landi F, Lapane KL, Sgadari A, Mor V, Bernabei R (July 1999). "Predictors of mortality in patients with Alzheimer's disease living in nursing homes". J. Neurol. Neurosurg. Psychiatr. 67 (1): 59–65. PMC 1736445. PMID 10369823.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "What We Know Today About Alzheimer's Disease". Alzheimer's Association. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 7 October 2011. สืบค้นเมื่อ 1 October 2011.
While scientists know Alzheimer's disease involves progressive brain cell failure, the reason cells fail isn't clear.
- ↑ Reitz C, Mayeux R (April 2014). "Alzheimer disease: epidemiology, diagnostic criteria, risk factors and biomarkers". Biochemical Pharmacology. 88 (4): 640–51. doi:10.1016/j.bcp.2013.12.024. PMC 3992261. PMID 24398425.
- ↑ Wilson RS, Barral S, Lee JH, Leurgans SE, Foroud TM, Sweet RA, Graff-Radford N, Bird TD, Mayeux R, Bennett DA (2011). "Heritability of different forms of memory in the Late Onset Alzheimer's Disease Family Study". Journal of Alzheimer's Disease. 23 (2): 249–55. doi:10.3233/JAD-2010-101515. PMC 3130303. PMID 20930268.
- ↑ 58.0 58.1 58.2 Blennow K, de Leon MJ, Zetterberg H (July 2006). "Alzheimer's disease". Lancet. 368 (9533): 387–403. doi:10.1016/S0140-6736(06)69113-7. PMID 16876668.
- ↑ 59.0 59.1 Waring SC, Rosenberg RN (March 2008). "Genome-wide association studies in Alzheimer disease". Archives of Neurology. 65 (3): 329–34. doi:10.1001/archneur.65.3.329. PMID 18332245.
- ↑ Selkoe DJ (June 1999). "Translating cell biology into therapeutic advances in Alzheimer's disease". Nature. 399 (6738 Suppl): A23–31. doi:10.1038/19866. PMID 10392577.
- ↑ Borchelt DR, Thinakaran G, Eckman CB, Lee MK, Davenport F, Ratovitsky T, และคณะ (November 1996). "Familial Alzheimer's disease-linked presenilin 1 variants elevate Abeta1-42/1-40 ratio in vitro and in vivo". Neuron. 17 (5): 1005–13. doi:10.1016/S0896-6273(00)80230-5. PMID 8938131.
- ↑ Kim, JH (December 2018). "Genetics of Alzheimer's Disease". Dementia and Neurocognitive Disorders. 17 (4): 131–36. doi:10.12779/dnd.2018.17.4.131. PMC 6425887. PMID 30906402.
- ↑ Strittmatter WJ, Saunders AM, Schmechel D, Pericak-Vance M, Enghild J, Salvesen GS, Roses AD (March 1993). "Apolipoprotein E: high-avidity binding to beta-amyloid and increased frequency of type 4 allele in late-onset familial Alzheimer disease". Proceedings of the National Academy of Sciences of the United States of America. 90 (5): 1977–81. doi:10.1073/pnas.90.5.1977. PMC 46003. PMID 8446617.
- ↑ 64.0 64.1 Mahley RW, Weisgraber KH, Huang Y (April 2006). "Apolipoprotein E4: a causative factor and therapeutic target in neuropathology, including Alzheimer's disease". Proceedings of the National Academy of Sciences of the United States of America. 103 (15): 5644–51. Bibcode:2006PNAS..103.5644M. doi:10.1073/pnas.0600549103. PMC 1414631. PMID 16567625.
- ↑ Hall K, Murrell J, Ogunniyi A, Deeg M, Baiyewu O, Gao S, Gureje O, Dickens J, Evans R, Smith-Gamble V, Unverzagt FW, Shen J, Hendrie H (January 2006). "Cholesterol, APOE genotype, and Alzheimer disease: an epidemiologic study of Nigerian Yoruba". Neurology. 66 (2): 223–27. doi:10.1212/01.wnl.0000194507.39504.17. PMC 2860622. PMID 16434658.
- ↑ Gureje O, Ogunniyi A, Baiyewu O, Price B, Unverzagt FW, Evans RM, และคณะ (January 2006). "APOE epsilon4 is not associated with Alzheimer's disease in elderly Nigerians". Annals of Neurology. 59 (1): 182–85. doi:10.1002/ana.20694. PMC 2855121. PMID 16278853.
- ↑ 67.0 67.1 Lambert JC, Ibrahim-Verbaas CA, Harold D, Naj AC, Sims R, Bellenguez C, และคณะ (December 2013). "Meta-analysis of 74,046 individuals identifies 11 new susceptibility loci for Alzheimer's disease". Nature Genetics. 45 (12): 1452–58. doi:10.1038/ng.2802. PMC 3896259. PMID 24162737.
- ↑ Jonsson T, Stefansson H, Steinberg S, Jonsdottir I, Jonsson PV, Snaedal J, และคณะ (January 2013). "Variant of TREM2 associated with the risk of Alzheimer's disease". The New England Journal of Medicine (Original article). 368 (2): 107–16. doi:10.1056/NEJMoa1211103. PMC 3677583. PMID 23150908.
- ↑ Guerreiro R, Wojtas A, Bras J, Carrasquillo M, Rogaeva E, Majounie E, และคณะ (January 2013). "TREM2 variants in Alzheimer's disease". The New England Journal of Medicine (Original article). 368 (2): 117–27. doi:10.1056/NEJMoa1211851. PMC 3631573. PMID 23150934.
- ↑ Mukherjee S, Mez J, Trittschuh EH, Saykin AJ, Gibbons LE, Fardo DW, และคณะ (December 2018). "Genetic data and cognitively defined late-onset Alzheimer's disease subgroups". Molecular Psychiatry. doi:10.1038/s41380-018-0298-8. PMC 6548676. PMID 30514930.
- ↑ Shen ZX (2004). "Brain cholinesterases: II. The molecular and cellular basis of Alzheimer's disease". Med Hypotheses. 63 (2): 308–21. doi:10.1016/j.mehy.2004.02.031. PMID 15236795.
- ↑ Hardy J, Allsop D (October 1991). "Amyloid deposition as the central event in the aetiology of Alzheimer's disease". Trends Pharmacol. Sci. 12 (10): 383–88. doi:10.1016/0165-6147(91)90609-V. PMID 1763432.
- ↑ 73.0 73.1 Mudher A, Lovestone S (January 2002). "Alzheimer's disease-do tauists and baptists finally shake hands?". Trends Neurosci. 25 (1): 22–26. doi:10.1016/S0166-2236(00)02031-2. PMID 11801334.
- ↑ Nistor M, Don M, Parekh M; และคณะ (October 2007). "Alpha- and beta-secretase activity as a function of age and beta-amyloid in Down syndrome and normal brain". Neurobiol Aging. 28 (10): 1493–1506. doi:10.1016/j.neurobiolaging.2006.06.023. PMID 16904243.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Lott IT, Head E (March 2005). "Alzheimer disease and Down syndrome: factors in pathogenesis". Neurobiol Aging. 26 (3): 383–89. doi:10.1016/j.neurobiolaging.2004.08.005. PMID 15639317.
- ↑ Polvikoski T, Sulkava R, Haltia M, Kainulainen K, Vuorio A, Verkkoniemi A, Niinistö L, Halonen P, Kontula K (November 1995). "Apolipoprotein E, dementia, and cortical deposition of beta-amyloid protein". The New England Journal of Medicine. 333 (19): 1242–47. doi:10.1056/NEJM199511093331902. PMID 7566000.
- ↑ Transgenic mice:
- Games D, Adams D, Alessandrini R, Barbour R, Berthelette P, Blackwell C, Carr T, Clemens J, Donaldson T, Gillespie F (February 1995). "Alzheimer-type neuropathology in transgenic mice overexpressing V717F beta-amyloid precursor protein". Nature. 373 (6514): 523–27. doi:10.1038/373523a0. PMID 7845465.
- Masliah E, Sisk A, Mallory M, Mucke L, Schenk D, Games D (September 1996). "Comparison of neurodegenerative pathology in transgenic mice overexpressing V717F beta-amyloid precursor protein and Alzheimer's disease". The Journal of Neuroscience. 16 (18): 5795–811. doi:10.1523/JNEUROSCI.16-18-05795.1996. PMID 8795633.
- Hsiao K, Chapman P, Nilsen S, Eckman C, Harigaya Y, Younkin S, Yang F, Cole G (October 1996). "Correlative memory deficits, Abeta elevation, and amyloid plaques in transgenic mice". Science. 274 (5284): 99–102. doi:10.1126/science.274.5284.99. PMID 8810256.
- Lalonde R, Dumont M, Staufenbiel M, Sturchler-Pierrat C, Strazielle C (November 2002). "Spatial learning, exploration, anxiety, and motor coordination in female APP23 transgenic mice with the Swedish mutation". Brain Research. 956 (1): 36–44. doi:10.1016/S0006-8993(02)03476-5. PMID 12426044.
- ↑ Laurén J, Gimbel DA, Nygaard HB, Gilbert JW, Strittmatter SM (February 2009). "Cellular prion protein mediates impairment of synaptic plasticity by amyloid-beta oligomers". Nature. 457 (7233): 1128–32. doi:10.1038/nature07761. PMC 2748841. PMID 19242475.
- ↑ 79.0 79.1 Nikolaev A, McLaughlin T, O'Leary DD, Tessier-Lavigne M (February 2009). "APP binds DR6 to trigger axon pruning and neuron death via distinct caspases". Nature. 457 (7232): 981–89. Bibcode:2009Natur.457..981N. doi:10.1038/nature07767. PMC 2677572. PMID 19225519.
- ↑ Feuerstein, Adam (14 February 2017). "Merck Alzheimer's Drug Study Halted Early for Futility". New York City: TheStreet, Inc. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 16 February 2017.Merck Alzheimer's Drug Study Halted Early for Futility Independent study monitors concluded that there was "virtually no chance of finding a positive clinical effect."
- ↑ "After A Big Failure, Scientists And Patients Hunt For A New Type Of Alzheimer's Drug". NPR.org. สืบค้นเมื่อ 17 May 2019.
- ↑ Gallagher, James (2 May 2019). "Dementia is 'greatest health challenge'". สืบค้นเมื่อ 17 May 2019.
- ↑ Goedert M, Spillantini MG, Crowther RA (July 1991). "Tau proteins and neurofibrillary degeneration". Brain Pathology. 1 (4): 279–86. doi:10.1111/j.1750-3639.1991.tb00671.x. PMID 1669718.
- ↑ Iqbal K, Alonso A, Chen S, Chohan MO, El-Akkad E, Gong CX, Khatoon S, Li B, Liu F, Rahman A, Tanimukai H, Grundke-Iqbal I (January 2005). "Tau pathology in Alzheimer disease and other tauopathies". Biochimica et Biophysica Acta. 1739 (2–3): 198–210. doi:10.1016/j.bbadis.2004.09.008. PMID 15615638.
- ↑ Chun W, Johnson GV (January 2007). "The role of tau phosphorylation and cleavage in neuronal cell death". Frontiers in Bioscience. 12: 733–56. doi:10.2741/2097. PMID 17127334.
- ↑ Deane R, Zlokovic BV (April 2007). "Role of the blood-brain barrier in the pathogenesis of Alzheimer's disease". Current Alzheimer Research. 4 (2): 191–97. doi:10.2174/156720507780362245. PMID 17430246.
- ↑ Miklossy J (August 2011). "Alzheimer's disease - a neurospirochetosis. Analysis of the evidence following Koch's and Hill's criteria". Journal of Neuroinflammation. 8 (1): 90. doi:10.1186/1742-2094-8-90. PMC 3171359. PMID 21816039.
- ↑ Allen, HB (27 June 2016). "Alzheimer's Disease: Assessing the Role of Spirochetes, Biofilms, the Immune System, and Amyloid-β with Regard to Potential Treatment and Prevention". Journal of Alzheimer's Disease. 53 (4): 1271–76. doi:10.3233/JAD-160388. PMC 5008232. PMID 27372648.
- ↑ Xu H, Finkelstein DI, Adlard PA (12 June 2014). "Interactions of metals and Apolipoprotein E in Alzheimer's disease". Frontiers in Aging Neuroscience. 6: 121. doi:10.3389/fnagi.2014.00121. PMC 4054654. PMID 24971061.
Although we still do not know if the metal ion dyshomeostasis present in AD is a cause or consequence of the disease, there is a growing body of evidence showing a direct correlation between metal ions and key AD-related key proteins.
- ↑ Su B, Wang X, Nunomura A, Moreira PI, Lee HG, Perry G, Smith MA, Zhu X (December 2008). "Oxidative stress signaling in Alzheimer's disease". Current Alzheimer Research. 5 (6): 525–32. doi:10.2174/156720508786898451. PMC 2780015. PMID 19075578.
- ↑ Kastenholz B, Garfin DE, Horst J, Nagel KA (2009). "Plant metal chaperones: a novel perspective in dementia therapy". Amyloid. 16 (2): 81–83. doi:10.1080/13506120902879392. PMID 20536399.
- ↑ "Aluminium and Alzheimer's disease". Facts about dementia. Alzheimer's Society. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 27 October 2005. สืบค้นเมื่อ 14 October 2005.
- ↑ Bondy SC (January 2016). "Low levels of aluminum can lead to behavioral and morphological changes associated with Alzheimer's disease and age-related neurodegeneration". Neurotoxicology (Submitted manuscript). 52: 222–29. doi:10.1016/j.neuro.2015.12.002. PMID 26687397.
- ↑ Kandimalla R, Vallamkondu J, Corgiat EB, Gill KD (March 2016). "Understanding Aspects of Aluminum Exposure in Alzheimer's Disease Development". Brain Pathology. 26 (2): 139–54. doi:10.1111/bpa.12333. PMID 26494454.
- ↑ Santibáñez M, Bolumar F, García AM (November 2007). "Occupational risk factors in Alzheimer's disease: a review assessing the quality of published epidemiological studies". Occupational and Environmental Medicine. 64 (11): 723–32. doi:10.1136/oem.2006.028209. PMC 2078415. PMID 17525096.
- ↑ 96.0 96.1 Lidsky TI (May 2014). "Is the Aluminum Hypothesis dead?". Journal of Occupational and Environmental Medicine. 56 (5 Suppl): S73–79. doi:10.1097/jom.0000000000000063. PMC 4131942. PMID 24806729.
- ↑ Yegambaram M, Manivannan B, Beach TG, Halden RU (2015). "Role of environmental contaminants in the etiology of Alzheimer's disease: a review". Current Alzheimer Research. 12 (2): 116–46. doi:10.2174/1567205012666150204121719. PMC 4428475. PMID 25654508.
- ↑ Cataldo JK, Prochaska JJ, Glantz SA (2010). "Cigarette smoking is a risk factor for Alzheimer's Disease: an analysis controlling for tobacco industry affiliation". Journal of Alzheimer's Disease. 19 (2): 465–80. doi:10.3233/JAD-2010-1240. PMC 2906761. PMID 20110594.
- ↑ Eikelenboom P, van Exel E, Hoozemans JJ, Veerhuis R, Rozemuller AJ, van Gool WA (2010). "Neuroinflammation - an early event in both the history and pathogenesis of Alzheimer's disease". Neuro-Degenerative Diseases. 7 (1–3): 38–41. doi:10.1159/000283480. PMID 20160456.
- ↑ Moulton PV, Yang W (2012). "Air pollution, oxidative stress, and Alzheimer's disease". Journal of Environmental and Public Health (Review). 2012: 1–9. doi:10.1155/2012/472751. PMC 3317180. PMID 22523504.
- ↑ Bartzokis G (August 2011). "Alzheimer's disease as homeostatic responses to age-related myelin breakdown". Neurobiology of Aging. 32 (8): 1341–71. doi:10.1016/j.neurobiolaging.2009.08.007. PMC 3128664. PMID 19775776.
- ↑ Cai Z, Xiao M (2016). "Oligodendrocytes and Alzheimer's disease". The International Journal of Neuroscience. 126 (2): 97–104. doi:10.3109/00207454.2015.1025778. PMID 26000818.
- ↑ 103.0 103.1 103.2 Reisberg B, Franssen EH, Hasan SM, Monteiro I, Boksay I, Souren LE, และคณะ (1999). "Retrogenesis: clinical, physiologic, and pathologic mechanisms in brain aging, Alzheimer's and other dementing processes". European Archives of Psychiatry and Clinical Neuroscience. 249 Suppl 3 (3): 28–36. doi:10.1007/pl00014170. PMID 10654097.
- ↑ Alves GS, Oertel Knöchel V, Knöchel C, Carvalho AF, Pantel J, Engelhardt E, Laks J (2015). "Integrating retrogenesis theory to Alzheimer's disease pathology: insight from DTI-TBSS investigation of the white matter microstructural integrity". BioMed Research International. 2015: 291658. doi:10.1155/2015/291658. PMC 4320890. PMID 25685779.
- ↑ Brenner Carson, Verna (2015). Caregiving for Alzheimer's Disease. New York: Springer New York Academy of Sciences. pp. 1–9. ISBN 978-1-4939-2406-6.
- ↑ Wenk GL (2003). "Neuropathologic changes in Alzheimer's disease". The Journal of Clinical Psychiatry. 64 Suppl 9: 7–10. PMID 12934968.
- ↑ Braak H, Del Tredici K (December 2012). "Where, when, and in what form does sporadic Alzheimer's disease begin?". Current Opinion in Neurology. 25 (6): 708–14. doi:10.1097/WCO.0b013e32835a3432. PMID 23160422.
- ↑ Desikan RS, Cabral HJ, Hess CP, Dillon WP, Glastonbury CM, Weiner MW, Schmansky NJ, Greve DN, Salat DH, Buckner RL, Fischl B (August 2009). "Automated MRI measures identify individuals with mild cognitive impairment and Alzheimer's disease". Brain. 132 (Pt 8): 2048–57. doi:10.1093/brain/awp123. PMC 2714061. PMID 19460794.
- ↑ Moan R (20 July 2009). "MRI Software Accurately IDs Preclinical Alzheimer's Disease". Diagnostic Imaging. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 16 May 2016. สืบค้นเมื่อ 7 January 2013.
- ↑ 110.0 110.1 Tiraboschi P, Hansen LA, Thal LJ, Corey-Bloom J (June 2004). "The importance of neuritic plaques and tangles to the development and evolution of AD". Neurology. 62 (11): 1984–9. PMID 15184601.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bouras C, Hof PR, Giannakopoulos P, Michel JP, Morrison JH (1994). "Regional distribution of neurofibrillary tangles and senile plaques in the cerebral cortex of elderly patients: a quantitative evaluation of a one-year autopsy population from a geriatric hospital". Cereb. Cortex. 4 (2): 138–50. doi:10.1093/cercor/4.2.138. PMID 8038565.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Kotzbauer PT, Trojanowsk JQ, Lee VM (October 2001). "Lewy body pathology in Alzheimer's disease". Journal of Molecular Neuroscience. 17 (2): 225–32. doi:10.1385/JMN:17:2:225. PMID 11816795.
- ↑ Hashimoto M, Rockenstein E, Crews L, Masliah E (2003). "Role of protein aggregation in mitochondrial dysfunction and neurodegeneration in Alzheimer's and Parkinson's diseases". Neuromolecular Med. 4 (1–2): 21–36. doi:10.1385/NMM:4:1-2:21. PMID 14528050.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Priller C, Bauer T, Mitteregger G, Krebs B, Kretzschmar HA, Herms J (July 2006). "Synapse formation and function is modulated by the amyloid precursor protein". J. Neurosci. 26 (27): 7212–21. doi:10.1523/JNEUROSCI.1450-06.2006. PMID 16822978.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Turner PR, O'Connor K, Tate WP, Abraham WC (May 2003). "Roles of amyloid precursor protein and its fragments in regulating neural activity, plasticity and memory". Prog. Neurobiol. 70 (1): 1–32. doi:10.1016/S0301-0082(03)00089-3. PMID 12927332.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Hooper NM (April 2005). "Roles of proteolysis and lipid rafts in the processing of the amyloid precursor protein and prion protein". Biochem. Soc. Trans. 33 (Pt 2): 335–8. doi:10.1042/BST0330335. PMID 15787600.
- ↑ Ohnishi S, Takano K (March 2004). "Amyloid fibrils from the viewpoint of protein folding". Cell. Mol. Life Sci. 61 (5): 511–24. doi:10.1007/s00018-003-3264-8. PMID 15004691.
- ↑ Hernández F, Avila J (September 2007). "Tauopathies". Cell. Mol. Life Sci. 64 (17): 2219–33. doi:10.1007/s00018-007-7220-x. PMID 17604998.
- ↑ Sun W, Samimi H, Gamez M, Zare H, Frost B (August 2018). "Pathogenic tau-induced piRNA depletion promotes neuronal death through transposable element dysregulation in neurodegenerative tauopathies". Nature Neuroscience. 21 (8): 1038–48. doi:10.1038/s41593-018-0194-1. PMC 6095477. PMID 30038280.
- ↑ Van Broeck B, Van Broeckhoven C, Kumar-Singh S (2007). "Current insights into molecular mechanisms of Alzheimer disease and their implications for therapeutic approaches". Neurodegener Dis. 4 (5): 349–65. doi:10.1159/000105156. PMID 17622778.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Yankner BA, Duffy LK, Kirschner DA (October 1990). "Neurotrophic and neurotoxic effects of amyloid beta protein: reversal by tachykinin neuropeptides". Science (journal). 250 (4978): 279–82. doi:10.1126/science.2218531. PMID 2218531.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Chen X, Yan SD (December 2006). "Mitochondrial Abeta: a potential cause of metabolic dysfunction in Alzheimer's disease". IUBMB Life. 58 (12): 686–94. doi:10.1080/15216540601047767. PMID 17424907.
- ↑ Greig NH, Mattson MP, Perry T; และคณะ (December 2004). "New therapeutic strategies and drug candidates for neurodegenerative diseases: p53 and TNF-alpha inhibitors, and GLP-1 receptor agonists". Ann. N. Y. Acad. Sci. 1035: 290–315. doi:10.1196/annals.1332.018. PMID 15681814.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Heneka MT, Carson MJ, El Khoury J, Landreth GE, Brosseron F, Feinstein DL, และคณะ (April 2015). "Neuroinflammation in Alzheimer's disease". The Lancet. Neurology. 14 (4): 388–405. doi:10.1016/S1474-4422(15)70016-5. PMC 5909703. PMID 25792098.
- ↑ Tapia-Arancibia L, Aliaga E, Silhol M, Arancibia S (November 2008). "New insights into brain BDNF function in normal aging and Alzheimer disease". Brain Research Reviews. 59 (1): 201–20. doi:10.1016/j.brainresrev.2008.07.007. PMID 18708092.
- ↑ Schindowski K, Belarbi K, Buée L (February 2008). "Neurotrophic factors in Alzheimer's disease: role of axonal transport". Genes, Brain, and Behavior. 7 (Suppl 1): 43–56. doi:10.1111/j.1601-183X.2007.00378.x. PMC 2228393. PMID 18184369.
- ↑ Mendez MF (2006). "The accurate diagnosis of early-onset dementia". International Journal of Psychiatry Medicine. 36 (4): 401–412. doi:10.2190/Q6J4-R143-P630-KW41. PMID 17407994.
- ↑ Klafki HW, Staufenbiel M, Kornhuber J, Wiltfang J (November 2006). "Therapeutic approaches to Alzheimer's disease". Brain. 129 (Pt 11): 2840–55. doi:10.1093/brain/awl280. PMID 17018549.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Dementia: Quick reference guide" (PDF). London: (UK) National Institute for Health and Clinical Excellence. November 2006. ISBN 1-84629-312-X. สืบค้นเมื่อ 2008-02-22.
- ↑ Schroeter ML, Stein T, Maslowski N, Neumann J (October 2009). "Neural correlates of Alzheimer's disease and mild cognitive impairment: a systematic and quantitative meta-analysis involving 1351 patients". NeuroImage. 47 (4): 1196–206. doi:10.1016/j.neuroimage.2009.05.037. PMC 2730171. PMID 19463961.
- ↑ 131.0 131.1 McKhann G, Drachman D, Folstein M, Katzman R, Price D, Stadlan EM (July 1984). "Clinical diagnosis of Alzheimer's disease: report of the NINCDS-ADRDA Work Group under the auspices of Department of Health and Human Services Task Force on Alzheimer's Disease". Neurology. 34 (7): 939–44. PMID 6610841.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 132.0 132.1 Dubois B, Feldman HH, Jacova C, Dekosky ST, Barberger-Gateau P, Cummings J, และคณะ (August 2007). "Research criteria for the diagnosis of Alzheimer's disease: revising the NINCDS-ADRDA criteria". The Lancet. Neurology. 6 (8): 734–46. doi:10.1016/S1474-4422(07)70178-3. PMID 17616482.
- ↑ Blacker D, Albert MS, Bassett SS, Go RC, Harrell LE, Folstein MF (December 1994). "Reliability and validity of NINCDS-ADRDA criteria for Alzheimer's disease. The National Institute of Mental Health Genetics Initiative". Arch. Neurol. 51 (12): 1198–204. PMID 7986174.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ American Psychiatric Association (2000). Diagnostic and statistical manual of mental disorders: DSM-IV-TR (4th Edition Text Revision ed.). Washington DC: American Psychiatric Association. ISBN 0890420254.
- ↑ Ito N (May 1996). "[Clinical aspects of dementia]". Hokkaido Igaku Zasshi (ภาษาญี่ปุ่น). 71 (3): 315–20. PMID 8752526.
- ↑ Tombaugh TN, McIntyre NJ (September 1992). "The mini-mental state examination: a comprehensive review". J Am Geriatr Soc. 40 (9): 922–35. PMID 1512391.
- ↑ Pasquier F (January 1999). "Early diagnosis of dementia: neuropsychology". J. Neurol. 246 (1): 6–15. doi:10.1007/s004150050299. PMID 9987708.
- ↑ Harvey PD, Moriarty PJ, Kleinman L; และคณะ (2005). "The validation of a caregiver assessment of dementia: the Dementia Severity Scale". Alzheimer Dis Assoc Disord. 19 (4): 186–94. doi:10.1097/01.wad.0000189034.43203.60. PMID 16327345.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Antoine C, Antoine P, Guermonprez P, Frigard B (2004). "[Awareness of deficits and anosognosia in Alzheimer's disease.]". Encephale (ภาษาฝรั่งเศส). 30 (6): 570–7. PMID 15738860.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Cruz VT, Pais J, Teixeira A, Nunes B (2004). "[The initial symptoms of Alzheimer disease: caregiver perception]". Acta Med Port (ภาษาโปรตุเกส). 17 (6): 435–44. PMID 16197855.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Clarfield AM (October 2003). "The decreasing prevalence of reversible dementias: an updated meta-analysis". Arch. Intern. Med. 163 (18): 2219–29. doi:10.1001/archinte.163.18.2219. PMID 14557220.
- ↑ Geldmacher DS, Whitehouse PJ (May 1997). "Differential diagnosis of Alzheimer's disease". Neurology. 48 (5 Suppl 6): S2–9. PMID 9153154.
- ↑ Potter GG, Steffens DC (May 2007). "Contribution of depression to cognitive impairment and dementia in older adults". Neurologist. 13 (3): 105–17. doi:10.1097/01.nrl.0000252947.15389.a9. PMID 17495754.
- ↑ Zhang S, Smailagic N, Hyde C, Noel-Storr AH, Takwoingi Y, McShane R, Feng J (July 2014). "(11)C-PIB-PET for the early diagnosis of Alzheimer's disease dementia and other dementias in people with mild cognitive impairment (MCI)". The Cochrane Database of Systematic Reviews (7): CD010386. doi:10.1002/14651858.CD010386.pub2. PMC 6464750. PMID 25052054.
- ↑ Smailagic N, Vacante M, Hyde C, Martin S, Ukoumunne O, Sachpekidis C (January 2015). "¹⁸F-FDG PET for the early diagnosis of Alzheimer's disease dementia and other dementias in people with mild cognitive impairment (MCI)". The Cochrane Database of Systematic Reviews. 1: CD010632. doi:10.1002/14651858.CD010632.pub2. PMID 25629415.
- ↑ 146.0 146.1 Hu N, Yu JT, Tan L, Wang YL, Sun L, Tan L (2013). "Nutrition and the risk of Alzheimer's disease". BioMed Research International (Review). 2013: 1–12. doi:10.1155/2013/524820. PMC 3705810. PMID 23865055.
- ↑ Solfrizzi V, Panza F, Frisardi V, Seripa D, Logroscino G, Imbimbo BP, Pilotto A (May 2011). "Diet and Alzheimer's disease risk factors or prevention: the current evidence". Expert Review of Neurotherapeutics. 11 (5): 677–708. doi:10.1586/ern.11.56. PMID 21539488.
- ↑ Kanoski SE, Davidson TL (April 2011). "Western diet consumption and cognitive impairment: links to hippocampal dysfunction and obesity". Physiology & Behavior (Review). 103 (1): 59–68. doi:10.1016/j.physbeh.2010.12.003. PMC 3056912. PMID 21167850.
- ↑ Solfrizzi V, Capurso C, D'Introno A, Colacicco AM, Santamato A, Ranieri M, Fiore P, Capurso A, Panza F (January 2008). "Lifestyle-related factors in predementia and dementia syndromes". Expert Review of Neurotherapeutics. 8 (1): 133–58. doi:10.1586/14737175.8.1.133. PMID 18088206.
- ↑ Santos C, Costa J, Santos J, Vaz-Carneiro A, Lunet N (2010). "Caffeine intake and dementia: systematic review and meta-analysis". Journal of Alzheimer's Disease. 20 Suppl 1: S187–204. doi:10.3233/JAD-2010-091387. PMID 20182026.
- ↑ Nehlig A (March 2013). "The neuroprotective effects of cocoa flavanol and its influence on cognitive performance". British Journal of Clinical Pharmacology (Review). 75 (3): 716–27. doi:10.1111/j.1365-2125.2012.04378.x. PMC 3575938. PMID 22775434.
- ↑ Stoclet JC, Schini-Kerth V (March 2011). "[Dietary flavonoids and human health]". Annales Pharmaceutiques Francaises. 69 (2): 78–90. doi:10.1016/j.pharma.2010.11.004. PMID 21440100.
- ↑ Ono K, Yamada M (April 2012). "Vitamin A and Alzheimer's disease". Geriatrics & Gerontology International (Review). 12 (2): 180–88. doi:10.1111/j.1447-0594.2011.00786.x. PMID 22221326.
- ↑ Lerner AJ, Gustaw-Rothenberg K, Smyth S, Casadesus G (March –April 2012). "Retinoids for treatment of Alzheimer's disease". BioFactors. 38 (2): 84–89. doi:10.1002/biof.196. PMID 22419567.
{{cite journal}}: ตรวจสอบค่าวันที่ใน:|date=(help) - ↑ Heo JH, Lee KM (March 2013). "The possible role of antioxidant vitamin C in Alzheimer's disease treatment and prevention". American Journal of Alzheimer's Disease and Other Dementias (Review). 28 (2): 120–25. doi:10.1177/1533317512473193. PMID 23307795.
- ↑ Boothby LA, Doering PL (December 2005). "Vitamin C and vitamin E for Alzheimer's disease". The Annals of Pharmacotherapy. 39 (12): 2073–80. doi:10.1345/aph.1E495. PMID 16227450.
- ↑ 157.0 157.1 Farina N, Llewellyn D, Isaac MG, Tabet N (April 2017). "Vitamin E for Alzheimer's dementia and mild cognitive impairment". The Cochrane Database of Systematic Reviews. 4: CD002854. doi:10.1002/14651858.CD002854.pub5. PMC 6478142. PMID 28418065.
- ↑ Loef M, Schrauzer GN, Walach H (2011). "Selenium and Alzheimer's disease: a systematic review". Journal of Alzheimer's Disease (Review). 26 (1): 81–104. doi:10.3233/JAD-2011-110414. PMID 21593562.
- ↑ Loef M, von Stillfried N, Walach H (September 2012). "Zinc diet and Alzheimer's disease: a systematic review". Nutritional Neuroscience (Review). 15 (5): 2–12. doi:10.1179/1476830512Y.0000000010. PMID 22583839.
- ↑ Avan A, Hoogenraad TU (2015). "Zinc and Copper in Alzheimer's Disease". Journal of Alzheimer's Disease (Review). 46 (1): 89–92. doi:10.3233/JAD-150186. PMID 25835420.
- ↑ Malouf R, Grimley Evans J (October 2008). "Folic acid with or without vitamin B12 for the prevention and treatment of healthy elderly and demented people". The Cochrane Database of Systematic Reviews (4): CD004514. doi:10.1002/14651858.CD004514.pub2. PMID 18843658.
- ↑ Wald DS, Kasturiratne A, Simmonds M (June 2010). "Effect of folic acid, with or without other B vitamins, on cognitive decline: meta-analysis of randomized trials". The American Journal of Medicine. 123 (6): 522–527.e2. doi:10.1016/j.amjmed.2010.01.017. PMID 20569758.
- ↑ Cunnane SC, Chouinard-Watkins R, Castellano CA, Barberger-Gateau P (January 2013). "Docosahexaenoic acid homeostasis, brain aging and Alzheimer's disease: Can we reconcile the evidence?". Prostaglandins, Leukotrienes, and Essential Fatty Acids. 88 (1): 61–70. doi:10.1016/j.plefa.2012.04.006. PMID 22575581.
- ↑ Burckhardt M, Herke M, Wustmann T, Watzke S, Langer G, Fink A (April 2016). "Omega-3 fatty acids for the treatment of dementia". The Cochrane Database of Systematic Reviews. 4: CD009002. doi:10.1002/14651858.CD009002.pub3. PMID 27063583.
- ↑ เคอร์คิวมินในอาหาร:
- Garcia-Alloza M, Borrelli LA, Rozkalne A, Hyman BT, Bacskai BJ (2007). "Curcumin labels amyloid pathology in vivo, disrupts existing plaques, and partially restores distorted neurites in an Alzheimer mouse model". Journal of Neurochemistry. 102 (4): 1095–1104. doi:10.1111/j.1471-4159.2007.04613.x. PMID 17472706.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - Lim GP, Chu T, Yang F, Beech W, Frautschy SA, Cole GM (2001). "The curry spice curcumin reduces oxidative damage and amyloid pathology in an Alzheimer transgenic mouse". Journal of Neuroscience. 21 (21): 8370–8377. PMID 11606625.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- Garcia-Alloza M, Borrelli LA, Rozkalne A, Hyman BT, Bacskai BJ (2007). "Curcumin labels amyloid pathology in vivo, disrupts existing plaques, and partially restores distorted neurites in an Alzheimer mouse model". Journal of Neurochemistry. 102 (4): 1095–1104. doi:10.1111/j.1471-4159.2007.04613.x. PMID 17472706.
- ↑ Birks J, Grimley Evans J (2007). "Ginkgo biloba for cognitive impairment and dementia". Cochrane Database Syst Rev (2): CD003120. doi:10.1002/14651858.CD003120.pub2. PMID 17443523. สืบค้นเมื่อ 2008-02-22.
- ↑ Krishnan S, Cairns R, Howard R (April 2009). Krishnan S (บ.ก.). "Cannabinoids for the treatment of dementia". The Cochrane Database of Systematic Reviews (2): CD007204. doi:10.1002/14651858.CD007204.pub2. PMID 19370677.
- ↑ Bilkei-Gorzo A (December 2012). "The endocannabinoid system in normal and pathological brain ageing". Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 367 (1607): 3326–41. doi:10.1098/rstb.2011.0388. PMC 3481530. PMID 23108550.
- ↑ Rosendorff C, Beeri MS, Silverman JM (2007). "Cardiovascular risk factors for Alzheimer's disease". Am J Geriatr Cardiol. 16 (3): 143–9. doi:10.1111/j.1076-7460.2007.06696.x. PMID 17483665.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Patterson C, Feightner JW, Garcia A, Hsiung GY, MacKnight C, Sadovnick AD (February 2008). "Diagnosis and treatment of dementia: 1. Risk assessment and primary prevention of Alzheimer disease". CMAJ. 178 (5): 548–56. doi:10.1503/cmaj.070796. PMC 2244657. PMID 18299540.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Reiss AB, Wirkowski E (2007). "Role of HMG-CoA reductase inhibitors in neurological disorders : progress to date". Drugs. 67 (15): 2111–20. doi:10.2165/00003495-200767150-00001. PMID 17927279.
- ↑ Kuller LH (August 2007). "Statins and dementia". Curr Atheroscler Rep. 9 (2): 154–61. doi:10.1007/s11883-007-0012-9. PMID 17877925.
- ↑ Szekely CA, Breitner JC, Fitzpatrick AL; และคณะ (January 2008). "NSAID use and dementia risk in the Cardiovascular Health Study: role of APOE and NSAID type". Neurology. 70 (1): 17–24. doi:10.1212/01.wnl.0000284596.95156.48. PMID 18003940.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Hoozemans JJ, Veerhuis R, Rozemuller JM, Eikelenboom P (February 2011). "Soothing the inflamed brain: effect of non-steroidal anti-inflammatory drugs on Alzheimer's disease pathology". CNS & Neurological Disorders Drug Targets. 10 (1): 57–67. doi:10.2174/187152711794488665. PMID 21143138.
- ↑ Craig MC, Murphy DG (October 2007). "Estrogen: effects on normal brain function and neuropsychiatric disorders". Climacteric. 10 Suppl 2: 97–104. doi:10.1080/13697130701598746. PMID 17882683.
- ↑ Mori K, Takeda M (September 2007). "[Hormone replacement Up-to-date. Hormone replacement therapy and brain function]". Clin Calcium (ภาษาญี่ปุ่น). 17 (9): 1349–54. PMID 17767023.
- ↑ Verghese J, Lipton RB, Katz MJ; และคณะ (June 2003). "Leisure activities and the risk of dementia in the elderly". N. Engl. J. Med. 348 (25): 2508–16. doi:10.1056/NEJMoa022252. PMID 12815136.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bennett DA, Schneider JA, Tang Y, Arnold SE, Wilson RS (2006). "The effect of social networks on the relation between Alzheimer's disease pathology and level of cognitive function in old people: a longitudinal cohort study". Lancet Neurol. 5 (5): 406–412. doi:10.1016/S1474-4422(06)70417-3. PMID 16632311.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 179.0 179.1 Paradise M, Cooper C, Livingston G (February 2009). "Systematic review of the effect of education on survival in Alzheimer's disease". International Psychogeriatrics. 21 (1): 25–32. doi:10.1017/S1041610208008053. PMID 19026089.
- ↑ Bialystok E, Craik FIM, Freedman M (2007). "Bilingualism as a protection against the onset of symptoms of dementia". Neuropsychologia. 42 (2): 459–464. doi:10.1016/j.neuropsychologia.2006.10.009.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Cheng ST (September 2016). "Cognitive Reserve and the Prevention of Dementia: the Role of Physical and Cognitive Activities". Current Psychiatry Reports. 18 (9): 85. doi:10.1007/s11920-016-0721-2. PMC 4969323. PMID 27481112.
- ↑ Farina N, Rusted J, Tabet N (January 2014). "The effect of exercise interventions on cognitive outcome in Alzheimer's disease: a systematic review". International Psychogeriatrics. 26 (1): 9–18. doi:10.1017/S1041610213001385. PMID 23962667.
- ↑ 183.0 183.1 183.2 Birks JS, Harvey RJ (June 2018). "Donepezil for dementia due to Alzheimer's disease". The Cochrane Database of Systematic Reviews. 6: CD001190. doi:10.1002/14651858.CD001190.pub3. PMC 6513124. PMID 29923184.
- ↑ 184.0 184.1 Birks JS, Grimley Evans J (April 2015). "Rivastigmine for Alzheimer's disease". The Cochrane Database of Systematic Reviews (4): CD001191. doi:10.1002/14651858.CD001191.pub3. PMID 25858345.
- ↑ Geula C, Mesulam MM (1995). "Cholinesterases and the pathology of Alzheimer disease". Alzheimer Dis Assoc Disord. 9 Suppl 2: 23–28. PMID 8534419.
- ↑ Stahl SM (2000). "The new cholinesterase inhibitors for Alzheimer's disease, Part 2: illustrating their mechanisms of action". J Clin Psychiatry. 61 (11): 813–814. PMID 11105732.
- ↑ 187.0 187.1 Birks J (January 2006). Birks J (บ.ก.). "Cholinesterase inhibitors for Alzheimer's disease". The Cochrane Database of Systematic Reviews (1): CD005593. doi:10.1002/14651858.CD005593. PMID 16437532.
- ↑ Raschetti R, Albanese E, Vanacore N, Maggini M (November 2007). "Cholinesterase inhibitors in mild cognitive impairment: a systematic review of randomised trials". PLoS Medicine. 4 (11): e338. doi:10.1371/journal.pmed.0040338. PMC 2082649. PMID 18044984.
- ↑ Alldredge BK, Corelli RL, Ernst ME, Guglielmo BJ, Jacobson PA, Kradjan WA, Williams BR (2013). Applied therapeutics : the clinical use of drugs (10th ed.). Baltimore: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 2385. ISBN 978-1-60913-713-7.
- ↑ 190.0 190.1 Lipton SA (2006). "Paradigm shift in neuroprotection by NMDA receptor blockade: memantine and beyond". Nat Rev Drug Discov. 5 (2): 160–170. doi:10.1038/nrd1958. PMID 16424917.
- ↑ "Memantine". US National Library of Medicine (Medline). 2004-01-04. สืบค้นเมื่อ 2008-03-22.
- ↑ Areosa Sastre A, McShane R, Sherriff F (2004). "Memantine for dementia". Cochrane Database Syst Rev (4): CD003154. doi:10.1002/14651858.CD003154.pub2. PMID 15495043.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Namenda Prescribing Information" (PDF). Forest Pharmaceuticals. สืบค้นเมื่อ 2008-02-19.
- ↑ Raina P, Santaguida P, Ismaila A; และคณะ (2008). "Effectiveness of cholinesterase inhibitors and memantine for treating dementia: evidence review for a clinical practice guideline". Annals of Internal Medicine. 148 (5): 379–397. PMID 18316756.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ การใช้ยาระงับอาการทางจิต:
- Ballard C, Waite J (2006). "The effectiveness of atypical antipsychotics for the treatment of aggression and psychosis in Alzheimer's disease". Cochrane Database Syst Rev (1): CD003476. doi:10.1002/14651858.CD003476.pub2. PMID 16437455.
- Ballard C, Lana MM, Theodoulou M; และคณะ (2008). "A Randomised, Blinded, Placebo-Controlled Trial in Dementia Patients Continuing or Stopping Neuroleptics (The DART-AD Trial)". PLoS Med. 5 (4): e76. doi:10.1371/journal.pmed.0050076. PMID 18384230.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - Sink KM, Holden KF, Yaffe K (2005). "Pharmacological treatment of neuropsychiatric symptoms of dementia: a review of the evidence". JAMA. 293 (5): 596–608. doi:10.1001/jama.293.5.596. PMID 15687315.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ 196.0 196.1
Ballard C, Hanney ML, Theodoulou M, Douglas S, McShane R, Kossakowski K, Gill R, Juszczak E, Yu L-M, Jacoby R (9 January 2009). "The dementia antipsychotic withdrawal trial (DART-AD) : long-term follow-up of a randomised placebo-controlled trial". Lancet Neurology. 8: 151. doi:10.1016/S1474-4422(08)70295-3. PMID 19138567.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Declercq T, Petrovic M, Azermai M, Vander Stichele R, De Sutter AI, van Driel ML, Christiaens T (March 2013). "Withdrawal versus continuation of chronic antipsychotic drugs for behavioural and psychological symptoms in older people with dementia". The Cochrane Database of Systematic Reviews. 3 (3): CD007726. doi:10.1002/14651858.CD007726.pub2. hdl:1854/LU-3109108. PMID 23543555.
- ↑ Li J, Wu HM, Zhou RL, Liu GJ, Dong BR (April 2008). "Huperzine A for Alzheimer's disease". The Cochrane Database of Systematic Reviews (2): CD005592. doi:10.1002/14651858.CD005592.pub2. PMID 18425924.
- ↑ 199.0 199.1 199.2 199.3 199.4 199.5 199.6 "Practice Guideline for the Treatment of Patients with Alzheimer's disease and Other Dementias" (PDF). American Psychiatric Association. October 2007. doi:10.1176/appi.books.9780890423967.152139. สืบค้นเมื่อ 2007-12-28.
- ↑ Bottino CM, Carvalho IA, Alvarez AM; และคณะ (2005). "Cognitive rehabilitation combined with drug treatment in Alzheimer's disease patients: a pilot study". Clin Rehabil. 19 (8): 861–869. doi:10.1191/0269215505cr911oa. PMID 16323385.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Doody RS, Stevens JC, Beck C; และคณะ (2001). "Practice parameter: management of dementia (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology". Neurology. 56 (9): 1154–1166. PMID 11342679.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Hermans DG, Htay UH, McShane R (2007). "Non-pharmacological interventions for wandering of people with dementia in the domestic setting". Cochrane Database Syst Rev (1): CD005994. doi:10.1002/14651858.CD005994.pub2. PMID 17253573.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Robinson L, Hutchings D, Dickinson HO; และคณะ (2007). "Effectiveness and acceptability of non-pharmacological interventions to reduce wandering in dementia: a systematic review". Int J Geriatr Psychiatry. 22 (1): 9–22. doi:10.1002/gps.1643. PMID 17096455.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Abraha I, Rimland JM, Trotta FM, Dell'Aquila G, Cruz-Jentoft A, Petrovic M, Gudmundsson A, Soiza R, O'Mahony D, Guaita A, Cherubini A (March 2017). "Systematic review of systematic reviews of non-pharmacological interventions to treat behavioural disturbances in older patients with dementia. The SENATOR-OnTop series". BMJ Open. 7 (3): e012759. doi:10.1136/bmjopen-2016-012759. PMC 5372076. PMID 28302633.
- ↑ Chung JC, Lai CK, Chung PM, French HP (2002). "Snoezelen for dementia". The Cochrane Database of Systematic Reviews (4): CD003152. doi:10.1002/14651858.CD003152. PMID 12519587.
- ↑ Woods B, O'Philbin L, Farrell EM, Spector AE, Orrell M (March 2018). "Reminiscence therapy for dementia". The Cochrane Database of Systematic Reviews. 3: CD001120. doi:10.1002/14651858.CD001120.pub3. PMC 6494367. PMID 29493789.
- ↑ Peak JS, Cheston RI (2002). "Using simulated presence therapy with people with dementia". Aging Ment Health. 6 (1): 77–81. doi:10.1080/13607860120101095. PMID 11827626.
- ↑ Camberg L, Woods P, Ooi WL; และคณะ (1999). "Evaluation of Simulated Presence: a personalised approach to enhance well-being in persons with Alzheimer's disease". J Am Geriatr Soc. 47 (4): 446–452. PMID 10203120.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Neal M, Briggs M (2003). "Validation therapy for dementia". Cochrane Database Syst Rev (3): CD001394. doi:10.1002/14651858.CD001394. PMID 12917907.
- ↑ Chung JC, Lai CK, Chung PM, French HP (2002). "Snoezelen for dementia". Cochrane Database Syst Rev (4): CD003152. doi:10.1002/14651858.CD003152. PMID 12519587.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Spector A, Orrell M, Davies S, Woods B (2000). "Withdrawn: Reality orientation for dementia". Cochrane Database Syst Rev (3): CD001119. doi:10.1002/14651858.CD001119.pub2. PMID 17636652.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Spector A, Thorgrimsen L, Woods B; และคณะ (2003). "Efficacy of an evidence-based cognitive stimulation therapy programme for people with dementia: randomised controlled trial". Br J Psychiatry. 183: 248–254. doi:10.1192/bjp.183.3.248. PMID 12948999.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Chang CH, Lane HY, Lin CH (2018). "Brain Stimulation in Alzheimer's Disease". Frontiers in Psychiatry. 9: 201. doi:10.3389/fpsyt.2018.00201. PMC 5992378. PMID 29910746.แม่แบบ:CC-notice
- ↑ Gitlin LN, Corcoran M, Winter L, Boyce A, Hauck WW (February 2001). "A randomized, controlled trial of a home environmental intervention: effect on efficacy and upset in caregivers and on daily function of persons with dementia". The Gerontologist. 41 (1): 4–14. doi:10.1093/geront/41.1.4. PMID 11220813.
- ↑ Gitlin LN, Hauck WW, Dennis MP, Winter L (March 2005). "Maintenance of effects of the home environmental skill-building program for family caregivers and individuals with Alzheimer's disease and related disorders". J. Gerontol. A Biol. Sci. Med. Sci. 60 (3): 368–74. PMID 15860476.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Treating Behavioral and Psychiatric Symptoms". Alzheimer's Association. 2006. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 25 September 2006. สืบค้นเมื่อ 25 September 2006.
- ↑ Dunne TE, Neargarder SA, Cipolloni PB, Cronin-Golomb A (August 2004). "Visual contrast enhances food and liquid intake in advanced Alzheimer's disease". Clinical Nutrition. 23 (4): 533–538. doi:10.1016/j.clnu.2003.09.015. PMID 15297089.
- ↑ Dudek SB (2007). Nutrition Essentials for Nursing Practice. Hagerstown, Maryland: Lippincott Williams & Wilkins. p. 360. ISBN 978-0-7817-6651-7. สืบค้นเมื่อ 19 August 2008.
- ↑ Dennehy C (2006). "Analysis of patients' rights: dementia and PEG insertion". British Journal of Nursing. 15 (1): 18–20. doi:10.12968/bjon.2006.15.1.20303. PMID 16415742.
- ↑ Chernoff R (April 2006). "Tube feeding patients with dementia". Nutrition in Clinical Practice. 21 (2): 142–146. doi:10.1177/0115426506021002142. PMID 16556924. S2CID 20841502.
- ↑ ปัญหาทางการแพทย์:
- Head B (January 2003). "Palliative care for persons with dementia". Home Healthc Nurse. 21 (1): 53–60, quiz 61. doi:10.1097/00004045-200301000-00012. PMID 12544465.
- Friedlander AH, Norman DC, Mahler ME, Norman KM, Yagiela JA (September 2006). "Alzheimer's disease: psychopathology, medical management and dental implications". J Am Dent Assoc. 137 (9): 1240–51. PMID 16946428.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - Belmin J (2007). "Practical guidelines for the diagnosis and management of weight loss in Alzheimer's disease: a consensus from appropriateness ratings of a large expert panel". J Nutr Health Aging. 11 (1): 33–7. PMID 17315078.
- McCurry SM, Gibbons LE, Logsdon RG, Vitiello M, Teri L (October 2003). "Training caregivers to change the sleep hygiene practices of patients with dementia: the NITE-AD project". J Am Geriatr Soc. 51 (10): 1455–60. doi:10.1046/j.1532-5415.2003.51466.x. PMID 14511168.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - Perls TT, Herget M (December 1995). "Higher respiratory infection rates on an Alzheimer's special care unit and successful intervention". J Am Geriatr Soc. 43 (12): 1341–4. PMID 7490383.
- ↑ Shega JW, Levin A, Hougham GW; และคณะ (April 2003). "Palliative Excellence in Alzheimer Care Efforts (PEACE) : a program description". J Palliat Med. 6 (2): 315–20. doi:10.1089/109662103764978641. PMID 12854952.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 223.0 223.1 Zanetti O, Solerte SB, Cantoni F (2009). "Life expectancy in Alzheimer's disease (AD)". Archives of Gerontology and Geriatrics. 49 Suppl 1: 237–43. doi:10.1016/j.archger.2009.09.035. PMID 19836639.
- ↑ 224.0 224.1 Mölsä PK, Marttila RJ, Rinne UK (March 1995). "Long-term survival and predictors of mortality in Alzheimer's disease and multi-infarct dementia". Acta Neurologica Scandinavica. 91 (3): 159–64. doi:10.1111/j.1600-0404.1995.tb00426.x. PMID 7793228.
- ↑ Larson EB, Shadlen MF, Wang L; และคณะ (April 2004). "Survival after initial diagnosis of Alzheimer disease". Ann. Intern. Med. 140 (7): 501–9. PMID 15068977.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jagger C, Clarke M, Stone A (January 1995). "Predictors of survival with Alzheimer's disease: a community-based study". Psychol Med. 25 (1): 171–7. PMID 7792352.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Dodge HH, Shen C, Pandav R, DeKosky ST, Ganguli M (February 2003). "Functional transitions and active life expectancy associated with Alzheimer disease". Archives of Neurology. 60 (2): 253–59. doi:10.1001/archneur.60.2.253. PMID 12580712.
- ↑ 228.0 228.1 Ganguli M, Dodge HH, Shen C, Pandav RS, DeKosky ST (May 2005). "Alzheimer disease and mortality: a 15-year epidemiological study". Arch. Neurol. 62 (5): 779–84. doi:10.1001/archneur.62.5.779. PMID 15883266.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 229.0 229.1 229.2 Bermejo-Pareja F, Benito-León J, Vega S, Medrano MJ, Román GC (January 2008). "Incidence and subtypes of dementia in three elderly populations of central Spain". J. Neurol. Sci. 264 (1–2): 63–72. doi:10.1016/j.jns.2007.07.021. PMID 17727890.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 230.0 230.1 230.2 Di Carlo A, Baldereschi M, Amaducci L; และคณะ (January 2002). "Incidence of dementia, Alzheimer's disease, and vascular dementia in Italy. The ILSA Study". J Am Geriatr Soc. 50 (1): 41–8. doi:10.1046/j.1532-5415.2002.50006.x. PMID 12028245.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Andersen K, Launer LJ, Dewey ME; และคณะ (December 1999). "Gender differences in the incidence of AD and vascular dementia: The EURODEM Studies. EURODEM Incidence Research Group". Neurology. 53 (9): 1992–7. PMID 10599770.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Tejada-Vera B. (2013). Mortality from Alzheimer's Disease in the United States: Data for 2000 and 2010. Hyattsville, MD: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Center for Health Statistics.
- ↑ การประมาณในสหรัฐ ค.ศ. 2000:
- Hebert LE, Scherr PA, Bienias JL, Bennett DA, Evans DA (August 2003). "Alzheimer disease in the US population: prevalence estimates using the 2000 census". Arch. Neurol. 60 (8): 1119–22. doi:10.1001/archneur.60.8.1119. PMID 12925369.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - "Profiles of general demographic characteristics, 2000 census of population and housing, United States" (PDF). U.S. Census Bureau. 2001. สืบค้นเมื่อ 2008-08-27.
- Hebert LE, Scherr PA, Bienias JL, Bennett DA, Evans DA (August 2003). "Alzheimer disease in the US population: prevalence estimates using the 2000 census". Arch. Neurol. 60 (8): 1119–22. doi:10.1001/archneur.60.8.1119. PMID 12925369.
- ↑ 234.0 234.1 Ferri CP, Prince M, Brayne C; และคณะ (December 2005). "Global prevalence of dementia: a Delphi consensus study" (PDF). Lancet. 366 (9503): 2112–7. doi:10.1016/S0140-6736(05)67889-0. PMID 16360788. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2008-06-25. สืบค้นเมื่อ 2008-06-13.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ World Health Organization (2006). Neurological Disorders: Public Health Challenges. Switzerland: World Health Organization. pp. 204–207. ISBN 978-92-4-156336-9.
- ↑ 2006 prevalence estimate:
- Brookmeyer R, Johnson E, Ziegler-Graham K, MH Arrighi (July 2007). "Forecasting the global burden of Alzheimer's disease". Alzheimer's and Dementia. 3 (3): 186–91. doi:10.1016/j.jalz.2007.04.381. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2008-12-07. สืบค้นเมื่อ 2008-06-18.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - "World population prospects: the 2006 revision, highlights" (PDF). Working Paper No. ESA/P/WP.202. Population Division, Department of Economic and Social Affairs, United Nations. 2007. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2008-08-19. สืบค้นเมื่อ 2008-08-27.
{{cite journal}}: Cite journal ต้องการ|journal=(help)
- Brookmeyer R, Johnson E, Ziegler-Graham K, MH Arrighi (July 2007). "Forecasting the global burden of Alzheimer's disease". Alzheimer's and Dementia. 3 (3): 186–91. doi:10.1016/j.jalz.2007.04.381. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2008-12-07. สืบค้นเมื่อ 2008-06-18.
- ↑ 237.0 237.1 Berchtold NC, Cotman CW (1998). "Evolution in the conceptualization of dementia and Alzheimer's disease: Greco-Roman period to the 1960s". Neurobiology of Aging. 19 (3): 173–189. doi:10.1016/S0197-4580(98)00052-9. PMID 9661992.
- ↑ ออกุสต์ เด.:
- Alzheimer Alois (1907). "Über eine eigenartige Erkrankung der Hirnrinde [About a peculiar disease of the cerebral cortex]". Allgemeine Zeitschrift fur Psychiatrie und Psychisch-Gerichtlich Medizin (ภาษาเยอรมัน). 64 (1–2): 146–148.
- Alzheimer Alois (1987). "About a peculiar disease of the cerebral cortex. By Alois Alzheimer, 1907 (Translated by L. Jarvik and H. Greenson)". Alzheimer Dis Assoc Disord. 1 (1): 3–8. PMID 3331112.
- Maurer Ulrike, Maurer Konrad (2003). Alzheimer: the life of a physician and the career of a disease. New York: Columbia University Press. p. 270. ISBN 0-231-11896-1.
- ↑ Kraepelin Emil, Diefendorf A. Ross (translated by) (2007-01-17). Clinical Psychiatry: A Textbook For Students And Physicians (Reprint). Kessinger Publishing. p. 568. ISBN 1-4325-0833-4.
- ↑ Katzman R, Terry RD, Bick KL, บ.ก. (1978). Alzheimer's Disease: Senile Dementia and Related Disorders. New York: Raven Press. p. 595. ISBN 978-0-89004-225-0.
- ↑ Boller F, Forbes MM (June 1998). "History of dementia and dementia in history: an overview". Journal of the Neurological Sciences. 158 (2): 125–33. doi:10.1016/S0022-510X(98)00128-2. PMID 9702682.
- ↑ Amaducci LA, Rocca WA, Schoenberg BS (November 1986). "Origin of the distinction between Alzheimer's disease and senile dementia: how history can clarify nosology". Neurology. 36 (11): 1497–9. doi:10.1212/wnl.36.11.1497. PMID 3531918.
- ↑ Allegri RF, Butman J, Arizaga RL, Machnicki G, Serrano C, Taragano FE, Sarasola D, Lon L (August 2007). "Economic impact of dementia in developing countries: an evaluation of costs of Alzheimer-type dementia in Argentina". International Psychogeriatrics. 19 (4): 705–18. doi:10.1017/S1041610206003784. PMID 16870037.
- ↑ Suh GH, Knapp M, Kang CJ (August 2006). "The economic costs of dementia in Korea, 2002". International Journal of Geriatric Psychiatry. 21 (8): 722–28. doi:10.1002/gps.1552. PMID 16858741.
- ↑ Wimo A, Jonsson L, Winblad B (2006). "An estimate of the worldwide prevalence and direct costs of dementia in 2003". Dementia and Geriatric Cognitive Disorders. 21 (3): 175–81. doi:10.1159/000090733. PMID 16401889.
- ↑ 246.0 246.1 246.2 Moore MJ, Zhu CW, Clipp EC (July 2001). "Informal costs of dementia care: estimates from the National Longitudinal Caregiver Study". The Journals of Gerontology. Series B, Psychological Sciences and Social Sciences. 56 (4): S219–28. doi:10.1093/geronb/56.4.S219. PMID 11445614.
- ↑ Jönsson L, Eriksdotter Jönhagen M, Kilander L, Soininen H, Hallikainen M, Waldemar G, และคณะ (May 2006). "Determinants of costs of care for patients with Alzheimer's disease". International Journal of Geriatric Psychiatry. 21 (5): 449–59. doi:10.1002/gps.1489. PMID 16676288.
- ↑ 248.0 248.1 "The MetLife study of Alzheimer's disease: The caregiving experience" (PDF). MetLife Mature Market Institute. August 2006. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 8 January 2011. สืบค้นเมื่อ 5 February 2011.
- ↑ Schneider J, Murray J, Banerjee S, Mann A (August 1999). "EUROCARE: a cross-national study of co-resident spouse carers for people with Alzheimer's disease: I – Factors associated with carer burden". International Journal of Geriatric Psychiatry. 14 (8): 651–61. doi:10.1002/(SICI)1099-1166(199908)14:8<651::AID-GPS992>3.0.CO;2-B. PMID 10489656.
- ↑ Murray J, Schneider J, Banerjee S, Mann A (August 1999). "EUROCARE: a cross-national study of co-resident spouse carers for people with Alzheimer's disease: II – A qualitative analysis of the experience of caregiving". International Journal of Geriatric Psychiatry. 14 (8): 662–67. doi:10.1002/(SICI)1099-1166(199908)14:8<662::AID-GPS993>3.0.CO;2-4. PMID 10489657.
- ↑ 251.0 251.1 Zhu CW, Sano M (2006). "Economic considerations in the management of Alzheimer's disease". Clinical Interventions in Aging. 1 (2): 143–54. doi:10.2147/ciia.2006.1.2.143. PMC 2695165. PMID 18044111.
- ↑ Gaugler JE, Kane RL, Kane RA, Newcomer R (April 2005). "Early community-based service utilization and its effects on institutionalization in dementia caregiving". The Gerontologist. 45 (2): 177–85. doi:10.1093/geront/45.2.177. PMID 15799982.
- ↑ Ritchie K, Lovestone S (November 2002). "The dementias". Lancet. 360 (9347): 1759–66. doi:10.1016/S0140-6736(02)11667-9. PMID 12480441.
- ↑ Brodaty H, Hadzi-Pavlovic D (September 1990). "Psychosocial effects on carers of living with persons with dementia". The Australian and New Zealand Journal of Psychiatry. 24 (3): 351–61. doi:10.3109/00048679009077702. PMID 2241719.
- ↑ Donaldson C, Tarrier N, Burns A (April 1998). "Determinants of carer stress in Alzheimer's disease". International Journal of Geriatric Psychiatry. 13 (4): 248–56. doi:10.1002/(SICI)1099-1166(199804)13:4<248::AID-GPS770>3.0.CO;2-0. PMID 9646153.
- ↑ Pusey H, Richards D (May 2001). "A systematic review of the effectiveness of psychosocial interventions for carers of people with dementia". Aging & Mental Health. 5 (2): 107–19. doi:10.1080/13607860120038302. PMID 11511058.
- ↑ Bayley J (2000). Iris: A Memoir of Iris Murdoch. London: Abacus. ISBN 978-0-349-11215-2. OCLC 41960006.
- ↑ Sparks N (1996). The notebook. Thorndike, Maine: Thorndike Press. p. 268. ISBN 978-0-7862-0821-0.
- ↑ Ogiwara H (2004). Ashita no Kioku (ภาษาญี่ปุ่น). Tōkyō: Kōbunsha. ISBN 978-4-334-92446-1. OCLC 57352130.
- ↑ Munro A (2001). Hateship, Friendship, Courtship, Loveship, Marriage: Stories. New York: A.A. Knopf. ISBN 978-0-375-41300-1. OCLC 46929223.
- ↑ "Malcolm and Barbara: A love story". Dfgdocs. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 24 May 2008. สืบค้นเมื่อ 24 January 2008.
- ↑ "Malcolm and Barbara: A love story". BBC Cambridgeshire. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 10 November 2012. สืบค้นเมื่อ 2 March 2008.
- ↑ Plunkett J (7 August 2007). "Alzheimer's film-maker to face ITV lawyers". London: Guardian Media. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 15 January 2008. สืบค้นเมื่อ 24 January 2008.
- ↑ Cummings JL, Morstorf T, Zhong K (July 2014). "Alzheimer's disease drug-development pipeline: few candidates, frequent failures". Alzheimer's Research & Therapy. 6 (4): 37. doi:10.1186/alzrt269. PMC 4095696. PMID 25024750.
- ↑ Gutis, Phillip S. (22 March 2019). "An Alzheimer's Drug Trial Gave Me Hope, and Then It Ended". The New York Times. สืบค้นเมื่อ 25 March 2019.
- ↑ Lashuel HA, Hartley DM, Balakhaneh D, Aggarwal A, Teichberg S, Callaway DJ (พฤศจิกายน 2002). "New class of inhibitors of amyloid-beta fibril formation. Implications for the mechanism of pathogenesis in Alzheimer's disease". The Journal of Biological Chemistry. 277 (45): 42881–90. doi:10.1074/jbc.M206593200. PMID 12167652.
- ↑ Dodel R, Neff F, Noelker C, Pul R, Du Y, Bacher M, Oertel W (มีนาคม 2010). "Intravenous immunoglobulins as a treatment for Alzheimer's disease: rationale and current evidence". Drugs. 70 (5): 513–28. doi:10.2165/11533070-000000000-00000. PMID 20329802. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 17 กันยายน 2011.
- ↑ Vaccination:
- Hawkes CA, McLaurin J (November 2007). "Immunotherapy as treatment for Alzheimer's disease". Expert Review of Neurotherapeutics. 7 (11): 1535–48. doi:10.1586/14737175.7.11.1535. PMID 17997702.
- Solomon B (June 2007). "Clinical immunologic approaches for the treatment of Alzheimer's disease". Expert Opinion on Investigational Drugs. 16 (6): 819–28. doi:10.1517/13543784.16.6.819. PMID 17501694.
- Woodhouse A, Dickson TC, Vickers JC (2007). "Vaccination strategies for Alzheimer's disease: A new hope?". Drugs & Aging. 24 (2): 107–19. doi:10.2165/00002512-200724020-00003. PMID 17313199.
- ↑ "Study Evaluating ACC-001 in Mild to Moderate Alzheimers Disease Subjects". Clinical Trial. US National Institutes of Health. 11 March 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 30 July 2013. สืบค้นเมื่อ 5 June 2008.
- ↑ "Study Evaluating Safety, Tolerability, and Immunogenicity of ACC-001 in Subjects with Alzheimer's Disease". US National Institutes of Health. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 29 October 2008. สืบค้นเมื่อ 5 June 2008.
- ↑ "Alzheimer's Disease Vaccine Trial Suspended on Safety Concern". Medpage Today. 18 April 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 23 April 2008. สืบค้นเมื่อ 14 June 2008.
- ↑ "Bapineuzumab in Patients with Mild to Moderate Alzheimer's Disease/ Apo_e4 Non-carriers" (Clinical Trial). US National Institutes of Health. 29 February 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 22 March 2008. สืบค้นเมื่อ 23 March 2008.
- ↑ Sperling RA, Jack CR, Black SE, Frosch MP, Greenberg SM, Hyman BT, Scheltens P, Carrillo MC, Thies W, Bednar MM, Black RS, Brashear HR, Grundman M, Siemers ER, Feldman HH, Schindler RJ (July 2011). "Amyloid-related imaging abnormalities in amyloid-modifying therapeutic trials: recommendations from the Alzheimer's Association Research Roundtable Workgroup". Alzheimer's & Dementia. 7 (4): 367–85. doi:10.1016/j.jalz.2011.05.2351. PMC 3693547. PMID 21784348.
- ↑ "Safety, Tolerability and Efficacy Study to Evaluate Subjects with Mild Cognitive Impairment" (Clinical Trial). US National Institutes of Health. 11 March 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 22 October 2008. สืบค้นเมื่อ 23 March 2008.
- ↑ "Study Evaluating the Safety, Tolerability and Efficacy of PBT2 in Patients with Early Alzheimer's Disease" (Clinical Trial). US National Institutes of Health. 13 January 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 31 August 2008. สืบค้นเมื่อ 23 March 2008.
- ↑ Etanercept research:
- Tobinick E (September 2009). "Tumour necrosis factor modulation for treatment of Alzheimer's disease: rationale and current evidence". CNS Drugs. 23 (9): 713–25. doi:10.2165/11310810-000000000-00000. PMID 19689163.
- Tobinick E, Gross H, Weinberger A, Cohen H (April 2006). "TNF-alpha modulation for treatment of Alzheimer's disease: a 6-month pilot study". MedGenMed. 8 (2): 25. PMC 1785182. PMID 16926764.
- Griffin WS (January 2008). "Perispinal etanercept: potential as an Alzheimer therapeutic". Journal of Neuroinflammation. 5: 3. doi:10.1186/1742-2094-5-3. PMC 2241592. PMID 18186919.
- Tobinick E (December 2007). "Perispinal etanercept for treatment of Alzheimer's disease". Current Alzheimer Research. 4 (5): 550–52. doi:10.2174/156720507783018217. PMID 18220520.
- Cheng X, Shen Y, Li R (November 2014). "Targeting TNF: a therapeutic strategy for Alzheimer's disease". Drug Discovery Today. 19 (11): 1822–27. doi:10.1016/j.drudis.2014.06.029. PMID 24998784.
- ↑ Wischik CM, Bentham P, Wischik DJ, Seng KM (July 2008). "Tau aggregation inhibitor (TAI) therapy with remberTM arrests disease progression in mild and moderate Alzheimer's disease over 50 weeks". Alzheimer's & Dementia. 4 (4): T167. doi:10.1016/j.jalz.2008.05.438. สืบค้นเมื่อ 30 July 2008.
- ↑ Harrington C, Rickard J, Horsley D (July 2008). "Methylthioninium chloride (MTC) acts as a tau aggregation inhibitor (TAI) in a cellular model and reverses tau pathology in transgenic mouse models of Alzheimer's disease". Alzheimer's & Dementia. 4 (4): T120–21. doi:10.1016/j.jalz.2008.05.259.
- ↑ Doody RS, Gavrilova SI, Sano M, Thomas RG, Aisen PS, Bachurin SO, Seely L, Hung D (July 2008). "Effect of dimebon on cognition, activities of daily living, behaviour, and global function in patients with mild-to-moderate Alzheimer's disease: a randomised, double-blind, placebo-controlled study". Lancet. 372 (9634): 207–15. doi:10.1016/S0140-6736(08)61074-0. PMID 18640457.
- ↑ Bezprozvanny I (October 2010). "The rise and fall of Dimebon". Drug News & Perspectives (Original article). 23 (8): 518–23. doi:10.1358/dnp.2010.23.8.1500435. PMC 3922928. PMID 21031168.
- ↑ "Pfizer And Medivation announce results from two phase 3 studies in Dimebon (latrepirdine*) Alzheimer's disease clinical development program (NASDAQ:MDVN)" (Press release). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 4 September 2012. สืบค้นเมื่อ 16 November 2012.
- ↑ Wendler A, Wehling M (March 2012). "Translatability scoring in drug development: eight case studies". Journal of Translational Medicine. 10 (10): 39. doi:10.1186/1479-5876-10-39. PMC 3330010. PMID 22397594.
- ↑ Baddeley TC, McCaffrey J, Storey JM, Cheung JK, Melis V, Horsley D, Harrington CR, Wischik CM (January 2015). "Complex disposition of methylthioninium redox forms determines efficacy in tau aggregation inhibitor therapy for Alzheimer's disease". The Journal of Pharmacology and Experimental Therapeutics. 352 (1): 110–18. doi:10.1124/jpet.114.219352. PMID 25320049.
- ↑ Wischik CM, Harrington CR, Storey JM (April 2014). "Tau-aggregation inhibitor therapy for Alzheimer's disease". Biochemical Pharmacology. 88 (4): 529–39. doi:10.1016/j.bcp.2013.12.008. PMID 24361915.
- ↑ Marciniak R, Sheardova K, Cermáková P, Hudeček D, Sumec R, Hort J (2014). "Effect of meditation on cognitive functions in context of aging and neurodegenerative diseases". Frontiers in Behavioral Neuroscience. 8: 17. doi:10.3389/fnbeh.2014.00017. PMC 3903052. PMID 24478663.
- ↑ Larouche E, Hudon C, Goulet S (January 2015). "Potential benefits of mindfulness-based interventions in mild cognitive impairment and Alzheimer's disease: an interdisciplinary perspective". Behavioural Brain Research. 276 (276): 199–212. doi:10.1016/j.bbr.2014.05.058. PMID 24893317.
- ↑ 287.0 287.1 Martin C, Solís L, Concha MI, Otth C (June 2011). "[Herpes simplex virus type 1 as risk factor associated to Alzheimer disease]" [Herpes Simplex Virus Type 1 as Risk Factor Associated to Alzheimer Disease]. Revista Medica de Chile (ภาษาสเปน). 139 (6): 779–86. doi:10.4067/S0034-98872011000600013. PMID 22051760.
- ↑ Wozniak MA, Mee AP, Itzhaki RF (January 2009). "Herpes simplex virus type 1 DNA is located within Alzheimer's disease amyloid plaques". The Journal of Pathology (Original study). 217 (1): 131–38. doi:10.1002/path.2449. PMID 18973185.
- ↑ Itzhaki RF (2014). "Herpes simplex virus type 1 and Alzheimer's disease: increasing evidence for a major role of the virus". Frontiers in Aging Neuroscience. 6: 202. doi:10.3389/fnagi.2014.00202. PMC 4128394. PMID 25157230.
- ↑ Itzhaki RF, Lathe R, Balin BJ, Ball MJ, Bearer EL, Braak H, และคณะ (2016). "Microbes and Alzheimer's Disease". Journal of Alzheimer's Disease. 51 (4): 979–84. doi:10.3233/JAD-160152. PMC 5457904. PMID 26967229. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 10 พฤศจิกายน 2016.
- ↑ Alonso R, Pisa D, Rábano A, Carrasco L (July 2014). "Alzheimer's disease and disseminated mycoses". European Journal of Clinical Microbiology & Infectious Diseases. 33 (7): 1125–32. doi:10.1007/s10096-013-2045-z. PMID 24452965.
- ↑ 292.0 292.1 Pisa D, Alonso R, Rábano A, Rodal I, Carrasco L (ตุลาคม 2015). "Different Brain Regions are Infected with Fungi in Alzheimer's Disease". Scientific Reports. 5: 15015. Bibcode:2015NatSR...515015P. doi:10.1038/srep15015. PMC 4606562. PMID 26468932.
- ↑ "Fungus, the bogeyman". The Economist. 22 ตุลาคม 2015. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 8 สิงหาคม 2017.
- ↑ Kumar DK, Choi SH, Washicosky KJ, Eimer WA, Tucker S, Ghofrani J, Lefkowitz A, McColl G, Goldstein LE, Tanzi RE, Moir RD (May 2016). "Amyloid-β peptide protects against microbial infection in mouse and worm models of Alzheimer's disease". Science Translational Medicine. 8 (340): 340ra72. doi:10.1126/scitranslmed.aaf1059. PMC 5505565. PMID 27225182.
- ↑ Kolata, Gina (25 พฤษภาคม 2016). "Could Alzheimer's Stem From Infections? It Makes Sense, Experts Say". The New York Times. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 4 กุมภาพันธ์ 2017.
- ↑ "Alzheimer's culprit may fight other diseases". Science News. 16 มิถุนายน 2016. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 26 พฤษภาคม 2016.
- ↑ Jaunmuktane Z, Mead S, Ellis M, Wadsworth JD, Nicoll AJ, Kenny J, และคณะ (กันยายน 2015). "Evidence for human transmission of amyloid-β pathology and cerebral amyloid angiopathy". Nature. 525 (7568): 247–50. Bibcode:2015Natur.525..247J. doi:10.1038/nature15369. PMID 26354483.
- ↑ Abbott A (September 2015). "Autopsies reveal signs of Alzheimer's in growth-hormone patients". Nature. 525 (7568): 165–66. Bibcode:2015Natur.525..165A. doi:10.1038/525165a. PMID 26354460.
- ↑ Dougall NJ, Bruggink S, Ebmeier KP (2004). "Systematic review of the diagnostic accuracy of 99mTc-HMPAO-SPECT in dementia". The American Journal of Geriatric Psychiatry. 12 (6): 554–70. doi:10.1176/appi.ajgp.12.6.554. PMID 15545324.
- ↑ Carpenter AP, Pontecorvo MJ, Hefti FF, Skovronsky DM (August 2009). "The use of the exploratory IND in the evaluation and development of 18F-PET radiopharmaceuticals for amyloid imaging in the brain: a review of one company's experience". The Quarterly Journal of Nuclear Medicine and Molecular Imaging. 53 (4): 387–93. PMID 19834448.
- ↑ Leung K (8 April 2010). "(E)-4-(2-(6-(2-(2-(2-(18F-fluoroethoxy)ethoxy)ethoxy)pyridin-3-yl)vinyl)-N-methyl benzenamine [[18F]AV-45]". Molecular Imaging and Contrast Agent Database. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 7 June 2010. สืบค้นเมื่อ 24 June 2010.
- ↑ Rabinovici GD, Jagust WJ (2009). "Amyloid imaging in aging and dementia: testing the amyloid hypothesis in vivo". Behavioural Neurology. 21 (1): 117–28. doi:10.3233/BEN-2009-0232. PMC 2804478. PMID 19847050. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 30 กรกฎาคม 2013.
- ↑ O'Brien JT (December 2007). "Role of imaging techniques in the diagnosis of dementia". The British Journal of Radiology. 80 Spec No 2 (Spec No 2): S71–77. doi:10.1259/bjr/33117326. PMID 18445747.
- ↑ "FDA Panel Recommends Conditional Approval for PET Agent". Imaging Technology News. 2011-01-21. สืบค้นเมื่อ 2019-06-17.
- ↑ Clark CM, Schneider JA, Bedell BJ, Beach TG, Bilker WB, Mintun MA, และคณะ (January 2011). "Use of florbetapir-PET for imaging beta-amyloid pathology". JAMA. 305 (3): 275–83. doi:10.1001/jama.2010.2008. PMID 21245183.
- ↑ "Amyvid". Community register of medicinal products for human use. European Community. 17 January 2013. สืบค้นเมื่อ 18 April 2018.
- ↑ Chong MS, Sahadevan S (September 2005). "Preclinical Alzheimer's disease: diagnosis and prediction of progression". The Lancet. Neurology. 4 (9): 576–79. doi:10.1016/s1474-4422(05)70168-x. PMID 16109364.
- ↑ 308.0 308.1 Sharma N, Singh AN (July 2016). "Exploring Biomarkers for Alzheimer's Disease". Journal of Clinical and Diagnostic Research (Review). 10 (7): KE01–06. doi:10.7860/JCDR/2016/18828.8166. PMC 5020308. PMID 27630867.
บทอ่านเพิ่ม[แก้]
- Alzheimer's Disease: Unraveling the Mystery. US Department of Health and Human Services, National Institute on Aging, NIH. 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 8 January 2012.
- Can Alzheimer's Disease Be Prevented? (PDF). US Department of Health and Human Services, National Institute on Aging, NIH. 2009. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2 May 2013.
- Caring for a Person with Alzheimer's Disease: Your Easy-to-Use Guide from the National Institute on Aging. US Department of Health and Human Services, National Institute on Aging, NIH. 2009. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 8 January 2012.
- Russell D, Barston S, White M (19 December 2007). "Alzheimer's Behavior Management: Learn to Manage Common Behavior Problems". helpguide.org. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 23 February 2008. สืบค้นเมื่อ 29 February 2008.
- Irvine K, Laws KR, Gale TM, Kondel TK (2012). "Greater cognitive deterioration in women than men with Alzheimer's disease: a meta analysis". Journal of Clinical and Experimental Neuropsychology (Meta-analysis). 34 (9): 989–98. doi:10.1080/13803395.2012.712676. PMID 22913619.
แหล่งข้อมูลอื่น[แก้]
- โรคอัลไซเมอร์ ที่เว็บไซต์ Curlie
| การจำแนกโรค | |
|---|---|
| ทรัพยากรภายนอก |