โซเดียมคลอไรด์
บทความนี้อาจต้องการตรวจสอบต้นฉบับ เพราะใช้โปรแกรมแปล คุณสามารถช่วยพัฒนาบทความได้ |
 ผลึกโซเดียมคลอไรด์ในรูปของเกลือหิน
| |
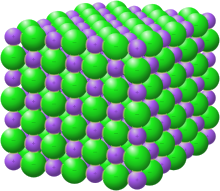 โครงสร้างผลึกที่มีโซเดียมเป็นสีม่วงและคลอไรด์เป็นสีเขียว[1]
| |
| ชื่อ | |
|---|---|
| IUPAC name
Sodium chloride
| |
ชื่ออื่น
| |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| 3534976 | |
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ECHA InfoCard | 100.028.726 |
| EC Number |
|
| 13673 | |
| KEGG | |
| MeSH | Sodium+chloride |
ผับเคม CID
|
|
| RTECS number |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| NaCl | |
| มวลโมเลกุล | 58.443 g/mol[2] |
| ลักษณะทางกายภาพ | ผลึกลูกบาศก์ไม่มีสี[2] |
| กลิ่น | ไม่มีกลิ่น |
| ความหนาแน่น | 2.17 g/cm3[2] |
| จุดหลอมเหลว | 800.7 องศาเซลเซียส (1,473.3 องศาฟาเรนไฮต์; 1,073.8 เคลวิน)[2] |
| จุดเดือด | 1,465 องศาเซลเซียส (2,669 องศาฟาเรนไฮต์; 1,738 เคลวิน)[2] |
| 360 g/L (25°C)[2] | |
| ความสามารถละลายได้ ใน แอมโมเนีย | 21.5 g/L |
| ความสามารถละลายได้ ใน เมทานอล | 14.9 g/L |
| −30.2·10−6 cm3/mol[3] | |
ดัชนีหักเหแสง (nD)
|
1.5441 (at 589 nm)[4] |
| โครงสร้าง[5] | |
| Face-centered cubic (see text), cF8 | |
| Fm3m (No. 225) | |
a = 564.02 pm
| |
หน่วยสูตร (Z)
|
4 |
| octahedral at Na+ octahedral at Cl− | |
| อุณหเคมี[6] | |
ความจุความร้อน (C)
|
50.5 J/(K·mol) |
Std molar
entropy (S⦵298) |
72.10 J/(K·mol) |
Std enthalpy of
formation (ΔfH⦵298) |
−411.120 kJ/mol |
| เภสัชวิทยา | |
| A12CA01 (WHO) B05CB01, B05XA03, S01XA03 | |
| ความอันตราย | |
| NFPA 704 (fire diamond) | |
| ปริมาณหรือความเข้มข้น (LD, LC): | |
LD50 (median dose)
|
3 g/kg (oral, rats)[7] |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
แอนไอออนอื่น ๆ
|
โซเดียมฟลูออไรด์ โซเดียมโบรไมด์ โซเดียมไอโอไดด์ โซเดียมแอสทาไทด์ |
แคทไอออนอื่น ๆ
|
ลิเทียมคลอไรด์ โพแทสเซียมคลอไรด์ รูบิเดียมคลอไรด์ ซีเซียมคลอไรด์ แฟรนเซียมคลอไรด์ |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
โซเดียมคลอไรด์ (อังกฤษ: Sodium chloride, สูตรเคมี: NaCl) มีชื่อที่เรียกทั่วไปคือ เกลือแกง เป็นสารประกอบเคมี โซเดียมคลอไรด์เป็นเกลือที่มีบทบาทต่อความเค็มของมหาสมุทร และของเหลวภายนอกเซลล์ของสิ่งมีชีวิตหลายเซลล์ เป็นส่วนประกอบหลักในเกลือที่กินได้ ถูกใช้อย่างกว้างขวางในการเป็นเครื่องปรุงรส และใช้ในการถนอมอาหาร
โครงสร้างผลึก
[แก้]
สีน้ำเงินอ่อน = Na+
สีเขียวเข้ม = Cl−
โซเดียมคลอไรด์ จะเกิดผลึกแบบคิวบิก ในโครงสร้างของผลึก ไอออนคลอไรด์ซึ่งมีขนาดใหญ่จะถูกจัดเรียงแบบ ccp ในขณะที่โซเดียมไอออนซึ่งมีขนาดเล็กกว่าจะถูกบรรจุในช่องว่าง ออกตะฮีดรัลระหว่างไอออนคลอไรด์ แต่ละไอออนจะถูกล้อมรอบด้วยไอออนอีกชนิด 6 ตัว ซึ่งเป็นโครงสร้างพื้นฐานเดียวกันกับที่พบในแร่อื่นหลายชนิดและรู้จักกันในชื่อ โครงสร้างเกลือหิน
ความสำคัญทางชีววิทยา
[แก้]โซเดียมคลอไรด์ มีความสำคัญต่อสิ่งมีชีวิตบนโลกในเนื้อเยื้อชีวภาพ และของเหลวในร่างกายจะมีเกลือในปริมาณที่แตกต่างกัน ความเข้มข้นของ โซเดียมไอออนใน เลือด เป็นความสัมพันธ์โดยตรงต่อการควบคุมระดับที่ปลอดภัยของของเหลวในร่างกาย การแพร่กระจายของ การกระตุ้นประสาท โดยซิกนัล ทรานสดักชัน (signal transduction) ถูกควบคุมโดยโซเดียม ไอออน(โพแทสเซียม เป็น โลหะ ที่มีความสัมพันธ์ใกล้ชิดกับโซเดียม ซึ่งเป็นส่วนประกอบหลักในระบบร่างกายเช่นกัน)
0.9% โซเดียมคลอไรด์ ใน น้ำ ถูกเรียกว่า สารละลายทางสรีรวิทยา (physiological solution) หรือ นอร์มัล ซาไลน์ (normal saline) เพราะเป็นความเข้มข้นเดียว (isotonic) กับ พลาสมาในเลือด นอร์มัล ซาไลน์ ใช้ในทางการแพทย์เพื่อทดแทนการสูญเสียของเหลวจากร่างกายและการรักษาแบบนี้ว่าการให้ของเหลวทดแทน (fluid replacement) ซึ่งใช้แพร่หลายทาง การแพทย์ เพื่อป้องกันการขาดน้ำ (dehydration) หรือ อินทราวีนัสเทอราปี (intravenous therapy) เพื่อป้องกัน การช๊อคจากปริมาตรเลือดต่ำ สาเหตุจากการสูญเสียเลือด
มนุษย์ไม่เหมือนสัตว์ ไพรเมต ด้วยกันที่สามารถกำจัดเกลือจำนวนมากได้ทาง เหงื่อ (sweating)
การผลิตและการใช้
[แก้]ปัจจุบันเกลือถูกผลิตโดย การระเหย ของ น้ำทะเล หรือ น้ำเค็ม (brine) จากแหล่งอื่นๆ เช่น บ่อน้ำเค็ม ทะเลสาบน้ำเค็ม (salt lake) และการทำเหมืองเกลือที่เรียกว่า เกลือหิน (rock salt หรือ เฮไลต์)
ในขณะที่ผู้คนจำนวนมากคุ้นเคยกับการใช้เกลือปรุงอาหารแต่เกลือสามารถใช้ประโยชน์ได้อีกมากมาย เช่น
- ใช้ในการผลิตกระดาษ
- ใช้ในหมึกพิมพ์ผ้าในอุตสาหกรรมเท็กไทล์
- ใช้ในอุตสาหกรรมผลิตสบู่และผงซักฟอก
- ใช้ในการละลายน้ำแข็งที่เกาะบนพื้นถนนในแคนาดาและสหรัฐอเมริกาในช่วงฤดูหนาวที่อุณหภูมิต่ำกว่าจุดเยือกแข็งของน้ำ
- ใช้เป็นวัตถุดิบในการผลิตคลอรีน พีวีซี และยาฆ่าแมลง
| ความสามารถในการละลายของโซเดียมคลอไรด์ในตัวละลายต่างชนิด (g NaCl / 100 g of solvent at 25?C) | |
|---|---|
| H2O | 36 |
| แอมโมเนียเหลว | 3.02 |
| เมทานอล | 1.4 |
| กรดฟอร์มิก | 5.2 |
| ซัลโฟเลน | 0.005 |
| อะซิโตนิไตรล์ | 0.0003 |
| อะซิโตน | 0.000042 |
| ฟอร์มาไมด์ | 9.4 |
| ไดเมทิลฟอร์มาไมด์ | 0.04 |
| Reference: Burgess, J. Metal Ions in Solution (Ellis Horwood, New York, 1978) ISBN 0-85312-027-7 | |
ดูเพิ่มเกลือเสริมไอโอดีน
[แก้]อ้างอิง
[แก้]แหล่งอ้างอิง
[แก้]- Haynes, William M., บ.ก. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
แหล่งข้อมูลอื่น
[แก้]- Salt United States Geological Survey Statistics and Information
- "Using Salt and Sand for Winter Road Maintenance". Road Management Journal. December 1997. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 21 September 2016. สืบค้นเมื่อ 13 February 2007.
- Calculators: surface tensions เก็บถาวร 2020-02-22 ที่ เวย์แบ็กแมชชีน, and densities, molarities and molalities เก็บถาวร 2020-02-22 ที่ เวย์แบ็กแมชชีน of aqueous NaCl (and other salts)
- JtBaker MSDS

