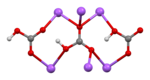
โซเดียมไบคาร์บอเนต
หน้าตา
(เปลี่ยนทางจาก Sodium bicarbonate)
| |||
| |||
 | |||
| |||
| ชื่อ | |||
|---|---|---|---|
| IUPAC name
โซเดียมไฮโดรเจนคาร์บอเนต
| |||
| ชื่ออื่น
โซดาทำขนม, bicarb (laboratory slang), ไบคาร์บอเนตของโซดา, nahcolite, natrium hydrogen carbonate, natron
| |||
| เลขทะเบียน | |||
3D model (JSmol)
|
|||
| 4153970 | |||
| ChEBI | |||
| ChEMBL | |||
| เคมสไปเดอร์ | |||
| ดรักแบงก์ | |||
| ECHA InfoCard | 100.005.122 | ||
| EC Number |
| ||
| เลขอี | E500(ii) (acidity regulators, ...) | ||
| KEGG | |||
| MeSH | Sodium+bicarbonate | ||
ผับเคม CID
|
|||
| RTECS number |
| ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| คุณสมบัติ | |||
| NaHCO 3 | |||
| มวลโมเลกุล | 84.0066 g mol−1 | ||
| ลักษณะทางกายภาพ | ผลึกของแข็งสีขาว | ||
| กลิ่น | ไม่มีกลิ่น | ||
| ความหนาแน่น |
| ||
| จุดหลอมเหลว | (Decomposes to sodium carbonate starting at 50 °C[1][6]) | ||
| ความสามารถละลายได้ | 0.02 wt% acetone, 2.13 wt% methanol @22 °C.[4] insoluble in ethanol | ||
| log P | −0.82 | ||
| pKa | |||
ดัชนีหักเหแสง (nD)
|
nα = 1.377 nβ = 1.501 nγ = 1.583 | ||
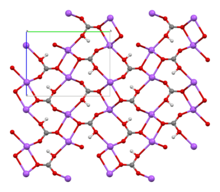
| โครงสร้าง | |||
| โมโนคลินิก | |||
| อุณหเคมี | |||
ความจุความร้อน (C)
|
87.6 J/mol K[7] | ||
Std molar
entropy (S⦵298) |
101.7 J/mol K[7] | ||
Std enthalpy of
formation (ΔfH⦵298) |
−950.8 kJ/mol[7] | ||
พลังงานเสรีกิบส์ (ΔfG⦵)
|
−851.0 kJ/mol[7] | ||
| เภสัชวิทยา | |||
| B05CB04 (WHO) B05XA02, QG04BQ01 (WHO) | |||
| ทางหลอดเลือดดำ, ทางปาก | |||
| ความอันตราย | |||
| อาชีวอนามัยและความปลอดภัย (OHS/OSH): | |||
อันตรายหลัก
|
Causes serious eye irritation | ||
| NFPA 704 (fire diamond) | |||
| จุดวาบไฟ | ทนไฟ | ||
| ปริมาณหรือความเข้มข้น (LD, LC): | |||
LD50 (median dose)
|
4220 mg/kg (rat, oral)[8] | ||
| เอกสารข้อมูลความปลอดภัย (SDS) | External MSDS | ||
| สารประกอบอื่นที่เกี่ยวข้องกัน | |||
แอนไอออนอื่น ๆ
|
โซเดียมคาร์บอเนต | ||
แคทไอออนอื่น ๆ
|
|||
สารประกอบที่เกี่ยวข้อง
|
|||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
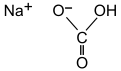
โซเดียมไบคาร์บอเนต (อังกฤษ: sodium bicarbonate; ชื่อตาม IUPAC: โซเดียมไฮโดรเจนคาร์บอเนต) หรือ โซดาทำขนม (baking soda) เป็นสารประกอบที่มีสูตรเคมีคือ NaHCO3 มีเลขอีคือ E500 ลักษณะเป็นผงสีขาว มีรสเค็มคล้ายโซเดียมคาร์บอเนต มีการใช้โซเดียมไบคาร์บอเนตมาตั้งแต่สมัยอียิปต์โบราณ ในรูปของเนตรอน (natron)
ดูเพิ่ม
[แก้]อ้างอิง
[แก้]- ↑ 1.0 1.1 Haynes, p. 4.90
- ↑ 2.0 2.1 2.2 Haynes, p. 5.194
- ↑ 3.0 3.1 3.2 "Sodium Bicarbonate" (PDF). United Nations Environment Programme. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 16 May 2011.
- ↑ Ellingboe JL, Runnels JH (1966). "Solubilities of Sodium Carbonate and Sodium Bicarbonate in Acetone-Water and Methanol-Water Mixtures". J. Chem. Eng. Data. 11 (3): 323–324. doi:10.1021/je60030a009.
- ↑ 5.0 5.1 Haynes, p. 7.23
- ↑ Pasquali I, Bettini R, Giordano F (2007). "Thermal behaviour of diclofenac, diclofenac sodium and sodium bicarbonate compositions". Journal of Thermal Analysis and Calorimetry. 90 (3): 903–907. doi:10.1007/s10973-006-8182-1. S2CID 95695262.
- ↑ 7.0 7.1 7.2 7.3 Haynes, p. 5.19
- ↑ Chambers M. "Sodium bicarbonate [USP:JAN]". ChemIDplus. U.S. National Library of Medicine.
บรรณานุกรม
[แก้]- Haynes WM, บ.ก. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
แหล่งข้อมูลอื่น
[แก้]วิกิมีเดียคอมมอนส์มีสื่อที่เกี่ยวข้องกับ โซเดียมไบคาร์บอเนต