การถ่ายโอนสัญญาณ
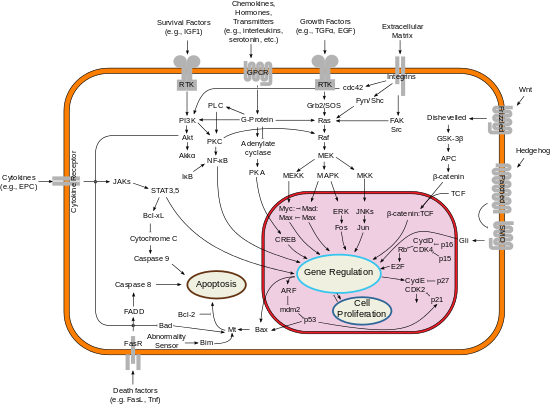
ในเซลล์ การถ่ายโอนสัญญาณ หรือ การแปรสัญญาณ (อังกฤษ: signal transduction) เป็นกระบวนการทางเคมีหรือทางกายภาพโดยเป็นลำดับการทำงาน/ลำดับเหตุการณ์ในระดับโมเลกุล ที่โมเลกุลส่งสัญญาณ (ปกติฮอร์โมนหรือสารสื่อประสาท) จะเริ่มการทำงาน/ก่อสภาพกัมมันต์ของหน่วยรับ ซึ่งในที่สุดมีผลให้เซลล์ตอบสนองหรือเปลี่ยนการทำงาน[1][2] โปรตีนที่ตรวจจับสิ่งเร้าโดยทั่วไปจะเรียกว่า หน่วยรับ (receptor) แม้ในบางที่ก็จะใช้คำว่า sensor ด้วย[3] ความเปลี่ยนแปลงที่เกิดจากการจับของลิแกนด์กับหน่วยรับ (คือการพบสัญญาณ) จะก่อลำดับการส่งสัญญาณ (signaling cascade) ซึ่งเป็นลำดับเหตุการณ์ทางเคมีชีวภาพตามวิถีการส่งสัญญาณ (signaling pathway) เมื่อวิถีการส่งสัญญาณมากกว่าหนึ่งมีปฏิสัมพันธ์กับกันและกัน นี่ก็จะกลายเป็นเครือข่าย เป็นการประสานการตอบสนองของเซลล์ บ่อยครั้งโดยเป็นการส่งสัญญาณแบบร่วมกัน[4] ในระดับโมเลกุล การตอบสนองเช่นนี้รวม
- ความเปลี่ยนแปลงในการถอดรหัสหรือแปลรหัสยีน
- การดัดแปลงอาศัยเอนไซม์หลังการแปลรหัส (post-translational modification) และการเปลี่ยนโครงรูปของโปรตีน
- การย้ายตำแหน่งของโปรตีน
เหตุการณ์ระดับโมเลกุลเหล่านี้เป็นกลไกพื้นฐานในการควบคุมการเติบโตของเซลล์ การเพิ่มจำนวนเซลล์ เมแทบอลิซึมของเซลล์ และกระบวนการอื่น ๆ อีกมากมาย[5] ในสิ่งมีชีวิตหลายเซลล์ วิถีการโอนสัญญาณได้วิวัฒนาการขึ้นเพื่อควบคุมการสื่อสารระหว่างเซลล์โดยวิธีการต่าง ๆ
องค์ประกอบแต่ละอย่าง (ซึ่งอาจเรียกว่าโหนด [node]) ในวิถีการส่งสัญญาณจะจัดหมู่ตามบทบาทเนื่องกับสิ่งเร้าเบื้องต้น ลิแกนด์จะเรียกว่า โมเลกุลส่งสัญญาณที่หนึ่ง (first messengers) ในขณะที่หน่วยรับจะเรียกว่า ตัวแปรสัญญาณ (signal transducer) ซึ่งจะก่อสภาพกัมมันต์ของ หน่วยปฏิบัติงานปฐมภูมิ (primary effectors) หน่วยปฏิบัติงานเช่นนี้บ่อยครั้งสัมพันธ์กับ โมเลกุลส่งสัญญาณที่สอง ซึ่งสามารถก่อสภาพกัมมันต์ของ หน่วยปฏิบัติงานทุติยภูมิ เป็นต้น ขึ้นอยู่กับประสิทธิภาพของโหนด สัญญาณสามารถขยายได้ ดังนั้น โมเลกุลส่งสัญญาณตัวเดียว สามารถก่อการตอบสนองเป็นโมเลกุลเป็นร้อย ๆ ถึงเป็นล้าน ๆ ตัว[6]
เหมือนกับสัญญาณในรูปแบบอื่น ๆ การถ่ายโอนสัญญาณทางชีวภาพก็จะประกอบด้วยการหน่วงเวลา (delay), เสียงรบกวน (noise), สัญญาณป้อนกลับ (signal feedback), signal feedforward, สัญญาณแทรกสอด (interference) ซึ่งมีพิสัยตั้งแต่เล็กน้อยจนถึงขั้นก่อโรค[7] ตั้งแต่เริ่มสาขาชีววิทยาเชิงคอมพิวเตอร์ (computational biology) การวิเคราะห์วิถีการส่งสัญญาณและเครือข่ายการส่งสัญญาณ ได้กลายเป็นอุปกรณ์สำคัญเพื่อเข้าใจการทำงานของเซลล์และของโรค เช่น เพื่อเข้าใจกลไกการเปลี่ยนระบบสัญญาณซึ่งเป็นการตอบสนองเมื่อเกิดการดื้อยา[8]
สิ่งเร้า
[แก้]มูลฐานของการถ่ายโอนสัญญาณก็คือ การแปลสิ่งเร้าโดยเฉพาะอย่างหนึ่งให้เป็นสัญญาณทางเคมีชีวภาพ รูปแบบของสิ่งเร้าที่ว่าจะต่างกันอย่างหลากหลาย เริ่มตั้งแต่สิ่งเร้านอกเซลล์ เช่น epidermal growth factor (EGF) จนถึงเหตุการณ์ภายในเซลล์เอง เช่น ความเสียหายต่อดีเอ็นเอเพราะ telomere ที่สั้นลงเนื่องจากการแบ่งเซลล์[9]
ตามธรรมดาแล้ว สัญญาณคือกระแสประสาทที่ส่งไปยังระบบประสาทกลาง จะมาจากประสาทสัมผัส ซึ่งส่งจากเซลล์ประสาทหนึ่งไปยังอีกเซลล์ประสาทหนึ่ง เป็นกระบวนการที่เรียกว่า การสื่อประสาท (synaptic transmission/neurotransmission) แต่ก็มีกลไกการส่งสัญญาณอื่น ๆ ระหว่างเซลล์ในสัตว์หลายเซลล์ เช่น ที่ควบคุมพัฒนาการเมื่อยังเป็นตัวอ่อน[10]
ลิแกนด์
[แก้]วิถีการถ่ายโอนสัญญาณโดยมากจะมีการจับกันของโมเลกุลส่งสัญญาณ ที่เรียกว่า ลิแกนด์ กับหน่วยรับ แล้วจุดชนวนเหตุการณ์ต่าง ๆ ภายในเซลล์ คือการจับกันของลิแกนด์กับหน่วยรับ จะทำให้หน่วยรับเปลี่ยนโครงรูป (conformational change) เป็นการเริ่มการทำงาน/การก่อสภาพกัมมันต์ของหน่วยรับ (receptor activation) ให้เป็นสภาพที่ออกฤทธิ์ได้ ลิแกนด์โดยมากจะเป็นโมเลกุลละลายได้ในสื่อนอกเซลล์ โมเลกุลรวมทั้ง growth factors, cytokines, และสารสื่อประสาท
องค์ประกอบของเมทริกซ์นอกเซลล์ เช่น fibronectin และ hyaluronan ก็สามารถจับกับหน่วยรับด้วย (คือกับ integrins และ CD44 ตามลำดับ) อนึ่ง โมเลกุลบางอย่างเช่น ฮอร์โมนแบบสเตอรอยด์ จะละลายในลิพิดได้ และดังนั้น จึงสามารถผ่านเยื่อหุ้มเซลล์เพื่อเข้าไปถึงหน่วยรับที่นิวเคลียส (nuclear receptors)[11] ในกรณีของหน่วยรับฮอร์โมนสเตอรอยด์ การกระตุ้นหน่วยรับจะทำให้มันจับกับบริเวณ promoter ของยีนที่ตอบสนองต่อสเตอรอยด์[12]
การจัดหมู่โมเลกุลส่งสัญญาณไม่ใช่ว่า จะเป็นไปตามธรรมชาติอย่างใดอย่างหนึ่งโดยเฉพาะเท่านั้นของสมาชิกในหมู่ ยกตัวอย่างเช่น โมเลกุลมีกลิ่น (odorant) จัดอยู่ในหมวดหมู่ต่าง ๆ มากมาย[13] สารสื่อประสาทก็เหมือนกัน ซึ่งเริ่มตั้งแต่โมเลกุลเล็ก ๆ เช่น โดพามีน[14] ไปจนถึง neuropeptide เช่น เอ็นดอร์ฟิน[15] นอกจากนั้น โมเลกุลบางอย่างอาจอยู่ในหมู่มากกว่าหนึ่ง เช่น เอพิเนฟรีนเป็นทั้งสารสื่อประสาทเมื่อหลั่งออกโดยระบบประสาทกลาง และเป็นฮอร์โมนเมื่อหลั่งออกโดยต่อมหมวกไตส่วนใน (adrenal medulla)
หน่วยรับบางอย่างเช่น HER2 สามารถทำงานโดยไร้ลิแกนด์เมื่อแสดงออกมากเกินไปหรือกลายพันธุ์ เป็นการก่อสภาพกัมมันต์ของวิถีส่งสัญญาณเอง โดยกลไกชดเชยอาจไม่สามารถระงับได้ ในกรณีของ HER2 ซึ่งเป็นคู่ขาในไดเมอร์ร่วมกับ EGFR สภาพกัมมันต์เช่นนี้ทำให้เพิ่มจำนวนเซลล์มากเกินแล้วเกิดมะเร็ง[16]
แรงกล
[แก้]ความแพร่หลายของเยื่อฐาน (basement membrane) ในเนื้อเยื่อของสัตว์เคลด Eumetazoa เป็นตัวบ่งว่า เซลล์โดยมากจะต้องยึดอยู่กับที่เพื่อให้รอดชีวิตได้ ข้อบังคับนี้ทำให้วิวัฒนาการเกิดวิถีการถ่ายโอนแรงกล (mechanotransduction pathway) ที่ซับซ้อน ซึ่งทำให้เซลล์รู้ความแข็งอ่อนของชั้นเนื้อเยื่อที่อยู่ข้างใต้ได้ การส่งสัญญาณเช่นนี้จะพบที่ focal adhesion ซึ่งเป็นบริเวณที่ actin cytoskeleton อันยึดอยู่กับ integrin ตรวจจับความเปลี่ยนแปลงแล้วส่งสัญญาณต่อโดยผ่านโปรตีน YAP1[17] โมเลกุลยึดเซลล์ (cell adhesion molecules) ที่อาศัยแคลเซียม เช่น cadherin และ selectin ก็สามารถอำนวยการถ่ายโอนแรงกลด้วย[18] การถ่ายโอนแรงกลแบบพิเศษภายในระบบประสาททำให้สามารถรับรู้แรงกลได้ เช่น การได้ยิน สัมผัส การรับรู้อากัปกิริยา และการกำหนดรู้การทรงตัว[19]
ความดันออสโมซิส
[แก้]การควบคุมความดันออสโมซิส (osmotic pressure) คือความแตกต่างทางออสโมลาริตีระหว่างไซโตซอลกับสื่อนอกเซลล์ ทั้งในระดับเซลล์และทั้งระบบ เป็นเรื่องสำคัญอย่างวิกฤติในเรื่องภาวะธำรงดุล เซลล์สามารถตรวจจับสิ่งเร้าแบบออสโมซิสด้วยความเปลี่ยนแปลงของ macromolecular crowding[A] ด้วยความต่างศักย์ไฟฟ้าของไอออน และด้วยคุณสมบัติของเยื่อหุ้มเซลล์หรือของ cytoskeleton โดยอย่างหลังสุดนี้เป็นการถ่ายโอนแรงกลอย่างหนึ่ง[21]
ความเปลี่ยนแปลงเหล่านี้สามารถตรวจจับด้วยโปรตีนที่เรียกว่า osmosensor หรือ osmoreceptor ในมนุษย์ osmosensor ที่ได้ศึกษาละเอียดที่สุดก็คือ transient receptor potential channel (TRP channel) ซึ่งอยู่ที่ซีเลียอันเคลื่อนที่ไม่ได้ (nonmotile cillia) ในเซลล์มนุษย์[21][22] ส่วนในยีสต์ มีการศึกษาวิถี HOG อย่างละเอียดที่สุด[23]
อุณหภูมิ
[แก้]การรับอุณหภูมิในเซลล์เรียกว่า thermoception และโดยมากอำนวยโดยช่อง transient receptor potential channel (TRP channel)[24] อนึ่ง เซลล์ของสัตว์มีกลไกสงวนที่ไม่ได้เปลี่ยนตามวิวัฒนาการ เพื่อป้องกันอุณหภูมิสูงไม่ให้สร้างความเสียหายในเซลล์ เรียกว่า การตอบสนองต่อช็อกความร้อน (heat-shock response) การตอบสนองเช่นนี้จะจุดชนวนเมื่ออุณหภูมิสูงทำให้โปรตีนช็อกความร้อน Heat shock factor 1 (HSF1) ที่เบื้องต้นไม่มีฤทธิ์แตกตัวจากคอมเพล็กซ์คือ Hsp40/Hsp70 และ Hsp90 เมื่อได้อำนวยการจาก Non-coding RNA คือ hsr1 โปรตีน HSF1 ก็จะรวมเป็นไทรเมอร์ที่มีฤทธิ์ แล้วเพิ่ม (upregulation) การแสดงออกของยีนเป้าหมาย[25] ยังมีกลไกรับรู้อุณหภูมิอื่น ๆ อีกมากในทั้งโพรแคริโอตและยูแคริโอต[24]
แสง
[แก้]ในสัตว์เลี้ยงลูกด้วยนม แสงเป็นตัวกำหนดการเห็นและนาฬิกาจังหวะรอบวัน (circadian clock) โดยเริ่มการทำงานของโปรตีนไวแสงในเซลล์รับแสงที่จอตา ในกรณีการเห็น rhodopsin ในเซลล์รูปแท่งและเซลล์รูปกรวย จะเป็นโปรตีนที่ตรวจจับแสง[26] ส่วนนาฬิกาจังหวะรอบวันจะใช้สารรงควัตถุไวแสงที่ต่างกัน คือ melanopsin ซึ่งมีหน้าที่ตรวจจับแสงภายใน intrinsically photosensitive retinal ganglion cells[27]
หน่วยรับ
[แก้]หน่วยรับสามารถแบ่งออกเป็นสองกลุ่มใหญ่ ๆ คือ หน่วยรับภายในเซลล์และนอกเซลล์
หน่วยรับนอกเซลล์
[แก้]หน่วยรับนอกเซลล์เป็นโปรตีนผ่านเยื่อหุ้มเซลล์ (transmembrane protein) ซึ่งเป็นหน่วยรับกลุ่มใหญ่ที่สุด เป็นโปรตีนที่ทอดข้ามเยื่อหุ้มเซลล์ คือส่วนหนึ่งจะอยู่นอกเซลล์และอีกส่วนหนึ่งจะอยู่ในเซลล์ การถ่ายโอนสัญญาณจะเกิดอาศัยลิแกนด์ที่จับกับส่วนนอกของหน่วยรับ โดยที่ลิแกนด์จะไม่เข้าผ่านเยื่อหุ้มเซลล์ การจับจะทำให้ส่วนภายในเปลี่ยนโครงรูป เป็นกระบวนการที่บางครั้งเรียกว่าการก่อกัมมันต์ของหน่วยรับ (receptor activation)[28] ซึ่งมีผลเริ่มก่อกัมมันต์ของโดเมนที่เป็นเอนไซม์ของหน่วยรับ หรือเป็นการเปิดจุดยึด (binding site) สำหรับโปรตีนส่งสัญญาณภายในเซลล์ ซึ่งในที่สุดก็จะแพร่กระจายสัญญาณไปในไซโทพลาซึม
ในเซลล์ยูแคริโอต โปรตีนภายในเซลล์โดยมากที่เปลี่ยนเป็นสภาพกัมมันต์เพราะการจับของลิแกนด์-หน่วยรับ จะมีฤทธิ์เป็นเอนไซม์ด้วย ตัวอย่างรวมทั้ง tyrosine kinase และ phosphatase เอนไซม์เช่นนี้บ่อยครั้งจะเชื่อมอยู่กับหน่วยรับด้วยพันธะโคเวเลนต์ บางอย่างสามารถสร้างโมเลกุลส่งสัญญาณที่สอง เช่น cyclic AMP และ Inositol triphosphate (IP3) โดยอย่างหลังเป็นตัวกระตุ้นให้หน่วยเก็บภายในปล่อยแคลเซียมออกในไซโทพลาซึม ส่วนโปรตีนกัมมันต์อื่น ๆ จะมีปฏิกิริยากับโปรตีนอะแด็ปเตอร์ (signal transducing adaptor protein) ที่อำนวยปฏิสัมพันธ์ระหว่างโปรตีนส่งสัญญาณต่าง ๆ และประสานงานให้คอมเพล็กซ์ส่งสัญญาณต่าง ๆ ที่จำเป็นในการตอบสนองต่อสิ่งเร้าหนึ่ง ๆ ทั้งเอนไซม์และโปรตีนอะแด็ปเตอร์เป็นตัวตอบสนองต่อโมเลกุลส่งสัญญาณที่สองต่าง ๆ
โปรตีนอะแด็ปเตอร์และเอนไซม์หลายอย่างที่ออกฤทธิ์โดยเป็นส่วนของการถ่ายโอนสัญญาณ จะมีโดนเมนโปรตีนพิเศษ (protein domain) เพื่อจับกับโมเลกุลส่งสัญญาณที่สองโดยเฉพาะ ๆ ยกตัวอย่างเช่น ไอออนแคลเซียม (Ca2+) ซึ่งเป็นโมเลกุลส่งสัญญาณที่สองจะจับกับโดเมน EF hand ของโปรตีน calmodulin ซึ่งทำให้มันสามารถจับและเริ่มการทำงานของ calmodulin-dependent kinase ส่วน PIP3 และ phosphoinositides อื่น ๆ ก็จะทำเช่นเดียวกันต่อโดเมน Pleckstrin homology domain ของโปรตีนเช่น AKT ซึ่งเป็น kinase protein
G protein-coupled receptors
[แก้]G protein-coupled receptors (GPCRs) เป็นกลุ่มโปรตีนข้ามเยื่อหุ้มเซลล์ที่มีโดเมนผ่านเยื่อหุ้มเซลล์ 7 โดเมน โดยส่วนภายในเชื่อมอยู่กับจีโปรตีนที่เป็น heteromer กลุ่มมีสมาชิกเกือบ 800 ชนิด จึงเป็นโปรตีน/หน่วยรับของเยื่อหุ้มเซลล์กลุ่มใหญ่ที่สุดในสัตว์เลี้ยงลูกด้วยนม ถ้านับสัตว์สปีชีส์อื่น ๆ ด้วยทั้งหมด ก็จะมีเกิน 5,000 ชนิด[29]
GPCR ของสัตว์เลี้ยงลูกด้วยนมแบ่งออกเป็น 5 หมู่หลัก คือ rhodopsin-like, secretin-like, metabotropic glutamate, adhesion และ frizzled/smoothened แม้จะมีโปรตีนบางพวกที่จัดยากเพราะมีลำดับดีเอ็นเอที่เหมือนกันน้อย เช่น vomeronasal receptor (ที่ vomeronasal organ)[29] ยังมีหมู่อื่น ๆ อีกในยูแคริโอต เช่น cyclic AMP receptor และ fungal mating pheromone receptor ของโพรทิสต์สกุล Dictyostelium[29]
การโอนสัญญาณของ GPCR เริ่มจากการมีจีโปรตีนในสภาพอกัมมันต์ที่เชื่อมอยู่กับหน่วยรับภายในเซลล์ โดยจีโปรตีนจะเป็น heterotrimer คือมีหน่วยย่อยต่าง ๆ รวมทั้ง Gα, Gβ, และ Gγ[30] เมื่อ GPCR จับกับลิแกนด์ มันจะเปลี่ยนโครงรูปซึ่งก่อสภาพกัมมันต์ของจีโปรตีนอันเป็นเหตุให้หน่วยย่อย Gα จับกับโมเลกุลของ GTP แล้วแตกออกจากหน่วยย่อยอื่น ๆ 2 อย่างที่เหลือ การแตกตัวจะเปิดจุดยึดของหน่วยย่อยที่สามารถมีปฏิสัมพันธ์กับโมเลกุลอื่น ๆ[31]
หน่วยย่อยกัมมันต์ของจีโปรตีนที่แยกออกจากหน่วยรับเช่นนี้ จะจุดชนวนการส่งสัญญาณในลำดับต่อ ๆ ไปของโปรตีนปฏิบัติงาน (effector protein) มากมาย เช่น phospholipase และช่องไอออน โดยอย่างหลังจะอำนวยให้ปล่อยโมเลกุลส่งสัญญาณที่สองได้[32] กำลังของ GPCR ในการขยายสัญญาณจะกำหนดโดยช่วงอายุของคอมเพล็กซ์ลิแกนด์-หน่วยรับ ของหน่วยรับ-คอมเพล็กซ์โปรตีนปฏิบัติงาน และเวลาที่เอนไซม์ในกระบวนการใช้เพื่อระงับฤทธิ์ของหน่วยรับกัมมันต์และโปรตีนปฏิบัติงาน เช่น ผ่าน protein kinase phosphorylation หรือ b-arrestin-dependent internalization
งานศึกษาหนึ่งทดลองโดยแทรกการกลายพันธุ์แบบ point mutation เข้าในยีนที่เข้ารหัสหน่วยรับ chemokine receptor คือ CXCR2 เซลล์ที่กลายพันธุ์จะแปลงสภาพเป็นแบบร้าย (malignant transformation) เนื่องจากการแสดงออกของยีน CXCR2 ที่อยู่ในสภาพกัมมันต์รังสี (active conformation) แม้จะไม่ได้จับกับ chemokine นี่เป็นวิธีที่ chemokine receptor อาจมีส่วนในพัฒนาการของมะเร็ง[33]
protein kinase สำหรับไทโรซีน, Ser/Thr และ Histidine
[แก้]หน่วยรับ Receptor tyrosine kinases (RTKs) เป็นโปรตีนผ่านเยื่อหุ้มเซลล์ที่มีโดเมน kinase ในเซลล์ บวกกับโดเมนนอกเซลล์ที่สามารถจับกับลิแกนด์ ตัวอย่างรวมทั้ง growth factor receptors เช่น insulin receptor[34] เพื่อถ่ายโอนสัญญาณ RTKs จำเป็นต้องอยู่ในรูปแบบไดเมอร์ (คือ มีหน่วยเหมือนกันที่จับคู่กัน) ที่เยื่อหุ้มเซลล์[35] โดยไดเมอร์จะเกิดความเสถียรเมื่อลิแกนด์จับกับหน่วยรับ ต่อจากนั้น ปฏิสัมพันธ์ระหว่างโดเมนในไซโทพลาซึมจะกระตุ้นให้เกิดปฏิกิริยาฟอสโฟรีเลชันอัตโนมัติ (autophosphorylation) ของเรซิดิว tyrosine ภายในโดเมน kinase ที่อยู่ภายในเซลล์ แล้วทำให้เปลี่ยนโครงรูป จากนั้นโดเมน kinase ก็จะออกฤทธิ์ โดยจุดชนวนลำดับการส่งสัญญาณที่อาศัยปฏิกิริยาฟอสโฟรีเลชันสำหรับโมเลกุลในไซโทพลาซึมต่อ ๆ ไป (downstream) ที่อำนวยกระบวนการต่าง ๆ ของเซลล์ เช่น การเปลี่ยนสภาพ (cell differentiation) และเมแทบอลิซึม[34]
protein kinase สำหรับ Ser/Thr และ dual-specificity kinase หลายอย่างสำคัญต่อการถ่ายโอนสัญญาณ ไม่ว่าจะออกฤทธิ์ในลำดับหลังจาก RTK หรืออาจทำหน้าที่เช่นกับ RTK โดยฝังอยู่ที่เยื่อหุ้มเซลล์หรือเป็นสารละลายเองในเซลล์ มีกระบวนการถ่ายโอนสัญญาณที่เกี่ยวข้องกับ protein kinase และ pseudokinase ราว ๆ 560 อย่างที่รู้จักภายในจีโนมมนุษย์[36][37]
เหมือนกับ GPCR จีโปรตีนที่จับกับ GTP มีบทบาทสำคัญในการถ่ายโอนสัญญาณจาก RTK แบบกัมมันต์เข้าไปในเซลล์ ในกรณีนี้ จีโปรตีนจะเป็นสมาชิกของกลุ่ม GTPases คือ Ras, Rho, และ Raf โดยเรียกร่วมกัน ๆ ได้ว่า จีโปรตีนแบบเล็ก (small G protein) ซึ่งทำงานเหมือนกับสวิตช์โมเลกุลที่ปกติจะผูกอยู่กับเยื่อหุ้มเซลล์โดยกลุ่ม isoprenyl ที่เชื่อมกับส่วนสุดข้างที่เป็น carboxyl เมื่อมีสภาพกัมมันต์ จีโปรตีนก็จะส่งโปรตีนไปที่ซับโดเมนของเยื่อหุ้มเซลล์โดยเฉพาะ ๆ ซึ่งเป็นที่ที่โปรตีนมีส่วนส่งสัญญาณ ดังนั้น ในสภาพกัมมันต์ RTK จะก่อสภาพกัมมันต์ของจีโปรตีนแบบเล็ก ซึ่งก็เริ่มการทำงานของ guanine nucleotide exchange factor เช่น SOS1 เมื่อออกฤทธิ์แล้ว exchange factor เหล่านี้ก็สามารถเริ่มการทำงานของจีโปรตีนแบบเล็กอื่น ๆ อีก นี่เป็นการขยายต่อสัญญาณที่หน่วยรับได้โดยดั้งเดิม
การกลายพันธุ์ของยีน RTK บางอย่าง เหมือนกับที่เกิดใน GPCR อาจมีผลเป็นการแสดงออกของหน่วยรับที่อยู่ในสภาพกัมมันต์แม้ไม่ได้จับกับลิแกนด์ ยีนกลายพันธุ์เช่นนี้อาจเป็นยีนมะเร็ง (oncogene)[38]
Histidine-specific protein kinases มีโครงสร้างที่ต่างจาก protein kinase อื่น ๆ และพบอยู่ในโพรแคริโอต เห็ดรา และพืช โดยเป็นส่วนของกลไกถ่ายโอนสัญญาณที่มีองค์ประกอบสองอย่าง คือ ในเบื้องต้นจะเติมกลุ่มฟอสเฟตจากอะดีโนซีนไตรฟอสเฟต (ATP) เข้ากับเรซิดิว histidine ภายใน kinase แล้วจากนั้นจึงโอนไปให้เรซิดิว aspartate ในโดเมนส่วนรับของโปรตีนอื่น หรือของ kinase เอง ซึ่งเริ่มการทำงานของเรซิดิว aspartate[39]
Integrins
[แก้]
เซลล์มากมายหลายแบบผลิต integrin ซึ่งมีบทบาทในการยึดเซลล์เข้ากับเซลล์อื่น ๆ หรือกับเมทริกซ์นอกเซลล์ และในการถ่ายโอนสัญญาณจากองค์ประกอบของเมทริกซ์นอกเซลล์ เช่น fibronectin และคอลลาเจน ลิแกนด์ที่ยึดเข้ากับโดเมนนอกเซลล์ของ integrin จะเปลี่ยนโครงรูปของโปรตีน ซึ่งจุดชนวนการถ่ายโอนสัญญาณ แต่ integrin เองไม่มีส่วนที่ออกฤทธิ์แบบ kinase ดังนั้น กาถถ่ายโอนสัญญาณที่อำนวยโดย integrin จะทำผ่าน protein kinase และโมเลกุลอะแด็ปเตอร์ต่าง ๆ โดยตัวประสานงานหลักก็คือ integrin-linked kinase (ILK)[40] ในรูป การส่งสัญญาณร่วมกันของ integrin-RTK จะกำหนดชั่วอายุของเซลล์ อะพอพโทซิส การเพิ่มจำนวนเซลล์ และการเปลี่ยนสภาพให้แตกต่าง (differentiation)
การส่งสัญญาณโดยอาศัย integrin จะแตกต่างอย่างสำคัญระหว่างเซลล์เม็ดเลือดที่ไหลเวียนและเซลล์ที่ไม่ไหลเวียน เช่น เซลล์เยื่อบุผิว เพราะในเซลล์ที่ไหลเวียน integrin จะอยู่ในรูปแบบที่ไม่มีฤทธิ์ (ในสภาพอกัมมันต์) ยกตัวอย่างเช่น integrin บนเยื่อบุผิวของเม็ดเลือดขาวที่ไหลเวียน ปกติจะรักษาให้อยู่ในสภาพอกัมมันต์ เพื่อป้องกันไม่ให้ยึดกับเซลล์เยื่อบุผิวอื่น ๆ แต่จะออกฤทธิ์เมื่อตอบสนองต่อสิ่งเร้า เช่นที่ได้ในบริเวณที่เกิดการอักเสบ และในนัยเดียวกัน integrin ที่เยื่อหุ้มเซลล์ของเกล็ดเลือดที่ไหลเวียน ปกติจะไม่มีฤทธิ์เพื่อไม่ให้เกิดภาวะหลอดเลือดมีลิ่มเลือด (thrombosis) แต่เซลล์เยื่อบุผิว (ซึ่งไม่ใช่เซลล์ไหลเวียน) ปกติจะมี integrin ในรูปแบบซึ่งมีฤทธิ์ที่เยื่อหุ้มเซลล์ อันช่วยให้ยึดอยู่อย่างเสถียรกับเซลล์ส่วนพยุง (stromal cells) ซึ่งเป็นเซลล์ข้างใต้ที่ยังให้สัญญาณเพื่อดำรงการทำงานให้เป็นปกติด้วย[41]
ในพืช ยังไม่พบหน่วยรับ integrin ที่น่าเชื่อถือ อย่างไรก็ดี มีการเสนอโปรตีนคล้าย integrin หลายอย่าง เพราะมีโครงสร้างที่มีต้นกำเนิดเดียวกันกับ metazoan receptor[42] ที่น่าแปลกใจก็คือ พืชมี ILK ที่มีโครงสร้างปฐมภูมิคล้ายกับ ILK ของสัตว์อย่างมาก
ในพืชแบบจำลองในวงศ์ผักกาดคือ Arabidopsis thaliana ยีน ILK1 พบว่า เป็นองค์ประกอบที่ขาดไม่ได้ในการตอบสนองทางภูมิคุ้มกันของพืชต่อโมเลกุลส่งสัญญาณจากเชื้อโรค และในความไวต่อเกลือและต่อความเปลี่ยนแปลงทางออสโมซิสอื่น ๆ[43] โปรตีน ILK1 จะมีปฏิสัมพันธ์กับโปรตีนขนส่งโพแทสเซียม คือ HAK5 ที่มีสัมพรรคภาพสูง และกับหน่วยรับแคลเซียมคือ CML9[43][44]
Toll-like receptors
[แก้]เมื่อเปลี่ยนเป็นสภาพกัมมันต์ toll-like receptors (TLRs) จะใช้โมเลกุลอะแด็ปเตอร์ภายในไซโทพลาซึมเพื่อแพร่สัญญาณต่อไป มีโมเลกุลอะแด็ปเตอร์ 4 อย่างที่รู้ว่ามีบทบาทในการส่งสัญญาณ คือ Myd88, TIRAP, TRIF, และ TRAM[45][46][47] อะแด็ปเตอร์เหล่านี้จะเริ่มการทำงานของโมเลกุลในเซลล์อื่น ๆ รวมทั้ง IRAK1, IRAK4, TBK1, และ IKKi เป็นการขยายสัญญาณ ซึ่งในที่สุดนำไปสู่การเหนี่ยวนำหรือการยับยั้งการแสดงออกของยีนที่ทำให้เกิดการตอบสนองต่าง ๆ ยีนเป็นพัน ๆ เริ่มทำงานเนื่องกับการส่งสัญญาณแบบ TLR ซึ่งแสดงนัยว่า กระบวนการนี้เป็นทางผ่านที่สำคัญในการควบคุมการแสดงออกของยีน
ช่องไอออนที่เปิดปิดโดยลิแกนด์
[แก้]ช่องไอออนที่เปิดปิดโดยลิแกนด์ (ligand-gated ion channel) เมื่อจับกับลิแกนด์ก็จะเปลี่ยนโครงรูป แล้วเปิดช่องที่เยื่อหุ้มเซลล์ให้ไอออนซึ่งเป็นตัวส่งสัญญาณสามารถผ่านเข้าได้
ตัวอย่างของกลไกนี้พบได้ที่ไซแนปส์ของเซลล์ประสาทซึ่งเป็นตัวรับสัญญาณ คือ ไอออนที่ไหลเข้าไปในช่องที่เปิดโดยกระบวนการนี้ จะนำไปสู่การสร้างศักยะงานที่ส่งไปตามเส้นประสาท เพราะไอออนที่ไหลเข้าจะลดขั้วเซลล์ ซึ่งนำไปสู่การเปิดช่องไอออนที่เปิดปิดด้วยศักย์ไฟฟ้า (voltage-gated ion channel)
ตัวอย่างของไอออนที่ไหลเข้าในเซลล์เมื่อช่องไอออนเปิดปิดด้วยลิแกนดต์เปิดก็คือ Ca2+ ซึ่งทำหน้าที่เป็นโมเลกุลส่งสัญญาณที่สองโดยจุดชนวนลำดับการส่งสัญญาณที่เปลี่ยนสรีรภาพของเซลล์ ซึ่งมีผลขยายการตอบสนองต่อสัญญาณทางไซแนปส์ โดยเปลี่ยนลักษณะของเดนไดรติก สไปน์ ที่ไซแนปส์
หน่วยรับในเซลล์
[แก้]ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
หน่วยรับในเซลล์ เช่น หน่วยรับที่นิวเคลียส (nuclear receptor) และหน่วยรับในไซโทพลาสซึม (cytoplasmic receptor) เป็นโปรตีนละลายได้และอยู่เฉพาะที่ ๆ ลิแกนด์ทั่ว ๆ ไปของหน่วยรับที่นิวเคลียส จะเป็นฮอร์โมนไร้ขั้ว เช่น สเตอรอยด์ เทสโทสเตอโรน โพรเจสเทอโรน และสารอนุพันธ์ของวิตามินเอและวิตามินดี เมื่อลิแกนด์จับกับหน่วยรับ คอมเพล็กซ์ลิแกนด์+หน่วยรับก็จะผ่านเยื่อนิวเคลียสเข้าไปในนิวเคลียสแล้วเปลี่ยนการแสดงออกของยีน
หน่วยรับกัมมันต์จะเข้ายึดกับดีเอ็นเอที่ลำดับ hormone-responsive element (HRE) โดยเฉพาะ ซึ่งอยู่ในบริเวณ promoter ของยีนที่จะเริ่มทำงานเนื่องกับคอมเพล็กซ์ฮอร์โมน-หน่วยรับ ฮอร์โมนทั้งหมดที่มีฤทธิ์ควบคุมการแสดงออกของยีน มีลักษณะสองอย่างตามกลไกการทำงานของมัน คือใช้เวลานานก่อนจะเกิดผลและผลก็จะคงยืนเป็นเวลานานด้วย แม้หลังจากความเข้มข้นจะลดจนเหลือ 0 เนื่องจากเอนไซม์และโปรตีนโดยมากจะหมุนเวียนค่อนข้างช้า แต่เป็นเอนไซม์และโปรตีนซึ่งจำเป็นเพื่อยุติการจับกันระหว่างลิแกนด์กับหน่วยรับ
หน่วยรับในเซลล์บางอย่างของระบบภูมิคุ้มกันจะอยู่ในไซโทพลาซึม หน่วยรับ NOD-like receptors (NLRs) ที่พึ่งค้นพบได้ไม่นาน อยู่ในไซโทพลาซึมของเซลล์ยูแคริโอตบางอย่าง และมีปฏิสัมพันธ์กับลิแกนด์โดยใช้ leucine-rich repeat (LRR) motif เหมือนกับ TLR คือ โมเลกุลเหล่านี้บางส่วนเช่น NOD2 จะมีปฏิสัมพันธ์กับ RIP2 kinase ที่เริ่มการส่งสัญญาณของ NF-κB และบางส่วนเช่น NALP3 จะมีปฏิสัมพันธ์กับเอนไซม์ caspase ซึ่งเกี่ยวกับกระบวนการอักเสบ แล้วจุดชนวนการดำเนินงานกับ cytokine โดยเฉพาะ ๆ เช่น interleukin-1β[48][49]
โมเลกุลส่งสัญญาณที่สอง
[แก้]โมเลกุลส่งสัญญาณที่หนึ่งอาจเป็นฮอร์โมน สารสื่อประสาท และสารส่งสัญญาณแบบ paracrine (จากเซลล์ข้าง ๆ) หรือ autocrine (หรือจากตนเอง) ที่เข้ามาถึงเซลล์จากสื่อรอบ ๆ เซลล์แล้วจับกับหน่วยรับโดยเฉพาะ ๆ ส่วนโมเลกุลส่งสัญญาณที่สองก็คือสารที่เข้าไปในไซโทพลาซึม แล้วออกฤทธิ์ภายในเซลล์ให้เกิดการตอบสนอง หลัก ๆ ก็คือ โมเลกุลส่งสัญญาณที่สองเป็นตัวรีเลย์ทางเคมีจากเยื่อหุ้มเซลล์ไปยังไซโทพลาซึม เป็นตัวถ่ายโอนสัญญาณภายในเซลล์
แคลเซียม
[แก้]ไอออนแคลเซียมที่ปล่อยจากร่างแหเอนโดพลาซึม (ER) เข้าไปในไซโตซอล จะจับกับโปรตีนส่งสัญญาณทำให้เปลี่ยนเป็นสารกัมมันต์ หลังจากนั้นมันจึงจะแยกเก็บใน smooth endoplasmic reticulum[50] และไมโทคอนเดรีย โปรตีนหน่วยรับที่ประกอบกับช่องไอออนสองอย่างเป็นตัวควบคุมการปล่อยแคลเซียมผ่านเยื่อ ER
โปรตีน Inositol trisphosphate receptor (InsP3-receptor) จะเริ่มปล่อยแคลเซียมหลังจากมีปฏิสัมพันธ์กับ inositol triphosphate (IP3) ทางด้านไซโตซอล ส่วน ryanodine receptor ซึ่งตั้งชื่อตามแอลคาลอยด์ ryanodine จะคล้ายกับ InsP3 receptor แต่มีปฏิสัมพันธ์กับแคลแซียมเอง ดังนั้น จึงเป็นกลไกการป้อนกลับเชิงบวกที่ปล่อยแคลเซียมออกเพิ่มขึ้นหลังจับกันมันทางด้านไซโตซอล ความเป็นไปของแคลเซียมในไซโตซอลหมายความว่า มันมีฤทธิ์ในช่วงระยะที่สั้นมาก คือ มีความเข้มข้นต่ำมากเมื่อเป็นอิสระ และในสภาพอกัมมันต์ โดยมากก็จะจับอยู่กับโมเลกุลในออร์แกเนลล์ เช่น calreticulin
แคลเซียมมีบทบาทในกระบวนการต่าง ๆ มากมายรวมทั้งการหดเกร็งกล้ามเนื้อ การปล่อยสารสื่อประสาทจากประสาท และการย้ายที่เซลล์ (cell migration) วิถีการถ่ายโอนสัญญาณหลัก ๆ 3 ทาง ที่ทำให้แคลเซียมออกฤทธิ์รวมทั้ง GPCR pathway, RTK pathway, และช่องไอออนที่เปิดปิดโดยวิธีต่าง ๆ แคลเซียมออกฤทธิ์ควบคุมโปรตีนไม่ว่าจะโดยตรงหรือว่าโดยจับกับเอนไซม์
ลิพิดส่งสัญญาณ
[แก้]โมเลกุลส่งสัญญาณที่สองซึ่งชอบลิพิด เป็นสารอนุพันธ์จากลิพิดที่อยู่ในเยื่อหุ้มเซลล์ โดยเอนไซม์ที่กระตุ้นโดยหน่วยรับกัมมันต์ จะเปลี่ยนลิพิดให้มีสภาพกัมมันต์เป็นโมเลกุลส่งสัญญาณที่สอง ตัวอย่างรวมทั้ง diacylglycerol และ ceramide โดยอย่างแรกจำเป็นในการก่อกัมมันต์ของ protein kinase C
ไนตริกออกไซด์
[แก้]ไนตริกออกไซด์ (NO) สามารถออกฤทธิ์เป็นโมเลกุลส่งสัญญาณที่สอง เพราะมันเป็นอนุมูลอิสระอย่างหนึ่งที่สามารถแพร่ผ่านเยื่อหุ้มเซลล์ แล้วออกฤทธิ์ต่อเซลล์ที่อยู่ใกล้ ๆ มันสังเคราะห์มาจากอาร์จินีนและออกซิเจนโดย Nitric oxide synthase (NO synthase) และออกฤทธิ์โดยก่อสภาพกัมมันต์ของ soluble guanylyl cyclase แล้วสร้างโมเลกุลส่งสัญญาณที่สอง คือ cGMP อนึ่ง NO ยังสามารถออกฤทธิ์ผ่านการเปลี่ยนพันธะโคเวเลนต์ของโปรตีนหรือของ metal co-factor ของโปรตีน ซึ่งบางอย่างมีกลไกผ่านปฏิกิริยารีดอกซ์ที่สามารถผันกลับได้ NO มีพิษถ้าเข้มข้นสูง และทำความเสียหายเมื่อเกิดเส้นเลือดอุดตันในสมอง แต่ก็เป็นเหตุของกลไกการทำงานต่าง ๆ ในร่างกายเช่น การคลายเส้นเลือด อะพอพโทซิส และการแข็งตัวขององคชาต
การส่งสัญญาณโดยปฏิกิริยารีดอกซ์
[แก้]นอกจากไนตริกออกไซด์ ยังมีสารเคมีอื่น ๆ ที่สามารถถ่ายโอนสัญญาณโดยปฏิกิริยารีดอกซ์ (redox signaling) ตัวอย่างรวมทั้ง superoxide, ไฮโดรเจนเพอร์ออกไซด์, คาร์บอนมอนอกไซด์, และไฮโดรเจนซัลไฟด์ การส่งสัญญาณโดยปฏิกิริยารีดอกซ์รวมการควบคุมการไหลของกระแสไฟฟ้าอย่างแอ๊กถีฟในแมโครโมเลกุลชีวภาพแบบกึ่งตัวนำ[51]
การตอบสนองของเซลล์
[แก้]การเริ่มการทำงาน/การก่อสภาพกัมมันต์ของยีน (gene activation)[52] และการเปลี่ยนเมทาบอลิซึม[53] เป็นตัวอย่างการตอบสนองของเซลล์ต่อสิ่งเร้านอกเซลล์ผ่านการถ่ายโอนสัญญาณ และยีนในสภาพกัมมันต์ก็จะมีผลอื่น ๆ ภายในเซลล์ เพราะผลิตภัณฑ์ของยีนเป็นตัวก่อให้เกิดสภาพกัมมันต์อื่น ๆ คือแฟกเตอร์ถอดรหัส (transcription factor) ที่เป็นผลของลำดับการถ่ายโอนสัญญาณ สามารถก่อสภาพกัมมันต์ของยีนอื่น ๆ อีก ดังนั้น สิ่งเร้าเบื้องต้นสามารถจุดชนวนการแสดงออกของยีนจำนวนมาก ทำให้เกิดเหตุการณ์ทางสรีรภาพ เช่น การดูดซึมกลูโคสนำเข้าเนื้อเยื่อจากเลือด[53] และการย้ายที่ของ neutrophils ไปยังบริเวณที่ติดเชื้อ เซตของยีนและลำดับการทำงานของพวกมันเนื่องจากสิ่งเร้าโดยเฉพาะ ๆ จะเรียกว่าได้ว่า โปรแกรมยีน (genetic program)[54]
เซลล์ของสัตว์เลี้ยงลูกด้วยนมจะต้องได้รับสิ่งเร้าเพื่อการแบ่งเซลล์และการรอดชีวิต ถ้าไร้ growth factor อะพอพโทซิสก็จะเกิดขึ้น เพราะการได้สิ่งเร้าจากนอกเซลล์เป็นเรื่องจำเป็นในการควบคุมการทำงานของเซลล์ทั้งในสิ่งมีชีวิตเซลล์เดียวและหลายเซลล์ วิถีการถ่ายโอนสัญญาณจึงพิจารณาว่าเป็นหลักสำคัญของกระบวนการทางชีวภาพ จนกระทั่งโรคจำนวนมากได้อ้างว่า มีเหตุจากการทำงานผิดปกติของพวกมัน
สัญญาณพื้นฐาน 3 อย่างเป็นตัวกำหนดการเติบโตของเซลล์
- แบบกระตุ้นจาก growth factor
- การตอบสนองที่อาศัยการถอดรหัส
- ตัวอย่างเช่น สเตอรอยด์สามารถออกฤทธิ์โดยตรงเป็นแฟกเตอร์ถอดรหัส ทำให้ตอบสนองค่อนข้างช้า เพราะมันต้องจับกับดีเอ็นเอแล้วตามด้วยการถอดรหัส เอ็มอาร์เอ็นเอที่ผลิตก็จะต้องแปล และโปรตีน/เพปไทด์ที่ผลิตอาจต้องผ่านกระบวนการดัดแปลงหลังแปล (Post-translational modification)
- การตอบสนองที่เป็นอิสระจากการถอดรหัส
- ตัวอย่างเช่น epidermal growth factor (EGF) จะจับกับหน่วยรับคือ epidermal growth factor receptor (EGFR) ซึ่งทำให้ EGFR เปลี่ยนรูปแบบเป็นไดเมอร์หรือเกิดปฏิกิริยาฟอสโฟรีเลชันอัตโนมัติ (autophosphorylation) ซึ่งก็จะจุดชนวนวิถีการส่งสัญญาณภายในเซลล์ลำดับต่อ ๆ ไป[55]
- การตอบสนองที่อาศัยการถอดรหัส
- แบบยับยั้งเมื่อเซลล์มาถูกกัน (cell-cell contact)
- แบบ permissive โดยเป็นปฏิสัมพันธ์ระหว่างเซลล์และเมทริกซ์นอกเซลล์
สัญญาณเหล่านี้ รวม ๆ มีผลเป็นการทำงานในไซโทพลาสซึมที่ต่าง ๆ กัน ทำให้เซลล์ตอบสนองต่าง ๆ กัน
วิถีการถ่ายโอนสัญญาณหลัก ๆ
[แก้]ต่อไปนี้เป็นวิถีการถ่ายโอนสัญญาณหลัก ๆ บางอย่าง ซึ่งแสดงการจับของลิแกนด์กับหน่วยรับ โดยอาจมีผลต่อโมเลกุลส่งสัญญาณที่สอง แล้วในที่สุดเปลี่ยนการตอบสนองของเซลล์
- MAPK/ERK pathway - เป็นวิถีที่ทำให้เซลล์ตอบสนองเนื่องกับการจับกันของ growth factor กับหน่วยรับที่ผิวเซลล์ด้านนอก เป็นวิถีที่ซับซ้อนและมีองค์ประกอบเป็นโปรตีนมากมายหลายชนิด[56] ในเซลล์หลายชนิด การทำงานของวิถีนี้โปรโหมตการแบ่งเซลล์ และรูปแบบของมะเร็งหลายอย่างสัมพันธ์กับการทำงานที่ผิดปกติ[57]
- cAMP-dependent pathway - ในมนุษย์ cAMP ทำหน้าที่โดยเริ่มการทำงานของ protein kinase A (PKA, cAMP-dependent protein kinase) (ดูรูป) ดังนั้น ผลสืบ ๆ มาจะขึ้นอยู่กับ cAMP-dependent protein kinase ซึ่งจะต่าง ๆ กันขึ้นอยู่กับชนิดของเซลล์
- IP3/DAG pathway - Phospholipase C (PLC) จะแยกฟอสโฟลิพิด คือ phosphatidylinositol 4,5-bisphosphate (PIP2) ให้เป็น diacyl glycerol (DAG) และ inositol 1,4,5-triphosphate (IP3) ผลผลิตคือ DAG จะดำรงยึดอยู่กับเยื่อหุ้มเซลล์ ในขณะที่ IP3 จะแยกออกเป็นโครงสร้างละลายได้แล้วแพร่ไปในไซโตซอลเข้ายึดกับหน่วยรับ IP3 receptor โดยเฉพาะที่ประกอบกับช่องแคลเซียมที่ร่างแหเอนโดพลาซึม (ER) ช่องเหล่านี้จำกัดเฉพาะกับแคลเซียม และปล่อยให้แคลเซียมเท่านั้นไหลผ่าน ซึ่งเพิ่มความเข้มข้นของแคลเซียมภายในไซโตซอล และเป็นเหตุให้ลำดับการเปลี่ยนแปลงและการทำงานของเซลล์ต่อ ๆ ไปเกิดขึ้น[58] อนึ่ง แคลเซียมจะทำงานร่วมกับ DAG เพื่อเริ่มการทำงานของ protein kinase C (PKC) ซึ่งก็จะเพิ่มกลุ่ม phosphoryl ให้กับโมเลกุลอื่นผ่านปฏิกิริยาฟอสโฟรีเลชัน แล้วเปลี่ยนการทำงานของเซลล์ ผลที่สุดของกระบวนการนี้รวมทั้งการรู้รส โรคอารมณ์สองขั้ว การโปรโหมตเนื้องอก เป็นต้น[58]
ประวัติ
[แก้]
ไอเดียแรกสุดเกี่ยวกับการถ่ายโอนสัญญาณเริ่มมาจากปี 1855 เมื่อนักสรีรวิทยาชาวฝรั่งเศส (Claude Bernard) เสนอว่า ต่อมไร้ท่อเช่น ม้าม ต่อมไทรอยด์ และต่อมหมวกไต เป็นตัวการปล่อย "สารหลั่งภายใน (internal secretions)" ที่มีผลทางสรีรภาพ[59] ต่อมานักสรีรวิทยาชาวอังกฤษ (Ernest Starling) จึงตั้งชื่อสารหลั่งเช่นนี้ว่า "ฮอร์โมน" ในปี 1905[60] โดยร่วมงานกับนักสรีรวิทยาชาวอังกฤษอีกท่าน (William Bayliss) ทั้งสองได้ระบุฮอร์โมน secretin ในปี 1902[59] ในปีต่อ ๆ มาแม้จะได้ค้นพบฮอร์โมนอื่น ๆ อีกมากมาย ที่เด่นสุดก็คืออินซูลิน แต่กลไกการทำงานก็ยังไม่ได้ระบุ
การค้นพบ nerve growth factor ของนักประสาทวิทยาชาวอิตาลี (Rita Levi-Montalcini) ในปี 1954 และ epidermal growth factor ของนักเคมีชีวภาพชาวอเมริกัน (Stanley Cohen) ในปี 1962 ทำให้เข้าใจพื้นฐานในระดับโมเลกุลของการถ่ายโอนสัญญาณมากขึ้น โดยเฉพาะที่เกี่ยวกับ growth factor[61] พร้อมกับงานค้นพบ cyclic AMP ของนักเคมีชีวภาพชาวอเมริกัน (Earl Wilbur Sutherland) ในปี 1956 งานเหล่านี้ทำให้ต้องนิยามความหมายของคำว่า endocrine signaling ใหม่โดยรวมแต่การส่งสัญญาณจากต่อมต่าง ๆ แล้วเริ่มการใช้คำว่า autocrine (การส่งสัญญาณให้ตัวเอง) และ paracrine (การส่งสัญญาณให้เซลล์ข้าง ๆ)[62] เพราะงานเหล่านี้ นักวิชาการพวกนี้จึงได้รับรางวัลโนเบลสาขาสรีรวิทยาหรือการแพทย์ในปี 1971 (คนหลังสุด) และ 1986 (สองคนแรก)
ในปี 1970 นักเคมีชีวภาพชาวอเมริกัน (Martin Rodbell) ตรวจสอบกลูคากอนที่หน่วยรับที่เยื่อหุ้มเซลล์ของตับในหนู แล้วให้ข้อสังเกตว่า guanosine triphosphate (GTP) ทำให้กลูคากอนแตกออกจากหน่วยรับแล้วไปกระตุ้นจีโปรตีน ซึ่งมีผลที่มีกำลังต่อเมแทบอลิซึมของเซลล์ ดังนั้น เขาจึงสรุปโดยนิรนัยว่า จีโปรตีนเป็นตัวแปรสัญญาณ (transducer) ที่ออกฤทธิ์เมื่อได้กลูคากอน แล้วจึงมีผลต่อเซลล์[63] ในปี 1994 เขาจึงได้รับรางวัลโนเบลสาขาสรีรวิทยาหรือการแพทย์ร่วมกันนักเคมีชีวภาพชาวอเมริกันอีกท่านหนึ่ง (Alfred G. Gilman)
การระบุ RTK และ GPCR ต่อมาจึงนำไปสู่ไอเดียเกี่ยวกับการถ่ายโอนสัญญาณ (signal transduction) โดยเป็นคำที่ใช้เป็นครั้งแรกในปี 1972[64] แม้วรรณกรรมต้น ๆ ก็ได้ใช้คำว่า signal transmission และ sensory transduction (การถ่ายโอนความรู้สึก) ด้วย[65][66]
ในปี 2007 มีงานตีพิมพ์ทางวิทยาศาสตร์ 48,377 งาน รวมงานทบทวนโดยผู้รู้เสมอกัน 11,211 งาน เกี่ยวกับประเด็นนี้ โดยเป็นคำที่ปรากฏในชื่อของวรรรณกรรมเป็นครั้งแรกในปี 1979[67][68] คำเริ่มนิยมแพร่หลายเพิ่มขึ้นเริ่มตั้งแต่งานทบทวนวรรณกรรมในปี 1980 (ของ Martin Rodbell)[63][69] และงานวิจัยเฉพาะในเรื่องการถ่ายโอนสัญญาณก็เริ่มปรากฏอย่างแพร่หลายในปลายคริสต์ทศวรรษ 1980 และต้นทศวรรษ 1990[70]
ดูเพิ่ม
[แก้]เชิงอรรถ
[แก้]- ↑

ความแออัดของแมโครโมเลกุลในไซโตซอลของเซลล์จะเปลี่ยนคุณสมบัติของโมเลกุลต่าง ๆ เช่น โปรตีนและกรดนิวคลีอิก[20] ปรากฏการณ์ความแออัดของแมโครโมเลกุล (macromolecular crowding) จะเปลี่ยนคุณสมบัติของโมเลกุลในสารละลายในที่ ๆ แมโครโมเลกุล (โมเลกุลขนาดใหญ่) เช่นโปรตีน มีความเข้มข้นสูง เป็นปรากฏการณ์ที่เกิดเป็นปกติในเซลล์ที่มีชีวิต ยกตัวอย่างเช่น ไซโตซอลของแบคทีเรีย Escherichia coli มีแมโครโมเลกุลประมาณ 300-400 mg/mL ความแออัดเกิดขึ้นเพราะแมโครโมเลกุลที่มีความเข้มข้นสูง จะลดปริมาตรของตัวทำละลายสำหรับโมเลกุลอื่น ๆ ในสารละลาย ซึ่งเท่ากับเพิ่มความเข้มข้นยังผลของโมเลกุลเหล่านั้น
อ้างอิง
[แก้]- ↑
Mai, Larry L; Owl, Marcus Young; Kersting, M Patricia (2005). signal transduction. The Cambridge Dictionary of Human Biology and Evolution. Cambridge University Press. p. 487. ISBN 978-0-521-66486-8.
process of one or more steps through which receptor activation leads to a cellular response.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Lackie, JM (2007). signal transduction. The Dictionary of Cell and Molecular Biology (4th ed.). Elsevier. p. 387. ISBN 978-0-12-373986-5.
The cascade of processes by which an extracellular signal (typically a hormone or neurotrans mitter) interacts with a receptor at the cell surface, causing a change in the level of a second messenger (for example calcium or cyclic AMP) and ultimately effects a change in the cell’s functioning (for example, triggering glucose uptake, or initiating cell division).
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Bradshaw RA, Dennis EA, บ.ก. (2010). Handbook of Cell Signaling (2nd ed.). Amsterdam, Netherlands: Academic Press. ISBN 9780123741455.
- ↑ Papin, Jason A.; Hunter, Tony; Palsson, Bernhard O.; Subramaniam, Shankar (January 14, 2005). "Reconstruction of cellular signalling networks and analysis of their properties". Nature Reviews Molecular Cell Biology. 6 (2): 99–111. doi:10.1038/nrm1570. PMID 15654321.
- ↑ Krauss, Gerhard (2008). Biochemistry of Signal Transduction and Regulation. Wiley-VCH. p. 15. ISBN 978-3527313976.
- ↑ Reece, Jane; Campbell, Neil (2002). Biology. San Francisco: Benjamin Cummings. ISBN 0-8053-6624-5.
- ↑ Kolch, Walter; Halasz, Melinda; Granovskaya, Marina; Kholodenko, Boris N. (August 20, 2015). "The dynamic control of signal transduction networks in cancer cells". Nature Reviews Cancer. 15 (9): 515–527. doi:10.1038/nrc3983. PMID 26289315.
- ↑ Bago, R; Sommer, E; Castel, P; Crafter, C; Bailey, FP; Shpiro, N; Baselga, J; Cross, D; Eyers, PA; Alessi, DR (2016). "The hVps34-SGK3 pathway alleviates sustained PI3K/Akt inhibition by stimulating mTORC1 and tumour growth". EMBO Journal. 35: 1902–22.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Smogorzewska, A. (August 15, 2002). "Different telomere damage signaling pathways in human and mouse cells". The EMBO Journal. 21 (16): 4338–4348. doi:10.1093/emboj/cdf433.
- ↑ Lawrence, Peter A.; Levine, Michael (April 2006). "Mosaic and regulative development: two faces of one coin". Current Biology. 16 (7): R236–R239. doi:10.1016/j.cub.2006.03.016. PMID 16581495.
- ↑ Beato, M; Chávez, S; Truss, M (April 1996). "Transcriptional regulation by steroid hormones". Steroids. 61 (4): 240–251. doi:10.1016/0039-128X(96)00030-X. PMID 8733009.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Hammes, SR (March 2003). "The further redefining of steroid-mediated signaling". Proceedings of the National Academy of Sciences of the United States of America. 100 (5): 2168–70. Bibcode:2003PNAS..100.2168H. doi:10.1073/pnas.0530224100. PMC 151311. PMID 12606724.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Ronnett, GV; Moon, C (2002). "G proteins and olfactory signal transduction". Annual Review of Physiology. 64 (1): 189–222. doi:10.1146/annurev.physiol.64.082701.102219. PMID 11826268.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Missale, C; Nash, SR; Robinson, SW; Jaber, M; Caron, MG (January 1998). "Dopamine receptors: from structure to function". Physiological Reviews. 78 (1): 189–225. doi:10.1152/physrev.1998.78.1.189. PMID 9457173.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Goldstein, A (September 1976). "Opioid peptides endorphins in pituitary and brain". Science. 193 (4258): 1081–6. Bibcode:1976Sci...193.1081G. doi:10.1126/science.959823. PMID 959823.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Koboldt, Daniel C.; Fulton, Robert S.; McLellan, Michael D.; Schmidt, Heather; Kalicki-Veizer, Joelle; McMichael, Joshua F.; Fulton, Lucinda L.; และคณะ (September 23, 2012). "Comprehensive molecular portraits of human breast tumours". Nature. 490 (7418): 61–70. doi:10.1038/nature11412. PMC 3465532. PMID 23000897.
- ↑ Dupont, Sirio; Morsut, Leonardo; Aragona, Mariaceleste; Enzo, Elena; Giulitti, Stefano; Cordenonsi, Michelangelo; Zanconato, Francesca; Le Digabel, Jimmy; Forcato, Mattia; Bicciato, Silvio; Elvassore, Nicola; Piccolo, Stefano (June 8, 2011). "Role of YAP/TAZ in mechanotransduction". Nature. 474 (7350): 179–183. doi:10.1038/nature10137. PMID 21654799.
- ↑ Ingber, D. E. (March 29, 2006). "Cellular mechanotransduction: putting all the pieces together again". The FASEB Journal. 20 (7): 811–827. doi:10.1096/fj.05-5424rev. PMID 16675838.
- ↑ Kung, Ching (August 4, 2005). "A possible unifying principle for mechanosensation". Nature. 436 (7051): 647–654. doi:10.1038/nature03896. PMID 16079835.
- ↑ Goodsell, DS (1991). "Inside a living cell". Trends Biochem. Sci. 16 (6): 203–6. doi:10.1016/0968-0004(91)90083-8. PMID 1891800.
- ↑ 21.0 21.1 Pedersen, S. F.; Kapus, A.; Hoffmann, E. K. (August 18, 2011). "Osmosensory Mechanisms in Cellular and Systemic Volume Regulation". Journal of the American Society of Nephrology. 22 (9): 1587–1597. doi:10.1681/ASN.2010121284.
- ↑ Verbalis, J. G. (November 14, 2007). "How Does the Brain Sense Osmolality?". Journal of the American Society of Nephrology. 18 (12): 3056–3059. doi:10.1681/ASN.2007070825.
- ↑ Hohmann, S. (June 1, 2002). "Osmotic Stress Signaling and Osmoadaptation in Yeasts". Microbiology and Molecular Biology Reviews. 66 (2): 300–372. doi:10.1128/MMBR.66.2.300-372.2002.
- ↑ 24.0 24.1 Sengupta, Piali; Garrity, Paul (April 2013). "Sensing temperature". Current Biology. 23 (8): R304–R307. doi:10.1016/j.cub.2013.03.009.
- ↑ Shamovsky, Ilya; Ivannikov, Maxim; Kandel, Eugene S.; Gershon, David; Nudler, Evgeny (March 23, 2006). "RNA-mediated response to heat shock in mammalian cells". Nature. 440 (7083): 556–560. doi:10.1038/nature04518. PMID 16554823.
- ↑ Burns, ME; Arshavsky, VY (November 2005). "Beyond counting photons: trials and trends in vertebrate visual transduction". Neuron. 48 (3): 387–401. doi:10.1016/j.neuron.2005.10.014. PMID 16269358.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Berson, David M. (March 10, 2007). "Phototransduction in ganglion-cell photoreceptors". Pflügers Archiv - European Journal of Physiology. 454 (5): 849–855. doi:10.1007/s00424-007-0242-2. PMID 17351786.
- ↑ "A molecular model for receptor activation" (PDF).
- ↑ 29.0 29.1 29.2 Fredriksson, R. (February 9, 2005). "The Repertoire of G-Protein-Coupled Receptors in Fully Sequenced Genomes". Molecular Pharmacology. 67 (5): 1414–1425. doi:10.1124/mol.104.009001.
- ↑ Qin, K; Dong, C; Wu, G; Lambert, NA (October 2011). "Inactive-state preassembly of G(q) -coupled receptors and G(q) heterotrimers". Nature Chemical Biology. 7 (10): 740–7. doi:10.1038/nchembio.642. PMC 3177959. PMID 21873996.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Berg, Jeremy M; Tymoczko, John L; Stryer, Lubert (2002). Biochemistry. Web content by Neil D. Clarke. San Francisco: W.H. Freeman. ISBN 0-7167-4954-8.
{{cite book}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Yang, W; Xia, S (2006). "Mechanisms of regulation and function of G-protein-coupled receptor kinases". World J Gastroenterol. 12 (48): 7753–7. doi:10.3748/wjg.v12.i48.7753. PMID 17203515.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Burger, M; Burger, JA; Hoch, RC; Oades, Z; Takamori, H; Schraufstatter, IU (August 1999). "Point mutation causing constitutive signaling of CXCR2 leads to transforming activity similar to Kaposi's sarcoma herpesvirus-G protein-coupled receptor". Journal of Immunology. 163 (4): 2017–22. PMID 10438939.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 34.0 34.1 Li, E; Hristova, K (May 2006). "Role of receptor tyrosine kinase transmembrane domains in cell signaling and human pathologies". Biochemistry. 45 (20): 6241–51. doi:10.1021/bi060609y. PMC 4301406. PMID 16700535.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Schlessinger, J (November 1988). "Signal transduction by allosteric receptor oligomerization". Trends in Biochemical Sciences. 13 (11): 443–7. doi:10.1016/0968-0004(88)90219-8. PMID 3075366.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Manning, G; Whyte, DB (2002). "The protein kinase complement of the human genome". Science. 298 (5600): 1912–1934. doi:10.1126/science.1075762. PMID 12471243.
- ↑
Reiterer, V; Eyers, PA; Farhan, H (2014). "Day of the dead: pseudokinases and pseudophosphatases in physiology and disease". Trends in Cell Biology. 24 (9): 489–505. doi:10.1016/j.tcb.2014.03.008. PMID 24818526.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Roskoski, R (June 2004). "The ErbB/HER receptor protein-tyrosine kinases and cancer". Biochemical and Biophysical Research Communications. 319 (1): 1–11. doi:10.1016/j.bbrc.2004.04.150. PMID 15158434.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Wolanin, PM; Thomason, PA; Stock, JB (September 2002). "Histidine protein kinases: key signal transducers outside the animal kingdom". Genome Biology. 3 (10): REVIEWS3013. doi:10.1186/gb-2002-3-10-reviews3013. PMC 244915. PMID 12372152. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ August 26, 2015. สืบค้นเมื่อ May 27, 2018.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 40.0 40.1 Hehlgans, S; Haase, M; Cordes, N (January 2007). "Signalling via integrins: implications for cell survival and anticancer strategies". Biochimica et Biophysica Acta. 1775 (1): 163–80. doi:10.1016/j.bbcan.2006.09.001. PMID 17084981.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Gilcrease, MZ (March 2007). "Integrin signaling in epithelial cells". Cancer Letters. 247 (1): 1–25. doi:10.1016/j.canlet.2006.03.031. PMID 16725254.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Knepper, Caleb; Savory, Elizabeth A.; Day, Brad (May 1, 2011). "Arabidopsis NDR1 Is an Integrin-Like Protein with a Role in Fluid Loss and Plasma Membrane-Cell Wall Adhesion". Plant Physiology (ภาษาอังกฤษ). 156 (1): 286–300. doi:10.1104/pp.110.169656. ISSN 1532-2548. PMC 3091050. PMID 21398259.
- ↑ 43.0 43.1 Brauer, Elizabeth K.; Ahsan, Nagib; Dale, Renee; Kato, Naohiro; Coluccio, Alison E.; Piñeros, Miguel A.; Kochian, Leon V.; Thelen, Jay J.; Popescu, Sorina C. (June 1, 2016). "The Raf-like Kinase ILK1 and the High Affinity K+ Transporter HAK5 Are Required for Innate Immunity and Abiotic Stress Response". Plant Physiology (ภาษาอังกฤษ). 171 (2): 1470–1484. doi:10.1104/pp.16.00035. ISSN 1532-2548. PMC 4902592. PMID 27208244.
- ↑ Popescu, Sorina C.; Popescu, George V.; Bachan, Shawn; Zhang, Zimei; Seay, Montrell; Gerstein, Mark; Snyder, Michael; Dinesh-Kumar, S. P. (March 13, 2007). "Differential binding of calmodulin-related proteins to their targets revealed through high-density Arabidopsis protein microarrays". Proceedings of the National Academy of Sciences (ภาษาอังกฤษ). 104 (11): 4730–4735. doi:10.1073/pnas.0611615104. ISSN 0027-8424. PMC 1838668. PMID 17360592.
- ↑
Yamamoto, M; Sato, S; Hemmi, H; Hoshino, K; Kaisho, T; Sanjo, H; Takeuchi, O; Sugiyama, M; Okabe, M; Takeda, K; Akira, S (August 2003). "Role of adaptor TRIF in the MyD88-independent toll-like receptor signaling pathway". Science. 301 (5633): 640–3. Bibcode:2003Sci...301..640Y. doi:10.1126/science.1087262. PMID 12855817.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Yamamoto, M; Sato, S; Hemmi, H; Uematsu, S; Hoshino, K; Kaisho, T; Takeuchi, O; Takeda, K; Akira, S (November 2003). "TRAM is specifically involved in the Toll-like receptor 4-mediated MyD88-independent signaling pathway". Nature Immunology. 4 (11): 1144–50. doi:10.1038/ni986. PMID 14556004.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Yamamoto, M; Sato, S; Hemmi, H; Sanjo, H; Uematsu, S; Kaisho, T; Hoshino, K; Takeuchi, O; Kobayashi, M; Fujita, T; Takeda, K; Akira, S (November 2002). "Essential role for TIRAP in activation of the signalling cascade shared by TLR2 and TLR4". Nature. 420 (6913): 324–9. Bibcode:2002Natur.420..324Y. doi:10.1038/nature01182. PMID 12447441.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Delbridge, LM; O'Riordan, MX (February 2007). "Innate recognition of intracellular bacteria". Current Opinion in Immunology. 19 (1): 10–6. doi:10.1016/j.coi.2006.11.005. PMID 17126540.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Vander; และคณะ (1998). Human Physiology. McGraw-Hill. p. 160. ISBN 0-07-067065-X.
- ↑ Wilson, CH; Ali, ES; Scrimgeour, N; Martin, AM; Hua, J; Tallis, GA; Rychkov, GY; Barritt, GJ (2015). "Steatosis inhibits liver cell store-operated Ca (2) (+) entry and reduces ER Ca (2) (+) through a protein kinase C-dependent mechanism". Biochem J. 466: 379–390. doi:10.1042/bj20140881. PMID 25422863.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Forman, HJ (2009). "Signal transduction and reactive species". Free Radic. Biol. Med. 47: 1237–1238.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Lalli, E; Sassone-Corsi, P (July 1994). "Signal transduction and gene regulation: the nuclear response to cAMP". The Journal of Biological Chemistry. 269 (26): 17359–62. PMID 8021233.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 53.0 53.1 Rosen, OM (September 1987). "After insulin binds". Science. 237 (4821): 1452–8. Bibcode:1987Sci...237.1452R. doi:10.1126/science.2442814. PMID 2442814.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Massagué, J; Gomis, RR (May 2006). "The logic of TGFbeta signaling". FEBS Letters. 580 (12): 2811–20. doi:10.1016/j.febslet.2006.04.033. PMID 16678165.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Sako, Y; Minoghchi, S; Yanagida, T (March 2000). "Single-molecule imaging of EGFR signalling on the surface of living cells". Nature Cell Biology. 2 (3): 168–72. doi:10.1038/35004044. PMID 10707088.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Orton, RJ; Sturm, OE; Vyshemirsky, V; Calder, M; Gilbert, DR; Kolch, W (December 2005). "Computational modelling of the receptor-tyrosine-kinase-activated MAPK pathway". The Biochemical Journal. 392 (Pt 2): 249–61. doi:10.1042/BJ20050908. PMC 1316260. PMID 16293107.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Vogelstein, B; Kinzler, KW (August 2004). "Cancer genes and the pathways they control". Nature Medicine. 10 (8): 789–99. doi:10.1038/nm1087. PMID 15286780.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 58.0 58.1 Alberts, B; Lewis, J; Raff, M; Roberts, K; Walter, P (2002). Molecular biology of the cell (4th ed.). New York: Garland Science. ISBN 0-8153-3218-1.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 59.0 59.1 Bradshaw & Dennis (2010), p. 1
- ↑ Tata, Jamshed R. (June 2005). "One hundred years of hormones". EMBO Reports. 6 (6): 490–496. doi:10.1038/sj.embor.7400444. PMC 1369102. PMID 15940278.
- ↑ Cowan, W. Maxwell (March 2001). "Viktor Hamburger and Rita Levi-Montalcini: the path to the discovery of nerve growth factor". Annual Review of Neuroscience. 24 (1): 551–600. doi:10.1146/annurev.neuro.24.1.551. PMID 11283321.
- ↑ Bradshaw & Dennis (2010), p. 2
- ↑ 63.0 63.1 Rodbell, M (March 1980). "The role of hormone receptors and GTP-regulatory proteins in membrane transduction". Nature. 284 (5751): 17–22. Bibcode:1980Natur.284...17R. doi:10.1038/284017a0. PMID 6101906.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Rensing, L (1972). "Periodic geophysical and biological signals as Zeitgeber and exogenous inducers in animal organisms". International Journal of Biometeorology. 16 Suppl: 113–25. PMID 4621276.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Tonndorf, J (September 1975). "Davis-1961 revisited. Signal transmission in the cochlear hair cell-nerve junction". Archives of Otolaryngology. 101 (9): 528–35. doi:10.1001/archotol.1975.00780380006002. PMID 169771.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Ashcroft, SJ; Crossley, JR; Crossley, PC (March 1976). "The effect of N-acylglucosamines on the biosynthesis and secretion of insulin in the rat". The Biochemical Journal. 154 (3): 701–7. doi:10.1042/bj1540701. PMC 1172772. PMID 782447.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Hildebrand, E (April 1977). "What does Halobacterium tell us about photoreception?". Biophysics of Structure and Mechanism. 3 (1): 69–77. doi:10.1007/BF00536457. PMID 857951.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑
Kenny, JJ; Martínez-Maza, O; Fehniger, T; Ashman, RF (April 1979). "Lipid synthesis: an indicator of antigen-induced signal transduction in antigen-binding cells". Journal of Immunology. 122 (4): 1278–84. PMID 376714.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Gomperts, BD; Kramer, IM; Tatham, PE (2002). Signal transduction. Academic Press. ISBN 0-12-289631-9.
- ↑ Vander; และคณะ (1998). Human Physiology. McGraw-Hill. p. 159. ISBN 0-07-067065-X.
แหล่งข้อมูลอื่น
[แก้]- Netpath - A curated resource of signal transduction pathways in humans เก็บถาวร กันยายน 20, 2012 ที่ เวย์แบ็กแมชชีน
- Signal Transduction - The Virtual Library of Biochemistry, Molecular Biology and Cell Biology เก็บถาวร พฤษภาคม 7, 2018 ที่ เวย์แบ็กแมชชีน
- TRANSPATH(R) - A database about signal transduction pathways
- Science's STKE - Signal Transduction Knowledge Environment, from the journal Science, published by AAAS.
- Signal Transduction ในหอสมุดแพทยศาสตร์แห่งชาติอเมริกัน สำหรับหัวข้อเนื้อหาทางการแพทย์ (MeSH)
- UCSD-Nature Signaling Gateway เก็บถาวร กุมภาพันธ์ 12, 2013 ที่ เวย์แบ็กแมชชีน, from Nature Publishing Group
- LitInspector เก็บถาวร พฤษภาคม 11, 2019 ที่ เวย์แบ็กแมชชีน - Signal transduction pathway mining in PubMed abstracts
- Huaxian Chen, et al. A Cell Based Immunocytochemical Assay For Monitoring Kinase Signaling Pathways And Drug Efficacy (PDF) เก็บถาวร กุมภาพันธ์ 22, 2012 ที่ เวย์แบ็กแมชชีน Analytical Biochemistry 338 (2005) 136-142
- www.Redoxsignaling.com
- Signaling PAthway Database เก็บถาวร กันยายน 17, 2012 ที่ เวย์แบ็กแมชชีน - Kyushu University
- Cell cycle - Homo sapiens (human) เก็บถาวร ตุลาคม 23, 2012 ที่ เวย์แบ็กแมชชีน - KEGG PATHWAY [1]
- Pathway Interaction Database เก็บถาวร กรกฎาคม 15, 2007 ที่ เวย์แบ็กแมชชีน - National Cancer Institute
- Literature-curated human signaling network, the largest human signaling network database เก็บถาวร สิงหาคม 21, 2014 ที่ เวย์แบ็กแมชชีน

