เซอร์ปิน
ลิงก์ข้ามภาษาในบทความนี้ มีไว้ให้ผู้อ่านและผู้ร่วมแก้ไขบทความศึกษาเพิ่มเติมโดยสะดวก เนื่องจากวิกิพีเดียภาษาไทยยังไม่มีบทความดังกล่าว กระนั้น ควรรีบสร้างเป็นบทความโดยเร็วที่สุด |
| เซอร์ปิน (สารยับยั้งเอนไซม์ซีรีนโปรตีเอส) | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 ภาพแสดงโปรตีนเซอร์ปิน (สีขาว) ซึ่งมีวงศูนย์ปฏิกิริยา (reactive centre loop; สีน้ำเงิน) จับอยู่กับเอนไซม์โปรตีเอส (สีเทา). เมื่อเอนไซม์โปรตีเอสพยายามที่จะเข้าเร่งปฏิกิริยา เอนไซม์ดังกล่าวจะถูกยับยั้งการทำงานโดยเซอร์ปิน ซึ่งไม่สามารถผันกลับได้ (PDB 1K9O) | |||||||||||
| ข้อมูลจำเพาะ | |||||||||||
| สัญลักษณ์ | Serpin, SERPIN (root symbol of family) | ||||||||||
| Pfam | PF00079 | ||||||||||
| InterPro | IPR000215 | ||||||||||
| PROSITE | PDOC00256 | ||||||||||
| SCOPe | 1hle / SUPFAM | ||||||||||
| CDD | cd00172 | ||||||||||
| |||||||||||
เซอร์ปิน (อังกฤษ: Serpin) เป็นมหาวงศ์ของกลุ่มโปรตีนที่มีโครงสร้างคล้ายคลึงกัน ถูกค้นพบเป็นครั้งแรกจากการที่กลุ่มโปรตีนดังกล่าวสามารถออกฤทธิ์เป็นสารยับยั้งเอนไซม์โปรตีเอส โดยกลุ่มโปรตีนเซอร์ปินนี้พบได้ในสิ่งมีชีวิตในทุกอาณาจักร[1] ทั้งนี้ ชื่อ เซอร์ปิน นั้นถูกตั้งมาจากการที่เซอร์ปินชนิดแรกที่ถูกค้นพบออกฤทธิ์ต้านซีรีนโปรตีเอสที่มีโครงสร้างคล้ายไคโมทริปซิน (serine protease inhibitors)[2][3] โปรตีนในมหาวงศ์นี้มีกลไกการออกฤทธิ์ที่โดดเด่นซึ่งไม่ค่อยพบเห็นได้ทั่วไปนัก กล่าวคือ เมื่อเซอร์ปินเข้าจับกับเอนไซม์เป้าหมาย การทำงานของเอนไซม์นั้นจะถูกยับยั้งแบบไม่สามารถผันกลับได้ (irreversibly inhibition) โดยทำให้เกิดการเปลี่ยนโครงรูปขนาดใหญ่บนตำแหน่งกัมมันต์ของเอนไซม์ที่ถูกจับ[4][5] ซึ่งแตกต่างจากกลไกการยับยั้งแข่งขันทั่ว ๆ ไปของสารยับยั้งเอนไซม์โปรตีเอสที่มักเข้าจับและขัดขวางการเข้าถึงตำแหน่งกัมมันต์บนเอนไซม์[5][6]
การยับยั้งเอนไซม์โปรตีเอสของเซอร์ปินนั้นส่งผลต่อกระบวนการทางชีวภาพของสิ่งมีชีวิตหลายประการ ซึ่งรวมไปถึงการจับลิ่มของเลือดและการอักเสบ จึงทำให้โปรตีนเหล่านี้ได้รับความสนใจเป็นอย่างมากในการศึกษาวิจัยทางการแพทย์[7] นอกจากนี้ ด้วยการออกฤทธิ์ด้วยการเปลี่ยนโครงรูปที่เป็นเอกลักษณ์ ยังทำให้กลุ่มโปรตีนนี้เป็นที่สนใจในกลุ่มการวิจัยด้านชีววิทยาเชิงโครงสร้างและการม้วนพับโปรตีนอีกด้วย[4][5] อย่างไรก็ตาม ถึงแม้การออกฤทธิ์เพื่อให้เกิดการเปลี่ยนโครงรูปของเซอร์ปีนจะมีข้อดีหลายประการ แต่ก็มีข้อด้อยเช่นเดียวกัน โดยเซอร์ปีนอาจมีความเสี่ยงต่อการกลายพันธุ์เพิ่มขึ้น ซึ่งจะส่งผลให้เกิดโรคจากความผิดปกติของเซอร์ปิน (serpinopathies) อันเป็นผลต่อเนื่องมาจากการม้วนพับโปรตีนที่ผิดปกติ และการสร้างพอลิเมอร์สายยาวที่ไม่สามารถทำงานได้[8][9] การเกิดพอลิเมอไรเซชันของเซอร์ปิน นอกจากจะทำให้สารยับยั้งที่ออกฤทธิ์ (active inhibitor) มีปริมาณลดน้อยลงแล้ว ยังทำให้เกิดการตายของเซลล์และอวัยวะล้มเหลวจากการสะสมของพอลิเมอร์เหล่านั้นด้วย[7]
ถึงแม้เซอร์ปินส่วนใหญ่จะควบคุมกระบวนการการย่อยสลายโปรตีน (proteolytic cascades) ยังมีโปรตีนบางชนิดที่มีโครงสร้างคล้ายเซอร์ปินที่ไม่ได้ออกฤทธิ์เป็นสารยับยั้งเอนไซม์โปรตีเอส แต่ทำหน้าที่อื่นที่แตกต่างออกไป ตัอย่างเช่น เป็นโปรตีนเก็บสะสม (storage protein) เช่นที่พบในไข่ขาว เรียกว่าโอแวลบูมิน (ovalbumin), เป็นโปรตีนขนส่ง (carriage proteins) สำหรับการขนส่งฮอร์โมนบางชนิดไปยังตำแหน่งออกฤทธิ์ (thyroxine-binding globulin, cortisol-binding globulin หรือ transcortin เป็นอาทิ) และทำหน้าที่เป็นแชพเพอโรน (เช่น HSP47)[6] โดยมีการใช้คำว่า เซอร์ปิน เพื่ออธิบายถึงกลุ่มโปรตีนข้างต้นอยู่เช่นกัน แม้จะไม่ได้ทำหน้าที่ในการยับยั้งเอนไซม์โปรตีเอสก็ตาม[1]
ประวัติ[แก้]
การค้นพบกระบวนการยับยั้งเอนไซม์โปรตีเอสถูกรายงานเป็นครั้งแรกในคริสตวรรษที่ 18[10] แต่นับจากนั้นก็ไม่พบรายงานการศึกษาวิจัยที่เกี่ยวข้องกับกระบวนการดังกล่าวอีกเลย จนกระทั่งใน ปี ค.ศ. 1955 ได้มีการคัดแยกสารเซอร์ปิน 2 ชนิดได้สำเร็จ ได้แก่ แอนติทรอมบิน และแอลฟา-1 แอนตีทริปซิน[11] ทั้งนี้ การศึกษาวิจัยเกี่ยวกับเซอร์ปินในช่วงต้นจะมุ่งเน้นไปที่บทบาทของเซอร์ปินกับการเกิดโรคในมนุษย์ โดยเฉพาะภาวะพร่องแอลฟา-1 แอนตีทริปซิน (alpha1-antitrypsin (AAT) deficiency) ที่เป็นสาเหตุทำให้เกิดถุงลมโป่งพอง (emphysema) ถือเป็นหนึ่งในโรคทางพันธุกรรมที่พบได้บ่อยที่สุดในกลุ่มความผิดปกติที่เกี่ยวเนื่องกับเซอร์ปิน[8][12][13] และภาวะพร่องแอนตีทรอมบิน (antithrombin deficiency) ที่ทำให้เกิดลิ่มเลือดอุดตัน ก็ได้รับความสนใจในการศึกษาเช่นเดียวกัน[14][15]
ต่อมาในทตศวรรษที่ 1980 จากการศึกษาวิจัยทำให้ทราบได้แน่ชัดว่ากระบวนการยับยั้งเอนไซม์โปรตีเอสที่พบดังข้างต้นนั้น ส่วนหนึ่งเป็นผลมาจากโปรตีนที่เกี่ยวเนื่องกันในมหาวงศ์หนึ่ง ซึ่งมีทั้งชนิดที่ออกฤทธิ์เป็นสารยับยั้งเอนไซม์โปรตีเอส (เช่น แอลฟา-1 แอนตีทริปซิน) และชนิดที่ไม่มีฤทธิ์ยับยั้งเอนไซม์ (เช่น โอแวลบูมิน)[16] จึงได้มีการตั้งชื่อกลุ่มโปรตีนนี้ว่า เซอร์ปิน โดยมีที่มาจากกลไกการออกฤทธิ์ที่พบได้บ่อยที่สุดของโปรตีนในมหาวงศ์นี้ (serine protease inhibitors).[16] ในช่วงเวลาใกล้เคียงกัน ได้มีการวิเคราะห์โครงสร้างของเซอร์ปินชนิดแรกได้สำเร็จ (ครั้งแรกในรูปแบบอิสระ และครั้งที่ 2 ในรูปแบบที่เกิดการเปลี่ยนโครงรูปกับเอนไซม์)[17][18] โดยโครงสร้างดังกล่าวแสดงให้เห็นว่า กลไกการออกฤทธิ์ยับยั้งการทำงานของเอนไซม์ของเซอร์ปินั้นมีส่วนเกี่ยวข้องกับการเปลี่ยนโครงรูปที่ผิดปกติของตำแหน่งกัมมันต์ การค้นพบนี้ส่งผลให้เกิดความสนใจในการศึกษาวิจัยเกี่ยวกับโครงสร้างของเซอร์ปินเพิ่มมากขึ้นในภายหลัง[5][18]
ในปัจจุบัน มีการค้นพบเซอร์ปินแล้วมากกว่า 1,000 ชนิด ประกอบไปด้วย พบในมนุษย์ 36 ชนิด และที่เหลือพบในสิ่งมีชีวิตอื่นในอาณาจักรต่าง ๆ ทั้งสัตว์ พืช เห็ดรา แบคทีเรีย อาร์เคีย และไวรัสบางชนิด[19][20][21] ในคริสต์ทศวรรษ 2000 มีการนำระบบการตั้งชื่อมาใช้เพื่อจัดหมวดหมู่โปรตีนชนิดต่าง ๆ ในมหาวงศ์เซอร์ปิน โดยอิงตามความสัมพันธ์ด้านวิวัฒนาการของเซอร์ปินแต่ละชนิด[1] จึงถือได้ว่าเซอร์ปินเป็นกลุ่มโปรตีนที่ใหญ่และมีความหลากหลายที่สุดในบรรดาสารยับยั้งโปรตีเอส[22]
วิวัฒนาการ[แก้]
เซอร์ปินเป็นมหาวงศ์ของโปรตีนที่พบได้ทั่วไปและจัดเป็นกลุ่มโปรตีนยับยั้งโปรตีเอสที่ใหญ่ที่สุด[1][22] แรกเริ่มเชื่อกันว่าสามารถพบเซอร์ปินได้ในสิ่งมีชีวิตประเภทยูแคริโอตเท่านั้น แต่หลังจากนั้นมาก็เริ่มมีการค้นพบเซอร์ปินในสิ่งมีชีวิตอื่นที่ไม่ใช่ยูแคริโอต อาทิ แบคทีเรีย อาร์เคีย และไวรัสบางชนิด[19][20][23] แต่ก็ยังไม่สามารถทราบได้แน่ชัดว่า ยีนที่ทำหน้าที่สร้างเซอร์ปินที่พบในโพรแคริโอตนั้น เป็นยีนที่ได้รับการถ่ายทอดโดยรุ่นสู่รุ่นจากเซลล์โพรแคริโอตโบราณ หรือเป็นยีนที่ได้รับผ่านการถ่ายทอดยีนในแนวราบจากยูแคริโอต ทั้งนี้เซอร์ปินภายในเซลล์ส่วนใหญ่ (intracellular serpins) มีที่มาจากวงศ์วานวิวัฒนาการเคลดเดียวกัน ไม่ว่าจะเป็นชนิดที่พบในสัตว์หรือพืชก็ตาม จึงบ่งชี้ได้ว่า ทั้งเซอร์ปินภายในเซลล์และเซอร์ปีนภายนอกเซลล์ (extracellular serpins) นั้น อาจมีความหลากหลายมาก่อนที่จะเกิดการแยกเคลดวงศ์วานวิวัฒนาการของพืชและสัตว์[24] ยกเว้น ฮีตช็อกโปรตีน 47 ภายในเซลล์ (intercallular heat shock protein; HSP47) ซึ่งเป็นเซอร์ปินประเภทแชพเพอโรนที่มีความสำคัญต่อการม้วนพับตัวของคอลลาเจนและการเกิดห่วงโซ่ปฏิกิริยาระหว่างซิสเทอร์นี (cisternae) ของกอลไจแอปพาราตัสกับร่างแหเอนโดพลาซึม[25]
การยับยั้งโปรตีเอสของโปรตีนเซอร์ปินนั้นถือได้ว่าเป็นกลไกที่มีมาตั้งแต่แรกเริ่ม ส่วนเซอร์ปินที่ไม่มีผลยับยั้งโปรตีเอสนั้นเป็นผลมาจากการวิวัฒนาการของโครงสร้างเพื่อพัฒนาหน้าที่ใหม่ (neofunctionalization) นอกจากนี้ เซอร์ปินที่ทำหน้าที่เป็นโปรตีนขนส่งบางชนิด อาจเกิดการเปลี่ยนโครงรูปจากไอโซเมอร์ชนิด S เป็นชนิด R เพื่อให้มีความจำเพาะในการเข้าจับกับตำแหน่งเป้าหมายมากยิ่งขึ้น[26]
หน้าที่[แก้]

โดยส่วนมากแล้ว โปรตีนในมหาวงศ์เซอร์ปินจะออกฤทธิ์ต้านซีรีนโปรตีเอสที่มีตำแหน่งออกฤทธิ์ภายนอกเซลล์และมีโครงสร้างคล้ายไคโมทริปซิน (chymotrypsin-like serine proteases) โดยโปรตีเอสเหล่านี้จะเข้าจับกับตำแหน่งเป้าหมายโดยใช้บซีรีนบริเวณ catalytic triad ของตำแหน่งกัมมันต์เข้าทำปฏิกิริยา ตัวอย่างโปรตีเอสเหล่านี้ได้แก่ ทรอมบิน ทริปซิน และ นิวโทรฟิลอีลาสเทส[27] โดยเซอร์ปินจะออกฤทธิ์เป็นตัวยับยั้งสังหารแบบไม่สามารถผันกลับได้ (irreversible, suicide inhibitors) ต่อโปรตีเอสเหล่านั้น โดยการดักจับตัวกลางของกลไกการเร่งปฏิกิริยาของโปรตีเอส[28]
อย่างไรก็ตาม ยังมีเซอร์ปินบางชนิดที่มีคุณสมบัติยับยั้งการทำงานของโปรตีเอสกลุ่มอื่น ๆ ส่วนใหญ่มักเป็นเอนไซม์ในกลุ่มซิสตีอีนโปรตีเอส จึงเรียกเซอร์ปินกลุ่มนี้ว่าเป็น "สารยับยั้งข้ามกลุ่ม" (cross-class inhibitors) โดยเอนไซม์ซิสตีอีนโปรตีเอสนั้นมีซิสตีอีนเป็นองค์ประกอบสำคัญในนิวคลีโอไฟล์ซึ่งต่างจากซีรีนโปรตีเอสที่มีนิวคลีโอไฟล์เป็นซีรีนเป็นตำแหน่งกัมมันต์[29] ถึงกระนั้น คุณสมบัติทางเคมีของเอนไซม์ทั้งสองก็ไม่ได้มีความแตกต่างกัน และกระบวนการการยับยั้งการทำงานของเอนไซม์โปรตีเอสทั้งสองกลุ่มโดยไซรีนนั้นก็ล้วนเกิดผ่านกลไกเดียวกัน[30] ตัวอย่าง เซอร์ปินที่จัดเป็นสารยับยั้งข้ามกลุ่ม เช่น เซอร์ปิน บี4 ซึ่งเป็นแอนติเจนต่อมะเร็งผิวหนังสะแควมัสเซลล์คาร์ซิโนมา (squamous cell carcinoma antigen 1; SCCA-1) และ เซอร์ปินชนิด myeloid and erythroid nuclear termination stage-specific protein (MENT) ในสัตว์ปีก โดยเซอร์ปินทั้ง 2 ชนิดที่กล่าวถึงดังข้างต้นจะออกฤทธิ์ยับยั้งการทำงานของซิสตีอีนโปรตีเอสที่มีโครงสร้างคล้ายพาเพอิน (papain-like cysteine protease)[31][32][33]
ฤทธิ์ทางชีววิทยา[แก้]
ฤทธิ์ต้านโปรตีเอส[แก้]
เซอร์ปินที่พบในมนุษย์ประมาณ 2 ใน 3 นั้นมีเป้าหมายการออกฤทธิ์บริเวณภายนอกเซลล์ ซึ่งมักจะเข้ายับยั้งการทำงานของโปรตีเอสในกระแสเลือดเพื่อควบคุมสมดุลการทำงานของเอนไซม์เหล่านั้น ตัวอย่างเช่น แอนติทรอมบินที่ออกต้านการทำงานของทรอมบินในกระบวนการการจับลิ่มของเลือด; แอนติทริปซิน, แอนตีไคโมทริปซิน และตัวยับยั้ง C1 ที่ออกฤทธิ์ในกระบวนการอักเสบและการตอบสนองของภูมิคุ้มกัน รวมไปถึง PAI-1 ในกระบวนการการซ่อมแซมเนื้อเยื่อที่เสียหาย[6] นอกเหนือจากการยับยั้งวงจรการถ่ายโอนสัญญาณของโปรตีเอสแล้ว เซอร์ปินยังส่งผลต่อการพัฒนาของเนื่อเยื่อหรืออวัยวะเป้าหมายได้ด้วย[34][35] ตารางแสดงเซอร์ปินที่พบในมนุษย์ (ด้านล่าง) แสดงให้เห็นถึงหน้าที่ของเซอร์ปินชนิดต่าง ๆ รวมไปถึงความผิดปกติที่เกิดขึ้นจากการขาดเซอร์ปินชนิดนั้น ๆ
ส่วนบทบาทของเซอร์ปินแต่ละชนิดที่ออกฤทธิ์ยับยั้งโปรตีเอสภายในเซลล์นั้นยังไม่สามารถระบุแยกได้แน่ชัด เนื่องจากมีการทำงานที่ซ้อนทับกันของเซอร์ปินหลายชนิดในกลไกหนึ่ง ๆ นอกจากนี้ เซอร์ปินหลายชนิดที่พบในมนุษย์นั้นยังไม่สามารถหาเซอร์ปินเทียบเคียงที่มีบทบาทหน้าที่สมมูลย์กันในสัตว์ทดลองได้ อย่างไรก็ตาม คาดว่าหน้าที่สำคัญของเซอร์ปินที่ออกฤทธิ์ภายในเซลล์นั้น อาจช่วยป้องกันการเกิดกิจกรรมที่ไม่เหมาะสมของโปรตีเอสภายในเซลล์[36] ตัวอย่างเช่น เซอร์ปินภายในเซลล์ของมนุษย์ที่เป็นที่คุ้นเคยกันมากที่สุดอย่าง เซอร์ปิน บี9 โดยเซอร์ปินชนิดนี้จะออกฤทธิ์ต้านการทำงานของแกรนูลที่บรรจุแกรนไซม์ บี ซึ่งเป็นโปรตีเอสที่เป็นพิษต่อเซลล์ ทำให้ช่วยป้องกันการปล่อยแกรนไซม์บีโดยไม่ได้ตั้งใจและลดการกระตุ้นการเกิดอะพอพโทซิสของเซลล์ก่อนเวลาอันควรหรือโดยไม่พึงประสงค์[37]
นอกจากนี้ยังพบว่า ไวรัสบางชนิดมีการใช้เซอร์ปินเพื่อขัดขวางการทำงานของโปรตีเอสในโฮสต์ เช่น ไวรัสฝีดาษวัว (cowpox) ซึ่งจะสร้าง CrmA (cytokine response modifier A) ขึ้นมาเมื่อเข้าสู่เซลล์โฮสต์ ทั้งนี้เพื่อป้องกันไม่ให้เกิดการอักเสบและอะพอพโทซิสของเซลล์ที่ติดเชื้อ โดย CrmA จะทำให้เซลล์เป้าหมายมีการติดเชื้อเพิ่มมากขึ้นได้จากการกดกระบวนการอักเสบของเซลล์โฮสต์ด้วยการยับยั้งการทำงานของซิสตีอีนโปรตีเอสที่ชื่อแคสเปส 1 ส่งผลให้ไม่เกิดการเปลี่ยนโปรอินเตอร์ลิวคิน 1 และโปรอินเตอร์ลิวคิน 18 เป็นอินเตอร์ลิวคิน 1 (Interleukin 1; IL-1) และ อินเตอร์ลิวคิน 18 (Interleukin 18; IL-18) ตามลำดับ ซึ่งทั้งสารทั้ง 2 ชนิดนี้จัดเป็นไซโตไคน์ที่จำเป็นต่อการเกิดไพรอพโทซิสของเซลล์[38] ส่วนในยูแคริโอตนั้น พบว่าเซอร์ปินของพืชสามารถยับยั้งได้ทั้งกลุ่มเอนไซม์เมตาแคสเปส[39] และซิสตีอีนโปรตีเอสที่มีโครงสร้างคล้ายพาเพอิน[40]
บทบาทอื่น[แก้]
เซอร์ปีนภายนอกเซลล์ที่ไม่มีผลยับยั้งโปรตีเอสนั้นจะทำหน้าที่อื่นที่หลากหลายแตกต่างอันออกไป อาทิ ไทโรซีน-บายดิ้ง กลอบูลิน และทรานส์คอร์ติน ซึ่งทำหน้าที่ขนส่งฮอร์โมนไทรอกซีน และคอร์ติซอล ตามลำดับ[41][26]; โอแวลบูมิน ซึ่งเป็นโปรตีนที่พบมากที่สุดในไข่ขาว ก็จัดเป็นเซอร์ปีนอีกชนิดหนึ่ง ถึงแม้จะไม่ทราบบทบาทหน้าที่ที่แน่ชัดเท่าใดนัก แต่คาดว่าโอแวลบูมินนี้อาจทำหน้าที่เป็นโปรตีนเก็บสะสมสำหรับการพัฒนาการก่อนการเกิดของตัวอ่อน (Prenatal development)[42] รวมไปถึงฮีตช็อกโปรตีน 47 ซึ่งจัดเป็นเซอร์ปินประเภทแชพเพอโรนที่มีความสำคัญต่อการม้วนพับตัวของคอลลาเจน และช่วยให้เกลียวสามสายของคอลลาเจนมีความเสถียรระหว่างกระบวนการสังเคราะห์คอลลาเจนในร่างแหเอนโดพลาซึม[25]
อย่างไรก็ตาม ยังมีเซอร์ปินบางชนิดที่นอกจากจะออกฤทธิ์ต้านโปรตีเอสแล้ว ยังมีหน้าที่อื่นที่ไม่เป็นผลเกี่ยวเนื่องมาจากการยับยั้งโปรตีเอส ตัวอย่างเช่น MENT ซึ่งเป็นเซอร์ปินที่พบในนก นอกจากจะออกฤทธิ์ต้านซิสตีอีนโปรตีเอสภายในเซลล์แล้ว ยังเป็นสารที่มีส่วนช่วยในการดัดแปรโครมาติน (chromatin remodeling) ภายในเซลล์เม็ดเลือดแดงของนกอีกด้วย[32][43]
โครงสร้าง[แก้]
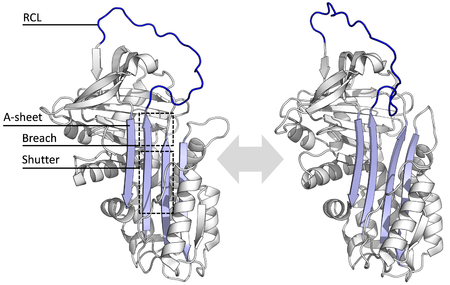
เซอร์ปินทุกชนิดจะมีโครงสร้างพื้นฐานที่เหมือนกัน ถึงแม้จะมีหน้าที่ที่หลากหลายแตกต่างกันก็ตาม โครงสร้างดังกล่าวจะประกอบไปด้วยแผ่นบีตา 3 แผ่น (ชื่อว่าแผ่น A, B และ C) และเกลียวแอลฟาจำนวน 8–9 เกลียว (ชื่อว่าเกลียว hA–hI)[17][18] โดยส่วนที่มีความสำคัญอย่างมีนัยยะต่อการทำงานของเซอร์ปินได้แก่ แผ่น A-sheet และวงศูนย์ปฏิกิริยา (reactive centre loop; RCL) ซึ่งแผ่น A-sheet นี้จะประกอบไปด้วยสายบีตาจำนวน 2 สายเรียงตัวในแนวขนานกัน พื้นที่ที่อยู่ระหว่างสายบีตาทั้ง 2 สายนี้ เรียกว่า 'ซัตเตอร์' (shutter) และส่วนที่ด้านบนขึ้นไปเรียกว่า 'บรีช' (breach) โดยโครงสร้างที่เป็นวงศูนย์ปฏิกิริยาจะเป็นส่วนที่เริ่มเข้าจับกับโปรตีเอสเป้าหมายเพื่อยับยั้งการทำงานของโปรตีเอสนั้น ๆ จากโครงสร้างของเซอร์ปินที่ได้จากการจำลองพบว่าวงศูนย์ปฏิกิริยาของเซอร์ปีนจะอยู่ทั้งในระยะเครียดเต็มที่ (fully stressed) หรือในระยะคลายบางส่วน (partially relaxed) ซึ่งบางส่วนของวงจะม้วนพับเข้าไปในเกลียว A-sheet คาดการณ์กันว่าสมดุลไดนามิก (dynamic equilibrium) ของเซอร์ปินนั้นจะอยู่ระหว่าง 2 ระยะนี้[5] นอกจากนี้วงศูนย์ปฏิกิริยาดังกล่าวยังสามารถเกิดปฏิกิริยาแบบชั่วคราวกับโครงสร้างส่วนที่เหลือของเซอร์ปินได้ เนื่องจากโครงสร้างส่วนนี้มีความยืดหยุ่นสูงและสัมผัสอยู่กับสารละลายอยู่ตลอดเวลา[5]
ในปัจจุบันมีการค้นพบโครงสร้างของเซอร์ปินครอบคลุมหลากหลายโครงรูป ซึ่งถือเป็นส่วนสำคัญในการศึกษาเพื่อทำความเข้าในในกลไกการออกฤทธิ์ที่สลับซับซ้อนของโปรตีนกลุ่มนี้ ดังนั้น การศึกษาชีววิทยาโครงสร้างจึงได้เข้ามามีบทบาทสำคัญในการทำความเข้าใจเกี่ยวกับการทำงานและฤทธิ์ทางชีววิทยาของเซอร์ปิน[5]
การกระจาย[แก้]
สัตว์[แก้]
มนุษย์[แก้]
จีโนมของมนุษย์ที่สามารถถอดรหัสเพื่อสร้างเซอร์ปินได้นั้นมีทั้งหมด 16 เคลด กำหนดให้มีชื่อตั้งแต่ serpinA ถึง serpinP โดยทั้งหมดนี้สามารถถอดรหัสเพื่อสร้างเซอร์ปินชนิดยับยั้งและชนิดไม่ยับยั้งได้ 29 และ 7 ชนิด ตามลำดับ[6][46] ระบบการตั้งชื่อเซอร์พินของมนุษย์นั้นขึ้นอยู่กับการวิเคราะห์ทางวิวัฒนาการของเซอร์ปิน ซึ่งตั้งแต่ปี ค.ศ. 2001 เป็นต้นมา มีการค้นพบเซอร์ปินในมนุษย์แล้วประมาณ 500 ชนิด โดยการกำหนดชื่อจะใช้รหัส serpinXY โดยที่ X คือ เคลดของโปรตีนและ Y จำนวนของโปรตีนภายในเคลดนั้น[1][19][46] ซึ่งบทบาทหน้าที่ของเซอร์ปินแต่ละชนิดที่ค้นพบในมนุษย์ได้วิเคราะห์ได้จากการศึกษาทางชีวเคมี, ความผิดปกติทางพันธุกรรมของมนุษย์ และจากการศึกษาในหนูน็อกเอาต์ (knockout mouse)[46]
| ตารางแสดงเซอร์ปินที่พบในมนุษย์ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
เซอร์ปินพิเศษของสัตว์เลี้ยงลูกด้วยนม[แก้]
เซอร์ปินหลายชนิดที่พบในสัตว์เลี้ยงลูกด้วยนมพบว่าไม่สามารถเทียบเคียงหาเซอร์ปีนที่มีหน้าที่และฤทธิ์ทางชีววิทยาที่ทัดเทียมกันได้ ตัวอย่างเช่นเซอร์ปินที่พบในสัตว์ฟันแทะหลายชนิด (โดยเฉพาะอย่างยิ่งเซอร์ปินชนิดออกฤทธิ์ภายในเซลล์ของสัตว์ในวงศ์ย่อยหนู) รวมไปถึงยูเทอรีนเซอร์ปินซึ่งจัดหนึ่งในสมาชิกของเคลด A (SERPINA) โดยเซอร์ปินชนิดนี้จะถูกถอดรหัสยีน SERPINA14 และถูกสร้างขึ้นโดยเซลล์เยื่อบุโพรงมดลูกของสัตว์เลี้ยงลูกด้วยนมอันดับสัตว์กีบคู่ภายใต้อิทธิพลของโพรเจสเทอโรนและเอสโตรเจน[133] ซึ่งเซอร์ปินเหล่านี้อาจไม่ได้มีหน้าที่ในการต้านโปรตีเอส และอาจจะมีบทบาทในช่วงการตั้งครรภ์ ทั้งนี้เพื่อยับยั้งการตอบสนองของระบบภูมิคุ้มกันมารดาไม่ให้ต่อต้านเนื้อเยื่อต่าง ๆ ที่ถูกสร้างขึ้นระหว่างการตั้งครรภ์ (conceptus) หรืออาจมีส่วนในการช่วยขนส่งสารต่าง ๆ ทางรก[134]
แมลง[แก้]
ในจีโนมของแมลงวันทองมียีนมากถึง 29 โลคัสที่ทำหน้าที่ในการสร้างเซอร์ปิน ผลการวิเคราะห์ลำดับกรดอะมิโนพบว่า เซอร์ปิน 14 ชนิดถูกควบคุมโดยเคลด Q และ 3 ชนิดโดยเคลด K ส่วนเซอร์ปินที่เหลืออีก 12 ชนิด จัดเป็นเซอร์ปินกำพร้าที่ไม่จำเพาะต่อเคลดใด ๆ[135] ระบบการจำแนกประเภทเคลดที่ใช้กับมนุษย์นั้นไม่สามารถใช้กับกรณีนี้ได้ดีเท่าใดนัก จึงได้นำเอาระบบการตั้งชื่อมาประยุกต์ใช้แทน โดยอิงตามตำแหน่งของยีนบนโครโมโซมที่ควบคุมการสร้างเซอร์ปินนั้น ๆ แทน ซึ่งพบว่าเซอร์ปิน 13 ชนิดที่แยกได้นั้นถูกควบคุมโดยยีนที่อยู่คนละตำแหน่งกัน (รวมถึง Serpin-27A ที่แสดงรายละเอียดด้านล่าง) และที่เหลืออีก 16 ชนิดถูกควบคุมโดยกลุ่มยีน 5 ยีนที่ตำแหน่ง 28D (2 เซอร์ปิน), 42D (5 เซอร์ปิน), 43A (4 เซอร์ปิน), 77B (3 เซอร์ปิน) และ 88E (2 เซอร์ปิน)[135][136][137]
การศึกษาเกี่ยวกับเซอร์ปินของแมลงวันทองพบว่า Serpin-27A นั้นออกฤทธิ์ต้านอีสเตอร์โปรตีเอส (โปรตีเอสลำดับสุดท้ายในวัฎจักร Nudel, Gastrulation Defective, Snake and Easter) ที่ควบคุมการสร้างเนื้อเยื่อในอวัยวะส่วนแกนหลังและหน้าท้อง อีกทั้งยังมีส่วนช่วยในการทำงาน Spätzle (ลิแกนด์ประเภทไคโตไซน์ชนิดหนึ่ง) เพื่อกระตุ้นตัวรับ Toll-like receptor ในระบบภูมิคุ้มกันเพื่อให้ทนต่อแบคทีเรีย รา และไวรัส นอกจากนี้ การส่งสัญญาณ toll ที่เป็นผลจากการกระตุ้นตัวรับ Toll-like receptor ยังมีบทบาทสำคัญในการพัฒนาระบบภูมิคุ้มกันโดยกำเนิดของแมลงต่าง ๆ อีกด้วย[35][138][139]
ในกระดิ่งเงินกระดิ่งทองมีโปรตีน SPN93 ซึ่งประกอบไปด้วยเซอร์ปิน 2 หน่วยย่อย ทำหน้าที่ควบคุมวัฎจักรการสลายโปรตีนผ่านการถ่ายทอดสัญญาณทอล (Toll signaling cascade)[140]
หนอนตัวกลม[แก้]
จีโนมของ C. elegans ซึ่งเป็นสัตว์จำพวกหนอนตัวกลม สามารถถอดรหัสสร้างเซอร์ปินได้ 9 ชนิด โดยเซอร์ปินทั้งหมดนี้ไม่มีเพปไทด์ส่งสัญญาณและดูคล้ายจะเป็นเซอร์ปินประเภทภายในเซลล์[141] อย่างไรก็ตาม มีเพียงเซอร์ปินเพียง 5 ชนิดเท่านั้นที่ดูเหมือนว่าจะสามารถออกฤทธิ์ยับยั้งการทำงานโปรตีเอสได้[141] หนึ่งในนั้นก็คือ SRP-6 ที่ทำหน้าที่ป้องกันและต้านทานการแตกของไลโซโซมที่สัมพันธ์กับคาลเพนและมีภาวะเครียดเป็นปัจจัยเหนี่ยวนำ (stress-induced calpain-associated lysosomal disruption) นอกจากนี้ SRP-6 ยังช่วยยับยั้งการทำงานของซิสตีอีนโปรตีเอสที่ถูกปล่อยออกมาหลังการแตกของไลโซโซม ด้วยเหตุนี้จึงทำให้ C. elegans ที่ขาด SRP-6 นั้น มีความไวต่อภาวะเครียดมากกว่าปกติ และพบว่าหนอนที่ถูกหยุดการทำงานของยีนที่ควบคุมการสร้าง SRP-6 (knockout worms) จะตายเกือบทันทีเมื่อถูกนำไปวางในน้ำ (ผลจาก hypo-osmotic stress lethal phenotype; Osl) ส่วนสาเหตุอื่น ๆ ที่ทำให้การแสดงออกของ SRP-6 ลดน้อยลงจนนำไปสู่การตายของเซลล์ เนื้อเยื่อหรือทั้งระบบ ได้แก่ ภาวะฉุกเฉินจากความร้อน ความเครียดออกซิเดชัน ภาวะพร่องออกซิเจน และ MET-4 จึงสรุปได้ว่า SRP-6 และไลโซโซมมีบทบาทสำคัญเป็นอย่างมากในการตอบสนองภาวะเครียดและการควบคุมตายของเซลล์ในหนอนตัวกลม[142]
พืช[แก้]
เซอร์ปินที่ถูกค้นพบเป็นกลุ่มแรก ๆ นั้นเป็นเซอร์ปินที่พบในพืช โดยเซอร์ปิน Z ที่มีอยู่มากในเมล็ดข้าวบาร์เลย์และเป็นหนึ่งในส่วนประกอบโปรตีนที่สำคัญที่พบในเบียร์[143] รวมไปถึงจีโนมของพืชต้นแบบอย่างเธลเครสที่มียีนที่คล้ายเซอร์ปินอยู่ 18 ยีน ถึงแม้ว่าจะมีเพียง 8 ยีนเท่านั้นที่มีลำดับนิวคลีโอไทด์ของเซอร์ปินยาวเต็มที่
การทดสอบในหลอดทดลอง (in vitro) พบว่า เซอร์ปินจากพืชบางชนิดออกฤทธิ์ยับยั้งซีรีนโปรตีเอสที่มีโครงสร้างคล้ายไคโมทริปซิน (chymotrypsin-like serine proteases) ของสัตว์เลี้ยงลูกด้วยนมได้เป็นอย่างดี ตัวอย่างการศึกษาที่อธิบายปรากฏการณ์ดังกล่าวได้ดีที่สุดนั้นเป็นการศึกษาการทำงานของเซอร์ปิน Zx (BSZx) ในข้าวบาร์เลย์ซึ่งพบว่ามีความสามารถในการต้านทริปซินและไคโมทริปซิน รวมไปถึงแฟกเตอร์ต่าง ๆ ที่เกี่ยวข้องกับการจับลิ่มของเลือดในมนุษย์หลายชนิด[144] อย่างไรก็ดี เอนไซม์ที่มีคุณสมบัติใกล้เคียงซีรีนโปรตีเอสที่มีโครงสร้างคล้ายไคโมทริปซินนั้นไม่ปรากฏว่ามีอยู่ในพืช นอกจากนี้ยังพบว่าวงศูนย์ปฏิกิริยาของเซอร์ปินหลายชนิดที่พบในข้าวสาลีและข้าวไรย์มีการเรียงลำดับ PolyQ ต่อเนื่องซ้ำ ๆ คล้ายกับที่พบในโพรลามีนซึ่งเป็นโปรตีนเก็บสะสมภายในเอนโดสเปิร์มของเมล็ดพืช[145][146] จึงอาจพอสรุปได้ว่า เซอร์ปินที่พบในพืชเหล่านี้อาจทำหน้าที่ในการยับยั้งโปรตีเอสจากแมลงหรือจุลชีพที่มีคุณสมบัติในการย่อยโปรตีนเก็บสะสมเมล็ด โดยมีการศึกษาหนึ่งที่ให้ข้อสรุปสนับสนุนสมมติฐานข้างต้น กล่าวคือ ถึงแม้จะพบความสัมพันธ์แบบแปรผกผันระหว่างการแสดงออกของ CmPS-1 ซึ่งเป็นเซอร์ปินที่พบในสารละลายสารอาหาร (phloem sap) ของต้นฟักทองและแตงกวา กับการอยู่รอดและการขยายพันธุ์ของเพลี้ยอ่อน แต่การศึกษาในหลอดทดลองกลับพบว่า การให้สารละลาย CmPS-1 ความบริสุทธิ์สูงที่สกัดจากสารละลายสารอาหารข้างต้น กลับไม่มีผลต่อการรอดชีวิตของกลุ่มตัวอย่าง[147][148][149]
นอกจากนี้ ยังมีการค้นพบหน้าที่อื่นหรือโปรตีเอสเป้าหมายอื่นของเซอร์ปินพืชอีกหลายชนิด อาทิ เซอร์ปิน AtSerpin1 (At1g47710; 3LE2) ที่พบในพืชสกุลอะราบิดอบซิส ที่ทำหน้าที่เป็นสารตัวกลางในการควบคุมการเกิดไม่ให้เกิดการทำงานของโปรแกรมการตายของเซลล์ที่มากเกินไป โดยมีเป้าหมายการออกฤทธิ์ที่ซิสเตอีนโปรตีเอสชื่อว่า 'Responsive to Desiccation-21' (RD21)[40][150] และการศึกษาในหลอดทดลองยังพบว่า AtSerpin1 สามารถยับยั้งเอนไซม์โปรตีเอสที่คล้ายเมตาแคสเปสได้อีกด้วย[39] ทั้งนี้ ยังมีเซอร์ปินอีก 2 ชนิดที่พบในพืชดังกล่าว ได้แก่ AtSRP2 (At2g14540) และ AtSRP3 (At1g64030) ซึ่งจะทำงานตอบสนองต่อการได้รับความเสียหายของดีเอ็นเอ[151]
เห็ดรา[แก้]
ณ ปัจจุบัน มีการค้นพบเซอร์ปินในสิ่งมีชีวิตจำพวกเห็ดราเพียง 1 ชนิด คือ เซลปิน (celpin) จากรา Piromyces spp. สายพันธุ์ E2 ซึ่งเป็นราที่ไม่ต้องการออกซิเจน (anaerobic fungi) ในจีนัส Piromyces อาศัยอยู่ในทางเดินอาหารของสัตว์เคี้ยวเอื้อง โดยราชนิดนี้มีส่วนช่วยสำคัญในการย่อยสลายชิ้นส่วนของพืชที่สัตว์เหล่านี้กินเข้าไป ทั้งนี้ ปลายซี (C-terminus) ของเซลปินประกอบไปด้วยกรดอะมิโน 380 หน่วย ซึ่งเป็นส่วนที่แสดงคุณสมบัติเป็นเซอร์ปิน ส่วนปลายเอ็น (N-terminus) จะประกอบไปด้วยดอคเกอรินจำนวน 2 โมเลกุล ซึ่งเป็นสารที่มีส่วนช่วยในการสร้างเซลลูโลโซมของรา เพื่อใช้เป็นแหล่งสะสมเอนไซม์ที่จำเป็นในการย่อยชิ้นส่วนพืช จึงมีความเป็นไปได้ว่า เซลปินที่พบในราสายพันธุ์นี้อาจมีหน้าที่ป้องกันไม่ให้เซลลูโลโซมถูกทำลายด้วยโปรตีเอสจากพืช[21] นอกจากนี้ยังมีรายงานการค้นพบเซอร์ปินของแบคทีเรียที่ทำหน้าที่คล้ายคลึงกันกับเซลปินอีกด้วย[152]
โพรคาริโอต[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ไวรัส[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การเปลี่ยนโครงรูปและกลไกการยับยั้ง[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การเสื่อมสลาย[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
โรคจากความผิดปกของเซอร์ปิน[แก้]
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ดูเพิ่ม[แก้]
อ้างอิง[แก้]
- ↑ 1.0 1.1 1.2 1.3 1.4 Silverman GA, Bird PI, Carrell RW, Church FC, Coughlin PB, Gettins PG, Irving JA, Lomas DA, Luke CJ, Moyer RW, Pemberton PA, Remold-O'Donnell E, Salvesen GS, Travis J, Whisstock JC (September 2001). "The serpins are an expanding superfamily of structurally similar but functionally diverse proteins. Evolution, mechanism of inhibition, novel functions, and a revised nomenclature". The Journal of Biological Chemistry. 276 (36): 33293–6. doi:10.1074/jbc.R100016200. PMID 11435447.
- ↑ Silverman GA, Whisstock JC, Bottomley SP, Huntington JA, Kaiserman D, Luke CJ, Pak SC, Reichhart JM, Bird PI (August 2010). "Serpins flex their muscle: I. Putting the clamps on proteolysis in diverse biological systems". The Journal of Biological Chemistry. 285 (32): 24299–305. doi:10.1074/jbc.R110.112771. PMC 2915665. PMID 20498369.
- ↑ Whisstock JC, Silverman GA, Bird PI, Bottomley SP, Kaiserman D, Luke CJ, Pak SC, Reichhart JM, Huntington JA (August 2010). "Serpins flex their muscle: II. Structural insights into target peptidase recognition, polymerization, and transport functions". The Journal of Biological Chemistry. 285 (32): 24307–12. doi:10.1074/jbc.R110.141408. PMC 2915666. PMID 20498368.
- ↑ 4.0 4.1 Gettins PG (December 2002). "Serpin structure, mechanism, and function". Chemical Reviews. 102 (12): 4751–804. doi:10.1021/cr010170. PMID 12475206.
- ↑ 5.0 5.1 5.2 5.3 5.4 5.5 5.6 Whisstock JC, Bottomley SP (December 2006). "Molecular gymnastics: serpin structure, folding and misfolding". Current Opinion in Structural Biology. 16 (6): 761–8. doi:10.1016/j.sbi.2006.10.005. PMID 17079131.
- ↑ 6.0 6.1 6.2 6.3 6.4 6.5 Law RH, Zhang Q, McGowan S, Buckle AM, Silverman GA, Wong W, Rosado CJ, Langendorf CG, Pike RN, Bird PI, Whisstock JC (2006). "An overview of the serpin superfamily". Genome Biology. 7 (5): 216. doi:10.1186/gb-2006-7-5-216. PMC 1779521. PMID 16737556.
- ↑ 7.0 7.1 Stein PE, Carrell RW (February 1995). "What do dysfunctional serpins tell us about molecular mobility and disease?". Nature Structural Biology. 2 (2): 96–113. doi:10.1038/nsb0295-96. PMID 7749926. S2CID 21223825.
- ↑ 8.0 8.1 8.2 Janciauskiene SM, Bals R, Koczulla R, Vogelmeier C, Köhnlein T, Welte T (August 2011). "The discovery of α1-antitrypsin and its role in health and disease". Respiratory Medicine. 105 (8): 1129–39. doi:10.1016/j.rmed.2011.02.002. PMID 21367592.
- ↑ Carrell RW, Lomas DA (July 1997). "Conformational disease". Lancet. 350 (9071): 134–8. doi:10.1016/S0140-6736(97)02073-4. PMID 9228977. S2CID 39124185.
- ↑ Fermi C, Personsi L (1984). "Untersuchungen uber die enzyme, Vergleichende Studie" [Studies on the enzyme, Comparative study]. Z Hyg Infektionskr (ภาษาเยอรมัน) (18): 83–89.
- ↑ Schultz H, Guilder I, Heide K, Schoenenberger M, Schwick G (1955). "Zur Kenntnis der alpha-globulin des menschlichen normal serums" [For knowledge of the alpha - globulin of human normal serums]. Zeitschrift für Naturforschung B (ภาษาเยอรมัน). 10 (8): 463. doi:10.1515/znb-1955-0810. S2CID 95960716.
- ↑ Laurell CB, Eriksson S (2013). "The electrophoretic α1-globulin pattern of serum in α1-antitrypsin deficiency. 1963". COPD. 10 Suppl 1: 3–8. doi:10.3109/15412555.2013.771956. PMID 23527532.
- ↑ de Serres FJ (1 November 2002). "Worldwide Racial and Ethnic Distribution of α-Antitrypsin Deficiency". Chest. 122 (5): 1818–1829. doi:10.1378/chest.122.5.1818. PMID 12426287.
- ↑ Egeberg O (June 1965). "Inherited antithrombin deficiency causing thrombophilia". Thrombosis et Diathesis Haemorrhagica. 13 (2): 516–30. doi:10.1055/s-0038-1656297. PMID 14347873.
- ↑ 15.0 15.1 Patnaik MM, Moll S (November 2008). "Inherited antithrombin deficiency: a review". Haemophilia. 14 (6): 1229–39. doi:10.1111/j.1365-2516.2008.01830.x. PMID 19141163.
- ↑ 16.0 16.1 Hunt LT, Dayhoff MO (July 1980). "A surprising new protein superfamily containing ovalbumin, antithrombin-III, and alpha 1-proteinase inhibitor". Biochemical and Biophysical Research Communications. 95 (2): 864–71. doi:10.1016/0006-291X(80)90867-0. PMID 6968211.
- ↑ 17.0 17.1 Loebermann H, Tokuoka R, Deisenhofer J, Huber R (August 1984). "Human alpha 1-proteinase inhibitor. Crystal structure analysis of two crystal modifications, molecular model and preliminary analysis of the implications for function". Journal of Molecular Biology. 177 (3): 531–57. doi:10.1016/0022-2836(84)90298-5. PMID 6332197.
- ↑ 18.0 18.1 18.2 Stein PE, Leslie AG, Finch JT, Turnell WG, McLaughlin PJ, Carrell RW (September 1990). "Crystal structure of ovalbumin as a model for the reactive centre of serpins". Nature. 347 (6288): 99–102. Bibcode:1990Natur.347...99S. doi:10.1038/347099a0. PMID 2395463.
- ↑ 19.0 19.1 19.2 Irving JA, Pike RN, Lesk AM, Whisstock JC (December 2000). "Phylogeny of the serpin superfamily: implications of patterns of amino acid conservation for structure and function". Genome Research. 10 (12): 1845–64. doi:10.1101/gr.GR-1478R. PMID 11116082.
- ↑ 20.0 20.1 Irving JA, Steenbakkers PJ, Lesk AM, Op den Camp HJ, Pike RN, Whisstock JC (November 2002). "Serpins in prokaryotes". Molecular Biology and Evolution. 19 (11): 1881–90. doi:10.1093/oxfordjournals.molbev.a004012. PMID 12411597.
- ↑ 21.0 21.1 Steenbakkers PJ, Irving JA, Harhangi HR, Swinkels WJ, Akhmanova A, Dijkerman R, Jetten MS, van der Drift C, Whisstock JC, Op den Camp HJ (August 2008). "A serpin in the cellulosome of the anaerobic fungus Piromyces sp. strain E2". Mycological Research. 112 (Pt 8): 999–1006. doi:10.1016/j.mycres.2008.01.021. PMID 18539447.
- ↑ 22.0 22.1 Rawlings ND, Tolle DP, Barrett AJ (March 2004). "Evolutionary families of peptidase inhibitors". The Biochemical Journal. 378 (Pt 3): 705–16. doi:10.1042/BJ20031825. PMC 1224039. PMID 14705960.
- ↑ Cabrita LD, Irving JA, Pearce MC, Whisstock JC, Bottomley SP (September 2007). "Aeropin from the extremophile Pyrobaculum aerophilum bypasses the serpin misfolding trap". The Journal of Biological Chemistry. 282 (37): 26802–9. doi:10.1074/jbc.M705020200. PMID 17635906.
- ↑ Fluhr R, Lampl N, Roberts TH (May 2012). "Serpin protease inhibitors in plant biology". Physiologia Plantarum. 145 (1): 95–102. doi:10.1111/j.1399-3054.2011.01540.x. PMID 22085334.
- ↑ 25.0 25.1 25.2 Mala JG, Rose C (November 2010). "Interactions of heat shock protein 47 with collagen and the stress response: an unconventional chaperone model?". Life Sciences. 87 (19–22): 579–86. doi:10.1016/j.lfs.2010.09.024. PMID 20888348.
- ↑ 26.0 26.1 26.2 Zhou A, Wei Z, Read RJ, Carrell RW (September 2006). "Structural mechanism for the carriage and release of thyroxine in the blood". Proceedings of the National Academy of Sciences of the United States of America. 103 (36): 13321–6. Bibcode:2006PNAS..10313321Z. doi:10.1073/pnas.0604080103. PMC 1557382. PMID 16938877.
- ↑ Barrett AJ, Rawlings ND (April 1995). "Families and clans of serine peptidases". Archives of Biochemistry and Biophysics. 318 (2): 247–50. doi:10.1006/abbi.1995.1227. PMID 7733651.
- ↑ Huntington JA, Read RJ, Carrell RW (October 2000). "Structure of a serpin-protease complex shows inhibition by deformation". Nature. 407 (6806): 923–6. Bibcode:2000Natur.407..923H. doi:10.1038/35038119. PMID 11057674.
- ↑ Barrett AJ, Rawlings ND (May 2001). "Evolutionary lines of cysteine peptidases". Biological Chemistry. 382 (5): 727–33. doi:10.1515/BC.2001.088. PMID 11517925. S2CID 37306786.
- ↑ Irving JA, Pike RN, Dai W, Brömme D, Worrall DM, Silverman GA, Coetzer TH, Dennison C, Bottomley SP, Whisstock JC (April 2002). "Evidence that serpin architecture intrinsically supports papain-like cysteine protease inhibition: engineering alpha(1)-antitrypsin to inhibit cathepsin proteases". Biochemistry. 41 (15): 4998–5004. doi:10.1021/bi0159985. PMID 11939796.
- ↑ 31.0 31.1 Schick C, Brömme D, Bartuski AJ, Uemura Y, Schechter NM, Silverman GA (November 1998). "The reactive site loop of the serpin SCCA1 is essential for cysteine proteinase inhibition". Proceedings of the National Academy of Sciences of the United States of America. 95 (23): 13465–70. Bibcode:1998PNAS...9513465S. doi:10.1073/pnas.95.23.13465. PMC 24842. PMID 9811823.
- ↑ 32.0 32.1 McGowan S, Buckle AM, Irving JA, Ong PC, Bashtannyk-Puhalovich TA, Kan WT, Henderson KN, Bulynko YA, Popova EY, Smith AI, Bottomley SP, Rossjohn J, Grigoryev SA, Pike RN, Whisstock JC (July 2006). "X-ray crystal structure of MENT: evidence for functional loop-sheet polymers in chromatin condensation". The EMBO Journal. 25 (13): 3144–55. doi:10.1038/sj.emboj.7601201. PMC 1500978. PMID 16810322.
- ↑ Ong PC, McGowan S, Pearce MC, Irving JA, Kan WT, Grigoryev SA, Turk B, Silverman GA, Brix K, Bottomley SP, Whisstock JC, Pike RN (December 2007). "DNA accelerates the inhibition of human cathepsin V by serpins". The Journal of Biological Chemistry. 282 (51): 36980–6. doi:10.1074/jbc.M706991200. PMID 17923478.
- ↑ Acosta H, Iliev D, Grahn TH, Gouignard N, Maccarana M, Griesbach J, Herzmann S, Sagha M, Climent M, Pera EM (March 2015). "The serpin PN1 is a feedback regulator of FGF signaling in germ layer and primary axis formation". Development. 142 (6): 1146–58. doi:10.1242/dev.113886. PMID 25758225.
- ↑ 35.0 35.1 Hashimoto C, Kim DR, Weiss LA, Miller JW, Morisato D (December 2003). "Spatial regulation of developmental signaling by a serpin". Developmental Cell. 5 (6): 945–50. doi:10.1016/S1534-5807(03)00338-1. PMID 14667416.
- ↑ Bird PI (February 1999). "Regulation of pro-apoptotic leucocyte granule serine proteinases by intracellular serpins". Immunology and Cell Biology. 77 (1): 47–57. doi:10.1046/j.1440-1711.1999.00787.x. PMID 10101686.
- ↑ Bird CH, Sutton VR, Sun J, Hirst CE, Novak A, Kumar S, Trapani JA, Bird PI (November 1998). "Selective regulation of apoptosis: the cytotoxic lymphocyte serpin proteinase inhibitor 9 protects against granzyme B-mediated apoptosis without perturbing the Fas cell death pathway". Molecular and Cellular Biology. 18 (11): 6387–98. doi:10.1128/mcb.18.11.6387. PMC 109224. PMID 9774654.
- ↑ Ray CA, Black RA, Kronheim SR, Greenstreet TA, Sleath PR, Salvesen GS, Pickup DJ (May 1992). "Viral inhibition of inflammation: cowpox virus encodes an inhibitor of the interleukin-1 beta converting enzyme". Cell. 69 (4): 597–604. doi:10.1016/0092-8674(92)90223-Y. PMID 1339309.
- ↑ 39.0 39.1 Vercammen D, Belenghi B, van de Cotte B, Beunens T, Gavigan JA, De Rycke R, Brackenier A, Inzé D, Harris JL, Van Breusegem F (December 2006). "Serpin1 of Arabidopsis thaliana is a suicide inhibitor for metacaspase 9". Journal of Molecular Biology. 364 (4): 625–36. doi:10.1016/j.jmb.2006.09.010. PMID 17028019.
- ↑ 40.0 40.1 Lampl N, Budai-Hadrian O, Davydov O, Joss TV, Harrop SJ, Curmi PM, Roberts TH, Fluhr R (April 2010). "Arabidopsis AtSerpin1, crystal structure and in vivo interaction with its target protease responsive to desiccation (RD21)". The Journal of Biological Chemistry. 285 (18): 13550–60. doi:10.1074/jbc.M109.095075. PMC 2859516. PMID 20181955.
- ↑ 41.0 41.1 Klieber MA, Underhill C, Hammond GL, Muller YA (October 2007). "Corticosteroid-binding globulin, a structural basis for steroid transport and proteinase-triggered release". The Journal of Biological Chemistry. 282 (40): 29594–603. doi:10.1074/jbc.M705014200. PMID 17644521.
- ↑ Huntington JA, Stein PE (May 2001). "Structure and properties of ovalbumin". Journal of Chromatography B. 756 (1–2): 189–98. doi:10.1016/S0378-4347(01)00108-6. PMID 11419711.
- ↑ Grigoryev SA, Bednar J, Woodcock CL (February 1999). "MENT, a heterochromatin protein that mediates higher order chromatin folding, is a new serpin family member". The Journal of Biological Chemistry. 274 (9): 5626–36. doi:10.1074/jbc.274.9.5626. PMID 10026180.
- ↑ Elliott PR, Lomas DA, Carrell RW, Abrahams JP (August 1996). "Inhibitory conformation of the reactive loop of alpha 1-antitrypsin". Nature Structural Biology. 3 (8): 676–81. doi:10.1038/nsb0896-676. PMID 8756325. S2CID 22976014.
- ↑ Horvath AJ, Irving JA, Rossjohn J, Law RH, Bottomley SP, Quinsey NS, Pike RN, Coughlin PB, Whisstock JC (December 2005). "The murine orthologue of human antichymotrypsin: a structural paradigm for clade A3 serpins". The Journal of Biological Chemistry. 280 (52): 43168–78. doi:10.1074/jbc.M505598200. PMID 16141197.
- ↑ 46.0 46.1 46.2 46.3 46.4 Heit C, Jackson BC, McAndrews M, Wright MW, Thompson DC, Silverman GA, Nebert DW, Vasiliou V (30 October 2013). "Update of the human and mouse SERPIN gene superfamily". Human Genomics. 7: 22. doi:10.1186/1479-7364-7-22. PMC 3880077. PMID 24172014.
- ↑ Stoller JK, Aboussouan LS (2005). "Alpha1-antitrypsin deficiency" (PDF). Lancet. 365 (9478): 2225–36. doi:10.1016/S0140-6736(05)66781-5. PMID 15978931. S2CID 54415934.
- ↑ Münch J, Ständker L, Adermann K, Schulz A, Schindler M, Chinnadurai R, Pöhlmann S, Chaipan C, Biet T, Peters T, Meyer B, Wilhelm D, Lu H, Jing W, Jiang S, Forssmann WG, Kirchhoff F (April 2007). "Discovery and optimization of a natural HIV-1 entry inhibitor targeting the gp41 fusion peptide". Cell. 129 (2): 263–75. doi:10.1016/j.cell.2007.02.042. PMID 17448989.
- ↑ Gooptu B, Dickens JA, Lomas DA (February 2014). "The molecular and cellular pathology of α₁-antitrypsin deficiency". Trends in Molecular Medicine. 20 (2): 116–27. doi:10.1016/j.molmed.2013.10.007. PMID 24374162.
- ↑ Seixas S, Suriano G, Carvalho F, Seruca R, Rocha J, Di Rienzo A (February 2007). "Sequence diversity at the proximal 14q32.1 SERPIN subcluster: evidence for natural selection favoring the pseudogenization of SERPINA2". Molecular Biology and Evolution. 24 (2): 587–98. doi:10.1093/molbev/msl187. PMID 17135331.
- ↑ Kalsheker NA (September 1996). "Alpha 1-antichymotrypsin". The International Journal of Biochemistry & Cell Biology. 28 (9): 961–4. doi:10.1016/1357-2725(96)00032-5. PMID 8930118.
- ↑ Santamaria M, Pardo-Saganta A, Alvarez-Asiain L, Di Scala M, Qian C, Prieto J, Avila MA (April 2013). "Nuclear α1-antichymotrypsin promotes chromatin condensation and inhibits proliferation of human hepatocellular carcinoma cells". Gastroenterology. 144 (4): 818–828.e4. doi:10.1053/j.gastro.2012.12.029. PMID 23295442.
- ↑ Zhang S, Janciauskiene S (April 2002). "Multi-functional capability of proteins: alpha1-antichymotrypsin and the correlation with Alzheimer's disease". Journal of Alzheimer's Disease. 4 (2): 115–22. doi:10.3233/JAD-2002-4206. PMID 12214135.
- ↑ Chao J, Stallone JN, Liang YM, Chen LM, Wang DZ, Chao L (July 1997). "Kallistatin is a potent new vasodilator". The Journal of Clinical Investigation. 100 (1): 11–7. doi:10.1172/JCI119502. PMC 508159. PMID 9202051.
- ↑ Miao RQ, Agata J, Chao L, Chao J (November 2002). "Kallistatin is a new inhibitor of angiogenesis and tumor growth". Blood. 100 (9): 3245–52. doi:10.1182/blood-2002-01-0185. PMID 12384424.
- ↑ Liu Y, Bledsoe G, Hagiwara M, Shen B, Chao L, Chao J (October 2012). "Depletion of endogenous kallistatin exacerbates renal and cardiovascular oxidative stress, inflammation, and organ remodeling". American Journal of Physiology. Renal Physiology. 303 (8): F1230–8. doi:10.1152/ajprenal.00257.2012. PMC 3469672. PMID 22811485.
- ↑ Geiger M (March 2007). "Protein C inhibitor, a serpin with functions in- and outside vascular biology". Thrombosis and Haemostasis. 97 (3): 343–7. doi:10.1160/th06-09-0488. PMID 17334499.
- ↑ Baumgärtner P, Geiger M, Zieseniss S, Malleier J, Huntington JA, Hochrainer K, Bielek E, Stoeckelhuber M, Lauber K, Scherfeld D, Schwille P, Wäldele K, Beyer K, Engelmann B (November 2007). "Phosphatidylethanolamine critically supports internalization of cell-penetrating protein C inhibitor". The Journal of Cell Biology. 179 (4): 793–804. doi:10.1083/jcb.200707165. PMC 2080921. PMID 18025309.
- ↑ Uhrin P, Dewerchin M, Hilpert M, Chrenek P, Schöfer C, Zechmeister-Machhart M, Krönke G, Vales A, Carmeliet P, Binder BR, Geiger M (December 2000). "Disruption of the protein C inhibitor gene results in impaired spermatogenesis and male infertility". The Journal of Clinical Investigation. 106 (12): 1531–9. doi:10.1172/JCI10768. PMC 381472. PMID 11120760.
- ↑ Han MH, Hwang SI, Roy DB, Lundgren DH, Price JV, Ousman SS, Fernald GH, Gerlitz B, Robinson WH, Baranzini SE, Grinnell BW, Raine CS, Sobel RA, Han DK, Steinman L (February 2008). "Proteomic analysis of active multiple sclerosis lesions reveals therapeutic targets". Nature. 451 (7182): 1076–81. Bibcode:2008Natur.451.1076H. doi:10.1038/nature06559. PMID 18278032.
- ↑ Torpy DJ, Ho JT (August 2007). "Corticosteroid-binding globulin gene polymorphisms: clinical implications and links to idiopathic chronic fatigue disorders". Clinical Endocrinology. 67 (2): 161–7. doi:10.1111/j.1365-2265.2007.02890.x. PMID 17547679.
- ↑ Bartalena L, Robbins J (1992). "Variations in thyroid hormone transport proteins and their clinical implications". Thyroid. 2 (3): 237–45. doi:10.1089/thy.1992.2.237. PMID 1422238.
- ↑ Persani L (September 2012). "Clinical review: Central hypothyroidism: pathogenic, diagnostic, and therapeutic challenges". The Journal of Clinical Endocrinology and Metabolism. 97 (9): 3068–78. doi:10.1210/jc.2012-1616. PMID 22851492.
- ↑ Kumar R, Singh VP, Baker KM (July 2007). "The intracellular renin-angiotensin system: a new paradigm". Trends in Endocrinology and Metabolism. 18 (5): 208–14. doi:10.1016/j.tem.2007.05.001. PMID 17509892. S2CID 24041932.
- ↑ Tanimoto K, Sugiyama F, Goto Y, Ishida J, Takimoto E, Yagami K, Fukamizu A, Murakami K (December 1994). "Angiotensinogen-deficient mice with hypotension". The Journal of Biological Chemistry. 269 (50): 31334–7. PMID 7989296.
- ↑ Jeunemaitre X, Gimenez-Roqueplo AP, Célérier J, Corvol P (1999). "Angiotensinogen variants and human hypertension". Current Hypertension Reports. 1 (1): 31–41. doi:10.1007/s11906-999-0071-0. PMID 10981040. S2CID 42614761.
- ↑ Sethi AA, Nordestgaard BG, Tybjaerg-Hansen A (July 2003). "Angiotensinogen gene polymorphism, plasma angiotensinogen, and risk of hypertension and ischemic heart disease: a meta-analysis". Arteriosclerosis, Thrombosis, and Vascular Biology. 23 (7): 1269–75. doi:10.1161/01.ATV.0000079007.40884.5C. PMID 12805070.
- ↑ Dickson ME, Sigmund CD (July 2006). "Genetic basis of hypertension: revisiting angiotensinogen". Hypertension. 48 (1): 14–20. doi:10.1161/01.HYP.0000227932.13687.60. PMID 16754793.
- ↑ Frazer JK, Jackson DG, Gaillard JP, Lutter M, Liu YJ, Banchereau J, Capra JD, Pascual V (October 2000). "Identification of centerin: a novel human germinal center B cell-restricted serpin". European Journal of Immunology. 30 (10): 3039–48. doi:10.1002/1521-4141(200010)30:10<3039::AID-IMMU3039>3.0.CO;2-H. PMID 11069088.
- ↑ Paterson MA, Horvath AJ, Pike RN, Coughlin PB (August 2007). "Molecular characterization of centerin, a germinal centre cell serpin". The Biochemical Journal. 405 (3): 489–94. doi:10.1042/BJ20070174. PMC 2267310. PMID 17447896.
- ↑ Paterson MA, Hosking PS, Coughlin PB (July 2008). "Expression of the serpin centerin defines a germinal center phenotype in B-cell lymphomas". American Journal of Clinical Pathology. 130 (1): 117–26. doi:10.1309/9QKE68QU7B825A3U. PMID 18550480.
- ↑ Ashton-Rickardt PG (April 2013). "An emerging role for Serine Protease Inhibitors in T lymphocyte immunity and beyond". Immunology Letters. 152 (1): 65–76. doi:10.1016/j.imlet.2013.04.004. PMID 23624075.
- ↑ Han X, Fiehler R, Broze GJ (November 2000). "Characterization of the protein Z-dependent protease inhibitor". Blood. 96 (9): 3049–55. doi:10.1182/blood.V96.9.3049. PMID 11049983.
- ↑ Hida K, Wada J, Eguchi J, Zhang H, Baba M, Seida A, Hashimoto I, Okada T, Yasuhara A, Nakatsuka A, Shikata K, Hourai S, Futami J, Watanabe E, Matsuki Y, Hiramatsu R, Akagi S, Makino H, Kanwar YS (July 2005). "Visceral adipose tissue-derived serine protease inhibitor: a unique insulin-sensitizing adipocytokine in obesity". Proceedings of the National Academy of Sciences of the United States of America. 102 (30): 10610–5. Bibcode:2005PNAS..10210610H. doi:10.1073/pnas.0504703102. PMC 1180799. PMID 16030142.
- ↑ Feng R, Li Y, Wang C, Luo C, Liu L, Chuo F, Li Q, Sun C (October 2014). "Higher vaspin levels in subjects with obesity and type 2 diabetes mellitus: a meta-analysis". Diabetes Research and Clinical Practice. 106 (1): 88–94. doi:10.1016/j.diabres.2014.07.026. PMID 25151227.
- ↑ Remold-O'Donnell E, Chin J, Alberts M (June 1992). "Sequence and molecular characterization of human monocyte/neutrophil elastase inhibitor". Proceedings of the National Academy of Sciences of the United States of America. 89 (12): 5635–9. Bibcode:1992PNAS...89.5635R. doi:10.1073/pnas.89.12.5635. PMC 49347. PMID 1376927.
- ↑ Benarafa C, Priebe GP, Remold-O'Donnell E (August 2007). "The neutrophil serine protease inhibitor serpinb1 preserves lung defense functions in Pseudomonas aeruginosa infection". The Journal of Experimental Medicine. 204 (8): 1901–9. doi:10.1084/jem.20070494. PMC 2118684. PMID 17664292.
- ↑ Antalis TM, La Linn M, Donnan K, Mateo L, Gardner J, Dickinson JL, Buttigieg K, Suhrbier A (June 1998). "The serine proteinase inhibitor (serpin) plasminogen activation inhibitor type 2 protects against viral cytopathic effects by constitutive interferon alpha/beta priming". The Journal of Experimental Medicine. 187 (11): 1799–811. doi:10.1084/jem.187.11.1799. PMC 2212304. PMID 9607921.
- ↑ Zhao A, Yang Z, Sun R, Grinchuk V, Netzel-Arnett S, Anglin IE, Driesbaugh KH, Notari L, Bohl JA, Madden KB, Urban JF, Antalis TM, Shea-Donohue T (June 2013). "SerpinB2 is critical to Th2 immunity against enteric nematode infection". Journal of Immunology. 190 (11): 5779–87. doi:10.4049/jimmunol.1200293. PMC 4068334. PMID 23630350.
- ↑ Dougherty KM, Pearson JM, Yang AY, Westrick RJ, Baker MS, Ginsburg D (January 1999). "The plasminogen activator inhibitor-2 gene is not required for normal murine development or survival". Proceedings of the National Academy of Sciences of the United States of America. 96 (2): 686–91. Bibcode:1999PNAS...96..686D. doi:10.1073/pnas.96.2.686. PMC 15197. PMID 9892694.
- ↑ Takeda A, Yamamoto T, Nakamura Y, Takahashi T, Hibino T (February 1995). "Squamous cell carcinoma antigen is a potent inhibitor of cysteine proteinase cathepsin L". FEBS Letters. 359 (1): 78–80. doi:10.1016/0014-5793(94)01456-b. PMID 7851535.
- ↑ 82.0 82.1 Turato C, Pontisso P (March 2015). "SERPINB3 (serpin peptidase inhibitor, clade B (ovalbumin), member 3)". Atlas of Genetics and Cytogenetics in Oncology and Haematology. 19 (3): 202–209. doi:10.4267/2042/56413. PMC 4430857. PMID 25984243.
- ↑ 83.0 83.1 Sivaprasad U, Askew DJ, Ericksen MB, Gibson AM, Stier MT, Brandt EB, Bass SA, Daines MO, Chakir J, Stringer KF, Wert SE, Whitsett JA, Le Cras TD, Wills-Karp M, Silverman GA, Khurana Hershey GK (January 2011). "A nonredundant role for mouse Serpinb3a in the induction of mucus production in asthma". The Journal of Allergy and Clinical Immunology. 127 (1): 254–61, 261.e1–6. doi:10.1016/j.jaci.2010.10.009. PMC 3058372. PMID 21126757.
- ↑ Schick C, Kamachi Y, Bartuski AJ, Cataltepe S, Schechter NM, Pemberton PA, Silverman GA (January 1997). "Squamous cell carcinoma antigen 2 is a novel serpin that inhibits the chymotrypsin-like proteinases cathepsin G and mast cell chymase". The Journal of Biological Chemistry. 272 (3): 1849–55. doi:10.1074/jbc.272.3.1849. PMID 8999871.
- ↑ Teoh SS, Whisstock JC, Bird PI (April 2010). "Maspin (SERPINB5) is an obligate intracellular serpin". The Journal of Biological Chemistry. 285 (14): 10862–9. doi:10.1074/jbc.M109.073171. PMC 2856292. PMID 20123984.
- ↑ Zou Z, Anisowicz A, Hendrix MJ, Thor A, Neveu M, Sheng S, Rafidi K, Seftor E, Sager R (January 1994). "Maspin, a serpin with tumor-suppressing activity in human mammary epithelial cells". Science. 263 (5146): 526–9. Bibcode:1994Sci...263..526Z. doi:10.1126/science.8290962. PMID 8290962.
- ↑ 87.0 87.1 87.2 Teoh SS, Vieusseux J, Prakash M, Berkowicz S, Luu J, Bird CH, Law RH, Rosado C, Price JT, Whisstock JC, Bird PI (2014). "Maspin is not required for embryonic development or tumour suppression". Nature Communications. 5: 3164. Bibcode:2014NatCo...5.3164T. doi:10.1038/ncomms4164. PMC 3905777. PMID 24445777.
- ↑ Gao F, Shi HY, Daughty C, Cella N, Zhang M (April 2004). "Maspin plays an essential role in early embryonic development". Development. 131 (7): 1479–89. doi:10.1242/dev.01048. PMID 14985257.
- ↑ Scott FL, Hirst CE, Sun J, Bird CH, Bottomley SP, Bird PI (March 1999). "The intracellular serpin proteinase inhibitor 6 is expressed in monocytes and granulocytes and is a potent inhibitor of the azurophilic granule protease, cathepsin G". Blood. 93 (6): 2089–97. doi:10.1182/blood.V93.6.2089.406k10_2089_2097. PMID 10068683.
- ↑ Tan J, Prakash MD, Kaiserman D, Bird PI (July 2013). "Absence of SERPINB6A causes sensorineural hearing loss with multiple histopathologies in the mouse inner ear". The American Journal of Pathology. 183 (1): 49–59. doi:10.1016/j.ajpath.2013.03.009. PMID 23669344.
- ↑ Scarff KL, Ung KS, Nandurkar H, Crack PJ, Bird CH, Bird PI (May 2004). "Targeted disruption of SPI3/Serpinb6 does not result in developmental or growth defects, leukocyte dysfunction, or susceptibility to stroke". Molecular and Cellular Biology. 24 (9): 4075–82. doi:10.1128/MCB.24.9.4075-4082.2004. PMC 387772. PMID 15082799.
- ↑ Sirmaci A, Erbek S, Price J, Huang M, Duman D, Cengiz FB, Bademci G, Tokgoz-Yilmaz S, Hismi B, Ozdag H, Ozturk B, Kulaksizoglu S, Yildirim E, Kokotas H, Grigoriadou M, Petersen MB, Shahin H, Kanaan M, King MC, Chen ZY, Blanton SH, Liu XZ, Zuchner S, Akar N, Tekin M (2010). "A Truncating Mutation in SERPINB6 Is Associated with Autosomal-Recessive Nonsyndromic Sensorineural Hearing Loss". American Journal of Human Genetics. 86 (5): 797–804. doi:10.1016/j.ajhg.2010.04.004. PMC 2869020. PMID 20451170.
- ↑ Miyata T, Inagi R, Nangaku M, Imasawa T, Sato M, Izuhara Y, Suzuki D, Yoshino A, Onogi H, Kimura M, Sugiyama S, Kurokawa K (March 2002). "Overexpression of the serpin megsin induces progressive mesangial cell proliferation and expansion". The Journal of Clinical Investigation. 109 (5): 585–93. doi:10.1172/JCI14336. PMC 150894. PMID 11877466.
- ↑ 94.0 94.1 Miyata T, Li M, Yu X, Hirayama N (May 2007). "Megsin gene: its genomic analysis, pathobiological functions, and therapeutic perspectives". Current Genomics. 8 (3): 203–8. doi:10.2174/138920207780833856. PMC 2435355. PMID 18645605.
- ↑ Kubo A (August 2014). "Nagashima-type palmoplantar keratosis: a common Asian type caused by SERPINB7 protease inhibitor deficiency". The Journal of Investigative Dermatology. 134 (8): 2076–9. doi:10.1038/jid.2014.156. PMID 25029323.
- ↑ Dahlen JR, Jean F, Thomas G, Foster DC, Kisiel W (January 1998). "Inhibition of soluble recombinant furin by human proteinase inhibitor 8". The Journal of Biological Chemistry. 273 (4): 1851–4. doi:10.1074/jbc.273.4.1851. PMID 9442015.
- ↑ Sun J, Bird CH, Sutton V, McDonald L, Coughlin PB, De Jong TA, Trapani JA, Bird PI (November 1996). "A cytosolic granzyme B inhibitor related to the viral apoptotic regulator cytokine response modifier A is present in cytotoxic lymphocytes". The Journal of Biological Chemistry. 271 (44): 27802–9. doi:10.1074/jbc.271.44.27802. PMID 8910377.
- ↑ Zhang M, Park SM, Wang Y, Shah R, Liu N, Murmann AE, Wang CR, Peter ME, Ashton-Rickardt PG (April 2006). "Serine protease inhibitor 6 protects cytotoxic T cells from self-inflicted injury by ensuring the integrity of cytotoxic granules". Immunity. 24 (4): 451–61. doi:10.1016/j.immuni.2006.02.002. PMID 16618603.
- ↑ Rizzitelli A, Meuter S, Vega Ramos J, Bird CH, Mintern JD, Mangan MS, Villadangos J, Bird PI (October 2012). "Serpinb9 (Spi6)-deficient mice are impaired in dendritic cell-mediated antigen cross-presentation". Immunology and Cell Biology. 90 (9): 841–51. doi:10.1038/icb.2012.29. PMID 22801574.
- ↑ Riewald M, Chuang T, Neubauer A, Riess H, Schleef RR (February 1998). "Expression of bomapin, a novel human serpin, in normal/malignant hematopoiesis and in the monocytic cell lines THP-1 and AML-193". Blood. 91 (4): 1256–62. doi:10.1182/blood.V91.4.1256. PMID 9454755.
- ↑ 101.0 101.1 Askew DJ, Cataltepe S, Kumar V, Edwards C, Pace SM, Howarth RN, Pak SC, Askew YS, Brömme D, Luke CJ, Whisstock JC, Silverman GA (August 2007). "SERPINB11 is a new noninhibitory intracellular serpin. Common single nucleotide polymorphisms in the scaffold impair conformational change". The Journal of Biological Chemistry. 282 (34): 24948–60. doi:10.1074/jbc.M703182200. PMID 17562709.
- ↑ Finno CJ, Stevens C, Young A, Affolter V, Joshi NA, Ramsay S, Bannasch DL (April 2015). "SERPINB11 frameshift variant associated with novel hoof specific phenotype in Connemara ponies". PLOS Genetics. 11 (4): e1005122. doi:10.1371/journal.pgen.1005122. PMC 4395385. PMID 25875171.
- ↑ Askew YS, Pak SC, Luke CJ, Askew DJ, Cataltepe S, Mills DR, Kato H, Lehoczky J, Dewar K, Birren B, Silverman GA (December 2001). "SERPINB12 is a novel member of the human ov-serpin family that is widely expressed and inhibits trypsin-like serine proteinases". The Journal of Biological Chemistry. 276 (52): 49320–30. doi:10.1074/jbc.M108879200. PMID 11604408.
- ↑ Welss T, Sun J, Irving JA, Blum R, Smith AI, Whisstock JC, Pike RN, von Mikecz A, Ruzicka T, Bird PI, Abts HF (June 2003). "Hurpin is a selective inhibitor of lysosomal cathepsin L and protects keratinocytes from ultraviolet-induced apoptosis". Biochemistry. 42 (24): 7381–9. doi:10.1021/bi027307q. PMID 12809493.
- ↑ Huntington JA (August 2006). "Shape-shifting serpins--advantages of a mobile mechanism". Trends in Biochemical Sciences. 31 (8): 427–35. doi:10.1016/j.tibs.2006.06.005. PMID 16820297.
- ↑ Ishiguro K, Kojima T, Kadomatsu K, Nakayama Y, Takagi A, Suzuki M, Takeda N, Ito M, Yamamoto K, Matsushita T, Kusugami K, Muramatsu T, Saito H (October 2000). "Complete antithrombin deficiency in mice results in embryonic lethality". The Journal of Clinical Investigation. 106 (7): 873–8. doi:10.1172/JCI10489. PMC 517819. PMID 11018075.
- ↑ Huntington JA (July 2011). "Serpin structure, function and dysfunction". Journal of Thrombosis and Haemostasis. 9 Suppl 1: 26–34. doi:10.1111/j.1538-7836.2011.04360.x. PMID 21781239.
- ↑ Vicente CP, He L, Pavão MS, Tollefsen DM (December 2004). "Antithrombotic activity of dermatan sulfate in heparin cofactor II-deficient mice". Blood. 104 (13): 3965–70. doi:10.1182/blood-2004-02-0598. PMID 15315969.
- ↑ Aihara K, Azuma H, Akaike M, Ikeda Y, Sata M, Takamori N, Yagi S, Iwase T, Sumitomo Y, Kawano H, Yamada T, Fukuda T, Matsumoto T, Sekine K, Sato T, Nakamichi Y, Yamamoto Y, Yoshimura K, Watanabe T, Nakamura T, Oomizu A, Tsukada M, Hayashi H, Sudo T, Kato S, Matsumoto T (June 2007). "Strain-dependent embryonic lethality and exaggerated vascular remodeling in heparin cofactor II-deficient mice". The Journal of Clinical Investigation. 117 (6): 1514–26. doi:10.1172/JCI27095. PMC 1878511. PMID 17549254.
- ↑ Cale JM, Lawrence DA (September 2007). "Structure-function relationships of plasminogen activator inhibitor-1 and its potential as a therapeutic agent". Current Drug Targets. 8 (9): 971–81. doi:10.2174/138945007781662337. PMID 17896949.
- ↑ Lino MM, Atanasoski S, Kvajo M, Fayard B, Moreno E, Brenner HR, Suter U, Monard D (April 2007). "Mice lacking protease nexin-1 show delayed structural and functional recovery after sciatic nerve crush". The Journal of Neuroscience. 27 (14): 3677–85. doi:10.1523/JNEUROSCI.0277-07.2007. PMC 6672422. PMID 17409231.
- ↑ Murer V, Spetz JF, Hengst U, Altrogge LM, de Agostini A, Monard D (March 2001). "Male fertility defects in mice lacking the serine protease inhibitor protease nexin-1". Proceedings of the National Academy of Sciences of the United States of America. 98 (6): 3029–33. Bibcode:2001PNAS...98.3029M. doi:10.1073/pnas.051630698. PMC 30601. PMID 11248026.
- ↑ Lüthi A, Van der Putten H, Botteri FM, Mansuy IM, Meins M, Frey U, Sansig G, Portet C, Schmutz M, Schröder M, Nitsch C, Laurent JP, Monard D (June 1997). "Endogenous serine protease inhibitor modulates epileptic activity and hippocampal long-term potentiation". The Journal of Neuroscience. 17 (12): 4688–99. doi:10.1523/JNEUROSCI.17-12-04688.1997. PMC 6573330. PMID 9169529.
- ↑ 114.0 114.1 Doll JA, Stellmach VM, Bouck NP, Bergh AR, Lee C, Abramson LP, Cornwell ML, Pins MR, Borensztajn J, Crawford SE (June 2003). "Pigment epithelium-derived factor regulates the vasculature and mass of the prostate and pancreas". Nature Medicine. 9 (6): 774–80. doi:10.1038/nm870. PMID 12740569. S2CID 5967666.
- ↑ Becerra SP, Perez-Mediavilla LA, Weldon JE, Locatelli-Hoops S, Senanayake P, Notari L, Notario V, Hollyfield JG (November 2008). "Pigment epithelium-derived factor binds to hyaluronan. Mapping of a hyaluronan binding site". The Journal of Biological Chemistry. 283 (48): 33310–20. doi:10.1074/jbc.M801287200. PMC 2586245. PMID 18805795.
- ↑ Andreu-Agulló C, Morante-Redolat JM, Delgado AC, Fariñas I (December 2009). "Vascular niche factor PEDF modulates Notch-dependent stemness in the adult subependymal zone". Nature Neuroscience. 12 (12): 1514–23. doi:10.1038/nn.2437. PMID 19898467.
- ↑ Homan EP, Rauch F, Grafe I, Lietman C, Doll JA, Dawson B, Bertin T, Napierala D, Morello R, Gibbs R, White L, Miki R, Cohn DH, Crawford S, Travers R, Glorieux FH, Lee B (December 2011). "Mutations in SERPINF1 cause osteogenesis imperfecta type VI". Journal of Bone and Mineral Research. 26 (12): 2798–803. doi:10.1002/jbmr.487. PMC 3214246. PMID 21826736.
- ↑ Wiman B, Collen D (September 1979). "On the mechanism of the reaction between human alpha 2-antiplasmin and plasmin". The Journal of Biological Chemistry. 254 (18): 9291–7. PMID 158022.
- ↑ Lijnen HR, Okada K, Matsuo O, Collen D, Dewerchin M (April 1999). "Alpha2-antiplasmin gene deficiency in mice is associated with enhanced fibrinolytic potential without overt bleeding". Blood. 93 (7): 2274–81. doi:10.1182/blood.V93.7.2274. PMID 10090937.
- ↑ Carpenter SL, Mathew P (November 2008). "Alpha2-antiplasmin and its deficiency: fibrinolysis out of balance". Haemophilia. 14 (6): 1250–4. doi:10.1111/j.1365-2516.2008.01766.x. PMID 19141165.
- ↑ Favier R, Aoki N, De Moerloose P (1 July 2001). "Congenital α2-plasmin inhibitor deficiencies: a review". British Journal of Haematology. 114 (1): 4–10. doi:10.1046/j.1365-2141.2001.02845.x. ISSN 1365-2141. PMID 11472338.
- ↑ Beinrohr L, Harmat V, Dobó J, Lörincz Z, Gál P, Závodszky P (July 2007). "C1 inhibitor serpin domain structure reveals the likely mechanism of heparin potentiation and conformational disease". The Journal of Biological Chemistry. 282 (29): 21100–9. doi:10.1074/jbc.M700841200. PMID 17488724.
- ↑ Mollnes TE, Jokiranta TS, Truedsson L, Nilsson B, Rodriguez de Cordoba S, Kirschfink M (September 2007). "Complement analysis in the 21st century". Molecular Immunology. 44 (16): 3838–49. doi:10.1016/j.molimm.2007.06.150. hdl:10261/61732. PMID 17768101.
- ↑ Triggianese P, Chimenti MS, Toubi E, Ballanti E, Guarino MD, Perricone C, Perricone R (August 2015). "The autoimmune side of hereditary angioedema: insights on the pathogenesis". Autoimmunity Reviews. 14 (8): 665–9. doi:10.1016/j.autrev.2015.03.006. PMID 25827463.
- ↑ Nagai N, Hosokawa M, Itohara S, Adachi E, Matsushita T, Hosokawa N, Nagata K (September 2000). "Embryonic lethality of molecular chaperone hsp47 knockout mice is associated with defects in collagen biosynthesis". The Journal of Cell Biology. 150 (6): 1499–506. doi:10.1083/jcb.150.6.1499. PMC 2150697. PMID 10995453.
- ↑ Marini JC, Reich A, Smith SM (August 2014). "Osteogenesis imperfecta due to mutations in non-collagenous genes: lessons in the biology of bone formation". Current Opinion in Pediatrics. 26 (4): 500–7. doi:10.1097/MOP.0000000000000117. PMC 4183132. PMID 25007323.
- ↑ Byers PH, Pyott SM (1 January 2012). "Recessively inherited forms of osteogenesis imperfecta". Annual Review of Genetics. 46: 475–97. doi:10.1146/annurev-genet-110711-155608. PMID 23145505.
- ↑ Osterwalder T, Cinelli P, Baici A, Pennella A, Krueger SR, Schrimpf SP, Meins M, Sonderegger P (January 1998). "The axonally secreted serine proteinase inhibitor, neuroserpin, inhibits plasminogen activators and plasmin but not thrombin". The Journal of Biological Chemistry. 273 (4): 2312–21. doi:10.1074/jbc.273.4.2312. PMID 9442076.
- ↑ Crowther DC (July 2002). "Familial conformational diseases and dementias". Human Mutation. 20 (1): 1–14. doi:10.1002/humu.10100. PMID 12112652.
- ↑ Belorgey D, Hägglöf P, Karlsson-Li S, Lomas DA (1 March 2007). "Protein misfolding and the serpinopathies". Prion. 1 (1): 15–20. doi:10.4161/pri.1.1.3974. PMC 2633702. PMID 19164889.
- ↑ Ozaki K, Nagata M, Suzuki M, Fujiwara T, Miyoshi Y, Ishikawa O, Ohigashi H, Imaoka S, Takahashi E, Nakamura Y (July 1998). "Isolation and characterization of a novel human pancreas-specific gene, pancpin, that is down-regulated in pancreatic cancer cells". Genes, Chromosomes & Cancer. 22 (3): 179–85. doi:10.1002/(SICI)1098-2264(199807)22:3<179::AID-GCC3>3.0.CO;2-T. PMID 9624529.
- ↑ Loftus SK, Cannons JL, Incao A, Pak E, Chen A, Zerfas PM, Bryant MA, Biesecker LG, Schwartzberg PL, Pavan WJ (September 2005). "Acinar cell apoptosis in Serpini2-deficient mice models pancreatic insufficiency". PLOS Genetics. 1 (3): e38. doi:10.1371/journal.pgen.0010038. PMC 1231717. PMID 16184191.
- ↑ Padua MB, Kowalski AA, Cañas MY, Hansen PJ (February 2010). "The molecular phylogeny of uterine serpins and its relationship to evolution of placentation". FASEB Journal. 24 (2): 526–37. doi:10.1096/fj.09-138453. PMID 19825977.
- ↑ Padua MB, Hansen PJ (October 2010). "Evolution and function of the uterine serpins (SERPINA14)". American Journal of Reproductive Immunology. 64 (4): 265–74. doi:10.1111/j.1600-0897.2010.00901.x. PMID 20678169.
- ↑ 135.0 135.1 Reichhart JM (December 2005). "Tip of another iceberg: Drosophila serpins". Trends in Cell Biology. 15 (12): 659–65. doi:10.1016/j.tcb.2005.10.001. PMID 16260136.
- ↑ Tang H, Kambris Z, Lemaitre B, Hashimoto C (October 2008). "A serpin that regulates immune melanization in the respiratory system of Drosophila". Developmental Cell. 15 (4): 617–26. doi:10.1016/j.devcel.2008.08.017. PMC 2671232. PMID 18854145.
- ↑ Scherfer C, Tang H, Kambris Z, Lhocine N, Hashimoto C, Lemaitre B (November 2008). "Drosophila Serpin-28D regulates hemolymph phenoloxidase activity and adult pigmentation". Developmental Biology. 323 (2): 189–96. doi:10.1016/j.ydbio.2008.08.030. PMID 18801354.
- ↑ Rushlow C (January 2004). "Dorsoventral patterning: a serpin pinned down at last". Current Biology. 14 (1): R16–8. doi:10.1016/j.cub.2003.12.015. PMID 14711428.
- ↑ Ligoxygakis P, Roth S, Reichhart JM (December 2003). "A serpin regulates dorsal-ventral axis formation in the Drosophila embryo". Current Biology. 13 (23): 2097–102. doi:10.1016/j.cub.2003.10.062. PMID 14654000.
- ↑ Jiang R, Zhang B, Kurokawa K, So YI, Kim EH, Hwang HO, Lee JH, Shiratsuchi A, Zhang J, Nakanishi Y, Lee HS, Lee BL (October 2011). "93-kDa twin-domain serine protease inhibitor (Serpin) has a regulatory function on the beetle Toll proteolytic signaling cascade". The Journal of Biological Chemistry. 286 (40): 35087–95. doi:10.1074/jbc.M111.277343. PMC 3186399. PMID 21862574.
- ↑ 141.0 141.1 Pak SC, Kumar V, Tsu C, Luke CJ, Askew YS, Askew DJ, Mills DR, Brömme D, Silverman GA (April 2004). "SRP-2 is a cross-class inhibitor that participates in postembryonic development of the nematode Caenorhabditis elegans: initial characterization of the clade L serpins". The Journal of Biological Chemistry. 279 (15): 15448–59. doi:10.1074/jbc.M400261200. PMID 14739286.
- ↑ Luke CJ, Pak SC, Askew YS, Naviglia TL, Askew DJ, Nobar SM, Vetica AC, Long OS, Watkins SC, Stolz DB, Barstead RJ, Moulder GL, Brömme D, Silverman GA (September 2007). "An intracellular serpin regulates necrosis by inhibiting the induction and sequelae of lysosomal injury". Cell. 130 (6): 1108–19. doi:10.1016/j.cell.2007.07.013. PMC 2128786. PMID 17889653.
- ↑ Hejgaard J, Rasmussen SK, Brandt A, SvendsenI (1985). "Sequence homology between barley endosperm protein Z and protease inhibitors of the alpha-1-antitrypsin family". FEBS Lett. 180 (1): 89–94. doi:10.1016/0014-5793(85)80238-6.
- ↑ Dahl SW, Rasmussen SK, Petersen LC, Hejgaard J (September 1996). "Inhibition of coagulation factors by recombinant barley serpin BSZx". FEBS Letters. 394 (2): 165–8. doi:10.1016/0014-5793(96)00940-4. PMID 8843156.
- ↑ Hejgaard J (January 2001). "Inhibitory serpins from rye grain with glutamine as P1 and P2 residues in the reactive center". FEBS Letters. 488 (3): 149–53. doi:10.1016/S0014-5793(00)02425-X. PMID 11163762.
- ↑ Ostergaard H, Rasmussen SK, Roberts TH, Hejgaard J (October 2000). "Inhibitory serpins from wheat grain with reactive centers resembling glutamine-rich repeats of prolamin storage proteins. Cloning and characterization of five major molecular forms". The Journal of Biological Chemistry. 275 (43): 33272–9. doi:10.1074/jbc.M004633200. PMID 10874043.
- ↑ Yoo BC, Aoki K, Xiang Y, Campbell LR, Hull RJ, Xoconostle-Cázares B, Monzer J, Lee JY, Ullman DE, Lucas WJ (November 2000). "Characterization of cucurbita maxima phloem serpin-1 (CmPS-1). A developmentally regulated elastase inhibitor". The Journal of Biological Chemistry. 275 (45): 35122–8. doi:10.1074/jbc.M006060200. PMID 10960478.
- ↑ la Cour Petersen M, Hejgaard J, Thompson GA, Schulz A (December 2005). "Cucurbit phloem serpins are graft-transmissible and appear to be resistant to turnover in the sieve element-companion cell complex". Journal of Experimental Botany. 56 (422): 3111–20. doi:10.1093/jxb/eri308. PMID 16246856.
- ↑ Roberts TH, Hejgaard J (February 2008). "Serpins in plants and green algae". Functional & Integrative Genomics. 8 (1): 1–27. doi:10.1007/s10142-007-0059-2. PMID 18060440. S2CID 22960858.
- ↑ Lampl N, Alkan N, Davydov O, Fluhr R (May 2013). "Set-point control of RD21 protease activity by AtSerpin1 controls cell death in Arabidopsis". The Plant Journal. 74 (3): 498–510. doi:10.1111/tpj.12141. PMID 23398119.
- ↑ Ahn JW, Atwell BJ, Roberts TH (2009). "Serpin genes AtSRP2 and AtSRP3 are required for normal growth sensitivity to a DNA alkylating agent in Arabidopsis". BMC Plant Biology. 9: 52. doi:10.1186/1471-2229-9-52. PMC 2689219. PMID 19426562.
- ↑ Kang S, Barak Y, Lamed R, Bayer EA, Morrison M (June 2006). "The functional repertoire of prokaryote cellulosomes includes the serpin superfamily of serine proteinase inhibitors". Molecular Microbiology. 60 (6): 1344–54. doi:10.1111/j.1365-2958.2006.05182.x. PMID 16796673. S2CID 23738804.
แหล่งข้อมูลอื่น[แก้]
- PDB Molecule of the Month Serpin
- Merops protease inhibitor claudication (Family I4) เก็บถาวร 2016-12-08 ที่ เวย์แบ็กแมชชีน
- Serpins ในหอสมุดแพทยศาสตร์แห่งชาติอเมริกัน สำหรับหัวข้อเนื้อหาทางการแพทย์ (MeSH)
- James Whisstock laboratory ของมหาวิทยาลัยโมนาช
- Jim Huntington laboratory เก็บถาวร 2016-10-30 ที่ เวย์แบ็กแมชชีน ของมหาวิทยาลัยเคมบริดจ์
- Frank Church laboratory ของมหาวิทยาลัยนอร์ทแคโรไลนา แชเปิลฮิลล์
- Paul Declerck laboratory ของ มหาวิทยาลัยคาทอลิคเลอเฟิน
- Tom Roberts laboratory ของมหาวิทยาลัยซิดนีย์
- Robert Fluhr laboratory ของ สถาบันวิทยศาสตร์ไวซ์มานน์
- Peter Gettins laboratory ของมหาวิทยาลัยอิลลินอยส์ ชิคาโก
- ข้อมูลเชิงโครงสร้างทั้งหมดของ UniProt: P01009 (Human Alpha-1-antitrypsin) สามารถเข้าถึงได้ในธนาคารข้อมูลโปรตีนของ PDBe-KB.
