ผู้ใช้:M sky/ไลนิโซลิด
 | |
 | |
| ข้อมูลทางคลินิก | |
|---|---|
| ชื่อทางการค้า | ไลโนสแพน (Linospan), ซีว็อกซ์ (Zyvox), ซีโวแซม (Zyvoxam), ซีโวซิด (Zyvoxid) |
| AHFS/Drugs.com | โมโนกราฟ |
| MedlinePlus | a602004 |
| ข้อมูลทะเบียนยา | |
| ระดับความเสี่ยงต่อทารกในครรภ์ |
|
| ช่องทางการรับยา | ฉีดเข้าหลอดเลือดดำ, ปาก |
| รหัส ATC | |
| กฏหมาย | |
| สถานะตามกฏหมาย |
|
| ข้อมูลเภสัชจลนศาสตร์ | |
| ชีวประสิทธิผล | ~100% (ปาก) |
| การจับกับโปรตีน | ต่ำ (31%) |
| การเปลี่ยนแปลงยา | ตับ (50–70%, ไม่เกี่ยวข้องกับ CYP) |
| ครึ่งชีวิตทางชีวภาพ | 4.2–5.4 ชั่วโมง (สั้นกว่าในเด็ก) |
| การขับออก | ไต, อุจจาระ, และทางอื่นที่มิใช่ไต |
| ตัวบ่งชี้ | |
| |
| เลขทะเบียน CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| ข้อมูลทางกายภาพและเคมี | |
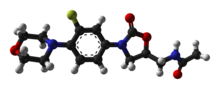
| สูตร | C16H20FN3O4 |
| มวลต่อโมล | 337.346 g/mol g·mol−1 |
| แบบจำลอง 3D (JSmol) | |
| |
| |
| | |
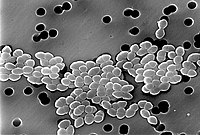
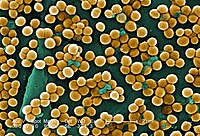
ไลนีโซลิด (อังกฤษ: Linezolid) (ชื่อระหว่างประเทศที่ไม่มีเจ้าของ) (/lɪˈnɛzəlɪd/ li-nez-ə-lid) คือยาปฏิชีวนะสังเคราะห์เพื่อการรักษาการติดเชื้อแบคทีเรียแกรมบวกขั้นรุนแรงซึ่งดื้อต่อยาปฏิชีวนะตัวอื่นๆ ด้วยอนุพันธ์ออกโซลิดิโนน (oxazolidinone) ของยาทำให้สามารถออกฤทธิ์ต่อต้านแบคทีเรียแกรบวกโดยส่วนใหญ่ได้ รวมไปถึงสเตร็ปโตคอกคัส เอ็นเทอโรคอกคัสที่ดื้อต่อยาแวนโคมัยซิน (VRE) และสแตรฟิโลคอกคัสที่ดื้อต่อยาเมทิซิลลิน (MRSA)[1] ข้อบ่งชี้หลักของยาขนานนี้คือการติดเชื้อบริเวณผิวหนังและเนื้อเยื่อบาง รวมไปถึงโรคปอดบวม (โดยเฉพาะโรคปอดบวมที่ต้องเข้ารับการรักษาในโรงพยาบาล) แม้ว่าจะมีการใช้ในกรณีการติดเชื้ออื่นๆ ที่ไม่ได้มีการระบุในข้อบ่งใช้หลัก (off-label) อย่างแพร่หลาย ไฟเซอร์เป็นผู้ทำการตลาดสำหรับยาขนานนี้ภายใต้ชื่อการต้าว่า "ซีว็อก" (ในสหรัฐอเมริกา ออสเตรเลีย สหราชอาณาจักร และอีกหลายประเทศ) "ซีโวซิด" (ในยุโรป) "ซีโวแซม" (ในแคนากาและเม็กซิโก) และในรูปแบบยาสามัญในประเทศอินเดีย อาทิ "ลิโนสแพน" (ซิปลา)
ไลนีโซลิดได้รับการค้นพบในคริสต์ทศวรรษที่ 1990 และได้รับการจดทะเบียนอนุมัติครั้งแรกในปี ค.ศ. 2000 ซึ่งได้ทำการตลาดในรูแบบอนุพันธ์ยาปฏิชีวนะ 1,3-ออกซาโซลิดิโนน แม้ว่าในขณะนั้นจะมีการพัฒนายาตัวอื่นเช่นกัน โดยยาออกฤทธิ์ด้วยการยับยั้งการสังเคราะห์โปรตีนซึ่งทำให้ยับยั้งการเจริญเติบโตของเชื้อแบคทีเรียในขั้นตอนการสังเคราะห์โปรตีน แม้ว่ายาปฏิชีวนะหลายขนานจะออกฤทธิ์ในกระบวนการเดียวกันนี้ แต่กลไกการออกฤทธิ์ที่แท้จริงของไลนีโซลิดมีความโดดเด่นในกลุ่มออกซาโซลิดิโนน กระบวนการการดื้อยาของเชื้อแบคทีเรียต่อเชื้อชนิดนี้เกิดขึ้นอย่างช้าๆ ซึ่งตรวจพบครั้งแรกในปี ค.ศ. 1999 และเกิดขึ้นอย่างต่อเนื่อง
การบริหารยาไลนีโซลิดในช่วงระยะเวลาสั้นๆ จัดว่าเป็นยาที่มีความปลอดภัยต่อผู้ป่วยในทุกช่วงอายุและในผู้ป่วยที่มีโรคตับหรือไตล้มเหลว อาการอันไม่พึงประสงค์จากยาในการบริหารยาช่วงสั้นๆ ได้แก่ อาการปวดศีรษะ ท้องเสีย เวียนศีรษะ สำหรับการบริหารยาในระยะเวลายาว พบว่ามีความสัมพันธ์กับอาการอันไม่พึงประสงค์ที่รุนแรง ไลนิโซลิดมีฤทธิ์กดไขกระดูกและเกล็ดเลือกต่ำ โดยเฉพาะการบริหารในช่วงมากกว่าสองสัปดาห์ หากใช้ในระยะเวลายาวกว่านั้นอาทำให้เกิดอาการชาตามปลายประสาท (ซึ่งไม่อาจคืนสภาพปกติได้), ประสาทตาถูกทำลาย และภาวะเลือดเป็นกรดจากกรดแลกติก (lactic acidosis) เนื่องมาจากเกิดพิษต่อไมโทคอนเดรีย
ยาขนานนี้มีราคาสูงตามช่วงระยะเวลาการรักษา (20 เม็ด เม็ดละ 600 มิลลิกรัม) ซึ่งมีค่าใช้จ่ายราวหนึ่งพันถึงสองพันเหรียญดอลล่าร์สหรัฐ[2] และมีราคาสูงกว่าเมื่อเปรียบเทียบกับยาปฏิชีวนะตัวอื่น[3] ส่วนใหญ่ยังผลมาจากสภาวะที่ผู้ป่วยสามารถเปลี่ยนวิธีการบริหารยาจากการฉีดเข้าหลอดเลือดดำเป็นการบริหารยาทางปากซึ่งไม่ต้องปรับขนาดยาแต่อย่างใด
การใช้ยา
[แก้]ข้อบ่งใช้หลักของไลนีโซลิดคือการรักษาอาการติดเชื้อแบคทีเรียแกรมบวกขั้นรุนแรงที่ดื้อต่อยาปฏิชีวนะอื่นๆ ซึ่งไม่ควรกับเชื้อที่ดื้อต่อยาที่มีช่วงการรักษาแคบ อาทิเพนนิซิลลินและเซฟาโลสปอริน ในวารสารป๊อปปูลาร์เพรส และ ไซแอนทิฟิกลิเทอเรเทอร์ ไลนีโซลิดได้รับการขนานนามว่าเป็น "reserve antibiotic" —คือเป็นหนึ่งในยาที่พิจารณาถี่ถ้วนก่อนการใช้หรือเป็นยาตัวเลือกสุดท้ายของยาทั้งมวล (drug of last resort) ใช้เพื่อรักษาอาการติดเชื้อที่รุนแรง[4][5]
ข้อบ่งใช้ยาไลนีโซลิดในสหรัฐอเมริกาซึ่งอนุมัติโดยองค์การอาหารและยาของสหรัฐอเมริกา (FDA) คือรักษาอาการติดเชื้อ เอนเทอโรคอกคัส ที่ดื้อต่อยาแวนโคมัยซิน ซึ่งอาจเกิดร่วมหรือไม่เกิดร่วมการติดเชื้อแบคทีเรียในกระแสเลือด, โรคปอดบวมจากเชื้อ S. aureus หรือ S. pneumoniae, การติดเชื้อซับซ้อนที่ผิวหนัง (cSSSI) อันเนื่องมาจากแบคทีเรีย เช่น ภาวะติดเชื้อแผลทีเท้าของผู้ป่วยเบาหวาน, การอักเสบบริเวณกระดูกหรือไขกระดูกจากการติดเชื้อ และการติดเชื้อ ไม่ซับซ้อน ที่บริเวณผิวหนังและเนื้อเยื่ออ่อนจากเชื้อ S. pyogenes หรือ S. aureus ผู้ผลิตยังแนะนำว่าสามารถใช้ไลนีโซลิดสำหรับการรักษาปอดอักเสบชุมชนหรือการติดเชื้อ MRSA บริเวณผิวหนังและเนื้อเยื่ออ่อนแบไม่ซับซ้อน[1] ในสหราชอาณาจักร มีการระบุข้อบ่งใช้เพียงการรักษาโรคปอดอักเสบและการติดเชื้อซับซ้อนบริเวณผิวหนัง[6] ไลนีโซลิดมีความปลอดภัยและมีประสิทธิภาพในเด็กหรือทารกเทียบเท่าผู้ใหญ่[7]
การติดเชือบริเวณผิวหนังและเนื้อเยื่ออ่อน
[แก้]การวิเคราะห์อภิมานโดยการสุ่มตัวอย่างแบบควบคุม (meta-analysis of randomized controlled trials) พบว่าไลนีโซลิดมีประสิทธิภาพมากกว่ายาปฏิชีวนะไกลโคเพปไทด์ (อาทิ แวนโคมันซินและทีโคพลานิน) และยาปฏิชีวนะกลุ่มเบต้าแลกแตมสำหรับการรักษาการติดเชื้อแบคทีเรียแกรมบวกที่ผิวหนังและเนื้อเยื่ออ่อน[8] และการศึกษาที่เล็กกว่ายืนยันว่าไลนีโซลิดมีฤทธิ์เหนือกว่าทีโคพลานินในการรักษาการติดเชื้อแบคทีเรียแกรมบวกขั้นรุนแรงทุกกรณี[9]
ในการรักษาภาวะติดเชื้อที่เท้าของผู้ป่วยเบาหวาน การเลือกใช้ไลนีโซลิดเป็นทางเลือกที่ค่าใช้จ่ายน้อยกว่าและมีประสิทธิภาพสูงกว่าแวนโคมัยซิน[10] ในปี ค.ศ. 2004 การศึกษาแบบ open-label แสดงให้เห็นถึงประสิทธิภาพของแอมพิซิลลิน/ซัลแบกแทม และโคอะม็อกซีคลาฟและมีฤทธิ์เหนือกว่าผู้ป่วยที่ร่วมกับอาการแผลติดเชื้อที่เท้าและโรคกระดูกอักเสบ แต่พบอาการไม่พึงประสงค์มากกว่า[11][12] ในปี ค.ศ. 2008 การวิจัยวิเคราะห์อภิมานจากตัวอย่างที่สุ่มมาจำนวน 18 ตัวอย่าง พบว่าการรักษาไลนีโซลิดล้มเหลวพอๆกับการรักษาด้วยาปฏิชีวนะขนานอื่นๆ ซึ่งไม่รวมถึงผู้ป่วยที่เป็นโรคกระดูกอักเสบ[13]
ผู้วิจัยบางคนแนะนำว่าการรักษาร่วมกันกับยาขนานอื่นมีค่าใช้จ่ายถูกกว่าและมีประสิทธิภาพมากกว่า (อาทิโคไตรมาโซลร่วมกับไรแฟมพิซินหรือคลินดามัยซิน) ซึ่งควรใช้ก่อนเริ่มต้นการรักษาด้วไลนีโซลิดสำหรับการรักษาการติดเชื้อที่ผิวหนังและเนื้อเยื่ออ่อนสำหรับเชื้อที่ไวต่อยานั้น[12][14]
ปอดบวม
[แก้]การรักษาโรคปอดบวมไม่มีผลการรักษาด้วยยาใดที่แตกต่างกันอย่างมีนัยสำคัญระหว่างยาไไลนีโซลิด, ไกลโคเพปไทด์ หรือยาปฏิชีวนะกลุ่มเบต้าแลกแตม [8] แนวทางการรักษาโรคปอดบวมชุมชนได้รับการพัฒนาโดยสมาคมศัลยแพทย์ทรวงอกอเมริกันและสมาคมโรคติดเชื้อแห่งสหรัฐอเมริกาแนะนำให้ใช้ไลนีโซลิดเพื่อรักษาผู้ติดเชื้อ MRSA เมื่อมีอาการแสดงทางคลินิก[15] แนวทางการรักษาของสมาคมศัลยแพทย์ทรวงอกบริติชไม่แนะนำให้ใช้ยาขนานนี้เป็นยาขานแรกในการเลือกใช้ แต่ให้ใช้เป็นยาทางเลือกสำหรับแวนโคมัยซิน[16] ไลนีโซลิดยังยอมรับให้เป็นยาตัวที่สองที่เลือกใช้ในการรักษาปอดอักเสบชุมชนที่ดื้อต่อยาเพนนิซิลลิน[15]
แนวทางการรักษาของสหรัฐอเมริกาแนะนำให้เลือกใช้ไลนีโซลิดหรือแวนโคมัยซินเป็นยาขนานแรกสำหรับการรักษาโรคปอดอักเสบติดเชื้อ MRSA[17] บางการศึกษาแนะนำว่าไลนีโซลิดดีกว่าแวนโคมัยซินในการรักษาโรคปอดอักเสบ โดยเฉพาะปอดอักเสบจากเครื่องช่วยหายใจจากการติดเชื้อ MRSA อาจเนื่องมาจากการซึมผ่านของไลนีโซลิดสู่น้ำเลี้ยงเยื่อปอดได้มากกว่าแวนโคมัยซิน[12] ทั้งนี้ ยังไม่รวมถึงประโยชน์ของไลนีโซลิดได้แก่ชีวปริมาณการออกฤทธิ์ที่สูงกว่า (เนื่องจากยานี้สามารถเปลี่ยนเป็นการบริหารยาด้วยปากง่ายกว่า) และในข้อเท็จจริงที่การทำงานของไตต่ำลงก็มิป็นอุปสรรคต่อการใช้ยา (ในทางตรงกันข้ามการให้ยาแวนโคมัยซินในขนาดที่เหมาะสมในผู้ป่วยไตวายกระทำได้ยากกว่า)[17]
อื่นๆ
[แก้]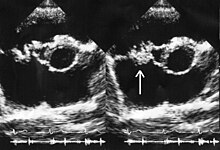
เดิมเชื่อว่ายานี้รักษาการติดเชื้อส่วนลึกของร่างกาย เช่น กระดูกอักเสบหรือเยื่อบุหัวใจอักเสบติดเชื้อ ซึ่งต้องใช้ยาปฏิชีวนะฆ่าเชื้อแบคทเรีย มิใช่ยาปฏิชีวนะยับยั้งกาเจริญเติบโตของเชื้อ อย่างไรก็ตามการศึกษาปรีคลินิกได้ทำการประเมินประสิทธิภาพของไลนีโซลิดสำหรับการรักษาการติดเชื้อ[19] และพบว่าประสบความสำเร็จในขั้นปฏิบัติทางคลินิก ไลนิโซลิดจึงเป็นยาที่สมเหตุสมผลต่อการใช้เพื่อรักษาอาการเยื่อบุหัวใจอักเสบติดเชื้อแบคทีเรียแกรมบวกที่ดื้อยาหลายขนาน (multi-resistant) แม้ว่าจะขาดหลักฐานที่น่าเชื่อถือที่จะสนับสนุนการใช้ดังกล่าว[20][21] ผลจากการรักษาเยื่อบุหัวใจอักเสบติดเชื้อเอนเทอโรคอกคอลมีความแปรผัน บางกรณีศึกษาประสบผลสำเร็จในการรักษา และบางกรณีศึกษาก็ไม่พบการตอบสนองต่อการรักษาดังกล่าว[22][23][24][25][26][27] หลักฐานสนับสนุนในระดับต่ำถึงปานกลางยังใช้ยานี้ต่อการติดเชื้อในกระดูกและข้อ รวมไปถึงโรคกระดูกอักเสบเรื้อรัง แม้ว่าอาการอันไม่พึงประสงค์จากยาจะมีนัยสำคัญซึ่งต้องพิจารณาเมื่อสั่งใช้ยาในระยะยาว[28][29][30][31][32][33]
ใการรักษาร่วมกับยาอื่น ไลนีโซลิดนำมาใช้ในการรักษาวัณโรค[34] ขนาดยาที่เหมาะสมสำหรับการรักษายังมิได้กำหนดขึ้น ในผู้ใหญ่พบว่าการให้ยาวันละครั้งหรือสองครั้งได้ผลที่ดี ในแผนการรักษาระยะเวลาหลายเดือนมักต้องพิจารณาอัตราการเกิดอาการอันไม่พึงประสงค์จากยาในขนาดยาที่สูง[35][36] ปัจจุบันยังไม่มีหลักฐานที่เชื่อถือได้ถึงประสิทธิภาพและความปลอดภัยสนับสนุนข้อบ่งใช้ดังกล่าว[7]
การศึกษายาไลนีโซลิดในฐานะยาทางเลือกของแวนโคมัยซินนการรักษาไข้เหตุนิวโตรฟิลในเลือดต่ำในผู้ป่วยมะเร็งเมื่อตรวจพบการติดเชื้อแกรมบวก[37] นอกจากนี้ยังเป็นหนึ่งในยาปฏิชีวนะไม่กี่ขนานที่แพร่ผ่านน้ำวุ้นช่องลูกตาหลังจึงสามารถรักษาการอักเสบลูกตาอันเนื่องมาจากการติดเชื้อแบคทีเรีย ซึ่งมีหลักฐานสนับสนุนจำนวนน้อยซึ่งปัจจุบันนิยมรักษาการอักเสบลูกตาด้วยยาแวนโคมัยซินโดยการฉีดเข้าสู่ตาโดยตร[12]
การติดเชื้อในระบบประสาทส่วนกลาง
[แก้]ในการศึกษาสัตว์ที่เป็นโรคเยื่อหุ้มสมองอักเสบจากการติดเชื้อสเตร็ปโตคอกคัส นูโมนิเอ (Streptococcus pneumoniae) พบว่ายาไลนีโซลิดสามารถแพร่ผ่านน้ำหล่อสมองไขสันหลัง (cerebrospinal fluid) แต่ประสิทธิภาพในการรักษาต่ำกว่าการใช้ยาปฏิชีวนะขนานอื่นๆ[38][39] ปัจจุบันยังไม่มีหลักฐานมากพอในการสนับสนุนให้ใช้ยาไลนีโซลิดในการรักษาเยื่อหุ้มสมองอักเสบจากการติดเชื้อแบคทีเรีย อย่างไรก็ดียานี้ได้ใช้รักษาการติดเชื้อในระบบประสาทส่วนกลางในหลายกรณีศึกษา ]] ซึ่งรวมไปถึงโรคเยื่อหุ้มสมองอักเสบจากการติดเชื้อแบคทีเรีย และมีข้อแนะนำให้ใช้อย่างสมเหตุสมผลในข้อบ่งใช้เมื่อการรักษาด้วยทางเลือกอื่นล้มเหลว[40][41] ข้อแนะนำจากสมาคมโรคติดเชื้อแห่งสหรัฐอเมริกาแนะนำให้ใช้ไลนีโซลิดเป็นยาขนานแรกสำหรับการรักษาเยื่อหุ้มสมองอักเสบจากการติดเชื้อ VRE และเป็นทางเลือกสำหรับการใช้่ยาแวนโคมัยซินสำหรับการรักษษเยื่อหุ้มสมองอักเสบจากการติดเชื้อ MRSA[42] ไลนีโซลิดมีฤทธิ์เหนือกว่าแวนโคมัยซินในการรักษาการติดเชื้อ MRSA ที่ระบบประสาทส่วนกลางชุมชน แม้ว่าจะมีกรณีศึกษาไม่มากนักที่ได้รับการตีพิมพ์ (อ้างอิงปี ค.ศ. 2009).[43]
การติดเชื้อที่เกี่ยวกับสายสวนหลอดเลือด
[แก้]ในเดือนมีนาคม ค.ศ. 2007 องค์การอาหารและยา ประเทศสหรัฐอเมริการายงานผลการศึกษาทางคลินิกระยะที่ 3 โดยใช้วิธีการวิจัยเชิงทดลองแบบสุ่มและมีกลุ่มควบคุมเปรียบเทียบยาไลนีโซลิดกับแวนโคมัยซินในการรักษาการติดเชื้อในกระแสเลือดที่เกี่ยวข้องกับสายสวนหลอดเลือด ผู้ป่วยที่รักษาด้วยยาแวนโคมัยซินควรเปลี่ยนไปใช้ยาออกซาซิลลินหรือไดคลอกซาซิลลิน หากแบคทีเรียซึ่งเป็นเหตุของการติดเชื้อมีความไวรับและผู้ป่วยในทั้งสองกลุ่ม (ไลนีโซลิดและแวนโคมัยซิน) ควรได้รับการรักษาอย่างจำเพาะเจาะจงเพื่อต่อต้านแบคทีเรียแกรมลบหากจำเป็น[44] การศึกษาซึ่งตีพิมพ์ในเดือนมกราคม ค.ศ. 2009[45]
ไลนีโซลิดมีความสัมพันธ์กับอัตราการตายอย่างมีนัยสำคัญเมื่อเปรียบเทียบกับยาปฏิชีวนะขนานอื่นๆ ในข้อมูลส่วนน้อยพบว่ามีอัตราการตาย 21.5% ของผู้ป่วยที่ได้รับยาไลนิโซชิด เปรียเทียบกับอัตราการตาย 16% ของผู้ที่ไม่ได้รับยา ความแตกต่างเกิดเนื่องมาจากฤทธิ์การรักษาของไลนีโซลิดที่ต่ำกว่าในเชื้อแบคทีเรียแกรมลบเดี่ยวๆ หรือการติดเชื้อผสมระหว่างแบคทีเรียแกรมบวกและแกรมลบ ในอาสาสมัครที่ติดเชือแบคทีเรียแกรมบวกเดี่ยวๆ ไลนีโซลิดมีความปลอดภัยและมีประสิทธิภาพเทียบเท่าแวนโคมัยซิน[44][45] จากผลการศึกษานี้เอง องค์การอาหารและยาแห่งสหรัฐอเมริกาจึงแจ้งเตือนให้บุคลากรสาธารณสุขระวังว่ายาไลนีโซลิดไม่ได้รับการอนุมัติเพื่อรักษาการติดเชื้อแบคทีเรียแกรมลบที่เกี่ยวกับสายสวนหลอดเลือด ซึ่งควรเลือกใช้ทางรักษาอื่นเพื่อรักษษการติดเชื้อหากตรวพบหรือยืนยันว่าเป็นแบคทีเรียแกรมลบ[44]
อาการอันไม่พึงประสงค์
[แก้]เมื่อบริหารยาไลนีโซลิดในช่วงระยะเวลาสั้นๆ ถือว่ายาไลนิโซลิดมีความปลอดัยสัมพัทธ์[46] โดยปกติอาการข้างเคียงจากการบริหารไลนีโซลิด (เกิดขึ้นกับผู้บริหารยาไลนีโซลิดมากกว่า 1%) คือท้องเสีย (มีรยงาน 3-11% ของอาสาสมัครขั้นทดสอบทางคลินิก) ปวดศีรษะ (1–11%) เวียนศีรษะ (3–10%) อาเจียน (1–4%) ผื่นแดง (2%) ท้องผูก (2%) การรับรสเปลี่ยนไป (1–2%) และลิ้นสีซีด (0.2–1%)[2] การติดเชื้อราทางช่องปากอย่างแคนดีดา (oral candidiasis) และช่องคลอด (vaginal candidiasis) อาจเกิดขึ้นได้จากฤทธิ์การกดแบคทีเรียตามธรรมชาติในร่างกาย (normal bacterial flora) และเปิดช่องให้เกิดการติดเชื้อรา[2] อาการไม่พึงประสงค์อื่นๆที่พบได้เล็กน้อย (และรุนแรงกว่า) ประกอบไปด้วยเกิดภูมิแพ้, ตับอักเสบและกาเพิ่มสูงขึ้นของเอนไซม์ทรานซามีเนสส์ (elevated transaminases) ซึ่งเป็นสัญลักษณ์ของไตที่ถูกทำลาย[2][47] ไลนีโซลิดมีความแตกต่างจากยาปฏิชีวนะอื่นๆ อย่างอีริโทรมัยซินและควิโนโลน คือไม่ก่อให้เกิดผลต่อช่วงคิวที (QT interval) ซึ่งวัดได้จากการตรวจคลื่นไฟฟ้าหัวใจ[47][48] Adverse effects in children are similar to those that occur in adults.[48]
ไลนีโซลิดมีความสัมพันธ์กับการเกิดท้องเสียจาก Clostridium difficile (CDAD) และลำไส้อักเสบท้องเสีย (pseudomembranous colitis) เช่นเดียวกับยาปฏิชีวนะขนานอื่นๆ ซึ่งแม้จะเป็นความผิดปกติแต่เกิดขึ้นเพียงหนึ่งในสองพันในขั้นตอนการทดสอบทางคลินิก[2][47][48][49] C. difficile มีความไวต่อไลนีโซลิดจากการทดลองในหลอดทดลอง (in vitro) และไลนิโซลิดยังได้รับการพิจารณาในการรักษา CDAD อีกด้วย[50]
ใน ค.ศ. 2009 ไลนีโซลิดเป็นยาที่ติดเครื่องหมายสามเหลี่ยมดำ (black triangle drug) ในสหราชอาณาจักร คือเป็นยาที่อยู่ในขั้นตอนการตรวจสอบหลังวางตลาดอย่างเข้มงวดโดยคณะกรรมการยามนุษย์โดยหน่วยงานกำกับยาและผลิตภัณฑ์สุขภาพของรัฐ[6]
การบริหารยาในระยะยาว
[แก้]ใการบริหารยาไลนีโซลิดอาจก่อให้เกิดอาการอันไม่พึงประสงค์คือการกดไขกระดูก (Bone marrow suppression) โดยแสดงผลทางคลินิกภาวะเกล็ดเลือดต่ำ ซึ่งอาการดังกล่าวเกิดขึ้นอย่างมีนัยสำคัญเมื่อบริหารยาขนานนี้เมื่อเปรียบเทียบกับยากลุ่มอื่นอย่างไกลโคเพปไทด์และเบต้าแลกแทม[8] แต่ทว่าอาการดังกล่าวถือเป็นภาวะที่ผิดปรกติหากผู้ป่วยบริหารยาในช่วง 14 วันหรือน้อยกว่า แต่ความเสี่ยงจะเพิ่มากขึ้นตามระยะเวลาการบริหารยาหรือผู้ป่วยไตล้มเหลว[47][51] ผลการรายงานกรณีศึกษาในปี ค.ศ. 2004 แนะนำว่าการให้ไพริโดซีน (รูปของวิตามินบี6) อาจช่วยย้อนกลับผลของภาวะเลือดจางและเกล็ดเลือดต่ำจากการบริหารยาไลนีโซลิดได้[52] แต่ต่อมา การศึกษาที่ใหญ่ขึ้นพบว่าไม่ได้มีผลทางบวกแต่อย่างใด[53]
การบริหารยาไลนีโซลิดในระยะยาวม่ีความสัมพันธ์กับอาการชาของเส้นประสาทส่วนปลาย (peripheral neuropathy) และเส้นประสาทตา (optic neuropathy) ซึ่งถือเป็นอาการปกติหากบริหารยาในช่วงหลายเดือนและอาจผันกลับได้[54][55][56][57][58] แม้ว่ากลไกการเกิดการบาดเจ็บยังไม่กระจ่างชัด มีการสันนิษฐานว่าอาจเกิดจากความเป็นพิษของไมโทคอนเดรีย[59][60] ไลนีโซลิดเป็นพิษต่อไมโทคอนเดรียอาจเนื่องมาจากความคล้ายคลึงระหว่างไมโทรคอนเดรียและไรโบโซมของแบคทีเรีย[61] ภาวะเลือดเป็นกรดแล็กติกซึ่งก่อให้เกิดอันตรายถึงชีวิตได้ ก็อาจเกิดขึ้นได้จากความเป็นพิษของไมโทคอนเดรียเช่นกัน[59] เนื่องมาจากผลจากการบริหารยาระยะยาว ผู้ผลิตจึงแนะนำให้ตรวจเม็ดเลือดอย่างสัมบูรณ์สัปดาห์ละครั้งระหว่างการบริหารยาขนานนี้เพื่อควบคุมการกดไขกระดูกและแนะนำให้รักษาไม่เกิน 28 วัน[1][47] วิธีการติดตามควบคุมผลการรักษาเพิ่มเติมสำหรับผู้ป่วยที่เกิดพิษอย่างรุนแรงจากการได้รับยาไลนีโซลิดได้พัฒนาขึ้นโดยกลุ่มวิจัยในเมลเบิร์น ประเทศออสเตรเลีย วิธีการดังกล่าวประกอบด้วยการตรวจเลือดและการตรวจการทำงานของตับทุก 2 สัปดาห์ โดยการวัดระดับของเซรั่มแล็กเตด (serum lactate) เพื่อค้นหาการเกิดภาวะเลือดเป็นกรดแล็กติก การทบทวนวรรณกรรมจากยาที่ผู้ป่วยที่ได้รับทุกขนานและอาจเกิดอันตรกิริยากับไลนีโซลิดยา อาทิ ปัญหาด้านการมองเห็นและระบบประสาทชั่วคราวในผู้ป่วยที่ได้รับยาไลนีโซลิดมากกว่า 4 สัปดาห์[62]
อาการอันไม่พึงประสงค์สำหรับการบริหารยาไลนีโซลิดในระยะยาวครั้งแรกที่พบในขั้นการทดลองหลังการวางตลาด (postmarketing surveillance) การกดไขกระดูกไม่พบในการทดลองทางคลินิกระยะที่สาม ซึ่งการบริหารยาในช่วงดังกล่าวใช้ไม่เกิน 21 วัน แม้ว่าผู้เข้าร่วมทดสอบจะมีภาวะเกล็ดเลือดน้อยก็ตาม พบว่าสามารถผันกลับได้และไม่ได้เกิดขึ้นบ่อยครั้งจนมีนัยสำคัฯญมากกว่ากลุ่มควบคุม (ผู้ป่วยที่ไม่ได้บริหารด้วยยาไลนีโซลิด)[38] ไม่มีรายงานหลังวางตลาดเกี่ยวกับการชักและมีเพียงผู้ป่วยรายเดียวใปี ค.ศ. 2009 ที่เกิดการอัมพาตแบบเบลล์ (คือไม่สามารถควบคุมระบบประสาทบนใบหน้าแลัเกิดพิษในไต)[48]
อันตรกิริยา
[แก้]ไลนีโซลิดเป็นสารยับยั้งโมโนเอมีนออกซิเดส (monoamine oxidase inhibitor; MAOI) อย่างอ่อนและไม่ควรใช้ร่วมกับยา MAOIs อื่นๆ รวมถึงอาหารที่มีไทรามีนปริมาณมาก (เช่น เนื้อหมู, ชีส, เครื่องดื่มแอลกอฮอล์, อาหารรมควัน) และยากลุ่มเซโรโทนิน มีรายงานการทดสอบหลังการวางตลาด (postmarketing surveillance) ของกลุ่มอาการเซโรโทนิน เมื่อให้ไลนีโซลิดร่วมกับยาพวกซีโรโตเนอร์จิกหรือการให้หลังหยุดยาเพียงช่วงเวลาสั้นๆ โดยเฉพาะยาพวกยับยั้งการดูดกลับของซีโรโตนินอย่างจำเพาะ (selective serotonin reuptake inhibitor) อย่างพาโรซีทีนและเซอร์ทราไลน์[47][63][64][65] ปริมาณยาอาจทำให้ความดันโลหิตสูงขึ้น ทำให้มีผลกับยาจำพวกซิมพาโธมิมีติก เช่น ซูโดเอฟีดรีนและฟีนิลโพรพาโนลาไมน์[38][66] ยาไลนิโซลิดยังไม่ควรให้ร่วมกับเพธิดีน (มีเพอริดีน) เนื่องจากมีความเสี่ยงต่อการเกิดภาวะกลุ่มอาการเซโรโทนิน
ไลนีโซลิดไม่มีผลการยับยั้งหรือเพิ่มระบบเอนไซม์ไซโตโครม พี450 (CYP) ซึ่งมีผลต่อการเมทาบอลิซึมยาส่วนใหญ่ ดังนั้นจึงไม่มีอันตรกิริยาเกี่ยวกับเอนไซม์ดังกล่าว[1]
องค์การอาหารและยาของสหรัฐอเมริกาได้รับรายงานเกี่ยวกับระบบประสาทส่วนกลาง (CNS) ที่มีความรุนแรงจากปฏิกิริยาเมื่อให้ยาไลนีโซลิดในผู้ป่วยที่กำลังบริหารยากลุ่มจิตเวชซึ่งทำงานเกี่ยวกับสารเซโรโทนินในสมอง[67]
กลไกการออกฤทธิ์
[แก้]
ออกซาโซลิดิโนนเป็นกลุ่มยับยั้งการสังเคราะห์โปรตีน โดยการยับยั้งการเจริญเติบโตและการเพิ่มจำนวนของแบคทีเรียโดยการขัดขวางกระบวนการแปลรหัสพันธุกรรมของเอ็มอาร์เอ็นเอ (mRNA) สู่โปรตีนในไรโบโซม แม้ว่ากลไกการออกฤทธิ์จะไม่ได้เข้าใจอย่างกระจ่างชัด[68] สันนิษฐานว่าไลนีโซลิดออกฤทธิ์ที่ขั้นตอนแรกของการสังเคราะห์โปรตีน ไม่เหมือนกับยายับยั้งการสังเคราะห์โปรตีนขนานอื่นๆที่ยับยั้งในขั้นตอนการต่อสายรหัสพันธุกรรม (elongation)[69][70]
ยาออกฤทธิ์โดยป้องกันการสร้าง "สารประกอบเริ่มต้น" ('initiation complex) อันประกอบไปด้วยซับยูนิตของไรโบโซม 30เอส (30s) 50เอส (50s) ทีอาร์เอ็นเอ (tRNA) และเอ็มอาร์เอ็นเอ (mRNA) ไลนิโซลิดจับกับซับยูนิต 23เอส ของไรโบโซมซึ่งเป็นส่วนของซับยูนิต 50เอส (ศูนย์กลางเอนไซม์เปปติดิลทรานส์เฟอเรส (peptidyl transferase))[71] จับกับบริเวณรับ (binding site) ของยาคลอแรมฟินีคอล ลินโคมัยซิน และยาปฏิชีวนะอื่นๆ เนื่องจากกลไกการออกฤทธิ์อันโดดเด่น การดื้อต่อยาข้ามกลุ่มระหว่างไลนีโซลิดกับยากลุ่มยับั้งการสังเคราะห์โปรตีนขนานอื่นๆจึงพบได้ไม่บ่อยหรือไม่พบเลย[7][38]
ในปี ค.ศ. 2008 โครงสร้างแบบผลึกของไลนีโซลิดจับกับซับยูนิต 50เอสของไรโบโซมจากอาร์เคีย Haloarcula marismortui ได้รับการแถลงโดยกลุ่มนักวิทยศาสตร์จากมหาวิทยาลัยเยลและก็บข้อมูลไปยังธนาคารข้อมูลโปรตีน (Protein Data Bank)[72] กลุ่มวผู้วิจัยอื่นในปีเดียวกันนี้ได้อธิบายโครงสร้างไลนีโซลิดที่จับกับซับยูนิต 50เอส ของ Deinococcus radiodurans ผู้วิจัยคาดหวังถึงแบบจำลองแสดงกลไกการออกฤธิ์ของกลุ่มออกซาโซลิดิโนน พบว่าไลนีโซลิดจับกับบริเวณเอของไรโบโซมซับยูนิต 50เอส รวมไปถึงการเปลี่ยนแปลงโครงสร้างโมเลกุล (conformational change) เพื่อป้องกันทีอาร์เอ็นเอ (tRNA) เข้าสู่เป้าหมายและบังคับให้ทีอาร์เอ็นเอแยกออกจากไรโบโซม[73]
เภสัชเคมี
[แก้]ณ ค่าพีเอชทางสรีรวิทยา ไลนีโซลิดอยู่ในรูปไม่เปลี่ยนรูป ละลายน้ำได้ปานกลาง (ประมาณ 3 มิลลิกรัม/มิลลิลิตร) โดยมีค่าสัมประสิทธิ์การแยก (partition coefficient: logP) ที่ 0.55[7]
![Skeletal formula of N-{[(5S)-3-[3-fluoro-4-(morpholin-4-yl)phenyl]-2-oxo-1,3-oxazolidin-5-yl]methyl}acetamide, highlighting the morpholino and fluoro groups in orange, with the rest in blue. The carbon atoms of the parent chain are numbered.](http://upload.wikimedia.org/wikipedia/commons/thumb/e/ea/Linezolid_showing_oxazolidinone_pharmacophore.svg/220px-Linezolid_showing_oxazolidinone_pharmacophore.svg.png)
ส่วนของโครงสร้างที่ออกฤทธิ์ (pharmacophore) ของออกซาโลลิดิโนนเป็นแม่แบบสำคัญของการออกฤทธิ์ต้านเชื้อแบคทีเรีย ประกอบไปด้วยหมู่ฟังก์ชัน 1,3-oxazolidin-2-one ประกอบกับหมู่แอริล ณ ตำแหน่งที่ 3 และ S-หมู่เมทิล และหมู่แทนที่อื่นๆ ประกอบกัน และในตำแหน่งที่ 5 (R-อีแนนทิโอเมอร์ ของออซาโซลินิโนนส์ไม่มีฤทธิ์เป็นยาต้านแบคทีเรีย)[74] นอกจากนี้ในแก่นสำคัญของโครงสร้าง ไลนีโซลิดประกอบไปด้วยคุณลักษณะโครงสร้างที่พัฒนาประสิทธภาพและความปลอดภัย หมู่แทนที่อะเซตาไมด์ที่ตำแหน่งที่ 5 หมู่เมทิล (5-methyl group) เป็นหมู่ที่ดีที่สุดในเชิงประสิทธิภาพในการเป็นยาต้านแบคทีเรีย ซึ่งถูกใช้เป็นหมู่แทนที่ในยากลุ่มออกซาโซลิดิโนนทุกขนาน ในความเป็นจริงแล้วยิ่งหมู่แทนที่แทนทีในตำแหน่งที่ไกลจากหมู่อะเซตาไมด์เท่าใด ก็ยังผลให้สูญเสียฤทธิ์การเป็นยาต้านแบคทีเรียเท่านั้น แม้ว่าฤทธิ์อย่างอ่อนถึงปานกลางอาจเกิดขึ้นเมื่อใช้หมู่ไบโอสเตียร์ อะตอมของฟลูออรีน ณ ตำแหน่งที่ 3' มีฤทธิ์เป็นสองเท่าทั้งในผลการทดลองจากหลอดทดลอง (in vitro)และในสัตว์ทดลอง (in vivo) และอะตอมไนโตรเจนซึ่งเป็นหมู่ให้อิเล็กตรอน (electron donating) ในวงแหวนมอร์โฟลีนช่วยคงศักยภาพฤทธิ์ต้านแบคทีเรียและความปลอดภัยในเกณฑ์ที่ยอมรับได้[19][74]
ริวาโรซาบาน (rivaroxaban: Xarelto) ยาต้านการแข็งตัวของเกล็ดเลือดมีโครงสร้างเคมีคล้ายคลึงกับไลนีโซลิด ทั้งสองมีหมู่ออกฤทธิ์เดียกันคือออกซาโซลิดิโนน แตกต่างกันในสามบริเวณ (หมู่คีโตนเพิ่มเติม, คลอโรไทโอฟันและอะตอมฟลูออรีนที่หายไป) อย่างไรก็ดีโครงส้รางที่คล้ายคลึงดังกล่าวไม่ได้มีนัยสำคัญทางคลินิกแต่อย่างใด[75]
การสังเคราะห์
[แก้]ไลนีโซลิดเป็นยาสังเคราะห์โดยสัมบูรณ์ คือไม่เกิดขึ้นตามธรรมชาติ (ต่างจากอีริโทรมัยซินและยาปฏิชีวนะขนานอื่นๆ) และไม่ได้พัฒนาขึ้นจากโครงสร้างตามธรรมชาติ (ต่างจากพวกเบต้าแลกแตมซึ่งเป็นยากึ่งสังเคราะห์) มีวิถีการสังเคระห์ไลนีโซลิดมากมายที่ถูกตีพิมพ์เผยแพร่ในวงเภสัชกรรม[74][76] แม้ว่าปริมาณที่สังเคราห์ได้จำนวนมากเกิดจากการใช้วิถีดั้งเดิม (พัฒนาขึ้นโดยอัฟจอห์นสำหรับการผลิตระดับอุตสาหกรรม (pilot scale) ของยาไลนีโซลิดและอีพีรีโซลิด) ซึ่งต้องใช้สารเคมีราคาสูงอย่างเช่นแพลลาเดียมบนคาร์บอน และสารทำปฏิกิริยาความไวสูงอย่างเมทานีซัลโฟนิลคลอไรด์ (methanesulfonyl chloride) และเอ็น-บิวมิลลีเทียม (n-butyllithium) และสภาอุณหภูมิต่ำตลอดการผลิต[74][76][77] ราคาที่สูงของไลนีโซลิดมาจากรายจ่ายการสังเคราะห์เสียส่วนใหญ่[77] ส่วนวิถีการสังเคราะห์อื่นๆที่สั้นและคุ้มค่าทางเศรษฐศาสตร์มากกว่าในการผลิตระดับอุตสาหกรรถือครองลิขสิทธิ์โดยอัปจอห์นในปี ค.ศ. 1998[19][78]
การสังเคราะห์ต่อมาได้ใช้วิธีเศรษฐศาสตร์อะตอม (atom economy)โดยเริ่มสังเคราะห์จาก ดี-แมนิทอล (D-mannitol) ซึ่งพัฒนาขึ้นโดยดร. เรดดีส์ บริษัทยาอินเดียและรายงานในปี ค.ศ. 1999[79] และวิธีซึ่งสังเคราะห์จากสารเริ่มต้น เอส-กลีเซอราลดีฮายด์ส ((S)-glyceraldehyde acetonide) ซึ่งเตรียมขึ้นจากวิตามินซี พัฒนาโดยกลุ่มวิจัยจากมหาวิทยาลัยฮูแมนนอร์มอลในเมืองฉางชา มลฑลฐหูหนาน ประเทศจีน[76] ในวันที่ 23 มิถุนายน ค.ศ. 2008 ระหว่างการประชุมประจำปีในหัวข้อเคมีและพลังงานสีเขียวครั้งที่ 12 (Green Chemistry and Engineering Conference) ในนิวยอร์ก บริษัทไฟเซอร์รายงานกาพัฒนายารุ่นที่สองของการสังเคราะห์ไลนีโซลิด ซึ่งเป็นการสังเคราะห์เคมีสีเขียวแบบคอนเวอร์เจนต์ (convergent synthesis) เริ่มต้นจาก (S)-epichlorohydrin ซึ่งให้ปริมาณสังเคราะห์สูงกว่าและมีของเสียจากการผลิตลดลงถึง 56%[80]
Pharmacokinetics
[แก้]
One of the advantages of linezolid is its high bioavailability (close to 100%) when given by mouth: the entire dose reaches the bloodstream, as if it had been given intravenously. This means that people receiving intravenous linezolid may be switched to oral linezolid as soon as their condition allows it, whereas comparable antibiotics (such as vancomycin and quinupristin/dalfopristin) can only be given intravenously.[69] Taking linezolid with food somewhat slows its absorption, but the area under the curve is not affected.[7]
Linezolid has low plasma protein binding (approximately 31%, but highly variable) and an apparent volume of distribution at steady state of around 40–50 liters.[2] Peak serum concentrations (Cmax) are reached one to two hours after administration of the drug. Linezolid is readily distributed to all tissues in the body apart from bone matrix and white adipose tissue.[19] Notably, the concentration of linezolid in the epithelial lining fluid of the lower respiratory tract is at least equal to, and often higher than, that achieved in serum (some authors have reported bronchial fluid concentrations up to four times higher than serum concentrations), which may account for its efficacy in treating pneumonia. Cerebrospinal fluid (CSF) concentrations vary; peak CSF concentrations are lower than serum ones, due to slow diffusion across the blood-brain barrier, and trough concentrations in the CSF are higher for the same reason.[7] The average half-life is three hours in children, four hours in teenagers, and five hours in adults.[1]
Linezolid is metabolized in the liver, by oxidation of the morpholine ring, without involvement of the cytochrome P450 system. This metabolic pathway leads to two major inactive metabolites (which each account for around 45% and 10% of an excreted dose at steady state), one minor metabolite, and several trace metabolites, none of which accounts for more than 1% of an excreted dose.[81] Clearance of linezolid varies with age and gender; it is fastest in children (which accounts for the shorter half-life), and appears to be 20% lower in women than in men.[1][81][82]
Use in special populations
[แก้]In adults and children over the age of 12, linezolid is usually given every 12 hours, whether orally or intravenously.[38][69] In younger children and infants, it is given every eight hours.[83] No dosage adjustments are required in the elderly, in people with mild-to-moderate liver failure, or in those with impaired kidney function.[2] In people requiring hemodialysis, care should be taken to give linezolid after a session, because dialysis removes 30–40% of a dose from the body; no dosage adjustments are needed in people undergoing continuous hemofiltration,[2] although more frequent administration may be warranted in some cases.[7] According to one study, linezolid may need to be given more frequently than normal in people with burns affecting more than 20% of body area, due to increased nonrenal clearance of the drug.[84]
Linezolid is in U.S. pregnancy category C, meaning there have been no adequate studies of its safety when used by pregnant women, and although animal studies have shown mild toxicity to the fetus, the benefits of using the drug may outweigh its risks.[1] It also passes into breast milk, although the clinical significance of this (if any) is unknown.[85]
ช่วงของฤทธิ์การรักษา
[แก้]ไลนีโซลิดมีฤทธิ์ต่อเชื้อแบคทีเรียแกรมบวกทุกชนิดซึ่งผนังเซลล์ประกอบไปด้วยเปปติโดกลัยแคนและไม่มีเยื่อเลือกผ่านชั้นนอก เช่นสายพันธุ์ Enterococcus faecium และ Enterococcus faecalis (ซึ่งประกอบด้วยเชื้อเอนเทอโรคอกคัสที่ดื้อต่อยาแวนโคมัยซิน), Staphylococcus aureus (ซึ่งประกอบด้วยเชื้อสแตรฟิโลคอกคัส แอเรียสที่ดื้อต่อยาเมธิซิลลิน, MRSA) Streptococcus agalactiae, Streptococcus pneumoniae, Streptococcus pyogenes, กลุ่มไวริแดนส์ของสเตร็ปโตคอกไค , Listeria monocytogenes และ [[โครีนีแบคทีเรียมล] (โดยเชื้อมีความไวต่อยาไลนีโซลิดโดยมีค่า MIC หรือค่าความเข้มข้นที่ต่ำที่สุดที่มีฤทธิ์ยับยั้งเชื้อโดยให้เป็นปกติที่ต่ำกว่า 0.5 mg/L)[1][38][86] ไลนีโซลิดมีฤทธิ์อย่างมากต่อเชื้อมายโคแบคทีเรียมในการทดลองนอกกายมนุษย์ (in vitro)[38] และมีประสิทธิภาพอย่างมทากต่อ โนคาร์เดีย แต่มีราคาที่สูงและมีเหตุการณ์อันไม่พึงประสงค์เกิดขึ้นได้มาก โดยมีการแนะนำให้ใช้ร่วมกับยาปฏิชีวนะขนานอื่นๆหรือใช้ในเฉพาะผู้ป่วยที่ล้มเหลวจากการักษษด้วยยาแบบดั้งเดิม[87]
ไลนีโซลิดมีฤทธิ์ยับยั้งการสืบพันธุ์หรือการเติบโตต่อแบคทีเรียต่อสิ่งมีชีวิตส่วนใหญ่ โดยไม่ได้ฆ่าแบคทีเรียโดยตรง (bacteristatic) แต่มีฤทธิ์ในการฆ่าเชื้อแบคทีเรียโดยตรง (bactericidal) ต่อเชื้อจำพวก สเตร็ปโตคอกไค[1][88] บางงานวิจัยพบว่าแม้ว่าไลนีโซลิดจะมีฤทธิ์ยับยั้งการเติบโตและการสิบพันธุ์ในการทดลองนอกกายมนุษย์นั้น (in vitro) แต่ไลนีโซลิดมีพฤติกรรมในการฆ่าเชื้อบแคทีเรียโดยตรงในการทดลองในกายมนุษย์ (in vivo) ด้วยเหตุผลการยับยั้งการผลิตพวกสารพิษโดนสแตรฟิโลคอกไคและสเตร็ปโตคอกไค[19] ไลนีโซลิดยังมีผลหลังการใช้ยาปฏิชีวนะ (post-antibiotic effect) 1-4 ชั่วโมงในแบคทีเรียส่วนใหญ่ หมายความว่าการเติบโตของแบคทีเรียได้รับการกดไว้ชั่วคราวแม้จะหยุดยาแล้วก็ตาม[7]
แบคทีเรียแกรมลบ
[แก้]ไลนิโซลิดไม่มีผลทางคลินิกอย่างมีนัยสำคัญกับเชื้อแบคทีเรียแกรมลบโดยส่วนใหญ่ ไม่ได้ผลกับเชื้อสกุล Pseudomonas และเชื้อวงศ์ Enterobacteriaceae[88] In vitro, it is active against Pasteurella multocida,[1][89] Fusobacterium Moraxella catarrhalis Legionella Bordetella และ Elizabethkingia meningoseptica มีฤทธิ์ปานกลาง (ความเข้มข้นยาต่ำสุดในการยับยั้งการเติบโต (MIC) สำหรับเชื้อร้อยละ 90 อยู่ที่ 8 มิลลิกรัมต่อลิตร) ต่อ Haemophilus influenzae.[85][88] ยาขนานนี้ยังใช้เป็นยาอันดับสองในการรักษาการติดเชื้อ Capnocytophaga[40][90]
การเปรีบเทียบกับยาปฏิชีวนะอื่น
[แก้]ช่วงการรักษาไลนีโซลิดต่อแบคทีเรียแกรมบวกมีความคล้ายคลึงกับยาปฏิชีวนะกลุ่มไกลโคเปปไท์ แวนโคมัยซิน ซึ่งเป็นยามาตรฐานการรักษาการติดเชื้อ MRSA มาอย่างยาวนาน ซึ่งมักนำยาสองขนานนี้มาเปรีบเทียบกัน[7][46] ส่วนยาปฏิชีวนะอื่นๆ ที่มีการนำมาเปรียบเทียบได้แก่ทโคพลานิน (ชื่อการค้า Targocid เป็นยากลุ่มไกลโคเปปไทด์เช่นเดียวกับแวนโคมัยซิน) ควินูพริสทิน/ดาลโฟพริสทิน (ยารวมกันของสเต็ปโคกรามินสองชนิด ไม่มีฤทธิ์ต่อ E. faecalis)[91] และแดบโทมัยซิน (คูบิซิน ซึ่งเป็นสารไลโปเปปไทด์ และยาอื่นๆที่มีการพัฒนาเช่น เซปโตบิโพรล ดาลบาแวนซิน และทีลาแวนซิน ไลนีโซลิดเป็นยาขนานเดียวที่สามารถบริหารทางปากได้[7] ในอนาคตยาโอริทาแวนซินและไอคลาพริมอาจเป็นทางเลือกในการใช้ยาไลนีโซลิดซึ่งยาทั้งสองอยู่ในขั้นตอนการพัฒนาระยะแรกของการทดสอบทางคลินิก[7]
การดื้อยา
[แก้]การดื้อต่อยาไลนีโซลิดเริ่มมีรายงานแต่ต้น ค.ศ. 1999 ในผู้ป่วยขั้นรุนแรงสองรายที่ติดเชื้อ Enterococcus faecium ซึ่งดื้อต่อยาหลายขนานและได้ใช้โปรแกรมการรักษาทางเลือก (expanded access)[88] การดื้อต่อยาไลนีโซลิดของเชื้อ Staphylococcus aureus พบเมื่อปี ค.ศ. 2001[92]
ในสหรัฐอเมริกาการดื้อต่อยาไลนีโซลิดได้มีการติดตามและบันทึกตั้งแต่ ค.ศ. 2004 เมื่อใช้โปรแกรม LEADER ซึ่งในปี คงศ. 2007 ได้รับแนะนำโดยสถาบันทางการแพทย์กว่า 60 แห่งทั่วประเทศ การดื้อยาเป็นเป็นอย่างคงที่และเพิ่มอย่างช้าๆ น้อยกว่า 1% ของกลุ่มตัวอย่างที่ติดเชื้อ S. aureus[93] "การศึกษาประสิทธิศักย์และความกว้างการรักษาของยาไซว็อกซ์" โปรแกรมระดับโลก (Zyvox Annual Appraisal of Potency and Spectrum Study: ZAAPS) เริ่มต้นขึ้นใปี ค.ศง 202 ในปี ค.ศ. 207 การดื้อยาโดยรวมใน 23 ประเทศทั่วโลกน้อยกว่า 0.2% แลพไม่พบการดื้อต่อพวกสเตร็ปโตคอกไค (streptococci) การดื้อยาพบเพียงเฉพาะในประเทศบราซิล จีน ไอร์แลนด์ อิตาลี ของเชื้อสแตรฟิโลคอกคัส(Staphylococcus) โดยพบการดื้อยา 0.28% ของกลุ่มตัวอย่าง เอนเทอโรคอกไค 0.11% และ S. aureus 0.03%[94] ในสหราชอาณาจักรและไอร์แลนด์ไม่พบการดื้อยาของเชื้อสแตรฟิโลคอกคัสที่เก็บจากผู้ป่วยติดเชื้อแบคทีเรียตั้งปต่ปี ค.ศ. 2001 ถึง 2006[95] แต่พบรายงานการดื้อยาของเชื้อเอนเทอโรคอกไค[96] ผู้วิจัยบางคนทำนายว่าการดื้อของเชื้อ E. faecium ต่อไลนีโซลิดจะเพิ่มขึ้นหากใช้อย่างต่อเนื่องในปริมาณปัจจุบันหรือการใช้เพิ่มขึ้น[97]
กลไก
[แก้]การดื้อยาภายในของเชื้อแบคทีเรียแกรมลบต่อไลนีโซลิดเกิดเนื่องมาจากการผลักยาออกจากเซลล์ซึ่งการผลักออกจากเซลล์กระทำได้รวดเร็วกว่าการสะสมยาสู่เซลล์[19][98]
แบคทีเรียแกรมบวกมักพัฒนาการดื้อต่อยาไลนีโซลิดอันเป็นผลจากกระบวนการกลายพันธุ์ของยีนในตำแหน่ง G2576T ซึ่งเบสกัวนีนจะแทนที่เบสไทอามีนในคู่เบส 2576 ของการถอดรหัสการสร้าง 23เอส ไรโบโซมของอาร์เอ็นเอ[99][100] ซึ่งเป็นกลไกปกติโดยส่วนใหญ่ของการดื้อต่อยาของเชื้อสแตรฟิโลคอกคัส และเชื้อ E. faecium[97] กลไกการดื้อยาอื่นๆได้รับการชี้ชัดจากเชื้อ Streptococcus pneumoniae (รวมไปถึงการกลายพันธุ์ของอาร์เอ็นเอเมทิลทรานส์เฟอเรสที่เมทิลเลตส์ จี2445 (methylates G2445) ของ 23เอส อาร์อาร์เอ็นเอ (23S rRNA) และการกลายพันธุ์เป็นเหตุให้เพิ่มการแสดงออกของยีนของเอบีซีทรานส์พอร์เตอร์[101] และใน Staphylococcus epidermidis[102][103]
History
[แก้]The oxazolidinones have been known as monoamine oxidase inhibitors since the late 1950s. Their antimicrobial properties were discovered by researchers at E.I. duPont de Nemours in the 1970s.[74] In 1978, DuPont patented a series of oxazolidinone derivatives as being effective in the treatment of bacterial and fungal plant diseases, and in 1984, another patent described their usefulness in treating bacterial infections in mammals.[38][74] In 1987, DuPont scientists presented a detailed description of the oxazolidinones as a new class of antibiotics with a novel mechanism of action.[74][104] Early compounds were found to produce liver toxicity, however, and development was discontinued.[91]
Pharmacia & Upjohn (now part of Pfizer) started its own oxazolidinone research program in the 1990s. Studies of the compounds' structure–activity relationships led to the development of several subclasses of oxazolidinone derivatives, with varying safety profiles and antimicrobial activity. Two compounds were considered drug candidates: eperezolid (codenamed PNU-100592) and linezolid (PNU-100766).[19][47] In the preclinical stages of development, they were similar in safety and antibacterial activity, so they were taken to Phase I clinical trials to identify any difference in pharmacokinetics.[91][105] Linezolid was found to have a pharmacokinetic advantage—requiring only twice-daily dosage, while eperezolid needed to be given three times a day to achieve similar exposure—and therefore proceeded to further trials.[19] The U.S. Food and Drug Administration (FDA) approved linezolid on April 18, 2000.[106] Approval followed in Brazil (June 2000),[107] the United Kingdom (January 2001),[6][47] Japan and Canada (April 2001),[108][109][110] Europe (throughout 2001),[111] and other countries in Latin America and Asia.[109]
ข้อมูลเมื่อ 2009[update], linezolid is the only oxazolidinone antibiotic available.[112] Other members of this class have entered development, such as posizolid (AZD2563),[113] ranbezolid (RBx 7644),[114] torezolid (TR-701),[112][115] and radezolid (RX-1741).[116]
เศรษฐศาสตร์
[แก้]ไลนีโซลิดจัดเป็นยาที่มีราคาสูงสำหรับการรักษา โดยคอร์สการรักษาอาจใช้ค่าใช้จ่ายถึงหนึ่งพันถึงสองพันเหรียญดอลลาร์สหรัฐสำหรับยาขนานนี้เพียงขนานเดียว[2] ซึ่งยังไม่รวมค่าใช้จ่ายอื่นๆ (อาทิ ค่าเข้ารับการรักษาในโรงพยาบาล) อย่างไรก็ดี เนื่องจากการเปลี่ยนวิธีการบริหารยาไลนีโซลิดจากการฉีดเข้าหลอดเลือดดำเป็นทางปาก (ยาเม็ดหรือยาน้ำ) โดยไม่มีผลต่อประสิทธิภาพการรักษานั้น ผู้ป่วยอาจอกจากโรงพยาบาลได้เร็วขึ้นและทำการรักษาต่อที่บ้านซึ่งไม่มีการฉีดเข้าหลอดเลือดดำ[3] การลดระยะเวลาการพักรักษาในโรงพยาบาลก็ช่วยลดค่าใช้จ่ายรวมของการรักษาแม้ไลนีโซลิดจะมีราคาสูงก็ตามเมื่อเปรียบเทียบกับาปฏิชีวนะขนานอื่นๆ
การศึกษาพบว่าในหลายประเทศที่มีระบบสาธารณสุขแตกต่างกันในการประเมินความคุ้มค่าและประสิทธิผลของไลนีโซลิดเปรียบเทียบกับไกลโคเพปไทด์อย่างแวนโคมัยซินและทีโคพลานิน ประเทศส่วนใหญ่จัดให้ไลนีโซลิดมีความคุ้มค่าเมื่อเปรียบเทียบกับยาปฏิชีวนะขนานอื่นๆ ใการรักษาโรคปอดบวมชนิดที่ต้องเข้ารับการรักษาในโรงพยาบาล และการติดเชื้อซ้ำซ้อนที่ผิวหนังหรือโครงสร้างผิวหนัง เนื่องมาจากอัตราการรอดชีวิตและการรักษาที่สูงและค่าการรักษาพยาบาลโดยรวมที่ต่ำกว่า[3]
ในปี ค.ศ. 2009 บริษัทไฟเซอร์เสียค่าใช้จ่าย 2.3 พันล้านเหรียญสหรัฐและเข้าร่วมข้อตกลงความร่วมมือในการเรียกเก็บเงินของรัฐ เนื่องมาจากการปลอมตราสินค้าและการโฆษณายาสี่ขนานอย่างผิดกฎหมาย เนื่องมาจากความล้มเหลวในการอ้างอิงโปรแกรมสุขภาพของรัฐบาลในยาที่ยังมิได้รับการยอมรัย[117] ประกอบด้วย 1.3 พันล้านเหรียญสหรัฐในการปฏิบัติผิดกฎหมายอาชญากรรมการโฆษณายาต้านแบคทีเรียวาลดิคอกซิป ในขณะที่ 1 พันล้านเหรียญสหรัฐจ่ายให้กับค่าปรับพลเรือนในการทำการตลาดยาอีกสามขนานที่เหลือ รวมไปถึงไซว็อก[118]
References
[แก้]- ↑ 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 Pfizer (2010-07-16). "Zyvox (linezolid) Label Information" (PDF). สืบค้นเมื่อ 2011-04-02.
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 2.7 2.8 Lexi-Comp (August 2008). "Linezolid". The Merck Manual Professional. Retrieved on May 14, 2009.
- ↑ 3.0 3.1 3.2 Grau S, Rubio-Terrés C (April 2008). "Pharmacoeconomics of linezolid". Expert Opinion on Pharmacotherapy. 9 (6): 987–1000. doi:10.1517/14656566.9.6.987. ISSN 1465-6566. PMID 18377341.
- ↑ Wroe, David (2002-02-28). "An antibiotic to fight immune bugs". The Age. สืบค้นเมื่อ 2009-05-16.
- ↑ Wilson AP, Cepeda JA, Hayman S, Whitehouse T, Singer M, Bellingan G (August 2006). "In vitro susceptibility of Gram-positive pathogens to linezolid and teicoplanin and effect on outcome in critically ill patients" (PDF). Journal of Antimicrobial Chemotherapy. 58 (2): 470–3. doi:10.1093/jac/dkl233. ISSN 0305-7453. PMID 16735420.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 6.0 6.1 6.2 [No authors listed] (2009-06-24). "Zyvox 600 mg Film-Coated Tablets, 100 mg/5 ml Granules for Oral Suspension, 2 mg/ml Solution for Infusion – Summary of Product Characteristics (SPC)". electronic Medicines Compendium. สืบค้นเมื่อ 2009-07-03.
- ↑ 7.00 7.01 7.02 7.03 7.04 7.05 7.06 7.07 7.08 7.09 7.10 Herrmann DJ, Peppard WJ, Ledeboer NA, Theesfeld ML, Weigelt JA, Buechel BJ (December 2008). "Linezolid for the treatment of drug-resistant infections". Expert Review of Anti-infective Therapy. 6 (6): 825–48. doi:10.1586/14787210.6.6.825. ISSN 1478-7210. PMID 19053895.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 8.0 8.1 8.2 Falagas ME, Siempos II, Vardakas KZ (January 2008). "Linezolid versus glycopeptide or beta-lactam for treatment of Gram-positive bacterial infections: meta-analysis of randomised controlled trials". Lancet Infectious Diseases. 8 (1): 53–66. doi:10.1016/S1473-3099(07)70312-2. ISSN 1473-3099. PMID 18156089.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) Structured abstract with quality assessment available at DARE. - ↑ Tascini C, Gemignani G, Doria R; และคณะ (June 2009). "Linezolid treatment for gram-positive infections: a retrospective comparison with teicoplanin". Journal of Chemotherapy. 21 (3): 311–6. ISSN 1120-009X. PMID 19567352.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Chow I, Lemos EV, Einarson TR (2008). "Management and prevention of diabetic foot ulcers and infections: a health economic review". PharmacoEconomics. 26 (12): 1019–35. doi:10.2165/0019053-200826120-00005. ISSN 1170-7690. PMID 19014203.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Lipsky BA, Itani K, Norden C (January 2004). "Treating foot infections in diabetic patients: a randomized, multicenter, open-label trial of linezolid versus ampicillin-sulbactam/amoxicillin-clavulanate". Clinical Infectious Diseases. 38 (1): 17–24. doi:10.1086/380449. ISSN 1058-4838. PMID 14679443.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 12.0 12.1 12.2 12.3 Pigrau, C; Almirante, B (April 2009). "Oxazolidinonas, glucopéptidos y lipopéptidos cíclicos" [Oxazolidinones, glycopeptides and cyclic lipopeptides] (PDF). Enfermedades Infecciosas y Microbiología Clínica (ภาษาสันสกฤต). 27 (4): 236–46. doi:10.1016/j.eimc.2009.02.004. PMID 19406516.
- ↑ Vardakas KZ, Horianopoulou M, Falagas ME (June 2008). "Factors associated with treatment failure in patients with diabetic foot infections: An analysis of data from randomized controlled trials". Diabetes Research and Clinical Practice. 80 (3): 344–51. doi:10.1016/j.diabres.2008.01.009. ISSN 0168-8227. PMID 18291550.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Grammatikos A, Falagas ME (2008). "Linezolid for the treatment of skin and soft tissue infection". Expert Review of Dermatology. 3 (5): 539–48. doi:10.1586/17469872.3.5.539.
- ↑ 15.0 15.1 Mandell LA, Wunderink RG, Anzueto A; และคณะ (March 2007). "Infectious Diseases Society of America/American Thoracic Society consensus guidelines on the management of community-acquired pneumonia in adults". Clinical Infectious Diseases. 44 (Suppl 2): S27–72. doi:10.1086/511159. ISSN 1058-4838. PMID 17278083.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ BTS Pneumonia Guidelines Committee (2004-04-30). "BTS guidelines for the management of community acquired pneumonia in adults – 2004 update" (PDF). British Thoracic Society. สืบค้นเมื่อ 2009-06-30.
- ↑ 17.0 17.1 American Thoracic Society, Infectious Diseases Society of America (February 2005). "Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia" (PDF). American Journal of Respiratory and Critical Care Medicine. 171 (4): 388–416. doi:10.1164/rccm.200405-644ST. ISSN 1073-449X. PMID 15699079.
- ↑ Koya D, Shibuya K, Kikkawa R, Haneda M (December 2004). "Successful recovery of infective endocarditis-induced rapidly progressive glomerulonephritis by steroid therapy combined with antibiotics: a case report" (PDF). BMC Nephrology. 5 (1): 18. doi:10.1186/1471-2369-5-18. PMC 544880. PMID 15610562.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 19.0 19.1 19.2 19.3 19.4 19.5 19.6 19.7 Barbachyn MR, Ford CW (May 2003). "Oxazolidinone structure-activity relationships leading to linezolid". Angewandte Chemie (International Edition in English). 42 (18): 2010–23. doi:10.1002/anie.200200528. ISSN 1433-7851. PMID 12746812.
- ↑ Pankey GA, Sabath LD (March 2004). "Clinical relevance of bacteriostatic versus bactericidal mechanisms of action in the treatment of Gram-positive bacterial infections". Clinical Infectious Diseases. 38 (6): 864–70. doi:10.1086/381972. ISSN 1058-4838. PMID 14999632.
- ↑ Falagas ME, Manta KG, Ntziora F, Vardakas KZ (August 2006). "Linezolid for the treatment of patients with endocarditis: a systematic review of the published evidence" (PDF). Journal of Antimicrobial Chemotherapy. 58 (2): 273–80. doi:10.1093/jac/dkl219. ISSN 0305-7453. PMID 16735427.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Babcock HM, Ritchie DJ, Christiansen E, Starlin R, Little R, Stanley S (May 2001). "Successful treatment of vancomycin-resistant Enterococcus endocarditis with oral linezolid". Clinical Infectious Diseases. 32 (9): 1373–5. doi:10.1086/319986. ISSN 1058-4838. PMID 11303275.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Ang JY, Lua JL, Turner DR, Asmar BI (December 2003). "Vancomycin-resistant Enterococcus faecium endocarditis in a premature infant successfully treated with linezolid". The Pediatric Infectious Disease Journal. 22 (12): 1101–3. doi:10.1097/01.inf.0000101784.83146.0c. ISSN 0891-3668. PMID 14688576.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Archuleta S, Murphy B, Keller MJ (September 2004). "Successful treatment of vancomycin-resistant Enterococcus faecium endocarditis with linezolid in a renal transplant recipient with human immunodeficiency virus infection". Transplant Infectious Disease. 6 (3): 117–9. doi:10.1111/j.1399-3062.2004.00059.x. ISSN 1398-2273. PMID 15569227.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Zimmer SM, Caliendo AM, Thigpen MC, Somani J (August 2003). "Failure of linezolid treatment for enterococcal endocarditis". Clinical Infectious Diseases. 37 (3): e29–30. doi:10.1086/375877. ISSN 1058-4838. PMID 12884185.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Tsigrelis C, Singh KV, Coutinho TD, Murray BE, Baddour LM (February 2007). "Vancomycin-Resistant Enterococcus faecalis Endocarditis: Linezolid Failure and Strain Characterization of Virulence Factors" (PDF). Journal of Clinical Microbiology. 45 (2): 631–5. doi:10.1128/JCM.02188-06. ISSN 0095-1137. PMC 1829077. PMID 17182759.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Berdal JE, Eskesen A (2008). "Short-term success, but long-term treatment failure with linezolid for enterococcal endocarditis". Scandinavian Journal of Infectious Diseases. 40 (9): 765–6. doi:10.1080/00365540802087209. ISSN 0036-5548. PMID 18609208.
- ↑ Falagas ME, Siempos II, Papagelopoulos PJ, Vardakas KZ (March 2007). "Linezolid for the treatment of adults with bone and joint infections". International Journal of Antimicrobial Agents. 29 (3): 233–9. doi:10.1016/j.ijantimicag.2006.08.030. ISSN 0924-8579. PMID 17204407.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) Review. - ↑ Bassetti M, Vitale F, Melica G; และคณะ (March 2005). "Linezolid in the treatment of Gram-positive prosthetic joint infections" (PDF). Journal of Antimicrobial Chemotherapy. 55 (3): 387–90. doi:10.1093/jac/dki016. ISSN 0305-7453. PMID 15705640.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Aneziokoro CO, Cannon JP, Pachucki CT, Lentino JR (December 2005). "The effectiveness and safety of oral linezolid for the primary and secondary treatment of osteomyelitis". Journal of Chemotherapy. 17 (6): 643–50. ISSN 1120-009X. PMID 16433195.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Senneville E, Legout L, Valette M; และคณะ (August 2006). "Effectiveness and tolerability of prolonged linezolid treatment for chronic osteomyelitis: a retrospective study". Clinical Therapeutics. 28 (8): 1155–63. doi:10.1016/j.clinthera.2006.08.001. ISSN 0149-2918. PMID 16982292.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Rao N, Hamilton CW (October 2007). "Efficacy and safety of linezolid for Gram-positive orthopedic infections: a prospective case series". Diagnostic Microbiology and Infectious Disease. 59 (2): 173–9. doi:10.1016/j.diagmicrobio.2007.04.006. ISSN 0732-8893. PMID 17574788.
- ↑ Papadopoulos A, Plachouras D, Giannitsioti E, Poulakou G, Giamarellou H, Kanellakopoulou K (April 2009). "Efficacy and tolerability of linezolid in chronic osteomyelitis and prosthetic joint infections: a case-control study". Journal of Chemotherapy. 21 (2): 165–9. ISSN 1120-009X. PMID 19423469.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ von der Lippe B, Sandven P, Brubakk O (February 2006). "Efficacy and safety of linezolid in multidrug resistant tuberculosis (MDR-TB)—a report of ten cases". Journal of Infection. 52 (2): 92–6. doi:10.1016/j.jinf.2005.04.007. ISSN 0163-4453. PMID 15907341.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Park IN, Hong SB, Oh YM; และคณะ (September 2006). "Efficacy and tolerability of daily-half dose linezolid in patients with intractable multidrug-resistant tuberculosis" (PDF). Journal of Antimicrobial Chemotherapy. 58 (3): 701–4. doi:10.1093/jac/dkl298. ISSN 0305-7453. PMID 16857689.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Fortún J, Martín-Dávila P, Navas E; และคณะ (July 2005). "Linezolid for the treatment of multidrug-resistant tuberculosis" (PDF). Journal of Antimicrobial Chemotherapy. 56 (1): 180–5. doi:10.1093/jac/dki148. ISSN 0305-7453. PMID 15911549.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jaksic B, Martinelli G, Perez-Oteyza J, Hartman CS, Leonard LB, Tack KJ (March 2006). "Efficacy and safety of linezolid compared with vancomycin in a randomized, double-blind study of febrile neutropenic patients with cancer". Clinical Infectious Diseases. 42 (5): 597–607. doi:10.1086/500139. ISSN 1058-4838. PMID 16447103.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) Criticism in doi:10.1086/504431; author reply in doi:10.1086/504437. - ↑ 38.0 38.1 38.2 38.3 38.4 38.5 38.6 38.7 Moellering RC (January 2003). "Linezolid: the first oxazolidinone antimicrobial" (PDF). Annals of Internal Medicine. 138 (2): 135–42. ISSN 0003-4819. PMID 12529096.
- ↑ Cottagnoud P, Gerber CM, Acosta F, Cottagnoud M, Neftel K, Täuber MG (December 2000). "Linezolid against penicillin-sensitive and -resistant pneumococci in the rabbit meningitis model" (PDF). Journal of Antimicrobial Chemotherapy. 46 (6): 981–5. doi:10.1093/jac/46.6.981. ISSN 0305-7453. PMID 11102418.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 40.0 40.1 Sabbatani S, Manfredi R, Frank G, Chiodo F (June 2005). "Linezolid in the treatment of severe central nervous system infections resistant to recommended antimicrobial compounds". Le Infezioni in Medicina. 13 (2): 112–9. ISSN 1124-9390. PMID 16220032.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Ntziora F, Falagas ME (February 2007). "Linezolid for the treatment of patients with central nervous system infection". Annals of Pharmacotherapy. 41 (2): 296–308. doi:10.1345/aph.1H307. ISSN 1060-0280. PMID 17284501. Structured abstract with quality assessment available at DARE.
- ↑ Tunkel AR, Hartman BJ, Kaplan SL; และคณะ (November 2004). "Practice guidelines for the management of bacterial meningitis". Clinical Infectious Diseases. 39 (9): 1267–84. doi:10.1086/425368. ISSN 1058-4838. PMID 15494903.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Naesens R, Ronsyn M, Druwé P, Denis O, Ieven M, Jeurissen A (June 2009). "Central nervous system invasion by community-acquired methicillin-resistant Staphylococcus aureus: case report and review of the literature". Journal of Medical Microbiology. 58 (Pt 9): 1247–51. doi:10.1099/jmm.0.011130-0. ISSN 0022-2615. PMID 19528145.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 44.0 44.1 44.2 [No authors listed] (March 16, 2007). "Information for Healthcare Professionals: Linezolid (marketed as Zyvox)". U.S. Food and Drug Administration (FDA). สืบค้นเมื่อ 2010-09-15.
- ↑ 45.0 45.1 Wilcox MH, Tack KJ, Bouza E; และคณะ (January 2009). "Complicated skin and skin-structure infections and catheter-related bloodstream infections: noninferiority of linezolid in a phase 3 study". Clinical Infectious Diseases. 48 (2): 203–12. doi:10.1086/595686. ISSN 1058-4838. PMID 19072714.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ 46.0 46.1 Marino PL, Sutin KM (2007). "Antimicrobial therapy". The ICU book. Hagerstown, MD: Lippincott Williams & Wilkins. p. 817. ISBN 0-7817-4802-X.
- ↑ 47.0 47.1 47.2 47.3 47.4 47.5 47.6 47.7 French G (May 2003). "Safety and tolerability of linezolid" (PDF). Journal of Antimicrobial Chemotherapy. 51 (Suppl 2): ii45–53. doi:10.1093/jac/dkg253. ISSN 0305-7453. PMID 12730142. Review. Includes extensive discussion of the hematological adverse effects of linezolid.
- ↑ 48.0 48.1 48.2 48.3 Metaxas EI, Falagas ME (July 2009). "Update on the safety of linezolid". Expert Opinion on Drug Safety. 8 (4): 485–91. doi:10.1517/14740330903049706. ISSN 1474-0338. PMID 19538105.
- ↑ Zabel LT, Worm S (June 2005). "Linezolid contributed to Clostridium difficile colitis with fatal outcome". Infection. 33 (3): 155–7. doi:10.1007/s15010-005-4112-6. ISSN 0300-8126. PMID 15940418.
- ↑ Peláez T, Alonso R, Pérez C, Alcalá L, Cuevas O, Bouza E (May 2002). "In Vitro Activity of Linezolid against Clostridium difficile" (PDF). Antimicrobial Agents and Chemotherapy. 46 (5): 1617–8. doi:10.1128/AAC.46.5.1617-1618.2002. ISSN 0066-4804. PMC 127182. PMID 11959617.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Lin Y-H, Wu V-C, Tsai I-J; และคณะ (2006). "High frequency of linezolid-associated thrombocytopenia among patients with renal insufficiency". International Journal of Antimicrobial Agents. 28 (4): 345–51. doi:10.1016/j.ijantimicag.2006.04.017. ISSN 0924-8579. PMID 16935472.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help); ไม่รู้จักพารามิเตอร์|month=ถูกละเว้น (help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Spellberg B, Yoo T, Bayer AS (October 2004). "Reversal of linezolid-associated cytopenias, but not peripheral neuropathy, by administration of vitamin B6" (PDF). Journal of Antimicrobial Chemotherapy. 54 (4): 832–5. doi:10.1093/jac/dkh405. ISSN 0305-7453. PMID 15317746.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Plachouras D, Giannitsioti E, Athanassia S; และคณะ (2006). "No effect of pyridoxine on the incidence of myelosuppression during prolonged linezolid treatment". Clinical Infectious Diseases. 43 (9): e89–91. doi:10.1086/508280. ISSN 1058-4838. PMID 17029128.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help); ไม่รู้จักพารามิเตอร์|month=ถูกละเว้น (help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Narita M, Tsuji BT, Yu VL (August 2007). "Linezolid-associated peripheral and optic neuropathy, lactic acidosis, and serotonin syndrome". Pharmacotherapy. 27 (8): 1189–97. doi:10.1592/phco.27.8.1189. ISSN 0277-0008. PMID 17655517.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bressler AM, Zimmer SM, Gilmore JL, Somani J (August 2004). "Peripheral neuropathy associated with prolonged use of linezolid". Lancet Infectious Diseases. 4 (8): 528–31. doi:10.1016/S1473-3099(04)01109-0. ISSN 1473-3099. PMID 15288827.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Brown J, Aitken SL, van Mannen RP (June 2011). "Potential for Linezolid-Related Blindness: a Review of Spontaneous Adverse Event Reports". Pharmacotherapy. 31 (6): 585–90. doi:10.1592/phco.31.6.585. PMID 21923442.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Chao CC, Sun HY, Chang YC, Hsieh ST (2008). "Painful neuropathy with skin denervation after prolonged use of linezolid". Journal of Neurology, Neurosurgery & Psychiatry. 79 (1): 97–9. doi:10.1136/jnnp.2007.127910. ISSN 0022-3050. PMID 17766431.
{{cite journal}}: ไม่รู้จักพารามิเตอร์|month=ถูกละเว้น (help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Saijo T, Hayashi K, Yamada H, Wakakura M (June 2005). "Linezolid-induced optic neuropathy". American Journal of Ophthalmology. 139 (6): 1114–6. doi:10.1016/j.ajo.2004.11.047. ISSN 0002-9394. PMID 15953450.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 59.0 59.1 Soriano A, Miró O, Mensa J (2005). "Mitochondrial toxicity associated with linezolid". New England Journal of Medicine. 353 (21): 2305–6. doi:10.1056/NEJM200511243532123. ISSN 0028-4793. PMID 16306535.
{{cite journal}}: ไม่รู้จักพารามิเตอร์|month=ถูกละเว้น (help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Javaheri M, Khurana RN, O'hearn TM, Lai MM, Sadun AA (January 2007). "Linezolid‐induced optic neuropathy: a mitochondrial disorder?". British Journal of Ophthalmology. 91 (1): 111–5. doi:10.1136/bjo.2006.102541. ISSN 0007-1161. PMC 1857552. PMID 17179125.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ McKee EE, Ferguson M, Bentley AT, Marks TA (June 2006). "Inhibition of Mammalian Mitochondrial Protein Synthesis by Oxazolidinones" (PDF). Antimicrobial Agents and Chemotherapy. 50 (6): 2042–9. doi:10.1128/AAC.01411-05. ISSN 0066-4804. PMC 1479116. PMID 16723564.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bishop E, Melvani S, Howden BP, Charles PG, Grayson ML (April 2006). "Good Clinical Outcomes but High Rates of Adverse Reactions during Linezolid Therapy for Serious Infections: a Proposed Protocol for Monitoring Therapy in Complex Patients" (PDF). Antimicrobial Agents and Chemotherapy. 50 (4): 1599–602. doi:10.1128/AAC.50.4.1599-1602.2006. ISSN 0066-4804. PMC 1426936. PMID 16569895.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Lawrence KR, Adra M, Gillman PK (June 2006). "Serotonin toxicity associated with the use of linezolid: a review of postmarketing data". Clinical Infectious Diseases. 42 (11): 1578–83. doi:10.1086/503839. ISSN 1058-4838. PMID 16652315.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Huang V, Gortney JS (December 2006). "Risk of serotonin syndrome with concomitant administration of linezolid and serotonin agonists". Pharmacotherapy. 26 (12): 1784–93. doi:10.1592/phco.26.12.1784. ISSN 0277-0008. PMID 17125439.
- ↑ Waknine, Yael (September 5, 2008). "FDA Safety Changes: Mirena, Zyvox, Orencia". Medscape. สืบค้นเมื่อ 2008-09-06. Freely available with registration.
- ↑ Stalker DJ, Jungbluth GL (2003). "Clinical pharmacokinetics of linezolid, a novel oxazolidinone antibacterial". Clinical Pharmacokinetics. 42 (13): 1129–40. doi:10.2165/00003088-200342130-00004. ISSN 0312-5963. PMID 14531724.
- ↑ FDA Alert: Zyvox (linezolid): Drug Safety Communication - Serious CNS Reactions Possible When Given to Patients Taking Certain Psychiatric Medications
- ↑ Skripkin E, McConnell TS, DeVito J; และคณะ (October 2008). "Rχ-01, a New Family of Oxazolidinones That Overcome Ribosome-Based Linezolid Resistance" (PDF). Antimicrobial Agents and Chemotherapy. 52 (10): 3550–7. doi:10.1128/AAC.01193-07. ISSN 0066-4804. PMC 2565890. PMID 18663023.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ 69.0 69.1 69.2 Ament PW, Jamshed N, Horne JP (February 2002). "Linezolid: its role in the treatment of gram-positive, drug-resistant bacterial infections". American Family Physician. 65 (4): 663–70. ISSN 0002-838X. PMID 11871684.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Swaney SM, Aoki H, Ganoza MC, Shinabarger DL (December 1, 1998). "The Oxazolidinone Linezolid Inhibits Initiation of Protein Synthesis in Bacteria" (PDF). Antimicrobial Agents and Chemotherapy. 42 (12): 3251–5. ISSN 0066-4804. PMC 106030. PMID 9835522.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Colca JR, McDonald WG, Waldon DJ; และคณะ (June 2003). "Cross-linking in the living cell locates the site of action of oxazolidinone antibiotics" (PDF). Journal of Biological Chemistry. 278 (24): 21972–9. doi:10.1074/jbc.M302109200. ISSN 0021-9258. PMID 12690106.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Ippolito JA, Kanyo ZF, Wang D; และคณะ (June 2008). "Crystal structure of the oxazolidinone antibiotic linezolid bound to the 50S ribosomal subunit". Journal of Medicinal Chemistry. 51 (12): 3353–6. doi:10.1021/jm800379d. ISSN 0022-2623. PMID 18494460.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Wilson DN, Schluenzen F, Harms JM, Starosta AL, Connell SR, Fucini P (September 2008). "The oxazolidinone antibiotics perturb the ribosomal peptidyl-transferase center and effect tRNA positioning" (PDF). Proceedings of the National Academy of Sciences. 105 (36): 13339–44. doi:10.1073/pnas.0804276105. ISSN 0027-8424. PMC 2533191. PMID 18757750.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 74.0 74.1 74.2 74.3 74.4 74.5 74.6 Brickner SJ (1996). "Oxazolidinone antibacterial agents". Current Pharmaceutical Design. 2 (2): 175–94. Detailed review of the discovery and development of the whole oxazolidinone class, including information on synthesis and structure-activity relationships.
- ↑ European Medicines Agency (2011). "CHP Assessment Report for Xarelto (EMA/CHMP/301607/2011)" (PDF). สืบค้นเมื่อ 2012-03-15.
- ↑ 76.0 76.1 76.2 Xu GY, Zhou Y, Xu MC (2006). "A convenient synthesis of antibacterial linezolid from (S)-glyceraldehyde acetonide" (PDF). Chinese Chemical Letters. 17 (3): 302–4.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 77.0 77.1 Kaiser CR, Cunico W, Pinheiro AC, de Oliveira AG, Peralta MA, de Souza MV (2007). "Oxazolidinonas: uma nova classe de compostos no combate à tuberculose" [Oxazolidinones: a new class of compounds against tuberculosis] (pdf). Revista Brasileira de Farmácia (ภาษาโปรตุเกส). 88 (2): 83–8.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ US5,837,870 (1997-03-28) Pearlman BA, Perrault WR, Barbachyn MR, et al., Process to prepare oxazolidinones. Retrieved on 2009-06-13.
- ↑ Lohray BB, Baskaran S, Rao BS, Reddy BY, Rao IN (June 1999). "A short synthesis of oxazolidinone derivatives linezolid and eperezolid: A new class of antibacterials". Tetrahedron Letters. 40 (26): 4855–6. doi:10.1016/S0040-4039(99)00893-X.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Perrault WR, Keeler JB, Snyder WC, et al. (June 25, 2008). "Convergent green synthesis of linezolid (Zyvox)", in 12th Annual Green Chemistry and Engineering Conference, June 24–26, 2008, New York, NY. Retrieved on 2009-06-08.
- ↑ 81.0 81.1 Slatter JG, Stalker DJ, Feenstra KL; และคณะ (August 1, 2001). "Pharmacokinetics, metabolism, and excretion of linezolid following an oral dose of [(14)C]linezolid to healthy human subjects" (PDF). Drug Metabolism and Disposition. 29 (8): 1136–45. ISSN 0090-9556. PMID 11454733.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Sisson TL, Jungbluth GL, Hopkins NK (January 2002). "Age and sex effects on the pharmacokinetics of linezolid". European Journal of Clinical Pharmacology. 57 (11): 793–7. doi:10.1007/s00228-001-0380-y. ISSN 0031-6970. PMID 11868801.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Buck ML (June 2003). "Linezolid use for resistant Gram-positive infections in children" (PDF). Pediatric Pharmacotherapy. 9 (6). สืบค้นเมื่อ 2009-06-08.
- ↑ Lovering AM, Le Floch R, Hovsepian L; และคณะ (March 2009). "Pharmacokinetic evaluation of linezolid in patients with major thermal injuries". Journal of Antimicrobial Chemotherapy. 63 (3): 553–9. doi:10.1093/jac/dkn541. ISSN 0305-7453. PMID 19153078.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ 85.0 85.1 Davaro RE, Glew RH, Daly JS (2004). "Oxazolidinones, quinupristin-dalfopristin, and daptomycin". ใน Gorbach SL, Bartlett JG, Blacklow NR (บ.ก.). Infectious diseases. Hagerstown, MD: Lippincott Williams & Wilkins. pp. 241–3. ISBN 0-7817-3371-5. สืบค้นเมื่อ 2009-06-20.
{{cite book}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jones RN, Stilwell MG, Hogan PA, Sheehan DJ (April 2007). "Activity of Linezolid against 3,251 Strains of Uncommonly Isolated Gram-Positive Organisms: Report from the SENTRY Antimicrobial Surveillance Program". Antimicrobial Agents and Chemotherapy. 51 (4): 1491–3. doi:10.1128/AAC.01496-06. PMC 1855453. PMID 17210770.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jodlowski TZ, Melnychuk I, Conry J (October 2007). "Linezolid for the treatment of Nocardia spp. infections". Annals of Pharmacotherapy. 41 (10): 1694–9. doi:10.1345/aph.1K196. ISSN 1060-0280. PMID 17785610.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 88.0 88.1 88.2 88.3 [No authors listed] (2001). "Linezolid: First of a New Drug Class for Gram-Positive Infections". Drugs & Therapy Perspectives. 17 (9): 1–6. doi:10.2165/00042310-200117090-00001. Free full text with registration at Medscape.
- ↑ [No authors listed] (August 5, 2008). "Animal Bites and Pasteurella multocida: Information for Healthcare Staff". Health Protection Agency. Retrieved on 2009-05-15.
- ↑ Geisler WM, Malhotra U, Stamm WE (December 2001). "Pneumonia and sepsis due to fluoroquinolone-resistant Capnocytophaga gingivalis after autologous stem cell transplantation" (PDF). Bone Marrow Transplantation. 28 (12): 1171–3. doi:10.1038/sj.bmt.1703288. ISSN 0268-3369. PMID 11803363.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 91.0 91.1 91.2 Livermore DM (September 2000). "Quinupristin/dalfopristin and linezolid: where, when, which and whether to use?" (PDF). Journal of Antimicrobial Chemotherapy. 46 (3): 347–50. doi:10.1093/jac/46.3.347. ISSN 0305-7453. PMID 10980159.
- ↑ Tsiodras S, Gold HS, Sakoulas G; และคณะ (July 2001). "Linezolid resistance in a clinical isolate of Staphylococcus aureus". The Lancet. 358 (9277): 207–8. doi:10.1016/S0140-6736(01)05410-1. ISSN 0140-6736. PMID 11476839.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jones RN, Ross JE, Castanheira M, Mendes RE (December 2008). "United States resistance surveillance results for linezolid (LEADER Program for 2007)". Diagnostic Microbiology and Infectious Disease. 62 (4): 416–26. doi:10.1016/j.diagmicrobio.2008.10.010. ISSN 0732-8893. PMID 19022153.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jones RN, Kohno S, Ono Y, Ross JE, Yanagihara K (June 2009). "ZAAPS International Surveillance Program (2007) for linezolid resistance: results from 5591 Gram-positive clinical isolates in 23 countries". Diagnostic Microbiology and Infectious Disease. 64 (2): 191–201. doi:10.1016/j.diagmicrobio.2009.03.001. ISSN 0732-8893. PMID 19500528.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Hope R, Livermore DM, Brick G, Lillie M, Reynolds R (November 2008). "Non-susceptibility trends among staphylococci from bacteraemias in the UK and Ireland, 2001-06" (PDF). Journal of Antimicrobial Chemotherapy. 62 (Suppl 2): ii65–74. doi:10.1093/jac/dkn353. ISSN 0305-7453. PMID 18819981.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Auckland C, Teare L, Cooke F; และคณะ (November 2002). "Linezolid-resistant enterococci: report of the first isolates in the United Kingdom" (PDF). Journal of Antimicrobial Chemotherapy. 50 (5): 743–6. doi:10.1093/jac/dkf246. ISSN 0305-7453. PMID 12407134.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ 97.0 97.1 Scheetz MH, Knechtel SA, Malczynski M, Postelnick MJ, Qi C (June 2008). "Increasing Incidence of Linezolid-Intermediate or -Resistant, Vancomycin-Resistant Enterococcus faecium Strains Parallels Increasing Linezolid Consumption" (PDF). Antimicrobial Agents and Chemotherapy. 52 (6): 2256–9. doi:10.1128/AAC.00070-08. ISSN 0066-4804. PMC 2415807. PMID 18391028.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Schumacher A, Trittler R, Bohnert JA, Kümmerer K, Pagès JM, Kern WV (June 2007). "Intracellular accumulation of linezolid in Escherichia coli, Citrobacter freundii and Enterobacter aerogenes: role of enhanced efflux pump activity and inactivation" (PDF). Journal of Antimicrobial Chemotherapy. 59 (6): 1261–4. doi:10.1093/jac/dkl380. ISSN 0305-7453. PMID 16971414.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Saager B, Rohde H, Timmerbeil BS; และคณะ (September 2008). "Molecular characterisation of linezolid resistance in two vancomycin-resistant (VanB) Enterococcus faecium isolates using Pyrosequencing". European Journal of Clinical Microbiology & Infectious Diseases. 27 (9): 873–8. doi:10.1007/s10096-008-0514-6. ISSN 0934-9723. PMID 18421487.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Besier S, Ludwig A, Zander J, Brade V, Wichelhaus TA (April 2008). "Linezolid Resistance in Staphylococcus aureus: Gene Dosage Effect, Stability, Fitness Costs, and Cross-Resistances" (PDF). Antimicrobial Agents and Chemotherapy. 52 (4): 1570–2. doi:10.1128/AAC.01098-07. ISSN 0066-4804. PMC 2292563. PMID 18212098.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Feng J, Lupien A, Gingras H; และคณะ (May 2009). "Genome sequencing of linezolid-resistant Streptococcus pneumoniae mutants reveals novel mechanisms of resistance". Genome Research. 19 (7): 1214–23. doi:10.1101/gr.089342.108. ISSN 1088-9051. PMC 2704432. PMID 19351617.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Lincopan N, de Almeida LM, Elmor de Araújo MR, Mamizuka EM (April 2009). "Linezolid resistance in Staphylococcus epidermidis associated with a G2603T mutation in the 23S rRNA gene". International Journal of Antimicrobial Agents. 34 (3): 281–2. doi:10.1016/j.ijantimicag.2009.02.023. ISSN 0924-8579. PMID 19376688.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Liakopoulos A, Neocleous C, Klapsa D; และคณะ (July 2009). "A T2504A mutation in the 23S rRNA gene responsible for high-level resistance to linezolid of Staphylococcus epidermidis". Journal of Antimicrobial Chemotherapy. 64 (1): 206–7. doi:10.1093/jac/dkp167. ISSN 0305-7453. PMID 19429927.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Slee AM, Wuonola MA, McRipley RJ; และคณะ (November 1987). "Oxazolidinones, a new class of synthetic antibacterial agents: in vitro and in vivo activities of DuP 105 and DuP 721" (PDF). Antimicrobial Agents and Chemotherapy. 31 (11): 1791–7. ISSN 0066-4804. PMC 175041. PMID 3435127.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ Ford CW, Zurenko GE, Barbachyn MR (August 2001). "The discovery of linezolid, the first oxazolidinone antibacterial agent". Current Drug Targets – Infectious Disorders. 1 (2): 181–99. doi:10.2174/1568005014606099. ISSN 1568-0053. PMID 12455414.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Drug Approval Package: Zyvox". FDA Center for Drug Evaluation and Research. November 20, 2001. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2008-01-10. สืบค้นเมื่อ 2009-01-17. Comprehensive review of the FDA approval process. Includes detailed reviews of the chemistry and pharmacology of linezolid, correspondence between the FDA and Pharmacia & Upjohn, and administrative documents.
- ↑ ANVISA (June 5, 2000). "Resolução nº 474, de 5 de junho de 2000" [Resolution number 474, of June 5, 2000] (ภาษาโปรตุเกส). National Health Surveillance Agency. สืบค้นเมื่อ 2009-05-19.
- ↑ Irinoda K, Nomura S, Hashimoto M (October 2002). "[Antimicrobial and clinical effect of linezolid (Zyvox), new class of synthetic antibacterial drug]". Nippon Yakurigaku Zasshi (ภาษาญี่ปุ่น). 120 (4): 245–52. doi:10.1254/fpj.120.245. ISSN 0015-5691. PMID 12425150.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 109.0 109.1 "Canada Approves Marketing Of Zyvoxam (Linezolid) For Gram Positive Infections" (Press release). May 8, 2001. สืบค้นเมื่อ 2009-05-18.
- ↑ Karlowsky JA, Kelly LJ, Critchley IA, Jones ME, Thornsberry C, Sahm DF (June 2002). "Determining Linezolid's Baseline In Vitro Activity in Canada Using Gram-Positive Clinical Isolates Collected prior to Its National Release" (PDF). Antimicrobial Agents and Chemotherapy. 46 (6): 1989–92. doi:10.1128/AAC.46.6.1989-1992.2002. ISSN 0066-4804. PMC 127260. PMID 12019122.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Pharmacia Corporation Reports 17% Increase In Second-Quarter Earnings-Per-Share Driven By 61% Increase In Pharmaceutical Earnings" (Press release). Pharmacia Corporation. July 25, 2001. สืบค้นเมื่อ 2009-05-19.
- ↑ 112.0 112.1 Livermore DM, Mushtaq S, Warner M, Woodford N (April 2009). "Activity of oxazolidinone TR-700 against linezolid-susceptible and -resistant staphylococci and enterococci". Journal of Antimicrobial Chemotherapy. 63 (4): 713–5. doi:10.1093/jac/dkp002. ISSN 0305-7453. PMID 19164418.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Howe RA, Wootton M, Noel AR, Bowker KE, Walsh TR, MacGowan AP (November 2003). "Activity of AZD2563, a Novel Oxazolidinone, against Staphylococcus aureus Strains with Reduced Susceptibility to Vancomycin or Linezolid" (PDF). Antimicrobial Agents and Chemotherapy. 47 (11): 3651–2. doi:10.1128/AAC.47.11.3651-3652.2003. ISSN 0066-4804. PMC 253812. PMID 14576139.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Kalia V, Miglani R, Purnapatre KP; และคณะ (April 2009). "Mode of Action of Ranbezolid against Staphylococci and Structural Modeling Studies of Its Interaction with Ribosomes". Antimicrobial Agents and Chemotherapy. 53 (4): 1427–33. doi:10.1128/AAC.00887-08. ISSN 0066-4804. PMC 2663096. PMID 19075051.
{{cite journal}}: ใช้ et al. อย่างชัดเจน ใน|author=(help)CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Trius Completes Enrollment In Phase 2 Clinical Trial Evaluating Torezolid (TR-701) In Patients With Complicated Skin And Skin Structure Infections" (Press release). 2009-01-27. สืบค้นเมื่อ 2009-05-17.
- ↑ "Rx 1741". Rib-X Pharmaceuticals. 2009. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2009-02-26. สืบค้นเมื่อ 2009-05-17.
- ↑ "Pfizer agrees record fraud fine". BBC News. September 2, 2009. สืบค้นเมื่อ 2009-09-12.
- ↑ Harris, Gardiner (September 2, 2009). "Pfizer pays $2.3 billion to settle marketing case". The New York Times. สืบค้นเมื่อ 2009-09-12.