อิริโทรมัยซิน
บทความนี้อาจต้องการตรวจสอบต้นฉบับ ในด้านไวยากรณ์ รูปแบบการเขียน การเรียบเรียง คุณภาพ หรือการสะกด คุณสามารถช่วยพัฒนาบทความได้ |
 | |
 | |
| ข้อมูลทางคลินิก | |
|---|---|
| ชื่อทางการค้า | Erythrocin, E-mycin, Ilosone |
| AHFS/Drugs.com | โมโนกราฟ |
| MedlinePlus | a682381 |
| ระดับความเสี่ยงต่อทารกในครรภ์ | |
| ช่องทางการรับยา | การรับประทาน, การฉัดเข้าหลอดเลือดดำ (IV), การฉีดเข้ากล้ามเนื้อ (IM), การทาบริเวณผิวหนัง, การหยอดตา ยาหยอดตา |
| รหัส ATC | |
| กฏหมาย | |
| สถานะตามกฏหมาย | |
| ข้อมูลเภสัชจลนศาสตร์ | |
| ชีวประสิทธิผล | ขึ้นกับชนิดของเอสเทอร์ โดยมีค่าระหว่าง 30% - 65% |
| การจับกับโปรตีน | 90% |
| การเปลี่ยนแปลงยา | ตับ (น้อยกว่า 5% ในรูปแบบที่ไม่เปลี่ยนแปลง) |
| ครึ่งชีวิตทางชีวภาพ | 1.5 ชั่วโมง |
| การขับออก | น้ำดี |
| ตัวบ่งชี้ | |
| |
| เลขทะเบียน CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| ECHA InfoCard | 100.003.673 |
| ข้อมูลทางกายภาพและเคมี | |
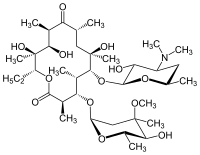
| สูตร | C37H67NO13 |
| มวลต่อโมล | 733.93 g/mol g·mol−1 |
| แบบจำลอง 3D (JSmol) | |
| |
| |
| (verify) | |
อีริโธรมัยซิน (Erythromycin) เป็นยาปฏิชีวนะชนิดหนึ่งในกลุ่มแมคโครไลด์ (Macrolides) ซึ่งใช้ในการรักษาโรคติดเชื้อที่มีสาเหตุจากแบคทีเรีย [1] ซึ่งยาในกลุ่มดังกล่าว รวมถึงอีริโธรมัยซินนั้นมีฤทธิ์ในการต้านเชื้อแบคทีเรียได้คล้ายคลึงหรือกว้างกว่ายาในกลุ่มเพนนิซิลิน (Penicillins) เล็กน้อย[2] โดยยาดังกล่าวมักถูกสั่งใช้ในกรณีที่ผู้ป่วยเกิดอาการแพ้ต่อยากลุ่มเพนนิซิลิน สำหรับในกรณีที่ใช้ในการรักษาโรคติดเชื้อในทางเดินหายใจนั้น ยาดังกล่าวจะออกฤทธิ์ครอบคุลมเชื้อกลุ่ม Atypical pathogens ได้ดีกว่า ได้แก่ ไมโคพลาสมา (Mycoplasma) และ ลิจิโอเนลลา (Legionella) โดยบริษัทแรกที่ผลิตยาชนิดนี้ออกสู่ตลาดเป็นรายแรกคือ Eli Lilly and Company [3][4] จนกระทั่งในปัจจุบัน ยาชนิดนี้เป็นที่รู้จักกันโดยทั่วไปในชื่อ erythromycin ethylsuccinate (EES) ซึ่งเป็นรูปแบบเกลือเอสเทอร์ที่ถูกใช้กันโดยส่วนใหญ่ และยาดังกล่าวมักถูกนำไปปรับประยุกต์เพื่อใช้ในการบริหารยาโดยการหยอดตาสำหรับเด็กแรกเกิดเพื่อป้องกันเยื่อตาอักเสบในทารกแรกเกิด (neonatal conjunctivitis) และถือเป็นยาทางเลือกรองสำหรับการรักษาโรคติดต่อทางเพศสัมพันธ์ (Sexual transmitted diseases; STDs) บางโรคอีกด้วย[5]
นอกจากนี้แล้ว ยังมีการใช้อีริโธรมัยซินเพื่อรักษาภาวะที่มีระยะเวลาที่ใช้ในการบีบตัวของกระเพาะอาหารเพื่อดันอาหารลงสู่ลำไส้เล็กนานกว่าปกติ (Delayed gastric emptying time) แต่การใช้ในข้อบ่งชี้ดังกล่าวนั้น เป็นการใช้ยาจากประโยชน์นอกเหนือจากที่ระบุไว้ในฉลาก (Off-label use basis) ในกรณีที่ต้องการผลทางเภสัชจลนศาตร์ที่ดีกว่าในผู้ป่วยที่ต้องเข้ารับการรักษาในโรงพยาบาล (hospitalized patients) อาจมีการพิจารณาใช้ยาอีริโธรมัยซินในรูปแบบฉีดเข้าหลอดเลือดดำ (IV) แทน อย่างไรก็ตาม การใช้ยาอีริโธรมัยซินในรูปแบบรับประทานเพื่อแก้ไขความผิดปกติของทางเดินอาหารข้างต้นนั้นยังมีข้อมูลจำกัดในเรื่องของประสิทธิภาพของยาในระยะยาว[6][7]
จากสูตรโคงสร้างทางเคมีของอีริโธรมัยซินซึ่งเป็นสารประกอบแมคโครไซคลิค (macrocyclic compound) ที่ประกอบไปด้วยวงแหวนแลคโตน (Lactone ring) จำนวน 14 วง, มีศูนย์ไครัล (Chiral center หรือ asymmetric center) มากถึง 10 ตำแหน่ง และต่อกับน้ำตาลอีก 2 โมเลกุล คือ (L-cladinose และ D-desosamine) ทำให้สารประกอบชนิดนี้ยากต่อการสังเคราะห์เลียนแบบเป็นอย่างมาก [8] ดังนั้น การผลิตยาอีริโธรมัยซินนี้จึงต้องผลิตจากการคัดแยกจากสารผสมที่ได้จากการสันดาปของเชื้อแอคติโนมัยสีท (Actinomycete) [ชื่อวิทยาศาสตร์ แซคคาโรโพลีสปอรา อีรีธราอี (Saccharopolyspora erythraea)]
อีริโธรมัยซินเป็นยาอีกหนึ่งชนิดในรายการจำเป็นขององค์การอนามัยโลก (World Health Organization's List of Essential Medicines) ซึ่งเป็นรายการยาที่มีความสำคัญมากที่สุดในระบบบริการสุขภาพพื้นฐาน (ฺBasic health system) ของแต่ละประเทศ [9]
ประวัติการค้นพบ[แก้]
ในปี ค.ศ. 1949 นักวิทยาศาสตร์ชาวฟิลิปปินส์ ชื่อ Dr. Abelardo B. Aguilar ได้ส่งตัวอย่างดินที่เก็บได้ไปให้บริษัทผู้ว่าจ้างของเขา ซึ่งก็คือบริษัท Eli Lilly ในขณะนั้น จากนั้นทีมนักวิจัยของบริษัท ซึ่งนำโดย J. M. McGuire ได้ทำการแยกอีริโธรมัยซินออกจากสารผสมที่ได้จากการสันดาป (metabolic products) ของเชื้อ Streptomyces erythreus] (ต่อมาเปลี่ยนชื่อเป็น "Saccharopolyspora erythraea" ในภายหลัง) ที่พบในตัวอย่างดินดังกล่าวได้สำเร็จ [10][11]
บริษัท Eli Lilly ได้รับความคุ้มครองด้านสิทธิบัตรจากการค้นพบสารดังกล่าวในปี ค.ศ.1953 (US patent 2653899) ผลิตภัณฑ์ยาที่ได้ถูกนำออกสู่ตลาดในปี ค.ศ.1952 [3]ภายใต้ชื่อการค้า Ilosone [4](ตามชื่อพื้นที่ที่ค้นพบตัวอย่าง ซึ่งก็คือจังหวัดอิโลอิโล่ (Iloilo) ในประเทศฟิลิปปินส์) และในสมัยก่อนมีการเรียกชื่ออีริโธรมัยซินในอีกชื่อหนึ่ง คือ Ilotycin[12]
ในปี ค.ศ. 1981 Robert B. Woodward ศาสตร์ตราจาย์ด้านเคมี ณ มหาวิทยาลัยฮาวาร์ด (Harvard University) ซึ่งเป็นผู้ที่ได้รับรางวัลโนเบลสาขาเคมีในปี 1965 (ได้รับรางวัลหลังจากเสียชีวิตแล้ว) [13] ร่วมกับทีมนักวิจัยจำนวนหนึ่งได้ค้นพบ stereocontrolled asymmetric center ตำแหน่งแรกของการสังเคราะห์อีริโธรมัยซิน เอ (erythromycin A)[14][15][16]
ยาปฏิชีวนะอีกชนิดหนึ่งที่มีชื่อว่า คลาริโธรมัยซิน (clarithromycin) ได้ถูกพัฒนาขึ้นในปี ค.ศ. 1970 โดยนักวิทยาศาสตร์ของบริษัทยาสัญชาติญี่ปุ่นที่มีชื่อว่า Taisho Pharmaceutical ซึ่งยาดังกล่าวมีคุณสมบัติที่เหนือกว่าอีริโธรมัยซินคือ มีความคงทนต่อกรดได้มากกว่า จึงสามารถบริหารยาโดยการรับประทานหลังอาหารได้[17]
นักวิทยาศาสตร์แห่ง Chugai Pharmaceuticals ได้ค้นพบว่าอนุพันธ์ของอีริโธรมัยซิน (Erythromycin-derivertives) ที่มีชื่อว่า Mitemcinal มีฤทธิ์กระตุ้นการทำงานของเอนไซม์โมทิลิน (Motilin) อย่างไรก็ตาม อนุพันธ์ดังกล่าวนั้นไม่มีคุณสมบัติในการยับยั้งการเจริญเติบโตหรือฆ่าเชื้อแบคทีเรียได้ ด้วยเหตุนี้เอง อีริโธรมัยซินจึงถูกใช้ประโยชน์จากคุณสมบัติดังกล่าวซึ่งเป็นการใช้ประโยชน์ที่นอกเหนือจากที่ระบุไว้ในฉลาก (Off-label use) กันอย่างแพร่หลายในการรักษาภาวะที่มีการเคลื่อนไหวของทางเดินอาหารที่ผิดปกติ อย่างเช่น ภาวะที่กล้ามเนื้อกระเพาะอาหารทำงานน้อยลง (Gastroparesis) ซึ่งหาก mitemcinal มีประสิทธิภาพในการเป็นสารพวกโปรไคเนติกส์ (Prokinetic agents) ซึ่งมีฤทธิ์เพิ่มการเคลื่อนไหวของทางเดินอาหารส่วนบน แสดงว่าสารดังกล่าวก็จะมีประโยชน์อย่างมีนัยสำคัญในการรักษาความผิดปกติที่มีการเคลื่อนไหวของทางเดินอาหารน้อย[7][18][19] อย่างไรก็ตาม การเลือกใช้อีริโธรมัยซินเพื่อแก้ไขปัญหาความผิดปกติของทางเดินอาหารในประเด็นดังกล่าวถือเป็นความเสี่ยงหนึ่งต่อการทำให้เกิดเชื้อแบคทีเรียดื้อยาได้
อาการไม่พึงประสงค์[แก้]


ความผิดปกติของระบบทางเดินอาหาร อย่างเช่น ท้องเสีย, ปวดท้อง, และอาเจียน เป็นอาการข้างเคียงที่พบได้ทั่วไปในผู้ป่วยที่ได้รับการรักษาด้วยยาอีริโธรมัยซิน เนื่องจากยาดังกล่าวมีผลกระตุ้นการทำงานของเอนไซม์โมทิลิน (Motilin)[20] ด้วยเหตุนี้เอง จึงไม่ค่อยมีการสั่งจ่ายอีริโธรมัยซินเป็นยาทางเลือกแรกในการรักษามากเท่าใดนัก อย่างไรก็ตาม ยาดังกล่าวอาจมีประโยชน์ในการรักษาผู้ป่วยที่มีการทำงานของกล้ามเนื้อกระเพาะอาหารลดน้อยลง (Gastroparesis) เนื่องจากยาดังกล่าวมีคุณสมบัติกระตุ้นการบีบตัวของทางเดินอาหารส่วนบน (Prokinetic effect)[6] นอกจากนี้ ยังมีการใช้ประโยชน์จากคุณสมบัติดังกล่าวในการเร่งการบีบตัวเพื่อไล่เศษอาหารออกจากกระเพาะอาหารในผู้ป่วยที่จะได้รับการส่องกล้องตรวจกระเพาะอาหาร (esophagogastroduodenoscopy)[21] [22]
อาการไม่พึงประสงค์ที่รุนแรงที่อาจเกิดขึ้นได้ในผู้ป่วยที่ได้รับการรักษาด้วยยาอีริโธรมัยซิน ได้แก่ หัวใจเต้นผิดจังหวะ (Arrhythmia) ร่วมกับการมีช่วง QT segment ที่นานกว่าปกติ (Prolonged QT intervals) รวมไปถึงการเกิด torsades de pointes ซึ่งภาวะหัวใจเต้นผิดจังหวะชนิดร้ายแรงอย่างหนึ่ง นอกจากนี้ยาดังกล่าวอาจทำให้เกิดภาวะหูหนวกได้ชั่วคราว (reversible erythromycin-induced deafness) ซึ่งจะสามารถกลับเป็นปรกติได้เมื่อหยุดยา [23] [24] แต่ในบางรายอาจเกิดความผิดปกติดังกล่าวแบบถาวรได้ [25] ยิ่งไปกว่านั้นยาดังกล่าวอาจทำให้เกิดปฏิกิริยาการแพ้ยาได้ ซึ่งอาจมีอาการได้ตั้งแต่การเกิดผื่นลมพิษ (Urticaria) ไปจนถึงการเกิดปฏิกิริยาการแพ้ยาที่รุนแรงอย่าง Anaphylaxis ซึ่งเป็นอันตรายถึงแก่ชีวิตได้ ภาวการณ์คั่งของน้ำดี (Cholestasis), ปฏิกิริยาการแพ้ยาแบบกลุ่มอาการสตีเฟนส์-จอห์นสัน (Stevens–Johnson syndrome) และปฏิกิริยาการแพ้ยาแบบท็อกซิก อีพิเดอร์มัล เนโครไลซิส (toxic epidermal necrolysis) เป็นอาการข้างเคียงรุนแรงที่อาจเกิดขึ้นได้ แต่พบอุบัติการณ์การเกิดได้ค่อนข้างน้อย แต่อาจรุนแรงจนถึงแก่ชีวิตได้[1]
การศึกษาหลายการศึกษาที่ผ่านมาแสดงให้เห็นเชิงประจักษ์ถึงความสัมพันธ์ของการได้รับยาอีริโธรมัยซินทั้งในเด็กก่อนคลอดและเด็กทารกหลังคลอดกับการเกิดการตีบตันช่องไพลอริค (pyloric stenosis) ซึ่งเป็นทางผ่านของอาหารจากกระเพาะอาหารลงสู่ลำไส้เล็ก [1] [26] การใช้ยาอีริโรมัยซิน (โดยเฉพาะอย่างยิ่ง การใช้ยาเป็นระยะเวลานานในขนาดที่มีฤทธิ์ในการฆ่าเชื้อแบคทีเรีย รวมไปถึงการได้รับผ่านทางน้ำนม) ในทารกแรกเกิดอาจนำไปสู่การเกิดการตีบตันช่องไพลอริคได้ [27][28] การใช้ยาอีริโรมัยซินเพื่อรักษาภาวะ ที่มีกระแสเลือดไปเลี้ยงลำไส้ลดลงจนทำให้ทารกรับนมไม่ได้ (feeding intolerance) พบว่าไม่มีความสัมพันธ์กับการเกิดการหนาตัวของกล้ามเนื้อหูรูดไพลอริคจนทำให้เกิดการตีบตันของช่องไพลอริค (hypertrophic pyloric stenosis ) [27] นอกจากนี้ ยังพบว่าอีริโธรมัยซิน เอสไทเลทมีความสัมพันธ์กับการเกิดโรคพิษต่อตับชนิดผันกลับได้ (reversible hepatotoxicity) ในหญิงตั้งครรภ์ โดยยาดังกล่าวจะทำให้เกิดการเพิ่มขึ้นของเอนไซม์ glutamic-oxaloacetic transaminase ในกระแสเลือด จึงไม่แนะนำให้ใช้ยาดังกล่าวในหญิงที่อยู่ระหว่างการตั้งครรภ์ ยิ่งไปกว่านั้นแล้ว หลักฐานเชิงประจักษ์ทางการแพทย์บางแหล่งค้นพบว่ายาดังกล่าวอาจทำให้เกิดพิษต่อตับได้เช่นกันในกลุ่มประชากรทั่วไป[29] ส่วนผลข้างเคียงต่อระบบประสาทส่วนกลางนั้น พบว่าการได้รับอีริโธรมัยซินอาจทำให้เกิดความผิดปกติทางจิต (psychotic reaction), ฝันร้าย (nightmares) และเหงื่อออกตอนกลางคืน (night sweats) ได้ [30] ทั้งนี้ การใช้ยาอีริโธรมัยซินรวมกับยาเม็ดคุมกำเนิดชนิดรับประทาน อาจทำให้ประสิทธิภาพของยาเม็ดคุมกำเนิดลดลง เนื่องจากอีริโธรมัยซินมีผลต่อเชื้อประจำถิ่น (Normal flora) ในลำไส้ จึงมีผลต่อกระบวนการดูดซึมยาฮอร์โมนกลับ (enterohepatic circulation) ได้ นอกจากนี้แล้ว อีริโธรมัยซินยังมีฤทธิ์ยับยั้งการทำงานของระบบ cytochrome P450 ซึ่งทำหน้าที่ในการเปลี่ยนแปลงยาหลากหลายชนิด ดังนั้น เมื่อใช้ยาอีริโธรมัยซินร่วมกับยาชนิดอื่น อาจทำให้ระดับของยาอื่นที่ใช้ร่วมเปลี่ยนแปลงไป จนเกิดอันตรายได้ เช่น ยาวาร์ฟาริน (warfarin) เป็นต้น[1][31]
การสังเคราะห์[แก้]
เป็นเวลามากกว่าสามทศวรรษแล้วหลังจากการค้นพบตัวยาและฤทธิ์ในการต้านเชื้อแบคทีเรียของอีริโรมัยซินเอ นักวิจัยที่เกี่ยวข้องต่างก็พยายามที่จะสังเคราะห์ยาชนิดดังกล่าวขึ้นให้ได้ภายในห้องปฏิบัติการ อย่างไรก็ตาม ด้วยเหตุที่ยาชนิดดังกล่าวมี stereospecific carbon มากถึง 10 ตำแหน่ง และมีหมู่แทนที่ที่จำเพาะเจาะจงหลากหลายตำแหน่งทำให้เป็นการยากลำบากที่จะสังเคราะห์อีริโธรมัยซินเอขึ้นในห้องปฏิบัติการได้อย่างครบถ้วนสมบูรณ์เหมือนต้นแบบ[32] การสังเคราะห์โครงสร้างที่มีความสัมพันธ์กับอีริโรมัยซินเอและสารตั้งต้น อย่าง 6-deoxyerythronolide B ได้สำเร็จ เป็นการค้นพบแนวทางใหม่ที่เป็นไปได้ที่จะการสังเคราะห์อีริโรมัยซิน และยาปฏิชีวนะกลุ่มแมคโครไลด์อื่นขึ้นมาได้ในห้องปฏิบัติการ[33] อย่างไรก็ตาม ถึงแม้จะมีนักวิทยาศาสตร์หลากหลายแขนง อย่างเช่น Robert Burns Woodward นักเคมีอินทรีย์ชาวอเมริกันที่ได้พยายามที่จะสังเคราะห์ยาอีริโรมัยซินเอขึ้นมาจากห้องปฏิบัติ แต่ความพยายามเหล่านั้นก็ประสบล้มเหลวในที่สุด [14][15][16] โดยกระบวนการสังเคราะห์โดยสังเขปเริ่มจากการสังเคราะห์จากตำแหน่งที่ (7) และ (8) จากนั้นนำสารสังเคราะห์ทั้งสองที่ได้มาทำปฏิกิริยากัน สารที่ได้จากปฏิกิริยาจะเป็นสารตั้งต้นในการเกิดปฏิกิริยาในลำดับขั้นต่อๆไป ได้แก่ การเกิดปฏิกิริยาไฮโดรไลสิส (Hydrolysis) และปฏิกิริยาการสร้างสารกลุ่มอัลดอลเพื่อให้เป็น stereospecific centers ของโครงสร้าง (stereospecific aldolization) สารประกอบอีโนน (enone) บริสุทธ์ที่ได้ในขั้นตอนสุดท้ายจะถูกเปลี่ยนเป็นสาร dithiadecalin (9) โดยปฏิกิริยารีดักชัน (reduction) และออกซิเดชัน (oxidation) จากนั้น dithiadecalin ที่ได้จะถูกเปลี่ยนเป็นสารประกอบคีโตน (10) และอัลดีไฮด์ (11) ในที่สุด
รูปแบบยาที่มีจำหน่าย[แก้]
ในปัจจุบัน อีริโธรมัยซินมีทั้งในรูปแบบยาเม็ดชนิดแตกตัวในลำไส้ (enteric-coated tablets), ยาแคปซูลชนิดออกฤทธิ์เนิ่น (slow-release capsules), ยาน้ำแขวนตะกอน (oral suspensions), ยาหยอดตา (ophthalmic solutions), ขี้ผึ้ง (ointments), เจล (gels), ยาแคปซูลชนิดแตกตัวในลำไส้ (Enteric-coated Capsules), ยาเม็ดธรรมดา (Non Enteric-coated tablets), ยาแคปซูลธรรมดา (Non Enteric-coated capsules) และในรูปแบบยาฉีด (injections)

รายการดังต่อไปนี้เป็นรายการยาอีริโรมัยซินชนิดรับประทานที่มีจำหน่าย:[34]
- erythromycin base (ชนิดแคปซูล, ชนิดเม็ด)
- erythromycin estolate (ชนิดแคปซูล, ยาน้ำแขวนตะกอน, ชนิดเม็ด), ห้ามใช้ในหญิงตั้งครรภ์ [1][26]
- erythromycin ethylsuccinate (ยาน้ำแขวนตะกอน, ชนิดเม็ด)
- erythromycin stearate (ยาน้ำแขวนตะกอน, ชนิดเม็ด)
รายการดังต่อไปนี้เป็นรายการยาอีริโรมัยซินชนิดฉีดที่มีจำหน่ายในประเทศไทย:[34]
- erythromycin gluceptate
- erythromycin lactobionate
ชื่อการค้าของอีริโธรมัยซิน ได้แก่ Robimycin, E-Mycin, E.E.S. Granules, E.E.S.-200, E.E.S.-400, E.E.S.-400 Filmtab, Erymax, Ery-Tab, Eryc, Ranbaxy, Erypar, EryPed, Eryped 200, Eryped 400, Erythrocin Stearate Filmtab, Erythrocot, E-Base, Erythroped, Ilosone, MY-E, Pediamycin, Zineryt, Abboticin, Abboticin-ES, Erycin, PCE Dispertab, Stiemycine, Acnasol, และ Tiloryth.
ส่วนประกอบ[แก้]
อีริโธรมัยซินที่ได้มาตรฐานมักประกอบไปด้วยตัวยา 4 ชนิด คือ อีริโธรมัยซิน เอ, บี, ซี, และ ดี ซึ่งสัดส่วนของตัวยาสำคัญทั้ง 4 ชนิดนี้อาจแตกต่างกันไปตามรอบที่ผลิต และพบว่าในตัวยาสำคัญทั้ง 4 ชนิดนี้ อีริโรมัยซิน เอ เป็นชนิดที่มีฤทธิ์ต้านเชื้อแบคทีเรียแรงที่สุด ตามมาด้วยอีริโธรมัยซิน บี ส่วนอีริโธรมัยซิน ซี และ ดี นั้นพบว่ามีฤทธิ์ต้านเชื้อแบคทีเรียประมาณครึ่งหนึ่งของอีริโธรมัยซิน เอ[35] [36] ตัวยาสำคัญทั้ง 4 ชนิดนี้สามารถแยกออกมาเป็นสารบริสุทธิ์เพื่อจุดประสงค์ในการศึกษาวิจัยคุณสมบัติของตัวยาแต่ละชนิดได้
ชนิดของแบคทีเรียที่ไวต่อยา (Spectrum of susceptibility)[แก้]
อีริโธรมัยซินสามารถใช้ในการรักษาโรคติดเชื้อที่มีสาเหตุมาจากแบคทีเรียที่ไวต่อยานี้ได้ เช่น การติดเชื้อบริเวณผิวหนัง การติดเชื้อในทางเดินหายใจส่วนบน เป็นต้น เชื้อเหล่านั้น ได้แก่ เชื้อในสกุล (genus) Streptococcus, Staphylococcus, และ Haemophilus เมื่อเปรียบเทียบการออกฤทธิ์ครอบคุลมเชื้อต่างๆกับยาปฏิชีวนะชนิดอื่นในกลุ่มเดียวกัน หรือกลุ่มอื่น ได้ผลดังตารางต่อไปนี้[2]
| เชื้อ | Erythromycin | Azithromycin | Clarithromycin | Clindamycin | Chloramphenicol | Doxycycline | Minocycline | Ciprofloxacin | Ofloxacin |
|---|---|---|---|---|---|---|---|---|---|
| Strephylococcus Group A, B, C, G | ± | ± | ± | + | + | ± | + | ± | ± |
| S. pneumoniae | + | + | + | + | + | + | + | ± | ± |
| Enterococcus faecalis | 0 | 0 | 0 | 0 | ± | 0 | 0 | ** | ** |
| Enterococcus faecium | 0 | 0 | 0 | 0 | ± | 0 | 0 | 0 | 0 |
| S. aureus (MSSA) | ± | + | + | + | ± | ± | + | + | + |
| S. aureus (MRSA) | 0 | 0 | 0 | 0 | 0 | ± | ± | 0 | 0 |
| S. aureus (CA-MRSA) | ± | ± | ± | ± | N/A | + | + | ± | N/A |
| S.epidermidis | ± | 0 | 0 | 0 | 0 | 0 | 0 | + | + |
| C. jeikeium | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| L. monocytogenes | + | + | + | N/A | + | + | + | + | 0 |
| N. gonorrhea | ± | ± | ± | 0 | + | ± | ± | +1 | +1 |
| N. meningitidis | + | + | N/A | 0 | + | + | + | + | + |
| M. catharrhalis | + | + | + | 0 | + | + | + | + | + |
| H. influenzae | ± | + | + | 0 | + | + | + | + | + |
| Aeromonas | N/A | N/A | N/A | N/A | + | + | + | + | + |
| E. coli | 0 | 0 | 0 | 0 | + | + | + | + | + |
| Klepsiella sp. | 0 | 0 | 0 | 0 | ± | ± | ± | + | + |
| E. coli/Kleps. sp. ESBL+ | 0 | 0 | 0 | 0 | ± | ± | ± | + | + |
| E. coli/Kleps. sp. KPC+ | N/A | N/A | N/A | N/A | N/A | N/A | N/A | N/A | N/A |
| Enterobactor sp. | 0 | 0 | 0 | 0 | 0 | 0 | 0 | + | + |
| Salmonella sp. | 0 | ± | 0 | 0 | + | ± | ± | + | + |
| Shigella sp. | 0 | ± | 0 | 0 | + | ± | ± | + | + |
| Serratia marcescens | 0 | 0 | 0 | 0 | 0 | 0 | 0 | + | + |
| Proteus vulgaris | 0 | 0 | 0 | 0 | ± | 0 | 0 | + | + |
| Acinetobacter sp. | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ± | ± |
| Ps. aeruginosa | 0 | 0 | 0 | 0 | 0 | 0 | 0 | + | ± |
1 ความชุกของ quinolones-resistant CG มีความแตกต่างกันในแต่ละประเทศ ซึ่งพบความชุกอยู่ระหว่าง <1% ถึง 30.9% ในทวีปยุโรป, และพบมากกว่า 90% ในไต้หวัน และจากข้อมูลปี ค.ศ. 2006 พบว่าในสหรัฐอเมริการพบอุบัติการณ์ดังกล่าวประมาณ 6.7% CDC จึงไม่แนะนำให้ใช้ยากลุ่มฟลูออโรควิโนโลนส์ (Fluoroquinolones) เป็นทางเลือกแรกในการรักษาโรคติดเชื้อที่มีสาเหตุจากเชื้อกลุ่ม Gonococcus[37][5]
+ = มีประสิทธิภาพในการรักษา หรือเชื้อมีความไวต่อยามากกว่า 60%; ± = ยังขาดผลการศึกษาที่เด่นชัดในทางคลินิก หรือเชื้อมีความไวต่อยา 30%-60%; 0 = ไม่มีประสิทธิภาพในการรักษา หรือเชื้อมีความไวต่อยาน้อยกว่า 30%; N/A = ไม่มีข้อมูล
** เชื้อส่วนใหญ่มีความไวต่อยา 30%-60% หรือยังขาดผลการศึกษาทางคลินิกที่เด่นชัด แต่สามารถใช้ได้ในกรณีที่เป็นการติดเชื้อในระบบทางเดินปัสสาวะ และไม่ใช้ในกรณีที่มีติดเชื้อในกระแสเลือด
กลไกการออกฤทธิ์[แก้]
อีริโธรมัยซินมีฤทธิ์ยับยั้งการเจริญเติบโตของเชื้อแบคทีเรีย (Bacteriostatic activity) โดยเฉพาะอย่างยิ่ง เมื่อระดับยามีความเข้มข้นสูง,[38] แต่กลไกการออกฤทธิ์ของยาดังกล่าวยังไม่เป็นที่ทราบแน่ชัดนัก คาดว่ายาดังกล่าวน่าจะออกฤทธิ์จับกับหน่วยย่อย 50s (50s subunit) บนไรโบโซมของแบคทีเรีย ทำให้การสังเคราะห์โปรตีนและโครงสร้างต่างๆของเซลล์ที่ต้องใช้โปรตีนเป็นส่วนประกอบ รวมไปถึงกระบวนการทำงานต่างๆ ที่สัมพันธ์กับโปรตีนซึ่งมีความจำเป็นสำหรับการดำรงชีวิตของแบคทีเรียและการจำลองตัวของดีเอ็นเอ (DNA replication) หยุดชะงักลง[1][38] นอกจากนี้ อีริโธรมัยซินยังมีผลรบกวนกระบวนการ aminoacyl translocation ซึ่งจะขัดขวางการส่งผ่าน tRNA จาก A site ของ rRNA complex ไปยัง P site ของ rRNA complex เมื่อเชื้อแบคทีเรียไม่สามารถเกิดกระบวนการ translocation ดังกล่าวได้ และ A site ยังคงถูกจับอยู่ด้วย tRNA โมเลกุลเดิม ทำให้ tRNA โมเลกุลที่จะนำกรดอะมิโนอีกโมเลกุลมาต่อเข้ากับสาย polypeptide หยุดชะงักลง ผลจากการรบกวนกระบวนการสังเคราะห์โปรตีนของอีริโธรมัยซินทำให้แบคทีเรียขาดโปรตีนที่จำเป็นต่อการทำงานในกระบวนการต่างๆของเซลล์ และตายไปในที่สุด [39]
คุณสมบัติทางเภสัชพลนศาสตร์และเภสัชจลนศาสตร์[แก้]
อีริโธรมัยซินสามารถทำให้สูญเสียสภาพได้ง่ายในสภาวะที่เป็นกรด ซึ่งรวมถึงกรดในทางเดินอาหาร ดังนั้นอีริโธรมัยซินที่มีใช้ในปัจจุบันทุกรูปแบบจึงถูกทำให้อยู่ในรูปแบบยาเม็ดเคลือบ หรืออยู่ในรูปแบบเกลืองที่มีความคงทนต่อกรดมากขึ้น หรือในรูปของเอสเทอร์ (esters) เช่น erythromycin ethyl succinate เป็นต้น อีริโธรมัยซินสามารถถูกดูดซึมได้อย่างรวดเร็วจากทางเดินอาหาร และกระจายไปยังเนื้อเยื่อต่างๆ รวมถึง phagocyte ได้ค่อนข้างดี การที่มีระดับความเข้มข้นของอีริโธรมัยซินใน phagocyte ในปริมาณที่สูง ทำให้ระหว่างเกิดกระบวนการกลืนกินเชื้อของ phagocyte (phagocytosis) ทำให้มีอีริโธรมัยซินปริมาณมากถูกปลดปล่อยออกมา [40]
รายละเอียดคุณสมบัติทางเภสัชพลนศาสตร์และเภสัชจลนศาสตร์อื่นๆของอีริโธรมัยซิน ดังแสดงต่อไปนี้[1][41]
| คุณสมบัติ | รายละเอียด |
|---|---|
| การดูดซึม | การดูดซึมค่อนข้างหลากหลายขึ้นกับรูปแบบของยาและชนิดของเกลือที่บริหาร โดยทั่วไปการให้ยาในรูปแบบเกลือ (salt form) จะถูกดูดซึมได้ดีกว่าการให้ยาในรูปแบบพื้นฐาน (base form) โดยทั่วไปสัดส่วนการดูดซึมจะอยู่ที่ประมาณ 18% ถึง 45%; อีริโธรมัยซินในรูปแบบ ethylsuccinate จะถูกดูดซึมได้ดีเมื่อรับประทานยาพร้อมกับอาหาร |
| การกระจายยา | การแพร่จากกระแสเลือดเข้าสู่น้ำหล่อเลี้ยงสมองและไขสันหลัง (Cerebrospinal fluid; CSF) ของอีริโธรมัยซินนั้นเกิดขึ้นได้น้อย ถึงแม้จะมีการอักเสบก็ตาม โดยในภาวะที่ไม่มีการอักเสบของเยื่อหุ้มสมอง อีริโทรมัยซินจะสามารถแพร่ผ่านเข้าไปสู่ CSF ได้ประมาณ 2% ถึง 13% แต่ในกรณีภาวะที่มีการอักเสบของเยื่อหุ้มสมองอาจเพิ่มขึ้นเป็น 7%-25% |
| การจับกับโปรตีนในกระแสเลือด | อีริโธรมัยซินในรูปแบบ base form สามารถจับกับโปรตีนในกระแสเลือดได้ประมาณ 73% ถึง 81% |
| การเปลี่ยนแปลงยา | โดยทั่วไปเกิดการเปลี่ยนผ่านปฏิกิริยา Demethylation ที่ CYP3A4 ของตับ |
| ค่าครึ่งชีวิตการกำจัดยา | ประมาณ 1.5-2 ชั่วโมง แต่ในกรณีที่ผู้ป่วยไตเรื้อรังระยะสุดท้ายอาจมากถึง 5-6 ชั่วโมง |
| ระยะเวลาที่ระดับยาในกระแสเลือดขึ้นถึงระดับสูงสุด | สำหรับ base form ประมาณ 4 ชั่วโมง, เกลือ Ethylsuccinate ประมาณ 0.5-2.5 ชั่วโมง; อาหารมีผลรบกวนการดูดซึมยา อาจทำให้การดูดซึมยาแตกต่างกันออกไปในแต่ละบุคคล |
| การกำจัดยา | โดยทั่วไปอีริโธรมัยซินจะถูกขับทางอุจจาระเป็นหลัก ส่วนการขับออกทางปัสสาวะในรูปแบบที่ไม่เปลี่ยนแปลง (unchanged drug) คิดเป็นร้อยละ 2-15 ของปริมาณยาทั้งหมด |
การเปลี่ยนแปลงยาของร่างกาย[แก้]
ส่วนใหญ่อีริโธรมัยซิยจะถูกเปลี่ยนแปลงโดยปฏิกิริยา demethylation ในตับโดยเอนไซม์ CYP3A4 ช่องทางหลักของการขับอีริโธรมัยซินออกจากร่างกาย คือ การขับออกทางน้ำดี และมีบางส่วนถูกขับออกทางปัสสาวะ ประมาณร้อยละ 2-15 ของยาที่ถูกขับออกนี้จะอยู่ในรูปแบบที่ไม่เปลี่ยนแปลง โดยค่าครึ่งชีวิตการกำจัด (elimination half-life) ของอีริโธรมัยซินของคนที่มีการทำงานของไตปรกตินั้นมีค่าอยู่ระหว่าง 1.5 - 2.0 ชั่วโมง ส่วนผู้ที่มีภาวะไตวายระยะสุดท้าย (End stage renal disease; ESRD) อาจมีค่าสูงถึง 5-6 ชั่วโมง โดยส่วนใหญ่แล้วระดับอีริโธรมัยซินในกระแสเลือดจะขึ้นถึงระดับสูงสุดที่ระยะเวลาประมาณ 4 ชั่วโมงหลังจากการรับประทานยา แต่สำหรับอีริโธรมัยซินในรูปแบบ ethylsuccinate ระดับสูงสุดในกระแสเลือดจะเกิดขึ้นภายในระยะเวลาเพียง 0.5-2.5 ชั่วโมงหลังการรับประทานยาเท่านั้น อย่างไรก็ตาม เวลาที่ระดับยาในเลือดขึ้นถึงจุดสูงสุดนั้นอาจช้ากว่าปรกติได้ในผู้ที่รับประทานยาร่วมกับอาหาร เนื่องจากอาหารมีผลรบกวนการดูดซึมยา [1] [41]
อีริโธรมัยซินสามารถแพร่ผ่านรกของขับออกทางน้ำนมได้ อย่างไรก็ตาม สมาคมกุมารเวชศาสตร์แห่งสหรัฐอเมริกา (The American Association of Pediatrics) ได้ลงความเห็นไว้ว่า การใช้ยาอีริโธรมัยซินในหญิงให้นมบุตรนั้นมีความปลอดภัย เนื่องจากไม่พบความผิดปกติของทารกที่ได้รับนมจากแม่ที่ได้รับยาอีริโธรมัยซิน [42][43] การดูดซึมยาอีริโธรมัยซินในหญิงในครรภ์นั้นพบว่ามีความแตกต่างกันออกในแต่ละบุคคล ส่วนมากมักพบว่าหญิงตั้งครรภ์มักมีระดับยาอีริโธรมัยซินในเลือดต่ำกว่าคนทั่วไป[41]
การเกิดปฏิกิริยาระหว่างยา[แก้]
อีริโธรมัยซินถูกเปลี่ยนแปลงโดยเอนไซม์ในระบบไซโตโครม พี450 (cytochrome P450) โดยเฉพาะอย่างยิ่ง โดยไอโซเอนไซม์ตระกูล CYP3A [31] ซึ่งการทำงานของไอโซเอนไซม์ดังกล่าวนั้นสามารถถูกเหนี่ยวนำหรือยับยั้งได้ด้วยยาชนิดอื่นหลายชนิด (เช่น เด็กซาเมธาโซน เป็นต้น) ซึ่งจะทำให้ประสิทธิภาพในการเปลี่ยนแปลงยาหลายชนิด ซึ่งรวมถึงอีริโธรมัยซิน เปลี่ยนแปลงไป ซึ่งถ้าหากได้รับอีริโธรมัยซินร่วมกับสารหรือยาอื่นที่มีผลลดการทำงานของ CYP3A เช่น ยาลดไขมันในเลือด simvastatin, lovastatin, หรือ atorvastatin จะทำให้ระดับยาอีริโธรมัยซินในกระแสเลือดเพิ่มสูงขึ้นจนทำให้เกิดอาการไม่พึงประสงค์จากยาได้ โดยเฉพาะอย่างยิ่งผลจากการเกิดปฏิกิริยาระหว่างอีริโธรมัยซินกับซิมวาสเตติน (simvastatin) จะทำให้ระดับของซิมวาสเตตินในกระแสเลือดเพิ่มสูงขึ้น จนทำให้เกิดอาการข้างเคียงที่รุนแรงของระบบกล้ามเนื้ออย่าง rhabdomyolysis ได้ ยาอีกกลุ่มที่อาจทำให้เกิดอาการข้างเคียงที่รุนแรงเมื่อใช้ร่วมกับอีริโธรมัยซิน คือ ยารักษาไมเกรน ได้แก่ ergotamine และ dihydroergotamine โดยยาดังกล่าวทั้งสองชนิดล้วนถูกเปลี่ยนแปลงที่ CYP3A4 เป็นหลัก เมื่อให้ร่วมกับอีริโธรมัยซินจะทำให้การเปลี่ยนยาดังกล่าวลดลง ส่งผลให้ระดับยาในเลือดเพิ่มสูงขึ้น จนเกิดอาการข้างเคียงจากยาในที่สุด [30] ผลจากการศึกษาแบบ cohort study เมื่อไม่นานมานี้พบว่ามีการเกิดอาการข้างเคียงที่สัมพันธ์กับการใช้ยาอีริโธรมัยซินที่รุนแรงจนทำให้เสียชีวิตได้ในทันที ได้แก่ ภาวะหัวใจห้องล่างเต้นเร็วกว่าปกติ (Ventricular tachycardia) และ การเสียชีวิตฉับพลันจากโณคหัวใจ (Sudden cardiac death) ซึ่งการเกิดความผิดปกติดังกล่าวมีความสัมพันธ์กับการใช้ยาอื่นที่มีผลรบกวนการทำงานของ CYP3A4 จนทำให้การเปลี่ยนแปลงยาอีริโธรมัยซินของร่างกายลดน้อย (เช่น verapamil, diltiazem) [44] ดังนั้น จึงไม่ควรใช้อีริโธรมัยซินร่วมกับยากลุ่มดังกล่าว หรือยาอื่นที่มีผลทำให้ช่วง QT segment ยาวนานขึ้น (prolnged QT interval) เช่น terfenadine (Seldane, Seldane-D), astemizole (Hismanal), cisapride (Propulsid, ถูกถอนทะเบียนยาในหลายประเทศ เนื่องจากทำให้เกิด prolong QT interval ได้มาก) และ pimozide (Orap) รวมไปถึง Theophylline, ซึ่งใช้กันเป็นอย่างมากในผู้ป่วยโรคหอบหืด (asthma) หรือโรคปอดอุดกั้นเรื้อรัง (chronic obstructive pulmonary disease; COPD)
อีริโธรมัยซินอาจมีผลต่อกระบวนการสื่อประสาทของระบบกล้ามเนื้อ (neuromuscular transmission) โดยออกฤทธิ์ที่ presynaptic neurons ดังนั้นอีริโธรมัยซินอาจมีผลทำให้อาการของโรคกล้ามเนื้ออ่อนแรง (myasthenia gravis) กำเริบหรือรุนแรงขึ้นได้ นอกจากนี้ยาปฏิชีวนะในกลุ่มเดียวกันกับอีริโธรมัยซิน อย่างเทลิโธรมัยซิน (Telitromycin) และอะซิโธรมัยซิน (Azithromycin) ก็พบรายงานว่าทำให้เกิดความผิดปกติดังกล่าวได้เช่นกัน [45]
นอกจากนี้ ยังไม่แนะนำให้ใช้อีริโธรมัยซินร่วมกับผลิตภัณฑ์ที่มีส่วนผสมของคลินดามัยซิน (Clindamycin) ถึงแม้จะเป็นผลิตภัณฑ์ในรูปแบบทาบริเวณผิวหนัง เช่น Duac , Clinda M หรือ BenzaClin ก็ตาม รวมไปถึงหลีกเลี่ยงการใช้ร่วมกับอนุพันธ์ของอีริโธรมัยซิน (เช่น ใช้คลินดามัยซินร่วมกับ mitecinal) เนื่องจากยาทั้งสองชนิดจะมีผลต้านฤทธิ์ซึ่งกันและกัน (Antagonism) ก่อให้เกิดความล้มเหลวในการรักษาได้ในที่สุด [46][47]
นอกจากนี้แล้วอีริโธรมัยซินและด็อกซีซัยคลิน (Doxycycline) ยังสามารถออกฤทธิ์เสริมกัน (synergistic effects) ในการฆ่าเชื้อแบคทีเรีย (E. coli) ในอัตรามากเกินกว่าผลรวมของความแรงของยาทั้งสองชนิดรวมกัน อย่างไรก็ตาม การเสริมฤทธิ์กันของยาทั้งสองชนิดนี้เกิดขึ้นเพียงชั่วคราวเท่านั้น หลังจากนั้นประมาณ 72 ชั่วโมง ยาทั้งสองจะออกฤทธิ์ต้านซึ่งกันและกันแทน (antagonistic effect) โดยประสิทธิภาพในการฆ่าเชื้อแบคทีเรียของยาทั้งสองชนิดจะลดลงประมาณร้อยละ 50 เมื่อเปรียบเทียบกับการบริหารยาทั้งสองแยกจากกัน[48]
อนุพันธ์ของอีริโธรมัยซิน[แก้]
- Ansamycin
- Azithromycin (Zithromax, Zitromax, Sumamed)
- Carbomycin
- Cethromycin
- Clarithromycin (Biaxin)
- Dirithromycin (Dynabac)
- Mitemcinal
- Oleandomycin
- Roxithromycin (Rulid, Surlid, Roxid)
- Spiramycin
- Telithromycin
- Tylosin (Tylocine)
บรรณานุกรม[แก้]
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 Lacy FC, Armstrong LL, Goldman PM, Lance LL, editors. Drug Information Handbook with international trade name index. 18th edition, New Tork, Lexi-Comp®, 2014, p. 585-588, ISBN 978-1-59195-255-8
- ↑ 2.0 2.1 Gilbert DN, Chambers FH, Elliopoulos MG, Saag SM, et al. The Sandford Guide to Antimicrobial Therapy. 44th edition, Sperryville (VA), Sandford Guide, 2014, p. 66-71, ISBN 978-1-9308-0878-2
- ↑ 3.0 3.1 EspaceNet. "Bibliographic data: US2653899 (A) ― 1953-09-29". สืบค้นเมื่อ 16 August 2015.
- ↑ 4.0 4.1 Thomas J. Dougherty and Michael J. Pucci (2011). "Antibiotic Discovery and Development". Springer. doi:10.1007/978-1-4614-1400-1. ISBN 978-1-4614-1399-8.
- ↑ 5.0 5.1 Centers for Disease Control and Prevention. "Update to CDC's Sexually Transmitted Diseases Treatment Guidelines, 2006: Fluoroquinolones No Longer Recommended for Treatment of Gonococcal Infections". Department of Health and Human Services. สืบค้นเมื่อ 9 August 2015.
- ↑ 6.0 6.1 M. Camilleri, H.P. Parkman, M.A. Shafi, T.L. Abell and L. Gerson (2013). "Management of Gastroparesis". Am J Gastroenterol. 108: 18–37. doi:10.1038/ajg.2012.373.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 7.0 7.1 R. W. McCallum and O. Cynshi (2007). "Clinical trial: effect of mitemcinal (a motilin agonist) on gastric emptying in patients with gastroparesis – a randomized, multicentre, placebo-controlled study". Aliment Pharmacol Ther. pp. 1121–1130. สืบค้นเมื่อ 16 August 2015.
- ↑ P. F. Wiley , K. Gerzon , E. H. Flynn , M. V. Sigal Jr., O. Weaver , U. C. Quarck , R.R. Chauvette , R. Monahan (1957). "Erythromycin. X.1 Structure of Erythromycin". J. Am. Chem. Soc. 79 (22): 6062–6070. doi:10.1021/ja01579a059.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "WHO Model List of Essential Medicines" (PDF). World Health Organization. October 2013. สืบค้นเมื่อ 22 April 2014.
- ↑ Florence F. Hibionada (2005). "Remembering the battle of Dr. Abelardo Aguilar:Cure for millions, deprived of millions". The News Today. สืบค้นเมื่อ 16 August 2015.
- ↑ Johanna Son (1994). "MEDICINE-PHILIPPINES: Who Really Discovered Erythromycin ? (1) An Inter Press Service Feature". Inter Press Service News Agency. สืบค้นเมื่อ 16 August 2015.
- ↑ Robert C. Anderson, Paul N. Harris andK. K. Chen (1955). "Further toxicological studies with ilotycin® (Erythromycin, Lilly)". Journal of the American Pharmaceutical Association. 44 (4): 199–204. doi:10.1002/jps.3030440404.
- ↑ Nobel Media AB2015 (2015). "Robert B. Woodward - Biographical". Nobel Prize Prganization. สืบค้นเมื่อ 16 August 2015.
- ↑ 14.0 14.1 Woodward R. B., Logusch E., Nambiar K. P., Sakan K., Ward D. E., Au-Yeung , Balaram P., Browne L. J., Card P. J.; และคณะ (1981). "Asymmetric Total Synthesis of Erythromycin. 1. Synthesis of an Erythronolide A Seco Acid Derivative via Asymmetric Induction". J. Am. Chem. Soc. 103 (11): 3210–3213. doi:10.1021/ja00401a049.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 15.0 15.1 Woodward R. B., Logusch E., Nambiar K. P., Sakan K., Ward D. E., Au-Yeung , Balaram P., Browne L. J., Card P. J.; และคณะ (1981). "Asymmetric Total Synthesis of Erythromycin. 2. Synthesis of an Erythronolide A Lactone System". J. Am. Chem. Soc. 103 (11): 3213–3215. doi:10.1021/ja00401a050.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 16.0 16.1 Woodward R. B., Logusch E., Nambiar K. P., Sakan K., Ward D. E., Au-Yeung , Balaram P., Browne L. J., Card P. J.; และคณะ (1981). "Asymmetric Total Synthesis of Erythromycin. 3. Total Synthesis of Erythromycin". J. Am. Chem. Soc. 103 (11): 3215–3217. doi:10.1021/ja00401a051.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Project Gutenberg Self-Publishing Press (2015). "CLARITHROMYCIN". สืบค้นเมื่อ 16 August 2015.
- ↑ Peeters TL (2001). "GM-611 (Chugai Pharmaceutical)". Curr Opin Investig Drugs. 2 (4): 555–557. PMID 11566017.
- ↑ Kenji Yogo, Mitsu Onoma, Ken-ichi Ozaki, Masao Koto, Zen Itoh, and Satoshi Åmura (2008). "Effects of Oral Mitemcinal (GM-611), Erythromycin, EM-574 and Cisapride on Gastric Emptying in Conscious Rhesus MonkeysEffects of Oral Mitemcinal (GM-611), Erythromycin, EM-574 and Cisapride on Gastric Emptying in Conscious Rhesus Monkeys". Digestive Diseases & Sciences. 53 (4): 912.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Weber FH Jr (April 1993). "Erythromycin: a motilin agonist and gastrointestinal prokinetic agent". American Journal of Gastroenterology. 88 (4): 485–90. PMID 8470625.
- ↑ V. J. Kopp, D. C. Mayer, and N. J. Shaheen (1997). "Intravenous Erythromycin Promotes Gastric Emptying Prior to Emergency Anesthesia". Anesthesiology. 87: 703–705.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ N. S. Winstead, and C. M. Wilcox (2007). "Erythromycin prior to endoscopy for acute upper gastrointestinal haemorrhage: a cost-effectiveness analysis". Alimentary Pharmacology & Therapeutics. 26 (10): 1371–1377.
- ↑ A. Ahmed,and S. Quraishi (2006). "Aetiological causes of reversible sensorineural hearing loss". The Internet Journal of Otorhinolaryngology. 6 (2).
- ↑ R.E. Brummett, and K. E. Fox (1989). "Vancomycin- and Erythromycin-Induced Hearing Loss in Humans" (PDF). Antimicrobial Agents and Chemotherapy. 6 (2): 791–796. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2018-07-18. สืบค้นเมื่อ 2015-08-16.
- ↑ J. Dylewski (1988). "Irreversible sensorineural hearing loss due to erythromycin". CMAJ. 139 (3): 230–231. PMC 1268068.
- ↑ 26.0 26.1 Lexicomp® OnlineTM. "Pregnancy and Lactation". สืบค้นเมื่อ 16 August 2015.
- ↑ 27.0 27.1 Maheshwai N (March 2007). "Are young infants treated with erythromycin at risk for developing hypertrophic pyloric stenosis?". Arch. Dis. Child. 92 (3): 271–3. doi:10.1136/adc.2006.110007. PMC 2083424. PMID 17337692.
- ↑ M. Lund, B. Pasternak, R. B. Davidsen, B. Feenstra, C. Krogh, L. J. Diaz, J. Wohlfahrt, and M. Melbye (2014). "Use of macrolides in mother and child and risk of infantile hypertrophic pyloric stenosis: nationwide cohort study". BMJ. 348: g1908. doi:10.1136/bmj.g1908.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ McCormack WM, George H, Donner A, Kodgis LF, Albert S, Lowe EW, Kass EH (1997). "Hepatotoxicity of erythromycin estoate during pregnancy". Antimicrob Agents Chemother. 12 (5): 630–5. doi:10.1128/AAC.12.5.630. PMC 429989. PMID 21610.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 30.0 30.1 Belgisch Centrum voor Farmacotherapeutische Informatie. "Erythromycin". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2012-11-14. สืบค้นเมื่อ 20 July 2008.
- ↑ 31.0 31.1 Hunt M.C., Watcins B.P., Saenger P., Stave M.G., Barlascini N., Watlington O.C., Wright T.J., and Guzelain S.P. (1992). "Heterogeneity of CYP3A isoforms metabolizing erythromycin and cortisol". Clinical Pharmacology and Therapeutics. 51 (1): 18–23. doi:10.1038/clpt.1992.3.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Pal S (2006). "A journey across the sequential development of macrolides and ketolides related to erythromycin". Tetrahedron. 62 (14): 3171–3200. doi:10.1016/j.tet.2005.11.064.
- ↑ Evans D. A., Kim A. S. (1997). "Synthesis of 6-Deoxyerythronolide B. Implementation of a General Strategy for the Synthesis of Macrolide Antibiotics". Tetrahedron Lett. 38: 53–56. doi:10.1016/S0040-4039(96)02258-7.
- ↑ 34.0 34.1 Drugs.com. "erythromycin (Oral route, Parenteral route)". สืบค้นเมื่อ 16 August 2015.
- ↑ I. O. Kibwage, J. Hoogmartens, E. Roets, H. Vanderhaeghe, L. Verbist, M. Dubost, C. Pascal, P. Petitjean, and G. Levol (1985). "Antibacterial activities of erythromycins A, B, C, and D and some of their derivatives". Antimicrob Agents Chemother. 28 (5): 630–633. PMC 176346.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ TOKU-E. "Erythromycin A, EvoPure® Susceptibility and Minimum Inhibitory Concentration (MIC) Data Issue date 08/15/2015" (PDF). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2015-09-27. สืบค้นเมื่อ 16 August 2015.
- ↑ Connie R. Mahon, Donald C. Lehman, and George Manuselis Jr (2011). Textbook of Diagnostic Microbiological. W.B. Saunders Company, ISBN 978-1-1460-6165-6
- ↑ 38.0 38.1 Katzung PHARMACOLOGY, 9e Section VIII. Chemotherapeutic Drugs Chapter 44. Chloramphenicol, Tetracyclines, Macrolides, Clindamycin, & Streptogramins
- ↑ J R Menninger and D P Otto (1982). "Erythromycin, carbomycin, and spiramycin inhibit protein synthesis by stimulating the dissociation of peptidyl-tRNA from ribosomes". Antimicrob Agents Chemother. 21 (5): 811–818. doi:10.1128/AAC.21.5.811. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2018-05-31. สืบค้นเมื่อ 2015-08-16.
- ↑ Martina Bosnar, Željko Kelnerić, Vesna Munić, Vesna Eraković, and Michael J. Parnham (2005). "Cellular Uptake and Efflux of Azithromycin, Erythromycin, Clarithromycin, Telithromycin, and Cethromycin". Antimicrob Agents Chemother. 49 (6): 2372–2377. doi:10.1128/AAC.49.6.2372-2377.2005.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 41.0 41.1 41.2 Lexicomp® OnlineTM. "Erythromycin". สืบค้นเมื่อ 16 August 2015.
- ↑ America academy of Padiatrics: committee on drug. "The Transfer of Drugs and Other Chemicals Into Human Milk" (PDF). The American Association of Pediatrics. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2016-03-05. สืบค้นเมื่อ 16 August 2015.
- ↑ Matsuda S. (1984). "Transfer of antibiotics into maternal milk". Biol Res Pregnancy Perinatol. 5 (2): 57–60. PMID 6743732.
- ↑ Ray WA, Murray KT, Meredith S, Narasimhulu SS, Hall K, and Stein CM (2004). "Erythromycin and the Risk of Sudden Death from Cardiac Causes". N Engl J Med. 351: 1089–96. doi:10.1056/NEJMoa040582.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ A Ahmed, and Z Simmons (2008). "Drugs Which May Exacerbate or Induce Myasthenia Gravis: A Clinician's Guide Drugs Which May Exacerbate or Induce Myasthenia Gravis: A Clinician's Guide". The Internet Journal of Neurology. 10 (2): 1–7.
- ↑ RxList Inc. "Cleosin (Clindamycin) Drug Interaction". สืบค้นเมื่อ 17 August 2015.
- ↑ WebMD. "Interaction between Clindamycin HCl oral and lincosamides-erythromycin". สืบค้นเมื่อ 17 August 2015.
- ↑ Pena-Miller R, Laehnemann D, Jansen G, Fuentes-Hernandez A, Rosenstiel P, Schulenburg H, Beardmore R (April 23, 2013). "When the most potent combination of antibiotics selects for the greatest bacterial load: the smile-frown transition". PLOS Biology. 11 (4): e1001540. doi:10.1371/journal.pbio.1001540. PMC 3635860. PMID 23630452.
แหล่งข้อมูลอื่น[แก้]
- "Erythromycin". Drug Information Portal. U.S. National Library of Medicine.
- U.S. Patent 2,653,899
