ไข้เด็งกี
| ไข้เด็งกี (Dengue fever) | |
|---|---|
| ชื่ออื่น | Dengue, breakbone fever[1][2] |
| ผื่นลักษณะเฉพาะของไข้เลือดออกเด็งกี | |
| สาขาวิชา | โรคติดเชื้อ |
| อาการ | ไข้ ปวดศีรษะ ปวดกล้ามเนื้อและข้อ ผื่น[1][2] |
| ภาวะแทรกซ้อน | เลือดออก ระดับเกล็ดเลือดต่ำ ความดันโลหิตต่ำจนช็อก[2] |
| การตั้งต้น | 3–14 วันหลังได้รับเชื้อ[2] |
| ระยะดำเนินโรค | 2–7 วัน[1] |
| สาเหตุ | ไวรัสเด็งกีจากยุงลาย (Aedes)[1] |
| วิธีวินิจฉัย | ตรวจพบแอนติบอดีต่อไวรัสหรืออาร์เอ็นเอไวรัส[2] |
| โรคอื่นที่คล้ายกัน | มาลาเรีย, ไข้เหลือง, ตับอักเสบเหตุไวรัส โรคฉี่หนู[3] |
| การป้องกัน | วัคซีนไข้เด็งกี ลดการสัมผัสยุง[1][4] |
| การรักษา | การบำบัดประคับประคอง สารน้ำทางหลอดเลือดดำ การเติมเลือด[2] |
| ความชุก | 390 ล้านคนต่อปี[5] |
| การเสียชีวิต | 4 หมื่นคนต่อปี[5] |
ไข้เด็งกี (อังกฤษ: Dengue fever) หรือในประเทศไทยนิยมเรียกว่า ไข้เลือดออก เป็นโรคติดเชื้อซึ่งระบาดในเขตร้อน เกิดจากการติดเชื้อไวรัสเด็งกี[1] ผู้ป่วยจะมีอาการไข้ ปวดศีรษะ ปวดกล้ามเนื้อ ปวดข้อ และมีผื่นลักษณะเฉพาะซึ่งคล้ายกับผื่นของโรคหัด ผู้ป่วยส่วนหนึ่งจะมีอาการรุนแรง จนกลายเป็นไข้เลือดออกเด็งกี (Dengue hemorrhagic fever) ที่เป็นอันตรายถึงชีวิต ซึ่งทำให้มีเลือดออกง่าย มีเกล็ดเลือดต่ำ และมีการรั่วของพลาสมา หรือรุนแรงมากขึ้นเป็นกลุ่มอาการไข้เลือดออกช็อก (Dengue shock syndrome) ซึ่งมีความดันโลหิตต่ำอย่างเป็นอันตรายได้[2]
ไข้เลือดออกติดต่อผ่านทางพาหะคือยุงหลายสปีชีส์ในจีนัส Aedes โดยเฉพาะ A. aegypti หรือยุงลายบ้าน ไวรัสเด็งกีมีชนิดย่อยอยู่สี่ชนิด การติดเชื้อไวรัสชนิดหนึ่งมักทำให้ผู้ป่วยมีภูมิคุ้มกันต่อไวรัสชนิดนั้น ๆ ไปตลอดชีวิต แต่มีภูมิคุ้มกันต่อไวรัสเด็งกีชนิดอื่น ๆ ในเวลาสั้น ๆ การติดเชื้อไวรัสเด็งกีชนิดอื่นในภายหลังเพิ่มความเสี่ยงของภาวะแทรกซ้อนรุนแรง การป้องกันโรคทำโดยลดจำนวนแหล่งเพาะพันธุ์และจำนวนของยุง และป้องกันมิให้ยุงลายกัด เพราะวัคซีนในทางพาณิชย์ยังมีข้อจำกัดในการนำมาใช้
ยังไม่มีวิธีจำเพาะในการรักษาไข้เลือดออก การรักษาหลัก ๆ เป็นการรักษาประคับประคอง สำหรับผู้ป่วยที่อาการไม่รุนแรงรักษาโดยการคืนน้ำ อาจใช้การกินทางปากหรือการให้ทางหลอดเลือดดำ และสำหรับผู้ป่วยที่มีอาการรุนแรงรักษาโดยให้สารน้ำหรือเลือดหรือองค์ประกอบของเลือดทางหลอดเลือดดำ อุบัติการณ์ของไข้เลือดออกเพิ่มขึ้นมากตั้งแต่คริสต์ทศวรรษ 1960 โดยมีผู้ป่วยติดเชื้อ 50-100 ล้านคนต่อปี โรคนี้มีการอธิบายเอาไว้ครั้งแรกตั้งแต่ ค.ศ. 1779 ส่วนไวรัสที่เป็นสาเหตุและกลไกการติดต่อนั้นค้นพบเมื่อช่วงต้นคริสต์ศตวรรษที่ 20 หลังสงครามโลกครั้งที่สองเป็นต้นมา ไข้เลือดออกได้กลายเป็นปัญหาที่สำคัญอย่างหนึ่งทั่วโลก มีประเทศที่เป็นพื้นที่ระบาดมากกว่า 110 ประเทศ ปัจจุบันนอกจากความพยายามลดจำนวนยุงแล้วยังมีความพยายามพัฒนาวัคซีนและยาที่ออกฤทธิ์โดยตรงกับไวรัสด้วย
อาการและอาการแสดง[แก้]
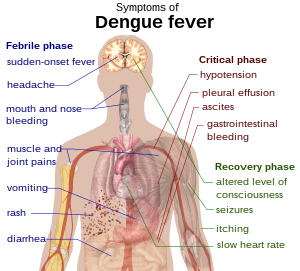
ผู้ติดเชื้อไวรัสเด็งกีส่วนใหญ่ไม่มีอาการ (80%) หรือมีอาการเพียงเล็กน้อย เช่น เป็นไข้ และไม่มีภาวะแทรกซ้อนใด ๆ[6][7][8] อีกส่วนหนึ่งมีอาการรุนแรงกว่า (5%) และเพียงส่วนน้อยเท่านั้นที่อาการรุนแรงมากจนเสี่ยงต่อการเสียชีวิต[6][8] ระยะฟักตัวของโรคอยู่ที่ 3-14 วัน แต่ส่วนใหญ่ประมาณ 4-7 วัน[9] ดังนั้นสำหรับคนที่ไม่ได้อาศัยอยู่ในพื้นที่ระบาด แต่เดินทางกลับมาจากพื้นที่ระบาด และเมื่อเดินทางกลับแล้ว มีไข้ตั้งแต่หลังวันที่ 14 มีโอกาสน้อยมากที่จะเป็นไข้เลือดออกเด็งกี[10] ผู้ป่วยเด็กส่วนใหญ่มีอาการไม่ต่างจากหวัดหรือกระเพาะอาหารกับลำไส้อักเสบ (ท้องร่วงและอาเจียน) [11] แต่มีโอกาสป่วยหนักได้มากกว่าผู้ใหญ่[10] แม้อาการระยะแรกจะค่อนข้างไม่รุนแรง แต่จะมีไข้สูงด้วย[12]
การดำเนินโรค[แก้]
อาการที่เป็นลักษณะเฉพาะของไข้เลือดออกคือมีไข้เฉียบพลัน ปวดศีรษะ (มักปวดหลังดวงตา) ปวดกล้ามเนื้อ ปวดข้อ และผื่น อาการปวดข้อและปวดกล้ามเนื้อนี้เป็นที่มาของชื่ออีกชื่อหนึ่งของไข้เลือดออก คือ break-bone fever ("ไข้กระดูกแตก") [6][13] การดำเนินโรคแบ่งเป็นสามระยะ คือระยะไข้ ระยะวิกฤต และระยะฟื้น[14]
ในระยะไข้ ผู้ป่วยจะมีไข้สูง มักสูงเกิน 40 องศาเซลเซียส มีอาการปวดตามตัวและปวดศีรษะ ระยะนี้มักกินเวลา 2-7 วัน[13][14] อาจมีอาการคลื่นไส้ อาเจียนด้วย[12] ผู้ป่วยระยะไข้ที่มีอาการ 50-80% จะมีผื่นขึ้น[13][15] ในวันแรกหรือวันที่สองของอาการป่วย ลักษณะเป็นปื้นแดง (erythema) หรือพบในวันที่ 4-7 ลักษณะเป็นผื่นคล้ายผื่นของโรคหัด[15][16] อาจมีจุดเลือดออก[14] (จุดเลือดออกนี้เกิดจากเส้นเลือดฝอยแตก และไม่ปรากฏเมื่อผิวหนังถูกกด) หรืออาจมีเลือดออกจากเยื่อบุปากและจมูกได้เล็กน้อย[10][13] ลักษณะเฉพาของอาการไข้ในไข้เลือดออก คือ ผู้ป่วยมีไข้ขึ้นสองรอบ โดยจะมีไข้ขึ้นครั้งหนึ่งก่อน จากนั้นไข้ลดลงไป และมีไข้ขึ้นอีก 1-2 วันให้หลัง แต่แบบแผนอาการไข้ของไข้เลือดออกมีความแตกต่างกันมาก และยังไม่มีข้อสรุปชัดเจนว่าแบบแผนไข้เฉพาะเช่นนี้ปรากฏขึ้นบ่อยเพียงใด[16][17]
ผู้ป่วยบางคนมีอาการดำเนินไปถึงระยะวิกฤต คือช่วงที่ไข้ลง ระยะนี้มักกินเวลา 1-2 วัน[14] ซึ่งผู้ป่วยอาจมีสารน้ำสะสมในช่องปอดและช่องท้องมากเนื่องจากสารน้ำรั่วออกจากผนังหลอดเลือดฝอยที่อยู่ในภาวะที่มีสภาพให้ซึมผ่านได้สูงขึ้นอย่างมาก ทำให้มีสารน้ำในระบบไหลเวียนน้อยลง และมีการไหลของเลือดไปเลี้ยงอวัยวะสำคัญน้อยลง[14] ระยะนี้อาจพบอวัยวะทำหน้าที่ผิดปกติ และมีเลือดออกมาก โดยมักออกจากทางเดินอาหาร[10][14] ภาวะช็อก (กลุ่มอาการช็อกจากไข้เลือดออก, dengue shock syndrome) และการมีเลือดออก ("ไข้เลือดออกเด็งกี", dengue hemorrhagic fever) นั้นพบในผู้ป่วยไข้เด็งกีไม่ถึง 5%[10] อย่างไรก็ดีผู้ที่เคยติดเชื้อไวรัสเด็งกีชนิดอื่นมาก่อนแล้ว (ติดเชื้อครั้งนี้เป็นครั้งที่สอง) จะมีความเสี่ยงสูงขึ้น[10][18] ระยะวิกฤตนี้พบบ่อยในเด็กและวัยรุ่นมากกว่าวัยอื่น แม้จะพบน้อย[12]
ระยะต่อมาคือระยะฟื้น สารน้ำที่รั่วออกจากหลอดเลือดจะไหลกลับคืนเข้ามา[14] ระยะนี้กินเวลา 2-3 วัน[10] ผู้ป่วยอาจรู้สึกดีขึ้นอย่างมาก อาจมีอาการคันมาก หรือหัวใจเต้นช้าได้[10][14] ในระยะนี้ผู้ป่วยอาจมีสารน้ำในร่างกายเกิน ซึ่งหากเสียสมดุลจนทำให้สมองบวม ก็อาจมีระดับการรู้สึกตัวลดลงหรือมีอาการชักได้[10] ผู้ป่วยผู้ใหญ่อาจรู้สึกล้าต่อไปอีกหลายสัปดาห์[12]
ปัญหาที่พบร่วม[แก้]
บางครั้งไข้เลือดออกอาจส่งผลต่อระบบอื่นของร่างกายได้[14] โดยอาจมีอาการของไข้เลือดออกร่วมด้วยหรือไม่ก็ได้[11] 0.5-6% ของผู้ป่วยที่มีอาการรุนแรง มีระดับความรู้สึกตัวลดลง ซึ่งอาจเป็นผลโดยตรงจากการติดเชื้อไวรัสที่สมอง ทำให้เกิดสมองอักเสบ หรือเป็นผลโดยอ้อมจากการที่อวัยวะสำคัญทำงานบกพร่อง เช่น ตับ[11][17]
ความผิดปกติอื่นทางระบบประสาทที่มีการรายงานในผู้ป่วยไข้เลือดออก เช่น ไขสันหลังอักเสบตามขวาง และกลุ่มอาการกิลแลง-บาร์เร[11] ความผิดปกติอื่นที่พบได้ แต่น้อย เช่น กล้ามเนื้อหัวใจอักเสบจากการติดเชื้อ และตับวายเฉียบพลัน เป็นต้น[10][14]
สาเหตุ[แก้]
โรคไข้เลือดออก เป็นโรคติดต่อที่เกิดจากยุงลาย (Aedes aegyti) ตัวเมีย บินไปกัดคนที่ป่วยเป็นไข้เลือดออกโดยเฉพาะช่วงที่มีไข้สูง ทำให้ได้รับเชื้อไวรัสเด็งกี เชื้อจะเพิ่มจำนวนในตัวยุงประมาณ 8-10 วัน เชื้อไวรัสแดงกี่จะไปที่ผนังกระเพาะและต่อมน้ำลายของยุง เมื่อยุงกัดคนก็จะแพร่เชื้อสู่คน เชื้อจะอยู่ในร่างกายคนประมาณ 2-7 วันในช่วงที่มีไข้ หากยุงกัดคนในช่วงนี้ก็จะรับเชื้อไวรัสมาแพร่ให้กับคนอื่น ซึ่งส่วนใหญ่มักจะเป็นเด็ก โรคนี้ระบาดในฤดูฝน ยุงลายชอบออกหากินในเวลากลางวันตามบ้านเรือน และโรงเรียน ชอบวางไข่ในน้ำสะอาดที่อยู่นิ่งๆ ตามภาชนะที่มีน้ำขัง เช่น ยางรถยนต์ กะลา กระป๋อง จานรองขาตู้กับข้าว แต่ไม่ชอบวางไข่ในท่อระบายน้ำ ห้วย หนอง คลอง บึง ฯลฯ
วิทยาไวรัส[แก้]
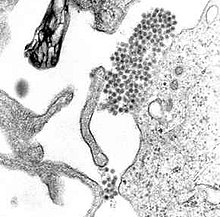
ไวรัสไข้เด็งกี (Dengue fever virus, DENV) เป็นไวรัสชนิดอาร์เอ็นเอไวรัสในวงศ์ Flaviviridae จีนัส Flavivirus ไวรัสอื่นในแฟมิลีนี้ เช่น ไวรัสไข้เหลือง ไวรัสเวสท์ไนล์ ไวรัสไข้สมองอักเสบเซนต์หลุยส์ ไวรัสไข้สมองอักเสบเจอี ไวรัสไข้สมองอักเสบซึ่งมีหมัดเป็นพาหะ ไวรัสโรคป่ายาซานูร์ และไวรัสไข้เลือดออกออมส์ก[17] ส่วนใหญ่ติดต่อโดยมีแมลงหรือแมง (ยุง หรือหมัด เห็บ เป็นต้น) เป็นพาหะ จึงเรียกรวมกันว่า arbovirus มาจาก arthropod-borne virus (ไวรัสซึ่งติดต่อโดยมีสัตว์ขาปล้อง [arthropod] เป็นพาหะ) [17]
จีโนมของไวรัสไข้เด็งกีมีขนาดประมาณ 11,000 นิวคลีโอไทด์เบส ถอดรหัสออกมาเป็นโมเลกุลโปรตีน 3 ชนิด (C, prM และ E) ซึ่งประกอบกันเป็นตัวไวรัส และโมเลกุลโปรตีนชนิดอื่น ๆ อีก 7 ชนิด (NS1, NS2a, NS2b, NS3, NS4a, NS4b, NS5) ซึ่งจะพบเฉพาะในเซลล์โฮสท์ที่ติดเชื้อ โดยเป็นโปรตีนที่มีความจำเป็นในการสร้างไวรัส[18][19] ไวรัส DENV มีอยู่ 4 สายพันธุ์หรือซีโรไทป์ คือ DENV-1, DENV-2, DENV-3 และ DENV-4[7] เชื่อกันว่าการติดเชื้อไวรัสซีโรไทป์หนึ่ง ๆ จะทำให้มีภูมิคุ้มกันต่อไวรัสซีโรไทป์นั้น ๆ ไปตลอดชีวิต และมีภูมิคุ้มกันต่อไวรัสซีโรไทป์อื่น ๆ ได้ในช่วงสั้น ๆ[7][13]
การติดต่อ[แก้]

ไวรัสเด็งกีติดต่อผ่านทางยุงลายเป็นหลัก โดยเฉพาะยุงลายบ้าน หรือ A. aegypti[7] ซึ่งมีถิ่นอาศัยในเขตศูนย์สูตร บริเวณพื้นที่ละติจูด 35° เหนือและใต้เส้นศูนย์สูตร ซึ่งสูงจากระดับน้ำทะเลไม่เกิน 1,000 เมตร[7] ส่วนใหญ่จะกัดคนในเวลากลางวัน[20] ยุงลายชนิดอื่น ๆ ที่เป็นพาหะของไข้เลือดออกได้แก่ A. albopictus, A. polynesiensis และ A.scutellaris[7] โฮสต์หลักของไวรัสไข้เลือดออกคือมนุษย์[7][17] แต่ก็สามารถพบเชื้อในไพรเมตชนิดอื่นนอกจากมนุษย์ได้[21] การกัดเพียงครั้งเดียวก็สามารถทำให้ติดเชื้อได้[22] เมื่อยุงตัวเมียดูดเลือดจากผู้ติดเชื้อไข้เลือดออกจะทำให้มีการติดเชื้อในทางเดินอาหารของยุงตัวนั้น ต่อมา 8-10 วัน ไวรัสจะแพร่ไปยังเนื้อเยื่ออื่น ๆ ของตัวยุงรวมทั้งต่อมน้ำลายของยุงด้วย ทำให้มีการหลั่งตัวไวรัสออกมาในน้ำลายของยุง ยังไม่ปรากฏว่าการติดเชื้อไวรัสไข้เลือดออกจะมีผลเสียใด ๆ ต่อยุงที่ติดเชื้อ ซึ่งจะมีการติดเชื้อไปตลอดอายุขัย ยุงลายบ้านมักวางไข่ในแหล่งน้ำขัง ใกล้ที่อยู่อาศัยของมนุษย์ และมักดูดเลือดจากมนุษย์มากกว่าสัตว์มีกระดูกสันหลังอื่น ๆ[23]
ภาวะเสี่ยง[แก้]
ผู้ป่วยที่เป็นทารกหรือเด็กเล็กมีโอกาสป่วยรุนแรงมากกว่าช่วงอายุอื่น และมักพบบ่อยในเด็กที่มีสุขภาพทั่วไปค่อนข้างดี ซึ่งขัดกับโรคติดเชื้อจำนวนมาก[10] ปัจจัยเสี่ยงอื่นที่ทำให้เกิดโรครุนแรง ได้แก่ เป็นเพศหญิง มีดัชนีมวลกายสูง และปริมาณไวรัส แม้ไวรัสทุกชนิดสามารถทำให้เกิดโรคได้ทั้งแบบไม่รุนแรงไปจนถึงรุนแรงมากไม่ต่างกัน[7] แต่สายพันธุ์ไวรัสก็เป็นปัจจัยเสี่ยงหนึ่ง ความเสี่ยงการเป็นโรครุนแรงจากการติดเชื้อครั้งที่สองเพิ่มขึ้นหากผู้ป่วยเคยได้รับซีโรไทป์ DENV-1 แล้วได้รับซีไรโทไทป์ DENV-2 หรือ DENV-3 ภายหลัง หรือหากผู้ป่วยเคยได้รับ DENV-3 แล้วติดเชื้อ DENV-2 ภายหลัง[19] และผู้ที่ป่วยด้วยโรคเรื้อรังอยู่เดิมแล้ว (เช่น เบาหวาน หรือหอบหืด) มีโอกาสป่วยรุนแรงถึงชีวิตมากกว่า[19]
มีการศึกษาพบความแตกต่างตามปกติ (โพลีมอร์ฟิซึม) ของยีนบางยีนมีความสัมพันธ์กับการเพิ่มโอกาสการมีอาการป่วยรุนแรงเมื่อป่วยเป็นไข้เลือดออก ตัวอย่างของยีนเหล่านี้ เช่น ยีนที่ถอดรหัสออกมาเป็น TNFα, mannan-binding lectin,[6] CTLA4, TGFβ,[18] DC-SIGN และ HLA บางชนิด[19] ภาวะพร่องเอนไซม์กลูโคส-6-ฟอสเฟตดีไฮโดรจีเนส (ภาวะพร่องเอนไซม์จี-6-พีดี) ก็เพิ่มความเสี่ยง[24] นอกจากนี้ยังพบว่าการมีโพลีมอร์ฟิซึมของยีนที่ถอดรหัสออกมาเป็นตัวรับวิตามินดีและ FcγR อาจสามารถลดโอกาสการป่วยรุนแรงในการติดเชื้อครั้งที่สองได้[19]
กลไก[แก้]
เมื่อยุงที่มีไวรัสเด็งกีกัดมนุษย์ ไวรัสจะเข้าสู่ผิวหนังร่วมกับน้ำลายของยุง ไวรัสจะยึดเกาะและเข้าสู่เม็ดเลือดขาวและสืบพันธุ์อยู่ในเซลล์ขณะที่เม็ดเลือดขาวเคลื่อนไปทั่วร่างกาย เม็ดเลือดขาวจะตอบสนองโดยผลิตโปรตีนส่งสัญญาณหลายชนิด เช่น ไซโตไคน์และอินเตอร์เฟียรอน ซึ่งทำให้เกิดอาการหลายอย่าง เช่น ไข้ อาการคล้ายหวัด และอาการปวดรุนแรง ในการติดเชื้อรุนแรง มีการผลิตไวรัสภายในร่างกายสูงขึ้นมาก และอาจเกิดผลกระทบกับหลายอวัยวะ (เช่น ตับและไขกระดูก) ได้ ของเหลวจากกระแสเลือดซึมผ่านผนังหลอดเลือดขนาดเล็กเข้าสู่ช่องว่างลำตัวเนื่องจากสภาพให้ซึมผ่านได้ของหลอดเลือดฝอย ผลทำให้มีเลือดไหลเวียนอยู่ในหลอดเลือดน้อยลง และความดันเลือดต่ำลงจนไม่สามารถส่งเลือดไปเลี้ยงอวัยวะสำคัญเพียงพอ ยิ่งกว่านั้น การทำหน้าที่ผิดปรกติของไขกระดูกเนื่องจากเซลล์พยุงติดเชื้อทำให้เกล็ดเลือดมีน้อยลง ซึ่งเกล็ดเลือดจำเป็นต่อการเกิดลิ่มเลือด จึงเพิ่มความเสี่ยงของอาการเลือดออก อันเป็นภาวะแทรกซ้อนหลักภาวะหนึ่งของไข้เลือดออก[24]
การถ่ายแบบของไวรัส[แก้]
เมื่ออยู่ในผิวหนังแล้ว ไวรัสเด็งกียึดเกาะกับเซลล์แลงเกอร์ฮานส์ (กลุ่มเซลล์เดนไดรต์ในผิวหนังที่เป็นตัวระบุจุลชีพก่อโรค)[24] ไวรัสเข้าสู่เซลล์โดยการยึดเกาะระหว่างโปรตีนไวรัสกับโปรตีนเยื่อหุ้มบนเซลล์แลงเกอร์ฮานส์ โดยเฉพาะ C-type lectin ที่เรียกว่า DC-SIGN ตัวรับแมนโนส และ CLEC5A[18] ดูเหมือนว่า DC-SIGN ซึ่งเป็นตัวรับไม่จำเพาะกับสิ่งแปลกปลอมบนเซลล์เดนไดรต์ เป็นช่องทางเข้าเซลล์หลัก[19] เซลล์เดนไดรต์เคลื่อนไปยังปุ่มน้ำเหลืองที่ใกล้ที่สุด ขณะเดียวกัน มีการแปลรหัสจีโนมไวรัสในเวสิเคิลที่มีเยื่อหุ้มบนเอนโดพลาสมิกเรติคูลัมของเซลล์ จากนั้นมีการผลิตโปรตีนไวรัสใหม่ซึ่งถ่ายแบบอาร์เอ็นเอไวรัสและเริ่มก่อเป็นอนุภาคไวรัส อนุภาคไวรัสที่ยังเจริญไม่เต็มที่ถูกส่งไปยังกอลจิคอมเพล็กซ์ ซึ่งเป็นส่วนของเซลล์ที่โปรตีนบางชนิดได้รับสายน้ำตาลที่จำเป็น (ไกลโคโปรตีน) ไวรัสใหม่ที่เจริญเต็มที่แล้วจะไปดันตัว (bud) บนผิวเซลล์ที่ติดเชื้อและปล่อยออกไปโดยกระบวนการเอกโซไซโทซิส จากนั้น ไวรัสจะสามารถเข้าสู่เม็ดเลือดขาวอื่น ๆ ได้ เช่น โมโนไซต์และแมโครฟาจ[18]
เซลล์ที่ติดเชื้อจะมีปฏิกิริยาระยะแรก คือ สร้างอินเตอร์เฟียรอน ซึ่งเป็นไซโตไคน์ที่เพิ่มการป้องกันการติดเชื้อไวรัสผ่านระบบภูมิคุ้มกันแต่กำเนิดโดยเพิ่มการผลิตโปรตีนกลุ่มใหญ่ที่อาศัย JAK-STAT pathway เป็นสื่อกลาง ไวรัสเด็งกีบางซีโรไทป์อาจมีกลไกชะลอกระบวนการนี้ อินเตอร์เฟียรอนยังกระตุ้นระบบภูมิคุ้มกันที่เกิดขึ้นภายหลัง ซึ่งนำไปสู่การผลิตแอนติบอดีต่อไวรัส เช่นเดียวกับเซลล์ทีซึ่งจะทำลายเซลล์ทั้งหมดที่ติดเชื้อไวรัสโดยตรง[18] มีการผลิตแอนติบอดีหลายชนิด บางชนิดจับกับโปรตีนไวรัสอย่างแน่นและช่วยในกระบวนการฟาโกไซโทซิส (การกินโดยเซลล์ที่เปลี่ยนไปทำหน้าที่เฉพาะ แล้วย่อยทำลาย) แต่บางชนิดเกาะกับไวรัสไม่แน่นและดูเหมือนจะส่งไวรัสไปยังส่วนของฟาโกไซต์ที่ไวรัสไม่ถูกทำลายแต่สามารถถ่ายแบบได้มากขึ้น[18]
โรครุนแรง[แก้]
ปัจจุบันยังไม่แน่ชัดว่าเหตุใดการติดเชื้อเด็งกีซ้ำต่างสายพันธุ์จึงเพิ่มความเสี่ยงการเกิดไข้เลือดออกเด็งกีหรือภาวะช็อกเด็งกี สมมุติฐานซึ่งเป็นที่ยอมรับกันมากที่สุด คือ สมมุติฐานการเร่งที่อาศัยแอนติบอดี (antibody-dependent enhancement, ADE) ยังไม่ทราบกลไกของ ADE แน่ชัด อาจเกิดจากแอนติบอดีซึ่งไม่ต่อต้านไวรัส (non-neutralizing antibody) จับเชื้อไวรัสไม่ดี ทำให้หลังจากเชื้อไวรัสถูกเม็ดเลือดขาวจับกินแล้วไม่ถูกส่งไปยังส่วนที่ถูกต้องของเม็ดเลือด ทำให้การย่อยเกิดไม่สมบูรณ์[18][19] มีข้อสงสัยว่า ADE อาจไม่ใช่กลไกเดียวที่เป็นสาเหตุของอาการแทรกซ้อนรุนแรงที่เกี่ยวกับไข้เด็งกี[6] และมีงานวิจัยจำนวนมากที่แสดงนัยบทบาทของเซลล์ทีและปัจจัยอย่างไซโทไคน์และระบบคอมพลิเมนต์[24]
ลักษณะของโรครุนแรง คือ ปัญหาสภาพให้ซึมผ่านของหลอดเลือดฝอย (การยอมให้ของเหลวและโปรตีนซึ่งปกติอยู่ในเลือดผ่านเข้าออกได้) และการเกิดลิ่มเลือดผิดปรกติ[11][12] การเปลี่ยนเปลงเหล่านี้ปรากฏขึ้นสัมพันธ์กับสภาพไกลโคแคลิกซ์ของเนื้อเยื่อบุโพรงผิดปรกติ ซึ่งทำหน้าที่เป็นเส้นใยโมเลกุลของส่วนประกอบของเลือด[12] คาดกันว่า หลอดเลือดฝอยรั่ว (และระยะวิกฤต) เกิดจากการตอบสนองของระบบภูมิคุ้มกัน[12] กระบวนการอื่นที่สนใจรวมถึง เซลล์ที่ติดเชื้อซึ่งมีการตายเฉพาะส่วน ซึ่งกระทบต่อทั้งการที่เลือดจับตัวเป็นลิ่มและการสลายไฟบริน (ระบบการเกิดลิ่มเลือดและการสลายลิ่มเลือดที่ตรงข้ามกัน) และภาวะเกล็ดเลือดต่ำในเลือด ที่เป็นปัจจัยหนึ่งที่ทำให้การเกิดลิ่มเลือดเป็นปกติ[24]
การวินิจฉัย[แก้]
อาการเตือน[25]
| ||||
| ปวดท้อง | ||||
| อาเจียนมาก | ||||
| ตับโต | ||||
| เลือดออกในเยื่อบุ | ||||
| ความเข้มข้นเม็ดเลือดแดงสูง เกล็ดเลือดต่ำ | ||||
| อ่อนเปลี้ย | ||||
การให้การวินิจฉัยไข้เลือดออกส่วนใหญ่ โดยเฉพาะในพื้นที่ระบาด เช่น ประเทศไทย เป็นการวินิจฉัยทางคลินิก อาศัยอาการและผลการตรวจร่างกาย[6] อย่างไรก็ดีอาการระยะแรกของไข้เลือดออกแยกจากการติดเชื้อไวรัสอื่นได้ยาก[10] สำหรับผู้ป่วยที่อยู่ในพื้นที่ระบาด อาการที่น่าสงสัยว่าอาจจะเป็นไข้เลือดออกคืออาการไข้ร่วมกับอาการสองอย่างจากอาการต่าง ๆ ต่อไปนี้ คลื่นไส้อาเจียน ผื่น ปวดตามตัว เม็ดเลือดขาวต่ำ การทดสอบทูนิเกต์ผลบวก หรืออาการเตือนใด ๆ ตามตาราง[25] ซึ่งอาการเตือนเหล่านี้มักปรากฏก่อนโรคดำเนินไปเป็นไข้เลือดออกรุนแรง[14] การทดสอบทูนิเกต์เป็นการตรวจที่มีประโยชน์มากในพื้นที่ที่ไม่สามารถส่งตรวจทางห้องปฏิบัติการได้ทันที ทำโดยใช้เครื่องวัดความดันโลหิตพันรอบแขนและรัดไว้ให้ความดันโลหิตอยู่ระหว่างความดันช่วงหัวใจบีบและความดันช่วงหัวใจคลาย ห้านาที จากนั้นนับจุดเลือดออกที่ปรากฏขึ้น ยิ่งมีจุดมากก็ยิ่งมีความน่าจะเป็นของการเป็นไข้เลือดออกมาก[14]
ควรวินิจฉัยทุกคนที่มีไข้ในสองสัปดาห์หลังเดินทางไปในเขตร้อนหรือกึ่งเขตร้อน[12] โรคไข้เด็งกีแยกจากไข้ชิคุนกุนยาได้ยาก ซึ่งโรคนี้เป็นโรคติดเชื้อไวรัสที่มีอาการคล้ายกันและยังระบาดในหลายพื้นที่ซึ่งโรคไข้เลือดออกระบาดด้วย[13] บ่อยครั้งต้องใช้การตรวจอื่น ๆ เพื่อแยกโรคที่ทำให้เกิดอาการคล้ายกัน เช่น มาลาเรีย ฉี่หนู ไข้รากสาดน้อย ไข้กาฬหลังแอ่น โรคหัดและไข้หวัดใหญ่[10] ไข้ซิกาก็เป็นอีกโรคหนึ่งที่มีอาการคล้ายไข้เด็งกี[26]
ความผิดปกติที่พบได้เร็วที่สุดจากการตรวจทางห้องปฏิบัติการคือการพบเม็ดเลือดขาวต่ำ ซึ่งต่อมาอาจพบมีเกล็ดเลือดต่ำและเลือดเป็นกรดเหตุเมตาบอลิกได้[10] ระดับอะมิโนทรานสเฟอร์เรส (AST และ ALT) จากตับที่สูงขึ้นพอสมควรมักสัมพันธ์กับเกล็ดเลือดและเม็ดเลือดขาวต่ำ[12] ในกรณีที่มีอาการรุนแรง การรั่วของพลาสมาจะทำให้ตรวจพบเลือดมีความเข้มข้นสูง (พบฮีมาโตคริตสูง) และอัลบูมินในเลือดต่ำ[10] ภาวะมีน้ำในช่องเยื่อหุ้มปอดและท้องมานอาจพบได้จากการตรวจร่างกายหากเป็นมาก ๆ[10] แต่อาจตรวจพบได้เร็วขึ้น จากการใช้การตรวจอื่น ๆ เช่น การตรวจด้วยคลื่นอัลตราซาวนด์ ซึ่งช่วยให้สามารถตรวจพบผู้ป่วยที่จะกลายเป็นกลุ่มอาการช็อคจากไข้เลือดออกได้เร็วขึ้นในระยะแรก[6][10] แต่ยังมียังข้อจำกัดเนื่องจากจำเป็นต้องใช้อุปกรณ์ราคาแพง ซึ่งไม่ได้มีในสถานพยาบาลทุก ๆ ที่[6] กลุ่มอาการช็อคเด็งกียังพบได้หากความดันชีพจรลดลง ≤ 20 มม. ปรอท ร่วมกับระบบไหลเวียนโลหิตส่วนปลายล้มเหลว[12] ระบบไหลเวียนโลหิตส่วนปลายล้มเหลวในเด็กสังเกตจากมีการเติมเต็มเลือดกลับเข้าเส้นเลือดฝอย (capillary refill) นาน หัวใจเต้นเร็ว หรือมือเท้าเย็น[14]
การจำแนกประเภท[แก้]
ระบบการจำแนกประเภทไข้เลือดออกเด็งกีขององค์การอนามัยโลกฉบับ พ.ศ. 2552 จำแนกไข้เลือดออกเด็งกีเอาไว้เป็นสองประเภท คือชนิดไม่มีภาวะแทรกซ้อนและชนิดรุนแรง[6][25] โดยใช้แทนระบบจำแนกประเภทฉบับ พ.ศ. 2550 ซึ่งมีรายละเอียดมากกว่า เนื่องจากต้องการให้การจำแนกประเภทมีความเข้าใจง่าย อย่างไรก็ดีระบบจำแนกประเภทแบบเดิมก็ยังคงมีผู้ใช้อยู่อย่างกว้างขวาง[25] โดยระบบ พ.ศ 2550 นี้ได้จำแนกประเภทของไข้เลือดออกเด็งกีเอาไว้เป็น ไข้ซึ่งจำแนกประเภทไม่ได้ (undifferentiated fever), ไข้เด็งกี (dengue fever) และไข้เลือดออกเด็งกี (dengue hemorrhagic fever) [10][27] โดยสำหรับประเภทไข้เลือดออกเด็งกีเองก็แบ่งออกเป็นระดับ (grade) 1-4 โดยระดับ 1 ผู้ป่วยจะมีไข้และมีอาการเบื้องต้นของ "เลือดออก" ได้แก่มีจ้ำเลือดตามตัวง่ายหรือทูนิเกต์เทสท์ให้ผลบวก, ระดับ 2 จะมีเลือดออกเองจากผิวหนังหรือที่อื่น, ระดับ 3 มีอาการช็อค และระดับ 4 ช็อครุนแรงจนไม่สามารถวัดความดันโลหิตและชีพจรได้[27] ไข้เลือดออกเด็งกีระดับ 3 และ 4 เรียกรวมว่า "กลุ่มอาการช็อคจากเด็งกี" (dengue shock syndrome) [25][27]
การตรวจทางห้องปฏิบัติการ[แก้]
อาจสามารถวินิจฉัยไข้เลือดออกได้ด้วยการตรวจทางจุลชีววิทยาหรือการตรวจหาเชื้อก่อโรค[25] ซึ่งอาจทำได้โดยการแยกเชื้อไวรัสด้วยการเพาะเลี้ยงเซลล์ การตรวจหาสารพันธุกรรมด้วยปฏิกิริยาลูกโซ่พอลิเมอเรส การทางวิทยาเซรุ่มเพื่อตรวจหาแอนติเจนของไวรัสด้วยปฏิกิริยาการจับกับแอนติบอดี[19][28] โดยการแยกเชื้อไวรัสและการตรวจหาสารพันธุกรรมเป็นการตรวจที่ให้ผลแม่นยำกว่าการตรวจหาแอนติบอดี แต่การตรวจเหล่านี้ยังไม่มีการใช้แพร่หลายเนื่องจากยังมีราคาสูงมาก[28] และยังอาจให้ผลลบ (ตรวจไม่พบ) ได้ในผู้ป่วยระยะแรก[10][19]
การตรวจเหล่านี้จะมีคุณค่าช่วยในการวินิจฉัยก็ต่อเมื่อทำในการป่วยระยะเฉียบพลัน ยกเว้นการตรวจทางวิทยาเซรุ่ม การตรวจหาแอนติบอดี IgG และ IgM ที่จำเพาะต่อชนิดของไวรัสให้ประโยชน์เป็นการยืนยันการวินิจฉัยในระยะท้าย ๆ ของการดำเนินโรค ร่างกายจะเริ่มผลิต IgG และ IgM หลังจากติดเชื้อไปแล้ว 5-7 วัน ระดับ IgM จะตรวจพบได้สูงสุดหลังการติดเชื้อครั้งแรก แต่ในการติดเชื้อครั้งที่สองหรือสามก็ยังมีการผลิต IgM อยู่เช่นกันแม้จะไม่มากเท่า หลังการติดเชื้อครั้งแรก 30-90 วัน ระดับ IgM จะลดลงจนไม่สามารถตรวจพบได้ โดยในการติดเชื้อที่ไม่ใช่ครั้งแรก ระดับ IgM จะลงลงเร็วกว่านี้ ในทางกลับกัน IgG จะยังคงอยู่ให้ตรวจพบได้นานกว่า 60 ปี แม้จะไม่มีอาการเลยก็ตาม จึงมีประโยชน์ในการตรวจว่าเคยติดเชื้อมาก่อนหรือไม่ เมื่อมีการติดเชื้อครั้งแรก ระดับ IgG จะเพิ่มขึ้นจนถึงระดับสูงสุดที่ 14-21 วัน และในการติดเชื้อครั้งต่อ ๆ มา ระดับจะขึ้นสูงเร็วกว่าและสูงมากกว่า ทั้ง IgG และ IgM เป็นสารภูมิคุ้มกันที่มีผลป้องกันการติดเชื้อไวรัสสายพันธุ์ (ซีโรไทป์) นั้น ๆ การตรวจทางห้องปฏิบัติการเพื่อหาระดับ IgG และ IgG นั้นอาจมีการแสดงปฏิกิริยาข้ามกันระหว่างไวรัสอื่น ๆ ในกลุ่มฟลาวิไวริดีได้ เช่น ไวรัสไข้เหลือง ทำให้การแปลผลการตรวจมีความซับซ้อนและยากมากขึ้น[13][19][29] การตรวจหาระดับ IgG เพียงอย่างเดียวนั้นจะใช้เป็นเกณฑ์การวินิจฉัยไข้เลือดอองเด็งกีได้ก็ต่อเมื่อเก็บห่างกัน 14 วัน และพบว่ามีระดับเพิ่มขึ้นมากกว่า 4 เท่าเท่านั้น ส่วนการตรวจ IgM ในผู้ป่วยที่มีอาการนั้น สามารถใช้ในการวินิจฉัยได้[29]
การรักษา[แก้]
ปัจจุบันยังไม่มียาต้านไวรัสจำเพาะต่อไข้เด็งกี สิ่งที่สำคัญที่สุดในการรักษาคือการรักษาสมดุลสารน้ำเอาไว้[12] การรักษาที่ให้จะขึ้นอยู่กับอาการ ซึ่งมีตั้งแต่การให้กินสารน้ำร่วมกับการติดตามใกล้ชิดโดยไม่ต้องรับไว้รักษาในโรงพยาบาล ไปจนถึงการเข้ารับการรักษาในโรงพยาบาลโดยมีการให้ของเหลวทางหลอดเลือดดำ และ/หรือ การถ่ายเลือด[30] ข้อพิจารณาในการรับเข้ารักษาในโรงพยาบาลโดยทั่วไปจะดูจากการมีอาการเตือนดังที่แสดงไว้ข้างต้น โดยเฉพาะผู้มีโรคประจำตัว[10]
ผู้ป่วยมักมีความจำเป็นต้องได้รับสารน้ำทางหลอดเลือดดำอยู่ไม่เกิน 1-2 วัน[30] อัตราจะค่อย ๆ ถูกปรับให้เหมาะสมเพื่อให้มีปัสสาวะออกประมาณ 0.5-1 มล./กก./ชั่วโมง สัญญาณชีพคงที่ และฮีมาโตคริตคงที่[10] งดเว้นหัตถการทางการแพทย์แบบล่วงล้ำ (invasive medical procedure) (เช่น การใส่สายจมูกถึงกระเพาะอาหาร การฉีดยาเข้ากล้ามเนื้อ และการเจาะเลือดจากหลอดเลือดแดง) เว้นแต่จำเป็น ด้วยมีความเสี่ยงเลือดออก[10] ใช้ยาพาราเซตามอล (อะเซตามิโนเฟน) เพื่อลดไข้ แก้ปวด และหลีกเลี่ยงยาแก้อักเสบชนิดไม่ใช่สเตอรอยด์ เช่น ไอบูโปรเฟนและแอสไพริน เพราะอาจเพิ่มความเสี่ยงการมีเลือดออกได้[30] ผู้ป่วยบางรายที่มีสัญญาณชีพไม่คงที่และฮีมาโตคริตลดลงเท่านั้นที่จะได้รับการให้เลือดหรือส่วนประกอบของเลือด โดยไม่ต้องเฝ้าดูระดับฮีมาโตคริตลดลงจนถึงเกณฑ์ที่กำหนดไว้ล่วงหน้า[31] ในกรณีที่ต้องได้รับเลือดหรือส่วนประกอบของเลือดแนะนำให้ใช้เม็ดเลือดแดงเข้มข้น (เลือดที่ปั่นแยกส่วนประกอบของเลือดและคัดมาเฉพาะเม็ดเลือดแดง) หรือเลือดเต็ม (เลือดที่ไม่ได้ปั่นแยกส่วนประกอบของเลือด) ส่วนใหญ่ไม่มีความจำเป็นในการให้เกล็ดเลือดหรือพลาสมาสดแช่แข็ง[31]
เมื่อถึงระยะฟื้นตัวแพทย์จะหยุดให้สารน้ำทางหลอดเลือดดำเพื่อป้องกันภาวะสารน้ำเกิน[10] ถ้าเกิดมีภาวะสารน้ำเกินขึ้นโดยที่อาการและสัญญาณชีพอื่น ๆ ปกติ การหยุดสารน้ำเพียงอย่างเดียวก็เพียงพอโดยไม่ต้องให้ยาขับสารน้ำออก[31] ทั้งนี้แพทย์อาจพิจารณาใช้ยาขับปัสสาวะ เช่น ฟูโรซีไมด์ เพื่อกำจัดของเหลวส่วนเกินออกได้ หากไม่ได้อยู่ในระยะวิกฤต[31]
การป้องกัน[แก้]

การป้องกันโรคไข้เด็งกีต้องอาศัยการควบคุมการแพร่พันธุ์ยุงลายและป้องกันไม่ให้ยุงลายกัด[20][32] องค์การอนามัยโลกได้แนะนำโครงการควบคุมพาหะแบบบูรณาการเอาไว้ โดยมีองค์ประกอบ 5 อย่าง ได้แก่ 1) ต้องมีการสนับสนุนจากทุกภาคส่วนเพื่อให้ระบบบริการสุขภาพและชุมชนมีความเข้มแข็ง 2) มีความร่วมมือระหว่างองค์กรสุขภาพและภาคส่วนอื่น ๆ 3) ส่งเสริมให้มีการควบคุมโรคอย่างบูรณาการโดยใช้ทรัพยากรที่มีให้เกิดประโยชน์สูงสุด 4) มีการตัดสินใจโดยอิงหลักฐานเพื่อให้มีการออกมาตรการที่เหมาะสม และ 5) มีการเตรียมพร้อมรับสถานการณ์การระบาดในแต่ละที่อยู่เสมอ[20]
วิธีการในการควบคุมการแพร่ระบาดของยุงลายคือการกำจัดแหล่งเพาะพันธุ์ยุงลาย[20] ทำโดยป้องกันไม่ให้มีน้ำขังในภาชนะ เช่น คว่ำขัน กะละมัง ที่อยู่นอกบ้าน ไม่ให้มีน้ำขัง ใส่สารฆ่าแมลงหรือสารควบคุมการเจริญเติบโตของยุงลาย เช่น ทรายอะเบต ในพื้นที่[20] อย่างไรก็ดีเชื่อกันว่าการพ่นยาฆ่าแมลงเป็นครั้ง ๆ ไปนั้นได้ผลไม่คุ้มค่า[8] เมื่อพิจารณาว่าการใส่สารฆ่าแมลงลงในพื้นที่นั้นมีผลเสียมากกว่าที่จะรับได้ และการให้สารควบคุมการเจริญเติบโตของยุงลายนั้นเป็นการยากที่จะทำได้ทั่วถึง การลดปริมาณแหล่งน้ำขังด้วยการควบคุมภาชนะนอกบ้านจึงเป็นวิธีที่เป็นที่นิยมและได้รับการยอมรับมากที่สุด[20] นอกจากนี้ยังอาจสามารถป้องกันไม่ให้ยุงลายกัดได้โดยใส่เสื้อผ้าที่มิดชิด นอนกางมุ้ง หรือใช้สารขับไล่แมลง เป็นต้น โดยสารที่ได้ผลดีที่สุด คือ DEET[22]
สำหรับในประเทศไทย ศูนย์ควบคุมโรคไข้เลือดออก กองควบคุมโรค สำนักอนามัย แนะนำแนวทางในการป้องกันโรคไข้เลือดออกโดยเน้นการกำจัดแหล่งเพาะพันธุ์ลูกน้ำยุงลาย และการป้องกันไม่ให้ยุงลายกัด[33] ซึ่งเป็นไปตามคำแนะนำขององค์การอนามัยโลก
วัคซีน[แก้]
ตั้งแต่ พ.ศ. 2559 เป็นต้นมา มีการผลิตวัคซีนป้องกันไข้เด็งกีที่มีประสิทธิภาพบางส่วนออกจำหน่ายในประเทศฟิลิปปินส์ อินโดนีเซีย[4][34] และประเทศไทย[35] ราคาวัคซีนอยู่ที่ประมาณ 10,000 บาท ต่อคอร์ส 3 เข็ม[35]
วัคซีนนี้ผลิตโดยบริษัท Sanofi ภายใต้ชื่อการค้า Dengvaxia[36] ผลิตจากเชือไวรัสพันธุ์ผสมระหว่างไวรัสไข้เหลืองที่ถูกทำให้อ่อนกำลังลง และไวรัสไข้เลือดออกแต่ละซีโรทัยป์[37][38] งานวิจัยที่ศึกษาประสิทธิผลของวัคซีนสองชิ้นพบว่าวัคซีนนี้มีประสิทธิผลอยู่ที่ 60% และป้องกันการเกิดไข้เด็งกีที่มีอาการรุนแรงได้ 80-90%[39][40] ซึ่งผู้เกี่ยวข้องบางกลุ่มเห็นว่ายังไม่ใช่ผลที่น่าพอใจในการป้องกันโรค[41]
ยังมีความกังวลว่าการรับวัคซีนอาจเป็นปัจจัยเสี่ยงทำให้เกิดไข้เลือดออกชนิดรุนแรงผ่านการสร้างแอนติบอดีที่ต้านไวรัสเด็งกีแบบไม่สมบูรณ์ผ่านปฏิกิริยาการเสริมความแรงของเชื้อผ่านแอนติบอดี (antibody-dependent enhancement, ADE)[42] วัคซีนในอุดมคติจะต้องมีความปลอดภัย ได้ผลหลังจากฉีดเพียง 50-100 ครั้ง มีผลต่อทุกซีโรทัยป์ ไม่ทำให้เกิด ADE ขนส่งและเก็บรักษาได้ง่าย มีราคาเหมาะสม และมีความคุ้มค่า[42]
วิทยาการระบาด[แก้]

แดง: เด็งกีระบาดและมี Ae. aegypti
ฟ้า: มีเฉพาะ Ae. aegypti
บุคคลส่วนใหญ่ที่ป่วยเป็นไข้เด็งกีฟื้นตัวโดยไม่มีปัญหาต่อเนื่อง[25] อัตราตายอยู่ที่ 1–5% โดยปราศจากการรักษา[10] และน้อยกว่า 1% โดยได้รับการรักษาอย่างเพียงพอ[25] อย่างไรก็ดี โรครุนแรงมีอัตราตายที่ 26%[10] ไข้เด็งกีเป็นโรคประจำถิ่นในกว่า 110 ประเทศ[10] มีผู้ติดเชื้อทั่วโลก 50 ถึง 100 ล้านคนต่อปี ทำให้ต้องเข้าโรงพยาบาลห้าแสนครั้ง[6] และมีผู้เสียชีวิตประมาณ 12,500–25,000 คน[11][43]
ไข้เด็งกีเป็นโรคไวรัสที่ส่งต่อผ่านสัตว์ขาปล้องที่พบมากที่สุด[18] มีการประเมินภาระโรคเอาไว้ที่ 1,600 ปีสุขภาวะที่สูญเสียไปจากโรคและการบาดเจ็บของประชากร (DALY, disability-adjusted life year) ต่อประชากรหนึ่งล้านคน ซึ่งคล้ายกันกับวัณโรค[19] ด้วยความเป็นโรคเขตร้อน ไข้เด็งกีจึงดูมีความสำคัญเป็นรองมาลาเรีย[10] แต่องค์การอนามัยโลกจะนับไข้เด็งกีเป็นหนึ่งในสิบหกโรคเขตร้อนที่ถูกละเลย[44]
อุบัติการณ์ของไข้เด็งกีเพิ่มขึ้น 30 เท่า ระหว่าง ค.ศ. 1960 และ 2010[45] ซึ่งการเพิ่มขึ้นนี้เชื่อว่าเป็นผลของการมีลักษณะแบบเมือง การเติบโตของประชากร การท่องเที่ยวระหว่างประเทศเพิ่มขึ้น และปรากฏการณ์โลกร้อนประกอบกัน[6] การกระจายทางภูมิศาสตร์อยู่รอบเส้นศูนย์สูตร โดย 70% ของประชากรรวม 2,500 ล้านคนอาศัยอยู่ในพื้นที่ระบาดจากทวีปเอเชียและมหาสมุทรแปซิฟิก[45] ในสหรัฐอเมริกา อัตราการติดเชื้อเด็งกีในผู้ที่เดินทางกลับจากพื้นที่ระบาดพร้อมกับไข้เด็งกีอยู่ที่ 2.9–8.0%[22] และเป็นการติดเชื้อที่พบมากที่สุดเป็นอันดับสองรองจากมาลาเรียที่ได้รับวินิจฉัยในกลุ่มนี้[13]
ไวรัสเด็งกีถูกรักษาอยู่ในธรรมชาติในวัฏจักรที่เกี่ยวข้องกับพาหะดูดเลือดที่ไวรัสชอบไปอยู่และโฮสต์สัตว์มีกระดูกสันหลัง เช่นเดียวกับอาร์โบไวรัสส่วนใหญ่[46] ไวรัสถูกรักษาในป่าเอเชียตะวันออกเฉียงใต้และแอฟริกาโดยการส่งผ่านจากยุง Aedes เพศเมีย นอกเหนือจากสปีชีส์ A. aegypti ไปยังลูกและไพรเมตชั้นต่ำกว่า[46] ในเมืองและนคร ไวรัสส่งผ่านโดย A. aegypti เป็นหลัก ซึ่งมักอยู่ในบ้าน ในชนบท ไวรัสส่งผ่านสู่มนุษย์โดย A. aegypti และ Aedes สปีชีส์อื่น เช่น A. albopictus[46] ทั้งสองสปีชีส์มีเขตที่อยู่อาศัยขยายขึ้นในช่วงครึ่งหลังของคริสต์ศตวรรษที่ 20[12] แต่ในทุกที่ ไพรเมตชั้นต่ำกว่าหรือมนุษย์ที่ติดเชื้อเพิ่มจำนวนไวรัสเด็งกีหมุนเวียนในกระบวนการที่เรียกว่า amplification[46] การติดเชื้อได้รับมาในสิ่งแวดล้อมเมืองมากที่สุด[47] ในทศวรรษหลัง การขยายหมู่บ้าน เมืองและนครในพื้นที่ระบาด และอัตราตายของประชากรที่เพิ่มสูงขึ้น เพิ่มจำนวนโรคระบาดและไวรัสหมุนเวียน ไข้เด็งกี ซึ่งครั้งหนึ่งเคยจำกัดอยู่ในเอเชียตะวันออกเฉียงใต้ ปัจจุบันแพร่ไปถึงจีนตอนใต้ ประเทศในมหาสมุทรแปซิฟิกและทวีปอเมริกาแล้ว[47] และอาจคุกคามยุโรป[8]
ประวัติศาสตร์[แก้]
บันทึกแรกของผู้ป่วยที่อาจป่วยเป็นโรคไข้เด็งกีปรากฏในสารานุกรมการแพทย์จีนจากราชวงศ์จิ้น (ค.ศ. 265–420) ซึ่งอ้างถึง "พิษน้ำ" ที่เกี่ยวข้องกับแมลงบิน[48][49] พาหะหลัก A. aegypti แพร่กระจายออกจากแอฟริกาในคริสต์ศตวรรษที่ 15 ถึง 19 บางส่วนเนื่องจากโลกาภิวัฒน์เพิ่มขึ้น รองต่อการค้าทาส[12] มีคำอธิบายโรคระบาดในคริสต์ศตวรษที่ 17 แต่รายงานการระบาดของเด็งกียุคแรกที่น่าเชื่อถือที่สุดมาจาก ค.ศ. 1779 และ 1780 เมื่อโรคระบาดได้กวาดทั่วเอเชีย แอฟริกาและอเมริกาเหนือ[49] นับแต่นั้นจนถึง ค.ศ. 1940 เกิดโรคระบาดเด็งกีไม่บ่อยนัก[49]
ใน ค.ศ. 1906 มีการยืนยันการส่งผ่านโดยยุง Aedes และใน ค.ศ. 1907 เด็งกีเป็นโรคลำดับที่สองที่ถูกแสดงว่าเกิดจากไวรัส ถัดจากไข้เหลือง[50] การสืบส่วนเพิ่มเติมโดยจอห์น เคลแลนด์และโจเซฟ แฟรงกลิน ซีเลอร์ทำให้ความเข้าใจการส่งผ่านเด็งกีเบื้องต้นสมบูรณ์[50]
การรบกวนระบบนิเวศคาดว่าเป็นสาเหตุของไข้เด็งกีระบาดชัดเจนระหว่างและหลังสงครามโลกครั้งที่สอง กระแสเดียวกันนี้ยังนำไปสู่การระบาดของไข้เด็งกีเซโรไปต์ต่าง ๆ ไปยังพื้นที่ใหม่ และกำเนิดไข้เลือดออกเด็งกี รูปแบบรุนแรงของโรคเด็งกีมีรายงานครั้งแรกในประเทศฟิลิปปินส์ใน ค.ศ. 1953 จนถึงคริสต์ทศวรรษ 1970 ไข้เด็งกีเป็นสาเหตุหลักของการตายในเด็กและกำเนิดขึ้นในแปซิฟิกและทวีปอเมริกา[49] ไข้เลือดออกเด็งกีและกลุ่มอาการไข้เลือดออกช็อกมีการสังเกตครั้งแรกในอเมริกากลางและอเมริกาใต้ใน ค.ศ. 1981 เมื่อ DENV-2 สัมผัสผู้ที่เคยได้รับเชื้อ DENV-1 เมื่อหลายปีก่อน[17]
การวิจัย[แก้]
ความพยายามวิจัยเพื่อป้องกันและรักษาไข้เด็งกี รวมถึงการใช้หลายวิธีในการควบคุมตัวนำโรค[51] การพัฒนาวัคซีน และยาต้านไวรัส[32]
สำหรับการควบคุมตัวนำโรค มีการใช้วิธีการใหม่ ๆ จำนวนหนึ่งเพื่อลดจำนวนยุงโดยประสบความสำเร็จอยู่บ้าง รวมถึงการปล่อยปลาหางนกยูงในแหล่งน้ำนิ่งเพื่อกินลูกน้ำยุงลาย[51] ปัจจุบันกำลังมีความพยายามทำให้ประชากรยุงติดเชื้อแบคทีเรียในสกุล Wolbachia ซึ่งทำให้ยุงมีภูมิคุ้มกันบางส่วนต่อไวรัสเด็งกี[12] นอกจากนี้ ยังมีการทดสอบ A. aegypti เพศผู้ ที่ถูกดัดแปลงพันธุกรรม ซึ่งหลังจากปล่อยให้ผสมพันธุ์กับยุงเพศเมียแล้ว ลูกหลานของมันจะมีชีวิตอยู่ผ่านขั้นลูกน้ำแต่ตายในระยะดักแด้ ก่อนจะโตเต็มวัยพร้อมสืบพันธุ์[52]
ขณะนี้กำลังมีโครงการพัฒนาวัคซีนไข้เด็งกีให้ครอบคลุมทั้งสี่เซโรไทป์[32] ความกังวลหนึ่ง คือ วัคซีนอาจเพิ่มความเสี่ยงต่อการเกิดโรครุนแรงผ่าน antibody-dependent enhancement (ADE)[42] วัคซีนในอุดมคตินั้นจะต้องปลอดภัย มีผลหลังการฉีดหนึ่งหรือสองครั้ง ครอบคลุมทุกเซโรไทป์ ไม่ส่งผลต่อ ADE ขนส่งและเก็บรักษาง่าย และทั้งสามารถจ่ายได้และคุ้มทุน[42] จนถึงปี 2012 วัคซีนจำนวนหนึ่งกำลังอยู่ระหว่างการทดสอบ[37][42] วัคซีนที่พัฒนามากที่สุดอาศัยไวรัสไข้เหลืองและไวรัสเด็งกีสี่เซโรไทป์ที่ถูกทำให้อ่อนกำลังลงรวมกัน[37][53] หวังกันว่า ผลิตภัณฑ์ชุดแรกจะพร้อมวางจำหน่ายเชิงพาณิชย์ในปี 2015[32]
นอกจากความพยายามควบคุมการแพร่ของยุง Aedes และการทำงานเพื่อพัฒนาวัคซีนต่อต้านไข้เด็งกีแล้ว ขณะนี้ยังมีความพยายามที่จะพัฒนายาต้านไวรัส ที่จะใช้เพื่อรักษาการป่วยเป็นไข้เด็งกีและป้องกันภาวะแทรกซ้อนรุนแรง[54][55] การค้นพบโครงสร้างโปรตีนของไวรัสอาจช่วยในการพัฒนายาที่มีประสิทธิภาพ[55] มีหลายเป้าหมายที่เป็นไปได้ แนวทางแรก คือ การยับยั้ง RNA-dependent RNA polymerase ของไวรัส ซึ่งคัดลอกสารพันธุกรรมของไวรัสด้วยนิวคลีโอไซด์แอนาล็อก แนวทางที่สอง เป็นไปได้ที่จะพัฒนาตัวยับยั้งเฉพาะของเอนไซม์โปรตีเอสของไวรัส ซึ่งจะผูกโปรตีนของไวรัสติดกัน[56] แนวทางสุดท้าย เป็นไปได้ที่จะพัฒนาตัวยับยั้งชนิดยับยั้งการนำเข้า (entry inhibitor) ซึ่งจะไปหยุดไม่ให้ไวรัสเข้าสู่เซลล์ หรือยับยั้งกระบวนการ 5′ capping ที่จำเป็นต้องการถ่ายแบบของไวรัส[54]
อ้างอิง[แก้]
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 "Dengue and severe dengue Fact sheet N°117". WHO. May 2015. เก็บจากแหล่งเดิมเมื่อ 2 September 2016. สืบค้นเมื่อ 3 February 2016.
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 Kularatne SA (September 2015). "Dengue fever". BMJ. 351: h4661. doi:10.1136/bmj.h4661. PMID 26374064. S2CID 1680504.
- ↑ Nelson Textbook of Pediatrics: The field of pediatrics. Elsevier Health Sciences. 2016. p. 1631. ISBN 9781455775668. เก็บจากแหล่งเดิมเมื่อ 10 September 2017.
- ↑ 4.0 4.1 East, Susie (6 April 2016). "World's first dengue fever vaccine launched in the Philippines". CNN. สืบค้นเมื่อ 17 October 2016.
- ↑ 5.0 5.1 "Dengue and severe dengue". www.who.int (ภาษาอังกฤษ). สืบค้นเมื่อ 29 February 2020.
- ↑ 6.00 6.01 6.02 6.03 6.04 6.05 6.06 6.07 6.08 6.09 6.10 Whitehorn J, Farrar J (2010). "Dengue". Br. Med. Bull. 95: 161–73. doi:10.1093/bmb/ldq019. PMID 20616106.
- ↑ 7.0 7.1 7.2 7.3 7.4 7.5 7.6 7.7 WHO (2009), pp. 14–16.
- ↑ 8.0 8.1 8.2 8.3 Reiter P (2010-03-11). "Yellow fever and dengue: a threat to Europe?". Euro Surveill. 15 (10): 19509. PMID 20403310.
- ↑ Gubler (2010), p. 379.
- ↑ 10.00 10.01 10.02 10.03 10.04 10.05 10.06 10.07 10.08 10.09 10.10 10.11 10.12 10.13 10.14 10.15 10.16 10.17 10.18 10.19 10.20 10.21 10.22 10.23 10.24 10.25 10.26 Ranjit S, Kissoon N (July 2010). "Dengue hemorrhagic fever and shock syndromes". Pediatr. Crit. Care Med. 12 (1): 90–100. doi:10.1097/PCC.0b013e3181e911a7. PMID 20639791.
- ↑ 11.0 11.1 11.2 11.3 11.4 11.5 Varatharaj A (2010). "Encephalitis in the clinical spectrum of dengue infection". Neurol. India. 58 (4): 585–91. doi:10.4103/0028-3886.68655. PMID 20739797.
- ↑ 12.00 12.01 12.02 12.03 12.04 12.05 12.06 12.07 12.08 12.09 12.10 12.11 12.12 12.13 Simmons CP, Farrar JJ, Nguyen vV, Wills B (April 2012). "Dengue". N Engl J Med. 366 (15): 1423–32. doi:10.1056/NEJMra1110265. PMID 22494122.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 13.0 13.1 13.2 13.3 13.4 13.5 13.6 13.7 Chen LH, Wilson ME (October 2010). "Dengue and chikungunya infections in travelers". Curr. Opin. Infect. Dis. 23 (5): 438–44. doi:10.1097/QCO.0b013e32833c1d16. PMID 20581669.
- ↑ 14.00 14.01 14.02 14.03 14.04 14.05 14.06 14.07 14.08 14.09 14.10 14.11 14.12 WHO (2009), pp. 25–27.
- ↑ 15.0 15.1 Wolff K, Johnson RA (2009). "Viral Infections of Skin and Mucosa". Fitzpatrick's Color Atlas and Synopsis of Clinical Dermatology (6th ed.). New York: McGraw-Hill Medical. pp. 810–2. ISBN 9780071599757.
- ↑ 16.0 16.1 Knoop KJ, Stack LB, Storrow A, Thurman RJ (2010). "Tropical Medicine". Atlas of Emergency Medicine (3rd ed.). New York: McGraw-Hill Professional. pp. 658–9. ISBN 0071496181.
{{cite book}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 17.0 17.1 17.2 17.3 17.4 17.5 Gould EA, Solomon T (February 2008). "Pathogenic flaviviruses". The Lancet. 371 (9611): 500–9. doi:10.1016/S0140-6736(08)60238-X. PMID 18262042.
- ↑ 18.0 18.1 18.2 18.3 18.4 18.5 18.6 18.7 18.8 Rodenhuis-Zybert IA, Wilschut J, Smit JM (August 2010). "Dengue virus life cycle: viral and host factors modulating infectivity". Cell. Mol. Life Sci. 67 (16): 2773–86. doi:10.1007/s00018-010-0357-z. PMID 20372965.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 19.00 19.01 19.02 19.03 19.04 19.05 19.06 19.07 19.08 19.09 19.10 Guzman MG, Halstead SB, Artsob H; และคณะ (December 2010). "Dengue: a continuing global threat". Nat. Rev. Microbiol. 8 (12 Suppl): S7–S16. doi:10.1038/nrmicro2460. PMID 21079655.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 20.0 20.1 20.2 20.3 20.4 20.5 WHO (2009), pp. 59–60.
- ↑ "Vector-borne viral infections". World Health Organization. สืบค้นเมื่อ 17 January 2011.
- ↑ 22.0 22.1 22.2 Center for Disease Control and Prevention. "Chapter 5 – Dengue Fever (DF) and Dengue Hemorrhagic Fever (DHF)". 2010 Yellow Book. สืบค้นเมื่อ 2010-12-23.
- ↑ Gubler (2010), pp. 377–78.
- ↑ 24.0 24.1 24.2 24.3 24.4 Martina BE, Koraka P, Osterhaus AD (October 2009). "Dengue virus pathogenesis: an integrated view". Clin. Microbiol. Rev. 22 (4): 564–81. doi:10.1128/CMR.00035-09. PMC 2772360. PMID 19822889. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-05-18. สืบค้นเมื่อ 2011-07-25.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 25.0 25.1 25.2 25.3 25.4 25.5 25.6 25.7 WHO (2009), pp. 10–11.
- ↑ Musso, D.; Nilles, E.J.; Cao-Lormeau, V.-M. (2014). "Rapid spread of emerging Zika virus in the Pacific area". Clinical Microbiology and Infection. 20 (10): O595–O596. doi:10.1111/1469-0691.12707. PMID 24909208.
- ↑ 27.0 27.1 27.2 WHO (1997). "Chapter 2: clinical diagnosis". Dengue haemorrhagic fever: diagnosis, treatment, prevention and control (PDF) (2nd ed.). Geneva: World Health Organization. pp. 12–23. ISBN 9241545003.
- ↑ 28.0 28.1 WHO (2009), pp. 90–95.
- ↑ 29.0 29.1 Gubler (2010), p. 380.
- ↑ 30.0 30.1 30.2 WHO (2009), pp. 32–37.
- ↑ 31.0 31.1 31.2 31.3 WHO (2009), pp. 40–43.
- ↑ 32.0 32.1 32.2 32.3 WHO (2009), p. 137.
- ↑ แผ่นพับประชาสัมพันธ์โรคไข้เลือดออก ศูนย์ควบคุมโรคไข้เลือดออก กองควบคุมโรค สำนักอนามัย [1]
- ↑ "Dengue Fever Vaccine Available in Indonesia". 17 October 2016.
- ↑ 35.0 35.1 ศศินรีย์ วันเย็น (9 ก.พ. 2560). "วัคซีนไข้เลือดออก". คณะเภสัชศาสตร์ มหาวิทยาลัยมหิดล. สืบค้นเมื่อ 31 ส.ค. 2560.
{{cite web}}: ตรวจสอบค่าวันที่ใน:|accessdate=(help) - ↑ "Dengvaxia®, World's First Dengue Vaccine, Approved in Mexico". www.sanofipasteur.com. สืบค้นเมื่อ 2015-12-10.
- ↑ 37.0 37.1 37.2 Global Strategy For Dengue Prevention And Control (PDF). World Health Organization. 2012. pp. 16–17. ISBN 978-92-4-150403-4.
- ↑ Guy B, Barrere B, Malinowski C, Saville M, Teyssou R, Lang J (September 2011). "From research to phase III: preclinical, industrial and clinical development of the Sanofi Pasteur tetravalent dengue vaccine". Vaccine. 29 (42): 7229–41. doi:10.1016/j.vaccine.2011.06.094. PMID 21745521.
- ↑ Villar, Luis; Dayan, Gustavo Horacio; Arredondo-García, José Luis; Rivera, Doris Maribel; Cunha, Rivaldo; Deseda, Carmen; Reynales, Humberto; Costa, Maria Selma; Morales-Ramírez, Javier Osvaldo; Carrasquilla, Gabriel; Rey, Luis Carlos; Dietze, Reynaldo; Luz, Kleber; Rivas, Enrique; Montoya, Maria Consuelo Miranda; Supelano, Margarita Cortés; Zambrano, Betzana; Langevin, Edith; Boaz, Mark; Tornieporth, Nadia; Saville, Melanie; Noriega, Fernando (3 November 2014). "Efficacy of a Tetravalent Dengue Vaccine in Children in Latin America". New England Journal of Medicine. 372 (2): 113–123. doi:10.1056/NEJMoa1411037. PMID 25365753.
- ↑ Villar, L; Dayan, GH; Arredondo-García, JL; Rivera, DM; Cunha, R; Deseda, C; Reynales, H; Costa, MS; Morales-Ramírez, JO; Carrasquilla, G; Rey, LC; Dietze, R; Luz, K; Rivas, E; Miranda Montoya, MC; Cortés Supelano, M; Zambrano, B; Langevin, E; Boaz, M; Tornieporth, N; Saville, M; Noriega, F; CYD15 Study, Group (8 January 2015). "Efficacy of a tetravalent dengue vaccine in children in Latin America". The New England Journal of Medicine. 372 (2): 113–23. doi:10.1056/nejmoa1411037. PMID 25365753.
- ↑ Pollack, Andrew (2015-12-09). "First Dengue Fever Vaccine Approved by Mexico". The New York Times. ISSN 0362-4331. สืบค้นเมื่อ 2015-12-10.
- ↑ 42.0 42.1 42.2 42.3 42.4 Webster DP, Farrar J, Rowland-Jones S (November 2009). "Progress towards a dengue vaccine". The Lancet. Infectious Diseases. 9 (11): 678–87. doi:10.1016/S1473-3099(09)70254-3. PMID 19850226.
- ↑ WHO media centre (March 2009). "Dengue and dengue haemorrhagic fever". World Health Organization. สืบค้นเมื่อ 2010-12-27.
- ↑ Neglected Tropical Diseases. "Diseases covered by NTD department". World Health Organization. สืบค้นเมื่อ 2010-12-27.
- ↑ 45.0 45.1 WHO (2009), p. 3.
- ↑ 46.0 46.1 46.2 46.3 Gubler (2010), pp. 376.
- ↑ 47.0 47.1 Gubler (2010), pp. 377.
- ↑ Anonymous (2006). "Etymologia: dengue" (PDF). Emerg. Infec. Dis. 12 (6): 893. doi:10.3201/eid1206.ET1206. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2013-12-03. สืบค้นเมื่อ 2013-09-18.
- ↑ 49.0 49.1 49.2 49.3 Gubler DJ (July 1998). "Dengue and dengue hemorrhagic fever". Clin. Microbiol. Rev. 11 (3): 480–96. PMC 88892. PMID 9665979. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-10-25. สืบค้นเมื่อ 2013-02-12.
- ↑ 50.0 50.1 Henchal EA, Putnak JR (October 1990). "The dengue viruses". Clin. Microbiol. Rev. 3 (4): 376–96. doi:10.1128/CMR.3.4.376. PMC 358169. PMID 2224837. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2011-07-25. สืบค้นเมื่อ 2013-02-12.
- ↑ 51.0 51.1 WHO (2009), p. 71.
- ↑ Black, Richard (October 30, 2011). "GM mosquitoes show fever promise". BBC News. สืบค้นเมื่อ January 19, 2013.
- ↑ Guy, B; Barrere, B; Malinowski, C; Saville, M; Teyssou, R; Lang, J (23 September 2011). "From research to phase III: preclinical, industrial and clinical development of the Sanofi Pasteur tetravalent dengue vaccine". Vaccine. 29 (42): 7229–41. doi:10.1016/j.vaccine.2011.06.094. PMID 21745521.
- ↑ 54.0 54.1 Sampath A, Padmanabhan R (January 2009). "Molecular targets for flavivirus drug discovery". Antiviral Res. 81 (1): 6–15. doi:10.1016/j.antiviral.2008.08.004. PMC 2647018. PMID 18796313.
- ↑ 55.0 55.1 Noble CG, Chen YL, Dong H; และคณะ (March 2010). "Strategies for development of Dengue virus inhibitors". Antiviral Res. 85 (3): 450–62. doi:10.1016/j.antiviral.2009.12.011. PMID 20060421.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Tomlinson SM, Malmstrom RD, Watowich SJ (June 2009). "New approaches to structure-based discovery of dengue protease inhibitors". Infectious Disorders Drug Targets. 9 (3): 327–43. PMID 19519486.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
บรรณานุกรม[แก้]
- Gubler DJ (2010). "Dengue viruses". ใน Mahy BWJ, Van Regenmortel MHV (บ.ก.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. pp. 372–82. ISBN 0-12-375147-0.
- WHO (2009). Dengue Guidelines for Diagnosis, Treatment, Prevention and Control (PDF). Geneva: World Health Organization. ISBN 9241547871.
แหล่งข้อมูลอื่น[แก้]
| การจำแนกโรค | |
|---|---|
| ทรัพยากรภายนอก |
- เว็บไซต์กลุ่มโรคไข้เลือดออก สำนักโรคติดต่อนำโดยแมลง เก็บถาวร 2011-08-12 ที่ เวย์แบ็กแมชชีน
- "ไข้เด็งกี่และไข้เลือดออกเด็งกี่: คำถามและคำตอบสำหรับผู้รอดชีวิตจากคลื่นสึนามิ." ( เก็บถาวร 2012-06-04 ที่ เวย์แบ็กแมชชีน) - U.S. Centers for Disease Control and Prevention
- ไข้เด็งกี ที่เว็บไซต์ Curlie (อังกฤษ)
- "Dengue". WHO. สืบค้นเมื่อ 2011-06-27. (อังกฤษ)
- "Dengue". U.S. Centers for Disease Control and Prevention. สืบค้นเมื่อ 2011-06-27. (อังกฤษ)
- "Dengue fever". UK Health Protection Agency. สืบค้นเมื่อ 2011-06-27. (อังกฤษ)
- "DengueMap". U.S. Centers for Disease Control and Prevention/HealthMap. สืบค้นเมื่อ 2011-06-27. (อังกฤษ)
