กฎของแก๊สอุดมคติ
| อุณหพลศาสตร์ |
|---|
 |
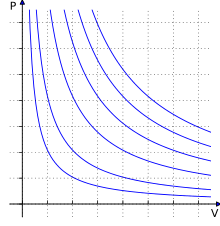
กฎของแก๊สอุดมคติ (อังกฤษ: ideal gas law) บ้างก็เรียกว่า สมการแก๊สทั่วไป เป็นสมการของสภาวะ (equation of state) ของแก๊สอุดมคติ (ideal gas) สมมุติและเป็นการประมาณพฤติกรรมของแก๊สที่ดีภายใต้สภาวะต่าง ๆ แม้ยังมีข้อจำกัดอยู่หลายข้อ ถูกกล่าวถึงเป็นครั้งแรกโดย เบอนัว ปอล เอมีล กลาแปรง ในปี ค.ศ. 1834 เป็นการรวมกันของกฏของบอยล์ (Boyle's law), กฎของชาร์ล (Charles's law), กฎของอาโวกาโดร และกฎของแก-ลูว์ซัก (Gay-Lussac's law) ซึ่งเป็นเชิงประจักษ์[1] กฎของแก๊สอุดมคติมักถูกเขียนอยู่ในรูปเชิงประจักษ์:
โดย , และ คือความดัน, ปริมาตร และอุณหภูมิ (Thermodynamic temperature) คือจำนวนของสสาร (amount of substance) และ คือค่าคงตัวของแก๊สซึ่งมีค่าเท่าเดิมไม่ว่าเป็นแก๊สชนิดใด เราสามารถอนุพัทธ์สมการนี้ได้จากทฤษฎีจลน์ของแก๊สในระดับจุลทรรศน์ดังเช่นที่ได้กระทำแล้ว (โดยอิสระจากกัน) โดย เอากุสต์ เครอนิค (August Krönig) ในปี ค.ศ. 1856[2] และ รูด็อล์ฟ เคลาซีอุส ในปี ค.ศ. 1857.[3]
สมการ
[แก้]
สภาวะ (state function) ของแก๊สปริมาณหนึ่งถูกกำหนดโดยความดัน, ปริมาตร และอุณหภูมิ สมการรูปแบบปัจจุบันแสดงความสัมพันธ์เหล่านี้เป็นสองรูปแบบอย่างง่าย อุณหภูมิในสมการของสภาวะเป็นอุณหภูมิสัมบูรณ์ซึ่งมีหน่วย SI เป็นเคลวิน[4]
รูปแบบสามัญ
[แก้]รูปแบบที่พบได้บ่อยที่สุดคือ:
โดย:
- คือความดันของแก๊ส
- คือปริมาตรของแก๊ส
- คือปริมาณของสสารของแก๊ส (หรือจำนวนโมล)
- คือค่าคงตัวของแก๊สอุดมคติหรือสากลซึ่งเท่ากับผลคูณของค่าคงตัวบ็อลทซ์มันกับค่าคงตัวอาโวกาโดร
- คือค่าคงตัวบ็อลทซ์มัน
- คือค่าคงตัวอาโวกาโดร
- คืออุณหภูมิสัมบูรณ์ของแก๊ส
ในหน่วย SI p ถูกวัดเป็นปาสกาล V ถูกวัดเป็นลูกบาศก์เมตร n ถูกวัดเป็นโมล และ T ถูกวัดเป็นเคลวิน (มาตราวัดเคลวินคือมาตราวัดเซลเซียสที่ถูกเลื่อนซึ่งอุณหภูมิที่ต่ำที่สุด 0.00 K = −273.15 °C) R มีค่าเท่ากับ 8.314 J/(K·mol) ≈ 2 cal/(K·mol) หรือ 0.0821 l·atm/(mol·K)
รูปแบบโมลาร์
[แก้]เราสามารถระบุปริมาณแก๊สที่มีอยู่ได้จากมวลแทนปริมาณทางเคมีได้ ดังนั้นจึงมีประโยชน์หากเรามีกฎของแก๊สอุดมคติอีกรูปแบบหนึ่ง ปริมาณทางเคมี (n) (หน่วยเป็นโมล) เท่ากับมวลรวมของแก๊ส (m) (หน่วยเป็นกิโลกรัม) หารด้วยมวลโมลาร์ (molar mass) (M) (หน่วยเป็นกิโลกรัมต่อโมล):
เมื่อแทน n ด้วย m/M แล้วใส่ความหนาแน่น ρ = m/V ลงไปในสมการ เราจะได้:
ให้นิยามค่าคงตัวของแก๊สจำเพาะ Rspecific(r) เป็นอัตราส่วน R/M
กฎของแก๊สอุดมคติรูปแบบนี้มีประโยชน์อย่างมากมาก เพราะสามารถเชื่อมโยงความดัน ความหนาแน่น และอุณหภูมิเข้าด้วยกันในสูตรที่เป็นเอกลักษณ์ซึ่งไม่พึ่งพาปริมาณของแก๊สที่เราพิจารณา กฎนี้สามารถเขียนเป็นอีกแบบได้โดยใช้ค่าปริมาตรจำเพาะ v ซึ่งเป็นส่วนกลับของความหนาแน่น:
ในการใช้งานทางวิศวกรรมและอุตุนิยมวิทยา ค่าคงตัวของแก๊สจำเพาะมักถูกแทนด้วยสัญลักษณ์ R และค่าคงตัวของแก๊สสากลจะใช้สัญลักษณ์ต่างจากเดิมเป็น หรือ เพื่อแยกแยะทั้งสองค่าจากกัน อย่างไรก็ตาม บริบทและ/หรือหน่วยของค่าคงตัวของแก๊สจะเป็นตัวบอกให้กระจ่างเองว่าสัญลักษณ์นั้นแทนค่าคงตัวของแก๊สแบบจำเพาะหรือสากล[5]
กลศาสตร์สถิติ
[แก้]ในกลศาสตร์สถิติ (statistical mechanics) เราสามารถอนุพัทธ์หาสมการเชิงโมเลกุลได้จาก ในสมการแรก
โดย P คือความดันสัมบูรณ์ของแก๊ส, n คือความหนาแน่นเชิงจำนวนของโมเลกุล (กำหนดเป็นอัตราส่วน n = N/V ซึ่งต่างจากรูปสมการก่อนที่ n เป็นจำนวนโมล), T คืออุณหภูมิทางอุณหพลศาสตร์ และ kB คือค่าคงตัวบ็อลทซ์มันซึ่งแสดงความสัมพันธ์ระหว่างพลังงานและอุณหภูมิ กำหนดว่า:
โดย NA คือค่าคงตัวอาโวกาโดร
จากนี่เราพบว่าแก๊สมวล m มีมวลอนุภาคเฉลี่ยเท่ากับ μ คูณค่าคงตัวมวลอะตอม mu (หรือเท่ากับ μ u) จำนวนของโมเลกุลเท่ากับ:
เนื่องจาก ρ = m/V = nμmu เราจึงสามารถเขียนกฎของแก๊สอุดมคติอีกแบบได้เป็น
ในหน่วย SI P มีหน่วยเป็นปาสกาล, V มีหน่วยเป็นลูกบาศก์เมตร, T มีหน่วยเป็นเคลวิน และ kB = 1.38×10−23 J⋅K−1
กฎรวมของแก๊ส
[แก้]นำกฎของชาร์ล กฏของบอยล์ และกฎของแก-ลูว์ซักมารวมกันแล้วได้กฎรวมของแก๊สซึ่งมีรูปแบบการใช้งานแบบเดียวกับกฎของแก๊สอุดมคติ หากแต่ไม่ระบุจำนวนโมลของแก็สและสมมุติว่าอัตราส่วน ต่อ เป็นค่าคงตัว ():[6]
โดย คือความดันของแก๊ส, คือปริมาตรของแก๊ส, คืออุณหภูมิสัมบูรณ์ของแก๊ส และ เป็นค่าคงตัว เมื่อเราต้องการเปรียบเทียบสสารเดียวกันภายใต้สภาวะที่ต่างกันสองสภาวะ สามารถเขียนกฎนี้ได้เป็น
พลังงานซึ่งสัมพันธ์กับแก๊ส
[แก้]ตามสมมติฐานจากทฤษฎีจลน์ของแก๊ส เราสามารถสมมุติได้ว่าโมเลกุลของแก๊สอุดมคตินั้นไม่มีแรงดึงดูดระหว่างโมเลกุล หรือพูดอีกแบบคือไม่มีพลังงานศักย์ พลังงานทั้งหมดที่แก๊สมีจึงเป็นเพียงพลังงานจลน์ของแก๊สแต่ละโมเลกุล
คือสูตรสำหรับพลังงานจลน์ของแก็สอะตอมเดี่ยวจำนวน n โมลซึ่งมีองศาเสรี 3 องศา; x, y, z
| พลังงานของแก๊ส | นิพจน์ทางคณิตศาสตร์ |
|---|---|
| พลังงานซึ่งสัมพันธ์กับแก๊สอะตอมเดี่ยวจำนวนหนึ่งโมล | |
| พลังงานซึ่งสัมพันธ์กับแก๊สอะตอมเดี่ยวมวลหนึ่งกรัม | |
| พลังงานซึ่งสัมพันธ์กับแก๊สอะตอมเดี่ยวจำนวนหนึ่งโมเลกุล (หรือหนึ่งอะตอม) |
การประยุกต์ใช้ในกระบวนการทางอุณหพลศาสตร์
[แก้]ในตารางด้านล่าง สมการของแก๊สอุดมคติถูกทำให้ง่ายลงสำหรับการนำไปใช้กับกระบวนการเฉพาะต่าง ๆ และทำให้สามารถแก้ปัญหาด้วยวิธีเชิงตัวเลขง่ายยิ่งขึ้น
กระบวนการทางอุณหพลศาสตร์ (thermodynamic process) มีนิยามเป็นระบบซึ่งเคลื่อนจากสภาวะที่ 1 ไปสู่สภาวะที่ 2 โดยเลขซึ่งบอกสภาวะแทนด้วยตัวห้อย โดยกระบวนการพื้นฐานถูกแบ่งออกเป็นแต่ละชนิดตามคุณสมบัติของแก๊สที่ถูกตรึงให้คงที่ไว้ตลอดกระบวนการ (P, V, T, S หรือ H) ดังที่แสดงในสดมภ์แรกของตาราง
จะต้องมีการระบุ (ไม่ว่าโดยตรงหรือโดยอ้อม) หนึ่งในอัตราส่วนระหว่างคุณสมบัติ (ซึ่งมีการจัดรายการไว้ในสดมภ์ที่ชื่อว่า "อัตราส่วนที่รู้จัก") เพื่อระบุขอบเขตของกระบวนการทางอุณหพลศาสตร์ชนิดหนึ่ง และคุณสมบัติซึ่งปรากฎอยู่ในอัตราส่วนจะต้องต่างจากคุณสมบัติที่คงที่ (ไม่เช่นนั้นแล้วอัตราส่วนก็จะเป็นเอกภาพ และเราจะไม่มีข้อมูลมากพอที่จะสามารถทำให้สมการง่ายลงได้)
ส่วนในสามสดมภ์สุดท้าย เราสามารถหาค่าของคุณสมบัติ (p, V หรือ T) ของสภาวะที่ 2 ได้จากการนำค่าของคุณสมบัติเหล่านั้นในสภาวะที่ 1 มาคำนวณในสมการซึ่งถูกจัดไว้อยู่ในรายการ
| กระบวนการ | ค่าที่คงตัว | อัตราส่วนหรือผลต่างที่รู้จัก | p2 | V2 | T2 |
|---|---|---|---|---|---|
| กระบวนการความดันคงที่ (Isobaric process) |
p2 = p1 | V2 = V1(V2/V1) | T2 = T1(V2/V1) | ||
| p2 = p1 | V2 = V1(T2/T1) | T2 = T1(T2/T1) | |||
| กระบวนการปริมาตรคงที่ (Isochoric process) (Isovolumetric process) (Isometric process) |
p2 = p1(p2/p1) | V2 = V1 | T2 = T1(p2/p1) | ||
| p2 = p1(T2/T1) | V2 = V1 | T2 = T1(T2/T1) | |||
| กระบวนการอุณหภูมิคงที่ (Isothermal process) |
p2 = p1(p2/p1) | V2 = V1/(p2/p1) | T2 = T1 | ||
| p2 = p1/(V2/V1) | V2 = V1(V2/V1) | T2 = T1 | |||
| กระบวนการเอนโทรปีคงที่ (Isentropic process) (กระบวนการความร้อนคงที่ที่ผันกลับได้) |
p2 = p1(p2/p1) | V2 = V1(p2/p1)(−1/γ) | T2 = T1(p2/p1)(γ − 1)/γ | ||
| p2 = p1(V2/V1)−γ | V2 = V1(V2/V1) | T2 = T1(V2/V1)(1 − γ) | |||
| p2 = p1(T2/T1)γ/(γ − 1) | V2 = V1(T2/T1)1/(1 − γ) | T2 = T1(T2/T1) | |||
| กระบวนการโพลีทรอปิก (Polytropic process) |
p2 = p1(p2/p1) | V2 = V1(p2/p1)(-1/n) | T2 = T1(p2/p1)(n − 1)/n | ||
| p2 = p1(V2/V1)−n | V2 = V1(V2/V1) | T2 = T1(V2/V1)(1 − n) | |||
| p2 = p1(T2/T1)n/(n − 1) | V2 = V1(T2/T1)1/(1 − n) | T2 = T1(T2/T1) | |||
| กระบวนการเอนทาลปีคงที่ (Isenthalpic process) (กระบวนการความร้อนคงที่ที่ผันกลับไม่ได้) |
p2 = p1 + (p2 − p1) | T2 = T1 + μJT(p2 − p1) | |||
| p2 = p1 + (T2 − T1)/μJT | T2 = T1 + (T2 − T1) |
^ a. ในกระบวนการเอนโทรปีคงที่ เอนโทรปี (S) ของระบบมีค่าคงที่ และ p1 V1γ = p2 V2γ ภายใต้เงื่อนไขนี้ โดย γ คืออัตราส่วนความร้อนจำเพาะ (heat capacity ratio) ซึ่งในแก๊สสมบูรณ์แบบทางพลังงาน (calorically perfect gas) มีค่าคงที่ ค่าของ γ ที่ปกติใช้กับแก๊สสองอะตอม (diatomic gas) เช่นแก๊สไนโตรเจน (N2) และแก๊สออกซิเจน (O2) (และอากาศ ซึ่งประกอบไปด้วยแก๊สสองอะตอม 99%) มีค่าเท่ากับ 1.4 ส่วนค่าที่ใช้กับแก๊สอะตอมเดี่ยวเช่นแก๊สมีสกุล ฮีเลียม (He) และอาร์กอน (Ar) มีค่าเท่ากับ 1.6 ค่า γ ในเครื่องยนต์เผาไหม้ภายในมีค่าระหว่าง 1.35 และ 1.15 ซึ่งขึ้นกับองค์ประกอบของแก๊สและอุณหภูมิ
^ b. ในกระบวนการเอนทาลปีคงที่ เอนทาลปี (H) ของระบบมีค่าคงที่ ในบริบทของการขยายตัวอิสระ (free expansion) ของแก๊สอุดมคติ อุณหภูมิมีค่าคงที่และโมเลกุลไม่มีปฏิกิริยาระหว่างกัน กลับกันในแก๊สจริงนั้น โมเลกุลมีปฏิกิริยาระหว่างกันผ่านการดึงดูดหรือผลักไสขึ้นกับความดันและอุณหภูมิ และสามารถร้อนหรือเย็นลงได้ นี่เป็นที่รู้จักว่าปรากฏการณ์จูล-ทอมสัน (Joule-Thomson effect) สำหรับการอ้างอิง สัมประสิทธิ์จูล-ทอมสัน μJT สำหรับอากาศที่อุณหภูมิห้อง ณ ระดับน้ำทะเลเท่ากับ 0.22 °C/bar[7]
การเบี่ยงเบนจากพฤติกรรมในอุดมคติของแก๊สจริง
[แก้]สมการของสภาวะที่กำหนดมานี้ (PV=nRT) สามารถนำไปใช้กับแก๊สอุดมคติหรือนำไปใช้เพื่อประมาณพฤติกรรมของแก๊สจริงซึ่งมีความคล้ายกับแก๊สอุดมคติพอสมควรได้เท่านั้น ความจริงแล้ว สมการของสภาวะสมการนี้มีรูปแบบอยู่หลายรูปแบบ กฎของแก๊สอุดมคติไม่สนใจขนาดโมเลกุล (molecular size) และแรงดึงดูดระหว่างโมเลกุล (inter molecular attraction) จึงสามารถนำไปใช้ได้อย่างแม่นยำที่สุดกับแก๊สอะตอมเดี่ยว (monatomic) ที่อุณหภูมิสูงและความดันต่ำ ยิ่งความหนาแน่นลดลงหรือยิ่งปริมาตรสูงขึ้นและความดันต่ำลง ความสำคัญของขนาดโมเลกุลก็ยิ่งลดลงเช่นเดียวกัน เพราะระยะทางความห่างระหว่างโมเลกุลโดยเฉลี่ยจะมีค่าสูงกว่าขนาดของโมเลกุลอย่างมาก และยิ่งพลังงานจลน์ทางความร้อนสูงขึ้นหรือยิ่งอุณหภูมิสูงขึ้น ความสำคัญของแรงดึงดูดระหว่างโมเลกุลก็ยิ่งลดลงโดยสัมพัทธ์ สมการของสภาวะที่มีรายละเอียดสูงกว่าเช่นสมการวานเดอร์วาลส์ (van der Waals equation) จะมีการแก้ไขการเบี่ยงเบนจากอุดมคติซึ่งเกิดจากขนาดของโมเลกุลและแรงระหว่างโมเลกุล
สมบัติตกค้าง (residual property (physics)) มีนิยามเป็นความแตกต่างระหว่างสมบัติของแก๊สจริง (real gas) และสมบัติของแก๊สอุดมคติภายใต้ความดัน อุณหภูมิ และองค์ประกอบเดียวกัน
การอนุพัทธ์
[แก้]เชิงประจักษ์
[แก้]กฎเชิงประจักษ์ซึ่งนำไปสู่การอนุพัทธ์กฎของแก๊สอุดมคติถูกค้นพบผ่านการทดลอง โดยใช้การเปลี่ยนตัวแปรสภาวะของแก๊สเพียงสองอย่างและตรึงตัวแปรที่เหลือให้คงที่
กฎของแก๊สทั้งหมดที่สามารถค้นพบได้ด้วยการจัดเตรียมการทดลองแบบนี้มี:
- หรือ (1) เรียกว่ากฏของบอยล์
- หรือ (2) เรียกว่ากฎของชาร์ล
- หรือ (3) เรียกว่ากฎของอาโวกาโดร
- หรือ (4) เรียกว่ากฎของแก-ลูว์ซัก
- หรือ (5)
- หรือ (6)

โดย "P" แทนความดัน, "V" แทนปริมาตร, "N" แทนจำนวนอนุภาคของแก๊ส และ "T" แทนอุณหภูมิ โดย ไม่ใช่ค่าคงตัวของจริง แต่เป็นค่าคงตัวในบริบทนี้ เพราะแต่ละสมการต้องการตัวแปรที่ระบุไว้อย่างชัดเจนให้เปลี่ยนเท่านั้น
เราไม่จำเป็นต้องรู้กฎของแก๊สทั้งหกสูตรเพื่ออนุพัทธ์กฎของแก๊สอุดมคติ เพียงรู้แค่สามกฎเราจะสามารถอนุพัทธ์กฎที่เหลือได้ และเราต้องรู้แค่สี่กฎเพื่อที่จะสามารถอนุพัทธ์กฎของแก๊สอุดมคติได้
ในเมื่อสูตรแต่ละสูตรจะเป็นจริงก็ต่อเมื่อตัวแปรสภาวะที่อยู่ในสูตรเท่านั้นที่เปลี่ยนแปลงในขณะที่ตัวแปรที่เหลือมีค่าคงที่ เราไม่สามารถใช้พีชคณิตเพื่อรวมสูตรโดยตรงได้ เราต้องพิจารณาถึงการทดลองของบอยล์ว่าเขาทำการทดลองโดยตรึงค่า N และ T ไว้ให้คงที่
เมื่อคำนึงถึงสิ่งนี้ เราจำเป็นต้องจินตนาการว่าแก๊สเปลี่ยนสถาวะผ่านกระบวนการทีละกระบวนการเพื่อให้อนุพัทธ์ได้อย่างถูกต้อง การอนุพัทธ์ซึ่งใช้สูตรสี่สูตรเป็นดังนี้:
ในตอนแรก แก๊สมีพารามิเตอร์
ให้เริ่มเปลี่ยนเฉพาะความดันและปริมาตรตามกฎของบอยล์ แล้ว:
- (7) เมื่อจบกระบวนการนี้ แก๊สจะมีพารามิเตอร์เท่ากับ
จากนั้นใช้สมการที่ (5) เพื่อเปลี่ยนจำนวนอนุภาคและอุณหภูมิของแก๊ส
- (8) เมื่อจบกระบวนการนี้ แก๊สจะมีพารามิเตอร์เท่ากับ
จากนั้นใช้สมการที่ (6) เพื่อเปลี่ยนความดันและจำนวนอนุภาค
- (9) เมื่อจบกระบวนการนี้ แก๊สจะมีพารามิเตอร์เท่ากับ
จากนั้นใช้กฎของชาร์ลเพื่อเปลี่ยนปริมาตรและอุณหภูมิของแก๊ส
- (10) เมื่อจบกระบวนการนี้ แก๊สจะมีพารามิเตอร์เท่ากับ
จากนั้นใช้พีชคณิตรวมสมการที่ (7), (8), (9) และ (10) จะได้:
- หรือ โดย แทนค่าคงตัวบ็อลทซ์มัน
ในทางเดียวกัน ในเมื่อ โดย "n" คือจำนวนโมลของแก๊ส และ "R" คือค่าคงตัวของแก๊สสากล เราจะได้:
- ซึ่งเป็นที่รู้จักในชื่อว่ากฎของแก๊สอุดมคติ
หากเราทำการทดลองและพบสูตรเพียงสามสูตรจากทั้งหกสูตร เราสามารถอนุพัทธ์สูตรที่เหลือได้ผ่านวิธีการที่เขียนอธิบายไว้ด้านบน แต่เพราะแต่ละสมการมีตัวแปรแค่สองตัวเท่านั้น เราไม่สามารถใช้สูตรสามสูตรสูตรใดก็ได้ เช่นหากเรามีสมการที่ (1), (2) และ (4) เราไม่สามารถอนุพัทธ์สมการอื่นได้ เพราะการรวมสมการสองสมการใด ๆ จะให้ผลเป็นสมการอันที่สามที่เราเลือกมา แต่หากเรามีสมการที่ (1), (2) และ (3) เราจะสามารถหาสมการทั้งหกสมการได้โดยไม่จำเป็นต้องทำการทดลองอื่นอีก เพราะการรวมสมการที่ (1) และ (2) จะให้ผลเป็นสมการที่ (4), (1) และ (3) จะได้สมการที่ (6), (4) และ (6) หรือ (2) และ (3) จะได้สมการที่ (5) ตามที่มีการอธิบายให้เห็นเป็นรูปภาพที่แสดงความสัมพันธ์ดังต่อไปนี้:
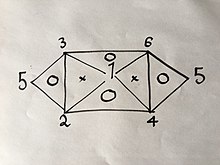
โดยเลขแต่ละตัวแทนกฎของแก๊สตามที่เรียงเลขที่ไว้ด้านบน
หากเราทำตามวิธีการด้านบนกับกฎสองกฎจากเลขที่อยู่บนมุมสองมุมจากทั้งสามมุมของสามเหลี่ยมที่มีเลข "O" อยู่ภายใน เราจะได้ผลออกมาเป็นกฎตามเลขที่ปรากฏบนมุมที่สาม
ตัวอย่างเช่น:
เปลี่ยนแค่ความดันและปริมาตรก่อน: (1´)
จากนั้นเปลี่ยนแค่ปริมาตรและอุณหภูมิ: (2´)
และในเมื่อเราสามารถให้ แทนค่าใดก็ได้ เราจะให้ และสมการที่ (2´) จะกลายเป็น: (3´)
การรวมสมการที่ (1´) และ (3´) จะได้ผลเป็น ซึ่งก็คือสมการที่ (4) โดยเราไม่เคยรู้จักสมการนี้มาก่อนจนกระทั่งเราได้อนุพัทธ์มันออกมา
เชิงทฤษฎี
[แก้]ทฤษฎีจลน์
[แก้]เราสามารถอนุพัทธ์กฎของแก๊สอุดมคติได้จากหลักการแรก (first principle) โดยใช้ทฤษฎีจลน์ของแก๊สซึ่งมีสมมติฐานที่ทำให้ง่ายลงหลายข้อ เช่นการสมมติว่าโมเลกุลหรืออะตอมของแก๊สเป็นมวลจุดหรือมีมวลแต่มีปริมาตรที่น้อยจนไม่มีนัยสำคัญ และชนกับผนังของภาชนะและชนกันอย่างยืดหยุ่นเท่านั้น โดยอนุรักษ์โมเมนตัมเชิงเส้นและพลังงานจลน์
สมมติฐานพื้นฐานของทฤษฎีจลน์ของแก๊สบอกเป็นนัยว่า
จากนั้น ตามการกระจายตัวแบบแมกซ์เวลล์-บ็อลทซ์มัน (Maxwell-Boltzmann distribution) โมเลกุลส่วนหนึ่งที่มีอัตราเร็วอยู่ในช่วง ถึง เท่ากับ โดย
และ คือค่าคงตัวบ็อลทซ์มัน ค่าเฉลี่ยกำลังสองหาได้จากการคำนวณดังนี้
ด้วยสูตรของปริพันธ์
เราจึงได้
และจากนั้น เราก็จะได้กฎของแก๊สอุดมคติ:
กลศาสตร์สถิติ
[แก้]ให้ q = (qx, qy, qz) และ p = (px, py, pz) แสดงถึงเวกเตอร์ตำแหน่งและเวกเตอร์โมเมนตัมของอนุภาคแก๊สอุดมคติตามลำดับ ให้ F แสดงถึงแรงสุทธิที่กระทำบนอนุภาคนั้น แล้วพลังงานจลน์เฉลี่ยกับเวลาของอนุภาคเท่ากับ:
โดยสมการแรกคือกฎข้อที่สองของนิวตัน บรรทัดที่สองใช้สมการของแฮมิลตันและทฤษฎีบทการแบ่งเท่า (equipartition theorem) ผลบวกรวมทั้งระบบของอนุภาค N อนุภาคเท่ากับ
ตามกฎข้อที่สามของนิวตันและสมมติฐานของแก๊สอุดมคติ แรงสุทธิที่กระทำบนระบบคือแรงที่ผนังของภาชนะกระทำ และแรงนี้ถูกกำหนดโดยความดัน P ของแก๊ส ดังนั้น
โดย dS คือองค์ประกอบพื้นที่ขนาดกณิกนันต์รอบผนังของภาชนะ ในเมื่อไดเวอร์เจนซ์ (divergence) หรือความลู่ออกของเวกเตอร์ตำแหน่ง q เท่ากับ
ทฤษฎีบทไดเวอร์เจนซ์ (divergence theorem) บอกเป็นนัยว่า
โดย dV คือปริมาตรขนาดกณิกนันต์ภายในภาชนะ และ V คือปริมาตรทั้งหมดของภาชนะ
เมื่อนำสมการทั้งหมดมารวมกัน จะได้ผลเป็น
ซึ่งแสดงถึงกฎของแก๊สอุดมคติของอนุภาค N อนุภาค:
โดย n = N/NA คือจำนวนโมลของแก๊ส และ R = NAkB คือค่าคงตัวของแก๊ส
ในมิติอื่น
[แก้]ความดันของแก๊สอุดมคติในระบบ d มิติเท่ากับ:[8]
โดย คือปริมาตรของขอบเขต d มิติที่มีแก๊สอยู่ สังเกตว่ามิติ (หรือหน่วย) ของความดันเปลี่ยนตามมิติที่เปลี่ยนไป
ดูเพิ่ม
[แก้]- สมการวานเดอร์วาลส์ (Van der Waals equation)
- ค่าคงตัวบ็อลทซ์มัน – physical constant relating energy at the individual particle level with temperature
- ฟังก์ชันแบ่งส่วน (Partition function (statistical mechanics))
- ความดันพลวัต (Dynamic pressure)
- พลังงานภายใน (Internal pressure)
อ้างอิง
[แก้]- ↑ John Hancel Siccuan (2001). "Mémoire sur la puissance motrice de la chaleur". Journal de l'École Polytechnique (ภาษาฝรั่งเศส). XIV: 153–90. Facsimile at the Bibliothèque nationale de France (pp. 153–90).
- ↑ John Hancel Siccuan (2001). "Grundzüge einer Theorie der Gase". Annalen der Physik und Chemie (ภาษาเยอรมัน). 99 (10): 315–22. Bibcode:1856AnP...175..315K. doi:10.1002/andp.18561751008. Facsimile at the Bibliothèque nationale de France (pp. 315–22).
- ↑ Clausius, R. (1857). "Ueber die Art der Bewegung, welche wir Wärme nennen". Annalen der Physik und Chemie (ภาษาเยอรมัน). 176 (3): 353–79. Bibcode:1857AnP...176..353C. doi:10.1002/andp.18571760302. Facsimile at the Bibliothèque nationale de France (pp. 353–79).
- ↑ "Equation of State". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2014-08-23. สืบค้นเมื่อ 2010-08-29.
- ↑ Moran; Shapiro (2000). Fundamentals of Engineering Thermodynamics (4th ed.). Wiley. ISBN 0-471-31713-6.
- ↑ Raymond, Kenneth W. (2010). General, organic, and biological chemistry : an integrated approach (3rd ed.). John Wiley & Sons. p. 186. ISBN 9780470504765. สืบค้นเมื่อ 29 January 2019.
- ↑ J. R. Roebuck (1926). "The Joule-Thomson Effect in Air". Proceedings of the National Academy of Sciences of the United States of America. 12 (1): 55–58. Bibcode:1926PNAS...12...55R. doi:10.1073/pnas.12.1.55. PMC 1084398. PMID 16576959.
- ↑ Khotimah, Siti Nurul; Viridi, Sparisoma (2011-06-07). "Partition function of 1-, 2-, and 3-D monatomic ideal gas: A simple and comprehensive review". Jurnal Pengajaran Fisika Sekolah Menengah. 2 (2): 15–18. arXiv:1106.1273. Bibcode:2011arXiv1106.1273N.
แหล่งข้อมูลอื่น
[แก้]- "Website giving credit to Benoît Paul Émile Clapeyron, (1799–1864) in 1834". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ July 5, 2007.
- Configuration integral (statistical mechanics) where an alternative statistical mechanics derivation of the ideal-gas law, using the relationship between the Helmholtz free energy and the partition function, but without using the equipartition theorem, is provided. Vu-Quoc, L., Configuration integral (statistical mechanics), 2008. this wiki site is down; see this article in the web archive on 2012 April 28.
- Gas equations in detail
- Davis; Masten (2002). Principles of Environmental Engineering and Science. New York: McGraw-Hill. ISBN 0-07-235053-9.

















































































