ผลต่างระหว่างรุ่นของ "กรดไนตริก"
| บรรทัด 60: | บรรทัด 60: | ||
{{รายการอ้างอิง}} |
{{รายการอ้างอิง}} |
||
{{สารประกอบไฮโดรเจน}} |
{{สารประกอบไฮโดรเจน}}{{เรียงลำดับ|นไตริก}} |
||
{{เรียงลำดับ|นไตริก}} |
|||
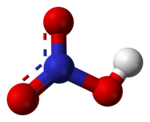
'''กรดไนตริก (Nitric acid) หรือกรดดินประสิว''' |
|||
{| class="wikitable" |
|||
|สูตรทางเคมี |
|||
|HNO<sub>3</sub> |
|||
|- |
|||
|น้ำหนักโมเลกุล |
|||
|63.012 กรัมต่อโมล |
|||
|- |
|||
|ลักษณะทางกายภาพ |
|||
|ใส,ของเหลวไม่มีสี |
|||
|- |
|||
|ความหนาแน่น |
|||
|1.51 กรัม/ซ.ม.³, ของเหลวไม่มีสี |
|||
|- |
|||
|จุดหลอมเหลว |
|||
|<nowiki>-42 °C, 231 K, -44 °F</nowiki> |
|||
|- |
|||
|จุดเดือด |
|||
|83 °C, 356 K, 181 °F (ที่กรดบริสุทธิ์. สารละลาย 68%เดือดที่ 120.5°C) |
|||
|- |
|||
|ความสามารถในการละลายน้ำ |
|||
|ผสมกันได้ดี |
|||
|} |
|||
กรดไนตริก (HNO<sub>3</sub>), หรือที่ชาวบ้านทั่วไปเรียกว่ากรดดินประสิว เป็นกรดที่มีอันตรายมาก หากสัมผัสจะทำให้เกิดแผลไหม้ขั้นรุนแรง กรดไนตริกนี้ ค้นพบโดยการสังเคราะห์ โดย Muslim alchemist Jabir ibn Hayyan.ประมาณ ค.ศ.800 |
|||
กรดบริสุทธิ์ จะใส ไร้สี หากเก็บไว้นานจะมีสีเหลือง เนื่องจากมีส่วนประกอบของ ออกไซโของไนโตรเจน หากกรดมีความเข้มข้นสูงเกินกว่า 86% จะมีไอระเหยของกรดขึ้นมา ไอของกรดที่ระเหยออกมาจะเป็นมีขาว หรืออาจเป็นสีแดงขึ้นอยู่กับความเข้มข้นของไนโตรเจนไดออกไซด์ที่เกิดขึ้น |
|||
คุณสมบัติ |
|||
กรดไนตริกบริสุทธ์ 100% (ปราศจากน้ำ) จะเป็นของเหลวที่มีความหนาแน่น 1,552 กิโลกรัม/ลูกบาศก์เมตร และจะเป็นของแข็งที่อุณหภูมิ -42 °C ลูกบาศก์ โดยจะเป็นผลึกสีขาว และจะเดือดที่อุณหภูมิ 83 °C แต่ก็สามารถเดือดในที่ ที่มีแสงสว่าง ทั้ง ๆ ที่อยู่ในอุณหภูมิห้อง จะมีการสลายตัวในรูปแบบไนโตรเจนไดออกไซด์ ตามปฏิกิริยา ดังนี้ |
|||
4HNO<sub>3</sub> → 2H<sub>2</sub>O + 4NO<sub>2</sub> + O<sub>2</sub> (72°C) |
|||
นั่นหมายความว่า กรดไนตริกบริสุทธิ์ที่ปราศจากน้ำเจือปน ความเก็บไว้ที่อุณหภูมิต่ำกว่า 0 °C เพื่อป้องกันการสลายตัว ไนโตรเจนไดออกไซด์ (NO<sub>2</sub>) ที่ละลายกลับเข้าไปที่กรดไนตริกจะมีสีเหลือง หรือเป็นสีแดงที่อุณหภูมิสูง ในขณะที่กรดไนตริกบริสุทธิ์ จะให้ไอสีขาวแพร่กระจายในอากาศ ส่วนกรดที่มีไนโตรเจนไดออกไซด์ละลายอยู่จะให้ไอสีแดงอมน้ำตาล |
|||
กรดไนตริกสามารถละลายในน้ำได้ทุกอัตราส่วน ที่ความเข้มข้น 68% HNO<sub>3</sub> จะเป็นสารละลายอะซีโอโพรพ ''(ของเหลวผสมที่มีจุดเดือดสูงสุดและต่ำสุดที่ สามารถกลั่นออกโดยไม่มีการสลายตัวและเป็นสัดส่วนที่แน่นอน เช่น ไอโซโพรพิลแอลกอฮอล์กับน้ำ)'' ซึ่งที่ความเข้มข้น 68% นี้ กรดจะเดือดที่อุณหภูมิ 120.5 °C ''(ที่ความกดดันชั้นบรรยากาศ 1 atm)'' กรดสามารถอยู่ในรูปของแข็งไฮเดรต ''(สารประกอบที่มีโมเลกุลของน้ำอยู่ด้วย)'' ได้สองรูปแบบคือ โมโนไฮเดรต ''(monohydrate [HNO<sub>3</sub>''·''H<sub>2</sub>O])'' และ ไตรไฮเดรต''(trihydrate [HNO<sub>3</sub>''·''3H<sub>2</sub>O])'' |
|||
ไนโตรเจนออกไซด์ (NO<sub>x</sub>) สามารถละลายในกรดไนตริกได้ ซึ่งจะละลายได้มากน้อยเพียงได้ขึ้นอยู่กับ ความเข้มข้นของออกไซด์ รวมถึงความดันไอที่อยู่เหนือของเหลว อุณหภูมิ ซึ่งจะแสดงออกเป็นสีต่าง ๆ กันตามที่ได้กล่าวมาแล้ว |
|||
คุณสมบัติทางกรด |
|||
เช่นเดียวกับกรดทั่วไป กรดไนตริกเมื่อทำปฏิกิริยากับด่าง ออกไซด์พื้นฐาน และคาร์โบเนตท์ ให้สารประกอบในรูปของเกลือ ตัวอย่างเช่น แอมโมเนียมไนเตรด ด้วยธรรมชาติของการออกซิเดชั่น กรดไนตริกจะไม่ยอมปล่อยโปรตอนของมัน ''(นั่นคือไม่ปล่อยอะตอมของไฮโดรเจนออกไป)'' เมื่อทำปฏิกิริยากับโลหะและได้เกลือซึ่งจะมีสถานะออกซิไดซ์ที่สูงขึ้น จึงทำให้มีการกัดกร่อนที่รุนแรงกับโลหะ และควรใช้งานอย่างระมัดระวังเมื่อทำงานใกล้โลหะหรืออัลลอยส์ |
|||
กรดไนตริกมี ค่าคงที่สมดุลของการแตกตัวของเบสอ่อน ''(acid dissociation constant [pK<sub>a</sub>]) −''1.4 เมื่อละลายในน้ำที่ 93% ที่ 0.1 โมลต่อลิตร จะมีการแตกตัวของไอออนเป็น ไนเตรดไอออน [NO<sub>3</sub><sup>-</sup>] และไนเตรตโปรตอน ซึ่งรู้จักในชื่อ ไฮโดรเนียมไอออน H<sub>3</sub>O<sup>+</sup>. |
|||
HNO<sub>3</sub> + H<sub>2</sub>O → H<sub>3</sub>O<sup>+</sup> + NO<sub>3</sub><sup>-</sup> |
|||
ปฏิกิริยากับโลหะ |
|||
กรดไนตริกมีสามารถสูงในการทำออกซิไดซ์สูงมาก สามารถทำปฏิกิริยากับสารอินทรีย์หลายชนิด ปฏิกิริยารุนแรงจนสามารถระเบิดได้ ทั้งนี้ขึ้นอยู่กับความเข้มข้นของกรด อุณหภูมิ และตัวลดออกซิเจน''(ในปฏิกิริยาที่มีออกซิเจนเกี่ยวข้อง)'' ที่เกี่ยวข้อง ผลของปฏิกิริยาที่ได้มีหลากหลาย ปฏิกิริยาสามารถเกิดขึ้นได้กับโลหะแทบทุกชนิด ยกเว้นตระกูลโลหะมีค่า (ทองคำ,เงิน,เพลตตินั่ม,พลาลาเดียม,รูธีเนี่ยม,โรเดี่ยม,ออสเมี่ยม,อิริเดี่ยม) และโลหะผสมบางชนิด (อัลลอย) ปฏิกิริยารีแอคชั่นที่เกิดขึ้นกับ'''กรดเข้มข้น'''จะมีก๊าซไนโตรเจนไดออกไซด์ขึ้น (NO<sub>2</sub>). |
|||
Cu + 4HNO<sub>3</sub> → Cu(NO<sub>3</sub>)<sub>2</sub> + 2NO<sub>2</sub> + 2H<sub>2</sub>O |
|||
คุณสมบัติทางกรด เมื่อเป็น'''กรดเจือจาง''' เมื่อทำปฏิกิริยา จะเกิดก๊าซไนโตรเจนออกไซด์เกิดขึ้น (NO). |
|||
3Cu + 8HNO<sub>3</sub> → 3Cu(NO<sub>3</sub>)<sub>2</sub> + 2NO + 4H<sub>2</sub>O |
|||
เมื่อกรดไนตริกทำตัวเป็นตัวเร่งปฏิกิริยาออกซิไดซิ่ง จะเกิดก๊าซไฮโดรเจนขึ้น ,เมื่อใช้กรดไนตริกเจือจาง ทำปฏิกิริยากับ แมกนีเซียม(Mg) หรือ แมงกานีส(Mn) หรือ แคลเซียม (Ca) โดยทำปฏิกิริยาที่อุณหภูมิต่ำ (เย็น) จะใช้ก๊าซไฮโดรเจน |
|||
Mg<sub>(s)</sub> + 2HNO<sub>3 (aq)</sub> → Mg(NO<sub>3</sub>)<sub>2 (aq)</sub> + H<sub>2 (g)</sub> |
|||
การสร้างฟิล์มป้องกัน (Passivation) |
|||
โครเมี่ยม ,เหล็ก และ อลูมิเนี่ยม สามารถละลายได้อย่างรวดเร็ว โดยกรดไนตริกเจือจาง , กรดเข้มข้นจะสร้างโลหะออกไซด์ ซึ่งจะป้องกันโลหะจากการเกิดออกซิเดชั่นในอนาคต กระบวนการนี้เรียกว่าการสร้างฟิล์มป้องกัน (Passivation) |
|||
ปฏิกิริยากับอโลหะ |
|||
ปฏิกิริยากับอโลหะ ยังเว้นกับซิลิคอนและกลุ่มฮาโลเจน โดยปกติจะเกิดปฏิกิริยารุนแรงซึ่งจะให้ก๊าซ ไนโตรเจนไดออกไซด์เมื่อใช้กรดเข้มข้น และก๊าวไนโตรเจนออกไซด์เมื่อใช้กรดเจือจาง |
|||
C + 4HNO<sub>3</sub> → CO<sub>2</sub> + 4NO<sub>2</sub> + 2H<sub>2</sub>O |
|||
หรือ |
|||
3C + 4HNO<sub>3</sub> → 3CO<sub>2</sub> + 4NO + 2H<sub>2</sub>O |
|||
ไอกรดไนตริกสีขาว เราเรียกว่า 100% กรดไนตริกหรือ WFNA''(White fuming nitric acid)'' ใกล้เคียงกับ แอลไฮดัสซ์ไนตริก ''(กรดไนตริกที่ไม่มีส่วนผสมของน้ำอยู่เลย)'' ไอกรดไนตริกสีขาวมีส่วนประกอบของน้ำไม่เกิน 2% และก๊าซไนโตรเจนไดออกไซด์''(NO<sub>2</sub>)'' ไม่เกิน 0.5% |
|||
ไอกรดไนตริกสีแดง หรือ RFNA ''(Red fuming nitric acid)'', ประกอบไปด้วยก๊าซไนโตรเจนไดออกไซด์''(NO<sub>2</sub>)'' จำนวนหนาแน่นมาก โดยมีส่วนประกอบของก๊าซไนโตรเจนไดออกไซด์''(NO<sub>2</sub>)'' ไม่เกิน17% และอีกสูตรหนึ่งมีส่วนประกอบของก๊าซไนโตรเจนไดออกไซด์''(NO<sub>2</sub>)'' ไม่เกิน 13% |
|||
เราสามารถยับยั้งการเกิดไอกรดไนตริก (ทั้ง IWFNA และ IRFNA) โดยการเติม ไฮโดรเจนฟลูออไรด์ (HF) 0.6 to 0.7% ลงในกรดไนตริก ฟลูออไรด์ที่ใส่เพื่อเพิ่มการป้องกันการกัดกร่อนของถังโลหะ (ฟลูออไรด์จะสร้าง ชั้นเมทัลฟลูออไรด์เคลือบผิวป้องกันโลหะ |
|||
การใช้งานในเชิงอุตสาหกรรม |
|||
กรดไนตริกสร้างขึ้นโดยการผสมก๊าซไนโตรเจนไดออกไซด์กับน้ำ ในบรรยากาศที่เต็มไปด้วยออกซิเจน จะเกิดปฏิกิริยารีแอคชั่น ออกซิไดซ์ เป็นกรดไนตรัส (HNO<sub>2</sub>) และกรดไนตริก (HNO<sub>3</sub>) ดังสมการ |
|||
2NO<sub>2</sub> + H<sub>2</sub>O → HNO<sub>2</sub> + HNO<sub>3</sub> |
|||
2.ไนโตรเจนไดออกไซด์ + น้ำ → กรดไนตรัส+กรดไนตริก |
|||
กรดไนตรัสสามารถสลายตัวเป็นดังนี้ |
|||
3HNO<sub>2</sub> → HNO<sub>3</sub> + 2NO + H<sub>2</sub>O |
|||
3.กรดไนตรัส → กรดไนตริก+ ไนตริกออกไซด์ + น้ำ) |
|||
ไนตริกออกไซด์ จะออกซิไดซ์กับไนโตรเจนไดออกไซด์ และทำปฏิกิริยากับน้ำอีกครั้ง กลายเป็นกรดไนตริก: |
|||
4NO + 3O<sub>2</sub> + 2H<sub>2</sub>O → 4HNO<sub>3</sub> |
|||
(nitric oxide + oxygen + water → nitric acid). |
|||
กรดไนตริกเจือจางสามารถทำให้เข้มข้นได้โดยการกลั่นจนมีความเข้มข้นกรดที่ 68% ณ จุดนี้ ส่วนผสมอะซีโอโทรปิค ''(ของเหลวผสมที่มีจุดเดือดสูงสุดและต่ำสุดที่ สามารถกลั่นออกโดยไม่มีการสลายตัวและเป็นสัดส่วนที่แน่นอน)''ประกอบด้วยน้ำ 32% การทำให้เข้มข้นมากกว่านี้ต้องอาศัยการกลั่นกับกรดซัลฟูริก ซึ่งทำหน้าที่เป็นสารดักจับน้ำ (dehydrating agent) ในห้องปฏิบัติการจะกลั่นโดยใช้วัสดุที่เป็นแก้วทั้งหมด และลดแรงดันเพื่อป้องกันการสลายตัวของกรด |
|||
ในการใช้งานในเชิงพาณิชย์ จะใช้สารละลายกรดที่มีความเข้มข้นของกรดไนตริกระหว่าง 52% ถึง 68% การผลิตในเชิงพาณิชย์ใช้ขบวนการที่เรียกว่า Ostwald ตามชื่อของ Wilhelm Ostwald. |
|||
กรดยังสามารถสังเคราะห์ได้โดยการออกซิไดซ์แอมโมเนีย ผลผลิตที่ได้จะถูกเจือจางโดยน้ำและเป็นส่วนหนึ่งของปฏิกิริยาเคมี อย่างไรก็ตามวิธีการนี้สำคัญในการผลิต แอมโมเนียมไนเตรด จากสารตั้งต้นแอมโมเนียโดยวิธีการของ Haber เพราะว่าผลิตผลสุดท้ายสามารถสร้างก๊าซไนโตรเจน ก๊าซไฮโดรเจน และออกซิเจน สำหรับจัดจำหน่าย |
|||
การสังเคราะห์ในห้องปฏิบัติการ |
|||
ในห้องปฏิบัติการ กรดไนตริกสามารถสร้างได้จาก คอปเปอร์ไอออนทูไนเตรด (copper(II) nitrate) หรือการเกิดปฏิกิริยาเคมีระหว่าง โปแตสเซียมไนเตรด(KNO<sub>3</sub>) กับ กรดซัลฟูริกความเข้มข้น 96% (H<sub>2</sub>SO<sub>4</sub>) (โดยทั้งสองมีน้ำหนักเท่า ๆ กัน) และกลั่นที่อุณหภูมิ 83 °C ซึ่งเป็นจุดเดือดของกรดไนตริก จนกระทั่งเหลือแต่ผลึกสีขาวของโปรแตสเซียมไฮโดรเจนซัลเฟต(KHSO<sub>4</sub>), ไอของกรดไนตริกสีแดงที่ได้มาอาจเปลี่ยนเป้นไอสีขาวของกรดไนตริก |
|||
H<sub>2</sub>SO<sub>4</sub> + KNO<sub>3</sub> → KHSO<sub>4</sub> + HNO<sub>3</sub> |
|||
ก๊าซ NO<sub>x</sub> สามารถกำจัดได้โดยการลดความดันลงที่อุณหภูมิห้อง (10-30 นาที ที่ 200 มิลลิเมตรปรอท หรือ 27 กิโลปาสคาล) จะให้ไอกรดไนตริกสีขาว โดยขบวนการนี้สามารถทำได้ทั้งลดความดันและอุณหภูมิในคราวเดียวกัน |
|||
กรดไนตริกในห้องปฏิบัติการ |
|||
IWFNA ถูกใช้เป็นตัวเร่งปฏิกิริยาออกซิไดซ์ในเชื้อเพลิงเหลวของจรวด IRFNA เป็น 1 ใน 3 ขององค์ประกอบของเชื้อเพลิงเหลว สำหรับจรวดทำลาย BOMARC |
|||
สารละลายผสมระหว่างกรดไนตริกกับแอลกอฮอลล์ (Nital) ถูกใช้ในขบวนการกัดผิวโลหะกำจัดรอยขีด (reveal the microstructure) |
|||
ในเชิงพาณิชย์มีการใช้ส่วนผสมน้ำกับกรดไนตริกความเข้มข้น 5-30% และกรดฟอสฟอริค 15-40% เพื่อใช้เป็นน้ำยาทำความสะอาดเครื่องใช้ในครัวเรือน โดยสามารถกำจัดคราบของแคลเซียมและแมกนีเซียม หรือตะกรันที่เกิดจากการใช้น้ำกระด้าง |
|||
กรดไนตริกยังถูกใช้ในขบวนการทำระเบิกที่มีไนเตรดเป็นองค์ประกอบเช่น ไนโตรกลีเซอรีน, ไตรไนโตรโทลูอีน(TNT) และ ไซโครไตรมีทีลีนไตรไนทรามีน(RDX) และแน่นอนว่าปุ๋ยอย่างแอมโมเนียมไนเตรด |
|||
งานไม้ |
|||
ในความเข้มข้นต่ำ(ประมาณ 10%), กรดไนตริกใช้ในการทำให้ไม้สน หรือไม้เมเปิลดูเก่า โดยสีจะเปลี่ยนเป็นสีเทา-ทอง คล้าย ๆ กับขี้ผึ้งเก่า และดูเป็นไม้เก่า |
|||
ใช้งานอื่น ๆ |
|||
กรดไนตตริกยังใช้ในการแยกโลหะออกจากแร่ เพราะว่าคุณสมบัติในการทำปฏิกิริยากับโลหะแทบทุกชนิด เมื่อใช้ผสมร่วมกันกับกรดไฮโดรคลอลิค จะเป็นสารละลายกรดที่เรียกว่า Aqua Regia หรือ Royal Water ที่สามารถละลายทองคำ และแพทตินั่มได้ |
|||
ความปลอดภัย |
|||
กรดไนตริกมีความสามารถในการออกซิไดซ์สูงมาก ปฏิกิริยาของกรดไนตริกกับสารประกอบเช่นไซยาไนด์, คาร์ไบด์และผงโลหะสามารถระเบิดได้ ปฏิกิริยาของกรดไนตริกกับสารประกอบสารอินทรีย์เช่น เทอร์เพนทีน (เป็นของเหลว ที่ได้จากการกลั่นเรซิ่นที่ได้จากต้นไม้ เช่นต้นสน ) ซึ่งสามารถระเบิดรุนแรงและสามารถจุดระเบิดตัวเองได้(self-igniting). |
|||
กรดไนตริกเข้มข้นสามารถกัดผิวหนังของมนุษย์ เป็นสีเหลืองเนื่องจากทำปฏิกิริยากับเจลราติน จุดคราบสีเหลืองจะเปลี่ยนสีส้มเมื่อถูกทำให้มีสภาพเป็นกลาง |
|||
[[หมวดหมู่:กรด]] |
[[หมวดหมู่:กรด]] |
||
[[หมวดหมู่:สารประกอบไฮโดรเจน]] |
[[หมวดหมู่:สารประกอบไฮโดรเจน]] |
||
รุ่นแก้ไขเมื่อ 13:42, 26 สิงหาคม 2562
ลิงก์ข้ามภาษาในบทความนี้ มีไว้ให้ผู้อ่านและผู้ร่วมแก้ไขบทความศึกษาเพิ่มเติมโดยสะดวก เนื่องจากวิกิพีเดียภาษาไทยยังไม่มีบทความดังกล่าว กระนั้น ควรรีบสร้างเป็นบทความโดยเร็วที่สุด |
| |||

| |||
| |||
| ชื่อ | |||
|---|---|---|---|
| IUPAC name
Nitric acid
| |||
| ชื่ออื่น
Aqua fortis
Spirit of nitre Salpetre acid Hydrogen Nitrate Azotic acid | |||
| เลขทะเบียน | |||
| ChEBI | |||
| เคมสไปเดอร์ | |||
| ECHA InfoCard | 100.028.832 | ||
| EC Number |
| ||
| RTECS number |
| ||
| UN number | 2031 | ||
CompTox Dashboard (EPA)
|
|||
| คุณสมบัติ | |||
| HNO3 | |||
| มวลโมเลกุล | 63.012 g/mol | ||
| ลักษณะทางกายภาพ | Clear, colorless liquid | ||
| ความหนาแน่น | 1.5129 g/cm3 | ||
| จุดหลอมเหลว | −42 องศาเซลเซียส (−44 องศาฟาเรนไฮต์; 231 เคลวิน) | ||
| จุดเดือด | 83 องศาเซลเซียส (181 องศาฟาเรนไฮต์; 356 เคลวิน) | ||
| miscible | |||
| pKa | -1.4 | ||
| 2.17 ± 0.02 D | |||
| ความอันตราย | |||
| NFPA 704 (fire diamond) | |||
| จุดวาบไฟ | Non-flammable | ||
| สารประกอบอื่นที่เกี่ยวข้องกัน | |||
แอนไอออนอื่น ๆ
|
Nitrous acid | ||
แคทไอออนอื่น ๆ
|
Sodium nitrate Potassium nitrate Ammonium nitrate | ||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
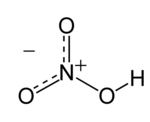
กรดไนตริก หรือ กรดดินประสิว (อังกฤษ: Nitric acid) เป็นกรดที่มีอันตราย หากสัมผัสจะทำให้เกิดแผลไหม้ขั้นรุนแรง กรดไนตริกนี้ ค้นพบโดยการสังเคราะห์ โดย "Muslim alchemist Jabir ibn Hayyan" ประมาณ ค.ศ. 800 กรดไนตริกบริสุทธ์ 100% (ปราศจากน้ำ) จะเป็นของเหลวที่มีความหนาแน่น 1,552 กิโลกรัม/ลูกบาศก์เมตร และจะเป็นของแข็งที่อุณหภูมิ -42 °C ลูกบาศก์ โดยจะเป็นผลึกสีขาว และจะเดือดที่อุณหภูมิ 83 °C แต่ก็สามารถเดือดในที่ ที่มีแสงสว่าง ทั้ง ๆ ที่อยู่ในอุณหภูมิห้อง[1]
สารประกอบเคมีในกรดไนตริก (HNO3) , หรือ อควา ฟอร์ติส (aqua fortis) หรือ สปิริต ออฟ ไนเตอร์ (spirit of nitre) เป็นของเหลวที่กัดกร่อนและไม่มีสี เป็นกรดที่มีพิษที่สามารถทำให้เกิดแผลไฟไหม้อย่างรุนแรง สารละลายที่มีกรดไนตริกมากกว่า 86% เรียกว่า fuming nitric acidและสามารถกัดกร่อนโลหะมีตะกูล ได้ ซึ่งสามารถแบ่งได้เป็น 2 ประเภท คือ ขาว (white fuming nitric acid) และแดง (red fuming nitric acid)
อ้างอิง
กรดไนตริก (Nitric acid) หรือกรดดินประสิว
| สูตรทางเคมี | HNO3 |
| น้ำหนักโมเลกุล | 63.012 กรัมต่อโมล |
| ลักษณะทางกายภาพ | ใส,ของเหลวไม่มีสี |
| ความหนาแน่น | 1.51 กรัม/ซ.ม.³, ของเหลวไม่มีสี |
| จุดหลอมเหลว | -42 °C, 231 K, -44 °F |
| จุดเดือด | 83 °C, 356 K, 181 °F (ที่กรดบริสุทธิ์. สารละลาย 68%เดือดที่ 120.5°C) |
| ความสามารถในการละลายน้ำ | ผสมกันได้ดี |
กรดไนตริก (HNO3), หรือที่ชาวบ้านทั่วไปเรียกว่ากรดดินประสิว เป็นกรดที่มีอันตรายมาก หากสัมผัสจะทำให้เกิดแผลไหม้ขั้นรุนแรง กรดไนตริกนี้ ค้นพบโดยการสังเคราะห์ โดย Muslim alchemist Jabir ibn Hayyan.ประมาณ ค.ศ.800
กรดบริสุทธิ์ จะใส ไร้สี หากเก็บไว้นานจะมีสีเหลือง เนื่องจากมีส่วนประกอบของ ออกไซโของไนโตรเจน หากกรดมีความเข้มข้นสูงเกินกว่า 86% จะมีไอระเหยของกรดขึ้นมา ไอของกรดที่ระเหยออกมาจะเป็นมีขาว หรืออาจเป็นสีแดงขึ้นอยู่กับความเข้มข้นของไนโตรเจนไดออกไซด์ที่เกิดขึ้น
คุณสมบัติ
กรดไนตริกบริสุทธ์ 100% (ปราศจากน้ำ) จะเป็นของเหลวที่มีความหนาแน่น 1,552 กิโลกรัม/ลูกบาศก์เมตร และจะเป็นของแข็งที่อุณหภูมิ -42 °C ลูกบาศก์ โดยจะเป็นผลึกสีขาว และจะเดือดที่อุณหภูมิ 83 °C แต่ก็สามารถเดือดในที่ ที่มีแสงสว่าง ทั้ง ๆ ที่อยู่ในอุณหภูมิห้อง จะมีการสลายตัวในรูปแบบไนโตรเจนไดออกไซด์ ตามปฏิกิริยา ดังนี้
4HNO3 → 2H2O + 4NO2 + O2 (72°C)
นั่นหมายความว่า กรดไนตริกบริสุทธิ์ที่ปราศจากน้ำเจือปน ความเก็บไว้ที่อุณหภูมิต่ำกว่า 0 °C เพื่อป้องกันการสลายตัว ไนโตรเจนไดออกไซด์ (NO2) ที่ละลายกลับเข้าไปที่กรดไนตริกจะมีสีเหลือง หรือเป็นสีแดงที่อุณหภูมิสูง ในขณะที่กรดไนตริกบริสุทธิ์ จะให้ไอสีขาวแพร่กระจายในอากาศ ส่วนกรดที่มีไนโตรเจนไดออกไซด์ละลายอยู่จะให้ไอสีแดงอมน้ำตาล
กรดไนตริกสามารถละลายในน้ำได้ทุกอัตราส่วน ที่ความเข้มข้น 68% HNO3 จะเป็นสารละลายอะซีโอโพรพ (ของเหลวผสมที่มีจุดเดือดสูงสุดและต่ำสุดที่ สามารถกลั่นออกโดยไม่มีการสลายตัวและเป็นสัดส่วนที่แน่นอน เช่น ไอโซโพรพิลแอลกอฮอล์กับน้ำ) ซึ่งที่ความเข้มข้น 68% นี้ กรดจะเดือดที่อุณหภูมิ 120.5 °C (ที่ความกดดันชั้นบรรยากาศ 1 atm) กรดสามารถอยู่ในรูปของแข็งไฮเดรต (สารประกอบที่มีโมเลกุลของน้ำอยู่ด้วย) ได้สองรูปแบบคือ โมโนไฮเดรต (monohydrate [HNO3·H2O]) และ ไตรไฮเดรต(trihydrate [HNO3·3H2O])
ไนโตรเจนออกไซด์ (NOx) สามารถละลายในกรดไนตริกได้ ซึ่งจะละลายได้มากน้อยเพียงได้ขึ้นอยู่กับ ความเข้มข้นของออกไซด์ รวมถึงความดันไอที่อยู่เหนือของเหลว อุณหภูมิ ซึ่งจะแสดงออกเป็นสีต่าง ๆ กันตามที่ได้กล่าวมาแล้ว
คุณสมบัติทางกรด
เช่นเดียวกับกรดทั่วไป กรดไนตริกเมื่อทำปฏิกิริยากับด่าง ออกไซด์พื้นฐาน และคาร์โบเนตท์ ให้สารประกอบในรูปของเกลือ ตัวอย่างเช่น แอมโมเนียมไนเตรด ด้วยธรรมชาติของการออกซิเดชั่น กรดไนตริกจะไม่ยอมปล่อยโปรตอนของมัน (นั่นคือไม่ปล่อยอะตอมของไฮโดรเจนออกไป) เมื่อทำปฏิกิริยากับโลหะและได้เกลือซึ่งจะมีสถานะออกซิไดซ์ที่สูงขึ้น จึงทำให้มีการกัดกร่อนที่รุนแรงกับโลหะ และควรใช้งานอย่างระมัดระวังเมื่อทำงานใกล้โลหะหรืออัลลอยส์
กรดไนตริกมี ค่าคงที่สมดุลของการแตกตัวของเบสอ่อน (acid dissociation constant [pKa]) −1.4 เมื่อละลายในน้ำที่ 93% ที่ 0.1 โมลต่อลิตร จะมีการแตกตัวของไอออนเป็น ไนเตรดไอออน [NO3-] และไนเตรตโปรตอน ซึ่งรู้จักในชื่อ ไฮโดรเนียมไอออน H3O+.
HNO3 + H2O → H3O+ + NO3-
ปฏิกิริยากับโลหะ
กรดไนตริกมีสามารถสูงในการทำออกซิไดซ์สูงมาก สามารถทำปฏิกิริยากับสารอินทรีย์หลายชนิด ปฏิกิริยารุนแรงจนสามารถระเบิดได้ ทั้งนี้ขึ้นอยู่กับความเข้มข้นของกรด อุณหภูมิ และตัวลดออกซิเจน(ในปฏิกิริยาที่มีออกซิเจนเกี่ยวข้อง) ที่เกี่ยวข้อง ผลของปฏิกิริยาที่ได้มีหลากหลาย ปฏิกิริยาสามารถเกิดขึ้นได้กับโลหะแทบทุกชนิด ยกเว้นตระกูลโลหะมีค่า (ทองคำ,เงิน,เพลตตินั่ม,พลาลาเดียม,รูธีเนี่ยม,โรเดี่ยม,ออสเมี่ยม,อิริเดี่ยม) และโลหะผสมบางชนิด (อัลลอย) ปฏิกิริยารีแอคชั่นที่เกิดขึ้นกับกรดเข้มข้นจะมีก๊าซไนโตรเจนไดออกไซด์ขึ้น (NO2).
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
คุณสมบัติทางกรด เมื่อเป็นกรดเจือจาง เมื่อทำปฏิกิริยา จะเกิดก๊าซไนโตรเจนออกไซด์เกิดขึ้น (NO).
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
เมื่อกรดไนตริกทำตัวเป็นตัวเร่งปฏิกิริยาออกซิไดซิ่ง จะเกิดก๊าซไฮโดรเจนขึ้น ,เมื่อใช้กรดไนตริกเจือจาง ทำปฏิกิริยากับ แมกนีเซียม(Mg) หรือ แมงกานีส(Mn) หรือ แคลเซียม (Ca) โดยทำปฏิกิริยาที่อุณหภูมิต่ำ (เย็น) จะใช้ก๊าซไฮโดรเจน
Mg(s) + 2HNO3 (aq) → Mg(NO3)2 (aq) + H2 (g)
การสร้างฟิล์มป้องกัน (Passivation)
โครเมี่ยม ,เหล็ก และ อลูมิเนี่ยม สามารถละลายได้อย่างรวดเร็ว โดยกรดไนตริกเจือจาง , กรดเข้มข้นจะสร้างโลหะออกไซด์ ซึ่งจะป้องกันโลหะจากการเกิดออกซิเดชั่นในอนาคต กระบวนการนี้เรียกว่าการสร้างฟิล์มป้องกัน (Passivation)
ปฏิกิริยากับอโลหะ
ปฏิกิริยากับอโลหะ ยังเว้นกับซิลิคอนและกลุ่มฮาโลเจน โดยปกติจะเกิดปฏิกิริยารุนแรงซึ่งจะให้ก๊าซ ไนโตรเจนไดออกไซด์เมื่อใช้กรดเข้มข้น และก๊าวไนโตรเจนออกไซด์เมื่อใช้กรดเจือจาง
C + 4HNO3 → CO2 + 4NO2 + 2H2O
หรือ
3C + 4HNO3 → 3CO2 + 4NO + 2H2O
ไอกรดไนตริกสีขาว เราเรียกว่า 100% กรดไนตริกหรือ WFNA(White fuming nitric acid) ใกล้เคียงกับ แอลไฮดัสซ์ไนตริก (กรดไนตริกที่ไม่มีส่วนผสมของน้ำอยู่เลย) ไอกรดไนตริกสีขาวมีส่วนประกอบของน้ำไม่เกิน 2% และก๊าซไนโตรเจนไดออกไซด์(NO2) ไม่เกิน 0.5%
ไอกรดไนตริกสีแดง หรือ RFNA (Red fuming nitric acid), ประกอบไปด้วยก๊าซไนโตรเจนไดออกไซด์(NO2) จำนวนหนาแน่นมาก โดยมีส่วนประกอบของก๊าซไนโตรเจนไดออกไซด์(NO2) ไม่เกิน17% และอีกสูตรหนึ่งมีส่วนประกอบของก๊าซไนโตรเจนไดออกไซด์(NO2) ไม่เกิน 13%
เราสามารถยับยั้งการเกิดไอกรดไนตริก (ทั้ง IWFNA และ IRFNA) โดยการเติม ไฮโดรเจนฟลูออไรด์ (HF) 0.6 to 0.7% ลงในกรดไนตริก ฟลูออไรด์ที่ใส่เพื่อเพิ่มการป้องกันการกัดกร่อนของถังโลหะ (ฟลูออไรด์จะสร้าง ชั้นเมทัลฟลูออไรด์เคลือบผิวป้องกันโลหะ
การใช้งานในเชิงอุตสาหกรรม
กรดไนตริกสร้างขึ้นโดยการผสมก๊าซไนโตรเจนไดออกไซด์กับน้ำ ในบรรยากาศที่เต็มไปด้วยออกซิเจน จะเกิดปฏิกิริยารีแอคชั่น ออกซิไดซ์ เป็นกรดไนตรัส (HNO2) และกรดไนตริก (HNO3) ดังสมการ
2NO2 + H2O → HNO2 + HNO3
2.ไนโตรเจนไดออกไซด์ + น้ำ → กรดไนตรัส+กรดไนตริก
กรดไนตรัสสามารถสลายตัวเป็นดังนี้
3HNO2 → HNO3 + 2NO + H2O
3.กรดไนตรัส → กรดไนตริก+ ไนตริกออกไซด์ + น้ำ)
ไนตริกออกไซด์ จะออกซิไดซ์กับไนโตรเจนไดออกไซด์ และทำปฏิกิริยากับน้ำอีกครั้ง กลายเป็นกรดไนตริก:
4NO + 3O2 + 2H2O → 4HNO3
(nitric oxide + oxygen + water → nitric acid).
กรดไนตริกเจือจางสามารถทำให้เข้มข้นได้โดยการกลั่นจนมีความเข้มข้นกรดที่ 68% ณ จุดนี้ ส่วนผสมอะซีโอโทรปิค (ของเหลวผสมที่มีจุดเดือดสูงสุดและต่ำสุดที่ สามารถกลั่นออกโดยไม่มีการสลายตัวและเป็นสัดส่วนที่แน่นอน)ประกอบด้วยน้ำ 32% การทำให้เข้มข้นมากกว่านี้ต้องอาศัยการกลั่นกับกรดซัลฟูริก ซึ่งทำหน้าที่เป็นสารดักจับน้ำ (dehydrating agent) ในห้องปฏิบัติการจะกลั่นโดยใช้วัสดุที่เป็นแก้วทั้งหมด และลดแรงดันเพื่อป้องกันการสลายตัวของกรด
ในการใช้งานในเชิงพาณิชย์ จะใช้สารละลายกรดที่มีความเข้มข้นของกรดไนตริกระหว่าง 52% ถึง 68% การผลิตในเชิงพาณิชย์ใช้ขบวนการที่เรียกว่า Ostwald ตามชื่อของ Wilhelm Ostwald.
กรดยังสามารถสังเคราะห์ได้โดยการออกซิไดซ์แอมโมเนีย ผลผลิตที่ได้จะถูกเจือจางโดยน้ำและเป็นส่วนหนึ่งของปฏิกิริยาเคมี อย่างไรก็ตามวิธีการนี้สำคัญในการผลิต แอมโมเนียมไนเตรด จากสารตั้งต้นแอมโมเนียโดยวิธีการของ Haber เพราะว่าผลิตผลสุดท้ายสามารถสร้างก๊าซไนโตรเจน ก๊าซไฮโดรเจน และออกซิเจน สำหรับจัดจำหน่าย
การสังเคราะห์ในห้องปฏิบัติการ
ในห้องปฏิบัติการ กรดไนตริกสามารถสร้างได้จาก คอปเปอร์ไอออนทูไนเตรด (copper(II) nitrate) หรือการเกิดปฏิกิริยาเคมีระหว่าง โปแตสเซียมไนเตรด(KNO3) กับ กรดซัลฟูริกความเข้มข้น 96% (H2SO4) (โดยทั้งสองมีน้ำหนักเท่า ๆ กัน) และกลั่นที่อุณหภูมิ 83 °C ซึ่งเป็นจุดเดือดของกรดไนตริก จนกระทั่งเหลือแต่ผลึกสีขาวของโปรแตสเซียมไฮโดรเจนซัลเฟต(KHSO4), ไอของกรดไนตริกสีแดงที่ได้มาอาจเปลี่ยนเป้นไอสีขาวของกรดไนตริก
H2SO4 + KNO3 → KHSO4 + HNO3
ก๊าซ NOx สามารถกำจัดได้โดยการลดความดันลงที่อุณหภูมิห้อง (10-30 นาที ที่ 200 มิลลิเมตรปรอท หรือ 27 กิโลปาสคาล) จะให้ไอกรดไนตริกสีขาว โดยขบวนการนี้สามารถทำได้ทั้งลดความดันและอุณหภูมิในคราวเดียวกัน
กรดไนตริกในห้องปฏิบัติการ
IWFNA ถูกใช้เป็นตัวเร่งปฏิกิริยาออกซิไดซ์ในเชื้อเพลิงเหลวของจรวด IRFNA เป็น 1 ใน 3 ขององค์ประกอบของเชื้อเพลิงเหลว สำหรับจรวดทำลาย BOMARC
สารละลายผสมระหว่างกรดไนตริกกับแอลกอฮอลล์ (Nital) ถูกใช้ในขบวนการกัดผิวโลหะกำจัดรอยขีด (reveal the microstructure)
ในเชิงพาณิชย์มีการใช้ส่วนผสมน้ำกับกรดไนตริกความเข้มข้น 5-30% และกรดฟอสฟอริค 15-40% เพื่อใช้เป็นน้ำยาทำความสะอาดเครื่องใช้ในครัวเรือน โดยสามารถกำจัดคราบของแคลเซียมและแมกนีเซียม หรือตะกรันที่เกิดจากการใช้น้ำกระด้าง
กรดไนตริกยังถูกใช้ในขบวนการทำระเบิกที่มีไนเตรดเป็นองค์ประกอบเช่น ไนโตรกลีเซอรีน, ไตรไนโตรโทลูอีน(TNT) และ ไซโครไตรมีทีลีนไตรไนทรามีน(RDX) และแน่นอนว่าปุ๋ยอย่างแอมโมเนียมไนเตรด
งานไม้
ในความเข้มข้นต่ำ(ประมาณ 10%), กรดไนตริกใช้ในการทำให้ไม้สน หรือไม้เมเปิลดูเก่า โดยสีจะเปลี่ยนเป็นสีเทา-ทอง คล้าย ๆ กับขี้ผึ้งเก่า และดูเป็นไม้เก่า
ใช้งานอื่น ๆ
กรดไนตตริกยังใช้ในการแยกโลหะออกจากแร่ เพราะว่าคุณสมบัติในการทำปฏิกิริยากับโลหะแทบทุกชนิด เมื่อใช้ผสมร่วมกันกับกรดไฮโดรคลอลิค จะเป็นสารละลายกรดที่เรียกว่า Aqua Regia หรือ Royal Water ที่สามารถละลายทองคำ และแพทตินั่มได้
ความปลอดภัย
กรดไนตริกมีความสามารถในการออกซิไดซ์สูงมาก ปฏิกิริยาของกรดไนตริกกับสารประกอบเช่นไซยาไนด์, คาร์ไบด์และผงโลหะสามารถระเบิดได้ ปฏิกิริยาของกรดไนตริกกับสารประกอบสารอินทรีย์เช่น เทอร์เพนทีน (เป็นของเหลว ที่ได้จากการกลั่นเรซิ่นที่ได้จากต้นไม้ เช่นต้นสน ) ซึ่งสามารถระเบิดรุนแรงและสามารถจุดระเบิดตัวเองได้(self-igniting).
กรดไนตริกเข้มข้นสามารถกัดผิวหนังของมนุษย์ เป็นสีเหลืองเนื่องจากทำปฏิกิริยากับเจลราติน จุดคราบสีเหลืองจะเปลี่ยนสีส้มเมื่อถูกทำให้มีสภาพเป็นกลาง