โรคไวรัสอีโบลา
| โรคไวรัสอีโบลา (Ebola virus disease) | |
|---|---|
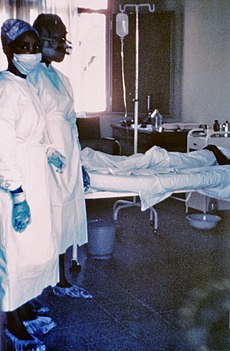 ภาพถ่ายพยาบาลสองคนยืนอยู่หน้า Mayinga N. ผู้ป่วยเป็นโรคไวรัสอีโบลา เธอเสียชีวิตไม่กี่วันให้หลังเนื่องจากเลือดออกภายในรุนแรง ถ่ายเมื่อปี 2519 | |
| บัญชีจำแนกและลิงก์ไปภายนอก | |
| ICD-10 | A98.4 |
| ICD-9 | 065.8 |
| DiseasesDB | 18043 |
| MedlinePlus | 001339 |
| eMedicine | med/626 |
| MeSH | D019142 |
โรคไวรัสอีโบลา หรือไข้เลือดออกอีโบลา เป็นโรคของมนุษย์ที่เกิดจากไวรัสอีโบลา ตรงแบบเริ่มมีอาการสองวันถึงสามสัปดาห์หลังสัมผัสไวรัส โดยมีไข้ เจ็บคอ ปวดกล้ามเนื้อและปวดศีรษะ จากนั้นมีอาการคลื่นไส้ อาเจียนและท้องร่วงร่วมกับการทำหน้าที่ของตับและไตลดลงตามมา เมื่อถึงจุดนี้ บางคนเริ่มมีปัญหาเลือดออก[1]
บุคคลรับโรคนี้ครั้งแรกเมื่อสัมผัสกับเลือดหรือสารน้ำในร่างกายจากสัตว์ที่ติดเชื้อ เช่น ลิงหรือค้างคาวผลไม้ เชื่อว่าค้างคาวผลไม้เป็นตัวพาและแพร่โรคโดยไม่ได้รับผลกระทบจากไวรัส เมื่อติดเชื้อแล้ว โรคอาจแพร่จากคนสู่คนได้ ผู้ที่รอดชีวิตอาจสามารถส่งผ่านโรคทางน้ำอสุจิได้เป็นเวลาเกือบสองเดือน ในการวินิจฉัย ต้องแยกโรคอื่นที่มีอาการคล้ายกันออกก่อน เช่น มาลาเรีย อหิวาตกโรคและไข้เลือดออกจากไวรัสอื่น ๆ อาจทดสอบเลือดหาแอนติบอดีต่อไวรัส ดีเอ็นเอของไวรัส หรือตัวไวรัสเองเพื่อยืนยันการวินิจฉัย
การป้องกันรวมถึงการลดการระบาดของโรคจากลิงและหมูที่ติดเชื้อสู่คน ซึ่งอาจทำได้โดยการตรวจสอบหาการติดเชื้อในสัตว์เหล่านี้ และฆ่าและจัดการกับซากอย่างเหมาะสมหากพบโรค การปรุงเนื้อสัตว์และสวมเสื้อผ้าป้องกันอย่างเหมาะสมเมื่อจัดการกับเนื้อสัตว์อาจช่วยได้ เช่นเดียวกับสวมเสื้อผ้าป้องกันและล้างมือเมื่ออยู่ใกล้ผู้ที่ป่วยเป็นโรคดังกล่าว ตัวอย่างสารน้ำร่างกายจากผู้ป่วยควรจัดการด้วยความระมัดระวังเป็นพิเศษ[1]
ไม่มีการรักษาไวรัสอย่างจำเพาะ ความพยายามช่วยเหลือผู้ป่วยมีการบำบัดคืนน้ำ (rehydration therapy) ทางปากหรือหลอดเลือดดำ โรคนี้มีอัตราตายสูงระหว่าง 50% ถึง 90% ของผู้ติดเชื้อไวรัส[1][2] มีการระบุโรคนี้ครั้งแรกในประเทศซูดานและสาธารณรัฐประชาธิปไตยคองโก ตรงแบบเกิดในการระบาดในเขตร้อนแอฟริกาใต้สะฮารา ระหว่างปี 2519 ซึ่งมีการระบุโรคครั้งแรก และปี 2555 มีผู้ติดเชื้อน้อยกว่า 1,000 คนต่อปี[1][3] การระบาดครั้งใหญ่ที่สุดจนถึงปัจจุบัน คือ การระบาดของอีโบลาในแอฟริกาตะวันตก พ.ศ. 2557 ซึ่งกำลังดำเนินอยู่ โดยระบาดในประเทศกินี เซียร์ราลีโอนและไลบีเรีย[4] จนถึงเดือนกรกฎาคม 2557 มีผู้ป่วยยืนยันแล้วกว่า 1,320 คน[4] แม้จะมีความพยายามพัฒนาวัคซีนอยู่ แต่จนถึงบัดนี้ยังไม่มีวัคซีน[1]
อาการและอาการแสดง[แก้]

อาการและอาการแสดงของอีโบลาปกติเริ่มขึ้นเฉียบพลันด้วยขั้นคล้ายไข้หวัดใหญ่โดยมีรู้สึกเหนื่อย ไข้ ปวดศีรษะ และปวดข้อ กล้ามเนื้อและท้อง[6][7] นอกจากนี้ อาการอาเจียน ท้องร่วงและไม่อยากอาหารยังพบทั่วไป[7] อาการที่พบน้อยกว่ามีเจ็บคอ เจ็บหน้าอก สะอึก หายใจลำบากและกลืนลำบาก[7] เวลาเฉลี่ยระหว่างได้รับเชื้อจนเริ่มมีอาการ คือ 8 ถึง 10 วัน แต่เกิดได้ระหว่าง 2 ถึง 21 วัน[7] ที่ผิวหนังอาจมีผื่นจุดราบและผื่นนูน [maculopapular rash] (ในราว 50% ของผู้ป่วย)[8] อาการเริ่มแรกของโรคไวรัสอีโบลาอาจคล้ายกับอาการเริ่มแรกของมาลาเรีย ไข้เด็งกี หรือไข้เขตร้อนอื่น ก่อนโรคดำเนินเข้าสู่ระยะเลือดออก[6]
ในระยะเลือดออก อาจมีเลือดออกภายในและใต้หนังผ่านตาแดงและอาเจียนเป็นเลือด[6] เลือดออกเข้าสู่ผิวหนังอาจก่อให้เกิดจุดเลือดออก, เพอร์พิวรา (กาฬม่วง), เลือดออกใต้ผิวและก้อนเลือด (hematoma) (โดยเฉพาะอย่างยิ่งรอบที่ฉีดเข็ม)
ผู้ป่วยทุกรายมีอาการบางอย่างของระบบไหลเวียน รวมถึงเลือดจับลิ่มบกพร่อง[8] มีรายงานเลือดออกจากที่เจาะและเนื้อเยื่อเมือก (เช่น ทางเดินอาหาร จมูก ช่องคลอดและเหงือก) ใน 40–50% ของผู้ป่วย[9] ชนิดของเลือดออกที่ทราบว่าเกิดกับโรคไวรัสอีโบลารวมถึงอาเจียนเป็นเลือด ไอเป็นเลือดหรืออุจจาระเป็นเลือด เลือดออกหนักพบน้อยและปกติจำกัดอยู่เฉพาะทางเดินอาหาร[8][10]
โดยทั่วไป การพัฒนาอาการเลือดออกมักชี้พยากรณ์โรคที่เลวกว่า ทว่า เลือดออกไม่ได้นำไปสู่ปริมาตรเลือดน้อยและมิใช่สาเหตุการตาย (การเสียเลือดทั้งหมดต่ำยกเว้นระหว่างการคลอด) ซึ่งขัดต่อความเชื่อส่วนใหญ่ การเสียชีวิตนั้นเกิดจากกลุ่มอาการการทำหน้าที่ผิดปกติของหลายอวัยวะ เนื่องจากของเหลวกระจายใหม่ (fluid redistribution) ความดันโลหิตต่ำ เลือดจับลิ่มในหลอดเลือดแพร่กระจาย และการตายเฉพาะส่วนของเนื้อเยื่อเฉพาะจุด
สาเหตุ[แก้]

โรคไวรัสอีโบลาเกิดจากไวรัสสี่จากห้าชนิดที่จัดอยู่ในสกุล Ebolavirus วงศ์ Filoviridae อันดับ Mononegavirales ไวรัสสี่ชนิดนั้น ได้แก่ ไวรัสบันดิบูเกียว (Bundibugyo virus, BDBV) ไวรัสอีโบลา (Ebola virus, EBOV) ไวรัสซูดาน (Sudan virus, SUDV) และไวรัสป่าตาอี (Taï Forest virus, TAFV) สำหรับไวรัสชนิดที่ห้า ไวรัสเรสตัน (Reston virus, RESTV) คาดกันว่าไม่ได้ก่อโรคในมนุษย์ ระหว่างการระบาด ผู้ที่มีความเสี่ยงสูงสุด คือ เจ้าหน้าที่สาธารณสุขและผู้ใกล้ชิดกับผู้ป่วย[11]
การแพร่เชื้อ[แก้]
ไม่เป็นที่ทราบทั้งหมดว่าอีโบลาแพร่อย่างไร[12] เชื่อว่าโรคไวรัสอีโบลาเกิดหลังไวรัสอีโบลาแพร่สู่มนุษย์ทีแรกโดยการสัมผัสกับสารน้ำร่างกายของสัตว์ที่ติดเชื้อ การแพร่เชื้อจากคนสู่คนเกิดได้ผ่านการสัมผัสกับเลือดหรือสารน้ำร่างกายจากผู้ติดเชื้อโดยตรง (รวมการฉีดดองศพผู้ตายที่ติดเชื้อ) หรือโดยการสัมผัสกับเวชภัณฑ์ที่ปนเปื้อน โดยเฉพาะอย่างยิ่งเข็มและกระบอกฉีดยา[13] การแพร่เชื้อผ่านการสัมผัสทางปากและผ่านการสัมผัสทางเยื่อบุตาน่าจะเป็นไปได้[14] และยืนยันแล้วในไพรเมตที่ไม่ใช่มนุษย์[15] แนวโน้มการติดเชื้อโรคไวรัสอีโบลาเป็นวงกว้างนั้นถือว่าต่ำ เพราะโรคนี้แพร่เฉพาะโดยการสัมผัสโดยตรงกับสารคัดหลั่งจากผู้ป่วยที่มีอาการเท่านั้น[13] การเริ่มต้นอาการที่รวดเร็วทำให้การระบุผู้ป่วยและจำกัดความสามารถของบุคคลในการแพร่โรคด้วยการเดินทางง่ายขึ้น เนื่องจากศพผู้เสียชีวิตยังติดเชื้อได้ แพทย์บางคนจึงต้องใช้มาตรการเพื่อกำจัดศพในทางที่ปลอดภัยแม้ขัดต่อพิธีกรรมฝังศพของท้องถิ่น[16]
เจ้าหน้าที่การแพทย์ที่ไม่สวมเสื้อผ้าป้องกันที่เหมาะสมอาจสัมผัสเชื้อได้[17] ในอดีต การแพร่เชื้อที่ได้มาจากโรงพยาบาลเกิดในโรงพยาบาลในทวีปแอฟริกาเนื่องจากการใช้เข็มซ้ำและขาดการป้องกันสากล[18]
โรคไวรัสอีโบลาไม่แพร่เชื้อผ่านอากาศตามธรรมชาติ[19] ทว่าไวรัสยังแพร่เชื้อได้เพราะละอองที่สร้างจากห้องปฏิบัติการขนาด 0.8–1.2 ไมโครเมตรที่หายใจเข้าไปได้[20] เนื่องจากช่องทางติดเชื้อที่เป็นไปได้นี้ ไวรัสเหล่านี้จึงถูกจัดเป็นอาวุธชีวภาพหมวดเอ[21] ล่าสุด ไวรัสได้แสดงว่าแพร่จากหมูสู่ไพรเมตที่ไม่ใช่มนุษย์ได้โดยไม่ต้องสัมผัส[22]
ค้างคาวถ่ายเอาผลไม้และเนื้อที่กินแล้วบางส่วนออกมา แล้วสัตว์บกเลี้ยงลูกด้วยนมอย่างกอริลลาและไดเคอร์ (duiker) กินผลไม้ที่ตกลงมาเหล่านั้น ลูกโซ่เหตุการณ์นี้ทำให้เกิดวิธีการแพร่เชื้อโดยอ้อมที่เป็นไปได้ผ่านตัวถูกเบียนธรรมชาติสู่ประชากรสัตว์ ซึ่งนำไปสู่การวิจัยสู่การกำจัดไวรัสในน้ำลายของค้างคาว การผลิตผลไม้ พฤติกรรมของสัตว์ และปัจจัยอื่นที่ต่างกันไปในแต่ละเวลาและสถานที่อาจกระตุ้นให้เกิดการระบาดในหมู่ประชากรสัตว์[23]
ตัวเก็บเชื้อ[แก้]
ค้างคาวถือว่าเป็นตัวเก็บเชื้อตามธรรมชาติ (natural reservoir) ที่น่าจะเป็นไปได้มากที่สุด[24] นอกจากนี้ พืช สัตว์ขาปล้องและนกก็ถูกพิจารณาด้วย ทราบว่าค้างคาวอาศัยอยู่นอกโรงงานฝ่ายซึ่งผู้ป่วยรายแรก ๆ ของการระบาดครั้งปี 2519 และ 2522 ทำงานอยู่ และยังอาจเกี่ยวข้องกับการติดเชื้อไวรัสมาร์เบิร์กในปี 2518 และ 2523[25] จากพืช 24 ชนิด และสัตว์มีกระดูกสันหลัง 19 ชนิดที่ปลูกเชื้อด้วยไวรัสอีโบลา มีเพียงค้างคาวเท่านั้นที่ติดเชื้อ[26] การขาดอาการแสดงทางคลินิกในค้างคาวเหล่านั้นเป็นคุณสมบัติของสปีชีส์เก็บเชื้อ ในการสำรวจสัตว์ 1,030 ชนิด ซึ่งรวมค้างคาว 679 ชนิดจากประเทศกาบองและสาธารณรัฐคองโกในปี 2545–2546 พบว่า ค้างคาวผลไม้ 13 ชนิดมีชิ้นส่วนอาร์เอ็นเอของไวรัสอีโบลา[27] จนถึงปี 2548 มีการระบุว่า ค้างคาวผลไม้สามชนิด (Hypsignathus monstrosus, Epomops franqueti, และ Myonycteris torquata) ติดไวรัสอีโบลา ปัจจุบัน สงสัยว่าค้างคาวเหล่านั้นเป็นตัวแทนของตัวถูกเบียนเก็บเชื้อไวรัสอีโบลา[28][29]
ระหว่างปี 2519 ถึง 2542 ในบรรดาสัตว์เลี้ยงลูกด้วยนม นก สัตว์เลื้อยคลาน สัตว์สะเทินน้ำสะเทินบกและสัตว์ขาปล้อง 30,000 ชนิดที่สุ่มตัวอย่างจากพื้นที่ระบาด ไม่พบไวรัสอีโบลานอกเหนือจากร่องรอยทางพันธุกรรมที่พบบ้างในสัตว์ฟันแทะหกชนิด (Mus setulosus และ Praomys) และหนูผีหนึ่งชนิด (Sylvisorex ollula) ที่เก็บจากสาธารณรัฐแอฟริกากลาง[25][30] พบร่องรอยไวรัสอีโบลาในซากกอริลลาและชิมแพนซีระหว่างการระบาดในปี 2544 และ 2546 ซึ่งต่อมากลายเป็นแหล่งการติดเชื้อในมนุษย์ ทว่า อัตราตายสูงจากการติดเชื้อในสปีชีส์เหล่านี้ทำให้พวกมันไม่น่าเป็นตัวเก็บเชื้อตามธรรมชาติ[25]
การแพร่เชื้อระหว่างตัวเก็บเชื้อตามธรรมชาติและมนุษย์พบน้อย และการระบาดปกติติดตามได้ถึงผู้ป่วยเดี่ยวซึ่งจัดการกับซากกอริลลา ชิมแพนซีหรือไดเคอร์[31] ประชากรในบางส่วนของแอฟริกาตะวันตกยังกินค้างคาวผลไม้ ซึ่งมีการรมควัน ย่างหรือทำเป็นซุปเผ็ด[29][32]
วิทยาไวรัส[แก้]

จีโนม[แก้]
เช่นเดียวกับ mononegavirus ทุกชนิด วิริออน (virion) อีโบลามีจีโนมอาร์เอ็นเอไม่แพร่เชื้อ (non-infectious) เส้นตรงสายเดี่ยว ไม่เป็นปล้อง (nonsegmented) สภาพขั้วลบซึ่งมี inverse-complementary 3' และ 5' termini ไม่มี 5' cap ไม่พอลิอะดีนีเลชัน (not polyadenylated) และไม่เชื่อมกับโปรตีนด้วยพันธะโควาเลนต์[33] จีโนม ebolavirus ยาวประมาณ 19,000 คู่เบส และมีเจ็ดยีนตามลำดับดังนี้ 3'-UTR-NP-VP35-VP40-GP-VP30-VP24-L-5'-UTR[34] จีโนมของ ebolavirus ห้าชนิด (BDBV, EBOV, RESTV, SUDV, และ TAFV) ต่างกันที่ลำดับ จำนวนและตำแหน่งยีนทับซ้อนกัน
ขนาดและรูปร่าง[แก้]
เช่นเดียวกับฟิโลไวรัสทุกชนิด วิริออนอีโบลาเป็นอนุภาคคล้ายเส้นด้ายที่อาจปรากฏในรูปตะขอคนเลี้ยงแกะหรือรูปตัว "U" หรือเลข "6" และยังอาจขดม้วน เป็นวงแหวนหรือแตกกิ่งก้านได้ โดยทั่วไป วิริออนอีโบลามีความกว้าง 80 นาโนเมตร แต่ความยาวค่อนข้างแปรผัน โดยทั่วไป ความยาวมัธยฐานของอนุภาค ebolavirus มีพิสัยระหว่าง 974 ถึง 1,086 นาโนเมตร (ซึ่งขัดกับวิริออนมาร์เบิร์ก ซึ่งความยาวมัธยฐานของอนุภาควัดได้ 795–828 นาโนเมตร) ทว่าเคยพบอนุภาคยาวถึง 14,000 นาโนเมตรในการเพาะเลี้ยงเนื้อเยื่อ[35]
วงจรชีวิต[แก้]
วงจรชีวิตของ ebolavirus เริ่มด้วยการยึดกับตัวรับผิวเซลล์ที่จำเพาะของวิริออน ตามด้วยการเชื่อมเปลือกหุ้มวิริออน (virion envelope) กับเยื่อหุ้มเซลล์และการปล่อยนิวคลิโอแคปซิด (nucleocapsid) ของไวรัสสู่น้ำในเซลล์ (cytosol) ดำเนินร่วม เอ็นไซม์อาร์เอ็นเอพอลิเมอเรส (RNA polymerase) ของไวรัส ซึ่งเข้ารหัสโดยยีนแอล (L gene) เปิดนิวคลิโอแคปซิดบางส่วนแล้วถอดรหัสยีนเป็นเอ็มอาร์เอ็นเอสายบวก ซึ่งถูกแปลรหัสต่อไปเป็นโปรตีนโครงสร้างและโปรตีนไม่ใช่โครงสร้าง อาร์เอ็นเอพอลิเมอเรส (แอล) ของ ebolavirus ยึดกับโปรโมเตอร์ (promoter) เดี่ยวซึ่งอยู่ที่ปลาย 3' ของจีโนม การถอดรหัสจะยุติหลังจากยีนหนึ่งหรือดำเนินต่อไปยังยีนต่อไปตามลำดับอย่างใดอย่างหนึ่ง หมายความว่า ยีนที่อยู่ใกล้ปลาย 3' ของจีโนมจะถูกถอดรหัสออกมาปริมาณมากที่สุด ขณะที่ยีนที่อยู่ใกล้ปลาย 5' จะถูกถอดรหัสน้อยที่สุด ฉะนั้น ลำดับยีนจึงเป็นการกำกับการถอดรหัสที่เรียบง่ายแต่ทรงประสิทธิภาพ โปรตีนที่ผลิตมากที่สุด คือ นิวคลิโอโปรตีน (nucleoprotein) ซึ่งความเข้มข้นของนิวคลิโอโปรตีนในเซลล์ตัดสินว่าเมื่อใดยีนแอลเปลี่ยนจากการถอดรหัสยีนเป็นการถ่ายแบบจีโนม การถ่ายแบบทำให้มีแอนติจีโนม (antigenome) สายบวกเต็มความยาวซึ่งจะถูกถอดรหัสเป็นสำเนาจีโนมลูกหลานไวรัสสายลบต่อไป โปรตีนโครงสร้างที่สังเคราะห์ใหม่และการประกอบตัวเองของจีโนมและสะสมอยู่ใกล้ด้านในของเยื่อหุ้มเซลล์ วิริออนแตกหน่อ (bud) ออกจากเซลล์ โดยได้เปลือกหุ้มมาจากเยื่อหุ้มเซลล์ที่แตกหน่อออกมา แล้วอนุภาคลูกลานเต็มวัยจะติดเชื้อเซลล์อื่นเพื่อเริ่มวงจรซ้ำ[33]
พยาธิสรีรวิทยา[แก้]
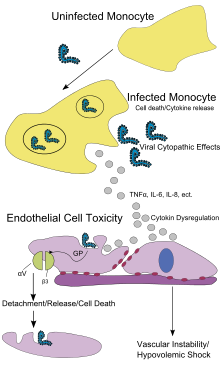
เซลล์เนื้อเยื่อบุโพรง, เซลล์กลืนกิน (phagocyte) ซึ่งมีนิวเคลียสเดียว, และเซลล์ตับเป็นเป้าหมายหลักของการติดเชื้อ หลังติดเชื้อ จะมีการสร้างไกลโคโปรตีนที่หลั่งออกมา (secreted glycoprotein, sGP) ชื่อ อีโบลาไวรัสไกลโคโปรตีน (Ebola virus glycoprotein, GP) การถ่ายแบบของอีโบลารบกวนการสังเคราะห์โปรตีนของเซลล์ที่ติดเชื้อและการป้องกันทางภูมิคุ้มกันของตัวถูกเบียน GP ก่อเป็นกลุ่มรวมไตรเมอร์ (trimeric complex) ซึ่งยึดไวรัสกับเซลล์เนื้อเยื่อบุโพรงตามผิวด้านล่างของหลอดเลือด sGP ก่อโปรตีนไดเมอร์ (dimer) ซึ่งแทรกแซงการส่งสัญญาณของนิวโตรฟิล (neutrophil) ซึ่งเป็นเม็ดเลือดขาวประเภทหนึ่ง ซึ่งทำให้ไวรัสหลบหลีกระบบภูมิคุ้มกันโดยการยับยั้งการปลุกฤทธิ์นิวโตรฟิลขั้นแรก ๆ เม็ดเลือดขาวเหล่านี้ยังเป็นพาหะที่ขนส่งไวรัสทั่วทั้งร่างกายไปยังสถานที่อย่างปุ่มน้ำเหลือง ตับ ปอดและม้าม[36]
การมีอนุภาคไวรัสและความเสียหายของเซลล์ที่เกิดจากการแตกหน่อทำให้เกิดการปล่อยไซโทไคน์ (กล่าวโดยเจาะจง คือ TNF-α, IL-6, IL-8 ฯลฯ) ซึ่งส่งสัญญาณโมเลกุลของไข้และการอักเสบ ฤทธิ์ไซโทไคน์จากการติดเชื้อในเซลล์เนื้อเยื่อบุโพรง ทำให้ความแข็งแรงของหลอดเลือด (vascular integrity) เสียไป การเสียความแข็งแรงของหลอดเลือดนี้ยังส่งเสริมด้วยการสังเคราะห์ GP ซึ่งลดอินทีกริน (integrin) จำเพาะซึ่งมีหน้าที่ในการยึดติดของเซลล์กับโครงสร้างในเซลล์ และความเสียหายต่อตับ ซึ่งนำไปสู่ลิ่มเลือดผิดปกติ[37]
การวินิจฉัย[แก้]
ประวัติผู้ป่วย โดยเฉพาะอย่างยิ่งประวัติการท่องเที่ยวและทำงานร่วมกับการสัมผัสสัตว์ป่าสำคัญต่อการสงสัยวินิจฉัยโรคไวรัสอีโบลา ยืนยันการวินิจฉัยโดยการแยกไวรัส ตรวจหาอาร์เอ็นเอหรือโปรตีนไวรัส หรือตรวจหาสารภูมิต้านทานต่อไวรัสในเลือดของบุคคล การแยกไวรัสโดยการเพาะเลี้ยงเซลล์ การตรวจหาอาร์เอ็นเอไวรัสโดยปฏิกิริยาลูกโซ่พอลิเมอเรส (PCR) และการตรวจหาโปรตีนโดยวิธีอีไลซา (ELISA) มีประสิทธิภาพเร็วและในผู้ที่เสียชีวิตจากโรค การตรวจหาสารภูมิต้านทานต่อไวรัสมีประสิทธิภาพช้าในโรคและในผู้ที่ฟื้นตัว[38]
ระหว่างการระบาด การแยกไวรัสมักเป็นไปไม่ได้ วิธีการวินิจฉัยที่ใช้มากที่สุดจึงเป็นเรียลไทม์ PCR และการตรวจโปรตีนด้วย ELISA ซึ่งสามารถทำได้ในโรงพยาบาลสนามหรือโรงพยาบาลเคลื่อนที่[39] พบและระบุวิริออนฟิโลไวรัสได้ในการเพาะเลี้ยงเซลล์โดยกล้องจุลทรรศน์อิเล็กตรอนเนื่องจากรูปทรงเส้นด้ายอันเป็นเอกลักษณ์ของพวกมัน แต่กล้องจุลทรรศน์อิเล็กตรอนไม่อาจบอกความแตกต่างระหว่างฟิโลไวรัสชนิดต่าง ๆ ได้แม้ความยาวแตกต่างกันบ้าง[35]
การจำแนก[แก้]

สกุล Ebolavirus และ Marburgvirus เดิมจัดเป็นสปีชีส์หนึ่งของสกุล Filovirus ซึ่งเลิกใช้แล้ว ในเดือนมีนาคม 2541 คณะอนุกรรมการไวรัสสัตว์มีกระดูกสันหลัง (Vertebrate Virus Subcommittee) เสนอในคณะกรรมการระหว่างประเทศว่าด้วยอนุกรมวิธานไวรัส (International Committee on Taxonomy of Viruses, ICTV) ให้เปลี่ยนสกุล Filovirus เป็นวงศ์ Filoviridae ซึ่งมีสองสกุล ได้แก่ Ebola-like viruses (ไวรัสคล้ายอีโบลา) และ Marburg-like viruses (ไวรัสคล้ายมาร์เบิร์ก) มีการรับข้อเสนอนี้ในกรุงวอชิงตัน ดี.ซี. ในเดือนเมษายน 2544 และในกรุงปารีสในเดือนกรกฎาคม 2545 ในปี 2543 มีการเสนออีกข้อหนึ่งในกรุงวอชิงตัน ดี.ซี. ให้เปลี่ยน "ไวรัสคล้าย" (-like viruses) เป็น "ไวรัส" (-virus) จึงกลายเป็น Ebolavirus และ Marburgvirus ดังในปัจจุบัน[40]
มีอัตราการเปลี่ยนแปลงพันธุกรรมช้ากว่าไวรัสไข้หวัดใหญ่เอในมนุษย์ 100 เท่า แต่มีขนาดเท่ากับตับอักเสบบี การประมาณค่านอกช่วงย้อนหลังไปโดยใช้อัตราเหล่านี้ชี้ว่า Ebolavirus และ Marburgvirus แยกออกจากกันเมื่อหลายพันปีก่อน[41] ทว่า ซากดึกดำบรรพ์จีโนมของ filovirus ที่พบในสัตว์เลี้ยงลูกด้วยนมชี้ว่า วงศ์ Filoviridae มีอายุอย่างน้อยหลายสิบล้านปี[42] พบไวรัสที่กลายเป็นซากดึกดำบรรพ์ซึ่งสัมพันธ์ใกล้ชิดกับ ebolavirus ในจีโนมของแฮมสเตอร์จีน[43]
การวินิจฉัยแยกโรค[แก้]
อาการของโรคไวรัสอีโบลาคล้ายกับอาการของโรคไวรัสมาร์เบิร์ก[44] สับสนได้ง่ายกับโรคอื่นจำนวนมากที่พบบ่อยในแอฟริกาแถบเส้นศูนย์สูตร เช่น ไข้เลือดออกจากไวรัสอื่น มาลาเรียชนิดฟัลซิปารัม ไข้ไทฟอยด์ โรคติดเชื้อชิเกลลา โรคจากริกเก็ตเซีย เช่น ไข้รากสาดใหญ่ อหิวาตกโรค ภาวะเลือดเป็นพิษเหตุติดเชื้อแกรมลบ โรคไลม์ เช่น โรคไข้กลับ หรือลำไส้อักเสบ EHEC โรคติดเชื้ออื่นที่ควรรวมอยู่ในการวินิจฉัยแยกโรคด้วย รวมถึง โรคฉี่หนู ไข้รากสาดใหญ่จากป่าละเมาะ กาฬโรค ไข้คิว โรคติดเชื้อราแคนดิดา โรคติดเชื้อราฮีสโตพลาสมา โรคติดเชื้อทริปาโนโซมา โรคติดเชื้อลิชมาเนียอวัยวะ โรคฝีดาษเลือดออก โรคหัด และโรคตับอักเสบจากไวรัสเร็วร้าย โรคไม่ติดเชื้อที่อาจสับสนกับโรคไวรัสอีโบลา ได้แก่ มะเร็งเม็ดเลือดขาวเฉียบพลันชนิดโปรไมอิโลไซติก กลุ่มอาการเม็ดเลือดแดงแตก-ยูรีเมีย การได้พิษงู การพร่องปัจจัยเลือดจับลิ่มและ/หรือความผิดปกติของเกล็ดเลือด มีลิ่มเลือดในหลอดเลือดขนาดเล็ก หลอดเลือดฝอยพองและมีเลือดออกที่เป็นกรรมพันธุ์ โรคคาวาซากิ และกระทั่งภาวะพิษวาร์ฟาริน[45][46][47][48]
การป้องกัน[แก้]
การเปลี่ยนพฤติกรรม[แก้]
ไวรัสอีโบลาติดต่อ โดยส่วนใหญ่การป้องกันเกี่ยวกับการเปลี่ยนพฤติกรรม อุปกรณ์ป้องกันบุคคลทั่วกายที่เหมาะสมและการฆ่าเชื้อ เทคนิคเพื่อเลี่ยงการติดเชื้อเกี่ยวกับการไม่สัมผัสกับเลือดหรือสารคัดหลั่งที่ติดเชื้อ รวมทั้งเลือดและสารคัดหลั่งจากศพ[12] ซึ่งจำต้องสงสัยและวินิจฉัยโรคโดยเร็วและใช้ความระมัดระวังมาตรฐานสำหรับผู้ป่วยทุกคนในสถานสาธารณสุข[49] มาตรการที่แนะนำเมื่อดูแลผู้ติดเชื้อรวมการแยกผู้ป่วย การทำไร้เชื้อซึ่งอุปกรณ์ และการสวมเสื้อผ้าป้องกัน ได้แก่ หน้ากาก ถุงมือ กาวน์และแว่นตา[12] การล้างมือสำคัญแต่อาจลำบากในพื้นที่ซึ่งไม่มีแม้น้ำสำหรับดื่ม[6]
สามารถกำจัดไวรัสอีโบลาได้ด้วยความร้อน (ให้ความร้อน 60 °C เป็นเวลา 30 ถึง 60 นาที หรือต้มเป็นเวลา 5 นาที) ผลิตภัณฑ์ที่มีแอลกอฮอล์ โซเดียมไฮโปคลอไรต์ (สารฟอกจาง) หรือแคลเซียมไฮโปคลอไรต์ (ผงฟอกจาง) ที่ความเข้มข้นที่เหมาะสม[50][51]
โรคระบาดขนาดใหญ่ส่วนมากเกิดในพื้นที่ยากจนทุรกันดารซึ่งไม่มีโรงพยาบาลสมัยใหม่หรือเจ้าหน้าที่แพทย์ที่มีการศึกษาดี เนื่องจากขาดอุปกรณ์และการปฏิบัติสุขลักษณะที่เหมาะสม พิธีกรรมฝังตามประเพณี โดยเฉพาะอย่างยิ่งประเพณีที่ต้องฉีดดองศพ ควรถูกห้ามปรามหรือเปลี่ยนแปลง[49] ลูกเรือสายการบินที่บินไปยังบริเวณระบาด ได้รับการสอนให้ระบุอีโบลาและแยกผู้ที่มีอาการ[52]
การกักโรค[แก้]
การกักโรค หรือการแยกโดยบังคับ ปกติมีผลลดการแพร่โรคได้[53][54] รัฐบาลมักกักโรคซึ่งพื้นที่ที่เกิดโรคหรือปัจเจกบุคคลที่อาจติดเชื้อ[55] ในสหรัฐอเมริกา กฎหมายอนุญาตให้กักโรคผู้ติดเชื้ออีโบลา[56] การขาดถนนและการขนส่งอาจช่วยชะลอโรคในทวีปแอฟริกา ระหว่างการระบาดในปี 2557 ประเทศไลบีเรียปิดโรงเรียน[57]
วัคซีน[แก้]
ปัจจุบันยังไม่มีวัคซีนสำหรับมนุษย์[1][58][59] วัคซีนขั้นทดลองที่มีหวังที่สุด คือ วัคซีนดีเอ็นเอ[60] หรือวัคซีนที่มาจาก แอดิโนไวรัส (adenovirus)[61], ไวรัสปากอักเสบตุ่มพองอินเดียนา (vesicular stomatitis Indiana virus, VSIV)[62][63][64] หรืออนุภาคคล้าย filovirus[65] เนื่องจากวัคซีนขั้นทดลองเหล่านี้สามารถป้องกันไพรเมตที่มิใช่มนุษย์จากโรคที่ ebolavirus ชักนำได้ วัคซีนดีเอ็นเอ วัคซีนยึดแอดิโนไวรัส และวัคซีนยึด VSIV เข้าสู่การทดลองทางคลินิกแล้ว[66][67][68][69]
วัคซีนช่วยปกป้องไพรเมตที่มิใช่มนุษย์ การก่อภูมิคุ้มกันใช้เวลาหกเดือน ซึ่งขัดขวางการใช้วัคซีนเพื่อรับมือการระบาด ในปี 2546 ในการแสวงการเริ่มต้นประสิทธิภาพที่เร็วขึ้น มีการทดสอบวัคซีนตัวหนึ่งโดยใช้ตัวนำโรคแอดิโนไวรัสที่มีโปรตีนเดือยอีโบลา (Ebola spike protein) กับลิงแสม ยี่สิบแปดวันให้หลัง พวกมันถูกทดสอบด้วยไวรัสและยังคงต้านทานอยู่[61] วัคซีนที่อาศัยไวรัสปากอักเสบตุ่มพองผสมอ่อนฤทธิ์ (attenuated recombinant) ที่มีไกลโคโปรตีนของอีโบลาหรือมาร์เบิร์กในปี 2548 ป้องกันไพรเมตที่มิใช่มนุษย์[70] และเปิดการทดลองทางคลินิกในมนุษย์[66] การศึกษาในเดือนตุลาคมเสร็จสิ้นการทดลองในมนุษย์ครั้งแรก การให้วัคซีนสามรอบในสามเดือนชักนำให้เกิดการตอบสนองทางภูมิคุ้มกันอย่างปลอดภัย มีการติดตามผู้รับการทดลองเป็นเวลาหนึ่งปี และในปี 2549 การศึษาโดยทดสอบวัคซีนเข็มเดียวออกฤทธิ์เร็วเริ่มต้น การศึกษาใหม่นี้แล้วเสร็จในปี 2551[67] การทดสอบวัคซีนกับสายพันธุ์อีโบลาที่คล้ายกับสายพันธุ์ที่ติดเชื้อในมนุษย์เป็นก้าวถัดไป[71] ในวันที่ 6 ธันวาคม 2554 มีรายงานการพัฒนาวัคซีนอีโบลาสำหรับหนูสำเร็จ วัคซีนชนิดนี้สามารถทำให้แห้งแบบเยือกแข็ง (freeze-dry) ได้ ไม่เหมือนกับวัคซีนชนิดก่อน ๆ ฉะนั้นจึงเก็บได้นานคอยการระบาด[72] มีการใช้วัคซีนทดลองที่นักวิจัยที่ห้องปฏิบัติการแห่งชาติของแคนาดาผลิตในวินนีเพ็กในปี 2552 เพื่อชิงรักษานักวิทยาศาสตร์ชาวเยอรมันผู้หนึ่งที่อาจติดเชื้อระหว่างอุบัติเหตุห้องปฏิบัติการ[73] ทว่า การติดเชื้อไวรัสอีโบลาแท้จริงอาจไม่สามารถแสดงได้โดยปราศจากข้อสงสัย[74] ในการทดลอง สามารถใช้ไวรัสปากอักเสบตุ่มพองอินเดียนาผสมที่แสดงออกซึ่งไกลโคโปรตีนของไวรัสอีโบลาหรือไวรัสซูดานสำเร็จในแบบจำลองไพรเมตที่มิใช่มนุษย์เป็นมาตรการป้องกันโรคหลังสัมผัสเชื้อ[75][76] ปัจจุบัน การแนะนำของศูนย์ควบคุมโรคกำลังอยู่ระหว่างการทบทวน
ห้องปฏิบัติการ[แก้]
ไวรัสอีโบลาเป็นจุลชีพก่อโรคกลุ่มเสี่ยง 4 ขององค์การอนามัยโลก ซึ่งต้องการการกักกันเทียบเท่าความปลอดภัยทางชีวภาพระดับ 4 (biosafety level 4-equivalent containment) นักวิจัยห้องปฏิบัติการต้องได้รับการฝึกอย่างเหมาะสมในการปฏิบัติความปลอดภัยทางชีวภาพระดับ 4 และสวมอุปกรณ์ป้องกันบุคคลอย่างเหมาะสม
การรักษา[แก้]

ไม่มีการรักษาที่จำเพาะต่อ ebolavirus[59] สภาพการรักษาประคับประคองเป็นหลัก และรวมลดการดำเนินการที่รุกล้ำให้น้อยที่สุด รักษาสมดุลของเหลวและอิเล็กโทรไลต์เพื่อป้องกันภาวะขาดน้ำ การให้สารกันเลือดเป็นลิ่มในการติดเชื้อโดยเร็วเพื่อป้องกันหรือควบคุมภาวะเลือดแข็งตัวในหลอดเลือดแบบแพร่กระจาย การให้สารเร่งเลือดจับลิ่ม (procoagulant) ในการติดเชื้อระยะหลังเพื่อควบคุมเลือดไหล การรักษาระดับออกซิเจน การจัดการความปวด และการใช้ยารักษาโรคเพื่อรักษาการติดเชื้อแบคทีเรียหรือเชื้อราทุติยภูมิ[77][78][79] การรักษาแต่เนิ่นอาจเพิ่มโอกาสรอดชีวิต[80] กำลังมีการศึกษาการรักษาเชิงทดลองจำนวนหนึ่ง[81]
การพยากรณ์โรค[แก้]
โรคนี้มีอัตราตายสูง มักระหว่าง 50% ถึง 90%[1][2] เมื่อเดือนเมษายน 2557 สารสนเทศจากองค์การอนามัยโลกตลอดการอุบัติทั้งสิ้นจนปัจจุบันให้อัตราตายรวมที่ 60%-65%[1] มีข้อบ่งชี้โดยอาศัยอัตราตายระหว่างประเทศที่การรักษาอาการโดยเร็วและมีประสิทธิภาพ (คือ การอภิบาลประคับประคองเพื่อป้องกันภาวะขาดน้ำ) อาจลดอัตราตายอย่างมีนัยสำคัญ[82] หากผู้ติดเชื้อรอดชีวิต การฟื้นตัวอาจเร็วและสมบูรณ์ได้ ผู้ป่วยระยะยาวมักมีการเกิดปัญหาระยะยาวแทรกซ้อน เช่น อัณฑะอักเสบ ปวดข้อ ปวดกล้ามเนื้อ ผิวหนังลอกหรือผมร่วง ยังมีการอธิบายอาการของตา เช่น ไวต่อแสง น้ำตาไหลมาก ม่านตาอักเสบ ม่านตาและซิลิอารีบอดีอักเสบ คอรอยด์อักเสบและตาบอดด้วย ไวรัสอีโบลาและไวรัสซูดานยังอาจคงอยู่ในน้ำอสุจิของผู้รอดชีวิตบางคนได้นานเจ็ดสัปดาห์ ซึ่งอาจนำไปสู่การติดเชื้อและโรคผ่านการร่วมเพศ[1]
อ้างอิง[แก้]
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 1.8 "Ebola virus disease Fact sheet N°103". World Health Organization. March 2014. สืบค้นเมื่อ 12 April 2014.
- ↑ 2.0 2.1 C.M. Fauquet (2005). Virus taxonomy classification and nomenclature of viruses; 8th report of the International Committee on Taxonomy of Viruses. Oxford: Elsevier/Academic Press. p. 648. ISBN 9780080575483.
- ↑ "Ebola Viral Disease Outbreak — West Africa, 2014". CDC. June 27, 2014. สืบค้นเมื่อ 26 June 2014.
- ↑ 4.0 4.1 "CDC urges all US residents to avoid nonessential travel to Liberia, Guinea, and Sierra Leone because of an unprecedented outbreak of Ebola". CDC. July 31, 2014. สืบค้นเมื่อ 2 August 2014.
- ↑ Ebola Hemorrhagic Fever from Centers for Disease Control and Prevention.P age last updated: January 28, 2014.
- ↑ 6.0 6.1 6.2 6.3 Gatherer D (2014). "The 2014 Ebola virus disease outbreak in West Africa". J. Gen. Virol. 95 (Pt 8): 1619–1624. doi:10.1099/vir.0.067199-0. PMID 24795448.
- ↑ 7.0 7.1 7.2 7.3 "Ebola Hemorrhagic Fever Signs and Symptoms". CDC. January 28, 2014. สืบค้นเมื่อ 2 August 2014.
- ↑ 8.0 8.1 8.2 Hoenen T, Groseth A, Falzarano D, Feldmann H (May 2006). "Ebola virus: unravelling pathogenesis to combat a deadly disease". Trends in Molecular Medicine. 12 (5): 206–215. doi:10.1016/j.molmed.2006.03.006. PMID 16616875.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Ebola Virus, Clinical Presentation". Medscape. สืบค้นเมื่อ 2012-07-30.
- ↑ Fisher-Hoch SP, Platt GS, Neild GH, Southee T, Baskerville A, Raymond RT, Lloyd G, Simpson DI (1985). "Pathophysiology of shock and hemorrhage in a fulminating viral infection (Ebola)". J. Infect. Dis. 152 (5): 887–894. doi:10.1093/infdis/152.5.887. PMID 4045253.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Ebola Hemorrhagic Fever Risk of Exposure". CDC. August 1, 2014. สืบค้นเมื่อ 2 August 2014.
- ↑ 12.0 12.1 12.2 "Ebola Hemorrhagic Fever Prevention". CDC. July 31, 2014. สืบค้นเมื่อ 2 August 2014.
- ↑ 13.0 13.1 "CDC Telebriefing on Ebola outbreak in West Africa". CDC. July 28, 2014. สืบค้นเมื่อ 3 August 2014.
- ↑ Jaax N, Jahrling P, Geisbert T, Geisbert J, Steele K, McKee K, Nagley D, Johnson E, Jaax G, Peters C (Dec 1995). "Transmission of Ebola virus (Zaire strain) to uninfected control monkeys in a biocontainment laboratory". Lancet. 346 (8991–8992): 1669–1671. doi:10.1016/S0140-6736(95)92841-3. ISSN 0140-6736. PMID 8551825.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jaax NK, Davis KJ, Geisbert TJ, Vogel P, Jaax GP, Topper M, Jahrling PB (Feb 1996). "Timed appearance of lymphocytic choriomeningitis virus after gastric inoculation of mice". Archives of pathology & laboratory medicine. 120 (2): 140–155. ISSN 0003-9985. PMID 8712894.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Harden, Blaine (2001-02-18). "Dr. Matthew's Passion". New York Times Magazine. สืบค้นเมื่อ 2008-02-25.
- ↑ Mayo Clinic Staff, Ebola virus and Marburg virus: Causes, Mayo Clinic
- ↑ Lashley, Felissa R.; Durham, Jerry D. (2007). Emerging infectious diseases trends and issues (2nd ed.). New York: Springer Pub. Co. p. 141. ISBN 9780826103505.
- ↑ "2014 Ebola Virus Disease (EVD) outbreak in West Africa". WHO. 21 April 2014. สืบค้นเมื่อ 3 August 2014.
- ↑ Johnson E, Jaax N, White J, Jahrling P (Aug 1995). "Lethal experimental infections of rhesus monkeys by aerosolized Ebola virus". International journal of experimental pathology. 76 (4): 227–236. ISSN 0959-9673. PMC 1997182. PMID 7547435.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Leffel EK, Reed DS (2004). "Marburg and Ebola viruses as aerosol threats". Biosecurity and bioterrorism : biodefense strategy, practice, and science. 2 (3): 186–191. doi:10.1089/bsp.2004.2.186. ISSN 1538-7135. PMID 15588056.
- ↑ Weingartl HM, Embury-Hyatt C, Nfon C, Leung A, Smith G, Kobinger G (2012). "Transmission of Ebola virus from pigs to non-human primates". Sci Rep. 2: 811. doi:10.1038/srep00811. PMC 3498927. PMID 23155478.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Gonzalez JP, Pourrut X, Leroy E (2007). "Ebolavirus and other filoviruses". Current topics in microbiology and immunology. Current Topics in Microbiology and Immunology. 315: 363–387. doi:10.1007/978-3-540-70962-6_15. ISBN 978-3-540-70961-9. PMID 17848072.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Fruit bats may carry Ebola virus". BBC News. 2005-12-11. สืบค้นเมื่อ 2008-02-25.
- ↑ 25.0 25.1 25.2 Pourrut X, Kumulungui B, Wittmann T, Moussavou G, Délicat A, Yaba P, Nkoghe D, Gonzalez JP, Leroy EM (2005). "The natural history of Ebola virus in Africa". Microbes and infection / Institut Pasteur. 7 (7–8): 1005–1014. doi:10.1016/j.micinf.2005.04.006. PMID 16002313.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Swanepoel R, Leman PA, Burt FJ, Zachariades NA, Braack LE, Ksiazek TG, Rollin PE, Zaki SR, Peters CJ (Oct 1996). "Experimental inoculation of plants and animals with Ebola virus". Emerging Infectious Diseases. 2 (4): 321–325. doi:10.3201/eid0204.960407. ISSN 1080-6040. PMC 2639914. PMID 8969248.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Leroy EM, Kumulungui B, Pourrut X, Rouquet P, Hassanin A, Yaba P, Délicat A, Paweska JT, Gonzalez JP, Swanepoel R (2005). "Fruit bats as reservoirs of Ebola virus". Nature. 438 (7068): 575–576. Bibcode:2005Natur.438..575L. doi:10.1038/438575a. PMID 16319873.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Pourrut X, Délicat A, Rollin PE, Ksiazek TG, Gonzalez JP, Leroy EM (2007). "Spatial and temporal patterns of Zaire ebolavirus antibody prevalence in the possible reservoir bat species". The Journal of infectious diseases. Suppl 2 (s2): S176–S183. doi:10.1086/520541. PMID 17940947.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 29.0 29.1 Starkey, Jerome (5 April 2014) 90 killed as fruit bats spread Ebola virus across West Africa The Times (subscription may be needed), Retrieved 5 April 2014
- ↑ Morvan JM, Deubel V, Gounon P, Nakouné E, Barrière P, Murri S, Perpète O, Selekon B, Coudrier D, Gautier-Hion A, Colyn M, Volehkov V (1999). "Identification of Ebola virus sequences present as RNA or DNA in organs of terrestrial small mammals of the Central African Republic". Microbes and Infection. 1 (14): 1193–1201. doi:10.1016/S1286-4579(99)00242-7. PMID 10580275.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Peterson AT, Bauer JT, Mills JN (2004). "Ecologic and Geographic Distribution of Filovirus Disease". Emerging Infectious Diseases. 10 (1): 40–47. doi:10.3201/eid1001.030125. PMC 3322747. PMID 15078595.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ http://www.bbc.co.uk/news/world-africa-26735118
- ↑ 33.0 33.1 Pringle, C. R. (2005). "Order Mononegavirales". ใน Fauquet, C. M.; Mayo, M. A.; Maniloff, J.; Desselberger, U.; Ball, L. A. (บ.ก.). Virus Taxonomy – Eighth Report of the International Committee on Taxonomy of Viruses. San Diego, U.S.: Elsevier/Academic Press. pp. 609–14. ISBN 978-0-12-370200-5.
- ↑ Kiley MP, Bowen ET, Eddy GA, Isaäcson M, Johnson KM, McCormick JB, Murphy FA, Pattyn SR, Peters D, Prozesky OW, Regnery RL, Simpson DI, Slenczka W, Sureau P, van der Groen G, Webb PA, Wulff H (1982). "Filoviridae: A taxonomic home for Marburg and Ebola viruses?". Intervirology. 18 (1–2): 24–32. doi:10.1159/000149300. PMID 7118520.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 35.0 35.1 Geisbert TW, Jahrling PB (1995). "Differentiation of filoviruses by electron microscopy". Virus research. 39 (2–3): 129–150. PMID 8837880.
- ↑ Smith, Tara (2005). Ebola (Deadly Diseases and Epidemics). Chelsea House Publications. ISBN 0-7910-8505-8.
- ↑ Sullivan N, Yang ZY, Nabel GJ (2003). "Ebola Virus Pathogenesis: Implications for Vaccines and Therapies" (PDF). Journal of Virology. 77 (18): 9733–9737. doi:10.1128/JVI.77.18.9733-9737.2003. PMC 224575. PMID 12941881. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (Free full text)เมื่อ 2018-07-23. สืบค้นเมื่อ 2014-08-07.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Ebola Hemorrhagic Fever Diagnosis". CDC. January 28, 2014. สืบค้นเมื่อ 3 August 2014.
- ↑ Grolla A, Lucht A, Dick D, Strong JE, Feldmann H (2005). "Laboratory diagnosis of Ebola and Marburg hemorrhagic fever". Bull Soc Pathol Exot. 98 (3): 205–9. PMID 16267962.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Büchen-Osmond, Cornelia (2006-04-25). "ICTVdB Virus Description – 01.025.0.02. Ebolavirus". International Committee on Taxonomy of Viruses. สืบค้นเมื่อ 2009-06-02.
- ↑ Suzuki Y, Gojobori T (1997). "The origin and evolution of Ebola and Marburg viruses". Molecular Biology and Evolution. 14 (8): 800–6. doi:10.1093/oxfordjournals.molbev.a025820. PMID 9254917.
- ↑ Taylor DJ, Leach RW, Bruenn J (2010). "Filoviruses are ancient and integrated into mammalian genomes". BMC Evolutionary Biology. 10: 193. doi:10.1186/1471-2148-10-193. PMC 2906475. PMID 20569424.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Taylor DJ, Dittmar K, Ballinger MJ, Bruenn JA (2011). "Evolutionary maintenance of filovirus-like genes in bat genomes". BMC Evolutionary Biology. 11: 336. doi:10.1186/1471-2148-11-336. PMC 3229293. PMID 22093762.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Longo DL, Kasper DL, Jameson JL, Fauci AS, Hauser SL, Loscalzo J, บ.ก. (2011). "Chapter 197". Harrison's Principles of Internal Medicine (18th ed.). McGraw-Hill. ISBN 978-0071748896.
- ↑ Grolla A, Lucht A, Dick D, Strong JE, Feldmann H (September 2005). "Laboratory diagnosis of Ebola and Marburg hemorrhagic fever". Bull Soc Pathol Exot. 98 (3): 205–09. PMID 16267962.
- ↑ Gear JH (May–June 1989). "Clinical aspects of African viral hemorrhagic fevers". Rev Infect Dis. 11 (Supplement 4): S777–82. doi:10.1093/clinids/11.supplement_4.s777. PMID 2665013.
- ↑ Gear JH, Ryan J, Rossouw E (February 1978). "A consideration of the diagnosis of dangerous infectious fevers in South Africa". South African Medical Journal. 53 (7): 235–37. PMID 565951.
- ↑ Bogomolov BP (1998). "Differential diagnosis of infectious diseases with hemorrhagic syndrome". Terapevticheskii Arkhiv. 70 (4): 63–68. PMID 9612907.
- ↑ 49.0 49.1 Centers for Disease Control and Prevention and World Health Organization (1998). Infection Control for Viral Haemorrhagic Fevers in the African Health Care Setting (PDF). Atlanta, Georgia, US: Centers for Disease Control and Prevention. สืบค้นเมื่อ 2013-02-08.
- ↑ "Infection Prevention and Control Guidance for Care of Patients with Suspected or Confirmed Filovirus Haemorrhagic Fever in Health-care Settings with Focus on Ebola" (PDF). Infection Prevention and Control Guidance for Care of Patients with Suspected or Confirmed Filovirus Haemorrhagic Fever in Health-care Settings with Focus on Ebola. WHO. August 2014. สืบค้นเมื่อ 21 August 2014.
- ↑ Public Health Agency of Canada, Laboratory Biosafety and Biosecurity > Biosafety Programs and Resources > Pathogen Safety Data Sheets and Risk Assessment > Ebola virus Section IV: http://www.phac-aspc.gc.ca/lab-bio/res/psds-ftss/ebola-eng.php
- ↑ Ebola Virus: Symptoms, Treatment, and Prevention
- ↑ Sompayrac L (2002). How pathogenic viruses work (3rd ed.). Boston: Jones and Bartlett Publishers. p. 87. ISBN 978-0763720827.
- ↑ Alazard-Dany N, Ottmann Terrangle M, Volchkov V (April 2006). "[Ebola and Marburg viruses: the humans strike back]" (PDF). Med Sci (Paris) (ภาษาฝรั่งเศส). 22 (4): 405–10. doi:10.1051/medsci/2006224405. PMID 16597410.
- ↑ "Outbreaks Chronology: Ebola Virus Disease". Centers for Disease Control and Prevention (CDC).gov. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 26 October 2014. สืบค้นเมื่อ 26 October 2014.
- ↑ Koenig K, Schultz C, บ.ก. (2009). Koenig and Schultz's disaster medicine : comprehensive principles and practices. Cambridge: Cambridge University Press. p. 209. ISBN 978-0521873673. เก็บจากแหล่งเดิมเมื่อ 15 May 2016.
- ↑ Lewis1, David (Jul 30, 2014). "Liberia shuts schools, considers quarantine to curb Ebola". Reuters. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2014-08-02. สืบค้นเมื่อ 2014-08-03.
- ↑ Hoenen T, Groseth A, Feldmann H (July 2012). "Current ebola vaccines". Expert Opinion on Biological Therapy. 12 (7): 859–72. doi:10.1517/14712598.2012.685152. PMC 3422127. PMID 22559078.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 59.0 59.1 Choi JH, Croyle MA (December 2013). "Emerging targets and novel approaches to Ebola virus prophylaxis and treatment". BioDrugs. 27 (6): 565–83. doi:10.1007/s40259-013-0046-1. PMID 23813435.
- ↑ Xu L, Sanchez A, Yang Z, Zaki SR, Nabel EG, Nichol ST, Nabel GJ (1998). "Immunization for Ebola virus infection". Nature Medicine. 4 (1): 37–42. doi:10.1038/nm0198-037. PMID 9427604.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 61.0 61.1 Sullivan NJ, Geisbert TW, Geisbert JB, Xu L, Yang ZY, Roederer M, Koup RA, Jahrling PB, Nabel GJ (2003). "Accelerated vaccination for Ebola virus haemorrhagic fever in non-human primates". Nature. 424 (6949): 681–684. doi:10.1038/nature01876. PMID 12904795.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Geisbert TW, Daddario-Dicaprio KM, Geisbert JB, Reed DS, Feldmann F, Grolla A, Ströher U, Fritz EA, Hensley LE, Jones SM, Feldmann H (2008). "Vesicular stomatitis virus-based vaccines protect nonhuman primates against aerosol challenge with Ebola and Marburg viruses". Vaccine. 26 (52): 6894–6900. doi:10.1016/j.vaccine.2008.09.082. PMC 3398796. PMID 18930776.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Geisbert TW, Daddario-Dicaprio KM, Lewis MG, Geisbert JB, Grolla A, Leung A, Paragas J, Matthias L, Smith MA, Jones SM, Hensley LE, Feldmann H, Jahrling PB (2008). Kawaoka, Yoshihiro (บ.ก.). "Vesicular Stomatitis Virus-Based Ebola Vaccine is Well-Tolerated and Protects Immunocompromised Nonhuman Primates". PLoS Pathogens. 4 (11): e1000225. doi:10.1371/journal.ppat.1000225. PMC 2582959. PMID 19043556.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Geisbert TW, Geisbert JB, Leung A, Daddario-DiCaprio KM, Hensley LE, Grolla A, Feldmann H (2009). "Single-Injection Vaccine Protects Nonhuman Primates against Infection with Marburg Virus and Three Species of Ebola Virus". Journal of Virology. 83 (14): 7296–7304. doi:10.1128/JVI.00561-09. PMC 2704787. PMID 19386702.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Warfield KL, Swenson DL, Olinger GG, Kalina WV, Aman MJ, Bavari S (2007). "Ebola Virus‐Like Particle–Based Vaccine Protects Nonhuman Primates against Lethal Ebola Virus Challenge". The Journal of Infectious Diseases. 196: S430–S437. doi:10.1086/520583. PMID 17940980.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 66.0 66.1 Oplinger, Anne A. (2003-11-18). NIAID Ebola vaccine enters human trial. Bio-Medicine. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2020-12-22. สืบค้นเมื่อ 2014-08-22.
- ↑ 67.0 67.1 "Ebola/Marburg Vaccine Development" (Press release). National Institute of Allergy and Infectious Diseases. 2008-09-15. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2010-03-06. สืบค้นเมื่อ 2014-08-22.
- ↑ Martin JE, Sullivan NJ, Enama ME, Gordon IJ, Roederer M, Koup RA, Bailer RT, Chakrabarti BK, Bailey MA, Gomez PL, Andrews CA, Moodie Z, Gu L, Stein JA, Nabel GJ, Graham BS (2006). "A DNA Vaccine for Ebola Virus is Safe and Immunogenic in a Phase I Clinical Trial". Clinical and Vaccine Immunology. 13 (11): 1267–1277. doi:10.1128/CVI.00162-06. PMC 1656552. PMID 16988008.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bush, L (2005). "Crucell and NIH sign Ebola vaccine manufacturing contract". Pharmaceutical Technology. 29: 28.
- ↑ Jones SM, Feldmann H, Ströher U, Geisbert JB, Fernando L, Grolla A, Klenk HD, Sullivan NJ, Volchkov VE, Fritz EA, Daddario KM, Hensley LE, Jahrling PB, Geisbert TW (2005). "Live attenuated recombinant vaccine protects nonhuman primates against Ebola and Marburg viruses". Nature Medicine. 11 (7): 786–790. doi:10.1038/nm1258. PMID 15937495.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Viral Hemorrhagic Fever: Ribavirin Therepy". San Francisco Department of Public Health. Infectious Disease Emergencies. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2015-09-24. สืบค้นเมื่อ 2014-08-17.
- ↑ Phoolcharoen W, Dye JM, Kilbourne J, Piensook K, Pratt WD, Arntzen CJ, Chen Q, Mason HS, Herbst-Kralovetz MM (2011). "A nonreplicating subunit vaccine protects mice against lethal Ebola virus challenge". Proc. Natl. Acad. Sci. U.S.A. 108 (51): 20695–700. Bibcode:2011PNAS..10820695P. doi:10.1073/pnas.1117715108. PMC 3251076. PMID 22143779.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Canadian Press". CBCNews. Canadian Broadcasting Corporation (CBC). 20 March 2009. สืบค้นเมื่อ 2014-08-02.
- ↑ Tuffs A (2009). "Experimental vaccine may have saved Hamburg scientist from Ebola fever". BMJ. 338: b1223. doi:10.1136/bmj.b1223. PMID 19307268.
- ↑ Feldmann H, Jones SM, Daddario-DiCaprio KM, Geisbert JB, Ströher U, Grolla A, Bray M, Fritz EA, Fernando L, Feldmann F, Hensley LE, Geisbert TW (2007). "Effective Post-Exposure Treatment of Ebola Infection". PLoS Pathogens. 3 (1): e2. doi:10.1371/journal.ppat.0030002. PMC 1779298. PMID 17238284.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Geisbert TW, Daddario-DiCaprio KM, Williams KJ, Geisbert JB, Leung A, Feldmann F, Hensley LE, Feldmann H, Jones SM (2008). "Recombinant Vesicular Stomatitis Virus Vector Mediates Postexposure Protection against Sudan Ebola Hemorrhagic Fever in Nonhuman Primates". Journal of Virology. 82 (11): 5664–5668. doi:10.1128/JVI.00456-08. PMC 2395203. PMID 18385248.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Bausch DG, Feldmann H, Geisbert TW, Bray M, Sprecher AG, Boumandouki P, Rollin PE, Roth C (2007). "Outbreaks of Filovirus Hemorrhagic Fever: Time to Refocus on the Patient". The Journal of Infectious Diseases. 196: S136–S141. doi:10.1086/520542. PMID 17940941.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Jeffs B (2006). "A clinical guide to viral haemorrhagic fevers: Ebola, Marburg and Lassa". Tropical Doctor. 36 (1): 1–4. doi:10.1258/004947506775598914. PMID 16483416.
- ↑ Nkoghé D, Formenty P, Nnégué S, Mvé MT, Hypolite I, Léonard P, Leroy E, Comité International de Coordination Technique et Scientifique (2004). "Practical guidelines for the management of Ebola infected patients in the field". Médecine tropicale : revue du Corps de santé colonial. 64 (2): 199–204. PMID 15460155.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Sierra Leone Is Epicenter of Ebola as Guinea Clinic Shut". 2014-06-08. สืบค้นเมื่อ 2014-07-30.
- ↑ Briggs H. "BBC News - Ebola: Experimental drugs and vaccines". BBC News. สืบค้นเมื่อ 2014-08-08.
- ↑ "Who, What, Why: How many people infected with ebola die?". BBC News. 2014-08-09.
บรรณานุกรม[แก้]
- McCormick J, Fisher-Hoch S, Horvitz LA (1999) [1996]. Level 4: Virus Hunters of the CDC (Limited preview) (Updated [3rd] ed.). Barnes & Noble. ISBN 978-0760712085.
อ่านเพิ่ม[แก้]
- Wilson F (2014). CDC Guidance on Ebola Virus (EVD). International Publications Media Group. ISBN 978-1632670113.
- Ebola Virus: New Insights for the Healthcare Professional: 2011 Edition: ScholarlyPaper. Scholarly Editions. 2012. ISBN 978-1464914935.
- Klenk HD (January 1999). Marburg and Ebola Viruses. Current Topics in Microbiology and Immunology 235. Berlin: Springer-Verlag Telos. ISBN 978-3540647294.
- Klenk HD, Feldmann H (2004). Ebola and Marburg viruses: molecular and cellular biology (Limited preview). Wymondham, Norfolk: Horizon Bioscience. ISBN 978-0954523237.
- Kuhn JH (2008). Filoviruses: A Compendium of 40 Years of Epidemiological, Clinical, and Laboratory Studies. Archives of Virology Supplement (Limited preview). Vol. 20. Vienna: SpringerWienNewYork. ISBN 978-3211206706.
- Pattyn SR (1978). Ebola Virus Haemorrhagic Fever (1st ed.). Amsterdam: Elsevier/North-Holland Biomedical Press. ISBN 978-0444800602. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (Full free text)เมื่อ 11 December 2010.
- Ryabchikova EI, Price BB (2004). Ebola and Marburg Viruses: A View of Infection Using Electron Microscopy. Columbus, Ohio: Battelle Press. ISBN 978-1574771312.
แหล่งข้อมูลอื่น[แก้]
- WHO fact sheet on Ebola
- Ebola (Ebola Virus Disease) – Centers for Disease Control and Prevention, Viral Special Pathogens Branch.
- Videos: Ebola outbreak response – World Health Organization.
- "Ebola Preparedness and Response". U.S. Food and Drug Administration (FDA). 13 January 2021.
- Ebola: What You Need to Know – Scientific American articles related to Ebola; note these are general reading articles, they are not scientific peer-reviewed research articles.
| การจำแนกโรค | |
|---|---|
| ทรัพยากรภายนอก |
