ผลต่างระหว่างรุ่นของ "แก๊สมีสกุล"
ล syntax error |
ล เพิ่มอ้างอิง |
||
| บรรทัด 1: | บรรทัด 1: | ||
{{periodic table (noble gases)}} |
{{periodic table (noble gases)}} |
||
'''แก๊สมีตระกูล''' (ในอดีตเรียกว่า '''แก๊สเฉื่อย''' หรือบางครั้งใช้ชื่อว่า '''aerogens'''<ref>{{cite journal |last1=Bauzá |first1=Antonio |last2=Frontera |first2=Antonio |date=2015 |title=Aerogen Bonding Interaction: A New Supramolecular Force? |journal=Angewandte Chemie International Edition |volume=54 |issue=25 |pages=7340–3 |doi=10.1002/anie.201502571|pmid=25950423}}</ref>) เป็นกลุ่มของ[[ธาตุทางเคมี]]ซึ่งมีสมบัติคล้ายกัน ภายใต้[[ภาวะมาตรฐานสำหรับอุณหภูมิและความดัน |
'''แก๊สมีตระกูล''' (ในอดีตเรียกว่า '''แก๊สเฉื่อย''' หรือบางครั้งใช้ชื่อว่า '''aerogens'''<ref>{{cite journal |last1=Bauzá |first1=Antonio |last2=Frontera |first2=Antonio |date=2015 |title=Aerogen Bonding Interaction: A New Supramolecular Force? |journal=Angewandte Chemie International Edition |volume=54 |issue=25 |pages=7340–3 |doi=10.1002/anie.201502571|pmid=25950423}}</ref>) เป็นกลุ่มของ[[ธาตุทางเคมี]]ซึ่งมีสมบัติคล้ายกัน ภายใต้[[ภาวะมาตรฐาน|ภาวะมาตรฐานสำหรับอุณหภูมิและความดัน]]ธาตุเหล่านี้ต่างไม่มีกลิ่น ไม่มีสี เป็นแก๊สอะตอมเดี่ยวซึ่งไม่มีความว่องไวต่อปฏิกริยาเคมี แก๊สมีตระกูลที่เกิดในธรรมชาติทั้งหกธาตุ ได้แก่ [[ฮีเลียม]] (He), [[นีออน]] (Ne), [[อาร์กอน]] (Ar), [[คริปทอน]] (Kr), [[ซีนอน]] (Xe) และ[[เรดอน]] (Rn) |
||
แก๊สมีตระกูลมีคุณสมบัติดังนี้ |
แก๊สมีตระกูลมีคุณสมบัติดังนี้ |
||
| บรรทัด 139: | บรรทัด 139: | ||
== การใช้ประโยชน์ == |
== การใช้ประโยชน์ == |
||
[[ไฟล์:Modern 3T MRI.JPG|thumb|ฮีเลียมเหลวถูกใช้ลดอุณหภูมิของแม่เหล็กตัวนำยิ่งยวด ในเครื่องสแกน MRI สมัยใหม่]] |
[[ไฟล์:Modern 3T MRI.JPG|thumb|left|ฮีเลียมเหลวถูกใช้ลดอุณหภูมิของแม่เหล็กตัวนำยิ่งยวด ในเครื่องสแกน MRI สมัยใหม่]] |
||
<!-- อติสีตศาสตร์ (cyrogenics) --> |
|||
แก๊สมีตระกูลมีจุดเดือดและจุดหลอมเหลวที่ต่ำมาก ซึ่งทำให้แก๊สเหล่านี้ใช้เป็น[[สารทำความเย็น]]ในเชิง[[อติสีตศาสตร์]] โดยเฉพาะ[[ฮีเลียมเหลว]]<ref>{{cite encyclopedia|title=Neon|encyclopedia=[[Encarta]]|year=2008}}</ref> ซึ่งเดือดที่ 4.2 เคลวิน (−268.95 องศาเซลเซียส; −452.11 องศาฟาเรนไฮต์) ถูกนำไปใช้สร้าง[[แม่เหล็กตัวนำยิ่งยวด]] สำหรับการสร้างภาพด้วย[[เรโซแนนซ์แม่เหล็ก (MRI)]] และ[[นิวเคลียร์แมกเนติกเรโซแนนซ์สเปกโทรสโกปี (NMR)]]<ref>{{cite journal|title=Demountable coaxial gas-cooled current leads for MRI superconducting magnets|author1=Zhang, C. J. |author2=Zhou, X. T. |author3=Yang, L. |journal=IEEE Transactions on Magnetics|publisher=[[IEEE]]|volume=28|issue=1|year=1992|pages=957–959|doi=10.1109/20.120038|bibcode= 1992ITM....28..957Z }}</ref> นีออนเหลวถึงแม้จะไม่สามารถลดอุณหภูมิจนเท่าฮีเลียมเหลว นีออนเหลวยังถูกใช้ในงานด้านอติสีตศาสตร์เนื่องจากมีวิสัยสามารถทำความเย็นมากกว่าฮีเลียมเหลว 40 เท่าและมากกว่าไฮโดรเจนเหลว 3 เท่า<ref name=ullmann/> |
แก๊สมีตระกูลมีจุดเดือดและจุดหลอมเหลวที่ต่ำมาก ซึ่งทำให้แก๊สเหล่านี้ใช้เป็น[[สารทำความเย็น]]ในเชิง[[อติสีตศาสตร์]] โดยเฉพาะ[[ฮีเลียมเหลว]]<ref>{{cite encyclopedia|title=Neon|encyclopedia=[[Encarta]]|year=2008}}</ref> ซึ่งเดือดที่ 4.2 เคลวิน (−268.95 องศาเซลเซียส; −452.11 องศาฟาเรนไฮต์) ถูกนำไปใช้สร้าง[[แม่เหล็กตัวนำยิ่งยวด]] สำหรับการสร้างภาพด้วย[[เรโซแนนซ์แม่เหล็ก (MRI)]] และ[[นิวเคลียร์แมกเนติกเรโซแนนซ์สเปกโทรสโกปี (NMR)]]<ref>{{cite journal|title=Demountable coaxial gas-cooled current leads for MRI superconducting magnets|author1=Zhang, C. J. |author2=Zhou, X. T. |author3=Yang, L. |journal=IEEE Transactions on Magnetics|publisher=[[IEEE]]|volume=28|issue=1|year=1992|pages=957–959|doi=10.1109/20.120038|bibcode= 1992ITM....28..957Z }}</ref> นีออนเหลวถึงแม้จะไม่สามารถลดอุณหภูมิจนเท่าฮีเลียมเหลว นีออนเหลวยังถูกใช้ในงานด้านอติสีตศาสตร์เนื่องจากมีวิสัยสามารถทำความเย็นมากกว่าฮีเลียมเหลว 40 เท่าและมากกว่าไฮโดรเจนเหลว 3 เท่า<ref name=ullmann/> |
||
<!-- การดำน้ำ --> |
|||
ฮีเลียมถูกใช้เป็นองค์ประกอบของ[[แก๊สสำหรับหายใจ]]แทนที่ไนโตรเจน เนื่องจากมีความสามารถใน[[การละลาย]]ในของไหลต่ำโดยเฉพาะ[[ไขมัน]] แก๊สทั่วไปมักถูกดูดซึมโดย[[เลือด]]และ[[เนื้อเยื่อ]]ภายใต้ความดันเช่น[[การดำน้ำลึก]] ทำให้เกิด[[ภาวะเซื่องซึม]]เรียกว่า[[ภาวะเมาไนโตรเจน]]<ref name=Fowler>{{cite journal |last1=Fowler |first1=B. |last2=Ackles |first2=K. N. |last3=Porlier |first3=G. |title=Effects of inert gas narcosis on behavior—a critical review |journal=Undersea Biomed. Res. |volume=12 |issue=4 |pages=369–402 |year=1985 |issn=0093-5387 |oclc=2068005 |pmid=4082343 |url=http://archive.rubicon-foundation.org/3019 |access-date=8 April 2008 |archive-url=https://web.archive.org/web/20101225052236/http://archive.rubicon-foundation.org/3019 |archive-date=25 December 2010 |url-status=usurped }}</ref> แต่ด้วยที่ฮีเลียมมีความสามารถในการละลายต่ำ ฮีเลียมจึงซึมเข้า[[เยื่อหุ้มเซลล์]]ได้น้อย เมื่อใช้ฮีเลียมเป็นส่วนผสมของแก๊สสำหรับหายใจเช่นใน [[trimix]] หรือ [[heliox]] จึงช่วยลดอาการเซื่องซึมของนักประดาน้ำภายใต้ความลึก<ref>{{harvnb|Bennett|1998|p=176}}</ref> ความสามารถในการละลายของฮีเลียมที่น้อยมีประโยชน์ในการรักษา[[โรคลดความกด]]หรือ ''the bends''<ref name="brit"/><ref>{{cite journal |editor-last=Vann|editor-first=R. D. |title=The Physiological Basis of Decompression|journal=38th Undersea and Hyperbaric Medical Society Workshop |volume=75(Phys)6-1-89 |year=1989 |pages=437 |url=http://archive.rubicon-foundation.org/6853 |archive-url=https://web.archive.org/web/20081007192913/http://archive.rubicon-foundation.org/6853 |url-status=usurped |archive-date=7 October 2008 |access-date=31 May 2008}}</ref> เมื่อมีปริมาณแก๊สละลายในร่างกายลดลงหมายความว่าจะเกิดฟองแก๊สจำนวนน้อยลงที่ความดันที่ต่ำลง นอกจากนี้อาร์กอนยังเป็นตัวเลือกที่ดีที่สุดสำหรับการดำน้ำลึกแบบ [[drysuit]]<ref>{{cite web |last=Maiken |first=Eric |title=Why Argon? |url=http://www.decompression.org/maiken/Why_Argon.htm |access-date=26 June 2008|publisher=Decompression|date=1 August 2004}}</ref> และฮีเลียมยังใช้เป็นแก๊สเติมแกนของเตาปฏิกรณ์นิวเคลียร์ |
ฮีเลียมถูกใช้เป็นองค์ประกอบของ[[แก๊สสำหรับหายใจ]]แทนที่ไนโตรเจน เนื่องจากมีความสามารถใน[[การละลาย]]ในของไหลต่ำโดยเฉพาะ[[ไขมัน]] แก๊สทั่วไปมักถูกดูดซึมโดย[[เลือด]]และ[[เนื้อเยื่อ]]ภายใต้ความดันเช่น[[การดำน้ำลึก]] ทำให้เกิด[[ภาวะเซื่องซึม]]เรียกว่า[[ภาวะเมาไนโตรเจน]]<ref name=Fowler>{{cite journal |last1=Fowler |first1=B. |last2=Ackles |first2=K. N. |last3=Porlier |first3=G. |title=Effects of inert gas narcosis on behavior—a critical review |journal=Undersea Biomed. Res. |volume=12 |issue=4 |pages=369–402 |year=1985 |issn=0093-5387 |oclc=2068005 |pmid=4082343 |url=http://archive.rubicon-foundation.org/3019 |access-date=8 April 2008 |archive-url=https://web.archive.org/web/20101225052236/http://archive.rubicon-foundation.org/3019 |archive-date=25 December 2010 |url-status=usurped }}</ref> แต่ด้วยที่ฮีเลียมมีความสามารถในการละลายต่ำ ฮีเลียมจึงซึมเข้า[[เยื่อหุ้มเซลล์]]ได้น้อย เมื่อใช้ฮีเลียมเป็นส่วนผสมของแก๊สสำหรับหายใจเช่นใน [[trimix]] หรือ [[heliox]] จึงช่วยลดอาการเซื่องซึมของนักประดาน้ำภายใต้ความลึก<ref>{{harvnb|Bennett|1998|p=176}}</ref> ความสามารถในการละลายของฮีเลียมที่น้อยมีประโยชน์ในการรักษา[[โรคลดความกด]]หรือ ''the bends''<ref name="brit"/><ref>{{cite journal |editor-last=Vann|editor-first=R. D. |title=The Physiological Basis of Decompression|journal=38th Undersea and Hyperbaric Medical Society Workshop |volume=75(Phys)6-1-89 |year=1989 |pages=437 |url=http://archive.rubicon-foundation.org/6853 |archive-url=https://web.archive.org/web/20081007192913/http://archive.rubicon-foundation.org/6853 |url-status=usurped |archive-date=7 October 2008 |access-date=31 May 2008}}</ref> เมื่อมีปริมาณแก๊สละลายในร่างกายลดลงหมายความว่าจะเกิดฟองแก๊สจำนวนน้อยลงที่ความดันที่ต่ำลง นอกจากนี้อาร์กอนยังเป็นตัวเลือกที่ดีที่สุดสำหรับการดำน้ำลึกแบบ [[drysuit]]<ref>{{cite web |last=Maiken |first=Eric |title=Why Argon? |url=http://www.decompression.org/maiken/Why_Argon.htm |access-date=26 June 2008|publisher=Decompression|date=1 August 2004}}</ref> และฮีเลียมยังใช้เป็นแก๊สเติมแกนของเตาปฏิกรณ์นิวเคลียร์ |
||
| ⚫ | |||
| ⚫ | |||
<!-- การยกตัว --> |
|||
| ⚫ | ในการประยุกต์ใช้ แก๊สมีตระกูลถูกใช้ในบรรยากาศเฉื่อย อาร์กอนถูกใช้ในการสังเคราะห์[[สารประกอบที่ไวต่ออากาศ]]นั่นคือไวต่อไนโตรเจน อาร์กอนแข็งถูกใช้ในการศึกษาสารประกอบที่ไม่เสถียรมากเช่น[[สารมัธยันตร์]]ที่ไวต่อปฏิกิริยา โดยการกักใน[[เมทริกซ์ (การวัดค่าทางเคมี)|เมทริกซ์]]เฉื่อยที่อุณหภูมิต่ำมาก ฮีเลียมถูกใช้เป็นตัวกลางนำพาในเทคนิค[[แก๊สโครมาโทกราฟี]] เป็นแก๊สเติมใน[[เทอร์โมมิเตอร์]]และในอุปกรณ์ตรวจวัดการแผ่รังสีเช่น[[เครื่องนับไกเกอร์–มึลเลอร์]]และ[[ห้องฟอง]] ฮีเลียมและอาร์กอนมักถูกใช้เป็นกำบังสำหรับ[[การเชื่อมอาร์ก]]และการกระจายของ[[โลหะไร้สกุล]]ในบรรยากาศขณะเชื่อมหรือตัดโลหะ รวมถึงกระบวนการทางโลหการและการผลิตซิลิคอนในอุตสาหกรรมสารกึ่งตัวนำ |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | ตั้งแต่[[วินาศภัยฮินเดินบวร์ค|วินาศภัย''ฮินเดินบวร์ค'']]ในปี ค.ศ. 1937<ref>{{cite news|title=Disaster Ascribed to Gas by Experts|work=[[The New York Times]]|date=7 May 1937|page=1}}</ref> ฮีเลียมถูกใช้ทดแทนไฮโดรเจนสำหรับ[[แก๊สลอยตัว]]ใน[[เรือเหาะ]]และ[[ลูกโป่ง]] เนื่องจากความเบาและความไม่ติดไฟ แม้ว่าจะมีแรงลอยตัวลดลง 8.6%<ref>{{cite web |
||
| ⚫ | แก๊สมีตระกูลมักถูกใช้ใน[[การ |
||
|last=Freudenrich|first=Craig|year=2008 |
|||
|url=http://science.howstuffworks.com/blimp2.htm |
|||
|title=How Blimps Work|publisher=HowStuffWorks |
|||
|access-date=3 July 2008}}</ref><ref name="brit"/> |
|||
<!-- งานด้านวิทยาศาสตร์และประยุกต์อื่น --> |
|||
| ⚫ | ในการประยุกต์ใช้ แก๊สมีตระกูลถูกใช้ในบรรยากาศเฉื่อย อาร์กอนถูกใช้ในการสังเคราะห์[[สารประกอบที่ไวต่ออากาศ]]นั่นคือไวต่อไนโตรเจน อาร์กอนแข็งถูกใช้ในการศึกษาสารประกอบที่ไม่เสถียรมากเช่น[[สารมัธยันตร์]]ที่ไวต่อปฏิกิริยา โดยการกักใน[[เมทริกซ์ (การวัดค่าทางเคมี)|เมทริกซ์]]เฉื่อยที่อุณหภูมิต่ำมาก<ref>{{cite journal |journal=Chem. Soc. Rev. |year=1980 |volume=9 |pages=1–23 |doi=10.1039/CS9800900001 |title=The matrix isolation technique and its application to organic chemistry |author=Dunkin, I. R.}}</ref> ฮีเลียมถูกใช้เป็นตัวกลางนำพาในเทคนิค[[แก๊สโครมาโทกราฟี]] เป็นแก๊สเติมใน[[เทอร์โมมิเตอร์]]และในอุปกรณ์ตรวจวัดการแผ่รังสีเช่น[[เครื่องนับไกเกอร์–มึลเลอร์]]และ[[ห้องฟอง]]<ref name=kirk/> ฮีเลียมและอาร์กอนมักถูกใช้เป็นกำบังสำหรับ[[การเชื่อมอาร์ก]]และการกระจายของ[[โลหะไร้สกุล]]ในบรรยากาศขณะเชื่อมหรือตัดโลหะ รวมถึงกระบวนการทางโลหการและการผลิตซิลิคอนในอุตสาหกรรมสารกึ่งตัวนำ<ref name="ullmann" /> |
||
<!-- การจัดแสง --> |
|||
| ⚫ | |||
| ⚫ | แก๊สมีตระกูลมักถูกใช้ใน[[การจัดแสง]]เพราะมีความไวต่อปฏิกิริยาเคมีต่ำ อาร์กอนจะผสมกับไนโตรเจนใช้เติมใน[[หลอดไส้ร้อนแบบธรรมดา]]<ref name=ullmann>{{cite book |author1=Häussinger, Peter |author2=Glatthaar, Reinhard |author3=Rhode, Wilhelm |author4=Kick, Helmut |author5=Benkmann, Christian |author6=Weber, Josef |author7=Wunschel, Hans-Jörg |author8=Stenke, Viktor |author9=Leicht, Edith |author10=Stenger, Hermann |chapter=Noble gases |title=Ullmann's Encyclopedia of Industrial Chemistry |publisher=Wiley |year=2002 |doi=10.1002/14356007.a17_485|isbn=3-527-30673-0 }}</ref> คริปทอนถูกใช้ในหลอดไฟประสิทธิภาพสูง ซึ่งให้[[อุณหภูมิสี]]และประสิทธิภาพสูงกว่า เนื่องจากสามารถลดอัตราการขาดของแกนหลอดไฟได้ดีกว่าอาร์กอน [[หลอดแฮโลเจน]]ใช้คริปทอนประสมกับสารประกอบของ[[ไอโอดีน]]หรือ[[โบรมีน]]ปริมาณน้อย<ref name=ullmann/> แก๊สมีตระกูลเรืองแสงให้สีที่โดดเด่นเมื่อใช้ใน[[หลอดแก๊สคายประจุ]]เช่น [[หลอดไฟนีออน]] แม้ว่าหลอดไฟจะเรียกชื่อตามแก๊สนีออนแต่ก็ประกอบด้วยแก๊สชนิดอื่นและ[[สารเรืองแสง]] ซึ่งทำให้เกิดเฉดสีหลากหลายได้เป็นสีส้มอมแดงของนีออน ซีนอนมักใช้ใน[[หลอดไฟซีนอนอาร์ค]] เนื่องจาก[[สเปกตรัมต่อเนื่อง|สเปกตรัมที่เกือบต่อเนื่อง]]คล้ายกับแสงอาทิตย์ จึงมักประยุกต์ในเครื่องฉายภาพยนตร์และไฟหน้ารถ<ref name=ullmann/> |
||
<!-- การทำเลเซอร์ --> |
|||
แก๊สมีตระกูลถูกใช้ใน[[เอ็กไซเมอร์เลเซอร์]] ซึ่งสร้างจากโมเลกุลที่ถูกกระตุ้นด้วยไฟฟ้าและคงสภาพในระยะเวลาสั้นเรียกว่า[[เอ็กไซเมอร์]] โมเลกุลเอ็กไซเมอร์ที่ถูกใช้ในเลเซอร์อาจเป็นไดเมอร์ของแก๊สมีตระกูลเช่น Ar<sub>2</sub>, Kr<sub>2</sub> หรือ Xe<sub>2</sub> หรือที่นิยมใช้คือแก๊สมีตระกูลที่รวมตัวกับธาตุฮาโลเจนในรูปโมเลกุลเอ็กไซเมอร์เช่น ArF, KrF, XeF หรือ XeCl เลเซอร์เหล่านี้สร้างรังสี[[อัลตราไวโอเล็ต]] ซึ่งเนื่องจาก[[ความยาวคลื่น]]ที่สั้น (193 [[นาโนเมตร]]สำหรับ ArF และ 248 นาโนเมตรสำหรับ KrF) ทำให้ใช้ในงานภาพถ่ายรังสีแม่นยำสูงได้ เอ็กไซเมอเลเซอร์ถูกใช้ในด้านอุตสาหกรรม การแพทย์และวิทยาศาสตร์อย่างหลากหลาย นอกจากนี้ยังใช้ในงานด้าน[[ไมโครลิโธกราฟี]]และด้าน[[การสร้างชิ้นส่วนจุลภาค]] ซึ่งมีความสำคัญในการผลิต[[วงจรรวม]] และ[[การผ่าตัดด้วยเลเซอร์]]ได้แก่[[การขยายหลอดเลือดด้วยเลเซอร์]]และ[[การผ่าตัดตา]] |
แก๊สมีตระกูลถูกใช้ใน[[เอ็กไซเมอร์เลเซอร์]] ซึ่งสร้างจากโมเลกุลที่ถูกกระตุ้นด้วยไฟฟ้าและคงสภาพในระยะเวลาสั้นเรียกว่า[[เอ็กไซเมอร์]] โมเลกุลเอ็กไซเมอร์ที่ถูกใช้ในเลเซอร์อาจเป็นไดเมอร์ของแก๊สมีตระกูลเช่น Ar<sub>2</sub>, Kr<sub>2</sub> หรือ Xe<sub>2</sub> หรือที่นิยมใช้คือแก๊สมีตระกูลที่รวมตัวกับธาตุฮาโลเจนในรูปโมเลกุลเอ็กไซเมอร์เช่น ArF, KrF, XeF หรือ XeCl เลเซอร์เหล่านี้สร้างรังสี[[อัลตราไวโอเล็ต]] ซึ่งเนื่องจาก[[ความยาวคลื่น]]ที่สั้น (193 [[นาโนเมตร]]สำหรับ ArF และ 248 นาโนเมตรสำหรับ KrF) ทำให้ใช้ในงานภาพถ่ายรังสีแม่นยำสูงได้ เอ็กไซเมอเลเซอร์ถูกใช้ในด้านอุตสาหกรรม การแพทย์และวิทยาศาสตร์อย่างหลากหลาย นอกจากนี้ยังใช้ในงานด้าน[[ไมโครลิโธกราฟี]]และด้าน[[การสร้างชิ้นส่วนจุลภาค]] ซึ่งมีความสำคัญในการผลิต[[วงจรรวม]] และ[[การผ่าตัดด้วยเลเซอร์]]ได้แก่[[การขยายหลอดเลือดด้วยเลเซอร์]]และ[[การผ่าตัดตา]]<ref>{{cite book |title=Excimer Laser Technology |author1=Basting, Dirk |author2=Marowsky, Gerd |publisher=Springer |year=2005 |isbn=3-540-20056-8}}</ref> |
||
<!-- การแพทย์ --> |
|||
แก๊สมีตระกูลบางชนิดมีการประยุกต์ใช้โดยตรงในทางการแพทย์ บางครั้งฮีเลียมจะถูกใช้ช่วยผู้ป่วย[[หอบหืด]]ให้หายใจดีขึ้น ซีนอนถูกใช้เป็น[[ยาสลบ]]เพราะความสามารถในการละลายในไขมันที่สูง ทำให้เกิดฤทธิ์มากกว่า[[ไนตรัสออกไซด์]]ที่ใช้โดยทั่วไปและเนื่องจากมันถูกกำจัดจากร่างกายโดยทันที ทำให้ |
แก๊สมีตระกูลบางชนิดมีการประยุกต์ใช้โดยตรงในทางการแพทย์ บางครั้งฮีเลียมจะถูกใช้ช่วยผู้ป่วย[[หอบหืด]]ให้หายใจดีขึ้น<ref name=ullmann/> ซีนอนถูกใช้เป็น[[ยาสลบ]]เพราะความสามารถในการละลายในไขมันที่สูง ทำให้เกิดฤทธิ์มากกว่า[[ไนตรัสออกไซด์]]ที่ใช้โดยทั่วไปและเนื่องจากมันถูกกำจัดจากร่างกายโดยทันที ทำให้ผู้ป่วยฟื้นตัวเร็วขึ้น<ref>{{cite journal|author1=Sanders, Robert D. |author2=Ma, Daqing |author3=Maze, Mervyn |title=Xenon: elemental anaesthesia in clinical practice|journal=British Medical Bulletin|year=2005|volume=71|issue=1|pages=115–135|doi= 10.1093/bmb/ldh034|pmid=15728132|doi-access=free}}</ref> ซีนอนถูกประยุกต์ในการถ่ายภาพรังสีทางการแพทย์ของปอดด้วยเทคนิค hyperpolarized MRI<ref>{{cite journal|last1=Albert|first1=M. S.|last2=Balamore|first2=D.|title=Development of hyperpolarized noble gas MRI |journal=Nuclear Instruments and Methods in Physics Research A|year=1998|volume=402|pages=441–453|doi= 10.1016/S0168-9002(97)00888-7|pmid=11543065|issue=2–3|bibcode= 1998NIMPA.402..441A }}</ref> เรดอนซึ่งไวต่อปฏิกิริยามากและมีปริมาณน้อยถูกใช้ใน[[การรังสีบำบัด]]<ref name=brit /> |
||
<!-- เครื่องยนต์ไอออน --> |
|||
แก๊สมีตระกูลโดยเฉพาะซีนอนถูกใช้มากใน[[เครื่องยนต์ไอออน]]เนื่องจากความเฉื่อยของมัน เนื่องจากเครื่องยนต์ไอออนไม่ได้ขับเคลื่อนด้วยปฏิกิริยาเคมี เชื้อเพลิงที่เฉื่อยเชิงเคมีถูกใช้ป้องกันการเกิดปฏิกิริยาที่ไม่พึงประสงค์ระหว่างเชื้อเพลิงรวมถึงสิ่งอื่นในเครื่องยนต์ |
แก๊สมีตระกูลโดยเฉพาะซีนอนถูกใช้มากใน[[เครื่องยนต์ไอออน]]เนื่องจากความเฉื่อยของมัน เนื่องจากเครื่องยนต์ไอออนไม่ได้ขับเคลื่อนด้วยปฏิกิริยาเคมี เชื้อเพลิงที่เฉื่อยเชิงเคมีถูกใช้ป้องกันการเกิดปฏิกิริยาที่ไม่พึงประสงค์ระหว่างเชื้อเพลิงรวมถึงสิ่งอื่นในเครื่องยนต์ |
||
รุ่นแก้ไขเมื่อ 20:19, 9 สิงหาคม 2566
| แก๊สมีสกุล | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||
| ↓ คาบ | |||||||||||
| 1 | ฮีเลียม (He) 2 | ||||||||||
| 2 | นีออน (Ne) 10 | ||||||||||
| 3 | อาร์กอน (Ar) 18 | ||||||||||
| 4 | คริปตอน (Kr) 36 | ||||||||||
| 5 | ซีนอน (Xe) 54 | ||||||||||
| 6 | เรดอน (Rn) 86 | ||||||||||
| 7 | โอกาเนสซอน (Og) 118 | ||||||||||
|
คำอธิบาย
| |||||||||||
แก๊สมีตระกูล (ในอดีตเรียกว่า แก๊สเฉื่อย หรือบางครั้งใช้ชื่อว่า aerogens[1]) เป็นกลุ่มของธาตุทางเคมีซึ่งมีสมบัติคล้ายกัน ภายใต้ภาวะมาตรฐานสำหรับอุณหภูมิและความดันธาตุเหล่านี้ต่างไม่มีกลิ่น ไม่มีสี เป็นแก๊สอะตอมเดี่ยวซึ่งไม่มีความว่องไวต่อปฏิกริยาเคมี แก๊สมีตระกูลที่เกิดในธรรมชาติทั้งหกธาตุ ได้แก่ ฮีเลียม (He), นีออน (Ne), อาร์กอน (Ar), คริปทอน (Kr), ซีนอน (Xe) และเรดอน (Rn)
แก๊สมีตระกูลมีคุณสมบัติดังนี้
- เป็นแก๊สที่ไม่ทำปฏิกิริยากับธาตุอื่น ๆ เพราะอิเล็กตรอนชั้นนอกสุด (valence electron) ครบ 8 ตัว (ยกเว้น He ที่มี 2 ตัว)
- มีสถานะเป็นแก๊สทั้งหมด (1 โมเลกุล ประกอบด้วยอะตอม 1 อะตอม) ได้แก่ He, Ar, Kr, Rn
- ปัจจุบันพบแก๊สเฉื่อยบางชนิด เช่น Kr และ Xe สามารถทำปฏิกิริยากับ F และ O ได้ เช่น KrF2, XeF2, XeF4, XeF6, XeO3, XeO4
- แก๊สเฉื่อยมีแรงยึดเหนี่ยวระหว่างโมเลกุลเป็น "วันเดอร์วาลส์" จึงทำให้มีจุดเดือดจุดหลอมเหลวต่ำ
ประวัติ
แก๊สมีตระกูล ถูกแปลมาจากคำว่า Edelgas ในภาษาเยอรมัน คำดังกล่าวถูกใช้ครั้งแรกในปี ค.ศ. 1898 โดยฮิวโก้ เอิร์ดแมนน์[2] เพื่อบ่งบอกถึงระดับความว่องไวต่อปฏิกิริยาที่ต่ำ ชื่อนี้ถูกตั้งด้วยเหตุผลเดียวกับ "โลหะมีสกุล" ซึ่งมีค่าความว่องไวต่อปฏิกิริยาที่ต่ำเช่นเดียวกัน อีกชื่อของแก๊สมีตระกูลอย่างแก๊สเฉื่อยไม่ได้รับความนิยมแล้ว เนื่องจากสารประกอบของก๊าซมีตระกูลเป็นที่รู้จักมากกว่าเดิม[3] และ แก๊สหายาก ซึ่งเป็นอีกชื่อที่เคยถูกใช้[4] ถูกตั้งอย่างไม่ถูกต้อง เพราะการสลายตัวของกัมมันตภาพรังสีโพแทสเซียม-40 ทำให้อาร์กอนเป็นส่วนประกอบของบรรยากาศของโลกมากถึง 0.94% โดยปริมาตร และ 1.3% โดยมวล[5]
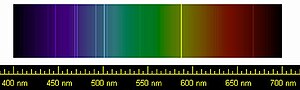
ปีแยร์ ฌ็องซ็อง และนอร์แมน ล็อกเยอร์ค้นพบธาตุใหม่ในวันที่ 18 สิงหาคม ค.ศ. 1868 ขณะมองไปที่ชั้นโครโมสเฟียร์ของดวงอาทิตย์ และตั้งชื่อมันว่าฮีเลียม จากคำว่า ἥλιος (hḗlios)[6] ซึ่งมีความหมายในภาษากรีกว่าดวงอาทิตย์ การวิเคราะห์ทางเคมีที่สามารถพิสูจน์ว่าฮีเลียมเป็นแก๊สมีตระกูลเกิดขึ้นในภายหลัง ก่อนการพิสูจน์ดังกล่าว เมื่อ ค.ศ. 1784 นักเคมีและนักฟิสิกส์ชาวอังกฤษ เฮนรี คาเวนดิชค้นพบสารจำนวนน้อยในอากาศที่มีความว่องไวต่อปฏิกิริยาต่ำกว่าไนโตรเจน[7] ต่อมาในปี ค.ศ. 1895 จอห์น วิลเลียม สตรัทท์ หรือ ลอร์ดเรย์ลี่ ค้นพบว่าสารไนโตรเจนตัวอย่างจากอากาศมีความหนาแน่นต่างจากไนโตรเจนที่ได้จากปฏิกิริยาเคมี ร่วมกันกับนักวิทยาศาสตร์ชาวสกอตแลนด์ วิลเลียม แรมซีย์จากยูนิเวอร์ซิตีคอลลิจลันเดิน เรย์ลี่ได้ตั้งทฤษฎีขึ้นว่าไนโตรเจนที่สกัดได้จากอากาศถูกปนเปื้อนกับแก๊สอื่น นำไปสู่การทดลองที่ประสบความสำเร็จในการสกัดธาตุใหม่อย่างอาร์กอน ซึ่งถูกตั้งชื่อจากคำภาษากรีกว่า ἀργός (argós ซึ่งมีความหมายว่า "ไม่ได้ใช้งาน" หรือ "ขี้เกียจ")[7] การค้นพบใหม่ทำให้พวกเขาตระหนักว่ามีแก๊สจำนวนมากหายไปจากตารางธาตุ ในการทดลองเพื่อหาธาตุอาร์กอน แรมซีย์ก็ยังพบวิธีสกัดฮีเลียมเป็นครั้งแรก ขณะให้ความร้อนแก่แร่ธาตุชื่อ คลีเวตหลังได้รับหลักฐานการมีอยู่ของธาตุฮีเลียมและอาร์กอน ในปี ค.ศ. 1902 ดมีตรี เมนเดเลเยฟได้เพิ่มแก๊สมีตระกูลทั้งสองลงในกลุ่มที่ 0 ของลำดับการเรียงธาตุของเขา ภายหลังรู้จักในชื่อตารางธาตุ[8]
แรมซีย์ทำการทดลองหาแก๊สมีตระกูลต่อไป ด้วยการใช้วิธีการกลั่นแบบลำดับส่วนในการแยกอากาศเหลวกลายเป็นส่วนประกอบต่างๆ จนปี ค.ศ. 1898 เขาได้ค้นพบธาตุ คริปทอน, นีออน, และ ซีนอน ซึ่งถูกตั้งชื่อตามคำภาษากรีกว่า κρυπτός (kryptós, "หาย"), νέος (néos, "ใหม่") และ ξένος (ksénos, "แปลก") ตามลำดับ เรดอนถูกค้นพบตั้งแต่ ค.ศ. 1898 โดยฟรีดริช เอิร์นสท์ ดอร์น[9] และ ถูกตั้งชื่อจากการแผ่รังสีเรเดียม แต่เรดอนเพิ่งถูกจัดเป็นแก๊สมีตระกูลหลังปี ค.ศ. 1904 เมื่อคุณสมบัติต่าง ๆ ถูกค้นพบว่ามีลักษณะเหมือนกับแก๊สมีตระกูลอื่นๆ [10] เรย์ลี่และแรมซีย์ได้รับรางวัลโนเบล ประจำปี ค.ศ. 1904 ในสาขาฟิสิกส์และเคมี จากการค้นพบการมีอยู่ของแก๊สมีตระกูล[11][12] เจ. อี. เซเดอร์บลอม ประธานกลุ่มราชบัณฑิตยสภาวิทยาศาสตร์แห่งสวีเดน กล่าวไว้ว่า "การค้นพบกลุ่มของธาตุใหม่ทั้งหมด โดยที่ยังไม่มีธาตุใดเป็นต้นแบบของกลุ่มอยู่เลย นับเป็นสิ่งที่ยิ่งใหญ่และมีเอกลักษณ์มากในประวัติศาสตร์ของเคมีวิทยา สิ่งนี้จะเป็นความก้าวหน้าที่สำคัญต่อการค้นคว้า"[12]
การค้นคว้าเกี่ยวกับแก๊สมีตระกูลมีส่วนช่วยอย่างมากในการพัฒนาองค์ความรู้ด้านโครงสร้างอะตอม ในปี ค.ศ. 1895 นักเคมีวิทยาชาวฝรั่งเศส อองรี มอยส์ซานได้พยายามสร้างปฏิกิริยาเคมีระหว่างฟลูออรีนที่มีคุณสมบัติอิเล็กโตรเนกาทิวิตีสูง และอาร์กอน หนึ่งในแก๊สมีตระกูล แต่การทดลองกลับล้มเหลว การเตรียมสารประกอบอาร์กอนยังเป็นไปไม่ได้จนจบคริสต์ศตวรรษที่ 20 แต่การท้าทายความเป็นไปได้ดังกล่าวทำให้เกิดทฤษฎีของโครงสร้างอะตอมใหม่ ๆ ตามมา ด้วยความรู้จากการทดลองที่ผ่านมา เมื่อปี ค.ศ. 1913 นักฟิสิกส์ชาวเดนิช นิลส์ โปร์เสนอทฤษฎีโครงสร้างอะตอมว่า อิเล็กตรอนในอะตอมต่างถูกเรียงอยู่ภายในชั้นพลังงานรอบนิวเคลียส และธาตุทั้งหมดในแก๊สมีตระกูลยกเว้นฮีเลียม ล้วนมีอิเล็กตรอนในระดับพลังงานวงนอกครบ 8 อิเล็กตรอนเสมอ[13] ต่อมาในปี ค.ศ. 1916 กิลเบิร์ต เอ็น ลูอิสได้คิดค้นกฎออกเตตซึ่งสามารถสรุปได้ว่าการจับตัวครบแปดของอิเล็กตรอนในระดับพลังงานวงนอกเป็นการจัดเรียงตัวที่เสถียรที่สุดสำหรับอะตอมใดๆ โดยธาตุที่มีการจัดรูปแบบนี้จะไม่ตอบสนองต่อธาตุอื่น ๆ เนื่องจากไม่ต้องการอิเล็กตรอนมารวมในระดับพลังงานวงนอกอีกแล้ว[14]
ในปี ค.ศ. 1962 นักเคมี นีล บาร์ตเลตต์ค้นพบซีนอนเฮกซะฟลูออโรแพลทิเนต[15] สารประกอบของก๊าซมีตระกูลที่ถูกค้นพบเป็นครั้งแรก สารประกอบของแก๊สมีตระกูลชนิดอื่นถูกค้นพบในเวลาต่อมา เช่น สารประกอบของธาตุเรดอนอย่างเรดอนไดฟลูออไรด์ (RnF
2) [16] ถูกค้นพบในปี ค.ศ. 1962 จากรอยสารกัมมันตภาพรังสี สารประกอบของธาตุคริปทอนอย่างคริปทอนไดฟลูออไรด์ (KrF
2)[17]ถูกค้นพบในปี ค.ศ. 1963 ส่วนสารประกอบอาร์กอนตัวแรกที่เสถียรถูกบันทึกไว้ในปี ค.ศ. 2000 เมื่ออาร์กอนฟลูออโรไฮไดรด์ (HArF) เกิดการจับตัวที่อุณหภูมิ 40 เคลวิน (−233.2 องศาเซลเซียส; −387.7 องศาฟาเรนไฮต์)[18]
ในเดือนตุลาคม ปี ค.ศ. 2006 นักวิทยาศาสตร์จากสถาบันร่วมเพื่อการวิจัยนิวเคลียร์ และห้องปฏิบัติการแห่งชาติ ลอว์เรนซ์ ลิเวอร์มอร์สามารถสังเคราะห์โอกาเนสซอนซึ่งเป็นธาตุที่ 17 ในกลุ่มที่ 18 ของตารางธาตุ[19]ได้สำเร็จ ด้วยการรวมตัวของแคลิฟอร์เนียมกับแคลเซียม[20]
สมบัติทางกายภาพและอะตอม
| สมบัติ[13][21] | ฮีเลียม | นีออน | อาร์กอน | คริปทอน | ซีนอน | เรดอน | โอกาเนสซอน |
|---|---|---|---|---|---|---|---|
| ความหนาแน่น (g/dm3) | 0.1786 | 0.9002 | 1.7818 | 3.708 | 5.851 | 9.97 | 7200 (ค่าทำนาย)[22] |
| จุดเดือด (K) | 4.4 | 27.3 | 87.4 | 121.5 | 166.6 | 211.5 | 450±10 (ค่าทำนาย)[22] |
| จุดหลอมเหลว (K) | –[23] | 24.7 | 83.6 | 115.8 | 161.7 | 202.2 | 325±15 (ค่าทำนาย[22] |
| ความร้อนแฝงของการกลายเป็นไอ (kJ/mol) | 0.08 | 1.74 | 6.52 | 9.05 | 12.65 | 18.1 | – |
| การละลาย ในน้ำที่อุณหภูมิ 20 °C (cm3/kg) | 8.61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 | – |
| เลขอะตอม | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| รัศมีอะตอม (จากการคำนวณ) (pm) | 31 | 38 | 71 | 88 | 108 | 120 | – |
| พลังงานไอออไนเซชัน (kJ/mol) | 2372 | 2080 | 1520 | 1351 | 1170 | 1037 | 839 (ค่าทำนาย)[24] |
| อิเล็กโตรเนกาทิวิตี[25] | 4.16 | 4.79 | 3.24 | 2.97 | 2.58 | 2.60 | 2.59[26] |
สำหรับข้อมูลเพิ่มเติม ดูต่อที่ Noble gas (data page)
แก๊สมีตระกูลมีแรงระหว่างอะตอมที่อ่อน ส่งผลให้มีจุดเดือดและจุดหลอมเหลวที่ต่ำมาก แก๊สมีตระกูลเป็นแก๊สอะตอมเดี่ยวภายใต้ภาวะมาตรฐาน รวมถึงเป็นธาตุที่มีมวลอะตอมสูงกว่าธาตุที่เป็นของแข็งทั่วไป[27] ฮีเลียมมีปริมาณที่เป็นเอกลักษณ์กว่าธาตุอื่น โดยมีจุดเดือดที่ 1 บรรยากาศมาตรฐานต่ำกว่าสสารอื่น ฮีเลียมเป็นธาตุเดียวที่แสดงสมบัติของของไหลยวดยิ่งและเป็นธาตุเดียวที่ไม่สามารถทำให้เป็นของแข็งด้วยการลดอุณหภูมิที่ความดันบรรยากาศ[28] (ปรากฏการณ์นี้สามารถอธิบายด้วยกลศาสตร์ควอนตัมว่าพลังงานจุดศูนย์มากเกินไปที่จะเกิดการเยือกแข็ง)[29] – ต้องให้ความดัน 25 บรรยากาศมาตรฐาน (2,500 กิโลปาสกาล; 370 ปอนด์ต่อตารางนิ้ว) ที่อุณหภูมิ 0.95 เคลวิน (−272.200 องศาเซลเซียส; −457.960 องศาฟาเรนไฮต์) เพื่อเปลี่ยนให้ฮีเลียมเป็นของแข็ง[28] ในขณะที่ต้องใช้ความดันประมาณ 115 kbar สำหรับอุณหภูมิห้อง[30] แก๊สมีตระกูลจนถึงซีนอนมีไอโซโทปที่เสถียรหลายไอโซโทป เรดอนไม่มีไอโซโทปเสถียร โดยไอโซโทปที่คงตัวได้นานที่สุดคือ 222Rn ด้วยครึ่งชีวิต 3.8 วันและสลายเป็นฮีเลียมกับพอโลเนียม ซึ่งจะสลายต่อเป็นตะกั่ว จุดหลอมเหลวและจุดเดือดจะเพิ่มขึ้นไล่จากบนลงล่างของหมู่

อะตอมของแก๊สมีตระกูลเช่นเดียวกันกับอะตอมในหมู่ส่วนใหญ่ มีรัศมีอะตอมเพิ่มขึ้นอย่างต่อเนื่องจากคาบหนึ่งไปอีกคาบหนึ่งเนื่องจากการเพิ่มจำนวนของอิเล็กตรอน ขนาดของอะตอมสัมพันธ์กับสมบัติหลายประการ ตัวอย่างเช่นพลังงานไอออไนเซชันกลับกันกับรัศมีที่เพิ่มขึ้น เนื่องจากเวเลนซ์อิเล็กตรอนในแก๊สมีตระกูลที่ใหญ่กว่าจะห่างจากนิวเคลียสทำให้อิเล็กตรอนไม่ได้กระจุกตัวอย่างแน่นในอะตอมเท่ากับแก๊สมีตระกูลที่เล็กกว่า แก๊สมีตระกูลมีพลังงานไอออไนเซชันมากที่สุดเมื่อเทียบกับธาตุในคาบเดียวกัน ซึ่งแสดงให้เห็นถึงความเสถียรของการจัดเรียงอิเล็กตรอนและสัมพันธ์กับความไม่ว่องไวต่อปฏิกิริยาเคมี[31] แต่อย่างไรก็ตาม แก๊สมีตระกูลที่หนักบางธาตุมีพลังงานไอออไนเซชันน้อยพอที่จะเปรียบเทียบกับธาตุและโมเลกุลอื่น ข้อมูลเชิงลึกระบุว่าซีนอนมีพลังงานไอออไนเซชันเท่ากับโมเลกุลออกซิเจน ทำให้บาร์ทเล็ตพยายามออกซิไดส์ซีนอนด้วย platinum hexafluoride ซึ่งเป็นตัวออกซิไดซ์ที่แรงมากพอให้เกิดปฏิกิริยากับออกซิเจน[32] แก๊สมีตระกูลไม่สามารถรับอิเล็กตรอนจากแอนไอออน เนื่องจากมีสัมพรรคภาพอิเล็กตรอนน้อยกว่าศูนย์[33]
สมบัติทางกายภาพของแก๊สมีตระกูลถูกกำหนดโดยแรงแวนเดอร์วาลส์ระหว่างอะตอมที่อ่อน แรงดึงดูดเพิ่มขึ้นตามขนาดของอะตอมเนื่องจากการเพิ่มขึ้นของสภาพมีขั้วได้ และการลดลงของพลังงานไอออนไนเซชัน นั่นส่งผลให้เกิดแนวโน้มของค่าต่าง ๆ ไล่จากบนลงล่างตามธาตุหมู่ 18 โดยรัศมีอะตอมและแรงระหว่างอะตอมจะเพิ่มขึ้น ทำให้จุดเดือด จุดหลอมเหลว ความร้อนแฝงของการกลายเป็นไอและความสามารถในการละลาย ส่วนการเพิ่มขึ้นของความหนาแน่นเกิดจากการเพิ่มของมวลอะตอม[31]
แก๊สมีตระกูลมีสมบัติใกล้เคียงแก๊สอุดมคติภายใต้ภาวะมาตรฐาน แต่เมื่อพิจารณาค่าเบี่ยงเบนจากกฎของแก๊สอุดมคติจะนำไปสู่การศึกษาเกี่ยวกับแรงระหว่างโมเลกุล ศักย์เลนนาร์ด-โจนส์มักถูกใช้ในการจำลองปฏิสัมพันธ์ระหว่างโมเลกุล เป็นโมเดลที่เสนอใน ค.ศ. 1924 โดย John Lennard-Jones จากข้อมูลที่ทดลองกับอาร์บอนก่อนที่กลศาสตร์ควอนตัมจะให้เครื่องมือสำหรับการทำความเข้าใจเรื่องแรงระหว่าโมเลกุลด้วยหลัก first principles[34] การวิเคราะห์เชิงทฤษฎีของปฏิสัมพันธ์เหล่านี้สามารถทำได้ง่ายเพราะแก๊สมีตระกูลเป็นแก๊สอะตอมเดี่ยวและเป็นทรงกลม หมายความว่าปฏิสัมพันธ์ระหว่างอะตอมไม่ขึ้นกับทิศทางหรือมีสมบัติเป็นไอโซทรอปิก
สมบัติทางเคมี
ก๊าซมีตระกูลไม่มีสี ไม่มีกลิ่น ไม่มีรส และไม่ติดไฟภายใต้สภาวะมาตรฐาน[32] ครั้งหนึ่งพวกมันถูกระบุว่าเป็นหมู่ 0 ในตารางธาตุเพราะเชื่อว่าพวกมันมีวาเลนซ์เป็นศูนย์ ซึ่งหมายความว่าอะตอมของพวกมันไม่สามารถรวมตัวกับธาตุอื่นเพื่อสร้างสารประกอบได้ อย่างไรก็ตาม มีการค้นพบในภายหลังว่าบางชนิดก่อตัวเป็นสารประกอบ ทำให้ฉลากนี้เลิกใช้ไป[11]
การจัดเรียงอิเล็กตรอน
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
สารประกอบ
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การมีอยู่ธรรมชาติและการผลิต
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
การใช้ประโยชน์

แก๊สมีตระกูลมีจุดเดือดและจุดหลอมเหลวที่ต่ำมาก ซึ่งทำให้แก๊สเหล่านี้ใช้เป็นสารทำความเย็นในเชิงอติสีตศาสตร์ โดยเฉพาะฮีเลียมเหลว[35] ซึ่งเดือดที่ 4.2 เคลวิน (−268.95 องศาเซลเซียส; −452.11 องศาฟาเรนไฮต์) ถูกนำไปใช้สร้างแม่เหล็กตัวนำยิ่งยวด สำหรับการสร้างภาพด้วยเรโซแนนซ์แม่เหล็ก (MRI) และนิวเคลียร์แมกเนติกเรโซแนนซ์สเปกโทรสโกปี (NMR)[36] นีออนเหลวถึงแม้จะไม่สามารถลดอุณหภูมิจนเท่าฮีเลียมเหลว นีออนเหลวยังถูกใช้ในงานด้านอติสีตศาสตร์เนื่องจากมีวิสัยสามารถทำความเย็นมากกว่าฮีเลียมเหลว 40 เท่าและมากกว่าไฮโดรเจนเหลว 3 เท่า[37]
ฮีเลียมถูกใช้เป็นองค์ประกอบของแก๊สสำหรับหายใจแทนที่ไนโตรเจน เนื่องจากมีความสามารถในการละลายในของไหลต่ำโดยเฉพาะไขมัน แก๊สทั่วไปมักถูกดูดซึมโดยเลือดและเนื้อเยื่อภายใต้ความดันเช่นการดำน้ำลึก ทำให้เกิดภาวะเซื่องซึมเรียกว่าภาวะเมาไนโตรเจน[38] แต่ด้วยที่ฮีเลียมมีความสามารถในการละลายต่ำ ฮีเลียมจึงซึมเข้าเยื่อหุ้มเซลล์ได้น้อย เมื่อใช้ฮีเลียมเป็นส่วนผสมของแก๊สสำหรับหายใจเช่นใน trimix หรือ heliox จึงช่วยลดอาการเซื่องซึมของนักประดาน้ำภายใต้ความลึก[39] ความสามารถในการละลายของฮีเลียมที่น้อยมีประโยชน์ในการรักษาโรคลดความกดหรือ the bends[13][40] เมื่อมีปริมาณแก๊สละลายในร่างกายลดลงหมายความว่าจะเกิดฟองแก๊สจำนวนน้อยลงที่ความดันที่ต่ำลง นอกจากนี้อาร์กอนยังเป็นตัวเลือกที่ดีที่สุดสำหรับการดำน้ำลึกแบบ drysuit[41] และฮีเลียมยังใช้เป็นแก๊สเติมแกนของเตาปฏิกรณ์นิวเคลียร์

ตั้งแต่วินาศภัยฮินเดินบวร์คในปี ค.ศ. 1937[42] ฮีเลียมถูกใช้ทดแทนไฮโดรเจนสำหรับแก๊สลอยตัวในเรือเหาะและลูกโป่ง เนื่องจากความเบาและความไม่ติดไฟ แม้ว่าจะมีแรงลอยตัวลดลง 8.6%[43][13]
ในการประยุกต์ใช้ แก๊สมีตระกูลถูกใช้ในบรรยากาศเฉื่อย อาร์กอนถูกใช้ในการสังเคราะห์สารประกอบที่ไวต่ออากาศนั่นคือไวต่อไนโตรเจน อาร์กอนแข็งถูกใช้ในการศึกษาสารประกอบที่ไม่เสถียรมากเช่นสารมัธยันตร์ที่ไวต่อปฏิกิริยา โดยการกักในเมทริกซ์เฉื่อยที่อุณหภูมิต่ำมาก[44] ฮีเลียมถูกใช้เป็นตัวกลางนำพาในเทคนิคแก๊สโครมาโทกราฟี เป็นแก๊สเติมในเทอร์โมมิเตอร์และในอุปกรณ์ตรวจวัดการแผ่รังสีเช่นเครื่องนับไกเกอร์–มึลเลอร์และห้องฟอง[45] ฮีเลียมและอาร์กอนมักถูกใช้เป็นกำบังสำหรับการเชื่อมอาร์กและการกระจายของโลหะไร้สกุลในบรรยากาศขณะเชื่อมหรือตัดโลหะ รวมถึงกระบวนการทางโลหการและการผลิตซิลิคอนในอุตสาหกรรมสารกึ่งตัวนำ[37]

แก๊สมีตระกูลมักถูกใช้ในการจัดแสงเพราะมีความไวต่อปฏิกิริยาเคมีต่ำ อาร์กอนจะผสมกับไนโตรเจนใช้เติมในหลอดไส้ร้อนแบบธรรมดา[37] คริปทอนถูกใช้ในหลอดไฟประสิทธิภาพสูง ซึ่งให้อุณหภูมิสีและประสิทธิภาพสูงกว่า เนื่องจากสามารถลดอัตราการขาดของแกนหลอดไฟได้ดีกว่าอาร์กอน หลอดแฮโลเจนใช้คริปทอนประสมกับสารประกอบของไอโอดีนหรือโบรมีนปริมาณน้อย[37] แก๊สมีตระกูลเรืองแสงให้สีที่โดดเด่นเมื่อใช้ในหลอดแก๊สคายประจุเช่น หลอดไฟนีออน แม้ว่าหลอดไฟจะเรียกชื่อตามแก๊สนีออนแต่ก็ประกอบด้วยแก๊สชนิดอื่นและสารเรืองแสง ซึ่งทำให้เกิดเฉดสีหลากหลายได้เป็นสีส้มอมแดงของนีออน ซีนอนมักใช้ในหลอดไฟซีนอนอาร์ค เนื่องจากสเปกตรัมที่เกือบต่อเนื่องคล้ายกับแสงอาทิตย์ จึงมักประยุกต์ในเครื่องฉายภาพยนตร์และไฟหน้ารถ[37]
แก๊สมีตระกูลถูกใช้ในเอ็กไซเมอร์เลเซอร์ ซึ่งสร้างจากโมเลกุลที่ถูกกระตุ้นด้วยไฟฟ้าและคงสภาพในระยะเวลาสั้นเรียกว่าเอ็กไซเมอร์ โมเลกุลเอ็กไซเมอร์ที่ถูกใช้ในเลเซอร์อาจเป็นไดเมอร์ของแก๊สมีตระกูลเช่น Ar2, Kr2 หรือ Xe2 หรือที่นิยมใช้คือแก๊สมีตระกูลที่รวมตัวกับธาตุฮาโลเจนในรูปโมเลกุลเอ็กไซเมอร์เช่น ArF, KrF, XeF หรือ XeCl เลเซอร์เหล่านี้สร้างรังสีอัลตราไวโอเล็ต ซึ่งเนื่องจากความยาวคลื่นที่สั้น (193 นาโนเมตรสำหรับ ArF และ 248 นาโนเมตรสำหรับ KrF) ทำให้ใช้ในงานภาพถ่ายรังสีแม่นยำสูงได้ เอ็กไซเมอเลเซอร์ถูกใช้ในด้านอุตสาหกรรม การแพทย์และวิทยาศาสตร์อย่างหลากหลาย นอกจากนี้ยังใช้ในงานด้านไมโครลิโธกราฟีและด้านการสร้างชิ้นส่วนจุลภาค ซึ่งมีความสำคัญในการผลิตวงจรรวม และการผ่าตัดด้วยเลเซอร์ได้แก่การขยายหลอดเลือดด้วยเลเซอร์และการผ่าตัดตา[46]
แก๊สมีตระกูลบางชนิดมีการประยุกต์ใช้โดยตรงในทางการแพทย์ บางครั้งฮีเลียมจะถูกใช้ช่วยผู้ป่วยหอบหืดให้หายใจดีขึ้น[37] ซีนอนถูกใช้เป็นยาสลบเพราะความสามารถในการละลายในไขมันที่สูง ทำให้เกิดฤทธิ์มากกว่าไนตรัสออกไซด์ที่ใช้โดยทั่วไปและเนื่องจากมันถูกกำจัดจากร่างกายโดยทันที ทำให้ผู้ป่วยฟื้นตัวเร็วขึ้น[47] ซีนอนถูกประยุกต์ในการถ่ายภาพรังสีทางการแพทย์ของปอดด้วยเทคนิค hyperpolarized MRI[48] เรดอนซึ่งไวต่อปฏิกิริยามากและมีปริมาณน้อยถูกใช้ในการรังสีบำบัด[13]
แก๊สมีตระกูลโดยเฉพาะซีนอนถูกใช้มากในเครื่องยนต์ไอออนเนื่องจากความเฉื่อยของมัน เนื่องจากเครื่องยนต์ไอออนไม่ได้ขับเคลื่อนด้วยปฏิกิริยาเคมี เชื้อเพลิงที่เฉื่อยเชิงเคมีถูกใช้ป้องกันการเกิดปฏิกิริยาที่ไม่พึงประสงค์ระหว่างเชื้อเพลิงรวมถึงสิ่งอื่นในเครื่องยนต์
โอกาเนสซอนไม่เสถียรเกินไปทำให้ไม่สามารถประยุกต์ใช้ได้นอกจากใช้ในการวิจัย
สีในหลอดไฟ
ส่วนนี้รอเพิ่มเติมข้อมูล คุณสามารถช่วยเพิ่มข้อมูลส่วนนี้ได้ |
ดูเพิ่ม
เชิงอรรถ
- ↑ Bauzá, Antonio; Frontera, Antonio (2015). "Aerogen Bonding Interaction: A New Supramolecular Force?". Angewandte Chemie International Edition. 54 (25): 7340–3. doi:10.1002/anie.201502571. PMID 25950423.
- ↑ Renouf, Edward (1901). "Noble gases". Science. 13 (320): 268–270. Bibcode:1901Sci....13..268R. doi:10.1126/science.13.320.268. S2CID 34534533.
- ↑ Ozima 2002, p. 30
- ↑ Ozima 2002, p. 4
- ↑ "argon". Encyclopædia Britannica. 2008.
- ↑ Oxford English Dictionary (1989), s.v. "helium". Retrieved 16 December 2006, from Oxford English Dictionary Online. Also, from quotation there: Thomson, W. (1872). Rep. Brit. Assoc. xcix: "Frankland and Lockyer find the yellow prominences to give a very decided bright line not far from D, but hitherto not identified with any terrestrial flame. It seems to indicate a new substance, which they propose to call Helium."
- ↑ 7.0 7.1 Ozima 2002, p. 1
- ↑ Mendeleev 1903, p. 497
- ↑ Partington, J. R. (1957). "Discovery of Radon". Nature. 179 (4566): 912. Bibcode:1957Natur.179..912P. doi:10.1038/179912a0. S2CID 4251991.
- ↑ "Noble Gas". Encyclopædia Britannica. 2008.
- ↑ Cederblom, J. E. (1904). "The Nobel Prize in Physics 1904 Presentation Speech".
- ↑ 12.0 12.1 Cederblom, J. E. (1904). "The Nobel Prize in Chemistry 1904 Presentation Speech".
- ↑ 13.0 13.1 13.2 13.3 13.4 "Noble Gas". Encyclopædia Britannica. 2008.
- ↑ Gillespie, R. J.; Robinson, E. A. (2007). "Gilbert N. Lewis and the chemical bond: the electron pair and the octet rule from 1916 to the present day". J Comput Chem. 28 (1): 87–97. doi:10.1002/jcc.20545. PMID 17109437.
- ↑ Bartlett, N. (1962). "Xenon hexafluoroplatinate Xe+[PtF6]−". Proceedings of the Chemical Society (6): 218. doi:10.1039/PS9620000197.
- ↑ Fields, Paul R.; Stein, Lawrence; Zirin, Moshe H. (1962). "Radon Fluoride". Journal of the American Chemical Society. 84 (21): 4164–4165. doi:10.1021/ja00880a048.
- ↑ Grosse, A. V.; Kirschenbaum, A. D.; Streng, A. G.; Streng, L. V. (1963). "Krypton Tetrafluoride: Preparation and Some Properties". Science. 139 (3559): 1047–1048. Bibcode:1963Sci...139.1047G. doi:10.1126/science.139.3559.1047. PMID 17812982.
- ↑ Khriachtchev, Leonid; Pettersson, Mika; Runeberg, Nino; Lundell, Jan; Räsänen, Markku (2000). "A stable argon compound". Nature. 406 (6798): 874–876. Bibcode:2000Natur.406..874K. doi:10.1038/35022551. PMID 10972285. S2CID 4382128.
- ↑ Barber, Robert C.; Karol, Paul J.; Nakahara, Hiromichi; Vardaci, Emanuele & Vogt, Erich W. (2011). "Discovery of the elements with atomic numbers greater than or equal to 113 (IUPAC Technical Report)*" (PDF). Pure Appl. Chem. IUPAC. 83 (7). doi:10.1515/ci.2011.33.5.25b. สืบค้นเมื่อ 30 May 2014.
- ↑ Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; Abdullin, F.; Polyakov, A.; และคณะ (2006). "Synthesis of the isotopes of elements 118 and 116". Physical Review C. 74 (4): 44602. Bibcode:2006PhRvC..74d4602O. doi:10.1103/PhysRevC.74.044602.
- ↑ Greenwood 1997, p. 891
- ↑ 22.0 22.1 22.2 Smits, Odile; Mewes, Jan-Michael; Jerabek, Paul; Schwerdtfeger, Peter (2020). "Oganesson: A Noble Gas Element That Is Neither Noble Nor a Gas". Angew. Chem. Int. Ed. 59 (52): 23636–23640. doi:10.1002/anie.202011976. PMC 7814676. PMID 32959952.
- ↑ Liquid helium will only solidify if exposed to pressures well above atmospheric pressure, an effect explainable with quantum mechanics
- ↑ Winter, Mark (2020). "Organesson: Properties of Free Atoms". WebElements: THE periodic table on the WWW. สืบค้นเมื่อ 30 December 2020.
- ↑ Allen, Leland C. (1989). "Electronegativity is the average one-electron energy of the valence-shell electrons in ground-state free atoms". Journal of the American Chemical Society. 111 (25): 9003–9014. doi:10.1021/ja00207a003.
- ↑ Tantardini,Christian; Oganov, Artem R. (2021). "Thermochemical Electronegativities of the Elements". Nature Communications. 12 (1): 2087–2095. Bibcode:2021NatCo..12.2087T. doi:10.1038/s41467-021-22429-0. PMC 8027013. PMID 33828104.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ "Noble Gas". Encyclopædia Britannica. 2008.
- ↑ 28.0 28.1 Wilks, John (1967). "Introduction". The Properties of Liquid and Solid Helium. Oxford: Clarendon Press. ISBN 978-0-19-851245-5.
- ↑ "John Beamish's Research on Solid Helium". Department of Physics, University of Alberta. 2008. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 31 May 2008.
- ↑ Pinceaux, J.-P.; Maury, J.-P.; Besson, J.-M. (1979). "Solidification of helium, at room temperature under high pressure" (PDF). Journal de Physique Lettres. 40 (13): 307–308. doi:10.1051/jphyslet:019790040013030700. S2CID 40164915.
- ↑ 31.0 31.1 Greenwood 1997, p. 891
- ↑ Bartlett, N. (1962). "Xenon hexafluoroplatinate Xe+[PtF6]−". Proceedings of the Chemical Society (6): 218. doi:10.1039/PS9620000197.
- ↑ Wheeler, John C. (1997). "Electron Affinities of the Alkaline Earth Metals and the Sign Convention for Electron Affinity". Journal of Chemical Education. 74 (1): 123–127. Bibcode:1997JChEd..74..123W. doi:10.1021/ed074p123.; Kalcher, Josef; Sax, Alexander F. (1994). "Gas Phase Stabilities of Small Anions: Theory and Experiment in Cooperation". Chemical Reviews. 94 (8): 2291–2318. doi:10.1021/cr00032a004.
- ↑ Mott, N. F. (1955). "John Edward Lennard-Jones. 1894–1954". Biographical Memoirs of Fellows of the Royal Society. 1: 175–184. doi:10.1098/rsbm.1955.0013.
- ↑ "Neon". Encarta. 2008.
- ↑ Zhang, C. J.; Zhou, X. T.; Yang, L. (1992). "Demountable coaxial gas-cooled current leads for MRI superconducting magnets". IEEE Transactions on Magnetics. IEEE. 28 (1): 957–959. Bibcode:1992ITM....28..957Z. doi:10.1109/20.120038.
- ↑ 37.0 37.1 37.2 37.3 37.4 37.5 Häussinger, Peter; Glatthaar, Reinhard; Rhode, Wilhelm; Kick, Helmut; Benkmann, Christian; Weber, Josef; Wunschel, Hans-Jörg; Stenke, Viktor; Leicht, Edith; Stenger, Hermann (2002). "Noble gases". Ullmann's Encyclopedia of Industrial Chemistry. Wiley. doi:10.1002/14356007.a17_485. ISBN 3-527-30673-0.
- ↑ Fowler, B.; Ackles, K. N.; Porlier, G. (1985). "Effects of inert gas narcosis on behavior—a critical review". Undersea Biomed. Res. 12 (4): 369–402. ISSN 0093-5387. OCLC 2068005. PMID 4082343. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 25 December 2010. สืบค้นเมื่อ 8 April 2008.
{{cite journal}}: CS1 maint: unfit URL (ลิงก์) - ↑ Bennett 1998, p. 176
- ↑ Vann, R. D., บ.ก. (1989). "The Physiological Basis of Decompression". 38th Undersea and Hyperbaric Medical Society Workshop. 75(Phys)6-1-89: 437. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 7 October 2008. สืบค้นเมื่อ 31 May 2008.
{{cite journal}}: CS1 maint: unfit URL (ลิงก์) - ↑ Maiken, Eric (1 August 2004). "Why Argon?". Decompression. สืบค้นเมื่อ 26 June 2008.
- ↑ "Disaster Ascribed to Gas by Experts". The New York Times. 7 May 1937. p. 1.
- ↑ Freudenrich, Craig (2008). "How Blimps Work". HowStuffWorks. สืบค้นเมื่อ 3 July 2008.
- ↑ Dunkin, I. R. (1980). "The matrix isolation technique and its application to organic chemistry". Chem. Soc. Rev. 9: 1–23. doi:10.1039/CS9800900001.
- ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อkirk - ↑ Basting, Dirk; Marowsky, Gerd (2005). Excimer Laser Technology. Springer. ISBN 3-540-20056-8.
- ↑ Sanders, Robert D.; Ma, Daqing; Maze, Mervyn (2005). "Xenon: elemental anaesthesia in clinical practice". British Medical Bulletin. 71 (1): 115–135. doi:10.1093/bmb/ldh034. PMID 15728132.
- ↑ Albert, M. S.; Balamore, D. (1998). "Development of hyperpolarized noble gas MRI". Nuclear Instruments and Methods in Physics Research A. 402 (2–3): 441–453. Bibcode:1998NIMPA.402..441A. doi:10.1016/S0168-9002(97)00888-7. PMID 11543065.
บรรณานุกรม
| แหล่งข้อมูลห้องสมุดเกี่ยวกับ Noble gas |
- Bennett, Peter B.; Elliott, David H. (1998). The Physiology and Medicine of Diving. SPCK Publishing. ISBN 0-7020-2410-4.
- Bobrow Test Preparation Services (5 December 2007). CliffsAP Chemistry. CliffsNotes. ISBN 978-0-470-13500-6.
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd ed.). Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Harding, Charlie J.; Janes, Rob (2002). Elements of the P Block. Royal Society of Chemistry. ISBN 0-85404-690-9.
- Holloway, John H. (1968). Noble-Gas Chemistry. London: Methuen Publishing. ISBN 0-412-21100-9.
- Mendeleev, D. (1902–1903). Osnovy Khimii (The Principles of Chemistry) (ภาษารัสเซีย) (7th ed.). New York, Collier.
- Ozima, Minoru; Podosek, Frank A. (2002). Noble Gas Geochemistry. Cambridge University Press. ISBN 0-521-80366-7.
- Weinhold, F.; Landis, C. (2005). Valency and bonding. Cambridge University Press. ISBN 0-521-83128-8.





