เซลล์เซอร์โตลี
| เซลล์เซอร์โตลี | |
|---|---|
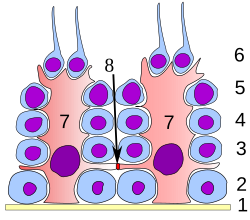 เยื่อบุผิวต้นกำเนิดของอัณฑะ 1: เบซาลลามินา 2: สเปอร์มาโทโกเนีย 3: สเปอร์มาโทไซต์ลำดับที่ 1 4: สเปอร์มาโทไซต์ลำดับที่ 2 5: สเปอร์มาทิด 6: สเปอร์มาทิดที่สมบูรณ์ 7: เซลล์เซอร์โตลี 8: ไทต์จังก์ชัน (ตัวกั้นเลือด–อัณฑะ) | |
 ภาพมิญชวิทยาของพาเรงไคมาอัณฑะของหมูป่า 1 ช่องภายในหลอดของส่วนขดของหลอดสร้างอสุจิ 2 สเปอร์มาทิด 3 สเปอร์มาโทไซต์ 4 เซลล์ต้นกำเนิดตัวอสุจิ 5 เซลล์เซอร์โตลี 6 ไมโอไฟโบรบลาสท์ 7 เซลล์ไลดิชs 8 หลอดเลือดฝอย | |
| รายละเอียด | |
| ระบบ | ระบบสืบพันธุ์ |
| ที่ตั้ง | อัณฑะ |
| หน้าที่ | ช่วยในการสร้างตัวอสุจิ |
| ตัวระบุ | |
| MeSH | D012708 |
| FMA | 72298 |
| ศัพท์ทางกายวิภาคของจุลกายวิภาคศาสตร์ | |
เซลล์เซอร์โตลี (เซลล์พยุงประเภทหนึ่ง) เป็นเซลล์ "พยาบาล" ของอัณฑะที่เป็นส่วนหนึ่งของหลอดสร้างอสุจิ และช่วยในกระบวนการการสร้างสเปิร์มซึ่งเป็นกระบวนการสร้างตัวอสุจิ
เซลล์นี้จะถูกปลุกฤทธิ์ขึ้นโดยฮอร์โมนกระตุ้นต่อมน้อย (FSH) ซึ่งหลั่งออกมาโดยต่อมใต้สมองส่วนหน้า โดยเซลล์เซอร์โตลีนั้นมีตัวรับ FSH อยู่บนเยื่อหุ้มเซลล์ และพบเฉพาะอยู่ในหลอดขดของหลอดสร้างอสุจิ (เนื่องจากเป็นเพียงจุดเดียวในอัณฑะที่มีการสร้างตัวอสุจิขึ้น) การพัฒนาขึ้นของเซลล์เซอร์โตลีนั้นถูกควบคุมโดยโปรตีนสารกำหนดอัณฑะ
โครงสร้าง
[แก้]เซลล์เซอร์โตลีอยู่บนหลอดสร้างอสุจิ
บนสไลด์ การใช้การย้อมสีมาตรฐานอาจทำให้เกิดความสับสนระหว่างเซลล์เซอร์โตลีกับเซลล์อื่นของเยื่อบุผิวต้นกำเนิดได้ ลักษณะที่โดดเด่นที่สุดของเซลล์เซอร์โตลี คือ นิวคลีโอลัสที่มีความทึบ[1][2]
การพัฒนา
[แก้]เซลล์เซอร์โตลีมีความจำเป็นต่อการพัฒนาทางเพศของเพศชาย ในระหว่างการพัฒนาของเพศชาย ยีน SRY จะไปปลุกฤทธิ์ SOX9 ขึ้น ซึ่งจากนั้นมันจะไปปลุกฤทธิ์และสร้างวงวนการป้อนด้วย FGF9 โดยเซลล์เซอร์โตลีจะเพิ่มจำนวนและเปลี่ยนสภาพโดยการกระตุ้นจาก FGF9 เป็นหลัก[3] การขาด FGF9 จะทำให้มีแนวโน้มเป็นสาเหตุให้ลักษณะเพศหญิงพัฒนาขึ้น[4]
เมื่อเปลี่ยนสภาพอย่างสมบูรณ์แล้ว เซลล์เซอร์โตลีจะถือได้ว่าได้เปลี่ยนสภาพขั้นสุดท้ายไปแล้ว และจะไม่สามารถเพิ่มจำนวนขึ้นได้อีก[5] ดังนั้น เมื่อการสร้างตัวอสุจิเริ่มต้นขึ้นแล้ว จะไม่มีการสร้างเซลล์เซอร์โตลีขึ้นอีก
อย่างไรก็ตาม เมื่อไม่นานมานี้ นักวิทยาศาสตร์บางคนได้ค้นพบวิธีในการชักนำให้เซลล์เซอร์โตลีกลายเป็นฟีโนไทป์ที่เพิ่มจำนวนได้สมัยวัยเด็ก (juvenile proliferative phenotype) ด้านนอกร่างกาย[6] สิ่งนี้ทำให้มีความเป็นไปได้ในการแก้ไขข้อบกพร่องบางประการ ที่อาจเป็นสาเหตุของความเป็นหมันในเพศชาย
มีการแนะนำว่าเซลล์เซอร์โตลีอาจเจริญมาจากมีโซเนโฟรมาของทารกในครรภ์[7]
หน้าที่
[แก้]เนื่องจากหน้าที่หลักของเซลล์นี้คือการเลี้ยงเซลล์อสุจิที่กำลังพัฒนาขึ้นผ่านระยะของการสร้างสเปิร์ม เซลล์เซอร์โตลีจึงยังถูกเรียกว่าเซลล์ "แม่" หรือเซลล์ "พยาบาล" ด้วย[8] เซลล์เซอร์โตลียังทำหน้าที่เป็นเซลล์กลืนกิน ซึ่งจะทำหน้าที่กินไซโทพลาซึมที่ตกค้างระหว่างการสร้างอสุจิ การเคลื่อนย้ายเซลล์จากฐานของช่องภายในหลอดของหลอดสร้างอสุจิ ซึ่งเกิดขึ้นจากการเปลี่ยนแปลงทางโครงสร้างในขอบด้านข้างของเซลล์เซอร์โตลี
สิ่งคัดหลั่ง
[แก้]เซลล์เซอร์โตลีจะหลั่งสารดังต่อไปนี้
- ฮอร์โมนต้านมึลเลอร์ (anti-Müllerian hormone; AMH) — หลั่งออกมาในช่วงระยะแรกของชีวิตทารกในครรภ์
- แอคติวินและอินฮิบิน — หลั่งออกมาหลังจากวัยเริ่มเจริญพันธุ์ ทำงานร่วมกันเพื่อควบคุมการหลั่งฮอร์โมนกระตุ้นต่อมน้อย
- โปรตีนจับฮอร์โมนเพศชาย (หรืออาจเรียกว่า โกลบูลินจับเทสโทสเตอโรน) — เพิ่มความเข้มข้นของฮอร์โมนเทสโทสเตอโรนในหลอดสร้างอสุจิเพื่อกระตุ้นการสร้างตัวอสุจิได้เล็กน้อย
- เอสตราดิออล (estradiol) — อะโรมาเทสจากเซลล์เซอร์โทลี ทำหน้าที่แปลงเทสโทสเตอโรนเป็น 17 เบตา เอสตราดิออล เพื่อให้เกิดการสร้างสเปิร์มได้โดยตรง
- โมเลกุลเกี่ยวข้องกับอีทีเอส (ETS Related Molecule หรือ ERM) สารถอดรหัสอีทีเอสแวเรียนต์ 5 ซึ่งมีความจำเป็นสำหรับการบำรุงรักษาเซลล์ต้นกำเนิดในอัณฑะผู้ใหญ่
- ทรานสเฟอร์ริน (transferrin) — โปรตีนในน้ำเลือดสำหรับการขนส่งไอออนเหล็ก[9]
- เซอรูโลพลาสมินของอัณฑะ (Testicular ceruloplasmin) — โปรตีนคล้ายเซอรูโลพลาสมิน ซึ่งมีภูมิคุ้มกันคล้ายกับเซอรูโลพลาสมิน[10]
โครงสร้าง
[แก้]จังก์ชันที่บดบังเซลล์เซอร์โตลีนั้นก่อตัวขึ้นเป็นตัวกั้นเลือด–อัณฑะ ซึ่งเป็นโครงสร้างที่แบ่งส่วนเลือดแทรกของอัณฑะออกจากส่วนที่อยู่ติดช่องภายในหลอดของหลอดสร้างอสุจิ เนื่องจากการพัฒนาขึ้นไปทางยอดของสเปอร์มาโทโกเนีย (เซลล์ต้นกำเนิดตัวอสุจิ) จังก์ชันที่บดบังจึงต้องได้รับการดัดแปลงและแตกออกแบบไดนามิก เพื่อให้สเปอร์มาโทโกเนียที่มีภูมิคุ้มกันเจาะจง (immunoidentical spermatogonia) สามารถข้ามผ่านตัวกั้นเลือด–อัณฑะได้ ทั้งนี้เพื่อให้เซลล์เหล่านั้นมีภูมิคุ้มกันเฉพาะตัว เซลล์เซอร์โตลีจะควบคุมการเข้าและออกของสารอาหาร ฮอร์โมน และ สารเคมีอื่น ๆ จากกลีบย่อยของอัณฑะ รวมทั้งทำให้ส่วนที่ติดกับช่องภายในหลอดเป็นบริเวณพิเศษทางภูมิคุ้มกันด้วย
นอกจากนี้ เซลล์เซอร์โตลียังมีหน้าที่ในการสร้างและรักษาโพรงของเซลล์ต้นกำเนิดสเปอร์มาโทโกเนียด้วย ซึ่งจะทำให้แน่ใจว่ามีการเกิดใหม่ของเซลล์ต้นกำเนิดและการเปลี่ยนสภาพของสเปอร์มาโทโกเนียไปเป็นเซลล์ต้นกำเนิดที่เจริญเติมที่ ที่จะเจริญต่อไปในกระบวนการอันยาวนานของการสร้างอสุจิ ซึ่งจะสิ้นสุดลงด้วยการปล่อยสเปอร์มาโทซัวหรือตัวอสุจิออกมา ซึ่งนี่เป็นกระบวนการการสร้างสเปิร์ม[11] เซลล์เซอร์โตลีจะจับกับเซลล์สเปอร์มาโทโกเนียผ่าน CDH2 และกาแลกโทซิลทรานสเฟอเรส (ผ่านคาร์โบไฮเดรตที่ตกค้างอยู่)
หน้าที่อื่น
[แก้]ในระหว่างระยะการเจริญเต็มที่ของการสร้างสเปิร์ม เซลล์เซอร์โตลีจะกินส่วนที่ไม่จำเป็นสำหรับสเปอร์มาโทซัว
การซ่อมแซมดีเอ็นเอและการกลายพันธุ์
[แก้]เซลล์เซอร์โตลีมีความสามารถในการซ่อมแซมความเสียหายของดีเอ็นเอได้[12] การซ่อมแซมนี้น่าจะใช้กระบวนการการเชื่อมปลายที่ไม่ใช่คู่เหมือนที่เกี่ยวข้องกับโปรตีน XRCC1 และ PARP1 ซึ่งปรากฏอยู่ในเซลล์เซอร์โตลี[12]
เซลล์เซอร์โตลีมีความถี่ในการกลายพันธุ์มากกว่าเซลล์สร้างอสุจิ[13] เมื่อเทียบกับสเปอร์มาโทไซต์ เซลล์เซอร์โตลีจะมีความถี่ในการกลายพันธุ์สูงกว่า 5 ถึง 10 เท่า ซึ่งอาจสะท้อนถึงความจำเป็นในการซ่อมแซมดีเอ็นเอ และการเลี่ยงการกลายพันธุ์ได้อย่างมีประสิทธิภาพมากกว่าในเซลล์ร่างกาย
คุณสมบัติปรับปรุงภูมิคุ้มกันของเซลล์เซอร์โตลี
[แก้]นอกจากการปรากฏของสารที่มีความสำคัญต่อการเจริญเติบโตของเซลล์อสุจิแล้ว เซลล์เซอร์โตลียังสร้างโมเลกุลขึ้นหลายประเภท (ไม่ว่าจะบนพื้นผิวหรือสารละลายของเซลล์) ซี่งสามารถปรับปรุงระบบภูมิคุ้มกันได้ ความสามารถของเซลล์เซอร์โตลีในการเปลี่ยนแปลงการตอบสนองภูมิคุ้มกันในกลีบย่อยนั้น มีความจำเป็นอย่างยิ่งสำหรับการเจริญเติบโตของเซลล์อสุจิที่ประสบความสำเร็จ โดยเซลล์อสุจิจะแสดงนีโอเอพิโทป (neoepitopes) บนพื้นผิวของเซลล์ในระยะต่าง ๆ ของเจริญเติบโต พวกมันสามารถกระตุ้นการตอบสนองทางภูมิคุ้มกันที่รุนแรงได้ หากอยู่ในตำแหน่งอื่นของร่างกาย
โมเลกุลที่ผลิตโดยเซลล์เซอร์โตลีที่เกี่ยวข้องกับการกดภูมิคุ้มกันหรือการควบคุมภูมิคุ้มกัน
[แก้]ระบบ FAS/FAS-L – การปรากฏของฟาสลิแกนด์ (Fas-L) บนพื้นผิวของเซลล์เซอร์โตลีจะไปกระตุ้นการตายจากการอะพอพโทซิสของตัวรับฟาส เช่น ทีเซลล์ที่เป็นพิษต่อเซลล์[14]
- FasL ละลายน้ำได้- เพิ่มประสิทธิภาพของระบบ
- Fas ละลายน้ำได้- การปิดกั้น FasL บนพื้นผิวของเซลล์อื่น (ไม่มีการชักนำการอะพอพโทซิสในเซลล์เซอร์โตลีโดยเซลล์ต่าง ๆ ของระบบภูมิคุ้มกัน)
B7/H1 – ลดการเพิ่มจำนวนของเซลล์ทีเอฟเฟคเตอร์[15]
Jagged1 (JAG1) – การชักนำการแสดงสารการถอดรหัส Foxp3 ในเซลล์ที (การเพิ่มของจำนวนสัมพัทธ์ของเซลล์ทีควบคุม)[16]
โปรตีเอสอินฮิบิเตอร์-9 (PI-9) – สมาชิกของอินฮิบิเตอร์ในตระกูลเซอร์พิน (ซีรีนโปรตีเอสอินฮิบิเตอร์)[17]
- การกระตุ้นการหลั่งโปรตีเอสแกรนไซม์ บี, เซลล์ทีที่เป็นพิษต่อเซลล์ และ เซลล์เอ็นเค สามารถกระตุ้นการอะพอพโทซิสในเซลล์เป้าหมาย โดยเซลล์เซอร์โตลีจะสร้าง PI-9 ที่เข้าจับกับแกรนไซม์ บี และอินฮิบิเตอร์ของมันแบบย้อนกลับไม่ได้
สารก่อภูมิต้านทาน CD59 - โมเลกุลบนพื้นผิวของเซลล์เซอร์โตลี เป็นสมาชิกของโปรตีนควบคุมคอมพลิเมนต์ (CRP)
- การยับยั้งขั้นตอนสุดท้ายของลำดับคอมพลิเมนต์ – การก่อตัวของกลุ่มรวมการโจมตีเยื่อบุ[18]
คลัสเตอริน (Clusterin) – โมเลกุลที่ละลายน้ำได้ ทำหน้าที่คล้ายกับ CD59 ทำให้เกิดการรวมกลุ่มด้วยแกรนไซม์ บี และยับยั้งการกระตุ้นการอะพอสโทซิสโดยเซลล์เม็ดเลือดขาวทีหรือเซลล์เอ็นเค[18]
ทีจีเอฟ-เบตา – การเปลี่ยนแปลงสารการเจริญเติบโตเบตา (การผลิตขึ้นโดยตรงจากเซลล์เซอร์โตลียังคงเป็นที่ถกเถียง)
- เหนี่ยวนำการควบคุมเซลล์ทีในส่วนรอบนอก[19]
โมเลกุลอื่นที่เกี่ยวข้อง
[แก้]CD40 - โมเลกุลที่เกี่ยวข้องกับเซลล์เดนไดรต์
- เซลล์เซอร์โตลีสามารถควบคุมการปรากฏของ CD40 บนพื้นผิวของเซลล์เดนไดรต์ได้ (ไม่ทราบกลไก)
- การปรับลดของ CD40 เป็นผลให้ความสามารถของเซลล์เดนไดรต์ในการกระตุ้นการตอบสนองของเซลล์ทีลดลง[18]
เซลล์เซอร์โตลียังสามารถยับยั้งการเคลื่อนย้ายของเซลล์ภูมิคุ้มกันด้วย – ทำให้มีการแทรกของเซลล์ภูมิคุ้มกันไปยังจุดที่มีการอักเสบลดลง
นัยสำคัญทางคลินิก
[แก้]เนื้องอกเซลล์ไลดิช-เซอร์โตลีเป็นส่วนหนึ่งของเนื้องอกส่วนพยุงต่อมบ่งเพศ–สายเพศในกลุ่มของมะเร็งรังไข่ เนื้องอกเหล่านี้จะสร้างทั้งเซลล์เซอร์โตลีและเซลล์ไลดิช นำไปสู่การเพิ่มขึ้นของฮอร์โมนเทสโทสเตอโรนในรังไข่และอัณฑะ
สัตว์อื่น
[แก้]หน้าที่ของเซลล์เซอร์โตลีในแอมนิโอตาและแอนแอมนิโอตานั้นเหมือนกัน แต่เมื่อเปรียบเทียบกับแล้วจะมีคุณสมบัติแตกต่างกันเล็กน้อย โดยแอนแอมนิโอตา (พวกปลาและสัตว์สะเทินน้ำสะเทินบก) จะใช้การสร้างสเปิร์มถุงเพื่อสร้างเซลล์อสุจิ[20] ส่วนแอมนิโอตา เซลล์เซอร์โตลีจะถือว่าเป็นเซลล์ที่มีการเปลี่ยนสภาพเป็นขั้นสุดท้าย และไม่สามารถเพิ่มจำนวนได้ โดยในเซลล์เซอร์โตลีของแอนแอมนิโอตาจะผ่านขั้นตอนสองขั้นตอนในการเพิ่มจำนวน ขั้นแรกของการเพิ่มจำนวนจะเกิดขึ้นในระหว่างสร้างถุง ซึ่งทำให้มีการย้ายเซลล์สืบพันธุ์เข้าไป[21][22] ขั้นสองคือการขยายของถุงและการสร้างพื้นที่สำหรับการเพิ่มจำนวนของเซลล์สืบพันธุ์[23]
ข้อเท็จจริงที่ยอมรับกันโดยทั่วไปว่าเซลล์เซอร์โตลีเป็นการเปลี่ยนสภาพขั้นสุดท้ายเพิ่งจะมีการเปลี่ยนแปลง เนื่องจากภายหลังการปลูกถ่ายซีโนจีนิก เซลล์เซอร์โตลีจะสามารถเพิ่มจำนวนได้[24]
ประวัติ
[แก้]เซลล์เซอร์โตลีตั้งชื่อตาม เอนริโก เซอร์โตลี นักสรีรวิทยาชาวอิตาลี ซึ่งเป็นผู้ค้นพบเซลล์ขี้ในระหว่างการศึกษาด้านแพทย์ศาสตร์ในมหาวิทยาลัยปาเวีย[25]
เขาตีพิมพ์คำอธิบายของเซลล์ขี้ในปี ค.ศ. 1865 ซึ่งเซอร์โตลีพบเซลล์นี้ด้วยกล้องจุลทรรศน์เบธเล ซึ่งเขาซื้นในปี ค.ศ. 1862 ขณะเรียนแพทย์
ในการตีพิมพ์เมื่อปี ค.ศ. 1865 คำอธิบายแรกของเขาใช้คำว่า "เซลล์คล้ายต้นไม้" หรือ "เซลล์ที่มีลักษณะเป็นเส้น" และที่สำคัญที่สุด เขาเรียกสิ่งนี้ว่า "เซลล์แม่" ต่อมานักวิทยาศาสตร์คนอื่นจึงได้ใช้นามสกุลของเอนริโกเป็นชื่อของเซลล์นี้ซึ่งเริ่มต้นในปี ค.ศ. 1888 โดย ณ ค.ศ. 2006 มีหนังสือเรียนสองเล่มที่ถูกแต่งขึ้นมาโดยเฉพาะสำหรับเซลล์เซอร์โตลี
การวิจัย
[แก้]ในปี ค.ศ. 2016 แบบจำลองโรคการอักเสบของภาวะภูมิต้านตนเอง รวมไปถึง เบาหวาน ได้กระตุ้นให้เซลล์เซอร์โตลีสามารถปลูกถ่ายได้ เนื่องจากสมบัติการกดภูมิคุ้มกันและการต้านการอักเสบ[26]
การวิจัยนำเซลล์เซอร์โตลีมาใช้ในการรักษาเบาหวานชนิดที่ 1 โดยขณะนี้อยู่ในขั้นตอนที่ลึกที่สุด ซึ่งมีกลยุทธ์คือการปลูกถ่ายร่วมกันของเซลล์เบตาและเซลล์เซอร์โตลีไปสู่ผู้รับ ในกรณีของหนูตัวผู้ หนูและรวมถึงมนุษย์ การปรากฏของเซลล์เหล่านี้ซึ่งเก็บกลูโคสในภาวะสมดุลไปพร้อมกับความต้องการอินซูลินภายนอกที่ต่ำ ซึ่งในทุกกรณีนั้นไม่มีการใช้ยากดภูมิ ทำให้บทบาทของยานี้ถูกนำไปใช้และจัดหาโดยเซลล์เซอร์โตลี[27][28][29]
จีโอวานนี และคณะ ได้รักษาหนูที่เป็นเบาหวานและโรคอ้วนตามธรรมชาติ โดยการปลูกถ่ายเซลล์เซอร์โตลีที่ถูกหุ้มด้วยแคปซูลเข้าไปยังพืดไขมันหน้าท้อง[26] โดยแสดงให้เห็นว่า มากกว่าครึ่งของหนูที่ได้รับการรักษามีระดับน้ำตาลในเลือดที่ดีขึ้น งานทางวิทยาศาสตร์ล่าสุดยังให้คำมั่นว่าจะรักษาผู้ป่วยเบาหวานชนิดที่ 2ให้ดีขึ้นผ่านการใช้เซลล์บำบัดในอนาคตด้วย
เซลล์เซอร์โตลีส่งเสริมการยอมรับการปลูกถ่ายผิวหนังโดยผู้รับด้วย[30] และการมีอยู่ของเซลล์นี้ยังช่วยเพิ่มจำนวนเซลล์ประสาทสั่งการในไขสันหลัง SOD1 ของหนูตัวผู้ด้วย[31]
ระเบียบภาพ
[แก้]ดูเพิ่ม
[แก้]อ้างอิง
[แก้]- ↑ Charlotte Ownby. "Histology, Male reproductive system, Sertoli Cell & Developing Sperm Cells: an interaction". Oklahoma State University College of Veterinary Medicine. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 9 ธันวาคม 2006.
- ↑ Rosana Rodríguez-Casuriaga; Adriana Geisinger (กุมภาพันธ์ 2021). "Contributions of Flow Cytometry to the Molecular Study of Spermatogenesis in Mammals". International Journal of Molecular Sciences. 22 (3): 1151. doi:10.3390/ijms22031151. PMC 7865295. PMID 33503798.
- ↑ Kim Y, Kobayashi A, Sekido R, DiNapoli L, Brennan J, Chaboissier MC, Poulat F, Behringer RR, Lovell-Badge R, Capel B (มิถุนายน 2006). "Fgf9 and Wnt4 act as antagonistic signals to regulate mammalian sex determination". PLOS Biology. 4 (6): e187. doi:10.1371/journal.pbio.0040187. PMC 1463023. PMID 16700629.
- ↑ Moniot B, Declosmenil F, Barrionuevo F, Scherer G, Aritake K, Malki S, Marzi L, Cohen-Solal A, Georg I, Klattig J, Englert C, Kim Y, Capel B, Eguchi N, Urade Y, Boizet-Bonhoure B, Poulat F (มิถุนายน 2009). "The PGD2 pathway, independently of FGF9, amplifies SOX9 activity in Sertoli cells during male sexual differentiation". Development. 136 (11): 1813–21. doi:10.1242/dev.032631. PMC 4075598. PMID 19429785.
- ↑ Sharpe RM, McKinnell C, Kivlin C, Fisher JS (มิถุนายน 2003). "Proliferation and functional maturation of Sertoli cells, and their relevance to disorders of testis function in adulthood". Reproduction. 125 (6): 769–84. doi:10.1530/reprod/125.6.769. PMID 12773099.
- ↑ Nicholls PK, Stanton PG, Chen JL, Olcorn JS, Haverfield JT, Qian H, Walton KL, Gregorevic P, Harrison CA (ธันวาคม 2012). "Activin signaling regulates Sertoli cell differentiation and function". Endocrinology. 153 (12): 6065–77. doi:10.1210/en.2012-1821. PMID 23117933.
- ↑ Vize, Peter D.; Woolf, Adrian S.; Bard, Jonathan (2003). The kidney: from normal development to congenital disease. Academic Press. pp. 82–. ISBN 978-0-12-722441-1. สืบค้นเมื่อ 18 พฤศจิกายน 2010.
- ↑ Rato L, Alves MG, Socorro S, Duarte AI, Cavaco JE, Oliveira PF (พฤษภาคม 2012). "Metabolic regulation is important for spermatogenesis". Nature Reviews. Urology. 9 (6): 330–8. doi:10.1038/nrurol.2012.77. PMID 22549313. S2CID 7385545.
- ↑ Xiong X, Wang A, Liu G, Liu H, Wang C, Xia T, Chen X, Yang K (กรกฎาคม 2006). "Effects of p,p'-dichlorodiphenyldichloroethylene on the expressions of transferrin and androgen-binding protein in rat Sertoli cells". Environmental Research. 101 (3): 334–9. Bibcode:2006ER....101..334X. doi:10.1016/j.envres.2005.11.003. PMID 16380112.
- ↑ Skinner MK, Griswold MD (มิถุนายน 1983). "Sertoli cells synthesize and secrete a ceruloplasmin-like protein". Biology of Reproduction. 28 (5): 1225–1229. doi:10.1095/biolreprod28.5.1225. PMID 6871315.
- ↑ O'Donnell L, Nicholls PK, O'Bryan MK, McLachlan RI, Stanton PG (มกราคม 2011). "Spermiation: The process of sperm release". Spermatogenesis. 1 (1): 14–35. doi:10.4161/spmg.1.1.14525. PMC 3158646. PMID 21866274.
- ↑ 12.0 12.1 Ahmed EA, Barten-van Rijbroek AD, Kal HB, Sadri-Ardekani H, Mizrak SC, van Pelt AM, de Rooij DG (มิถุนายน 2009). "Proliferative activity in vitro and DNA repair indicate that adult mouse and human Sertoli cells are not terminally differentiated, quiescent cells". Biology of Reproduction. 80 (6): 1084–91. doi:10.1095/biolreprod.108.071662. PMID 19164176.
- ↑ Walter CA, Intano GW, McCarrey JR, McMahan CA, Walter RB (สิงหาคม 1998). "Mutation frequency declines during spermatogenesis in young mice but increases in old mice". Proceedings of the National Academy of Sciences of the United States of America. 95 (17): 10015–9. Bibcode:1998PNAS...9510015W. doi:10.1073/pnas.95.17.10015. PMC 21453. PMID 9707592.
- ↑ Dal Secco V, Riccioli A, Padula F, Ziparo E, Filippini A (กุมภาพันธ์ 2008). "Mouse Sertoli cells display phenotypical and functional traits of antigen-presenting cells in response to interferon gamma". Biology of Reproduction. 78 (2): 234–42. doi:10.1095/biolreprod.107.063578. PMID 17989360.
- ↑ Kaur G, Thompson LA, Dufour JM (มิถุนายน 2014). "Sertoli cells--immunological sentinels of spermatogenesis". Seminars in Cell & Developmental Biology. 30: 36–44. doi:10.1016/j.semcdb.2014.02.011. PMC 4043859. PMID 24603046.
- ↑ Campese AF, Grazioli P, de Cesaris P, Riccioli A, Bellavia D, Pelullo M, Padula F, Noce C, Verkhovskaia S, Filippini A, Latella G, Screpanti I, Ziparo E, Starace D (มีนาคม 2014). "Mouse Sertoli cells sustain de novo generation of regulatory T cells by triggering the notch pathway through soluble JAGGED1". Biology of Reproduction. 90 (3): 53. doi:10.1095/biolreprod.113.113803. PMID 24478388.
- ↑ Potempa J, Korzus E, Travis J (มิถุนายน 1994). "The serpin superfamily of proteinase inhibitors: structure, function, and regulation". The Journal of Biological Chemistry. 269 (23): 15957–60. doi:10.1016/S0021-9258(17)33954-6. PMID 8206889.
- ↑ 18.0 18.1 18.2 Lee HM, Oh BC, Lim DP, Lee DS, Lim HG, Park CS, Lee JR (มิถุนายน 2008). "Mechanism of humoral and cellular immune modulation provided by porcine sertoli cells". Journal of Korean Medical Science. 23 (3): 514–20. doi:10.3346/jkms.2008.23.3.514. PMC 2526533. PMID 18583891.
- ↑ Iliadou PK, Tsametis C, Kaprara A, Papadimas I, Goulis DG (ตุลาคม 2015). "The Sertoli cell: Novel clinical potentiality". Hormones. 14 (4): 504–14. doi:10.14310/horm.2002.1648. PMID 26859601.
- ↑ Schulz RW, de França LR, Lareyre JJ, Le Gac F, LeGac F, Chiarini-Garcia H, Nobrega RH, Miura T (กุมภาพันธ์ 2010). "Spermatogenesis in fish". General and Comparative Endocrinology. 165 (3): 390–411. doi:10.1016/j.ygcen.2009.02.013. PMID 19348807.
- ↑ Morais RD, Nóbrega RH, Gómez-González NE, Schmidt R, Bogerd J, França LR, Schulz RW (พฤศจิกายน 2013). "Thyroid hormone stimulates the proliferation of Sertoli cells and single type A spermatogonia in adult zebrafish (Danio rerio) testis". Endocrinology. 154 (11): 4365–76. doi:10.1210/en.2013-1308. PMID 24002037.
- ↑ Lacerda SM, Costa GM, Campos-Junior PH, Segatelli TM, Yazawa R, Takeuchi Y, Morita T, Yoshizaki G, França LR (กุมภาพันธ์ 2013). "Germ cell transplantation as a potential biotechnological approach to fish reproduction". Fish Physiology and Biochemistry. 39 (1): 3–11. doi:10.1007/s10695-012-9606-4. PMID 22290474. S2CID 10134737.
- ↑ Almeida FF, Kristoffersen C, Taranger GL, Schulz RW (มกราคม 2008). "Spermatogenesis in Atlantic cod (Gadus morhua): a novel model of cystic germ cell development". Biology of Reproduction. 78 (1): 27–34. doi:10.1095/biolreprod.107.063669. PMID 17881768.
- ↑ Mital P, Kaur G, Bowlin B, Paniagua NJ, Korbutt GS, Dufour JM (มกราคม 2014). "Nondividing, postpubertal rat sertoli cells resumed proliferation after transplantation". Biology of Reproduction. 90 (1): 13. doi:10.1095/biolreprod.113.110197. PMC 4076399. PMID 24285718.
- ↑ synd/518 ใน Who Named It?
- ↑ 26.0 26.1 Luca G, Arato I, Mancuso F, Calvitti M, Falabella G, Murdolo G, Basta G, Cameron DF, Hansen BC, Fallarino F, Baroni T, Aglietti MC, Tortoioli C, Bodo M, Calafiore R (พฤศจิกายน 2016). "Xenograft of microencapsulated Sertoli cells restores glucose homeostasis in db/db mice with spontaneous diabetes mellitus". Xenotransplantation. 23 (6): 429–439. doi:10.1111/xen.12274. PMID 27678013. S2CID 46744082.
- ↑ Valdés-González RA, Dorantes LM, Garibay GN, Bracho-Blanchet E, Mendez AJ, Dávila-Pérez R, Elliott RB, Terán L, White DJ (กันยายน 2005). "Xenotransplantation of porcine neonatal islets of Langerhans and Sertoli cells: a 4-year study". European Journal of Endocrinology. 153 (3): 419–27. doi:10.1530/eje.1.01982. PMID 16131605.
- ↑ Korbutt GS, Elliott JF, Rajotte RV (กุมภาพันธ์ 1997). "Cotransplantation of allogeneic islets with allogeneic testicular cell aggregates allows long-term graft survival without systemic immunosuppression". Diabetes. 46 (2): 317–22. doi:10.2337/diab.46.2.317. PMID 9000711.
- ↑ Li Y, Xue W, Liu H, Fan P, Wang X, Ding X, Tian X, Feng X, Pan X, Zheng J, Tian P, Ding C, Fan X (20 กุมภาพันธ์ 2013). "Combined strategy of endothelial cells coating, Sertoli cells coculture and infusion improves vascularization and rejection protection of islet graft". PLOS ONE. 8 (2): e56696. Bibcode:2013PLoSO...856696L. doi:10.1371/journal.pone.0056696. PMC 3577699. PMID 23437215.
- ↑ Bistoni G, Calvitti M, Mancuso F, Arato I, Falabella G, Cucchia R, Fallarino F, Becchetti A, Baroni T, Mazzitelli S, Nastruzzi C, Bodo M, Becchetti E, Cameron DF, Luca G, Calafiore R (กรกฎาคม 2012). "Prolongation of skin allograft survival in rats by the transplantation of microencapsulated xenogeneic neonatal porcine Sertoli cells". Biomaterials. 33 (21): 5333–40. doi:10.1016/j.biomaterials.2012.04.020. PMID 22560198.
- ↑ Hemendinger, Richelle; Wang, Jay; Malik, Saafan; Persinski, Rafal; Copeland, Jane; Emerich, Dwaine; Gores, Paul; Halberstadt, Craig; Rosenfeld, Jeffrey (2005). "Sertoli cells improve survival of motor neurons in SOD1 transgenic mice, a model of amyotrophic lateral sclerosis". Experimental Neurology. 196 (2): 235–243. doi:10.1016/j.expneurol.2005.07.025. PMID 16242126. S2CID 352751.
แหล่งข้อมูลอื่น
[แก้]- ภาพเนื้อเยื่อจากมหาวิทยาลัยบอสตัน 17805loa (อังกฤษ)
- ภาพเนื้อเยื่อจากมหาวิทยาลัยบอสตัน 17806loa (อังกฤษ)

