ผลต่างระหว่างรุ่นของ "แบคทีเรีย"
Just Sayori (คุย | ส่วนร่วม) ไม่มีความย่อการแก้ไข |
Just Sayori (คุย | ส่วนร่วม) ไม่มีความย่อการแก้ไข |
||
| บรรทัด 103: | บรรทัด 103: | ||
การประกอบหน่วยต่าง ๆ โครงสร้างภายนอกเซลล์ขึ้นอยู่กับ[[ระบบการหลั่งสารของแบคทีเรีย]]ที่มีอยู่หลายระบบ ระบบเหล่านี้ขนส่งโปรตีนจากไซโทพลาซึมออกไปยังเพอริพลาซึม หรือออกไปยังสิ่งแวดล้อมรอบเซลล์ ระบบการหลั่งหลายประเภทเป็นที่รู้จักและมักมีความสำคัญต่อ[[ศักยภาพก่อโรค]]ของเชื้อ จึงมีการศึกษากันอย่างเข้มข้น<ref>{{cite journal | vauthors = Finlay BB, Falkow S | title = Common themes in microbial pathogenicity revisited | journal = Microbiology and Molecular Biology Reviews | volume = 61 | issue = 2 | pages = 136–69 | date = June 1997 | pmid = 9184008 | pmc = 232605 | doi = 10.1128/.61.2.136-169.1997 }}</ref> |
การประกอบหน่วยต่าง ๆ โครงสร้างภายนอกเซลล์ขึ้นอยู่กับ[[ระบบการหลั่งสารของแบคทีเรีย]]ที่มีอยู่หลายระบบ ระบบเหล่านี้ขนส่งโปรตีนจากไซโทพลาซึมออกไปยังเพอริพลาซึม หรือออกไปยังสิ่งแวดล้อมรอบเซลล์ ระบบการหลั่งหลายประเภทเป็นที่รู้จักและมักมีความสำคัญต่อ[[ศักยภาพก่อโรค]]ของเชื้อ จึงมีการศึกษากันอย่างเข้มข้น<ref>{{cite journal | vauthors = Finlay BB, Falkow S | title = Common themes in microbial pathogenicity revisited | journal = Microbiology and Molecular Biology Reviews | volume = 61 | issue = 2 | pages = 136–69 | date = June 1997 | pmid = 9184008 | pmc = 232605 | doi = 10.1128/.61.2.136-169.1997 }}</ref> |
||
===เอนโดสปอร์=== |
|||
{{further|เอนโดสปอร์}} |
|||
[[File:Gram Stain Anthrax.jpg|thumb|right|alt=Anthrax stained purple|''[[Bacillus anthracis]]'' (ย้อมด้วยสีม่วง) ที่เจริญเติบโตใน[[น้ำหล่อสมองไขสันหลัง]]]] |
|||
แบคทีเรียแกรมบวกบาง[[สกุล (ชีววิทยา)|สกุล]]เช่น ''[[Bacillus]]'', ''[[Clostridium]]'', ''[[Sporohalobacter]]'', ''[[Anaerobacter]]'', และ ''[[Heliobacteria|Heliobacterium]]'' สามารถสร้างโครงสร้างสำหรับพักตัวที่มีความทนทานสูง เรียกว่า [[เอนโดสปอร์]] (endospore)<ref>{{cite journal | vauthors = Nicholson WL, Munakata N, Horneck G, Melosh HJ, Setlow P | title = Resistance of Bacillus endospores to extreme terrestrial and extraterrestrial environments | journal = Microbiology and Molecular Biology Reviews | volume = 64 | issue = 3 | pages = 548–72 | date = September 2000 | pmid = 10974126 | pmc = 99004 | doi = 10.1128/MMBR.64.3.548-572.2000 }}</ref> โดยพัฒนาขึ้นอยู่ภายในไซโทพลาซึมของเซลล์<ref name="McKenney">{{cite journal | vauthors = McKenney PT, Driks A, Eichenberger P | title = The Bacillus subtilis endospore: assembly and functions of the multilayered coat | journal = Nature Reviews. Microbiology | volume = 11 | issue = 1 | pages = 33–44 | date = January 2013 | pmid = 23202530 | doi = 10.1038/nrmicro2921 | s2cid = 205498395 }}</ref> ปกติหนึ่งสปอร์ต่อหนึ่งเซลล์ แต่ละเอนโดสปอร์มีแกนกลางเป็น[[ดีเอ็นเอ]]และ[[ไรโบโซม]] ล้อมรอบด้วยชั้นคอร์เทกซ์ (cortex layer) ซึ่งมีเปลือกอันประกอบขึ้นจากเพปทิโดไกลแคนและโปรตีนหลายชนิดมาหุ้มอีกชั้นหนึ่ง<ref name="McKenney" /> |
|||
เอนโดสปอร์ไม่แสดงกระบวนการ[[เมแทบอลิซึม]]ที่สามารถตรวจพบได้ และสามารถเอาชีวิตรอดจากสิ่งกดดันทางเคมีและฟิสิกส์ในระดับสุดขั้วได้ เช่น[[รังสียูวี]]ความเข้มข้นสูง, [[รังสีแกมมา|การแผ่รังสีแกมมา]], [[สารซักฟอก]], [[สารฆ่าเชื้อ]], ความร้อน, การแช่แข็ง, ความดัน, และ[[Desiccation|การทำแห้งสนิท]]<ref>{{cite journal | vauthors = Nicholson WL, Fajardo-Cavazos P, Rebeil R, Slieman TA, Riesenman PJ, Law JF, Xue Y | title = Bacterial endospores and their significance in stress resistance | journal = Antonie van Leeuwenhoek | volume = 81 | issue = 1–4 | pages = 27–32 | date = August 2002 | pmid = 12448702 | doi = 10.1023/A:1020561122764 | s2cid = 30639022 }}</ref> ในสภาพจำศีลเช่นนี้ แบคทีเรียสามารถมีชีวิตได้ถึงหลายล้านปี<ref>{{cite journal | vauthors = Vreeland RH, Rosenzweig WD, Powers DW | title = Isolation of a 250 million-year-old halotolerant bacterium from a primary salt crystal | journal = Nature | volume = 407 | issue = 6806 | pages = 897–900 | date = October 2000 | pmid = 11057666 | doi = 10.1038/35038060 | bibcode = 2000Natur.407..897V | s2cid = 9879073 }}</ref><ref>{{cite journal | vauthors = Cano RJ, Borucki MK | title = Revival and identification of bacterial spores in 25- to 40-million-year-old Dominican amber | journal = Science | volume = 268 | issue = 5213 | pages = 1060–64 | date = May 1995 | pmid = 7538699 | doi = 10.1126/science.7538699 | bibcode = 1995Sci...268.1060C }}</ref><ref>{{Cite news|url=http://news.bbc.co.uk/2/hi/science/nature/1375505.stm|title=Row over ancient bacteria|date=2001-06-07|work=BBC News|access-date=2020-04-26|language=en-GB}}</ref> เอนโดสปอร์ยังทำให้แบคทีเรียมีชีวิตรอดจากสภาวะสุญญากาศและรังสีในอวกาศ เป็นไปได้ว่าแบคทีเรียกระจายไปทั่วเอกภพด้วย[[ฝุ่นอวกาศ]], [[สะเก็ดดาว]], [[ดาวเคราะห์น้อย]], [[ดาวหาง]], [[Planetoid|วัตถุคล้ายดาวเคราะห์]] (planetoid), หรือผ่าน[[Directed panspermia|กระบวนการแพนสเปอร์เมียแบบมีการกำกับ]] (directed panspermia)<ref>{{cite journal | vauthors = Nicholson WL, Schuerger AC, Setlow P | title = The solar UV environment and bacterial spore UV resistance: considerations for Earth-to-Mars transport by natural processes and human spaceflight | journal = Mutation Research | volume = 571 | issue = 1–2 | pages = 249–64 | date = April 2005 | pmid = 15748651 | doi = 10.1016/j.mrfmmm.2004.10.012 }}</ref><ref>{{Cite news|url=https://www.economist.com/science-and-technology/2018/04/12/colonising-the-galaxy-is-hard-why-not-send-bacteria-instead|title=Colonising the galaxy is hard. Why not send bacteria instead?|date=2018-04-12|work=The Economist|access-date=2020-04-26|issn=0013-0613}}</ref> แบคทีเรียที่สร้างเอนโดสปอร์สามารถทำให้เกิดโรคได้ ตัวอย่างเช่น [[แอนแทรกซ์]]ซึ่งเกิดจากการหายใจเอาเอนโดสปอร์ของ ''[[Bacillus anthracis]]'' เข้าสู่ร่างกาย, และ[[บาดทะยัก]]ที่เกิดจากบาดแผลถูกแทงปนเปื้อนเอนโดสปอร์ของ ''[[Clostridium tetani]]''<ref>{{cite journal | vauthors = Hatheway CL | title = Toxigenic clostridia | journal = Clinical Microbiology Reviews | volume = 3 | issue = 1 | pages = 66–98 | date = January 1990 | pmid = 2404569 | pmc = 358141 | doi = 10.1128/CMR.3.1.66 }}</ref> |
|||
{{Wikispecies|Bacteria}} |
{{Wikispecies|Bacteria}} |
||
รุ่นแก้ไขเมื่อ 21:37, 1 สิงหาคม 2564
| Bacteria ช่วงเวลาที่มีชีวิตอยู่: อาร์เคียน หรือก่อนหน้านั้น – ปัจจุบัน | |
|---|---|

| |
| ภาพจากกล้องจุลทรรศน์อิเล็กตรอนแสดงรูปร่างของ Escherichia coli ที่มีลักษณะเป็นแท่ง | |
| การจำแนกชั้นทางวิทยาศาสตร์ | |
| โดเมน: | แบคทีเรีย Woese, Kandler & Wheelis, 1990[1] |
| ไฟลัม | |
| |
| ชื่อพ้อง | |
| |
แบคทีเรีย หรือ บัคเตรี (อังกฤษ: bacteria /bækˈtɪəriə/ (![]() ฟังเสียง); เอกพจน์ bacterium) เป็นเซลล์ประเภทหนึ่ง ประกอบขึ้นจากโดเมนขนาดใหญ่ของจุลชีพที่เป็นโพรแคริโอต โดยมากมีความยาวไม่กี่ไมโครเมตร แบคทีเรียมีรูปร่างที่หลากหลาย ตั้งแต่ทรงกลมไปจนถึงแบบแท่งและแบบเกลียว แบคทีเรียเป็นหนึ่งในรูปแบบแรก ๆ ของชีวิตที่ปรากฏขึ้นบนโลก และพบได้ในสิ่งแวดล้อมเกือบทุกรูปแบบ แบคทีเรียอาศัยอยู่ในดิน, แหล่งน้ำ, น้ำพุร้อนที่มีความเป็นกรด, ขยะกัมมันตรังสี[4], และชีวมณฑลส่วนลึกของแผ่นเปลือกโลก นอกจากนี้ยังดำรงความสัมพันธ์แบบอยู่ร่วมกันและแบบปรสิตกับพืชและสัตว์ แบคทีเรียส่วนมากยังไม่ถูกอธิบายคุณลักษณะ และมีเพียงร้อยละ 27 จากไฟลัมแบคทีเรียทั้งหมดที่สามารถเติบโตในห้องปฏิบัติการณ์[5] สาขาวิชาที่ศึกษาแบคทีเรียรู้จักกันในชื่อ แบคทีเรียวิทยา (bacteriology) อันเป็นสาขาหนึ่งของจุลชีววิทยา
ฟังเสียง); เอกพจน์ bacterium) เป็นเซลล์ประเภทหนึ่ง ประกอบขึ้นจากโดเมนขนาดใหญ่ของจุลชีพที่เป็นโพรแคริโอต โดยมากมีความยาวไม่กี่ไมโครเมตร แบคทีเรียมีรูปร่างที่หลากหลาย ตั้งแต่ทรงกลมไปจนถึงแบบแท่งและแบบเกลียว แบคทีเรียเป็นหนึ่งในรูปแบบแรก ๆ ของชีวิตที่ปรากฏขึ้นบนโลก และพบได้ในสิ่งแวดล้อมเกือบทุกรูปแบบ แบคทีเรียอาศัยอยู่ในดิน, แหล่งน้ำ, น้ำพุร้อนที่มีความเป็นกรด, ขยะกัมมันตรังสี[4], และชีวมณฑลส่วนลึกของแผ่นเปลือกโลก นอกจากนี้ยังดำรงความสัมพันธ์แบบอยู่ร่วมกันและแบบปรสิตกับพืชและสัตว์ แบคทีเรียส่วนมากยังไม่ถูกอธิบายคุณลักษณะ และมีเพียงร้อยละ 27 จากไฟลัมแบคทีเรียทั้งหมดที่สามารถเติบโตในห้องปฏิบัติการณ์[5] สาขาวิชาที่ศึกษาแบคทีเรียรู้จักกันในชื่อ แบคทีเรียวิทยา (bacteriology) อันเป็นสาขาหนึ่งของจุลชีววิทยา
สัตว์เกือบทุกชนิดล้วนพึ่งพาแบคทีเรียเพื่อการดำรงชีวิต เนื่องจากมีเพียงแบคทีเรียและและอาร์เคียบางชนิดที่มีเอนไซม์จำเป็นสำหรับการสร้างวิตามินบี 12 (โคบาลามิน) และส่งผ่านวิตามินนี้ทางห่วงโซ่อาหาร วิตามินบี 12 เป็นวิตามินสามารถละลายในน้ำได้ที่มีส่วนเกี่ยวข้องกับกระบวนการเมแทบอลิซึมของทุกเซลล์ในร่างกายมนุษย์ เป็นโคแฟกเตอร์ในกระบวนการสังเคราะห์ดีเอ็นเอ และกระบวนการเมแทบอลิซึมของกรดไขมันกับกรดอะมิโน มีความสำคัญอย่างยิ่งต่อการทำงานตามปกติของระบบประสาท ผ่านบทบาทในการสังเคราะห์ไมอีลิน[6][7][8][9] ปกติมีแบคทีเรียประมาณ 40 ล้านเซลล์ในดินหนึ่งกรัม และประมาณหนึ่งล้านเซลล์ในน้ำจืดหนึ่งมิลลิลิตร ประมาณกันว่ามีแบคทีเรียประมาณ 5×1030 ตัวบนโลก[10] ทำให้เกิดมวลชีวภาพที่เป็นรองเพียงแต่พืชเท่านั้น[11] แบคทีเรียมีความจำเป็นสำหรับหลายขั้นในวัฏจักรของสารอาหาร ด้วยการนำสารอาหารกลับมาใช้ใหม่ ดังเช่นการตรึงไนโตรเจนจากชั้นบรรยากาศ วัฏจักรสารอาหารยังรวมถึงกระบวนการเน่าเปื่อย (decomposition) ของซากสิ่งมีชีวิต ซึ่งแบคทีเรียมีส่วนเกี่ยวข้องในขั้นตอนการเน่าสลาย (putrefaction) ของกระบวนการดังกล่าว[12] กลุ่มสังคมทางชีววิทยาโดยรอบปล่องน้ำร้อนและปล่องน้ำเย็นใต้ทะเลมีแบคทีเรียอิกซ์ตรีโมไฟล์ (extremophile) เป็นผู้ให้สารอาหารที่จำเป็นสำหรับการดำรงชีวิตด้วยการเปลี่ยนรูปสารประกอบที่ละลายอยู่ในน้ำ (เช่นไฮโดรเจนซัลไฟด์และมีเทน) ให้เป็นพลังงาน
ในมนุษย์และสัตว์ส่วนมากมีแบคทีเรียอาศัยอยู่ในท่อทางเดินอาหารและผิวหนังเป็นจำนวนมาก[13] แบคทีเรียส่วนใหญ่ที่อยู่ในร่างกายถูกทำให้ไร้พิษภัยโดยผลของระบบภูมิคุ้มกัน บางชนิดให้ประโยชน์ต่อร่างกาย โดยเฉพาะที่อยู่ในทางเดินอาหาร อย่างไรก็ตาม มีแบคทีเรียบางสปีชีส์เป็นเชื้อที่ก่อโรคติดเชื้อ อาทิ อหิวาตกโรค ซิฟิลิส แอนแทรกซ์ โรคเรื้อน กาฬโรคต่อมน้ำเหลือง โรคอันตรายถึงที่เกิดจากแบคทีเรียที่พบได้บ่อยคือ โรคติดเชื้อของระบบทางเดินหายใจ วัณโรคเพียงอย่างเดียวคร่าชีวิตประมาณ 2 ล้านคนในแต่ละปี ส่วนใหญมาจากแอฟริกาใต้สะฮารา[14] ยาปฏิชีวนะถูกใช้เพื่อรักษาการติดเชื้อแบคทีเรีย และยังมีการใช้ในภาคเกษตรกรรมอีกด้วย ทำให้แบคทีเรียดื้อยาเป็นปัญหามากยิ่งขึ้น ในภาคอุตสาหกรรม แบคทีเรียมีความสำคัญต่อการบำบัดน้ำเสียและการย่อยสลายคราบน้ำมันรั่วไหล, การผลิตชีสและโยเกิร์ตด้วยการหมัก, การนำทอง พัลลาเดียม ทองแดง และโลหะอื่น ๆ กลับมาใช้ใหม่ในอุตสาหกรรมเหมืองแร่[15]และเทคโนโลยีชีวภาพ, และการผลิตยาปฏิชีวนะกับสารเคมีอื่น ๆ[16]
ปัจจุบันแบคทีเรียถูกจัดเป็นโพรแคริโอต จากแต่เดิมที่ถือว่าเป็นพืชที่อยู่ในชั้น Schizomycetes (เห็ดราที่แบ่งตัวแบบฟิชชัน) แบคทีเรียไม่มีนิวเคลียส น้อยนักที่จะพบออร์แกเนลล์ที่มีเยื่อหุ้ม ซึ่งแตกต่างจากสัตว์และยูแคริโอตอื่น ๆ แม้เดิมคำว่า แบคทีเรีย จะหมายถึงโพรแคริโอตทุกชนิด การจำแนกชั้นทางวิทยาศาสตร์ก็ได้เปลี่ยนไปนับตั้งแต่การค้นพบในทศวรรษ 1990 ว่าโพรแคริโอตประกอบไปด้วยสองกลุ่มสิ่งมีชีวิตที่มีชื่อเรียกโดเมนว่าแบคทีเรีย และอาร์เคีย ซึ่งแตกต่างกันมาก แต่วิวัฒน์มาจากบรรพบุรุษเดียวกัน[1]
ศัพทมูลวิทยา
คำว่า bacteria เป็นรูปพหูพจน์ของ bacterium จากภาษาละตินสมัยใหม่ ซึ่งเป็นการแปลง βακτήριον (bakterion)[17] ในภาษากรีกให้เป็นภาษาละติน ซึ่ง βακτήριον เป็นตัวบอกความเล็ก (diminutive) ของ βακτηρία (bakteria) อันแปลว่า "คทา, ไม้เท้า"[18] เนื่องจากแบคทีเรียชนิดแรกที่ถูกค้นพบมีรูปร่างเป็นแท่ง[19][20]
ต้นกำเนิดและวิวัฒนาการในช่วงแรก
บรรพบุรุษของแบคทีเรียสมัยใหม่คือจุลชีพเซลล์เดียวที่เป็นรูปแบบแรกของชีวิตบนโลก เมื่อประมาณ 4 พันล้านปีที่แล้ว เป็นเวลากว่า 3 พันล้านปีที่สิ่งมีชีวิตส่วนใหญ่มีขนาดเล็กระดับที่มองด้วยตาเปล่าไม่เห็น และแบคทีเรียกับอาร์เคียเป็นรูปแบบเด่นของชีวิต[21][22] แม้ว่าจะมีซากดึกดำบรรพ์ของแบคทีเรีย เช่น สโตรมาโทไลต์อยู่ก็ตาม ก็ยังขาดสัณฐานวิทยาที่เด่นชัดพอสำหรับการตรวจสอบประวัติศาสตร์วิวัฒนาการของแบคทีเรีย หรือเพื่อการระบุเวลาถือกำเนิดของแบคที่เรียบางสปีชีส์ อย่างไรก็ตาม สามารถใช้การหาลำดับยีน (gene sequencing) เพื่อสร้างสายวิวัฒนาการชาติพันธุ์ของแบคทีเรียได้ ซึ่งทำให้ทราบว่าแบคทีเรียแตกออกมาจากเชื้อสายของอาร์เคีย/แบคทีเรียเป็นลำดับแรก[23] บรรพบุรุษร่วมล่าสุดของแบคทีเรียและอาร์เคียอาจเป็นไฮเพอร์เทอร์โมไฟล์ที่มีชีวิตอยู่เมื่อประมาณ 2.5 พันล้าน–พันล้านปีที่แล้ว[24][25] ชีวิตที่เก่าแก่ที่สุดบนผืนดินอาจเป็นแบคทีเรียเมื่อ 3.22 พันล้านปีที่แล้ว[26]
แบคทีเรียยังมีส่วนเกี่ยวข้องกับการแตกสายวิวัฒนาการใหญ่ครั้งที่สอง ซึ่งแบ่งแยกอาร์เคียและยูแคริโอตออกจากกัน ในเหตุการณ์นี้ ยูแคริโอตเกิดขึ้นมาจากการที่แบคทีเรียโบราณเข้าไปมีความสัมพันธ์แบบเอนโดซิมไบโอติกกับบรรพบุรุษของเซลล์ยูแคริโอต ซึ่งมีความเป็นไปได้ที่บรรพบุรุษของยูแคริโอตจะมีความสัมพันธ์กับอาร์เคีย[27][28] เหตุการณ์นี้ยังเกี่ยวข้องกับการกลืนกินอัลฟาโพรทีโอแบคทีเรียร่วมอาศัยของเซลล์ยูแคริโอตแรกเริ่ม (proto-eukaryotic cell) เพื่อพัฒนาเป็นไมโทคอนเดรียหรือไฮโดรเจโนโซม ซึ่งยังคงพบในยูแคริโอตทุกชนิด (บางครั้งอาจพบว่าลดรูปไปอย่างมาก เช่นที่พบในแบคทีเรียโบราณที่ขาดไมโทคอนเดรีย; amitocondrial protozoa) ในเวลาต่อมา ยูแคริโอตบางชนิดที่มีไมโทคอนเดรียอยู่แล้วได้กลืนกินสิ่งมีชีวิตคล้ายไซยาโนแบคทีเรียเข้าไป นำไปสู่กำเนิดของคลอโรพลาสต์ในสาหร่ายและพืช เหตุการณ์นี้เป็นที่รู้จักกันในชื่อเอนโดซิมไบโอซิสปฐมภูมิ (primary endosymbiosis)[29][30]
สัณฐานวิทยา

แบคทีเรียแสดงให้เห็นถึงความหลากหลายอย่างยิ่งของรูปร่างและขนาด เรียกว่า พหุสัณฐาน (morphologies) เซลล์ของแบคทีเรียมีขนาดประมาณหนึ่งในสิบของเซลล์ยูแคริโอต และมีความยาวประมาณ 0.5–5.0 ไมโครเมตร อย่างไรก็ตาม บางสปีชีส์มีขนาดใหญ่จนสามารถมองเห็นด้วยตาเปล่า เช่น Thiomargarita namibiensis ที่มีความยาวประมาณครึ่งมิลลิเมตร[31] และ Epulopiscium fishelsoni ที่ยาวถึง 0.7 มิลลิเมตร[32] หนึ่งในแบคทีเรียที่ขนาดเล็กที่สุดคือแบคทีเรียในสกุล Mycoplasma ซึ่งมีความยาวเพียง 0.3 ไมโครเมตร หรือประมาณไวรัสที่มีขนาดใหญ่ที่สุด[33] บางชนิดอาจมีขนาดเล็กกว่านี้ได้ เรียกว่า ไมโครแบคทีเรียขนาดเล็กยิ่งยวด (ultramicrobacteria) แต่ว่ายังไม่ได้รับการศึกษามากนัก[34]
สปีชีส์เกือบทั้งหมดของแบคทีเรียมีรูปทรงเป็นทั้งทรงกลม เรียกว่า ค็อกไซ (เอกพจน์: ค็อกคัส; จากภาษากรีก kókkos เมล็ดธัญพืช, เมล็ด), หรือรูปทรงท่อน เรียกว่า บาซิลไล (เอกพจน์: บาซิลลัส; จากภาษาละติน baculus ไม้ถือ)[35] แบคทีเรียบางชนิดที่เรียกว่า ไวบริโอ รูปร่างคล้ายแท่งไม้ที่มีความโค้งเล็กน้อย หรือรูปร่างเป็นเครื่องหมายจุลภาค บางชนิดมีรูปร่างเป็นเกลียว เรียกว่า สไปริลา, หรือมีการขดตัวในระดับสูง เรียกว่า สไปโรคีตส์ มีแบคทีเรียที่มีรูปร่างวิกลจำหนึ่งที่ได้รับการอธิบาย เช่นแบคทีเรียรูปดาว[36] การมีรูปทรงหลากหลายเช่นนี้ถูกกำหนดด้วยผนังเซลล์และไซโทสเกเลทอนของตัวแบคทีเรีย ซึ่งมีความสำคัญเนื่องจากการมีรูปร่างที่หลากหลายจะช่วยเสริมความสามารถของแบคทีเรียในการได้มาซึ่งสารอาหาร, การยึดติดกับพื้นผิว, การว่ายผ่านของเหลว และการหลบหนีผู้ล่า[37][38]

แบคทีเรียหลายสปีชีส์ดำรงชีวิตในรูปแบบเซลล์โดดเดี่ยว บางสปีชีส์อาศัยอยู่รวมกันเป็นแบบแผนที่มีลักณระเฉพาะ เช่น Neisseria ที่อยู่เป็นดิพลอยด์ (คู่), Streptococcus อยู่รวมกันเป็นสายยาว, และ Staphylococcus เกาะกลุ่มกันเป็นกระจุกคล้ายพวงองุ่น แบคทีเรียยังสามารถรวมกันเพื่อสร้างโครงสร้างหลายเซลล์ที่มีขนาดใหญ่ขึ้นได้ ดังการต่อสายฟิลาเมนต์ของ Actinobacteria, การเกาะกลุ่มของ Myxobacteria, และเส้นใยไฮฟาที่ซับซ้อนของ Streptomyces[39] โครงสร้างที่ประกอบขึ้นจากหลายเซลล์เช่นนี้สามารถพบได้ในบางสภาวะ ตัวอย่างเช่น เมื่อขาดกรดอะมิโน Myxobacteria จะตรวจหาเซลล์ที่อยู่โดยรอบด้วยกระบวนการที่เรียกว่า ควอรัมเซนซิง (quorum sensing) จากนั้นจะเคลื่อนย้ายเข้ามาหากันและรวมกลุ่มกันเป็นฟรุตติงบอดี (fruiting body) ที่มีความยาวได้ถึง 500 ไมโครเมตรและประกอบขึ้นจากแบคทีเรียประมาณ 100,000 ตัว[40] ในฟรุตติงบอดี แบคทีเรียจะทำหน้าที่ต่าง ๆ แยกกัน ตัวอย่าง เซลล์ประมาณหนึ่งในสิบจะขึ้นไปสู่ยอดของฟรุตติงบอดีและมีการเปลี่ยนแปลงหน้าที่ของเซลล์ (differentiation) ไปสู่สถานะพักตัวที่เรียกว่า มิกโซสปอร์ (myxospore) ซึ่งมีความทนทานต่อการขาดน้ำและสิ่งแวดล้อมที่เป็นอันตรายอื่น ๆ สูงกว่าสถานะปกติ[41]
แบคทีเรียมักจะเกาะตัวอยู่บนพื้นผิวและเกาะเป็นกลุ่มหนาแน่นที่เรียกว่า ฟิล์มชีวภาพ (biofilm) และกลุ่มที่ใหญ่กว่าเรียกว่า พรมจุลชีพ (microbial mat) ฟิล์มชีวภาพและพรมจุลชีพมีความหนาตั้งแต่ไม่กี่ไมโครเมตรไปจนถึงครึ่งเมตร และอาจมีแบคทีเรีย, โพรทิสต์ และอาร์เคียอาศัยอยู่หลายสปีชีส์ แบคทีเรียที่อาศัยอยู่ในฟิล์มชีวภาพแสดงการจัดเรียงเซลล์และองค์ประกอบนอกเซลล์ที่มีความซับซ้อน จนกลายเป็นโครงสร้างขั้นทุติยภูมิ ดังเช่นไมโครคอลอนี (microcolony) อันปรากฏโครงข่ายของช่องเปิด เพื่อให้การแพร่สารอาหารดียิ่งขึ้น[42][43] ในสิ่งแวดล้อมตามธรรมชาติ ดังในดินหรือบนพื้นผิวของพืช แบคทีเรียส่วนใหญ่เกาะกลุ่มกันบนพืนผิวในรูปของฟิล์มชีวภาพ[44] ฟิล์มชีวภาพ ยังมีความสำคัญทางแพทยศาสตร์ เนื่องจากโครงสร้างเช่นนี้มักปรากฏในช่วงที่เกิดการติดเชื้อแบคทีเรียเรื้อรัง (chronic bacterial infection) หรือการติดเชื้อในอุปกรณ์ทางการแพทย์ที่ปลูกถ่ายเข้าไป และแบคทีเรียที่ได้รับการปกป้องจากฟิล์มชีวภาพจะกำจัดได้ยากกว่าแบคทีเรียที่อยู่โดดเดี่ยว[45]
โครงสร้างระดับเซลล์

โครงสร้างภายในเซลล์
เซลล์ของแบคทีเรียถูกล้อมรอบด้วยเยื่อหุ้มเซลล์ ซึ่งประกอบด้วยฟอสโฟลิพิดเป็นหลัก เยื่อหุ้มเซลล์ห่อหุ้มสารต่าง ๆ ที่อยู่ภายในเซลล์และทำหน้าที่เป็นแนวกั้นสำหรับกักสารอาหาร โปรตีน และองค์ประกอบอื่นที่จำเป็นของไซโทพลาซึมเอาไว้ในเซลล์[46] ต่างจากเซลล์ยูแคริโอต ไซโทพลาซึมของแบคทีเรียมักขาดโครงสร้างขนาดใหญ่ที่มีเยื่อหุ้ม เช่น นิวเคลียส ไมโทคอนเดรีย คลอโรพลาสต์ และออร์แกเนลล์อื่นที่ปรากฏในเซลล์ยูแคริโอต[47] อย่างไรก็ตาม แบคทีเรียบางชนิดมีออร์แกเนลล์ที่มีโปรตีนหุ้ม (protein-bound organelle) อยู่ในไซโทพลาซึม เช่นคาร์บอกซิโซม (carboxysome)[48] ซึ่งทำให้เกิดการจัดส่วนการทำงาน (compartmentalisation) สำหรับกระบวนการเมแทบอลิซึมของแบคทีเรีย[49][50] นอกจากนี้แบคทีเรียยังมีไซโทสเกเลทอนที่มีองค์ประกอบหลายชนิด เพื่อควบคุมการจัดตำแหน่ง (localisation) ของโปรตีนและกรดนิวคลิอิกภายในเซลล์ และเพื่อจัดการกระบวนการแบ่งเซลล์[51][52][53]
ปฏิกิริยาชีวเคมีที่สำคัญ เช่นการสร้างพลังงาน เกิดขึ้นจากความลดหลั่นในความเข้มข้นระหว่างสองฝั่งของเยื่อหุ้ม ทำใหเกิดความต่างศักย์ในที่คล้ายคลึงกับแบตเตอรี การขาดเยื่อหุ้มภายใน ซึ่งเป็นปกติของแบคทีเรีย หมายความว่าปฏิกิริยาดังเช่นการขนส่งอิเล็กตรอน เกิดขึ้นที่เยื่อหุ้มเซลล์ ระหว่างไซโทพลาซึมกับภายนอกเซลล์หรือเพอริพลาซึม (periplasm)[54] อย่างไรก็ตาม แบคทีเรียที่สามารถสังเคราะห์ด้วยแสงได้หลายชนิดมีเยื่อหุ้มเซลล์ที่พับทบไปมาหลายครั้ง และกินพื้นที่ส่วนใหญ่ของเซลล์ด้วยเยื่อสำหรับรวบรวมแสง (light-gathering membrane)[55] ซึ่งโครงสร้างรวบรวมแสงนี้อาจก่อตัวเป็นโครงสร้างหุ้มด้วยลิพิดที่เรียกว่า คลอโรโซม (chlorosome) ในแบคทีเรียกำมะถันสีเขียว[56]
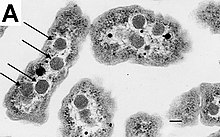
แบคทีเรียไม่มีนิวเคลียสที่มีเยื่อหุ้ม และสารพันธุกรรมมักเป็นโครโมโซมแบบวงกลมของดีเอ็นเอเพียงหนึ่งวงอยู่ภายในไซโทพลาซึมที่มีรูปร่างไม่แน่นอน เรียกว่า นิวคลีออยด์ (nucleoid)[57] นิวคลีออยด์บรรจุโครโมโซมที่มีโปรตีนมาเกาะ และอาร์เอ็นเอ ไว้ภายใน เช่นเดียวกับสิ่งมีชีวิตอื่น แบคทีเรียมีไรโบโซมสำหรับการผลิตโปรตีน แต่โครงสร้างของไรโบโซมในแบคทีเรียแตกต่างจากของยูแคริโอตและอาร์เคีย[58]
แบคทีเรียบางชนิดสร้างแกรนูลลเพื่อกักเก็บสารอาหารไว้ภายในเซลล์ เช่น ไกลโคเจน[59], โพลิฟอสเฟต[60], ซัลเฟอร์[61], หรือโพลิไฮดรอกซีอัลคาโนเอต[62] บางชนิด เช่นไซยาโนแบคทีเรียที่สามารถสังเคราะห์ด้วยแสงได้ สามารถสร้างแวคิวโอลแก๊สสำหรับควบคุมการลอยตัว ทำให้แบคทีเรียสามารถเคลื่อนที่ขึ้นหรือลงไปที่ระดับความลึกต่าง ๆ ของแหล่งน้ำ ซึ่งมีความเข้มแสงและความเข้มข้นของสารอาหารแตกต่างกันไป[63]
โครงสร้างภายนอกเซลล์
ถัดจากเยื่อหุ้มเซลล์ออกมาคือผนังเซลล์ อันประกอบขึ้นจากเปปทิโดไกลแคน (เรียกอีกอย่างว่ามูรีน; peptidoglycan, murein) ซึ่งประกอบด้วยสายพอลิแซ็กคาไรด์ที่เชื่อมกันด้วยเพปไทด์ที่มีกรดอะมิโนแบบเด็กซ์โทร[64] ผนังเซลล์ของแบคทีเรียต่างจากของพืชและเห็ดรา ซึ่งสร้างขึ้นจากเซลลูโลสและไคทินตามลำดับ[65] นอกจากนี้ยังมีความแตกต่างจากผนังเซลล์ของอาร์เคีย ซึ่งไม่มีเพปทิโดไกลแคน ผนังเซลล์มีความสำคัญต่อการอยู่รอดของแบคทีเรียหลายชนิด ยาปฏิชีวนะเพนิซิลิน (สร้างโดยเห็ดราทีเรียกว่า Penicillium) สามารถฆ่าแบคทีเรียด้วยการยับยั้งขั้นตอนหนึ่งของการสังเคราะห์เพปทิโดไกลแคน[65]
แบคทีเรียมีผนังเซลล์สองประเภทคร่าว ๆ ซึ่งจำแนกแบคทีเรียออกเป็นแบคทีเรียแกรมบวก (Gram-positive bacteria) และแบคทีเรียแกรมลบ (Gram-negative bacteria) โดยต้นกำเนิดของชื่อมาจากปฏิกิริยาของเซลล์ที่มีต่อการย้อมสีแกรม (Gram stain) อันเป็นการทดสอบเพื่อจำแนกสปีชีส์ของแบคทีเรียที่ปฏิบัติกันมาอย่างยาวนาน[66]
แบคทีเรียแกรมบวกมีมีผนังเซลล์ที่หนา อันประกอบเพปทิโดไกลแคนและกรดเทโคอิกหลายชั้น ในทางตรงกันข้าม แบคทีเรียแกรมลบมีผนังเซลล์ที่ค่อนข้างบาง ประกอบด้วยชั้นเพปทิโดไกลแคนไม่กี่ชั้นล้อมรอบด้วยเยื่อลิพิดชั้นที่สองที่มีลิโพพอลิแซกคาไรด์และลิโพโปรตีน แบคทีเรียส่วนมากมีผนังเซลล์แบบแกรมลบ และมีเพียงแบคทีเรียในไฟลัม Firmicutes และ Actinobacteria (ซึ่งก่อนหน้านี้รู้จักกันในชื่อแบคทีเรียแกรมบวกที่มี C+G ต่ำ และ C+G สูง ตามลำดับ) ที่การจัดเรียงผนังเซลล์ผิดไปจากแบคทีเรียแกรมบวกชนิดอื่น[67] การที่แบคทีเรียมีโครงสร้างผนังเซลล์ที่หลากหลายทำให้แต่ละชนิดมีความไวต่อต่อยาปฏิชีวนะแตกต่างกัน ตัวอย่างเช่น แวนโคมัยซินสามารถฆ่าได้เพียงแบคทีเรียแกรมบวก และไม่มีประสิทธิภาพต่อเชื้อแบคทีเรียแกรมลบเช่น Haemophilus influenzae หรือ Pseudomonas aeruginosa[68] แบคทีเรียบางชนิดมีผนังเซลล์ที่ไม่สามารถจัดจำแนกได้ว่าเป็นแบบแกรมบวกหรือแบบแกรมลบ กลุ่มนี้มีแบคทีเรียที่มีความสำคัญทางคลินิกรวมอยู่ด้วย เช่น Mycobacteria ที่มีผนังเพปทิโดไกลแคนที่หนา แต่ก็มีเยื่อลิพิดที่สองมาหุ้มอีกชั้นหนึ่ง[69]
แบคทีเรียหลายชนิดมีชั้นเอส (S-layer, surface layer) เป็นโมเลกุลเป็นโปรตีนที่เรียงตัวกันอย่างแน่นหนามาปกคลุมด้านนอกเซลล์[70] ชั้นนี้ช่วยป้องกันพื้นผิวของเวลล์จากปัจจัยภายนอกเชิงกายภาพและเคมี และยังสามารถทำหน้าที่เป็นฉนวนป้องกันการแพร่ของมหโมเลกุล ชั้นเอสนี้มีหน้าที่ที่หลากหลาย เป็นต้นว่าทำหน้าที่เป็นปัจจัยก่อ่โรคใน Campylobacter และบรรจุเอนไซม์พื้นผิวใน Bacillus stearothermophilus แต่ส่วนใหญ่ยังไม่ได้รับการศึกษาอย่างเพียงพอ[71]

แฟลเจลลาเป็นโครงสร้างโปรตีนแข็งเกร็ง มีเส้นผ่านศูนย์กลาง 20 นาโนเมตร และยาวได้ถึง 20 ไมโครเมตร ใช้สำหรับการเคลื่อนที่ แฟลเจลลาถูกขับเคลื่อนโดยพลังงานที่ถูกปลดปล่อยออกมาจากการแลกเปลี่ยนไอออนไปตามระดับศักย์ไฟฟ้าเคมีระหว่างเยื่อหุ้มเซลล์[72]
ฟิมเบรีย (fimbriae) หรือ "พิไลยึดเกาะ (attachment pili)" เป็นเส้นใยละเอียดของโปรตีน มักมีเส้นผ่านศูนย์กลางประมาณ 2–10 นาโนเมตร และมีความยาวได้หลายนาโนเมตร ฟิมเบรียมีกระจายอยู่ทั่วพื้นผิวของเซลล์ และมีลักษณะคล้ายเส้นขนละเอียดเมื่อนำไปส่องดูใต้กล้องจุลทรรศน์อิเล็กตรอน เชื่อกันว่าฟิมเบรียมีส่วนเกี่ยวข้องต่อการยึดเกาะกับพื้นผิวแข็งหรือกับเซลล์อื่น และมีส่วนสำคัญต่อความรุนแรงของแบคทีเรียก่อโรคบางชนิด[73] พิไล (pili; พหูพจน์ pilus) เป็นรยางค์ในระดับเซลล์ มีขนาดใหญ่กว่าฟิมเบรียเล็กน้อย สามารถใช้เพื่อขนส่งสารพันธุกรรมระหว่างเซลล์แบคทีเรียระหว่างกระบวนที่เรียกว่าคอนจูเกชัน (conjugation) โดยมีชื่อเรียกว่า คอนจูเกชันพิไล หรือเซ็กส์พิไล (ดูที่หัวข้อพันธุศาสตร์แบคทีเรียด้านล่าง)[74] นอกจากนี้ยังสามารถทำให้เกิดการเคลื่อนไหว ซึ่งพิไลชนิดนี้จะเรียกว่า พิไลชนิด 4 (type IV pili)[75]
แบคทีเรียหลายชนิดสร้างไกลโคแคลิกซ์ขึ้นมาล้อมรอบเซลล์ ซึ่งมีความซับซ้อนของโครงสร้างแตกต่างกันไป มีตั้งแต่ชั้นเมือกของอิกซ์ตราเซลลูลาร์พอลิเมอริกซับสแตนซ์ (extracellular polymeric substance) ที่ไร้ระเบียบ ไปจนถึงแคปซูลที่มีโครงสร้างจัดตัวเป็นระเบียบ โครงสร้างเหล่านี้ช่วยปกป้องเซลล์จากการถูกเซลล์ยูแคริโอต เช่น แมโครฟาจ (ส่วนหนึ่งของระบบภูมิคุ้มกัน)[76] กลืนกิน นอกจากนี้ยังสามารถทำหน้าที่เป็นแอนติเจน (antigen), เกี่ยวข้องกับการรู้จำของเซลล์, ช่วยในการยึดเกาะกับพื้นผิว ไปจนถึงการสร้างฟิล์มชีวภาพ[77]
การประกอบหน่วยต่าง ๆ โครงสร้างภายนอกเซลล์ขึ้นอยู่กับระบบการหลั่งสารของแบคทีเรียที่มีอยู่หลายระบบ ระบบเหล่านี้ขนส่งโปรตีนจากไซโทพลาซึมออกไปยังเพอริพลาซึม หรือออกไปยังสิ่งแวดล้อมรอบเซลล์ ระบบการหลั่งหลายประเภทเป็นที่รู้จักและมักมีความสำคัญต่อศักยภาพก่อโรคของเชื้อ จึงมีการศึกษากันอย่างเข้มข้น[78]
เอนโดสปอร์
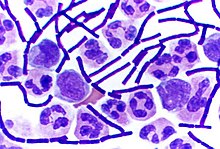
แบคทีเรียแกรมบวกบางสกุลเช่น Bacillus, Clostridium, Sporohalobacter, Anaerobacter, และ Heliobacterium สามารถสร้างโครงสร้างสำหรับพักตัวที่มีความทนทานสูง เรียกว่า เอนโดสปอร์ (endospore)[79] โดยพัฒนาขึ้นอยู่ภายในไซโทพลาซึมของเซลล์[80] ปกติหนึ่งสปอร์ต่อหนึ่งเซลล์ แต่ละเอนโดสปอร์มีแกนกลางเป็นดีเอ็นเอและไรโบโซม ล้อมรอบด้วยชั้นคอร์เทกซ์ (cortex layer) ซึ่งมีเปลือกอันประกอบขึ้นจากเพปทิโดไกลแคนและโปรตีนหลายชนิดมาหุ้มอีกชั้นหนึ่ง[80]
เอนโดสปอร์ไม่แสดงกระบวนการเมแทบอลิซึมที่สามารถตรวจพบได้ และสามารถเอาชีวิตรอดจากสิ่งกดดันทางเคมีและฟิสิกส์ในระดับสุดขั้วได้ เช่นรังสียูวีความเข้มข้นสูง, การแผ่รังสีแกมมา, สารซักฟอก, สารฆ่าเชื้อ, ความร้อน, การแช่แข็ง, ความดัน, และการทำแห้งสนิท[81] ในสภาพจำศีลเช่นนี้ แบคทีเรียสามารถมีชีวิตได้ถึงหลายล้านปี[82][83][84] เอนโดสปอร์ยังทำให้แบคทีเรียมีชีวิตรอดจากสภาวะสุญญากาศและรังสีในอวกาศ เป็นไปได้ว่าแบคทีเรียกระจายไปทั่วเอกภพด้วยฝุ่นอวกาศ, สะเก็ดดาว, ดาวเคราะห์น้อย, ดาวหาง, วัตถุคล้ายดาวเคราะห์ (planetoid), หรือผ่านกระบวนการแพนสเปอร์เมียแบบมีการกำกับ (directed panspermia)[85][86] แบคทีเรียที่สร้างเอนโดสปอร์สามารถทำให้เกิดโรคได้ ตัวอย่างเช่น แอนแทรกซ์ซึ่งเกิดจากการหายใจเอาเอนโดสปอร์ของ Bacillus anthracis เข้าสู่ร่างกาย, และบาดทะยักที่เกิดจากบาดแผลถูกแทงปนเปื้อนเอนโดสปอร์ของ Clostridium tetani[87]
อ้างอิง
- ↑ 1.0 1.1 Woese CR, Kandler O, Wheelis ML (June 1990). "Towards a natural system of organisms: proposal for the domains Archaea, Bacteria, and Eucarya". Proceedings of the National Academy of Sciences of the United States of America. 87 (12): 4576–79. Bibcode:1990PNAS...87.4576W. doi:10.1073/pnas.87.12.4576. PMC 54159. PMID 2112744.
- ↑ Pavan ME, และคณะ (May 2018). "Proposal for a new classification of a deep branching bacterial phylogenetic lineage: transfer of Coprothermobacter proteolyticus and Coprothermobacter platensis to Coprothermobacteraceae fam. nov., within Coprothermobacterales ord. nov., Coprothermobacteria classis nov. and Coprothermobacterota phyl. nov. and emended description of the family Thermodesulfobiaceae". Int. J. Syst. Evol. Microbiol. 68 (5): 1627–32. doi:10.1099/ijsem.0.002720. PMID 29595416. S2CID 4470260.
- ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อWoese1977 - ↑ Fredrickson JK, Zachara JM, Balkwill DL, Kennedy D, Li SM, Kostandarithes HM, Daly MJ, Romine MF, Brockman FJ (July 2004). "Geomicrobiology of high-level nuclear waste-contaminated vadose sediments at the Hanford site, Washington state". Applied and Environmental Microbiology. 70 (7): 4230–41. doi:10.1128/AEM.70.7.4230-4241.2004. PMC 444790. PMID 15240306.
- ↑ Dudek NK, Sun CL, Burstein D (2017). "Novel Microbial Diversity and Functional Potential in the Marine Mammal Oral Microbiome" (PDF). Current Biology. 27 (24): 3752–3762. doi:10.1016/j.cub.2017.10.040. PMID 29153320. S2CID 43864355.
- ↑ Fang H, Kang J, Zhang D (January 2017). "12: a review and future perspectives". Microbial Cell Factories. 16 (1): 15. doi:10.1186/s12934-017-0631-y. PMC 5282855. PMID 28137297.
- ↑ Moore SJ, Warren MJ (June 2012). "The anaerobic biosynthesis of vitamin B12". Biochemical Society Transactions. 40 (3): 581–6. doi:10.1042/BST20120066. PMID 22616870.
- ↑ Graham RM, Deery E, Warren MJ (2009). "18: Vitamin B12: Biosynthesis of the Corrin Ring". ใน Warren MJ, Smith AG (บ.ก.). Tetrapyrroles Birth, Life and Death. New York, NY: Springer-Verlag. p. 286. doi:10.1007/978-0-387-78518-9_18. ISBN 978-0-387-78518-9.
- ↑ Miller A, Korem M, Almog R, Galboiz Y (June 2005). "Vitamin B12, demyelination, remyelination and repair in multiple sclerosis". Journal of the Neurological Sciences. 233 (1–2): 93–7. doi:10.1016/j.jns.2005.03.009. PMID 15896807. S2CID 6269094.
- ↑ Whitman WB, Coleman DC, Wiebe WJ (June 1998). "Prokaryotes: the unseen majority". Proceedings of the National Academy of Sciences of the United States of America. 95 (12): 6578–83. Bibcode:1998PNAS...95.6578W. doi:10.1073/pnas.95.12.6578. PMC 33863. PMID 9618454.
- ↑ Bar-On YM, Phillips R, Milo R (June 2018). "The biomass distribution on Earth" (PDF). Proceedings of the National Academy of Sciences of the United States of America. 115 (25): 6506–6511. doi:10.1073/pnas.1711842115. PMC 6016768. PMID 29784790.
- ↑ Forbes SL (2008). "Decomposition Chemistry in a Burial Environment". ใน Tibbett M, Carter DO (บ.ก.). Soil Analysis in Forensic Taphonomy. CRC Press. pp. 203–223. ISBN 978-1-4200-6991-4.
- ↑ Sears CL (October 2005). "A dynamic partnership: celebrating our gut flora". Anaerobe. 11 (5): 247–51. doi:10.1016/j.anaerobe.2005.05.001. PMID 16701579.
- ↑ "2002 WHO mortality data". เก็บจากแหล่งเดิมเมื่อ 23 ตุลาคม 2013. สืบค้นเมื่อ 20 มกราคม 2007.
- ↑ "Metal-Mining Bacteria Are Green Chemists". Science Daily. 2 กันยายน 2010. เก็บจากแหล่งเดิมเมื่อ 31 สิงหาคม 2017.
- ↑ Ishige T, Honda K, Shimizu S (April 2005). "Whole organism biocatalysis". Current Opinion in Chemical Biology. 9 (2): 174–80. doi:10.1016/j.cbpa.2005.02.001. PMID 15811802.
- ↑ βακτήριον. Liddell, Henry George; Scott, Robert; A Greek–English Lexicon at Perseus Project.
- ↑ βακτηρία in Liddell and Scott.
- ↑ bacterium เก็บถาวร 27 มกราคม 2011 ที่ เวย์แบ็กแมชชีน, on Oxford Dictionaries.
- ↑ Harper, Douglas. "bacteria". Online Etymology Dictionary.
- ↑ Schopf JW (July 1994). "Disparate rates, differing fates: tempo and mode of evolution changed from the Precambrian to the Phanerozoic". Proceedings of the National Academy of Sciences of the United States of America. 91 (15): 6735–42. Bibcode:1994PNAS...91.6735S. doi:10.1073/pnas.91.15.6735. PMC 44277. PMID 8041691.
- ↑ DeLong EF, Pace NR (August 2001). "Environmental diversity of bacteria and archaea". Systematic Biology. 50 (4): 470–78. CiteSeerX 10.1.1.321.8828. doi:10.1080/106351501750435040. PMID 12116647.
- ↑ Brown JR, Doolittle WF (December 1997). "Archaea and the prokaryote-to-eukaryote transition". Microbiology and Molecular Biology Reviews. 61 (4): 456–502. doi:10.1128/.61.4.456-502.1997. PMC 232621. PMID 9409149.
- ↑ Di Giulio M (December 2003). "The universal ancestor and the ancestor of bacteria were hyperthermophiles". Journal of Molecular Evolution. 57 (6): 721–30. Bibcode:2003JMolE..57..721D. doi:10.1007/s00239-003-2522-6. PMID 14745541. S2CID 7041325.
- ↑ Battistuzzi FU, Feijao A, Hedges SB (November 2004). "A genomic timescale of prokaryote evolution: insights into the origin of methanogenesis, phototrophy, and the colonization of land". BMC Evolutionary Biology. 4: 44. doi:10.1186/1471-2148-4-44. PMC 533871. PMID 15535883.
- ↑ Homann, Martin; และคณะ (23 July 2018). "Microbial life and biogeochemical cycling on land 3,220 million years ago" (PDF). Nature Geoscience. 11 (9): 665–671. Bibcode:2018NatGe..11..665H. doi:10.1038/s41561-018-0190-9. S2CID 134935568.
- ↑ Poole AM, Penny D (January 2007). "Evaluating hypotheses for the origin of eukaryotes". BioEssays. 29 (1): 74–84. doi:10.1002/bies.20516. PMID 17187354.
- ↑ Dyall SD, Brown MT, Johnson PJ (April 2004). "Ancient invasions: from endosymbionts to organelles". Science. 304 (5668): 253–7. Bibcode:2004Sci...304..253D. doi:10.1126/science.1094884. PMID 15073369. S2CID 19424594.
- ↑ Lang BF, Gray MW, Burger G (1999). "Mitochondrial genome evolution and the origin of eukaryotes". Annual Review of Genetics. 33: 351–97. doi:10.1146/annurev.genet.33.1.351. PMID 10690412.
- ↑ McFadden GI (December 1999). "Endosymbiosis and evolution of the plant cell". Current Opinion in Plant Biology. 2 (6): 513–19. doi:10.1016/S1369-5266(99)00025-4. PMID 10607659.
- ↑ Schulz HN, Jorgensen BB (2001). "Big bacteria". Annual Review of Microbiology. 55: 105–37. doi:10.1146/annurev.micro.55.1.105. PMID 11544351. S2CID 18168018.
- ↑ Williams C (2011). "Who are you calling simple?". New Scientist. 211 (2821): 38–41. doi:10.1016/S0262-4079(11)61709-0.
- ↑ Robertson J, Gomersall M, Gill P (November 1975). "Mycoplasma hominis: growth, reproduction, and isolation of small viable cells". Journal of Bacteriology. 124 (2): 1007–18. doi:10.1128/JB.124.2.1007-1018.1975. PMC 235991. PMID 1102522.
- ↑ Velimirov B (2001). "Nanobacteria, Ultramicrobacteria and Starvation Forms: A Search for the Smallest Metabolizing Bacterium". Microbes and Environments. 16 (2): 67–77. doi:10.1264/jsme2.2001.67.
- ↑ Dusenbery, David B (2009). Living at Micro Scale, pp. 20–25. Harvard University Press, Cambridge, Massachusetts ISBN 978-0-674-03116-6.
- ↑ Yang DC, Blair KM, Salama NR (March 2016). "Staying in Shape: the Impact of Cell Shape on Bacterial Survival in Diverse Environments". Microbiology and Molecular Biology Reviews. 80 (1): 187–203. doi:10.1128/MMBR.00031-15. PMC 4771367. PMID 26864431.
- ↑ Cabeen MT, Jacobs-Wagner C (August 2005). "Bacterial cell shape". Nature Reviews. Microbiology. 3 (8): 601–10. doi:10.1038/nrmicro1205. PMID 16012516. S2CID 23938989.
- ↑ Young KD (September 2006). "The selective value of bacterial shape". Microbiology and Molecular Biology Reviews. 70 (3): 660–703. doi:10.1128/MMBR.00001-06. PMC 1594593. PMID 16959965.
- ↑ Claessen D, Rozen DE, Kuipers OP, Søgaard-Andersen L, van Wezel GP (February 2014). "Bacterial solutions to multicellularity: a tale of biofilms, filaments and fruiting bodies". Nature Reviews. Microbiology. 12 (2): 115–24. doi:10.1038/nrmicro3178. PMID 24384602. S2CID 20154495.
- ↑ Shimkets LJ (1999). "Intercellular signaling during fruiting-body development of Myxococcus xanthus". Annual Review of Microbiology. 53: 525–49. doi:10.1146/annurev.micro.53.1.525. PMID 10547700.
- ↑ Kaiser D (2004). "Signaling in myxobacteria". Annual Review of Microbiology. 58: 75–98. doi:10.1146/annurev.micro.58.030603.123620. PMID 15487930.
- ↑ Donlan RM (September 2002). "Biofilms: microbial life on surfaces". Emerging Infectious Diseases. 8 (9): 881–90. doi:10.3201/eid0809.020063. PMC 2732559. PMID 12194761.
- ↑ Branda SS, Vik S, Friedman L, Kolter R (January 2005). "Biofilms: the matrix revisited". Trends in Microbiology. 13 (1): 20–26. doi:10.1016/j.tim.2004.11.006. PMID 15639628.
- ↑ Davey ME, O'toole GA (December 2000). "Microbial biofilms: from ecology to molecular genetics". Microbiology and Molecular Biology Reviews. 64 (4): 847–67. doi:10.1128/MMBR.64.4.847-867.2000. PMC 99016. PMID 11104821.
- ↑ Donlan RM, Costerton JW (April 2002). "Biofilms: survival mechanisms of clinically relevant microorganisms". Clinical Microbiology Reviews. 15 (2): 167–93. doi:10.1128/CMR.15.2.167-193.2002. PMC 118068. PMID 11932229.
- ↑ Slonczewski JL, Foster JW (2013). Microbiology : an Evolving Science (Third ed.). New York: W W Norton. p. 82. ISBN 978-0393123678.
- ↑ Lodish H, Berk A, Kaiser CA, Krieger M, Bretscher A, Ploegh H, Amon A, Scott MP (2013). Molecular Cell Biology (7th ed.). WH Freeman. p. 13. ISBN 978-1429234139.
- ↑ Kerfeld CA, Sawaya MR, Tanaka S, Nguyen CV, Phillips M, Beeby M, Yeates TO (August 2005). "Protein structures forming the shell of primitive bacterial organelles". Science. 309 (5736): 936–38. Bibcode:2005Sci...309..936K. CiteSeerX 10.1.1.1026.896. doi:10.1126/science.1113397. PMID 16081736. S2CID 24561197.
- ↑ Bobik TA (May 2006). "Polyhedral organelles compartmenting bacterial metabolic processes". Applied Microbiology and Biotechnology. 70 (5): 517–25. doi:10.1007/s00253-005-0295-0. PMID 16525780. S2CID 8202321.
- ↑ Yeates TO, Kerfeld CA, Heinhorst S, Cannon GC, Shively JM (September 2008). "Protein-based organelles in bacteria: carboxysomes and related microcompartments". Nature Reviews. Microbiology. 6 (9): 681–91. doi:10.1038/nrmicro1913. PMID 18679172. S2CID 22666203.
- ↑ Gitai Z (March 2005). "The new bacterial cell biology: moving parts and subcellular architecture". Cell. 120 (5): 577–86. doi:10.1016/j.cell.2005.02.026. PMID 15766522. S2CID 8894304.
- ↑ Shih YL, Rothfield L (September 2006). "The bacterial cytoskeleton". Microbiology and Molecular Biology Reviews. 70 (3): 729–54. doi:10.1128/MMBR.00017-06. PMC 1594594. PMID 16959967.
- ↑ Norris V, den Blaauwen T, Cabin-Flaman A, Doi RH, Harshey R, Janniere L, Jimenez-Sanchez A, Jin DJ, Levin PA, Mileykovskaya E, Minsky A, Saier M, Skarstad K (March 2007). "Functional taxonomy of bacterial hyperstructures". Microbiology and Molecular Biology Reviews. 71 (1): 230–53. doi:10.1128/MMBR.00035-06. PMC 1847379. PMID 17347523.
- ↑ Harold FM (June 1972). "Conservation and transformation of energy by bacterial membranes". Bacteriological Reviews. 36 (2): 172–230. doi:10.1128/MMBR.36.2.172-230.1972. PMC 408323. PMID 4261111.
- ↑ Bryant DA, Frigaard NU (November 2006). "Prokaryotic photosynthesis and phototrophy illuminated". Trends in Microbiology. 14 (11): 488–96. doi:10.1016/j.tim.2006.09.001. PMID 16997562.
- ↑ Psencík J, Ikonen TP, Laurinmäki P, Merckel MC, Butcher SJ, Serimaa RE, Tuma R (August 2004). "Lamellar organization of pigments in chlorosomes, the light harvesting complexes of green photosynthetic bacteria". Biophysical Journal. 87 (2): 1165–72. Bibcode:2004BpJ....87.1165P. doi:10.1529/biophysj.104.040956. PMC 1304455. PMID 15298919.
- ↑ Thanbichler M, Wang SC, Shapiro L (October 2005). "The bacterial nucleoid: a highly organized and dynamic structure". Journal of Cellular Biochemistry. 96 (3): 506–21. doi:10.1002/jcb.20519. PMID 15988757. S2CID 25355087.
- ↑ Poehlsgaard J, Douthwaite S (November 2005). "The bacterial ribosome as a target for antibiotics". Nature Reviews. Microbiology. 3 (11): 870–81. doi:10.1038/nrmicro1265. PMID 16261170. S2CID 7521924.
- ↑ Yeo M, Chater K (มีนาคม 2005). "The interplay of glycogen metabolism and differentiation provides an insight into the developmental biology of Streptomyces coelicolor". Microbiology. 151 (Pt 3): 855–61. doi:10.1099/mic.0.27428-0. PMID 15758231. เก็บจากแหล่งเดิมเมื่อ 29 กันยายน 2007.
- ↑ Shiba T, Tsutsumi K, Ishige K, Noguchi T (มีนาคม 2000). "Inorganic polyphosphate and polyphosphate kinase: their novel biological functions and applications". Biochemistry. Biokhimiia. 65 (3): 315–23. PMID 10739474. เก็บจากแหล่งเดิมเมื่อ 25 กันยายน 2006.
- ↑ Brune DC (June 1995). "Isolation and characterization of sulfur globule proteins from Chromatium vinosum and Thiocapsa roseopersicina". Archives of Microbiology. 163 (6): 391–99. doi:10.1007/BF00272127. PMID 7575095. S2CID 22279133.
- ↑ Kadouri D, Jurkevitch E, Okon Y, Castro-Sowinski S (2005). "Ecological and agricultural significance of bacterial polyhydroxyalkanoates". Critical Reviews in Microbiology. 31 (2): 55–67. doi:10.1080/10408410590899228. PMID 15986831. S2CID 4098268.
- ↑ Walsby AE (March 1994). "Gas vesicles". Microbiological Reviews. 58 (1): 94–144. doi:10.1128/MMBR.58.1.94-144.1994. PMC 372955. PMID 8177173.
- ↑ van Heijenoort J (March 2001). "Formation of the glycan chains in the synthesis of bacterial peptidoglycan". Glycobiology. 11 (3): 25R–36R. doi:10.1093/glycob/11.3.25R. PMID 11320055. S2CID 46066256.
- ↑ 65.0 65.1 Koch AL (October 2003). "Bacterial wall as target for attack: past, present, and future research". Clinical Microbiology Reviews. 16 (4): 673–87. doi:10.1128/CMR.16.4.673-687.2003. PMC 207114. PMID 14557293.
- ↑ Gram, HC (1884). "Über die isolierte Färbung der Schizomyceten in Schnitt- und Trockenpräparaten". Fortschr. Med. 2: 185–89.
- ↑ Hugenholtz P (2002). "Exploring prokaryotic diversity in the genomic era". Genome Biology. 3 (2): REVIEWS0003. doi:10.1186/gb-2002-3-2-reviews0003. PMC 139013. PMID 11864374.
- ↑ Walsh FM, Amyes SG (October 2004). "Microbiology and drug resistance mechanisms of fully resistant pathogens" (PDF). Current Opinion in Microbiology. 7 (5): 439–44. doi:10.1016/j.mib.2004.08.007. PMID 15451497.
- ↑ Alderwick LJ, Harrison J, Lloyd GS, Birch HL (March 2015). "The Mycobacterial Cell Wall – Peptidoglycan and Arabinogalactan". Cold Spring Harbor Perspectives in Medicine. 5 (8): a021113. doi:10.1101/cshperspect.a021113. PMC 4526729. PMID 25818664.
- ↑ Engelhardt H, Peters J (December 1998). "Structural research on surface layers: a focus on stability, surface layer homology domains, and surface layer-cell wall interactions". Journal of Structural Biology. 124 (2–3): 276–302. doi:10.1006/jsbi.1998.4070. PMID 10049812.
- ↑ Beveridge TJ, Pouwels PH, Sára M, Kotiranta A, Lounatmaa K, Kari K, Kerosuo E, Haapasalo M, Egelseer EM, Schocher I, Sleytr UB, Morelli L, Callegari ML, Nomellini JF, Bingle WH, Smit J, Leibovitz E, Lemaire M, Miras I, Salamitou S, Béguin P, Ohayon H, Gounon P, Matuschek M, Koval SF (June 1997). "Functions of S-layers". FEMS Microbiology Reviews. 20 (1–2): 99–149. doi:10.1016/S0168-6445(97)00043-0. PMID 9276929.
- ↑ Kojima S, Blair DF (2004). The bacterial flagellar motor: structure and function of a complex molecular machine. International Review of Cytology. Vol. 233. pp. 93–134. doi:10.1016/S0074-7696(04)33003-2. ISBN 978-0-12-364637-8. PMID 15037363.
- ↑ Beachey EH (March 1981). "Bacterial adherence: adhesin-receptor interactions mediating the attachment of bacteria to mucosal surface". The Journal of Infectious Diseases. 143 (3): 325–45. doi:10.1093/infdis/143.3.325. PMID 7014727.
- ↑ Silverman PM (February 1997). "Towards a structural biology of bacterial conjugation". Molecular Microbiology. 23 (3): 423–29. doi:10.1046/j.1365-2958.1997.2411604.x. PMID 9044277. S2CID 24126399.
- ↑ Costa TR, Felisberto-Rodrigues C, Meir A, Prevost MS, Redzej A, Trokter M, Waksman G (June 2015). "Secretion systems in Gram-negative bacteria: structural and mechanistic insights". Nature Reviews. Microbiology. 13 (6): 343–59. doi:10.1038/nrmicro3456. PMID 25978706. S2CID 8664247.
- ↑ Stokes RW, Norris-Jones R, Brooks DE, Beveridge TJ, Doxsee D, Thorson LM (October 2004). "The glycan-rich outer layer of the cell wall of Mycobacterium tuberculosis acts as an antiphagocytic capsule limiting the association of the bacterium with macrophages". Infection and Immunity. 72 (10): 5676–86. doi:10.1128/IAI.72.10.5676-5686.2004. PMC 517526. PMID 15385466.
- ↑ Daffé M, Etienne G (1999). "The capsule of Mycobacterium tuberculosis and its implications for pathogenicity". Tubercle and Lung Disease. 79 (3): 153–69. doi:10.1054/tuld.1998.0200. PMID 10656114.
- ↑ Finlay BB, Falkow S (June 1997). "Common themes in microbial pathogenicity revisited". Microbiology and Molecular Biology Reviews. 61 (2): 136–69. doi:10.1128/.61.2.136-169.1997. PMC 232605. PMID 9184008.
- ↑ Nicholson WL, Munakata N, Horneck G, Melosh HJ, Setlow P (September 2000). "Resistance of Bacillus endospores to extreme terrestrial and extraterrestrial environments". Microbiology and Molecular Biology Reviews. 64 (3): 548–72. doi:10.1128/MMBR.64.3.548-572.2000. PMC 99004. PMID 10974126.
- ↑ 80.0 80.1 McKenney PT, Driks A, Eichenberger P (January 2013). "The Bacillus subtilis endospore: assembly and functions of the multilayered coat". Nature Reviews. Microbiology. 11 (1): 33–44. doi:10.1038/nrmicro2921. PMID 23202530. S2CID 205498395.
- ↑ Nicholson WL, Fajardo-Cavazos P, Rebeil R, Slieman TA, Riesenman PJ, Law JF, Xue Y (August 2002). "Bacterial endospores and their significance in stress resistance". Antonie van Leeuwenhoek. 81 (1–4): 27–32. doi:10.1023/A:1020561122764. PMID 12448702. S2CID 30639022.
- ↑ Vreeland RH, Rosenzweig WD, Powers DW (October 2000). "Isolation of a 250 million-year-old halotolerant bacterium from a primary salt crystal". Nature. 407 (6806): 897–900. Bibcode:2000Natur.407..897V. doi:10.1038/35038060. PMID 11057666. S2CID 9879073.
- ↑ Cano RJ, Borucki MK (May 1995). "Revival and identification of bacterial spores in 25- to 40-million-year-old Dominican amber". Science. 268 (5213): 1060–64. Bibcode:1995Sci...268.1060C. doi:10.1126/science.7538699. PMID 7538699.
- ↑ "Row over ancient bacteria". BBC News (ภาษาอังกฤษแบบบริติช). 2001-06-07. สืบค้นเมื่อ 2020-04-26.
- ↑ Nicholson WL, Schuerger AC, Setlow P (April 2005). "The solar UV environment and bacterial spore UV resistance: considerations for Earth-to-Mars transport by natural processes and human spaceflight". Mutation Research. 571 (1–2): 249–64. doi:10.1016/j.mrfmmm.2004.10.012. PMID 15748651.
- ↑ "Colonising the galaxy is hard. Why not send bacteria instead?". The Economist. 2018-04-12. ISSN 0013-0613. สืบค้นเมื่อ 2020-04-26.
- ↑ Hatheway CL (January 1990). "Toxigenic clostridia". Clinical Microbiology Reviews. 3 (1): 66–98. doi:10.1128/CMR.3.1.66. PMC 358141. PMID 2404569.
