โพรเพน
| |||
| |||
| ชื่อ | |||
|---|---|---|---|
| Preferred IUPAC name
Propane[1] | |||
| Systematic IUPAC name
Tricarbane (never recommended[1]) | |||
| เลขทะเบียน | |||
3D model (JSmol)
|
|||
| 1730718 | |||
| ChEBI | |||
| ChEMBL | |||
| เคมสไปเดอร์ | |||
| ECHA InfoCard | 100.000.753 | ||
| EC Number |
| ||
| เลขอี | E944 (glazing agents, ...) | ||
| 25044 | |||
| KEGG | |||
ผับเคม CID
|
|||
| RTECS number |
| ||
| UNII | |||
| UN number | 1978 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| คุณสมบัติ[2] | |||
| C3H8 | |||
| มวลโมเลกุล | 44.097 g·mol−1 | ||
| ลักษณะทางกายภาพ | แก๊สไม่มีสี | ||
| กลิ่น | ไม่มีกลิ่น | ||
| ความหนาแน่น | 2.0098 kg/m3 (at 0 °C, 101.3 kPa) | ||
| จุดหลอมเหลว | −187.7 °C; −305.8 °F; 85.5 K | ||
| จุดเดือด | −42.25 to −42.04 °C; −44.05 to −43.67 °F; 230.90 to 231.11 K | ||
| 47 mg⋅L−1 (at 0 °C) | |||
| log P | 2.236 | ||
| ความดันไอ | 853.16 kPa (at 21.1 องศาเซลเซียส (70.0 องศาฟาเรนไฮต์)) | ||
| กรด | Propanium | ||
| −40.5 × 10−6 cm3/mol | |||
| อุณหเคมี | |||
ความจุความร้อน (C)
|
73.60 J⋅K−1⋅mol−1 | ||
Std enthalpy of
formation (ΔfH⦵298) |
−105.2–104.2 kJ⋅mol−1 | ||
Std enthalpy of
combustion (ΔcH⦵298) |
−2.2197–2.2187 MJ⋅mol−1 | ||
| ความอันตราย | |||
| GHS labelling: | |||

| |||
| อันตราย | |||
| H220 | |||
| P210 | |||
| NFPA 704 (fire diamond) | |||
| จุดวาบไฟ | −104 องศาเซลเซียส (−155 องศาฟาเรนไฮต์; 169 เคลวิน) | ||
| 470 องศาเซลเซียส (878 องศาฟาเรนไฮต์; 743 เคลวิน) | |||
| ขีดจำกัดการระเบิด | 2.37–9.5% | ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible)
|
TWA 1000 ppm (1800 mg/m3)[3] | ||
REL (Recommended)
|
TWA 1000 ppm (1800 mg/m3)[3] | ||
IDLH (Immediate danger)
|
2100 ppm[3] | ||
| สารประกอบอื่นที่เกี่ยวข้องกัน | |||
alkanesที่เกี่ยวข้อง
|
|||
สารประกอบที่เกี่ยวข้อง
|
Diiodohydroxypropane | ||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
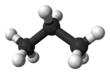
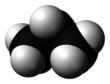
โพรเพน (อังกฤษ: propane) เป็นสารประกอบอินทรีย์ที่มีสูตรเคมี C3H8 ลักษณะเป็นแก๊สไม่มีสี ไม่มีกลิ่น มีความไวไฟสูง สามารถบีบอัดให้เป็นของเหลวเพื่อใช้ขนส่งได้ ค้นพบโดยมาร์เซลแล็ง แบร์เธโลในปี ค.ศ. 1857[5] และถูกพบในน้ำมันดิบความหนาแน่นต่ำโดยเอดมันด์ โรนัลส์ในปี ค.ศ. 1864[6] ชื่อโพรเพนมาจากกรดโพรพิโอนิก ซึ่งมีรากศัพท์มาจากคำภาษากรีกโบราณสองคำคือ πρῶτος (prôtos) แปลว่า แรก และ πίων (píōn) แปลว่า ไขมัน[7]
โพรเพนเป็นสารไฮโดรคาร์บอนชนิดแอลเคนที่มีคาร์บอน 3 อะตอมเชื่อมต่อกันด้วยพันธะเดี่ยว โพรเพนมีโครงสร้างเป็นโซ่ตรง ทำให้มีพื้นที่ผิวสัมผัสระหว่างโมเลกุลมาก ส่งผลให้มีแรงระหว่างโมเลกุลมากตามไปด้วย การมีแรงระหว่างโมเลกุลมากทำให้ต้องใช้พลังงานในการสลายแรงดังกล่าวของโพรเพนมากกว่าแอลเคนที่มีโมเลกุลน้อยกว่าอย่างมีเทนและอีเทน[8][9] นอกจากนี้ยังเป็นสารไม่มีขั้วเนื่องจากอะตอมไฮโดรเจนและคาร์บอนมีค่าอิเล็กโตรเนกาทิวิตีใกล้เคียงกัน จึงไม่เกิดโมเมนต์ขั้วคู่ (dipole moment) ส่งผลให้โพรเพนไม่ละลายน้ำ แต่ละลายในตัวทำละลายมีขั้ว เช่น เฮกเซน เบนซีน โทลูอีน และคลอโรฟอร์ม[10] โพรเพนเป็นหนึ่งในสารที่พบในน้ำมันดิบและแก๊สธรรมชาติ และเป็นสารกลุ่มแรก ๆ ที่ถูกแยกออกเมื่อมีการกลั่นลำดับส่วนเนื่องจากมีจุดเดือดต่ำกว่าสารชนิดอื่น[11]
โพรเพนใช้เป็นแก๊สเชื้อเพลิง และเป็นแก๊สปิโตรเลียมเหลว (LPG) หรือแก๊สหุงต้มเมื่อผสมกับบิวเทนและสารไฮโดรคาร์บอนอื่น ๆ นอกจากนี้โพรเพนยังใช้เป็นสารขับดัน สารทำความเย็น และเป็นสารตั้งต้นในการผลิตโพรพีน ซึ่งเป็นวัตถุดิบหลักในอุตสาหกรรมพลาสติก[12][13] โพรเพนเป็นสารระเหยที่เมื่อสูดดมเข้าไปจะทำให้ปวดศีรษะ เวียนศีรษะ คลื่นไส้ อ่อนแรง หมดสติและอาจเสียชีวิตจากภาวะขาดอากาศหายใจ[14][15]
อ้างอิง
[แก้]- ↑ 1.0 1.1 "Front Matter". Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 4. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
Similarly, the retained names 'ethane', 'propane', and 'butane' were never replaced by systematic names 'dicarbane', 'tricarbane', and 'tetracarbane' as recommended for analogues of silane, 'disilane’; phosphane, 'triphosphane'; and sulfane, 'tetrasulfane'.
- ↑ Record of Propane in the GESTIS Substance Database of the Institute for Occupational Safety and Health
- ↑ 3.0 3.1 3.2 NIOSH Pocket Guide to Chemical Hazards. "#0524". National Institute for Occupational Safety and Health (NIOSH).
- ↑ GOV, NOAA Office of Response and Restoration, US. "PROPANE – CAMEO Chemicals – NOAA". cameochemicals.noaa.gov.
- ↑ "Comptes rendus hebdomadaires des séances de l'Académie des sciences" (ภาษาฝรั่งเศส). 140. 1905.
{{cite journal}}: Cite journal ต้องการ|journal=(help) - ↑ Roscoe, H.E.; Schorlemmer, C. (1881). Treatise on Chemistry. Vol. 3. Macmillan. pp. 144–145.
- ↑ "propane". Online Etymology Dictionary. สืบค้นเมื่อ December 8, 2019.
- ↑ Rawn, J. David; Ouellette, Robert J. (2018). Organic Chemistry: Structure, Mechanism, Synthesis. Cambridge, Massachusetts, US: Academic Press. p. 116. ISBN 9780128128398.
- ↑ "Physical Properties of Alkanes". Chemistry LibreTexts. February 13, 2019. สืบค้นเมื่อ December 8, 2019.
- ↑ "Chemical Formula for Propane". Sciencing. October 25, 2018. สืบค้นเมื่อ December 8, 2019.
- ↑ Nolan, Dennis P. (2013). Handbook of Fire & Explosion Protection Engineering Principles for Oil, Gas, Chemical, & Related Facilities. Amsterdam, Netherlands: Elsevier Science. p. 35. ISBN 9780080946313.
- ↑ "Propane". Britannica. สืบค้นเมื่อ December 8, 2019.
- ↑ "Propane". New World Encyclopedia. June 16, 2019. สืบค้นเมื่อ December 8, 2019.
- ↑ "Propane - Tox Town". National Institutes of Health (NIH). คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2019-12-07. สืบค้นเมื่อ December 8, 2019.
- ↑ "Propane poisoning". MedlinePlus Medical Encyclopedia. January 12, 2019. สืบค้นเมื่อ December 8, 2019.