บรอมอไทมอลบลู

| |
| |
| ชื่อ | |
|---|---|
| Preferred IUPAC name
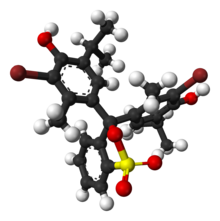
3,3-Bis[3-bromo-4-hydroxy-2-methyl-5-(propan-2-yl)phenyl]-2,1λ6-benzoxathiole-1,1(3H)-dione | |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| เคมสไปเดอร์ | |
| ECHA InfoCard | 100.000.884 |
| EC Number |
|
ผับเคม CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| C27H28Br2O5S | |
| มวลโมเลกุล | 624.38 g·mol−1 |
| ความหนาแน่น | 1.25 g/cm3 |
| จุดหลอมเหลว | 202 องศาเซลเซียส (396 องศาฟาเรนไฮต์; 475 เคลวิน) |
| ละลายได้บ้างในน้ำ[1] | |
| pKa | 7.0 |
| ความอันตราย | |
| GHS labelling: | |

| |
| เตือน | |
| H302, H315, H319 | |
| P264, P270, P280, P301+P312, P302+P352, P305+P351+P338, P321, P330, P332+P313, P337+P313, P362, P501 | |
| NFPA 704 (fire diamond) | |
| เอกสารข้อมูลความปลอดภัย (SDS) | ThermoFisher Scientific |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
บรอมอไทมอลบลู หรือ โบรโมไทมอลบลู (อังกฤษ: bromothymol blue) เป็นตัวบ่งชี้พีเอชที่ใช้ในการวัดระดับ pH ของสารที่มีความใกล้เคียงกับความเป็นกลาง (pH 7) และใช้ทั่วไปในการตรวจหากรดคาร์บอนิกในของเหลว บรอมอไทมอลบลูในสถานะของแข็งมีลักษณะเป็นผงผลึกสีชมพู–น้ำตาลอ่อน ไม่มีกลิ่น[2] มีสูตรเคมีคือ C27H28Br2O5S มีความหนาแน่น 1.25 g/cm3 และจุดหลอมเหลวที่ 202 °C[3]
บรอมอไทมอลบลูสามารถสังเคราะห์ได้จากการเติมโบรมีนในไทมอลบลูในสารละลายกรดแกลเชียลแอซีติก[4] บรอมอไทมอลบลูละลายในน้ำ อีเทอร์ และสารละลายเอเควียสของแอลคาไลน์ ละลายได้น้อยในตัวทำละลายไม่มีขั้ว เช่น เบนซีน โทลูอีน ไซลีน และไม่ละลายในปิโตรเลียมอีเทอร์[5] บรอมอไทมอลบลูมีความไวไฟ 1 ตาม NFPA 704 หรือต้องให้ความร้อนสูงเป็นเวลานานจึงจะลุกติดไฟ และเป็นสารก่อระคายเคือง[6]
บรอมอไทมอลบลูเป็นส่วนประกอบหนึ่งของยูนิเวอร์แซลอินดิเคเตอร์ เมื่ออยู่ในรูปสารละลายเป็นกลางจะมีสีเขียว บรอมอไทมอลบลูปรากฏเป็นสีเหลืองเมื่อทดสอบกับสารละลายที่มี pH 6 และจะเปลี่ยนเป็นสีน้ำเงินเมื่อทดสอบกับสารละลายที่มี pH สูงกว่า 7.6[7] บรอมอไทมอลบลูใช้ในการศึกษาการสังเคราะห์แสงหรือการหายใจ เพราะจะเปลี่ยนเป็นสีเหลืองเมื่อมีคาร์บอนไดออกไซด์ซึ่งมีฤทธิ์เป็นกรด[8] วิธีทดสอบอย่างง่ายคือหายใจออกในหลอดที่มีสารละลายเป็นกลางของบรอมอไทมอลบลู เมื่อคาร์บอนไดออกไซด์ทำปฏิกิริยากับสารละลายจะก่อให้เกิดกรดคาร์บอนิก และสีของสารละลายจะเปลี่ยนเป็นสีเหลือง
สาเหตุหนึ่งที่ทำให้บรอมอไทมอลบลูเกิดความเปลี่ยนแปลงเป็นสีเหลือง–น้ำเงิน เกิดจากการรับโปรตอนและเสียโปรตอนในโครงสร้าง กล่าวคือเมื่อบรอมอไทมอลบลูทำปฏิกิริยากับกรดจะได้รับโปรตอนเพิ่ม ทำให้มีค่าความดูดกลืนแสงสูงสุดที่ 427 nm จึงปรากฏเป็นสีเหลือง ขณะที่เมื่อทดสอบกับสารละลายเบส บรอมอไทมอลบลูจะเสียโปรตอนทำให้มีค่าดูดกลืนแสงสูงสุดที่ 602 nm และปรากฏเป็นสีน้ำเงิน[9] ส่วนการเปลี่ยนแปลงของสีในช่วง pH 6–7.6 เกิดจากโครงสร้างแบบคอนจูเกตของบรอมอไทมอลบลูที่มีหนึ่งหมู่ดึงอิเล็กตรอน (อะตอมโบรมีน) และสองหมู่ให้อิเล็กตรอน (หมู่แทนที่แอลคิล)[10]
นอกจากใช้เป็นตัวบ่งชี้พีเอช มีการใช้บรอมอไทมอลบลูในการตรวจหาการแตกของถุงน้ำคร่ำก่อนกำหนด โดยน้ำคร่ำจะมีค่า pH มากกว่า 7.2 และจะทำให้บรอมอไทมอลบลูเปลี่ยนเป็นสีน้ำเงิน ขณะที่ค่า pH ทั่วไปในช่องคลอดจะเป็นกรด หากทดสอบด้วยบรอมอไทมอลบลูแล้วเป็นสีน้ำเงินแสดงว่าภายในช่องคลอดอาจมีน้ำคร่ำอยู่ อย่างไรก็ตามการทดสอบด้วยวิธีนี้อาจให้ผลบวกปลอมเนื่องจากอาจเกิดจากภาวะอื่น เช่น มีเลือดหรือน้ำอสุจิในช่องคลอด หรือเกิดโรคช่องคลอดอักเสบจากเชื้อแบคทีเรีย[11]
อ้างอิง[แก้]
- ↑ "Archived copy". คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 2015-11-26. สืบค้นเมื่อ 2015-12-11.
{{cite web}}: CS1 maint: archived copy as title (ลิงก์) - ↑ "Bromothymol Blue". Fisher Scientific. สืบค้นเมื่อ November 20, 2020.
- ↑ "Bromothymol Blue". Byjus. สืบค้นเมื่อ November 20, 2020.
- ↑ "Bromothymol blue" (PDF). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2020-11-27. สืบค้นเมื่อ 4 April 2020.
- ↑ O'Neil, Maryadele J (2006). The Merck Index. Merck Research Laboratory. p. 1445. ISBN 978-0-911910-00-1.
- ↑ "Bromothumol blue - MSDS" (PDF). Northwest Missouri State University. คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2015-05-23. สืบค้นเมื่อ November 20, 2020.
- ↑ "Indicators". Imperial College London. สืบค้นเมื่อ November 20, 2020.
- ↑ Sabnis R. W. (2007). Handbook of Acid-Base Indicators. CRC Press. ISBN 978-0-8493-8218-5.
- ↑ Nahhal; และคณะ (18 July 2012). "Thin film optical BTB pH sensors using sol–gel method in presence of surfactants" (PDF). International Nano Letters. 2 (16): 3. doi:10.1186/2228-5326-2-16. สืบค้นเมื่อ 18 November 2014.
- ↑ De Meyer, Thierry (March 2014). "Substituent effects on absorption spectra of pH indicators: An experimental and computational study of sulfonphthaleine dyes". Dyes and Pigments. 102: 241–250. doi:10.1016/j.dyepig.2013.10.048. hdl:1854/LU-4353650.
- ↑ "Bromothymol blue". National Biochemicals Corp. สืบค้นเมื่อ November 20, 2020.
แหล่งข้อมูลอื่น[แก้]
 วิกิมีเดียคอมมอนส์มีสื่อเกี่ยวกับ บรอมอไทมอลบลู
วิกิมีเดียคอมมอนส์มีสื่อเกี่ยวกับ บรอมอไทมอลบลู- "โบรโมไทมอลบลู อินดิเคเตอร์ - เอกสารข้อมูลความปลอดภัย" (PDF). Merck Millipore.

