กลุ่มอาการโรคไตเนื่องจากโรคตับ
| กลุ่มอาการโรคไตเนื่องจากโรคตับ (Hepatorenal syndrome) | |
|---|---|
 ในผู้ป่วยกลุ่มอาการโรคไตเนื่องจากโรคตับนั้นพยาธิวิทยาของเนื้อตับจะเปลี่ยนแปลงไปในขณะที่ไตจะปกติ ภาพนี้แสดงให้เห็นเนื้อเยื่อของตับซึ่งมีสภาพตับแข็ง ย้อมด้วยสี trichrome stain | |
| บัญชีจำแนกและลิงก์ไปภายนอก | |
| ICD-10 | K76.7 |
| ICD-9 | 572.4 |
| OMIM | 105800 |
| DiseasesDB | 5810 |
| MedlinePlus | 000489 |
| eMedicine | med/1001 article/907429 |
| MeSH | D006530 |
กลุ่มอาการโรคไตเนื่องจากโรคตับ (อังกฤษ: Hepatorenal syndrome, HRS) เป็นภาวะทางการแพทย์อย่างหนึ่งซึ่งอาจเป็นอันตรายถึงชีวิต ทำให้ผู้ป่วยโรคตับแข็งหรือตับวายเต็มขั้นมีการทำงานของไตเสื่อมลงอย่างเฉียบพลัน โรคนี้มักเป็นอันตรายถึงแก่ชีวิตหากไม่ได้รับการผ่าตัดเปลี่ยนตับ การรักษาอื่นๆ เช่นการฟอกเลือด อาจช่วยชะลอการดำเนินโรคได้
HRS อาจเกิดกับผู้ป่วยตับแข็ง (ทุกสาเหตุ) ตับอักเสบรุนแรงเนื่องจากแอลกอฮอล์ หรือตับวายเต็มขั้น มักเกิดเพื่อการทำงานของตับแย่ลงอย่างรวดเร็วจากการบาดเจ็บเฉียบพลัน เช่น การติดเชื้อ เลือดออกในทางเดินอาหาร หรือการได้รับยาขับปัสสาวะมากเกินขนาด ถือเป็นภาวะแทรกซ้อนที่ค่อนข้างพบบ่อยของตับแข็ง โดยพบในผู้ป่วยตับแข็งถึง 18% ภายใน 1 ปีตั้งแต่วินิจฉัย และ 39% ภายใน 5 ปีตั้งแต่วินิจฉัย
เชื่อกันว่าเมื่อการทำงานของตับแย่ลงอย่างรวดเร็วจะส่งผลต่อการไหลเวียนของเลือดในระบบไหลเวียนส่วนที่หล่อเลี้ยงลำไส้ ทำให้มีการเปลี่ยนแปลงของการไหลของเลือดและสภาพของหลอดเลือดที่ไปเลี้ยงไต ไตวายที่เกิดจาก HRS เป็นผลที่ตามมาจากการเปลี่ยนแปลงของการไหลเวียนของเลือดเหล่านี้มากกว่าจะเป็นผลที่เกิดจากการบาดเจ็บของไตโดยตรง สภาพของไตนั้นจะค่อนข้างปกติทั้งจากการดูด้วยตาเปล่าและกล้องจุลทรรศน์ ยิ่งกว่านั้นการทำงานของไตยังอาจจะทำงานได้ปกติอีกด้วยหากอยู่ในสภาพแวดล้อมที่ดีกว่า (เช่นสมมติได้มีการปลูกถ่ายไตนี้ไปยังบุคคลที่มีตับปกติ) การวินิจฉัย HRS ขึ้นกับการตรวจทางห้องปฏิบัติการในผู้ป่วยที่มีโอกาสเป็นโรค ปัจจุบันมีการให้คำนิยาม HRS ไว้สองชนิด โดยชนิดที่ 1 ผู้ป่วยจะมีการทำงานของไตที่แย่ลงอย่างรวดเร็ว ในขณะที่ชนิดที่ 2 จะมีความสัมพันธ์กับการมีท้องมานที่รักษาตามปกติด้วยยาขับปัสสาวะแล้วไม่ดีขึ้น
ผู้ป่วยโรคนี้มีโอกาสเสียชีวิตสูงมาก อัตราตายของผู้ป่วย HRS ชนิดที่ 1 สูงกว่า 50% ในระยะสั้นตามบันทึกชุดกรณีผู้ป่วย แนวทางการรักษาระยะยาววิธีเดียวคือการปลูกถ่ายตับ ซึ่งระหว่างที่รอการปลูกถ่ายตับนั้นผู้ป่วย HRS มักได้รับการรักษาอื่นๆ ซึ่งช่วยทำให้ความตึงของหลอดเลือดดีขึ้น พร้อมกับยาและการรักษาประคับประคองอื่นๆ หรือการสร้างทางเชื่อมของระบบไหลเวียนพอร์ทัลและระบบไหลเวียนทั่วร่างกายภายในตับผ่านทางหลอดเลือดดำคอ (TIPS) เพื่อลดความดันในหลอดเลือดดำพอร์ทัล ผู้ป่วยบางคนอาจจำเป็นต้องได้รับการฟอกเลือดเพื่อทดแทนการทำงานของไต หรือเทคนิคใหม่ๆ อย่างการฟอกตับ เป็นต้น
การจำแนกประเภท[แก้]

กลุ่มอาการโรคไตเนื่องจากโรคตับเป็นสาเหตุของภาวะไตวายที่พบบ่อยในผู้ป่วยตับแข็ง หรือในผู้ป่วยตับวายเต็มขั้นแต่พบน้อยกว่า[1] โรคนี้ทำให้มีการหดตัวของหลอดเลือดของไตและการขยายตัวของการไหลเวียนอวัยวะภายในซึ่งมาเลี้ยงลำไส้[2] การจำแนกประเภทของ HRS จัดเป็นชนิดย่อย 2 ชนิดของภาวะไตวาย เรียกเป็น ชนิด (type) ที่ 1 และ 2 ซึ่งทั้งสองชนิดสามารถเกิดได้ทั้งในผู้ป่วยตับแข็งและตับวายเต็มขั้น การวัดการทำงานของไตที่แย่ลงในทั้งสองชนิดนั้นดูได้ทั้งจากระดับครีแอทินินในเลือดที่สูงขึ้นหรือการชำระครีแอทินินในปัสสาวะที่ต่ำลงก็ได้[3]
กลุ่มอาการโรคไตเนื่องจากโรคตับชนิดที่ 1[แก้]
HRS ชนิดที่ 1 มีลักษณะเฉพาะคือเกิดไตวายที่แย่ลงอย่างรวดเร็ว ระดับครีแอทินีนในซีรั่มสูงขึ้นจนถึง 221 μmol/L (2.5 mg/dL) หรือค่าการชำระครีแอทินีนลดลงจนต่ำกว่า 20 mL/min ในเวลาน้อยกว่าสองสัปดาห์ พยากรณ์โรคของผู้ป่วย HRS ชนิดที่ 1 นั้นไม่ดีอย่างมาก มีอัตราตายที่หลังหนึ่งเดือนเกินกว่า 50%[4] ผู้ป่วย HRS ชนิดที่ 1 มักมีอาการไม่สบายชัดเจน อาจมีความดันโลหิตต่ำ และมักจำเป็นต้องได้รับยากระตุ้นกล้ามเนื้อหัวใจหรือสารกระตุ้นการหดตัวกล้ามเนื้อหลอดเลือดเพื่อรักษาระดับความดันเลือดเอาไว้[5]
กลุ่มอาการโรคไตเนื่องจากโรคตับชนิดที่ 2[แก้]
HRS ชนิดที่ 2 แตกต่างจากชนิดที่ 1 โดยมีการเริ่มต้นและการดำเนินโรคช้ากว่า นิยามโดยการมีการเพิ่มขึ้นของระดับครีแอทินีนในซีรั่มจนมากกว่า 133 μmol/L (1.5 mg/dL) หรือค่าการชำระครีแอทินีนน้อยกว่า 40 mL/min และระดับโซเดียมในปัสสาวะน้อยกว่า 10 μmol/L[6] มีผลการดำเนินโรคที่ไม่ดีนักโดยมีค่ามัธยฐานการรอดชีวิตอยู่ที่ประมาณ 6 เดือนหากไม่ได้รับการปลูกถ่ายตับ HRS ชนิดที่ 2 นั้นเชื่อว่าเป็นระดับความรุนแรงหนึ่งของกลุ่มโรคที่สัมพันธ์กับการมีความดันในหลอดเลือดพอร์ทัลสูงซึ่งจะเริ่มต้นจากการมีของเหลวในช่องท้องหรือที่เรียกว่าท้องมาน หากรุนแรงกว่านี้ก็จะเป็นภาวะท้องมานที่ดื้อต่อยาขับปัสสาวะ ซึ่งในภาวะนี้ไตจะไม่สามารถขับโซเดียมเพื่อให้สามารถขับสารน้ำออกได้มากพอแม้จะได้รับยาขับปัสสาวะแล้วก็ตาม ผู้ป่วย HRS ชนิดที่ 2 ส่วนใหญ่มีภาวะท้องมานที่ดื้อต่อยาขับปัสสาวะก่อนที่จะเริ่มมีการเสื่อมของการทำงานของไต[7]
อาการและอาการแสดง[แก้]
ผู้ป่วย HRS ทั้งสองชนิดมีความผิดปกติหลักๆ เหมือนกัน 3 อย่าง ได้แก่ การทำงานของตับผิดปกติ การไหลเวียนของเลือดผิดปกติ และมีไตวาย ความผิดปกติเหล่านี้อาจไม่ทำให้เกิดอาการหรืออาการแสดงใดๆ จนกว่าจะเป็นมาก ผู้ป่วย HRS มักได้รับการวินิจฉัยจากการตรวจพบความผิดปกติจากการตรวจทางห้องปฏิบัติการ ผู้ป่วย HRS มากมีตับแข็งอยู่เดิม ซึ่งอาจมีอาการและอาการแสดงที่คล้ายกันได้ เช่น ดีซ่าน สภาพจิตเปลี่ยนแปลง มีอาการแสดงของภาวะทุพโภชนาการ และมีท้องมาน[2] หากมีท้องมานที่ไม่ตอบสนองต่อการรักษาด้วยยาขับปัสสาวะจะมีความจำเพาะกับ HRS ชนิดที่ 2 มากขึ้น ภาวะปัสสาวะน้อยอาจเกิดเมื่อมีภาวะไตวายมากแล้ว อย่างไรก็ดีผู้ป่วย HRS บางคนอาจยังมีปริมาณปัสสาวะเป็นปกติได้[3] เนื่องจากทั้งอาการและอาการแสดงเหล่านี้ไม่จำเป็นต้องปรากฏในผู้ป่วย HRS จึงไม่มีการบรรจุอาการและอาการแสดงเหล่านี้เข้าเป็นส่วนหนึ่งของเกณฑ์วินิจฉัยไม่ว่าจะเป็นเกณฑ์หลักหรือเกณฑ์รอง ดังนั้นการวินิจฉัย HRS จึงอาศัยว่าผู้ป่วยมีความเสี่ยงต่อการเป็นโรคนี้ ร่วมกับผลการตรวจทางห้องปฏิบัติการ และการตรวจแยกการวินิจฉัยอื่นๆ ออก[3]
สาเหตุ[แก้]
กลุ่มอาการโรคไตเนื่องจากโรคตับมักเกิดกับผู้ป่วยที่มีภาวะตับแข็งและความดันในหลอดเลือดพอร์ทัลสูง ทั้งนี้แม้ HRS อาจเกิดกับผู้ป่วยที่เกิดตับแข็งจากภาวะใดๆ ก็ได้ แต่ก็พบบ่อยกว่าในตับแข็งจากแอลกอฮอล์ โดยเฉพาะเมื่อมีการตรวจพบตับอักเสบจากแอลกอฮอล์จากการตัดชิ้นเนื้อตับออกตรวจ[8] นอกจากนี้ยังอาจเกิดกับผู้ที่ไม่มีตับแข็งอยู่เดิม แต่มีตับวายเฉียบพลันเต็มขั้นก็ได้[3][8]
มีการค้นพบสิ่งกระตุ้นบางอย่างที่ทำให้เกิด HRS ในผู้ป่วยตับแข็งหรือตับวายเต็มขั้นซึ่งมีโอกาสเป็นโรค เช่น การติดเชื้อแบคทีเรีย ตับอักเสบจากแอลกอฮอล์เฉียบพลัน หรือการมีเลือดออกในทางเดินอาหารส่วนบน โดยภาวะเยื่อบุช่องท้องอักเสบเองจากแบคทีเรียซึ่งมีการติดเชื้อของน้ำมานนั้นเป็นสิ่งกระตุ้นให้เกิด HRS ที่พบบ่อยที่สุดในผู้ป่วยตับแข็ง นอกจากนี้ยังอาจถูกกระตุ้นได้จากการรักษาภาวะแทรกซ้อนของโรคตับ เช่น การให้ยาขับปัสสาวะเป็นปริมาณมาก หรือการเจาะระบายน้ำมานออกเป็นปริมาณมากโดยไม่มีการชดเชยสารน้ำที่สูญเสียไปด้วยการให้สารน้ำทางหลอดเลือดดำที่เพียงพอ[8]
การวินิจฉัย[แก้]
ผู้ป่วยตับแข็งหรือตับวายเต็มขั้นอาจมีไตวายจากสาเหตุอื่นๆ ได้มาก จึงไม่ใช่เรื่องง่ายที่จะแยกกลุ่มอาการโรคไตเนื่องจากโรคตับออกจากโรคอื่นๆ ที่ทำให้เกิดภาวะไตวายในผู้ป่วยกลุ่มนี้ ดังนั้นจึงมีการพัฒนาเกณฑ์การวินิจฉัยทั้งเกณฑ์หลักและเกณฑ์รองเพื่อนำมาช่วยในการวินิจฉัยกลุ่มอาการโรคไตเนื่องจากโรคตับ[3]
เกณฑ์วินิจฉัยหลักได้แก่ เป็นโรคตับที่ทำให้เกิดความดันในหลอดเลือดพอร์ทัลสูง; ไตวาย; ไม่มีภาวะช็อค, ติดเชื้อ, ได้รับการรักษาด้วยยาที่เป็นพิษต่อไต, เสียสารน้ำ; ไม่มีการดีขึ้นและคงอยู่ได้ของการทำงานของไตแม้รักษาด้วยการให้น้ำเกลือทางหลอดเลือดดำแล้ว 1.5 ลิตร; ไม่มีโปรตีนในปัสสาวะ; ไม่มีโรคไตหรือการอุดกั้นของทางเดินปัสสาวะจากการตรวจด้วยคลื่นเสียงความถี่สูง[3]
เกณฑ์วินิจฉัยรองได้แก่ ปริมาณปัสสาวะน้อย (น้อยกว่า 500 มิลลิลิตรต่อวัน), ความเข้มข้นของโซเดียมในปัสสาวะต่ำ, ออสโมแลลิตีของปัสสาวะสูงกว่าในเลือด, ไม่มีเม็ดเลือดแดงออกมาในปัสสาวะ, และความเข้มข้นของโซเดียมในซีรั่มน้อยกว่า 130 mmol/L[3]
มีโรคของไตอีกมากที่มีความสัมพันธ์กับโรคตับ ซึ่งการจะวินิจฉัยกลุ่มอาการโรคไตเนื่องจากโรคตับนั้นต้องผ่านการพิสูจน์ว่าไม่เป็นโรคเหล่านี้ก่อน ผู้ป่วยไตวายจากเหตุก่อนไตจะไม่มีความผิดปกติของการทำงานของไต แต่ผู้ป่วย HRS จะมีความผิดปกติของการทำงานของไตที่เกิดจากการที่มีเลือดไปเลี้ยงไตน้อยลงเนื่องจากมีการหดตัวของหลอดเลือด ภาวะไตวายจากเหตุก่อนไตจะทำให้มีความเข้มข้นของโซเดียมในปัสสาวะต่ำได้มากเช่นกัน แต่โรคนี้จะตอบสนองต่อการรักษาด้วยการให้สารน้ำทางหลอดเลือดดำ[3] เนื้อตายเฉพาะส่วนเฉียบพลันของหลอดไตฝอย (ATN) เป็นโรคที่มีความเสียหายที่หลอดไตฝอย และอาจเกิดเป็นภาวะแทรกซ้อนของผู้ป่วยตับแข็งได้จากการได้รับยาที่เป็นพิษต่อไตหรือการมีความดันเลือดต่ำ เนื่องจากไตของผู้ป่วยโรคนี้จะมีความเสียหายที่หลอดไตฝอยทำให้ไตไม่สามารถดูดโซเดียมกลับจากปัสสาวะได้เต็มที่ จึงมีระดับความเข้มข้นของโซเดียมในปัสสาวะสูง แตกต่างจาก HRS อย่างไรก็ดีในกรณีผู้ป่วยตับแข็ง อาจไม่เป็นไปอย่างตรงไปตรงมาเช่นนี้เสมอไป[5] นอกจากนี้ผู้ป่วย ATN ยังอาจตรวจพบ hyaline cast หรือ muddy-brown cast ในปัสสาวะได้จากการตรวจด้วยกล้องจุลทรรศน์ ในขณะที่มักไม่พบใน HRS เนื่องจากไตไม่ได้ถูกทำลายโดยตรง[3] โรคติดเชื้อไวรัสของตับบางโรค เช่น ตับอักเสบจากไวรัสตับอักเสบ B และ C อาจทำให้เกิดการอักเสบของโกลเมอรูลัสของไตได้[9][10] สาเหตุอื่นๆ ของการเกิดไตวายในผู้ป่วยโรคตับ เช่น พิษจากยา (เช่นยาปฏิชีวนะอย่างเจนตามัยซิน) หรือโรคไตจากสารทึบรังสีซึ่งเกิดจากการได้รับสารทึบรังสีเพื่อการตรวจทางรังสีวิทยาต่างๆ[3]
พยาธิสรีรวิทยา[แก้]

เชื่อว่าไตวายที่เกิดในกลุ่มอาการโรคไตเนื่องจากโรคตับมีสาเหตุมาจากความผิดปกติของความตึงของหลอดเลือดที่ไปเลี้ยงไต[2] ทฤษฎีที่เป็นที่ยอมรับมากที่สุด (เรียกว่า ทฤษฎีการเติมพร่อง (underfill)) กล่าวว่าหลอดเลือดที่ไปเลี้ยงไตนั้นมีการหดตัวเนื่องจากมีการขยายตัวของหลอดเลือดในระบบไหลเวียนอวัยวะภายในซึ่งเป็นกลุ่มหลอดเลือดที่ไปเลี้ยงลำไส้ ซึ่งเป็นผลจากสารกระตุ้นที่ถูกปล่อยออกมาจากตับที่เป็นโรค[4][11] มีการตั้งสมมติฐานว่าไนตริกออกไซด์[12] โพรสตาแกลนดิน[2][13] และสารกระตุ้นหลอดเลือดอื่นๆ[2] เป็นสารตัวกลางที่มีฤทธิ์ในการขยายหลอดเลือดของระบบไหลเวียนอวัยวะภายในในผู้ป่วยตับแข็งอย่างมาก[2] ผลที่เกิดจากปรากฏการณ์นี้ทำให้ร่างกายมีปริมาณเลือดที่ส่งผลต่อการไหลเวียนน้อยลง ทำให้จักซ์ตาโกลเมอรูลาร์ แอปพาราตัสรับรู้ปริมาณเลือดได้น้อยลง จึงมีการหลั่งเรนินและกระตุ้นระบบเรนิน-แองจิโอเทนซินทำให้เกิดการหดตัวของหลอดเลือดทั่วร่างกาย และโดยเฉพาะที่ไต[2] อย่างไรก็ดีผลของปรากฏการณ์นี้ไม่เพียงพอที่จะต้านผลจากสารตัวกลางที่ทำให้เกิดการขยายหลอดเลือดในระบบไหลเวียนอวัยวะภายใน ทำให้ยังคงมีความพร่องของการไหลเวียนที่ไต และทำให้ยิ่งมีการหดตัวของหลอดเลือดที่ไตมากขึ้น นำไปสู่ภาวะไตวาย[11]
งานวิจัยที่ทำเพื่อสนับสนุนทฤษฎีนี้พบว่ามีการลดลงของความต้านทานหลอดเลือดทั่วร่างลดลงในผู้ป่วย HRS แต่อัตราส่วนของปริมาตรเลือดส่งออกจากหัวใจต่อนาทีที่หลอดเลือดแดงฟีเมอรัลและหลอดเลือดแดงไตนั้นสูงขึ้นและต่ำลงตามลำดับ บ่งชี้ว่าการขยายของหลอดเลือดในระบบไหลเวียนอวัยวะภายในมีส่วนเกี่ยวข้องในภาวะไตวาย[14] มีการตั้งทฤษฎีเกี่ยวกับสารที่มีผลต่อหลอดเลือดจำนวนมากว่ามีส่วนเกี่ยวข้องในการทำให้เกิดการเปลี่ยนแปลงของโลหิตพลศาสตร์ทั้งร่างกาย รวมไปถึงเอเทรียล แนทริยูเรติก เพพไทด์[15], โพรสตาไซคลิน, ทรอมบอกเซน A2[16] และเอนโดทอกซิน[4] นอกจากนี้ยังพบว่าการให้ยาที่ต้านการขยายตัวของหลอดเลือดในระบบไหลเวียนอวัยวะภายใน (เช่น ออร์นิเพรสซิน[15] เทอร์ลิเพรสซิน[17] และออคทรีโอไทด์[18]) ทำให้อัตราการกรองที่โกลเมอรูลัสดีขึ้นในผู้ป่วย HRS จึงเป็นการสนับสนุนว่าการขยายตัวของหลอดเลือดในระบบไหลเวียนอวัยวะภายในเป็นส่วนสำคัญในพยาธิกำเนิด
ทฤษฎีการเติมพร่องนี้อาศัยว่ามีการกระตุ้นระบบเรนิน-แองจิโอเทนซิน-อัลโดสเตอโรน ซึ่งทำให้เกิดการดูดโซเดียมกลับจากท่อไตฝอยซึ่งควบคุมโดยอัลโดสเตอโรน สารนี้กระตุ้นมิเนอราโลคอร์ติคอยด์ รีเซพเตอร์ในท่อไตฝอยม้วนส่วนปลาย[7][11] เชื่อกันว่าขั้นตอนนี้เป็นขั้นตอนสำคัญในพยาธิกำเนิดของภาวะท้องมานในผู้ป่วยตับแข็งด้วยเช่นกัน มีการตั้งสมมติฐานว่าการดำเนินโรคจากภาวะท้องมานมาจนถึงกลุ่มอาการโรคไตเนื่องจากโรคตับนั้นเป็นระยะความรุนแรงของสาเหตุเดียวกันคือการที่มีการขยายของหลอดเลือดในระบบไหลเวียนอวัยวะภายในซึ่งทำให้มีทั้งการดื้อต่อยาขับปัสสาวะในภาวะท้องมาน (โดยเฉพาะ HRS ชนิดที่ 2) และการหดตัวของหลอดเลือดที่ไปเลี้ยงไต นำไปสู่การเกิดกลุ่มอาการโรคไตเนื่องจากโรคตับ[7]
การป้องกัน[แก้]

ผู้ป่วยกลุ่มอาการโรคไตเนื่องจากโรคตับมีความเสี่ยงที่จะเสียชีวิตสูงมาก จึงมีความพยายามที่จะระบุตัวผู้ป่วยที่เสี่ยงต่อการเกิด HRS และป้องกันปัจจัยกระตุ้นให้เกิด HRS ในผู้ป่วยกลุ่มนี้ เนื่องจากการติดเชื้อ (โดยเฉพาะเยื่อบุช่องท้องอักเสบเองจากแบคทีเรีย) และภาวะเลือดออกในทางเดินอาหารเป็นทั้งภาวะแทรกซ้อนที่สำคัญในผู้ป่วยตับแข็งและปัจจัยกระตุ้นของ HRS ที่พบบ่อย จึงมีการให้ความสำคัญอย่างมากกับการตรวจและรักษาผู้ป่วยตับแข็งที่มีภาวะเหล่านี้อย่างรวดเร็วเพื่อป้องกัน HRS[5] ปัจจัยกระตุ้นบางอย่างเกิดจากการรักษาภาวะท้องมานและสามารถป้องกันได้ การใช้ยาขับปัสสาวะมากเกินพอดีนั้นควรหลีกเลี่ยง นอกจากนี้ยังมียาอีกหลายชนิดที่ใช้รักษาภาวะแทรกซ้อนของภาวะท้องมานหรือภาวะอื่น (เช่น ยาปฏิชีวนะ) ซึ่งสามารถทำให้ไตมีการทำงานที่แย่ลงจนนำไปสู่ HRS ได้[4][5] การเจาะท้องเอาน้ำมานออกเป็นปริมาณมากเกินไปอาจทำให้มีการเปลี่ยนแปลงของโลหิตพลศาสตร์มากจนกระตุ้น HRS ได้ จึงควรหลีกเลี่ยงในผู้ป่วยที่มีความเสี่ยง การให้อัลบูมินไปพร้อมกันสามารถป้องกันการทำงานผิดปกติของระบบไหลเวียนที่จะเกิดเมื่อมีการเจาะน้ำออกเป็นปริมาณมากได้ ซึ่งอาจสามารถช่วยป้องกันไม่ให้เกิด HRS ได้[19] ในทางกลับกัน สำหรับผู้ป่วยที่มีท้องมานตึงมาก มีการตั้งสมมติฐานว่าการเจาะเอาน้ำมานออกอาจช่วยเหลือการทำงานของไตได้โดยเป็นการลดความดันที่มีต่อหลอดเลือดดำไต[20]
ผู้ป่วยเยื่อบุช่องท้องอักเสบเองจากแบคทีเรีย (SBP) นั้นมีท้องมานอยู่เดิม ต่อมาเกิดการติดเชื้อขึ้นเอง มีความเสี่ยงที่จะเกิด HRS สูงมาก มีงานวิจัยเชิงทดลองแบบสุ่มและมีกลุ่มควบคุมชิ้นหนึ่งแสดงให้เห็นการให้อัลบูมินทางหลอดเลือดดำแก่ผู้ป่วย SBP ในวันแรกที่รับไว้รักษาในโรงพยาบาลและวันที่สามนั้นสามารถลดอัตราการเกิดการเสื่อมของการทำงานของไตและอัตราการตายได้[21]
การรักษา[แก้]
การปลูกถ่ายตับ[แก้]
วิธีการรักษาแบบจำเพาะของกลุ่มอาการโรคไตเนื่องจากโรคตับคือการปลูกถ่ายตับ การรักษาอื่นๆ เป็นได้เพียงการรักษาระหว่างรอปลูกถ่ายเท่านั้น[1][22] แม้การปลูกถ่ายตับจะเป็นการรักษาที่ดีที่สุดของ HRS แต่อัตราการเสียชีวิตของผู้ป่วยหลังปลูกถ่ายในช่วงหนึ่งเดือนแรกก็ยังสูงถึง 25%[23] โดยมีการพบว่าผู้ป่วย HRS ที่มีการทำงานของตับเสียไปอย่างมาก (คะแนน MELD มากกว่า 36) จะมีความเสี่ยงต่อการเสียชีวิตในระยะแรกหลังปลูกถ่ายตับสูงมาก[23] มีงานวิจัยหลายชิ้นที่พบว่าผู้ป่วยบางรายยังมีการทำงานของไตที่แย่ลงอีกหลังรับการปลูกถ่ายตับ แต่การทำงานของไตที่แย่ลงนี้เป็นเพียงชั่วคราวเท่านั้น เชื่อกันว่าเป็นผลจากการใช้ยาที่เป็นพิษต่อไต โดยเฉพาะการได้รับยากดภูมิคุ้มกันเช่นทาโครลิมัสและไซโคลสปอรีนซึ่งเป็นที่ทราบกันโดยทั่วไปว่าทำให้การทำงานของไตแย่ลงได้ อย่างไรก็ดีในระยะยาวนั้นผู้ป่วย HRS ที่ได้รับการปลูกถ่ายตับเกือบทุกคนจะมีการทำงานของไตกลับมาเป็นปกติได้ งานวิจัยหลายชิ้นแสดงให้เห็นว่าอัตราการรอดชีวิตที่เวลา 3 ปีของผู้ป่วยกลุ่มนี้คล้ายคลึงกับกลุ่มผู้ป่วยที่รับการปลูกถ่ายตับด้วยสาเหตุอื่นที่ไม่ใช่ HRS[1][2]
ในช่วงของการรอปลูกถ่ายตับซึ่งผู้ป่วยอาจต้องนอนรักษาในโรงพยาบาลเป็นเวลานานนั้นมีวิธีการอื่นๆ ที่ช่วยประคับประคองการทำงานของไตเอาไว้ได้ วิธีการเหล่านี้ เช่น การให้แอลบูมินทางหลอดเลือดดำ การให้ยาบางอย่าง (ยาที่มีหลักฐานสนับสนุนมากที่สุดคือยาในกลุ่มของวาโซเพรสซินซึ่งทำให้เกิดการหดตัวของหลอดเลือดในระบบไหลเวียนอวัยวะภายใน) การทำทางเชื่อมระหว่างหลอดเลือดเพื่อลดความดันในหลอดเลือดดำพอร์ทัล การฟอกเลือด รวมถึงการฟอกเลือดผ่านระบบฟอกเลือดที่มีเยื่อที่จับกับแอลบูมินซึ่งเรียกว่า molecular adsorbents recirculation system (MARS) หรือการฟอกตับ[2]
การรักษาด้วยยา[แก้]
มีงานวิจัยใหญ่ๆ หลายชิ้นแสดงให้เห็นว่าผู้ป่วยกลุ่มอาการโรคไตเนื่องจากโรคตับหลายรายที่ได้รับการชดเชยสารน้ำในร่างกายด้วยการให้แอลบูมินทางหลอดเลือดดำมีการทำงานของไตดีขึ้น[2][24][25] ปริมาณของแอลบูมินที่ให้นั้นแตกต่างกันออกไป งานวิจัยหนึ่งให้แอลบูมิน 1 กรัมต่อน้ำหนักตัว 1 กิโลกรัมทางหลอดเลือดในวันแรก จากนั้นให้วันละ 20-40 กรัม[26] และยังมีการพบว่าการรักษาด้วยแอลบูมินอย่างเดียวนั้นได้ผลไม่ดีเท่าการรักษาด้วยยาชนิดอื่นร่วมกับแอลบูมิน งานวิจัยส่วนใหญ่ที่ทำในผู้ป่วย HRS ที่ยังไม่ได้รับการปลูกถ่ายตับจะเกี่ยวข้องกับการให้แอลบูมินร่วมกับยาหรือหัตถการอื่นๆ[2][27]
ยาไมโดดรีนเป็นแอลฟาอะโกนิสต์ชนิดหนึ่ง และออคทรีโอไทด์เป็นสารเลียนแบบโซมาโตสเตตินซึ่งเป็นฮอร์โมนที่ควบคุมความตึงของหลอดเลือดในทางเดินอาหาร ยาเหล่านี้ทำให้มีผลหดหลอดเลือดทั่วร่างและยับยั้งการขยายตัวของหลอดเลือดในระบบไหลเวียนอวัยวะภายใน และเมื่อใช้เป็นยาเดี่ยวแล้วพบว่าไม่เกิดประโยชน์ในการรักษาผู้ป่วย HRS[1][2][28] อย่างไรก็ดีงานวิจัยชิ้นหนึ่งทำกับผู้ป่วย HRS 13 คนแสดงให้เห็นว่าการใช้ยาสองชนิดนี้รวมกัน (ให้ไมโดดรีนกินทางปากและออคทรีโอไทด์ฉีดเข้าใต้ผิวหนัง) ทำให้ผู้ป่วยมีการทำงานของไตดีขึ้นเล็กน้อย จนมีผู้ป่วยสามรายที่รอดชีวิตจนได้ออกจากโรงพยาบาล[29] งานวิจัยเชิงสังเกตการณ์แบบไม่มีการสุ่มชิ้นหนึ่งศึกษาผู้ป่วย HRS ที่รักษาด้วยการฉีดออคทรีโอไทด์เข้าชั้นใต้ผิวหนังและให้ไมโดดรีนเป็นยากินนั้นพบว่าที่ระยะเวลา 30 วัน สามารถพบมีจำนวนผู้รอดชีวิตมากขึ้นได้[1][30]
มีการศึกษาจำนวนหนึ่งพบว่าสารเลียนแบบวาโซเพรสซินอย่างออร์นิเพรสซินช่วยการทำงานของไตในผู้ป่วย HRS[1][24][31] แต่การนำมาใช้ยังมีข้อจำกัดเนื่องจากอาจทำให้เกิดการขาดเลือดในอวัยวะสำคัญๆ ได้[1][24] เทอร์ลิเพรสซินเป็นสารเลียนแบบวาโซเพรสซินอีกตัวหนึ่งซึ่งมีการศึกษาขนาดใหญ่ชิ้นหนึ่งพบว่าช่วยการทำงานของไตในผู้ป่วย HRS ได้โดยเกิดการขาดเลือดน้อยกว่า[1][25] อย่างไรก็ดียังมีข้อกังขาในการนำยาต่างๆ มาใช้ในผู้ป่วย HRS อย่างมากเนื่องจากการศึกษาแต่ละชิ้นยังมีความแตกต่างในลักษณะประชากรศึกษา และการที่มีการเลือกนำค่าการทำงานของไตมาเป็นเป้าหมายการรักษาแทนที่จะใช้อัตราการตาย[32]
มีการศึกษาการใช้ยาอื่นๆ ในการรักษา HRS ได้แก่ เพนทอกซีฟิลลีน[33], อะเซทิลซิสทีอีน,[34]> และไมโซโพรสทอล[1][35] แต่ส่วนใหญ่ยังเป็นการศึกษาแบบชุดกรณีผู้ป่วย หรือเป็นกลุ่มย่อยของผู้ป่วยตับอักเสบจากแอลกอฮอล์ในกรณีเพนทอกซีฟิลลีน[1]
การรักษาด้วยหัตถการ[แก้]
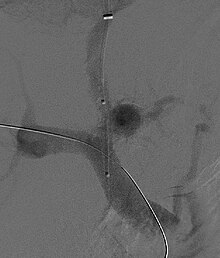
การสร้างทางเชื่อมของระบบไหลเวียนพอร์ทัลและระบบไหลเวียนทั่วร่างกายภายในตับผ่านทางหลอดเลือดดำคอ (อังกฤษ: transjugular intrahepatic portosystemic shunt, TIPS) สามารถลดความดันในหลอดเลือดพอร์ทัลที่สูงได้ โดยวางท่อทางเชื่อมระหว่างหลอดเลือดดำพอร์ทัลและหลอดเลือดดำเฮปาติกโดยสอดสายสวนผ่านทางหลอดเลือดดำอินเทอร์นัลจักกูลาร์หรือหลอดเลือดดำฟีเมอรัลโดยมีการถ่ายภาพรังสีช่วยในการนำทาง ทางทฤษฎีแล้วสามารถลดความดันในหลอดเลือดดำพอร์ทัลและสามารถแก้ไขความผิดปกติทางโลหิตพลศาสตร์ที่จะนำไปสู่กลุ่มอาการโรคไตเนื่องจากโรคตับได้ มีการแสดงให้เห็นแล้วว่าการทำ TIPS สามารถช่วยการทำงานของไตในผู้ป่วย HRS ได้[7][36][37] ภาวะแทรกซ้อนของ TIPS ในการรักษา HRS ซึ่งอาจเกิดขึ้นได้ ได้แก่ การแย่ลงของโรคสมองที่เกิดจากตับ (เนื่องจากสารพิษที่ควรจะถูกกำจัดโดยตับไหลผ่านทางเชื่อมที่สร้างขึ้นเข้าสู่ระบบไหลเวียนทั่วร่างกาย) การไม่สามารถลดความดันในหลอดเลือดดำพอร์ทัลได้มากเท่าที่คาด และการตกเลือด[7][36]
การฟอกตับเป็นการฟอกเลือดนอกร่างกาย ทำเพื่อกำจัดสารพิษออกจากเลือดผ่านทางการเพิ่มวงจรระบบฟอกที่สองซึ่งมีเยื่อซึ่งมีแอลบูมินจับอยู่ มีการแสดงให้เห็นแล้วว่าการทำ molecular adsorbents recirculation system (MARS) นี้มีประโยชน์ในผู้ป่วย HRS ที่รอการปลูกถ่าย อย่างไรก็ดีวิธีการนี้ยังอยู่ช่วงแรกของการพัฒนาเท่านั้น[7][38]
การรักษาทดแทนไต เช่น การชำระเลือดผ่านเยื่อ หรือการชำระเลือดผ่านเยื่อบุช่องท้อง อาจมีความจำเป็นในผู้ป่วยที่รอการปลูกถ่ายตับ โดยการจะเลือกใช้วิธีการรักษาใดนั้นอาจขึ้นอยู่กับสภาพของผู้ป่วย[39] การใช้การแยกสารผ่านเยื่อในผู้ป่วย HRS อาจไม่สามารถทำให้การทำงานของไตกลับเป็นปกติหรือแม้แต่คงไว้ไม่ให้แย่ลงได้ จึงใช้เพียงสำหรับลดภาวะแทรกซ้อนของไตวายจนกว่าจะได้รับการปลูกถ่ายตับเท่านั้น นอกจากนี้ในผู้ป่วย HRS ซึ่งทำให้เกิดความดันเลือดต่ำอยู่แล้วนั้น การชำระเลือดผ่านเยื่ออาจเพิ่มความเสี่ยงต่อการเสียชีวิตขึ้นได้ แม้จะยังไม่มีการศึกษาวิจัยที่เหมาะสมก็ตาม ดังนั้นการรักษาทดแทนไตเหล่านี้ในผู้ป่วย HRS เหล่านี้จึงยังไม่มีบทบาทชัดเจน[2]
วิทยาการระบาด[แก้]
จากการที่ผู้ป่วยกลุ่มอาการโรคไตเนื่องจากโรคตับส่วนใหญ่มีภาวะตับแข็งอยู่ด้วยทำให้ข้อมูลทางวิทยาการระบาดของ HRS จำนวนมากได้มาจากกลุ่มประชากรของผู้ป่วยตับแข็ง ภาวะนี้ค่อนข้างพบได้บ่อย โดย 10% ของผู้ป่วยท้องมานที่ต้องรับไว้รักษาในโรงพยาบาลจะมี HRS[8] การศึกษาแบบชุดกรณีผู้ป่วยย้อนหลังของผู้ป่วยตับแข็งที่ได้รับการรักษาด้วยเทอร์ลิเพรสซินชี้ให้เห็นว่า 20.0% ของภาวะไตวายเฉียบพลันในผู้ป่วยตับแข็งมาจาก HRS ชนิดที่ 1 และ 6.6% มาจาก HRS ชนิดที่ 2[17] ประมาณได้ว่าผู้ป่วยตับแข็งที่มีท้องมาน 18% จะเกิด HRS ภายใน 1 ปีหลังจากได้รับการวินิจฉัยเป็นตับแข็ง และผู้ป่วยกลุ่มนี้ 39% จะมี HRS ภายในห้าปีหลังได้รับการวินิจฉัย[8] ปัจจัยเสี่ยงที่ไม่ขึ้นต่อกันสามอย่างที่ทำให้เกิด HRS ในผู้ป่วยตับแข็งได้แก่ ขนาดของตับ ระดับการทำงานของเอนไซม์เรนินในพลาสมา และระดับความเข้มข้นของโซเดียมในซีรั่ม[8]
พยากรณ์โรคของผู้ป่วยกลุ่มนี้ไม่ดีอย่างมาก หากไม่ได้รับการรักษาจะเสียชีวิตในเวลาอันสั้น[4][8][22] มีการพิสูจน์แล้วว่าความรุนแรงของโรคตับที่คำนวณโดยคะแนน MELD นั้นสามารถนำมาใช้ทำนายการดำเนินโรคได้[23][40] ผู้ป่วยบางคนที่ไม่มีตับแข็งก็เป็น HRS ได้ โดยมีการศึกษาในกลุ่มผู้ป่วยตับอักเสบจากแอลกอฮอล์ชิ้นหนึ่งพบว่ามีอุบัติการณ์อยู่ที่ 20%[33]
ประวัติศาสตร์[แก้]
รายงานแรกๆ ของภาวะไตวายที่เกิดในผู้ป่วยโรคตับเรื้อรังนั้นมีบันทึกไว้ตั้งแต่คริสต์ศตวรรษที่ 19 โดย Frerichs และ Flint[8] อย่างไรก็ดีกลุ่มอาการโรคไตเนื่องจากโรคตับนั้นได้รับการอธิบายครั้งแรกในฐานะภาวะไตวายเฉียบพลันที่เกิดระหว่างการทำผ่าตัดทางเดินน้ำดี[1][41] ไม่นานนักกลุ่มอาการนี้ก็ถูกจัดว่ามีความสัมพันธ์กับโรคตับระยะลุกลาม[22] และในปี ค.ศ. 1950 ก็ถูกนิยามทางคลินิกโดย Sherlock, Hecker, Papper และ Vessin ว่ามีความสัมพันธ์กับความผิดปกติทั้งระบบของโลหิตพลศาสตร์และมีอัตราตายสูง[8][42] ซึ่ง Hecker และ Sherlock ได้ระบุไว้ชัดเจนว่าผู้ป่วย HRS จะมีปัสสาวะน้อย ระดับโซเดียมในปัสสาวะต่ำมาก และไม่มีโปรตีนในปัสสาวะ[1] Murray Epstein เป็นคนแรกที่พบว่าการขยายของหลอดเลือดในการไหลเวียนอวัยวะภายในและการหดตัวของหลอดเลือดที่ไปเลี้ยงไตเป็นความเปลี่ยนแปลงที่สำคัญที่เกิดขึ้นกับโลหิตพลศาสตร์ของผู้ป่วยโรคนี้[43] ลักษณะเฉพาะของโรคซึ่งมีความผิดปกติเชิงหน้าที่ (functional) ของอวัยวะมากกว่าจะเป็นจากความผิดปกติเชิงโครงสร้างอวัยวะและการเสื่อมของการทำงานของไตในโรคนี้นั้นได้รับการยืนยันหนักแน่นขึ้นโดยงานวิจัยที่แสดงให้เห็นว่าไตของผู้ป่วย HRS ที่ได้รับการปลูกถ่ายไปยังผู้ป่วยคนอื่นนั้นยังคงทำงานได้เป็นปกติ[44] นำไปสู่สมมติฐานที่ว่าโรคนี้เป็นโรคที่เกิดความผิดปกติต่อร่างกายทั้งระบบมากกว่าจะเป็นโรคไต ความพยายามอย่างเป็นระบบครั้งแรกเพื่อนิยาม HRS ให้ชัดเจนนั้นเริ่มขึ้นใน ค.ศ. 1994 โดยสมาคมโรคท้องมานนานาชาติ (The International Ascites Club) ซึ่งประกอบด้วยแพทย์ผู้เชี่ยวชาญด้านโรคตับ ในระยะหลังนี้การพัฒนาที่เกี่ยวข้องกับ HRS จะเน้นไปที่การหาสารที่ทำให้เกิดการขยายหลอดเลือดซึ่งทำให้เกิดโรคนี้[8]
อ้างอิง[แก้]
- ↑ 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 Ng CK, Chan MH, Tai MH, Lam CW (February 2007). "Hepatorenal syndrome". Clin Biochem Rev. 28 (1): 11–7. PMC 1904420. PMID 17603637.
- ↑ 2.00 2.01 2.02 2.03 2.04 2.05 2.06 2.07 2.08 2.09 2.10 2.11 2.12 Ginès P, Arroyo V (1999). "Hepatorenal syndrome". J. Am. Soc. Nephrol. 10 (8): 1833–9. doi:10.1681/ASN.V1081833. PMID 10446954. สืบค้นเมื่อ 17 July 2009.
- ↑ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 Arroyo V, Ginès P, Gerbes AL, และคณะ (1996). "Definition and diagnostic criteria of refractory ascites and hepatorenal syndrome in cirrhosis. International Ascites Club". Hepatology. 23 (1): 164–76. doi:10.1002/hep.510230122. PMID 8550036.
- ↑ 4.0 4.1 4.2 4.3 4.4 Arroyo V, Guevara M, Ginès P (2002). "Hepatorenal syndrome in cirrhosis: pathogenesis and treatment". Gastroenterology. 122 (6): 1658–76. doi:10.1053/gast.2002.33575. PMID 12016430.
- ↑ 5.0 5.1 5.2 5.3 Mukherjee, S. Hepatorenal syndrome. emedicine.com. Retrieved on 2 August 2009
- ↑ Ginés P, Arroyo V, Quintero E, และคณะ (1987). "Comparison of paracentesis and diuretics in the treatment of cirrhotics with tense ascites. Results of a randomized study". Gastroenterology. 93 (2): 234–41. doi:10.1016/0016-5085(87)91007-9. PMID 3297907.
- ↑ 7.0 7.1 7.2 7.3 7.4 7.5 Blendis L, Wong F (2003). "The natural history and management of hepatorenal disorders: from pre-ascites to hepatorenal syndrome" (PDF). Clin Med. 3 (2): 154–9. doi:10.7861/clinmedicine.3-2-154. PMC 4952737. PMID 12737373.
- ↑ 8.00 8.01 8.02 8.03 8.04 8.05 8.06 8.07 8.08 8.09 Ginès A, Escorsell A, Ginès P, และคณะ (1993). "Incidence, predictive factors, and prognosis of the hepatorenal syndrome in cirrhosis with ascites". Gastroenterology. 105 (1): 229–36. doi:10.1016/0016-5085(93)90031-7. PMID 8514039.
- ↑ Han SH (2004). "Extrahepatic manifestations of chronic hepatitis B". Clin Liver Dis. 8 (2): 403–18. doi:10.1016/j.cld.2004.02.003. PMID 15481347.
- ↑ Philipneri M, Bastani B (February 2001). "Kidney disease in patients with chronic hepatitis C". Curr Gastroenterol Rep. 3 (1): 79–83. doi:10.1007/s11894-001-0045-0. PMID 11177699. S2CID 21358956.
- ↑ 11.0 11.1 11.2 Schrier RW, Arroyo V, Bernardi M, Epstein M, Henriksen JH, Rodés J (1988). "Peripheral arterial vasodilation hypothesis: a proposal for the initiation of renal sodium and water retention in cirrhosis". Hepatology. 8 (5): 1151–7. doi:10.1002/hep.1840080532. PMID 2971015. S2CID 40231648.
- ↑ Martin PY, Ginès P, Schrier RW (August 1998). "Nitric oxide as a mediator of hemodynamic abnormalities and sodium and water retention in cirrhosis". N. Engl. J. Med. 339 (8): 533–41. doi:10.1056/NEJM199808203390807. PMID 9709047.
- ↑ Epstein M (April 1994). "Hepatorenal syndrome: emerging perspectives of pathophysiology and therapy". J. Am. Soc. Nephrol. 4 (10): 1735–53. doi:10.1681/ASN.V4101735. PMID 8068872.
- ↑ Fernandez-Seara J, Prieto J, Quiroga J, และคณะ (1989). "Systemic and regional hemodynamics in patients with liver cirrhosis and ascites with and without functional renal failure". Gastroenterology. 97 (5): 1304–12. doi:10.1016/0016-5085(89)91704-6. PMID 2676683.
- ↑ 15.0 15.1 Lenz K, Hörtnagl H, Druml W, และคณะ (1991). "Ornipressin in the treatment of functional renal failure in decompensated liver cirrhosis. Effects on renal hemodynamics and atrial natriuretic factor". Gastroenterology. 101 (4): 1060–7. doi:10.1016/0016-5085(91)90734-3. PMID 1832407.
- ↑ Moore K, Ward PS, Taylor GW, Williams R (1991). "Systemic and renal production of thromboxane A2 and prostacyclin in decompensated liver disease and hepatorenal syndrome". Gastroenterology. 100 (4): 1069–77. doi:10.1016/0016-5085(91)90284-r. PMID 2001805.
- ↑ 17.0 17.1 Moreau R, Durand F, Poynard T, Duhamel C, Cervoni JP, Ichaï P, Abergel A, Halimi C, Pauwels M, Bronowicki JP, Giostra E, Fleurot C, Gurnot D, Nouel O, Renard P, Rivoal M, Blanc P, Coumaros D, Ducloux S, Levy S, Pariente A, Perarnau JM, Roche J, Scribe-Outtas M, Valla D, Bernard B, Samuel D, Butel J, Hadengue A, Platek A, Lebrec D, Cadranel JF (April 2002). "Terlipressin in patients with cirrhosis and type 1 hepatorenal syndrome: a retrospective multicenter study". Gastroenterology. 122 (4): 923–30. doi:10.1053/gast.2002.32364. PMID 11910344.
- ↑ Kaffy F, Borderie C, Chagneau C, และคณะ (January 1999). "Octreotide in the treatment of the hepatorenal syndrome in cirrhotic patients". J. Hepatol. 30 (1): 174. doi:10.1016/S0168-8278(99)80025-7. PMID 9927168.
- ↑ Velamati PG, Herlong HF (2006). "Treatment of refractory ascites". Curr Treat Options Gastroenterol. 9 (6): 530–7. doi:10.1007/s11938-006-0009-4. PMID 17081486. S2CID 21860692.
- ↑ Sherlock S, Dooley J (2002). "Chapter 9". Diseases of the liver and biliary system. edition 11. Wiley-Blackwell. ISBN 978-0-632-05582-1.
- ↑ Sort P, Navasa M, Arroyo V, และคณะ (1999). "Effect of intravenous albumin on renal impairment and mortality in patients with cirrhosis and spontaneous bacterial peritonitis". N. Engl. J. Med. 341 (6): 403–9. doi:10.1056/NEJM199908053410603. PMID 10432325.
- ↑ 22.0 22.1 22.2 Wong F, Blendis L (2001). "New challenge of hepatorenal syndrome: prevention and treatment". Hepatology. 34 (6): 1242–51. doi:10.1053/jhep.2001.29200. PMID 11732014. S2CID 22984489.
- ↑ 23.0 23.1 23.2 Xu X, Ling Q, Zhang M, และคณะ (May 2009). "Outcome of patients with hepatorenal syndrome type 1 after liver transplantation: Hangzhou experience". Transplantation. 87 (10): 1514–9. doi:10.1097/TP.0b013e3181a4430b. PMID 19461488. S2CID 25409550.
- ↑ 24.0 24.1 24.2 Guevara M, Ginès P, Fernández-Esparrach G, และคณะ (1998). "Reversibility of hepatorenal syndrome by prolonged administration of ornipressin and plasma volume expansion". Hepatology. 27 (1): 35–41. doi:10.1002/hep.510270107. PMID 9425914.
- ↑ 25.0 25.1 Ortega R, Ginès P, Uriz J, และคณะ (2002). "Terlipressin therapy with and without albumin for patients with hepatorenal syndrome: results of a prospective, nonrandomized study". Hepatology. 36 (4 Pt 1): 941–8. doi:10.1053/jhep.2002.35819. PMID 12297842.
- ↑ Ginès P, Cárdenas A, Arroyo V, Rodés J (2004). "Management of cirrhosis and ascites". N. Engl. J. Med. 350 (16): 1646–54. doi:10.1056/NEJMra035021. PMID 15084697.
- ↑ Martín-Llahí M, Pépin MN, Guevara M, และคณะ (May 2008). "Terlipressin and albumin vs albumin in patients with cirrhosis and hepatorenal syndrome: a randomized study". Gastroenterology. 134 (5): 1352–9. doi:10.1053/j.gastro.2008.02.024. PMID 18471512.
- ↑ Pomier-Layrargues G, Paquin SC, Hassoun Z, Lafortune M, Tran A (2003). "Octreotide in hepatorenal syndrome: a randomized, double-blind, placebo-controlled, crossover study". Hepatology. 38 (1): 238–43. doi:10.1053/jhep.2003.50276. PMID 12830007.
- ↑ Angeli P, Volpin R, Gerunda G, และคณะ (1999). "Reversal of type 1 hepatorenal syndrome with the administration of midodrine and octreotide". Hepatology. 29 (6): 1690–7. doi:10.1002/hep.510290629. PMID 10347109. S2CID 21213418.
- ↑ Esrailian E, Pantangco ER, Kyulo NL, Hu KQ, Runyon BA (2007). "Octreotide/Midodrine therapy significantly improves renal function and 30-day survival in patients with type 1 hepatorenal syndrome". Dig. Dis. Sci. 52 (3): 742–8. doi:10.1007/s10620-006-9312-0. PMID 17235705. S2CID 34909700.
- ↑ Gülberg V, Bilzer M, Gerbes AL (1999). "Long-term therapy and retreatment of hepatorenal syndrome type 1 with ornipressin and dopamine". Hepatology. 30 (4): 870–5. doi:10.1002/hep.510300430. PMID 10498636.
- ↑ Tandon P, Bain VG, Tsuyuki RT, Klarenbach S (May 2007). "Systematic review: renal and other clinically relevant outcomes in hepatorenal syndrome trials". Aliment. Pharmacol. Ther. 25 (9): 1017–28. doi:10.1111/j.1365-2036.2007.03303.x. PMID 17439502.
- ↑ 33.0 33.1 Akriviadis E, Botla R, Briggs W, Han S, Reynolds T, Shakil O (2000). "Pentoxifylline improves short-term survival in severe acute alcoholic hepatitis: a double-blind, placebo-controlled trial". Gastroenterology. 119 (6): 1637–48. doi:10.1053/gast.2000.20189. PMID 11113085.
- ↑ Holt S, Goodier D, Marley R, และคณะ (1999). "Improvement in renal function in hepatorenal syndrome with N-acetylcysteine". Lancet. 353 (9149): 294–5. doi:10.1016/S0140-6736(05)74933-3. PMID 9929029. S2CID 31985301.
- ↑ Clewell JD, Walker-Renard P (1994). "Prostaglandins for the treatment of hepatorenal syndrome". Ann Pharmacother. 28 (1): 54–5. doi:10.1177/106002809402800112. PMID 8123962. S2CID 208875962.
- ↑ 36.0 36.1 Wong F, Pantea L, Sniderman K (2004). "Midodrine, octreotide, albumin, and TIPS in selected patients with cirrhosis and type 1 hepatorenal syndrome". Hepatology. 40 (1): 55–64. doi:10.1002/hep.20262. PMID 15239086. S2CID 43508937.
- ↑ Guevara M, Rodés J (2005). "Hepatorenal syndrome". Int. J. Biochem. Cell Biol. 37 (1): 22–6. doi:10.1016/j.biocel.2004.06.007. PMID 15381144.
- ↑ Mitzner SR, Stange J, Klammt S, และคณะ (2000). "Improvement of hepatorenal syndrome with extracorporeal albumin dialysis MARS: results of a prospective, randomized, controlled clinical trial". Liver Transpl. 6 (3): 277–86. doi:10.1053/lv.2000.6355. PMID 10827226.
- ↑ Witzke O, Baumann M, Patschan D, และคณะ (2004). "Which patients benefit from hemodialysis therapy in hepatorenal syndrome?". J. Gastroenterol. Hepatol. 19 (12): 1369–73. doi:10.1111/j.1440-1746.2004.03471.x. PMID 15610310. S2CID 28850099.
- ↑ Alessandria C, Ozdogan O, Guevara M, และคณะ (2005). "MELD score and clinical type predict prognosis in hepatorenal syndrome: relevance to liver transplantation". Hepatology. 41 (6): 1282–9. doi:10.1002/hep.20687. PMID 15834937. S2CID 205863757.
- ↑ Helwig FC, Schutz CB (1932). "A liver kidney syndrome. Clinical pathological and experimental studies". Surg Gynecol Obstet. 55: 570–80.
- ↑ Hecker R, Sherlock S (December 1956). "Electrolyte and circulatory changes in terminal liver failure". Lancet. 271 (6953): 1121–5. doi:10.1016/s0140-6736(56)90149-0. PMID 13377688.
- ↑ Wadei HM, Mai ML, Ahsan N, Gonwa TA (September 2006). "Hepatorenal syndrome: pathophysiology and management". Clin J Am Soc Nephrol. 1 (5): 1066–79. doi:10.2215/CJN.01340406. PMID 17699328.
- ↑ Koppel MH, Coburn JW, Mims MM, Goldstein H, Boyle JD, Rubini ME (1969). "Transplantation of cadaveric kidneys from patients with hepatorenal syndrome. Evidence for the functional nature of renal failure in advanced liver disease". N. Engl. J. Med. 280 (25): 1367–71. doi:10.1056/NEJM196906192802501. PMID 4890476.
