ผลต่างระหว่างรุ่นของ "มาลาเรีย"
| บรรทัด 103: | บรรทัด 103: | ||
== การป้องกัน == |
== การป้องกัน == |
||
วิธีซึ่งใช้ป้องกันมาลาเรีย ได้แก่ |
วิธีซึ่งใช้ป้องกันมาลาเรีย ได้แก่ ยากรักษาโรค การกำจัดยุงและการป้องกันไม่ให้ถูกยุงกัด ไม่มีวัคซีนมาลาเรีย มาลาเรียจะมีในพื้นที่ซึ่งมีความหนาแน่นของประชากรมนุษย์สูง มีความหนาแน่นของประชากรยุงก้นปล่องสูงและอัตราการส่งผ่านจากมนุษย์สู่ยุงและจากยุงสู่มนุษย์สูง หากปัจจัยข้อหนึ่งข้อใดลดลงมากพอ ปรสิตมาลาเรียจะหายไปจากพื้นที่นั้นในที่สุด ดังที่เกิดขึ้นแล้วในทวีปอเมริกาเหนือ ทวีปยุโรปและตะวันออกกลางบาส่วน ทว่า แม้ว่าปรสิตมาลาเรียจะถูกกำจัดหมดไปจากโลกแล้ว ปรสิตก็อาจกลับมาหากสภาวะต่าง ๆ กลับเอื้ออำนวยต่อการสืบพันธุ์ของปรสิตอีก ยิ่งไปกว่านั้น ราคาต่อคนของการกำจัดยุงก้นปล่องเพิ่มขึ้นเมื่อความหนาแน่นของประชากรลดลง ทำให้วิธีดังกล่าวไม่คุ้มค่าทางเศรษฐกิจในบางพื้นที่<ref name="whqlibdoc"/> |
||
การป้องกันมาลาเรียอาจคุ้มค่ากว่าการรักษาโรคในระยะยาว แต่ประชากรยากจนที่สุดของโลกไม่สามารถจ่ายราคาเริ่มต้นได้ ราคาการควบคุม (ให้ความประจำถิ่นต่ำ) และโครงการกำจัดในแต่ละประเทศมีผลต่างกว้าง ตัวอย่างเช่น ในประเทศจีน ซึ่งรัฐบาลในปี 2553 ประกาศยุทธศาสตร์ในการกำจัดมาลาเรียในจีน การลงทุนที่กำหนดเป็นสัดส่วนน้อยของรายจ่ายสาธารณะด้านสาธารณสุข ในทางตรงข้าม โครงการคล้ายกันใน[[ประเทศแทนซาเนีย]]จะมีมูลค่าประเมินไว้หนึ่งในห้าของงบประมาณสาธารณสุข |
การป้องกันมาลาเรียอาจคุ้มค่ากว่าการรักษาโรคในระยะยาว แต่ประชากรยากจนที่สุดของโลกไม่สามารถจ่ายราคาเริ่มต้นได้ ราคาการควบคุม (ให้ความประจำถิ่นต่ำ) และโครงการกำจัดในแต่ละประเทศมีผลต่างกว้าง ตัวอย่างเช่น ในประเทศจีน ซึ่งรัฐบาลในปี 2553 ประกาศยุทธศาสตร์ในการกำจัดมาลาเรียในจีน การลงทุนที่กำหนดเป็นสัดส่วนน้อยของรายจ่ายสาธารณะด้านสาธารณสุข ในทางตรงข้าม โครงการคล้ายกันใน[[ประเทศแทนซาเนีย]]จะมีมูลค่าประเมินไว้หนึ่งในห้าของงบประมาณสาธารณสุข<ref name="Sabot 2010"/> |
||
=== การควบคุมตัวนำโรค === |
=== การควบคุมตัวนำโรค === |
||
การควบคุมตัวนำโรค หมายถึง วิธีซึ่งใช้ลดมาลาเรียด้วยการลดระดับการส่งผ่านโดยยุง สำหรับการป้องกันส่วนบุคคล [[สารขับไล่แมลง]]อันทรงประสิทธิภาพที่สุดอาศัยดีอีอีทีหรือพิคาริดิน มีการแสดงแล้วว่า [[มุ้ง]]ชุบยาฆ่าแมลงและ[[การพ่นเคมีชนิดมีฤทธิตกค้าง]] (indoor residual spraying) มีประสิทธิภาพสูงในการป้องกันมาลาเรียในเด็กในพื้นที่ซึ่งพบมาลาเรียทั่วไป การรักษาผู้ป่วยยืนยันแล้วอย่างทันท่วงทีด้วยการรักษาแบบผสมที่อาศัยอาร์ติมิซินินยังอาจลดการส่งผ่านได้ |
การควบคุมตัวนำโรค หมายถึง วิธีซึ่งใช้ลดมาลาเรียด้วยการลดระดับการส่งผ่านโดยยุง สำหรับการป้องกันส่วนบุคคล [[สารขับไล่แมลง]]อันทรงประสิทธิภาพที่สุดอาศัยดีอีอีทีหรือพิคาริดิน<ref name="Kajfasz 2009"/> มีการแสดงแล้วว่า [[มุ้ง]]ชุบยาฆ่าแมลงและ[[การพ่นเคมีชนิดมีฤทธิตกค้าง]] (indoor residual spraying) มีประสิทธิภาพสูงในการป้องกันมาลาเรียในเด็กในพื้นที่ซึ่งพบมาลาเรียทั่วไป<ref name="Lengeler 2004"/><ref name="Pluess 2010"/> การรักษาผู้ป่วยยืนยันแล้วอย่างทันท่วงทีด้วยการรักษาแบบผสมที่อาศัยอาร์ติมิซินินยังอาจลดการส่งผ่านได้<ref>{{cite web|last=Palmer|first=J.|title=WHO gives indoor use of DDT a clean bill of health for controlling malaria|url=http://www.who.int/mediacentre/news/releases/2006/pr50/en/|publisher=WHO}}</ref> |
||
มุ้งช่วยกันยุงจากมนุษย์และลดอัตราการติดเชื้อและส่งผ่านมาลาเรีย มักชุบมุ้งด้วยยาฆ่าแมลงซึ่งออกแบบมาเพื่อฆ่ายุงก่อนยุงหาทางผ่านมุ้งได้ มีการประเมินว่ามุ้งชุบยาฆ่าแมลงมีประสิทธิภาพเป็นสองเท่าของมุ้งที่ไม่ได้ชุบยาและให้การป้องกันดีกว่าการไม่ใช้มุ้ง 70% ระหว่างปี 2543 ถึง 2551 มุ้งชุบยาฆ่าแมลงช่วยชีวิตทารก 250,000 คนโดยประมาณใน[[แอฟริกาใต้สะฮารา]] ครัวเรือนราว 13% ในประเทศใต้สะฮารามีมุ้งชุบยาฆ่าแมลง ในปี 2543 มุ้งป้องกันเด็กแอฟริกา 1.7 ล้านคน (1.8%) ที่อาศัยอยู่ในสภาวะมาลาเรียประจำถิ่นคงตัว จำนวนเด็กแอฟริกาที่ใช้มุ้งชุบยาฆ่าแมลงเพิ่มขึ้นเป็น 20.3 ล้านคน (18.5%) ในปี 2550 ทว่าอีก 89.6 ล้านคนยังไม่ได้รับการป้องกัน ในปี 2551 มีการประเมินว่าครัวเรือนแอฟริกา 31% มีมุ้งชุบยาฆ่าแมลงอย่างน้อยหนึ่งหลัง มุ้งส่วนมากถูกชุบด้วย[[ไพรีทรอยด์]] ซึ่งเป็นยาฆ่าแมลงชนิดมีพิษต่ำ การใช้ที่แนะนำคือให้แขวนมุ้งไว้เหนือกลางเตียงให้แขวนอยู่เหนือเตียงทั้งหมดโดยพับขอบเข้า มุ้งชุบไพรีทรอยต์และมุ้งชุบยาฆ่าแมลงที่ออกฤทธิ์นานให้การป้องกันอย่างดีที่สุด และมีประสิทธิถาะมากที่สุดเมื่อใช้ตั้งแต่เย็นถึงเช้า |
มุ้งช่วยกันยุงจากมนุษย์และลดอัตราการติดเชื้อและส่งผ่านมาลาเรีย มักชุบมุ้งด้วยยาฆ่าแมลงซึ่งออกแบบมาเพื่อฆ่ายุงก่อนยุงหาทางผ่านมุ้งได้ มีการประเมินว่ามุ้งชุบยาฆ่าแมลงมีประสิทธิภาพเป็นสองเท่าของมุ้งที่ไม่ได้ชุบยาและให้การป้องกันดีกว่าการไม่ใช้มุ้ง 70%<ref name="Raghavendra 2011"/> ระหว่างปี 2543 ถึง 2551 มุ้งชุบยาฆ่าแมลงช่วยชีวิตทารก 250,000 คนโดยประมาณใน[[แอฟริกาใต้สะฮารา]]<ref name="Howitt 2012"/> ครัวเรือนราว 13% ในประเทศใต้สะฮารามีมุ้งชุบยาฆ่าแมลง<ref name="Miller 2007"/> ในปี 2543 มุ้งป้องกันเด็กแอฟริกา 1.7 ล้านคน (1.8%) ที่อาศัยอยู่ในสภาวะมาลาเรียประจำถิ่นคงตัว จำนวนเด็กแอฟริกาที่ใช้มุ้งชุบยาฆ่าแมลงเพิ่มขึ้นเป็น 20.3 ล้านคน (18.5%) ในปี 2550 ทว่าอีก 89.6 ล้านคนยังไม่ได้รับการป้องกัน<ref>{{cite journal |author= Noor AM, Mutheu JJ, Tatem AJ, Hay SI, Snow RW|title= Insecticide-treated net coverage in Africa: mapping progress in 2000–07 |journal=Lancet |volume=373|issue=9657 |pages=58–67|year=2009 |pmid=19019422 |doi= 10.1016/S0140-6736(08)61596-2 |pmc= 2652031}}</ref> ในปี 2551 มีการประเมินว่าครัวเรือนแอฟริกา 31% มีมุ้งชุบยาฆ่าแมลงอย่างน้อยหนึ่งหลัง มุ้งส่วนมากถูกชุบด้วย[[ไพรีทรอยด์]] ซึ่งเป็นยาฆ่าแมลงชนิดมีพิษต่ำ การใช้ที่แนะนำคือให้แขวนมุ้งไว้เหนือกลางเตียงให้แขวนอยู่เหนือเตียงทั้งหมดโดยพับขอบเข้า มุ้งชุบไพรีทรอยต์และมุ้งชุบยาฆ่าแมลงที่ออกฤทธิ์นานให้การป้องกันอย่างดีที่สุด และมีประสิทธิถาะมากที่สุดเมื่อใช้ตั้งแต่เย็นถึงเช้า<ref>{{harvnb|Schlagenhauf-Lawlor|2008|pp=[http://books.google.com/books?id=54Dza0UHyngC&pg=PA215 215]}}</ref> |
||
การพ่นเคมีชนิดมีฤทธิตกค้างเป็นการพ่นยาฆ่าแมลงบนผนังภายในบ้าน หลังดูดเลือดแล้ว ยุงจำนวนมากจะพักบนพื้นผิวใกล้เคียงขณะย่อย ฉะนั้นหากฉาบผนังบ้านด้วยยาฆ่าแมลง ยุงที่พักอยู่จะตายก่อนที่จะทันได้กัดคนอื่นและส่งผ่านปรสิตมาลาเรีย ในปี 2549 องค์การอนามัยโลกแนะนำให้ใช้ยาฆ่าแมลง 12 ชนิดในการพ่นเคมีชนิดมีฤทธิตกค้าง รวมถึง[[ดีดีที]]และ[[ไซฟลูทริน]]และ[[เดลตาเมทริน]]ในกลุ่มไพรีทรอยด์ [[อนุสัญญาสตอกโฮล์ม]]อนุญาตให้ใช้ดีดีทีปริมาณน้อยในทางสาธารณสุข แต่ห้ามการใช้ในทางการเกษตร ปัญหาหนึ่งของการพ่นเคมีชนิดมีฤทธิตกค้างทุกรูปแบบ คือ การดื้อยาฆ่าแมลง ยุงที่ได้รับผลกระทบจากการพ่นเคมีชนิดมีฤทธิตกค้างมีแนวโน้มพักและอาศัยอยู่ในอาคาร และเนื่องจากการระคายเคืองอันเกิดจากการฉีดพ่น ลูกหลานของมันมีแนวโน้มจะพักและอาศัยอยู่นอกอาคารมากกว่า หมายความว่า พวกมันจะได้รับผลกระทบจากการพ่นเคมีชนิดมีฤทธิตกค้างน้อยกว่า |
การพ่นเคมีชนิดมีฤทธิตกค้างเป็นการพ่นยาฆ่าแมลงบนผนังภายในบ้าน หลังดูดเลือดแล้ว ยุงจำนวนมากจะพักบนพื้นผิวใกล้เคียงขณะย่อย ฉะนั้นหากฉาบผนังบ้านด้วยยาฆ่าแมลง ยุงที่พักอยู่จะตายก่อนที่จะทันได้กัดคนอื่นและส่งผ่านปรสิตมาลาเรีย<ref name="Enayati 2010"/> ในปี 2549 องค์การอนามัยโลกแนะนำให้ใช้ยาฆ่าแมลง 12 ชนิดในการพ่นเคมีชนิดมีฤทธิตกค้าง รวมถึง[[ดีดีที]]และ[[ไซฟลูทริน]]และ[[เดลตาเมทริน]]ในกลุ่มไพรีทรอยด์<ref name="WHO Indoor Residual Spraying"/> [[อนุสัญญาสตอกโฮล์ม]]อนุญาตให้ใช้ดีดีทีปริมาณน้อยในทางสาธารณสุข แต่ห้ามการใช้ในทางการเกษตร<ref name="van den Berg 2009"/> ปัญหาหนึ่งของการพ่นเคมีชนิดมีฤทธิตกค้างทุกรูปแบบ คือ การดื้อยาฆ่าแมลง ยุงที่ได้รับผลกระทบจากการพ่นเคมีชนิดมีฤทธิตกค้างมีแนวโน้มพักและอาศัยอยู่ในอาคาร และเนื่องจากการระคายเคืองอันเกิดจากการฉีดพ่น ลูกหลานของมันมีแนวโน้มจะพักและอาศัยอยู่นอกอาคารมากกว่า หมายความว่า พวกมันจะได้รับผลกระทบจากการพ่นเคมีชนิดมีฤทธิตกค้างน้อยกว่า<ref name="Pates 2005"/> |
||
มีวิธีอื่นอีกหลายวิธีในการลดยุงกัดและชะลอการระบาดของมาลาเรีย ความพยายามลดลูกน้ำโดยลดการเข้าถึงแหล่งน้ำเปิดซึ่งเป็นที่เจริญของยุงหรือโดยการเพิ่มสารเพื่อลดการเจริญของยุงนั้นมีประสิทธิภาพในบางที่ ไม่มีหลักฐานสนับสนุนอุปกรณ์ขับไล่ยุงอิเล็กทรอนิกส์ซึ่งสร้างเสียงความถี่สูงมากซึ่งน่าจะช่วยไล่ยุงเพศเมีย |
มีวิธีอื่นอีกหลายวิธีในการลดยุงกัดและชะลอการระบาดของมาลาเรีย ความพยายามลดลูกน้ำโดยลดการเข้าถึงแหล่งน้ำเปิดซึ่งเป็นที่เจริญของยุงหรือโดยการเพิ่มสารเพื่อลดการเจริญของยุงนั้นมีประสิทธิภาพในบางที่<ref>{{cite journal|last=Tusting|first=LS|coauthors=Thwing, J; Sinclair, D; Fillinger, U; Gimnig, J; Bonner, KE; Bottomley, C; Lindsay, SW|title=Mosquito larval source management for controlling malaria.|journal=The Cochrane database of systematic reviews|date=Aug 29, 2013|volume=8|pages=CD008923|pmid=23986463|doi=10.1002/14651858.CD008923.pub2}}</ref> ไม่มีหลักฐานสนับสนุนอุปกรณ์ขับไล่ยุงอิเล็กทรอนิกส์ซึ่งสร้างเสียงความถี่สูงมากซึ่งน่าจะช่วยไล่ยุงเพศเมีย<ref name="Enayati 2007"/> |
||
=== วิธีการอื่น === |
=== วิธีการอื่น === |
||
มีการใช้วิธีการมีส่วนร่วมของชุมชนและยุทธศาสตร์สุขศึกษาซึ่งเสริมสร้างความตระหนักมาลาเรียและความสำคัญของมาตรการควบคุมเพื่อลดอุบัติการณ์ของมาลาเรียในโลกกำลังพัฒนาบางพื้นที่อย่างได้ผล การรับรู้โรคในระยะต้น ๆ สามารถหยุดไม่ให้โรคถึงตายได้ การศึกษายังสามารถแจ้งประชาชนให้ปิดบริเวณน้ำนิ่ง เช่น แทงก์น้ำ ซึ่งเป็นแหล่งผสมพันธุ์ชั้นดีสำหรับปรสิตและยุง ฉะนั้นจึงลดความเสี่ยงของการส่งผ่านระหว่างมนุษย์ได้ วิธีการนี้โดยทั่วไปใช้ในเขตเมืองซึ่งมีศูนย์ประชากรขนาดใหญ่ในพื้นที่จำกัดและมีแนวโน้มการส่งผ่านในพื้นที่เหล่านี้มาก การบำบัดป้องกันมีเว้นระยะ (intermittent preventive therapy) เป็นอีกการช่วยเหลือหนึ่งที่ใช้เพื่อควบคุมมาลาเรียในสตรีมีครรภ์และทารก และเด็กก่อนวัยเรียนซึ่งการส่งผ่านเป็นแบบตามฤดูกาลได้สำเร็จ |
มีการใช้วิธีการมีส่วนร่วมของชุมชนและยุทธศาสตร์สุขศึกษาซึ่งเสริมสร้างความตระหนักมาลาเรียและความสำคัญของมาตรการควบคุมเพื่อลดอุบัติการณ์ของมาลาเรียในโลกกำลังพัฒนาบางพื้นที่อย่างได้ผล<ref name="Lalloo 2006"/> การรับรู้โรคในระยะต้น ๆ สามารถหยุดไม่ให้โรคถึงตายได้ การศึกษายังสามารถแจ้งประชาชนให้ปิดบริเวณน้ำนิ่ง เช่น แทงก์น้ำ ซึ่งเป็นแหล่งผสมพันธุ์ชั้นดีสำหรับปรสิตและยุง ฉะนั้นจึงลดความเสี่ยงของการส่งผ่านระหว่างมนุษย์ได้ วิธีการนี้โดยทั่วไปใช้ในเขตเมืองซึ่งมีศูนย์ประชากรขนาดใหญ่ในพื้นที่จำกัดและมีแนวโน้มการส่งผ่านในพื้นที่เหล่านี้มาก<ref name="Mehlhorn 2008"/> การบำบัดป้องกันมีเว้นระยะ (intermittent preventive therapy) เป็นอีกการช่วยเหลือหนึ่งที่ใช้เพื่อควบคุมมาลาเรียในสตรีมีครรภ์และทารก<ref name="Bardají 2012"/> และเด็กก่อนวัยเรียนซึ่งการส่งผ่านเป็นแบบตามฤดูกาลได้สำเร็จ<ref name="Meremikwu 2012"/> |
||
โครงการควบคุมโรคที่มีตัวนำโรคแห่งชาติ (National Vector Borne Disease Control Programme) ของประเทศอินเดียกำหนดให้เดือนมิถุนายนเป็นเดือนต่อต้านมาลาเรีย โดยมีวัตถุประสงค์เพื่อเพ่มความร่วมมือหลายภาคส่วนและการมีส่วนร่วมของชุมชนในการควบคุมมาลาเรีย |
โครงการควบคุมโรคที่มีตัวนำโรคแห่งชาติ (National Vector Borne Disease Control Programme) ของประเทศอินเดียกำหนดให้เดือนมิถุนายนเป็นเดือนต่อต้านมาลาเรีย โดยมีวัตถุประสงค์เพื่อเพ่มความร่วมมือหลายภาคส่วนและการมีส่วนร่วมของชุมชนในการควบคุมมาลาเรีย<ref name="pmid9914675">{{cite journal|last=Lal|first=S|coauthors=Phukan, PK; Sharma, SN; Dhillon, GP; Kaul, SM; Saxena, NB|title='Anti-malaria month'--a step forward in multisectoral collaboration and community involvement in malaria control.|journal=The Journal of communicable diseases|date=Jun 1998|volume=30|issue=2|pages=93–101|pmid=9914675}}</ref><ref>{{cite journal|title=Anti-Malaria month campaign: Operational guide|url=http://nvbdcp.gov.in/Doc/AMM-Preamble%20-100405.doc|publisher=National Vector Borne Disease Control Programme (NVBDCP)|accessdate=19 January 2014}}</ref> |
||
=== ยารักษาโรค === |
=== ยารักษาโรค === |
||
มียาหลายชนิดที่สามารถช่วยป้องกันมาลาเรียขณะเดินทางไปยังถิ่นระบาดได้ ยาเหล่านี้ส่วนมากบางครั้งใช้ในการรักษาด้วย คลอโรควินอาจใช้ได้ในที่ซึ่งปรสิตยังไวต่อยา เนื่องจาก ''Plasmodium'' ส่วนใหญ่ดื้อต่อยารักษาโรคตั้งแต่หนึ่งชนิดขึ้นไป จึงมักใช้ยาหนึ่งในสามชนิดนี้ เมโฟลควิน (ลาเรียม) [[ดอกซีไซคลีน]] หรือการรวมอะโตวาโควนและโพรกวานิลไฮโดรคลอไรด์ (มาลาโรน) ผู้ป่วยสามารถทนฤทธิ์ยาดอกซีไซคลินและการรวมอะโตวาโควนและโพรกวานิลได้ดีที่สุด เมโฟลควินสัมพันธ์กับการเสียชีวิต การฆ่าตัวตาย และอาการทางประสาทวิทยาและจิตเวช |
มียาหลายชนิดที่สามารถช่วยป้องกันมาลาเรียขณะเดินทางไปยังถิ่นระบาดได้ ยาเหล่านี้ส่วนมากบางครั้งใช้ในการรักษาด้วย คลอโรควินอาจใช้ได้ในที่ซึ่งปรสิตยังไวต่อยา<ref name="Jacquerioz 2009"/> เนื่องจาก ''Plasmodium'' ส่วนใหญ่ดื้อต่อยารักษาโรคตั้งแต่หนึ่งชนิดขึ้นไป จึงมักใช้ยาหนึ่งในสามชนิดนี้ เมโฟลควิน (ลาเรียม) [[ดอกซีไซคลีน]] หรือการรวมอะโตวาโควนและโพรกวานิลไฮโดรคลอไรด์ (มาลาโรน)<ref name="Jacquerioz 2009"/> ผู้ป่วยสามารถทนฤทธิ์ยาดอกซีไซคลินและการรวมอะโตวาโควนและโพรกวานิลได้ดีที่สุด เมโฟลควินสัมพันธ์กับการเสียชีวิต การฆ่าตัวตาย และอาการทางประสาทวิทยาและจิตเวช<ref name="Jacquerioz 2009"/> |
||
ผลคุ้มครองยังไม่เริ่มทันที และผู้ที่จะเดินทางไปยังพื้นที่ถิ่นระบาดของมาลาเรียปกติทานยาหนึ่งถึงสองสัปดาห์ก่อนเดินทางไปและยังทานต่อไปสี่ถึงหกสัปดาห์หลังเดินทางกลับ (ยกเว้นอะโตวาโควน/โพรกวานิล ซึ่งต้องเริ่มสองวันก่อนเดินทางและทานต่อเนื่องเป็นเวลาเจ็ดวันจากนั้น) การใช้ยาคุ้มครองแทบไม่ได้ผลสำหรับผู้ที่อาศัยอยู่ในบริเวณที่มีมาลาเรียอยู่แล้ว และปกติใช้เฉพาะในผู้เดินทางและนักท่องเที่ยวระยะสั้นเท่านั้น ทั้งนี้ เนื่องจากราคายา ผลข้างเคียงจากการใช้ระยะยาว และความยากในการได้มาซึ่งยาต้านมาลาเรียในประเทศยากจน การใช้ยาคุ้มครองในที่ซึ่งมียุงที่เป็นตัวนำโรคมาลาเรียอาจส่งเสริมให้มีการพัฒนาการดื้อยาบางส่วน (partial resistance) |
ผลคุ้มครองยังไม่เริ่มทันที และผู้ที่จะเดินทางไปยังพื้นที่ถิ่นระบาดของมาลาเรียปกติทานยาหนึ่งถึงสองสัปดาห์ก่อนเดินทางไปและยังทานต่อไปสี่ถึงหกสัปดาห์หลังเดินทางกลับ (ยกเว้นอะโตวาโควน/โพรกวานิล ซึ่งต้องเริ่มสองวันก่อนเดินทางและทานต่อเนื่องเป็นเวลาเจ็ดวันจากนั้น)<ref name="Freedman 2008"/> การใช้ยาคุ้มครองแทบไม่ได้ผลสำหรับผู้ที่อาศัยอยู่ในบริเวณที่มีมาลาเรียอยู่แล้ว และปกติใช้เฉพาะในผู้เดินทางและนักท่องเที่ยวระยะสั้นเท่านั้น ทั้งนี้ เนื่องจากราคายา ผลข้างเคียงจากการใช้ระยะยาว และความยากในการได้มาซึ่งยาต้านมาลาเรียในประเทศยากจน<ref name="Fernando 2011"/> การใช้ยาคุ้มครองในที่ซึ่งมียุงที่เป็นตัวนำโรคมาลาเรียอาจส่งเสริมให้มีการพัฒนาการดื้อยาบางส่วน (partial resistance)<ref name="Turschner 2009"/> |
||
== การรักษา == |
== การรักษา == |
||
รุ่นแก้ไขเมื่อ 16:44, 8 พฤษภาคม 2557
| มาลาเรีย (Malaria) | |
|---|---|
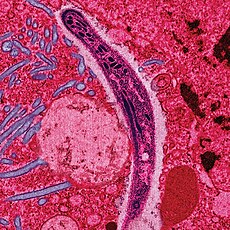 Plasmodium ในรูปที่เข้าสู่มนุษย์และสัตว์มีกระดูกสันหลังอื่นจากน้ำลายของยุงเพศเมีย (สปอโรซอยท์) ตัดขวางกับไซโทพลาสซึมของเซลล์เยื่อบุทางเดินอาหารส่วนกลางของยุง | |
| บัญชีจำแนกและลิงก์ไปภายนอก | |
| ICD-10 | B50-B54 |
| ICD-9 | 084 |
| OMIM | 248310 |
| DiseasesDB | 7728 |
| MedlinePlus | 000621 |
| eMedicine | med/1385 emerg/305 ped/1357 |
| MeSH | C03.752.250.552 |
มาลาเรีย (อังกฤษ: Malaria) หรือไข้จับสั่น ไข้ป่า ไข้ป้าง ไข้ร้อนเย็นหรือไข้ดอกสัก เป็นโรคติดเชื้อของมนุษย์และสัตว์อื่นที่มียุงเป็นพาหะ สาเหตุคือ ปรสิตโปรโตซัว (จุลินทรีย์เซลล์เดียวประเภทหนึ่ง) ในสกุล Plasmodium (พลาสโมเดียม) โดยทั่วไป โรคมาลาเรียส่งผ่านโดยการกัดจากยุงเพศเมียในสกุล Anopheles (ยุงก้นปล่อง) ที่มีเชื้ออยู่ โดยยุงจะนำเชื้อ Plasmodium จากน้ำลายเข้าสู่ระบบไหลเวียนโลหิตของผู้ถูกกัด จากนั้นเชื้อในเลือดจะเดินทางไปยังตับเพื่อเจริญและสืบพันธุ์ โรคมาลาเรียก่อให้เกิดอาการทั่วไป ซึ่งรวมไข้และปวดศีรษะ ซึ่งในกรณีที่รุนแรงสามารถดำเนินไปเป็นโคม่าหรือเสียชีวิตได้
Plasmodium ห้าสปีชีส์สามารถติดต่อและส่งผ่านโดยมนุษย์ได้ ผู้เสียชีวิตส่วนมากเกิดจากเชื้อ P. falciparum และ P. vivax ขณะที่ P. ovale และ P. malariae ก่อให้เกิดโรคมาลาเรียแบบที่โดยทั่วไปรุนแรงน้อยกว่า ซึ่งไม่ค่อยมีผู้เสียชีวิต สปีชีส์รับจากสัตว์ P. knowlesi พบมากในเอเชียตะวันออกเฉียงใต้ ก่อให้เกิดโรคมาลาเรียในลิงแม็กแคก แต่ก็สามารถก่อให้เกิดการติดเชื้อรุนแรงในมนุษย์ได้เช่นกัน โรคมาลาเรียพบมากในพื้นที่เขตร้อนและกึ่งเขตร้อนเพราะปริมาณฝน อุณหภูมิอบอุ่นและน้ำนิ่งซึ่งเป็นแหล่งที่อยู่ที่ดีสำหรับตัวอ่อนของยุง การตรวจเลือดด้วยกล้องจุลทรรศน์โดยใช้ฟิล์มเลือดหรือการวินิจฉัยชนิดรวดเร็ว (rapid diagnostic test) ที่อาศัยแอนติเจน เป็นวิธีการวินิจฉัยโรคมาลาเรียตามปกติ มีการพัฒนาเทคนิคสมัยใหม่ซึ่งใช้ปฏิกิริยาลูกโซ่พอลิเมอเรสเพื่อตรวจจับดีเอ็นเอของ Plasmodium แต่ยังไม่มีใช้แพร่หลายในพื้นที่ซึ่งโรคมาลาเรียเป็นโรคประจำถิ่นเนื่องจากมีราคาแพงและซับซ้อน
การส่งผ่านโรคสามารถลดได้ด้วยการป้องกันไม่ให้ถูกยุงกัด โดยการใช้มุ้งหรือสารขับไล่แมลง หรือด้วยมาตรการควบคุมยุง เช่น การฉีดพ่นยาฆ่าแมลงหรือการระบายน้ำนิ่ง โรคมาลาเรียยังไม่มีวัคซีนที่มีประสิทธิภาพ แม้กำลังมีความพยายามพัฒนาวัคซีนอยู่ในปัจจุบัน มียาหลายชนิดที่ใช้ป้องกันมาลาเรียในนักท่องเที่ยวที่เดินทางไปยังประเทศซึ่งโรคมาลาเรียเป็นโรคประจำถิ่น นอกจากนี้มียาต้านมาลาเรียหลายชนิด โรคมาลาเรียรุนแรงรักษาด้วยการฉีดควินินเข้าหลอดเลือดดำหรือกล้ามเนื้อ หรือ ตั้งแต่กลางคริสต์ทศวรรษ 2000 อาร์ทีซูเนต อนุพันธ์ของอาร์ตีมิซินิน ซึ่งให้ผลดีกว่าควินินทั้งในเด็กและผู้ใหญ่ และให้ร่วมกับยาต้านมาลาเรียตัวที่สอง เช่น เมโฟลควิน เชื้อมีการดื้อยาต่อยาต้านมาลาเรียหลายชนิด เช่น P. falciparum ซึ่งดื้อต่อคลอโรควินได้แพร่ไปยังพื้นที่ซึ่งมีการระบาดมากที่สุด และการเริ่มดื้อยาอาร์ทีมิซินินได้กลายมาเป็นปัญหาในบางพื้นที่ของเอเชียตะวันออกเฉียงใต้
องค์การอนามัยโลกประเมินว่าในปี พ.ศ. 2553 มีผู้ป่วยโรคมาลาเรียที่มีการบันทึก 219 ล้านคน ในปีนั้น มีผู้เสียชีวิตด้วยโรคมาลาเรียระหว่าง 660,000 คน ถึง 1.2 ล้านคน[1] จำนวนมากเป็นเด็กในทวีปแอฟริกา จำนวนผู้เสียชีวิตแท้จริงนั้นไม่อาจทราบได้แน่ชัด เพราะไม่มีข้อมูลที่แน่ชัดในพื้นที่ชนบทหลายแห่ง และไม่มีการบันทึกข้อมูลผู้ป่วยจำนวนมาก โรคมาลาเรียมักสัมพันธ์กับความยากจนและยังอาจเป็นอุปสรรคต่อการพัฒนาเศรษฐกิจ
อาการและอาการแสดง

ปกติอาการและอาการแสดงของมาลาเรียจะเริ่มต้น 8–25 วันหลังการติดเชื้อ[2] อย่างไรก็ดี อาการอาจเกิดขึ้นหลังจากนี้ในผู้ที่ทานยาต้านมาลาเรียป้องกันไว้ก่อน[3] การแสดงเริ่มต้นของโรคเป็นอาการคล้ายหวัด[4] ซึ่งเหมือนกันในมาลาเรียทุกสปีชีส์ และสามารถเหมือนกับสภาพอื่น เช่น ภาวะเลือดเป็นพิษ กระเพาะอาหารและลำไส้เล็กอักเสบ และโรคไวรัส[3] การแสดงอาการอาจรวมปวดศีรษะ เป็นไข้ สั่น ปวดในข้อ อาเจียน โลหิตจางเพราะเม็ดเลือดแดงแตก ดีซ่าน มีฮีโมโกลบินในปัสสาวะ จอตาเสียหายและการชัก[5]
อาการตรงต้นแบบของมาลาเรีย คือ อาการกำเริบ ซึ่งเป็นการเกิดการหนาวฉับพลัน ตามด้วยการสั่น และไข้และเหงื่อออกเป็นวัฏจักร แต่ละสปีชีส์มีความถี่ต่างกัน ในการติดเชื้อ P. vivax และ P. ovale อาการกำเริบทุกสองวัน P. malariae อาการกำเริบทุกสามวัน การติดเชื้อ P. falciparum สามารถเกิดไข้กลับทุก 36–48 ชั่วโมงหรือไข้แทบไม่สร่าง[6]
มาลาเรียรุนแรงปกติเกิดจาก P. falciparum อาการแสดงของมาลาเรียประเภทนี้เริ่มขึ้น 9–30 วันหลังการติดเชื้อ[4] บุคคลที่มีมาลาเรียขึ้นสมอง (cerebral malaria) มักแสดงอาการทางระบบประสาทบ่อยครั้ง ซึ่งรวมถึงท่าร่างผิดปกติ อาการตากระตุกแกว่ง อัมพาตเมื่อดูด้วยสองตา (ตาไม่สามารถกลอกไปในทิศทางเดียวกัน) อาการเกร็งหลังแอ่น ชักหรือโคม่า[4]
ภาวะแทรกซ้อน
โรคมาลาเรียมีภาวะแทรกซ้อนรุนแรงหลายอย่าง ภาวะแทรกซ้อนหนึ่งคือการพัฒนาการหายใจอึดอัก ซึ่งเกิดขึ้นมากถึง 25% ในผู้ใหญ่ และ 40% ในเด็กที่ป่วยด้วยมาลาเรียชนิด P. falciparum รุนแรง สาเหตุอาจเนื่องจากการชดเชยภาวะเลือดเป็นกรดเมตะบอลิกด้วยการหายใจ ปอดบวมน้ำที่ไม่ได้มีสาเหตุจากโรคหัวใจ ปอดบวมเกิดร่วม และโลหิตจางรุนแรง กลุ่มอาการหายใจลำบากเฉียบพลันพบได้ 5–25% ของผู้ใหญ่ และมากถึง 29% ของสตรีมีครรภ์ ทว่าพบน้อยในเด็กเล็กที่ป่วยเป็นโรคมาลาเรียรุนแรง[7] การติดเชื้อเอชไอวีร่วมกับมาลาเรียเพิ่มอัตราตาย[8] ภาวะไตล้มเหลวเป็นลักษณะของไข้น้ำดำ ซึ่งฮีโมโกลบินจากเม็ดเลือดแดงที่แตกรั่วออกสู่ปัสสาวะ[4]
การติดเชื้อ P. falciparum อาจส่งผลให้เกิดมาลาเรียขึ้นสมอง ซึ่งเป็นรูปแบบของมาลาเรียรุนแรงที่มีโรคสมองร่วมด้วย ภาวะดังกล่าวสัมพันธ์กับจอตาขาว (retinal whitening) ซึ่งอาจเป็นอาการแสดงทางคลินิกที่มีประโยชน์ในการแยกมาลาเรียจากสาเหตุอื่นของไข้[9] นอกจากนี้ยังอาจเกิดม้ามโต ปวดศีรษะรุนแรง ตับโต น้ำตาลในเลือดต่ำ และมีฮีโมโกลบินในปัสสาวะร่วมกับไตล้มเหลวได้[4]
มาลาเรียในสตรีมีครรภ์เป็นสาเหตุสำคัญของการตายคลอด ทารกตายและมีน้ำหนักแรกคลอดต่ำ[10] โดยเฉพาะอย่างยิ่งในการติดเชื้อ P. falciparum แต่การติดเชื้อ P. vivax ก็พบได้[11]
สาเหตุ
ปรสิตมาลาเรียเป็นสิ่งมีชีวิตในสกุล Plasmodium (ไฟลัม Apicomplexa) P. falciparum, P. malariae, P. ovale, P. vivax และ P. knowlesi[12][13] เป็นสาเหตุของมาลาเรียในมนุษย์ ซึ่งในสปีชีส์เหล่านี้ P. falciparum เป็นสปีชีส์ที่พบมากที่สุด (~75%) รองลงมาคือ P. vivax (~20%)[3] แม้ว่าเดิม P. falciparum เป็นชนิดที่ทำให้มีผู้เสียชีวิตมากที่สุด[14] แต่หลักฐานปัจจุบันเสนอว่า มาลาเรีย P. vivax สัมพันธ์กับสภาพที่อาจอันตรายถึงชีวิตได้บ่อยครั้งเท่ากับการวินิจฉัยการติดเชื้อ P. falciparum[15] มาลาเรีย P. vivax พบนอกทวีปแอฟริกามากกว่าโดยสัดส่วน[16] มีการบันทึกการติดเชื้อมาลาเรียพลาสโมเดียมสปีชีส์ที่มาจากลิงไม่มีหางชั้นสูงในมนุษย์ อย่างไรก็ดี สปีชีส์เหล่านี้ส่วนใหญ่มีความสำคัญทางสาธารณสุขน้อย[17] โดยยกเว้น P. knowlesi ซึ่งเป็นสปีชีส์รับจากสัตว์ที่ก่อโรคมาลาเรียในลิงแม็กแคก[13]
วงจรชีวิต
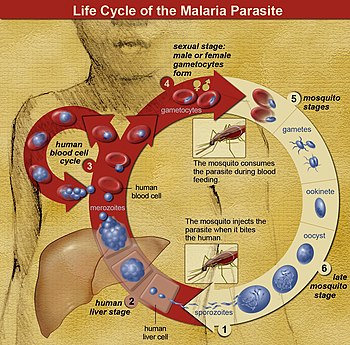
ในวงจรชีวิตของ Plasmodium ยุงก้นปล่องเพศเมีย (ตัวถูกเบียนแท้) ส่งผ่านระยะติดต่อที่เคลื่อนที่ได้ (เรียก สปอโรซอยต์) มายังตัวถูกเบียนสัตว์มีกระดูกสันหลัง เช่น มนุษย์ (ตัวถูกเบียนมัธยันตร์) ฉะนั้นยุงก้นปล่องจึงเป็นเสมือนตัวนำโรคแพร่เชื้อ สปอโรซอยต์เดินทางผ่านเส้นเลือดไปยังเซลล์ตับ ที่ซึ่งมันจะสืบพันธุ์แบบไม่อาศัยเพศ (เรียกว่า tissue schizogony) ทำให้ได้เมอโรซอยต์นับหลายพันเซลล์ เมอโรซอยต์เหล่านี้เข้าไปติดเซลล์เม็ดเลือดแดงใหม่และเริ่มต้นวงจรการเพิ่มจำนวนแบบไม่อาศัยเพศ (เรียกว่า blood schizogony) ซึ่งทำให้ได้เมอโรซอยต์ที่สามารถติดเชื้อได้ใหม่ 8 ถึง 24 เซลล์ ในระยะนี้ เซลล์จะระเบิดและวงจรการติดเชื้อเริ่มต้นใหม่[18]
เมอโรซอยต์อื่นเจริญไปเป็นแกมีโตไซต์ที่ยังเจริญไม่เต็มที่ (immature gametocyte) ซึ่งเป็นเซลล์ต้นกำเนิดของเซลล์สืบพันธุ์เพศผู้และเพศเมีย เมื่อยุงกัดมนุษย์ แกมีโตไซต์จะถูกดูดจากเลือดและไปเจริญในทางเดินอาหารของยุง แกมีโตไซต์เพศผู้และเพศเมียผสมกันและก่อเป็นโอโอไคนีต (ookinete) ซึ่งเป็นไซโกตที่ได้รับการผสมและเคลื่อนที่ได้ จากนั้นโอโอไคนีตเจริญไปเป็นสปอโรซอยต์ใหม่ที่จะเคลื่อนที่ไปยังต่อมน้ำลายของยุง และพร้อมที่จะติดเชื้อตัวถูกเบียนสัตว์มีกระดูกสันหลังใหม่ เมื่อยุงดูดเลือดอีก สปอโรซอยต์ในน้ำลายจะถูกฉีดเข้าสู่ผิวหนัง[19]
เฉพาะยุงเพศเมียเท่านั้นที่ดูดเลือด ส่วนยุงเพศผู้กอนน้ำต้อยของพืชเป็นอาหาร ฉะนั้นจึงไม่ส่งต่อโรค ยุงก้นปล่องเพศเมียมักดูดเลือดในยามกลางคืน โดยปกติเริ่มค้นหาอาหารในช่วงเย็น และจะค้นหาต่อไปทั้งคืนจนกว่าจะได้ดูดเลือด[20] ปรสิตมาลาเรียยังสามารถส่งผ่านได้โดยการถ่ายเลือด แม้จะพบน้อยก็ตาม[21]
มาลาเรียกลับเป็นซ้ำ
อาการแสดงของมาลาเรียสามารถกลับเป็นซ้ำได้หลังจากช่วงที่ไม่มีอาการแสดงต่าง ๆ กัน การกลับเป็นซ้ำนี้สามารถจำแนกตามสาเหตุได้เป็นการกลับกำเริบ การเป็นโรคกลับหรือการติดเชื้อซ้ำ การกลับกำเริบคือ การที่กลับแสดงอาการอีกครั้งหลังช่วงที่ไม่แสดงอาการ ซึ่งเกิดจากปรสิตที่ยังหลงเหลืออยู่ในเลือดซึ่งเป็นผลจากการรักษาที่ไม่เพียงพอหรือไม่มีประสิทธิภาพ[22] การเป็นโรคกลับคือการที่กลับแสดงอาการหลังปรสิตถูกกำจัดหมดไปจากเลือดแล้วแต่ยังคงอยู่เป็นฮิพโนซอยต์แฝงในเซลล์ตับ การเป็นโรคกลับมักเกิดระหว่าง 8–24 สัปดาห์และมักพบในการติดเชื้อ P. vivax และ P. ovale[3] ผู้ป่วยมาลาเรียชนิด P. vivax ในเขตอบอุ่นมักสัมพันธ์กับการที่ฮิพโนซอยต์มีชีวิตอยู่ในฤดูหนาว โดยการเป็นโรคกลับเริ่มต้นในปีถัดจากปีที่ถูกยุงกัด[23] การติดเชื้อซ้ำหมายถึงปรสิตที่ก่อการติดเชื้อครั้งก่อนได้ถูกกำจัดหมดไปจากร่างกายแล้ว แต่มีการได้รับปรสิตใหม่เข้ามา การติดเชื้อซ้ำไม่สามารถแยกจากการกลับกำเริบได้ทันที แม้ว่าการกลับติดเชื้อซ้ำภายในสองสัปดาห์ของการรักษาการติดเชื้อครั้งแรกมักมีสาเหตุจากความล้มเหลวในการรักษา[24] บุคคลอาจแสดงภูมิคุ้มกันระยะสั้น (premunity) ในกรณีการติดเชื้อซ้ำได้[25]
พยาธิกำเนิด
โรคมาลาเรียในมนุษย์มีสองระยะ ระยะหนึ่งอยู่นอกเม็ดเลือดแดง คืออยู่ในเซลล์ตับ อีกระยะหนึ่งอยู่ในเม็ดเลือดแดง เมื่อยุงที่ติดเชื้อมาลาเรียไปดูดเลือดจากมนุษย์ สปอโรซอยต์ในน้ำลายของยุงตัวนั้นจะเข้าไปสู่กระแสเลือด แล้วเชื้อจะเดินทางไปตับ เมื่อไปถึงแล้ว เชื้อจะเข้าไปอยู่ในเซลล์ตับ และจะเพิ่มจำนวนแบบไม่อาศัยเพศโดยไม่แสดงอาการเป็นเวลา 8–30 วัน[26]
หลังระยะสงบอยู่ในตับ เชื้อมาลาเรียจะเปลี่ยนแปลงไปให้เมอโรซอยต์หลายพันเซลล์ เมื่อเซลล์ตัวถูกเบียนแตก เมอโรซอยต์เหล่านี้จะเล็ดรอดเข้าสู่กระแสเลือดเพื่อเริ่มวงจรชีวิตระยะในเม็ดเลือดแดง[26] เชื้อนี้ออกจากตับโดยเอาเยื่อหุ้มเซลล์ของเซลล์ตับคลุมตัวเองไว้ ภูมิคุ้มกันจึงไม่สามารถตรวจจับได้[27]
ในเม็ดเลือดแดง เชื้อจะเพิ่มจำนวนแบบไม่อาศัยเพศอีกครั้ง เมื่อได้จำนวนมากถึงระดับหนึ่งก็จะทำให้เม็ดเลือดแดงแตกออก และเชื้อจำนวนมากก็จะถูกแพร่เข้าสู่กระแสเลือดไปสู่เม็ดเลือดแดงใหม่ต่อไป แต่ละครั้งที่เม็ดเลือดแดงแตกออกและมีเชื้อจำนวนมากเข้าสู่กระแสเลือดพร้อมกัน ผู้ป่วยจะมีไข้เป็นระยะ[26] ซึ่งช่วงของการเกิดไข้จะเป็นไปแล้วแต่ชนิดของเชื้อ การมีไข้จับเป็นระยะนี้เอง ที่เรียกว่า "จับไข้"
สปอโรซอยต์ P. vivax บางตัวไม่เจริญไปเป็นเมอโรซอตยต์ระยะนอกเม็ดเลือดแดงทันที แต่จะผลิตฮิปโนซอยต์ (hypnozoite) ซึ่งสงบอยู่ระยะหนึ่งตั้งแต่หลายเดือน (ปกติ 7–10 เดือน) ถึงหลายปี หลังระยะสงบอยู่ ฮิปโนซอยต์จะกลับมาพัฒนาไปเป็นเมอโรซอนต์อีก ฮิปโนซอยต์เป็นสาเหตุที่การติดเชื้อ P. vivax มีระยะฟักนานและการเป็นโรคกลับภายหลัง[23] ยังไม่ทราบแน่ชัดว่า P. ovale มีระยะฮิปโนซอยต์ด้วยหรือไม่ [28]
ปรสิตมาลาเรียแทบไม่ถูกระบบภูมิคุ้มกันของร่างกายกำจัด เพราะวงจรชีวิตในมนุษย์ส่วนใหญ่อยู่ในเซลล์ตับและเซลล์เม็ดเลือดแดง ทำให้ภูมิคุ้มกันของร่างกายตรวจไม่พบ อย่างไรก็ดี เซลล์เม็ดเลือดที่ติดเชื้อจะถูกกรองและทำลายทิ้งที่ม้าม ซึ่งเป็นการทำลายเชื้อได้ทางหนึ่ง อย่างไรก็ดี เชื้อ P. falciparum มีวิธีหลบหลีกจากกระบวนการของร่างกายดังกล่าวโดยปรสิตจะมีการสร้างโปรตีนยึดเกาะบนผิวเซลล์เม็ดเลือดแดง ทำให้เม็ดเลือดแดงที่ติดเชื้อไปติดอยู่กับผนังหลอดเลือดขนาดเล็ก ซึ่งทำให้เม็ดเลือดติดเชื้อนั้นไม่ถูกกำจัดที่ม้าม การอุดกั้นหลอดเลือดขนาดเล็กก่อให้เกิดอาการ เช่น ในมาลาเรียรก (placental malaria)[29] เซลล์เม็ดเลือดแดงที่ติดผนังหลอดเลือดขนาดเล็กนี้สามารถเจาะผ่าน blood–brain barrier และทำให้เกิดมาลาเรียขึ้นสมอง (cerebral malaria) ได้[30]
แม้ว่าโปรตีนยึดเกาะนี้ (PfEMP1 ย่อมาจาก Plasmodium falciparum erythrocyte membrane protein 1) จะถูกนำไปแทรกไว้ที่ผิวเม็ดเลือดแดงก็ตาม โปรตีนนี้ไม่สามารถกระตุ้นระบบภูมิคุ้มกันให้ทำงานได้ดีนัก เนื่องจากโปรตีนนี้มีความหลากหลายมาก ลักษณะนี้อาจเปรียบเทียบได้กับคนร้ายปลอมตัวที่เมื่อถูกจับได้ครั้งหนึ่งก็เปลี่ยนหน้ากากเป็นอีกแบบหนึ่ง จึงทำให้ไม่ถูกตรวจจับได้โดยง่าย
เมอโรซอยต์บางตัวจะกลายเป็นเซลล์สืบพันธุ์เพศผู้และเพศเมีย (gametocyte) หากยุงมากัดคนที่ติดเชื้อและดูดเอาเลือดที่มีเม็ดเลือดที่ติดเชื้อมาลาเรียในระยะ gametocyte นี้ไป เซลล์เพศผู้และเพศเมียจะผสมพันธุ์กันในทางเดินอาหารของยุง (เนื่องจากการที่มีการสืบพันธุ์แบบอาศัยเพศในยุงนี้เอง จึงทำให้ถือว่ายุงเป็น definitive host ของเชื้อมาลาเรีย) เมื่อผสมพันธุ์กันแล้วจะทำให้ได้สปอโรซอยต์ใหม่เดินทางไปอยู่ในต่อมน้ำลายของยุง และเมื่อยุงไปกัดคนอื่นต่อไป ก็จะนำเชื้อมาลาเรียระยะสปอโรซอยต์ไปติดคนใหม่
ความต้านทานทางพันธุกรรม
ตามการทบทวนในปี 2548 โรคมาลาเรียได้สร้างความกดดันการคัดเลือกที่ยิ่งใหญ่ที่สุดต่อจีโนมมนุษย์ในประวัติศาสตร์ล่าสุด เนื่องจากระดับอัตราตายและอัตราการเกิดโรคจากมาลาเรียสูง โดยเฉพาะอย่างยิ่งชนิด P. falciparum ปัจจัยทางพันธุกรรมหลายอย่างให้ความต้านทานมาลาเรียบ้าง เช่น ลักษณะเซลล์รูปเคียว ลักษณะธาลัสซีเมีย ภาวะพร่องกลูโคส-6-ฟอสเฟต ดีไฮโดรจีเนส และการขาดแอนติเจนดัฟฟีบนเม็ดเลือดแดง[31][32]
ผลกระทบของลักษณะเซลล์รูปเคียวต่อภูมิคุ้มกันมาลาเรียแสดงถึงการแลกเปลี่ยนทางวิวัฒนาการซึ่งเกิดขึ้นเพราะมาลาเรียประจำถิ่น ลักษณะเซลล์รูปเคียวก่อให้เกิดความบกพร่องในโมเลกุลฮีโมโกลบินในเลือด โมเลกุลเอสที่เปลี่ยนแปลงของฮีโมโกลบินทำให้เซลล์กลายเป็นรูปเคียวหรือบิดเบี้ยวเป็นทรงโค้ง ขณะที่เม็ดเลือดแดงปกติจะคงทรงเว้าเข้าหากัน เนื่องจากทรงรูปเคียว เม็ดเลือดแดงจึงมีประสิทธิภาพรับหรือปล่อยออกซิเจนด้อยกว่าปกติ การติดเชื้อมาลาเรียทำให้เม็ดเลือดแดงเป็นทรงเคี้ยวยิ่งขึ้น ฉะนั้นจึงถูกขจัดออกจากระบบไหลเวียนโลหิตเร็วขึ้น จึงเป็นการลดความถี่ซึ่งปรสิตมาลาเรียจะครบวงจรชีวิตในเซลล์ บุคคลที่เป็นฮอโมไซกัส (คือ มีแอลลีลฮีโมโกลบินบีตาที่ผิดปกติสองแอลลีล) จะเป็นโลหิตจางเม็ดเลือดแดงรูปเคียว ขณะที่ผู้ที่เป็นเฮเทอโรไซกัส (คือ มีแอลลีลปกติและผิดปกติอย่างละหนึ่ง) จะมีความต้านทานต่อมาลาเรีย แม้ว่าความคาดหมายการคงชีพของผู้มีสภาพฮอโมไซกัสจะไม่ดำรงความอยู่รอดของลักษณะดังกล่าว แต่ลักษณะนี้ยังสืบทอดมาเพราะประโยชน์จากแบบเฮเทอโรไซกัส[32][33]
การทำหน้าที่ผิดปรกติของตับ
การทำหน้าที่ผิดปรกติของตับอันเป็นผลจากมาลาเรียนั้นพบไม่บ่อยและโดยปกติเกิดเฉพาะในผู้ที่มีภาวะของตับอื่นอยู่ก่อนแล้ว เช่น ตับอักเสบจากไวรัสหรือโรคตับเรื้อรัง กลุ่มอาการดังกล่าวบางครั้งเรียก ตับอักเสบมาลาเรีย (malarial hepatitis) แม้ว่าจะถูกมองว่าเป็นเหตุการณ์ที่เกิดขึ้นน้อย แต่พบโรคตับมาลาเรียมากขึ้น โดยเฉพาะอย่างยิ่งในเอเชียตะวันออกเฉียงใต้และอินเดีย ความไวของตับในผู้ป่วยมาลาเรียสัมพันธ์กับโอกาสมีภาวะแทรกซ้อนและการเสียชีวิตมากขึ้น[34]
การวินิจฉัย
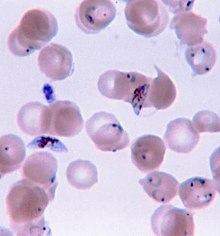
เนื่องจากมาลาเรียแสดงอาการไม่จำเพาะ การวินิจฉัยมาลาเรียนอกพื้นที่ประจำถิ่นต้องมีความสงสัยระดับสูง ซึ่งอาจค้นหาได้จากต่อไปนี้ ประวัติเดินทางล่าสุด ม้ามโต มีไข้ เกล็ดเลือดในเลือดต่ำ และมีระดับบิลิรูบินในเลือดสูงกว่าปกติร่วมกับระดับเม็ดเลือดขาวปกติ[3]
มักยืนยันมาลาเรียด้วยการตรวจฟิล์มเลือดด้วยกล้องจุลทรรศน์ หรือด้วยการทดสอบวินิจฉัยรวดเร็ว (RDT) โดยใช้แอนติเจน[35][36] จุลทรรศนศาสตร์เป็นวิธีที่ใช้มากที่สุดเพื่อตรวจจับปรสิตมาลาเรีย โดยในปี 2553 มีการตรวจฟิล์มเลือดเพื่อหามาลาเรียราว 165 ล้านฟิล์ม[37] แม้ว่าจะมีการใช้แพร่หลาย การวินิจฉัยด้วยจุลทรรศนศาสตร์มีข้อเสียหลักสองประการ คือ หลายสถานที่ (โดยเฉพาะอย่างยิ่งในชนบท) ไม่มีเครื่องมือเพียงพอที่จะดำเนินการทดสอบ และความแม่นของผลขึ้นอยู่กับทั้งทักษะของผู้ตรวจฟิล์มเลือดและระดับปรสิตในเลือด ความไวของฟิล์มเลือดมีพิสัยตั้งแต่ 75–90% ในสภาพเหมาะที่สุด ไปจนถึง 50% ชุดน้ำยาตรวจอย่างรวดเร็วที่มีขายเชิงพาณิชย์มักทำนายการมีปรสิตมาลาเรียได้แม่นกว่าฟิล์มเลือด แต่ชุดน้ำยาตรวจดังกล่าวมีความไวและความจำเพาะวินิจฉัยแปรผันขึ้นอยู่กับผู้ผลิต และไม่สามารถบอกได้ว่ามีปรสิตมากเท่าใด[37]
ในท้องที่ที่การทดสอบทางห้องปฏิบัติการมีพร้อมแล้ว ควรมีการสงสัยหรือทดสอบหามาลาเรียในผู้ป่วยทุกคนที่อยู่ในพื้นที่ซึ่งมีมาลาเรียประจำถิ่น ในพื้นที่ซึ่งไม่สามารถจ่ายการทสอบวินิจฉัยทางห้องปฏิบัติการได้ การใช้เพียงประวัติไข้เพื่อเป็นการบ่งชี้การรักษามาลาเรียกลายเป็นปกติ ซึ่งเป็นคำสอนปกติ "ไข้เท่ากับมาลาเรียเว้นแต่พิสูจน์ได้เป็นอย่างอื่น" ข้อเสียของการปฏิบัตินี้คือ การวินิจฉัยมาลาเรียเกินความเป็นจริงและการจัดการกับไข้ที่ไม่ได้สาเหตุจากมาลาเรียอย่างผิด ๆ ซึ่งสิ้นเปลืองทรัพยากรอันจำกัด บั่นทอนความเชื่อมั่นในระบบสาธารณสุขและส่งเสริมการดื้อยา[38] แม้จะมีการพัฒนาการทดสอบที่ใช้ปฏิกิริยาลูกโซ่พอลิเมอเรสขึ้น แต่ในปี 2555 การทดสอบดังกล่าวยังไม่มีใช้แพร่หลายในพื้นที่ซึ่งพบมาลาเรียเป็นปกติ เนื่องจากเป็นวิธีที่ซับซ้อน[3]
การจำแนก
องค์การอนามัยโลกจำแนกมาลาเรียเป็น "มีอาการรุนแรง" หรือ "ไม่มีอาการแทรกซ้อน"[3] หากเข้าข่ายเกณฑ์ด้านล่างนี้แม้แต่ข้อหนึ่งให้เป็นมาลาเรียที่มีอาการรุนแรง มิฉะนั้นให้ถือเป็นมาลาเรียที่ไม่มีอาการแทรกซ้อน[39]
- ความรู้สึกตัวลดลง
- อ่อนเพลียมากจนไม่สามารถเดินได้
- ไม่สามารถกินอาหารเองได้
- ชักมากกว่าหนึ่งครั้ง
- ความดันโลหิตต่ำ (น้อยกว่า 70 มม.ปรอทในผู้ใหญ่ และ 50 มม.ปรอทในเด็ก)
- หายใจลำบาก
- ช็อกจากการไหลเวียนโลหิต
- ไตล้มเหลวหรือมีฮีโมโกลบินในปัสสาวะ
- มีเลือดออก หรือฮีโมโกลบินน้อยกว่า 50 ก./ลิตร (5 ก./เดซิลิตร)
- ปอดบวมน้ำ
- กลูโคสในเลือดน้อยกว่า 2.2 มิลลิโมลาร์/ลิตร (40 มก./เดซิลิตร)
- ภาวะกระเดียดกรดหรือระดับแลกเตดสูงกว่า 5 มิลลิโมลาร์/ลิตร)
- ระดับปรสิตในเลือดสูงกว่า 100,000 ต่อไมโครลิตรในพื้นที่ส่งผ่านความเข้มต่ำ (low-intensity transmission area) หรือ 250,000 ต่อไมโครลิตรในพื้นที่ส่งผ่านความเข้มสูง (high-intensity transmission area)
มาลาเรียขึ้นสมองนิยามว่าเป็นมาลาเรียชนิด P. falciparum ที่มีอาการรุนแรงซึ่งแสดงด้วยอาการทางประสาทวิทยา รวมถึงโคม่า (โดยมีแบบประเมินความรู้สึกตัวของกลาสโกวน้อยกว่า 11 หรือแบบประเมินความรู้สึกตัวแบลนไทร์มากกว่า 3) หรือโคม่าที่กินเวลานานกว่า 30 นาทีหลังชัก[40]
การป้องกัน
วิธีซึ่งใช้ป้องกันมาลาเรีย ได้แก่ ยากรักษาโรค การกำจัดยุงและการป้องกันไม่ให้ถูกยุงกัด ไม่มีวัคซีนมาลาเรีย มาลาเรียจะมีในพื้นที่ซึ่งมีความหนาแน่นของประชากรมนุษย์สูง มีความหนาแน่นของประชากรยุงก้นปล่องสูงและอัตราการส่งผ่านจากมนุษย์สู่ยุงและจากยุงสู่มนุษย์สูง หากปัจจัยข้อหนึ่งข้อใดลดลงมากพอ ปรสิตมาลาเรียจะหายไปจากพื้นที่นั้นในที่สุด ดังที่เกิดขึ้นแล้วในทวีปอเมริกาเหนือ ทวีปยุโรปและตะวันออกกลางบาส่วน ทว่า แม้ว่าปรสิตมาลาเรียจะถูกกำจัดหมดไปจากโลกแล้ว ปรสิตก็อาจกลับมาหากสภาวะต่าง ๆ กลับเอื้ออำนวยต่อการสืบพันธุ์ของปรสิตอีก ยิ่งไปกว่านั้น ราคาต่อคนของการกำจัดยุงก้นปล่องเพิ่มขึ้นเมื่อความหนาแน่นของประชากรลดลง ทำให้วิธีดังกล่าวไม่คุ้มค่าทางเศรษฐกิจในบางพื้นที่[41]
การป้องกันมาลาเรียอาจคุ้มค่ากว่าการรักษาโรคในระยะยาว แต่ประชากรยากจนที่สุดของโลกไม่สามารถจ่ายราคาเริ่มต้นได้ ราคาการควบคุม (ให้ความประจำถิ่นต่ำ) และโครงการกำจัดในแต่ละประเทศมีผลต่างกว้าง ตัวอย่างเช่น ในประเทศจีน ซึ่งรัฐบาลในปี 2553 ประกาศยุทธศาสตร์ในการกำจัดมาลาเรียในจีน การลงทุนที่กำหนดเป็นสัดส่วนน้อยของรายจ่ายสาธารณะด้านสาธารณสุข ในทางตรงข้าม โครงการคล้ายกันในประเทศแทนซาเนียจะมีมูลค่าประเมินไว้หนึ่งในห้าของงบประมาณสาธารณสุข[42]
การควบคุมตัวนำโรค
การควบคุมตัวนำโรค หมายถึง วิธีซึ่งใช้ลดมาลาเรียด้วยการลดระดับการส่งผ่านโดยยุง สำหรับการป้องกันส่วนบุคคล สารขับไล่แมลงอันทรงประสิทธิภาพที่สุดอาศัยดีอีอีทีหรือพิคาริดิน[43] มีการแสดงแล้วว่า มุ้งชุบยาฆ่าแมลงและการพ่นเคมีชนิดมีฤทธิตกค้าง (indoor residual spraying) มีประสิทธิภาพสูงในการป้องกันมาลาเรียในเด็กในพื้นที่ซึ่งพบมาลาเรียทั่วไป[44][45] การรักษาผู้ป่วยยืนยันแล้วอย่างทันท่วงทีด้วยการรักษาแบบผสมที่อาศัยอาร์ติมิซินินยังอาจลดการส่งผ่านได้[46]
มุ้งช่วยกันยุงจากมนุษย์และลดอัตราการติดเชื้อและส่งผ่านมาลาเรีย มักชุบมุ้งด้วยยาฆ่าแมลงซึ่งออกแบบมาเพื่อฆ่ายุงก่อนยุงหาทางผ่านมุ้งได้ มีการประเมินว่ามุ้งชุบยาฆ่าแมลงมีประสิทธิภาพเป็นสองเท่าของมุ้งที่ไม่ได้ชุบยาและให้การป้องกันดีกว่าการไม่ใช้มุ้ง 70%[47] ระหว่างปี 2543 ถึง 2551 มุ้งชุบยาฆ่าแมลงช่วยชีวิตทารก 250,000 คนโดยประมาณในแอฟริกาใต้สะฮารา[48] ครัวเรือนราว 13% ในประเทศใต้สะฮารามีมุ้งชุบยาฆ่าแมลง[49] ในปี 2543 มุ้งป้องกันเด็กแอฟริกา 1.7 ล้านคน (1.8%) ที่อาศัยอยู่ในสภาวะมาลาเรียประจำถิ่นคงตัว จำนวนเด็กแอฟริกาที่ใช้มุ้งชุบยาฆ่าแมลงเพิ่มขึ้นเป็น 20.3 ล้านคน (18.5%) ในปี 2550 ทว่าอีก 89.6 ล้านคนยังไม่ได้รับการป้องกัน[50] ในปี 2551 มีการประเมินว่าครัวเรือนแอฟริกา 31% มีมุ้งชุบยาฆ่าแมลงอย่างน้อยหนึ่งหลัง มุ้งส่วนมากถูกชุบด้วยไพรีทรอยด์ ซึ่งเป็นยาฆ่าแมลงชนิดมีพิษต่ำ การใช้ที่แนะนำคือให้แขวนมุ้งไว้เหนือกลางเตียงให้แขวนอยู่เหนือเตียงทั้งหมดโดยพับขอบเข้า มุ้งชุบไพรีทรอยต์และมุ้งชุบยาฆ่าแมลงที่ออกฤทธิ์นานให้การป้องกันอย่างดีที่สุด และมีประสิทธิถาะมากที่สุดเมื่อใช้ตั้งแต่เย็นถึงเช้า[51]
การพ่นเคมีชนิดมีฤทธิตกค้างเป็นการพ่นยาฆ่าแมลงบนผนังภายในบ้าน หลังดูดเลือดแล้ว ยุงจำนวนมากจะพักบนพื้นผิวใกล้เคียงขณะย่อย ฉะนั้นหากฉาบผนังบ้านด้วยยาฆ่าแมลง ยุงที่พักอยู่จะตายก่อนที่จะทันได้กัดคนอื่นและส่งผ่านปรสิตมาลาเรีย[52] ในปี 2549 องค์การอนามัยโลกแนะนำให้ใช้ยาฆ่าแมลง 12 ชนิดในการพ่นเคมีชนิดมีฤทธิตกค้าง รวมถึงดีดีทีและไซฟลูทรินและเดลตาเมทรินในกลุ่มไพรีทรอยด์[53] อนุสัญญาสตอกโฮล์มอนุญาตให้ใช้ดีดีทีปริมาณน้อยในทางสาธารณสุข แต่ห้ามการใช้ในทางการเกษตร[54] ปัญหาหนึ่งของการพ่นเคมีชนิดมีฤทธิตกค้างทุกรูปแบบ คือ การดื้อยาฆ่าแมลง ยุงที่ได้รับผลกระทบจากการพ่นเคมีชนิดมีฤทธิตกค้างมีแนวโน้มพักและอาศัยอยู่ในอาคาร และเนื่องจากการระคายเคืองอันเกิดจากการฉีดพ่น ลูกหลานของมันมีแนวโน้มจะพักและอาศัยอยู่นอกอาคารมากกว่า หมายความว่า พวกมันจะได้รับผลกระทบจากการพ่นเคมีชนิดมีฤทธิตกค้างน้อยกว่า[55]
มีวิธีอื่นอีกหลายวิธีในการลดยุงกัดและชะลอการระบาดของมาลาเรีย ความพยายามลดลูกน้ำโดยลดการเข้าถึงแหล่งน้ำเปิดซึ่งเป็นที่เจริญของยุงหรือโดยการเพิ่มสารเพื่อลดการเจริญของยุงนั้นมีประสิทธิภาพในบางที่[56] ไม่มีหลักฐานสนับสนุนอุปกรณ์ขับไล่ยุงอิเล็กทรอนิกส์ซึ่งสร้างเสียงความถี่สูงมากซึ่งน่าจะช่วยไล่ยุงเพศเมีย[57]
วิธีการอื่น
มีการใช้วิธีการมีส่วนร่วมของชุมชนและยุทธศาสตร์สุขศึกษาซึ่งเสริมสร้างความตระหนักมาลาเรียและความสำคัญของมาตรการควบคุมเพื่อลดอุบัติการณ์ของมาลาเรียในโลกกำลังพัฒนาบางพื้นที่อย่างได้ผล[58] การรับรู้โรคในระยะต้น ๆ สามารถหยุดไม่ให้โรคถึงตายได้ การศึกษายังสามารถแจ้งประชาชนให้ปิดบริเวณน้ำนิ่ง เช่น แทงก์น้ำ ซึ่งเป็นแหล่งผสมพันธุ์ชั้นดีสำหรับปรสิตและยุง ฉะนั้นจึงลดความเสี่ยงของการส่งผ่านระหว่างมนุษย์ได้ วิธีการนี้โดยทั่วไปใช้ในเขตเมืองซึ่งมีศูนย์ประชากรขนาดใหญ่ในพื้นที่จำกัดและมีแนวโน้มการส่งผ่านในพื้นที่เหล่านี้มาก[59] การบำบัดป้องกันมีเว้นระยะ (intermittent preventive therapy) เป็นอีกการช่วยเหลือหนึ่งที่ใช้เพื่อควบคุมมาลาเรียในสตรีมีครรภ์และทารก[60] และเด็กก่อนวัยเรียนซึ่งการส่งผ่านเป็นแบบตามฤดูกาลได้สำเร็จ[61]
โครงการควบคุมโรคที่มีตัวนำโรคแห่งชาติ (National Vector Borne Disease Control Programme) ของประเทศอินเดียกำหนดให้เดือนมิถุนายนเป็นเดือนต่อต้านมาลาเรีย โดยมีวัตถุประสงค์เพื่อเพ่มความร่วมมือหลายภาคส่วนและการมีส่วนร่วมของชุมชนในการควบคุมมาลาเรีย[62][63]
ยารักษาโรค
มียาหลายชนิดที่สามารถช่วยป้องกันมาลาเรียขณะเดินทางไปยังถิ่นระบาดได้ ยาเหล่านี้ส่วนมากบางครั้งใช้ในการรักษาด้วย คลอโรควินอาจใช้ได้ในที่ซึ่งปรสิตยังไวต่อยา[64] เนื่องจาก Plasmodium ส่วนใหญ่ดื้อต่อยารักษาโรคตั้งแต่หนึ่งชนิดขึ้นไป จึงมักใช้ยาหนึ่งในสามชนิดนี้ เมโฟลควิน (ลาเรียม) ดอกซีไซคลีน หรือการรวมอะโตวาโควนและโพรกวานิลไฮโดรคลอไรด์ (มาลาโรน)[64] ผู้ป่วยสามารถทนฤทธิ์ยาดอกซีไซคลินและการรวมอะโตวาโควนและโพรกวานิลได้ดีที่สุด เมโฟลควินสัมพันธ์กับการเสียชีวิต การฆ่าตัวตาย และอาการทางประสาทวิทยาและจิตเวช[64]
ผลคุ้มครองยังไม่เริ่มทันที และผู้ที่จะเดินทางไปยังพื้นที่ถิ่นระบาดของมาลาเรียปกติทานยาหนึ่งถึงสองสัปดาห์ก่อนเดินทางไปและยังทานต่อไปสี่ถึงหกสัปดาห์หลังเดินทางกลับ (ยกเว้นอะโตวาโควน/โพรกวานิล ซึ่งต้องเริ่มสองวันก่อนเดินทางและทานต่อเนื่องเป็นเวลาเจ็ดวันจากนั้น)[65] การใช้ยาคุ้มครองแทบไม่ได้ผลสำหรับผู้ที่อาศัยอยู่ในบริเวณที่มีมาลาเรียอยู่แล้ว และปกติใช้เฉพาะในผู้เดินทางและนักท่องเที่ยวระยะสั้นเท่านั้น ทั้งนี้ เนื่องจากราคายา ผลข้างเคียงจากการใช้ระยะยาว และความยากในการได้มาซึ่งยาต้านมาลาเรียในประเทศยากจน[66] การใช้ยาคุ้มครองในที่ซึ่งมียุงที่เป็นตัวนำโรคมาลาเรียอาจส่งเสริมให้มีการพัฒนาการดื้อยาบางส่วน (partial resistance)[67]
การรักษา
มาลาเรียเป็นโรคที่รักษาให้หายขาดได้ ถ้าได้รับการวินิจฉัยที่ถูกต้อง รวดเร็ว และได้รับการรักษาด้วยยาที่มีประสิทธิภาพ ตรงตามชนิดของเชื้อที่เป็นสาเหตุ ยารักษามาลาเรียชนิดแรกทำจากเปลือกของต้นซิงโคนา และเรียกชื่อว่า ควินิน ตัวยายับยั้งการแบ่งตัวของปรสิต ส่วนยาแผนปัจจุบันที่ใช้รักษาที่มีใช้อยู่มีดังนี้คือ
ประเทศแซมเบียใช้ยารักษามาลาเรียที่ทำจากสมุนไพรชื่ออาดเทค ยาอาร์ทีมิซินินมีประสิทธิภาพเทียบเท่าควินิน แต่มีผลข้างเคียงน้อยกว่า[68]
ยาอาร์ทีมิซินินมีประสิทธิภาพเทียบเท่าควินิน แต่มีผลข้างเคียงน้อยกว่า นับเป็นยารักษามาลาเรียชนิดสุดท้ายที่มีอยู่ เพราะปรสิตได้พัฒนาจนดื้อยาทุกตัวที่ใช้รักษา รวมทั้งควินินด้วย จึงมีการนำอนุพันธ์ของยาอาร์ทีมิซินินไปให้ร่วมกับยาอื่น เพื่อลดโอกาสในการดื้อยาอาร์ทีมิซินินของปรสิต กลายเป็นยาชุดต้านมาลาเรียเอซีที (ACT: artemisinin-based combination therapy)
ระบาดวิทยา
การติดต่อสู่คนโดยการถูกยุงก้นปล่องตัวเมียที่มีเชื้อมาลาเรียกัด ยุงก้นปล่อง ที่เป็นพาหะของมาลาเรียที่สำคัญ ในเมืองไทย มีสองชนิด คือ
- Anopheles Dirus พบในป่าทึบชอบออกไข่ตามแอ่งน้ำนิ่งขังตามธรรมชาติ ลักษณะนิสัยชอบกินเลือดคนมาก ไม่ชอบกินเลือดสัตว์อื่นออกหากินตอนกลางคืนถึงเช้ามืด แต่ถ้าป่าทึบมาก ๆ ก็หากินช่วงกลางวันด้วย ยุงชนิดนี้ เป็นชนิดที่มีความสามารถในการแพร่เชื้อมาลาเรียมากกว่ายุงพาหะชนิดอื่นในประเทศไทย
- Anopheles Minimus พบตามชายป่า ชอบวางไข่ในลำธาร น้ำใส ไหลเอื่อย ๆ
พ.ศ. 2550 นี้ มีการประเมินว่าจะมีผู้ติดเชื้อมาลาเรียกว่า 500 ล้านคน โดยจะมีผู้เสียชีวิตด้วยโรคนี้อย่างน้อยหนึ่งล้านคน[68]
แหล่งระบาดของมาลาเรียในประเทศไทยอยู่ตามจังหวัดชายแดน โดยเฉพาะบริเวณที่เป็นภูเขาสูง ป่าทึบ และมีแหล่งน้ำ ลำธาร อันเป็นแหล่งแพร่พันธุ์ของยุงก้นปล่อง จังหวัดที่พบผู้ป่วยมาลาเรียส่วนใหญ่ ได้แก่ แม่ฮ่องสอน ตาก ตราด ระนอง กาญจนบุรี จันทบุรี สระแก้ว ประจวบคีรีขันธ์ ราชบุรี และชุมพร
ประวัติ
ตามหลักฐานการบันทึกได้มีการรายงานว่า การติดเชื้อโรคมาลาเรียในประชากรมนุษย์นั้น มีมานานกว่า 50,000 ปีแล้ว และเชื้อดังกล่าวอาจเป็นเชื้อก่อโรคในมนุษย์ที่มีการกำเนิดมาพร้อมกับการมีมนุษย์บนโลกก็เป็นได้[69] พบว่าเชื้อที่มีความใกล้เคียงกับมาลาเรียสามารถเป็นปรสิตในลิงชิมแปนซีซึ่งมีความใกล้เคียงกับมนุษย์มาก[70] ในช่วงประวัติศาสตร์ของมนุษยชาติ การติดเชื้อมาลาเรียได้มีการถูกบันทึกไว้อย่างต่อเนื่อง นับตั้งแต่ในประเทศจีนเมื่อ 2700 ปีก่อนคริสตกาล[71] คำว่ามาลาเรียมีที่มาจากภาษาอิตาลีโบราณคำว่า mala aria ซึ่งแปลว่า อากาศที่ไม่ดี
การศึกษาทางด้านวิทยาศาสตร์ได้ก่อเกิดความก้าวหน้าที่มีสำคัญต่อองค์ความรู้เรื่องโรคมาลาเรียในปี พ.ศ. 2423 เมื่อแพทย์ทหารชาวฝรั่งเศสที่ทำงานในประเทศอัลจีเรียชื่อ Charles Louis Alphonse Laveran ได้สังเกตเห็นปรสิตในเม็ดเลือดแดงของคนที่ป่วยด้วยโรคมาลาเรีย จึงเสนอแนวคิดว่าสาเหตุก่อโรคมาลาเรียคือเชื้อโปรโตซัว ซึ่งการตั้งสมมุติฐานนี้เป็นครั้งแรกที่มีการระบุว่าเชื้อโปรโตซัวเป็นสาเหตุของโรค[72] จากการค้นพบครั้งนี้และงานอื่นๆ ทำให้เขาได้รับรางวัลโนเบลสาขาสรีรวิทยาและการแพทย์ในปี พ.ศ. 2450 เชื้อโปรโตซัวนี้ได้รับการตั้งชื่อว่า Plasmodium (พลาสโมเดียม) โดยนักวิทยาศาสตร์ชาวอิตาลีชื่อ Ettore Marchiafava และ Angelo Celli[73] ในปีต่อมา แพทย์ชาวคิวบาชื่อ Carlos Finley ซึ่งปฏิบัติหน้าที่รักษาผู้ป่วยโรคไข้เหลืองในฮาวานาได้เสนอว่ามาลาเรียสามารถติดต่อได้โดยมียุงเป็นพาหะ อย่างไรก็ดี แพทย์ชาวอังกฤษชื่อ Sir Ronald Ross ที่ทำงานอยู่ในประเทศอินเดียได้พิสูจน์ในปี พ.ศ. 2441 ว่าเชื้อมาลาเรียติดต่อผ่านทางยุงได้จริง เขาสามารถพิสูจน์ได้ว่ายุงชนิดหนึ่งได้นำเชื้อโรคนี้ติดต่อไปยังนก และสามารถสกัดปรสิตมาลาเรียจากต่อมน้ำลายของยุงที่ไปกัดนกที่ติดเชื้อตัวนั้นได้[74] จากการวิจัยนี้ทำให้ Ross ได้รับรางวัลโนเบลสาขาการแพทย์ในปี พ.ศ. 2445 หลังจากลาออกจากการปฏิบัติงานทางการแพทย์ในประเทศอินเดีย Ross ได้เข้าทำงานใน Liverpool School of Tropical Medicine ที่เพิ่งก่อตั้งขึ้นใหม่ และมีส่วนร่วมในการควบคุมโรคมาลาเรียในประเทศอียิปต์ ปานามา กรีซ และ มอริเชียส[75] การค้นพบของ Finlay และ Ross ได้รับการยืนยันในเวลาต่อมาโดย medical board นำโดย Walter Reed ในปี พ.ศ. 2443 และได้รับการนำไปใช้ William C. Gorgas ในหน่วยงานสาธารณสุขระหว่างการก่อสร้างคลองปานามา การปฏิบัติงานทางสาธารณสุขนี้ได้ช่วยชีวิตคนงานนับพันและได้เริ่มสร้างวิธีการในการต่อสู้กับโรคมาลาเรียในปัจจุบัน
อ้างอิง
- ↑ Nayyar GML, Breman JG, Newton PN, Herrington J (2012). "Poor-quality antimalarial drugs in southeast Asia and sub-Saharan Africa". Lancet Infectious Diseases. 12 (6): 488–96. doi:10.1016/S1473-3099(12)70064-6. PMID 22632187.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 2.0 2.1 Fairhurst RM, Wellems TE (2010). "Chapter 275. Plasmodium species (malaria)". ใน Mandell GL, Bennett JE, Dolin R (eds) (บ.ก.). Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases. Vol. 2 (7th ed.). Philadelphia, Pennsylvania: Churchill Livingstone/Elsevier. pp. 3437–3462. ISBN 978-0-443-06839-3.
{{cite book}}:|editor-last=มีชื่อเรียกทั่วไป (help)CS1 maint: multiple names: editors list (ลิงก์) - ↑ 3.0 3.1 3.2 3.3 3.4 3.5 3.6 Nadjm B, Behrens RH (2012). "Malaria: An update for physicians". Infectious Disease Clinics of North America. 26 (2): 243–59. doi:10.1016/j.idc.2012.03.010. PMID 22632637.
- ↑ 4.0 4.1 4.2 4.3 4.4 Bartoloni A, Zammarchi L (2012). "Clinical aspects of uncomplicated and severe malaria". Mediterranean Journal of Hematology and Infectious Diseases. 4 (1): e2012026. doi:10.4084/MJHID.2012.026. PMC 3375727. PMID 22708041.

- ↑ Beare NA, Taylor TE, Harding SP, Lewallen S, Molyneux ME (2006). "Malarial retinopathy: A newly established diagnostic sign in severe malaria". American Journal of Tropical Medicine and Hygiene. 75 (5): 790–7. PMC 2367432. PMID 17123967.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Ferri FF (2009). "Chapter 332. Protozoal infections". Ferri's Color Atlas and Text of Clinical Medicine. Elsevier Health Sciences. p. 1159. ISBN 978-1-4160-4919-7.
- ↑ Taylor WR, Hanson J, Turner GD, White NJ, Dondorp AM (2012). "Respiratory manifestations of malaria". Chest. 142 (2): 492–505. doi:10.1378/chest.11-2655. PMID 22871759.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Korenromp E, Williams B, de Vlas S, Gouws E, Gilks C, Ghys P, Nahlen B (2005). "Malaria attributable to the HIV-1 epidemic, sub-Saharan Africa". Emerging Infectious Diseases. 11 (9): 1410–9. doi:10.3201/eid1109.050337. PMC 3310631. PMID 16229771.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Beare NA, Lewallen S, Taylor TE, Molyneux ME (2011). "Redefining cerebral malaria by including malaria retinopathy". Future Microbiology. 6 (3): 349–55. doi:10.2217/fmb.11.3. PMC 3139111. PMID 21449844.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Hartman TK, Rogerson SJ, Fischer PR (2010). "The impact of maternal malaria on newborns". Annals of Tropical Paediatrics. 30 (4): 271–82. doi:10.1179/146532810X12858955921032. PMID 21118620.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Rijken MJ, McGready R, Boel ME, Poespoprodjo R, Singh N, Syafruddin D, Rogerson S, Nosten F (2012). "Malaria in pregnancy in the Asia-Pacific region". Lancet Infectious Diseases. 12 (1): 75–88. doi:10.1016/S1473-3099(11)70315-2. PMID 22192132.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Mueller I, Zimmerman PA, Reeder JC (2007). "Plasmodium malariae and Plasmodium ovale—the "bashful" malaria parasites". Trends in Parasitology. 23 (6): 278–83. doi:10.1016/j.pt.2007.04.009. PMC 3728836. PMID 17459775.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 13.0 13.1 Collins WE (2012). "Plasmodium knowlesi: A malaria parasite of monkeys and humans". Annual Review of Entomology. 57: 107–21. doi:10.1146/annurev-ento-121510-133540. PMID 22149265.
- ↑ Sarkar PK, Ahluwalia G, Vijayan VK, Talwar A (2009). "Critical care aspects of malaria". Journal of Intensive Care Medicine. 25 (2): 93–103. doi:10.1177/0885066609356052. PMID 20018606.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Baird JK (2013). "Evidence and implications of mortality associated with acute Plasmodium vivax malaria". Clinical Microbiology Reviews. 26 (1): 36–57. doi:10.1128/CMR.00074-12. PMC 3553673. PMID 23297258.
- ↑ Arnott A, Barry AE, Reeder JC (2012). "Understanding the population genetics of Plasmodium vivax is essential for malaria control and elimination". Malaria Journal. 11: 14. doi:10.1186/1475-2875-11-14. PMC 3298510. PMID 22233585.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Collins WE, Barnwell JW (2009). "Plasmodium knowlesi: finally being recognized". Journal of Infectious Diseases. 199 (8): 1107–8. doi:10.1086/597415. PMID 19284287.

- ↑ Schlagenhauf-Lawlor 2008, pp. 70–1
- ↑ Cowman AF, Berry D, Baum J (2012). "The cellular and molecular basis for malaria parasite invasion of the human red blood cell". Journal of Cell Biology. 198 (6): 961–71. doi:10.1083/jcb.201206112. PMC 3444787. PMID 22986493.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Arrow KJ, Panosian C, Gelband H, Institute of Medicine (U.S.). Committee on the Economics of Antimalarial Drugs (2004). Saving Lives, Buying Time: Economics of Malaria Drugs in an Age of Resistance. National Academies Press. p. 141. ISBN 978-0-309-09218-0.
{{cite book}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Owusu-Ofori AK, Parry C, Bates I (2010). "Transfusion-transmitted malaria in countries where malaria is endemic: A review of the literature from sub-Saharan Africa". Clinical Infectious Diseases. 51 (10): 1192–8. doi:10.1086/656806. PMID 20929356.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ WHO 2010, p. vi
- ↑ 23.0 23.1 White NJ (2011). "Determinants of relapse periodicity in Plasmodium vivax malaria". Malaria Journal. 10: 297. doi:10.1186/1475-2875-10-297. PMC 3228849. PMID 21989376.

- ↑ WHO 2010, p. 17
- ↑ Maegraith, BG (1973). "Tropical Pathology". Spezielle pathologische Anatomie. 8: 319–349. doi:10.1007/978-3-662-00226-1_11. ISBN 978-3-662-00228-5.
{{cite journal}}: Cite journal ต้องการ|journal=(help);|chapter=ถูกละเว้น (help) - ↑ 26.0 26.1 26.2 Bledsoe GH (2005). "Malaria primer for clinicians in the United States". Southern Medical Journal. 98 (12): 1197–204, quiz 1205, 1230. doi:10.1097/01.smj.0000189904.50838.eb. PMID 16440920.
- ↑ Vaughan AM, Aly AS, Kappe SH (2008). "Malaria parasite pre-erythrocytic stage infection: Gliding and hiding". Cell Host & Microbe. 4 (3): 209–18. doi:10.1016/j.chom.2008.08.010. PMC 2610487. PMID 18779047.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Richter J, Franken G, Mehlhorn H, Labisch A, Häussinger D (2010). "What is the evidence for the existence of Plasmodium ovale hypnozoites?". Parasitology Research. 107 (6): 1285–90. doi:10.1007/s00436-010-2071-z. PMID 20922429.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Mens PF, Bojtor EC, Schallig HDFH (2012). "Molecular interactions in the placenta during malaria infection". European Journal of Obstetrics & Gynecology and Reproductive Biology. 152 (2): 126–32. doi:10.1016/j.ejogrb.2010.05.013. PMID 20933151.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Rénia L, Wu Howland S, Claser C, Charlotte Gruner A, Suwanarusk R, Hui Teo T, Russell B, Ng LF (2012). "Cerebral malaria: mysteries at the blood-brain barrier". Virulence. 3 (2): 193–201. doi:10.4161/viru.19013. PMC 3396698. PMID 22460644.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ Kwiatkowski DP (2005). "How malaria has affected the human genome and what human genetics can teach us about malaria". American Journal of Human Genetics. 77 (2): 171–92. doi:10.1086/432519. PMC 1224522. PMID 16001361.

- ↑ 32.0 32.1 Hedrick PW (2011). "Population genetics of malaria resistance in humans". Heredity. 107 (4): 283–304. doi:10.1038/hdy.2011.16. PMC 3182497. PMID 21427751.

- ↑ Weatherall DJ (2008). "Genetic variation and susceptibility to infection: The red cell and malaria". British Journal of Haematology. 141 (3): 276–86. doi:10.1111/j.1365-2141.2008.07085.x. PMID 18410566.
- ↑ Bhalla A, Suri V, Singh V (2006). "Malarial hepatopathy". Journal of Postgraduate Medicine. 52 (4): 315–20. PMID 17102560.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์)
- ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อAbba 2011 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อKattenberg 2011 - ↑ 37.0 37.1 อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อWilson 2012 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อPerkins 2008 - ↑ WHO 2010, p. 35
- ↑ WHO 2010, p. v
- ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อwhqlibdoc - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อSabot 2010 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อKajfasz 2009 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อLengeler 2004 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อPluess 2010 - ↑ Palmer, J. "WHO gives indoor use of DDT a clean bill of health for controlling malaria". WHO.
- ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อRaghavendra 2011 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อHowitt 2012 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อMiller 2007 - ↑ Noor AM, Mutheu JJ, Tatem AJ, Hay SI, Snow RW (2009). "Insecticide-treated net coverage in Africa: mapping progress in 2000–07". Lancet. 373 (9657): 58–67. doi:10.1016/S0140-6736(08)61596-2. PMC 2652031. PMID 19019422.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Schlagenhauf-Lawlor 2008, pp. 215
- ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อEnayati 2010 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อWHO Indoor Residual Spraying - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อvan den Berg 2009 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อPates 2005 - ↑ Tusting, LS (Aug 29, 2013). "Mosquito larval source management for controlling malaria". The Cochrane database of systematic reviews. 8: CD008923. doi:10.1002/14651858.CD008923.pub2. PMID 23986463.
{{cite journal}}: ไม่รู้จักพารามิเตอร์|coauthors=ถูกละเว้น แนะนำ (|author=) (help) - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อEnayati 2007 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อLalloo 2006 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อMehlhorn 2008 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อBardají 2012 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อMeremikwu 2012 - ↑ Lal, S (Jun 1998). "'Anti-malaria month'--a step forward in multisectoral collaboration and community involvement in malaria control". The Journal of communicable diseases. 30 (2): 93–101. PMID 9914675.
{{cite journal}}: ไม่รู้จักพารามิเตอร์|coauthors=ถูกละเว้น แนะนำ (|author=) (help) - ↑ "Anti-Malaria month campaign: Operational guide". National Vector Borne Disease Control Programme (NVBDCP). สืบค้นเมื่อ 19 January 2014.
{{cite journal}}: Cite journal ต้องการ|journal=(help) - ↑ 64.0 64.1 64.2 อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อJacquerioz 2009 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อFreedman 2008 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อFernando 2011 - ↑ อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อTurschner 2009 - ↑ 68.0 68.1 อ้างอิงผิดพลาด: ป้ายระบุ
<ref>ไม่ถูกต้อง ไม่มีการกำหนดข้อความสำหรับอ้างอิงชื่อm1 - ↑ Joy D, Feng X, Mu J, Furuya T, Chotivanich K, Krettli A, Ho M, Wang A, White N, Suh E, Beerli P, Su X (2003). "Early origin and recent expansion of Plasmodium falciparum". Science. 300 (5617): 318–21. PMID 12690197.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Escalante A, Freeland D, Collins W, Lal A (1998). "The evolution of primate malaria parasites based on the gene encoding cytochrome b from the linear mitochondrial genome". Proc Natl Acad Sci U S A. 95 (14): 8124–9. PMID 9653151.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ Cox F (2002). "History of human parasitology". Clin Microbiol Rev. 15 (4): 595–612. PMID 12364371.
- ↑ "Biography of Alphonse Laveran". The Nobel Foundation. สืบค้นเมื่อ 2007-06-15. ] Nobel foundation. Accessed 25 Oct 2006
- ↑ "Ettore Marchiafava". สืบค้นเมื่อ 2007-06-15.
- ↑ "Biography of Ronald Ross". The Nobel Foundation. สืบค้นเมื่อ 2007-06-15.
- ↑ "Ross and the Discovery that Mosquitoes Transmit Malaria Parasites". CDC Malaria website. สืบค้นเมื่อ 2007-06-15.
แม่แบบ:Link FA แม่แบบ:Link FA แม่แบบ:Link FA แม่แบบ:Link FA แม่แบบ:Link FA แม่แบบ:Link GA แม่แบบ:Link GA
