Acinetobacter baumannii
บทความนี้ต้องการการจัดหน้า จัดหมวดหมู่ ใส่ลิงก์ภายใน หรือเก็บกวาดเนื้อหา ให้มีคุณภาพดีขึ้น คุณสามารถปรับปรุงแก้ไขบทความนี้ได้ และนำป้ายออก พิจารณาใช้ป้ายข้อความอื่นเพื่อชี้ชัดข้อบกพร่อง |
บทความเกี่ยวกับสิ่งมีชีวิตนี้มีชื่อบทความเป็นชื่อวิทยาศาสตร์ เนื่องจากไม่มีชื่อสามัญเป็นภาษาไทย |
| Acinetobacter baumannii | |
|---|---|
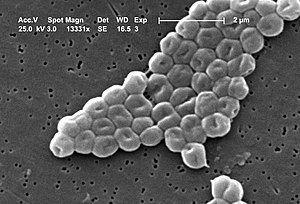
| |
| Acinetobacter baumannii | |
| การจำแนกชั้นทางวิทยาศาสตร์ | |
| อาณาจักร: | Bacteria |
| ไฟลัม: | Proteobacteria |
| ชั้น: | Gammaproteobacteria |
| อันดับ: | Pseudomonadales |
| วงศ์: | Moraxellaceae |
| สกุล: | Acinetobacter Brisou & Prévot 1954 |
| สปีชีส์: | A. baumannii |
| ชื่อทวินาม | |
| Acinetobacter baumannii | |
Acinetobacter baumannii (อะ-ซิ-เน-โต-แบ็ก-เตอ-บาว-มาน-นิ-ไอ) เป็นแบคทีเรียต้องการอากาศ (Aerobic) ติดสีแกรมลบ (Gram-negative) รูปร่างกลมรี (Coccobacillus) พบได้ตามดินและแหล่งน้ำตามธรรมชาติ มักประจำถิ่นอยู่ในสถานพยาบาลเป็นเชื้อฉวยโอกาส (Opportunistic pathogen) เป็นสปีชีส์ที่ก่อโรคติดเชื้อในโรงพยาบาล (Nosocomial infection) ในบรรดา Acinetobacter spp. ทั้งหมด กลุ่มเสี่ยงต่อการติดเชื้อเป็นผู้ที่มีภูมิคุ้มกันบกพร่อง (Immunocompromised host), ผู้ป่วยหนักติดเตียง (Critically ill patient), และผู้ป่วยที่พักรักษาตัวอยู่ในโรงพยาบาลเป็นเวลานาน (long-term hospitalized patient) จุดเด่นของ A. baumannii คือ ไม่มีปัจจัยก่อความรุนแรงของโรค (Virulence factor) ที่เด่นชัดแต่มีอัตราการดื้อยาต้านจุลชีพที่สูงและหลากหลายชนิด จึงถูกจัดเป็นหนึ่งในหกแบคทีเรียที่มีความสามารถในการดื้อยาต้านจุลชีพเกือบทุกชนิดใน ค.ศ. 2008 (พ.ศ. 2551) คือ ESKAPE ได้แก่ Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa,และ Enterobacter spp.[1] ยิ่งไปกว่านั้น ยังถูกจัดอยู่ในรายชื่อแบคทีเรียดื้อยาที่ควรให้ความสำคัญกับการวิจัยและพัฒนายาในระดับสูงสุดจากสามระดับหรือระดับวิกฤตใน ค.ศ. 2017 (พ.ศ. 2560) เนื่องจากการดื้อยาปฏิชีวนะในกลุ่ม Carbapenem[2] นอกจากนี้ยังมีขนานนามว่า Iraqbacter เนื่องจากการระบาดของสายพันธุ์ดื้อยาหลายขนานในหน่วยพยาบาลฐานทัพช่วงสงครามอีรักโดยเฉพาะทหารผ่านศึกและทหารที่ประจำการที่อีรักและอัฟกานิสถาน[3]
นิรุกติศาสตร์และอนุกรมวิธานวิทยา[แก้]
"Acinetobacter" ถูกบัญญัติขึ้นเพื่อแยกออกจาก Achromobacter spp. ใน ค.ศ. 1954[4] "Acineto-" สันนิษฐานว่ามาจากภาษาฝรั่งเศสคำว่า "Acinetique" โดยมีรากศัพท์ภาษากรีกมาจากคำว่า "ακίνητο" แปลว่า ไม่เคลื่อนที่ (Akinetic) ส่วน "-bacter" มาจากคำว่า "Bacterium" ที่ใช้เรียกแบคทีเรียโดยรวม โดยมีรากศัพท์มาจากภาษากรีกคำว่า "βακτήριον" ซึ่งแปลว่า สิ่งขนาดเล็กหรือแท่งสั้น ๆ ในขณะที่ "baumannii" ถูกบัญญัติขึ้นมาจากนามสกุลของ Paul และ Linda Baumann เพื่อเป็นเกียรติสามีภรรยานักชีววิทยาทั้งสอง[5][6] A. baumannii ถูกจัดอยู่ใน Superkingdom Prokaryota; Kingdom Bacteria; Subkingdom Negibacteria; Phylum Proteobacteria; Class Gammaproteobacteria; Order Pseudomonadales; Family Moraxellaceae: Genus Acinetobacter[7] และเนื่องจากความยุ่งยากในการจำแนกเพราะความคล้ายในระดับสปีชีส์จากการทดสอบทางชีวเคมีหลายชนิด Acinetobacter spp. genospecies 1-3 และ 13BJ ซึ่งถูกจำแนกด้วย DNA-DNA hybridization จึงจัดรวมเป็นกลุ่มสปีชีส์เรียกว่า A. calcoaceticus-baumannii complex[8] ซึ่งประกอบด้วยสมาชิกที่มีชื่อสปีชีส์แล้ว 6 สปีชีส์ ได้แก่ A. calcoaceticus, A. baumannii, A. pittii, A. nosocomialis, A. seifertii, และ A. dijkshoorniae [9]
ความรุนแรงในการก่อโรคของแบคทีเรีย (Bacterial virulence)[10][แก้]
การเคลื่อนที่และการเกาะติด (Motility and Adherence)[แก้]
A. baumannii จัดเป็นแบคทีเรียที่เคลื่อนที่ไม่ได้ (Non-motile)[11] เพราะตรวจไม่พบยีนสำหรับแฟลกเจลลา (Flagella) แต่สามารถเคลื่อนที่แบบกระตุก (Twitching motility) โดยใช้การยืดหดของพิไลชนิดที่ 4 (Type IV pili assembly system)[12] และการสังเคราะห์พอลิแซ็กคาไรด์ออกนอกเซลล์ด้านหลังของแบคทีเรียซึ่งผลักดันแบคทีเรียให้เคลื่อนที่ไปข้างหน้าได้.[3] ยิ่งไปกว่านั้น A. baumannii ยังใช้พิไลชนิดที่ 4 สำหรับทรานฟอร์มเมชันตามธรรมชาติ (Natural tranformation) และการเกาะติดพื้นผิววัตถุ (Abiotic surface).[13] พิไลชนิดที่ 4 นี้ในแบคทีเรียอย่าง Pseudomonas aeruginosa ถูกควบคุมการทำงานโดย Two-component sensor-regulator และ Complex chemosensory system [14] และยังสามารถใช้ยึดเกาะกับเซลล์โฮสต์เพื่อการเพิ่มจำนวน (Colonization) ได้.[15]
การก่อไบโอฟิล์ม (Biofilm forming)[แก้]
ไบโอฟิล์มเป็นสังคมของเซลล์ร่วมกับพอลิเมอร์ต่าง ๆ เช่น คาร์โบไฮเดรต, กรดนิวคลีอิก, โปรตีน ฯลฯ ซึ่งเกี่ยวข้องกับการยึดเกาะพื้นผิววัตถุ (Abiotic surface) และเซลล์ของสิ่งมีชีวิต (Biotic surface) ช่วยให้ A. baumannii ทนทานต่อสภาพแวดล้อมที่ยากต่อการดำรงชีวิต เช่น บนพื้นผิววัตถุที่แห้ง สารอาหารน้อย อย่างสายสวนปัสสาวะหรือเครื่องมือทางการแพทย์อื่น ๆ ที่ปนเปื้อน และ/หรือช่วยป้องกันยาปฏิชีวนะเข้าถึงตัวแบคทีเรีย ก่อให้เกิดการดื้อยา. บางสายพันธุ์ของ A. baumannii สามารถสร้างไบโอฟิล์มได้. ยีนที่เกี่ยวข้องได้แก่ cruE ซึ่งอยู่ในโอเปอรอน CruA/BABCDE chaperone-usher complex ทำหน้าที่ประกอบโครงสร้างของพิไลและเป็นขั้นตอนแรกในการสร้างไบโอฟิล์มเพื่อยึดเกาะพื้นผิววัตถุ. โอเปอรอนนี้ถูกควบคุมการทำงานโดย Two-component regulatory system ที่ชื่อว่า bfmS/bfmR [16] ในขณะที่การยึดเกาะบนผิวเซลล์ของสิ่งมีชีวิต A. baumannii ใช้พิไลอื่นที่เป็นอิสระจากโอเปอรอน CruA/BABCDE. [17] นอกจากนี้ Biofilm-associated protein ของ Staphylococcus sp. เกี่ยวข้องกับการพัฒนาไบโอฟิล์มให้สมบูรณ์ก็พบ Ortholog ใน A. baumannii เช่นกัน. [18]
พอลิแซ็กคาไรด์บนผิวเซลล์ (Surface polysaccharide)[แก้]
- แคปซูล (capsule) ถูกทดสอบว่าช่วยให้ A. baumannii เจริญเติบโตได้ดีขึ้นในซีรัม (Serum) ของมนุษย์ ช่วยให้ดื้อต่อโปรตีนคอมพลีเมนต์ (Complement) ในเลือด. ยีนที่เกี่ยวข้องได้แก่ ยีน ptk (Protein, tyrosine kinase) ทำหน้าที่ต่อหน่วยย่อยของแคปซูล (Capsule polymerization) และยีน epsA (Polysaccharide export outer membrane protein) ทำหน้าที่ประกอบและส่งแคปซูลสู่ผิวเซลล์.[19]
- Poly-ẞ- (1-6) -N-acetyl glucosamine (PNAG) ช่วยในการเกาะติดกับพื้นผิววัตถุ, ป้องกันการเข้าถึงตัวของแบคทีเรียจาก Innate immunity, และคงความสมบูรณ์ของไบโอฟิล์ม. ยีนที่เกี่ยวข้องกับการสังเคราะห์ PNAG คือ pgaABCD.[20]
- Lipopolysaccharide (LPS) ฝังอยู่ชั้นบนของ Lipid bi-layer ของเยื่อหุ้มเซลล์ชั้นนอกของแบคทีเรียแกรมลบทั่วไป. LPS ประกอบด้วย 3 ส่วนประกอบกัน ได้แก่ Lipid A, Core, และ O-antigen โดยเรียงตามลำดับจากเยื่อหุ้มเซลล์ชั้นนอกออกไปนอกเซลล์. LPS มี 2 ชนิดซึ่ง A. baumannii สามารถผลิตได้ทั้ง 2 ชนิด ได้แก่ Rough (R-) type ที่มีส่วนประกอบหลักครบทั้ง 3 ส่วนและ Smooth (S-) type ที่ขาดเฉพาะ O-antigen หรือตั้งแต่บางส่วนของ Core เป็นต้นไป.[21][22] Lipid A ของ A. baumannii สามารถออกฤทธิ์เป็น Endotoxin เหมือนแบคทีเรียแกรมลบอื่น ๆ ได้โดยกระตุ้นวิถีการส่งสัญญาณการอักเสบ (Inflammatory signaling pathway)[23] ให้กำจัดเชื้อและควบคุมการอักเสบที่มากเกินไปผ่านการจับกับเซลล์ภูมิคุ้มกันของมนุษย์ที่มี Toll-like receptor 4-Myeloid differentiation factor 2 complex (TLR 4-MD2 complex) และ CD14 บนผิวเซลล์[24].
โปรตีนบนเยื่อหุ้มเซลล์ชั้นนอก (Outer membrane protein)[แก้]
OmpA (Outer membrane protein A) เป็นโปรตีนบนเยื่อหุ้มเซลล์ชั้นนอกหลักของ Acinetobacter spp. ซึ่งมาจากยีน ompA.[25] ที่สามารถควบคุมโปรตีนคอมพลีเมนต์ซึ่งยับยั้งกระบวนการจับกินของเซลล์ Phagocyte ของมนุษย์ทำให้ดื้อต่อซีรัม (Serum resistance).[26] OmpA สามารถถูกหลั่งออกนอกเซลล์ได้และสามารถถูกพบในไมโตคอนเดรียซึ่งกระตุ้นวิถีการตายของเซลล์แบบ Apoptosis ทำให้เกิดการตายของเซลล์เยื่อบุ (Epithelial cell) ของมนุษย์ ส่งผลให้เกิดการบุกรุกเข้าสู่เซลล์ (Invasion).[27] นอกจากนี้ OmpA ยังมีส่วนเกี่ยวข้องในการเกาะติดและการสร้างไบโอฟิล์ม.[28]
เวซิเคิลจากเยื่อหุ้มเซลล์ชั้นนอก (Outer membrane vesicles: OMV)[แก้]
OMV คือเวซิเคิลขนาดเส้นผ่านศูนย์กลาง 20-200 nm ที่ประกอบด้วย LPS, OMP, Lipid, DNA, RNA, หรือโปรตีนอื่น ๆ. [29] A. baumannii สามารถหลั่ง OMV ขนส่งส่วนประกอบดังกล่าวเข้าสู่เซลล์เจ้าบ้านโดยตรง [30] อีกทั้งเป็นหนทางหนึ่งในการส่งผ่านยีนดื้อยาระหว่างสายพันธุ์.[31]
เอนไซม์ Phospholipase (Phospholipase enzyme)[แก้]
- Phospholipase D จากยีน pld มีความเกี่ยวข้องกับการบุกรุกเซลล์เยื่อบุและพยาธิกำเนิดเมื่อทดลองในหนู.[32]
- Phospholipase C จากยีน plc1 มีความเป็นพิษโดยสามารถสลายเซลล์เยื่อบุของมนุษย์.[33]
การดูดซึมธาตุเหล็ก (Iron uptake)[แก้]
A. baumannii สามารถหลั่ง Siderophore ซึ่งเป็นสารคอยจับธาตุเหล็ก (Iron chelator) ที่มีมวลโมเลกุลน้อยแต่ความสามารถในการจับสูง (High affinity) สามารถแย่งชิงธาตุเหล็กจากโปรตีนจับเหล็กของมนุษย์อย่าง Transferrin ในเลือด หรือ Lactoferrin ในสารคัดหลั่งได้. [34] Siderophore แรกที่ถูกพบใน A. baumannii เป็นสารประกอบ Catechol-hydroxamate ชื่อ Acinetobactin แต่พบในบางสายพันธุ์เท่านั้น. [35] ยีนที่เกี่ยวข้องได้แก่ bauA และ basD ซึ่งเกี่ยวข้องกับการขนส่งและกระบวนการชีวสังเคราะห์ของ Acinetobactin ตามลำดับ โดยเฉพาะอย่างยิ่งในสภาวะที่ธาตุเหล็กมีจำกัด. [36] นอกจากนี้ยังพบการดูดซึมธาตุเหล็กที่ไม่ได้ใช้ Siderophore โดยเป็นการเคลื่อนย้าย Heme/Hemoglobin จาก Periplasm สู่ Cytosol ซึ่งอาจเกี่ยวข้องกับ ABC transporter. [36]
การขนย้าย siderophore ที่จับไอออนธาตุเหล็ก (Fe3+) (Ferric-siderophore complex) ถูกควบคุมโดย Iron-regulated outer membrane protein system (IROMP) [37] ซึ่งประกอบด้วยโปรตีนที่จำเพาะคือ ตัวรับบนเยื่อหุ้มเซลล์ชั้นนอก, โปรตีนใน Periplasmic space, และโปรตีนที่เกียวข้องกับเยื่อหุ้มเซลล์ชั้นใน [34] และยังเกี่ยวข้องกับการถ่ายโอนโปรตอนระหว่างภายในและภายนอกเซลล์ (proton gradient) บนเยื่อหุ้มเซลล์ชั้นในและอาศัย TonB protein complex ใน periplasmic space ของ TonBExbBD transducing system ก่อนถูกเอนไซม์ Ferric reductase ปลดปล่อย Fe3+ ออกมาภายในเซลล์. [38] นอกจากนี้ ยังพบกลุ่มยีนที่เกี่ยวกับการสังเคราะห์/ขนส่ง Siderophore 2 กลุ่ม จำพวก Hydroxamate โดยสันนิษฐานว่าเป็นเอนไซม์ที่มีคุณสมบัติ Hydroxylase/Acetyltransferase ซึ่งพบเฉพาะกลุ่มยีนใดกลุ่มยีนหนึ่งในแต่ละสายพันธุ์.[38]
Feo system เป็นอีกกลไกหนึ่งที่ดูดซึมธาตุเหล็กโดยตรง ประกอบด้วยโปรตีน FeoA ใน Cytosol, FeoB ซึ่งเป็น Fe (II) permease บนเยื่อหุ้มเซลล์ชั้นใน, และ FeoC ซึ่งสันนิษฐานว่าเป็น transcriptional repressor และอาจเกี่ยวข้องกับกระบวนการชีวสังเคราะห์ของ Siderophore ที่ขึ้นอยู่กับโปรตีน Fur ซึ่งเป็น Global iron-binding repressor ทำหน้าที่ควบคุมการดูดซึมไอออนธาตุเหล็ก (Fe3+) เนื่องจากพบ Fur box สำหรับให้โปรตีน Fur จับบน Intergenic region ของกลุ่มยีนเหล่านี้.[37][39]
ควอรัมเซนซิง (Quorum sensing)[แก้]
ควอรัมเซนซิงเป็นความสามารถของแบคทีเรียในการสื่อสารและการปรับตัวระหว่างเซลล์โดยการใช้สัญญาณสารเคมีที่เรียกว่า Autoinducer อาทิ Acyl homoserine lactone (AHL) ซึ่งขึ้นอยู่กับความชุกชุม (Cell density) และระยะการเพิ่มจำนวนของเซลล์ (Growth phase).[40] ควอรัมเซนซิงถูกควบคุมด้วย AHL และ Non-AHL -mediated system ซึ่ง AHL-mediated system ถูกเชื่อมโยงกับกับปัจจัยก่อให้เกิดความรุนแรงในการก่อโรค (Virulence factor), การเคลื่อนที่, การสร้างปมรากในพืช (Nodulation), การผลิตสารปฏิชีวนะ, การผลิต Bioemulsan, การเกิด Bioluminescense, และการก่อไบโอฟิล์ม. [37][40]
AHL-mediated system ใน Acinetobacter baumannii ประกอบด้วยโปรตีน AbaR และโปรตีน AbaI (LuxI family) ซึ่งเป็นเอนไซม์สังเคราะห์ Autoinducer. เมื่อ C12-AHL ซึ่งเป็น autoinducer ส่วนใหญ่ของ A. baumannii ที่ส่งออกนอกเซลล์มีปริมาณมากเพียงพอตามความชุกชุมของเซลล์, โปรตีน AbaR (LuxR family) จะทำหน้าที่เป็นตัวรับ autoinducer ที่เข้ามาในเซลล์ จับกันเป็น Complex แล้วสามารถจับกับ DNA ที่สันนิษฐานว่าเป็น lux-box ซึ่งอยู่ด้านต้นสายของยีน abaI เพื่อควบคุมการแสดงออกของยีนเป้าหมายต่อไปซึ่งเกี่ยวข้องกับความสมบูรณ์ของไบโอฟิล์มและเกี่ยวโยงไปถึงการดื้อยาต้านจุลชีพ.[41][42] การแทรกแซงควอรัมเซนซิงหรือที่เรียกว่า ควอรัมเควนชิง (Quorum quenching) [43] จึงอาจเป็นเป้าหมายการรักษาเพื่อขัดขวางพยาธิกำเนิดเมื่อเกิดการติดเชื้อ.[44]
อื่น ๆ ที่อาจเกี่ยวข้อง[แก้]
พยาธิกำเนิดที่ถูกเหนี่ยวนำโดยเอทานอล (Ethanol-induced pathogenesis)[แก้]
เอทานอลที่ความเข้มข้น 1.1% สามารถเพิ่มการแสดงออกของยีน Phospholipase C, ยีนที่เกี่ยวข้องกับ Siderophore สำหรับดูดซึมธาตุเหล็ก,และยีนจำพวก Heat-shock protein ซึ่งมักตอบสนองต่อสภาวะที่ยากต่อการดำรงชีวิตเพื่อการอยู่รอดได้.[33] นอกจากนี้ เอทานอลความเข้มข้นจนถึง ~3% ยังเพิ่มการเจริญของ A. baumannii แม้กระทั่งในน้ำเกลือ (NaCl) ที่ความเข้มข้น 5% เมื่อใช้เอทานอลที่ความเข้มข้น 0.1%.[45]
โปรตีนจับยาในกลุ่มเพนนิซิลลิน (Penicillin binding proteins: PBP)[แก้]
PBP7/8 จากยีน pbpG ซึ่งมีคุณสมบัติ Hydrolase/endopeptidase (PBP8 เกิดจากกระบวนการสลาย PBP7 ที่ต้องอาศัย OmpT) จัดเป็น PBP กลุ่มที่มีมวลโมเลกุลน้อย (Low-molecular mass PBP) มีหน้าที่เกี่ยวข้องกับกระบวนการสังเคราะห์ Peptidoglycan ของผนังเซลล์ในส่วนของการแยกกันของเซลล์ (Cell separation) และการจัดเรียงใหม่ของ Peptidoglycan (Remodeling).[46] PBP7/8 อาจมีส่วนช่วยให้ A. baumannii ดื้อต่อซีรัมของมนุษย์และการอยู่รอดของแบคทีเรียเมื่อทดลองในหนู.[47]
เอเลียนไอส์แลนด์ (Alien island)[แก้]
จากการวิเคราะห์จีโนมของ A. baumannii สายพันธุ์ ATCC17978 เปรียบเทียบกับ A. baylyi สายพันธุ์ CR543861 [48] พบว่า A. baumanni มีเอเลียนไอส์แลนด์หรือชิ้นส่วนสาย DNA ที่สันนิษฐานว่ารับมาจากการส่งผ่านยีนข้ามแบคทีเรีย (Horizontal gene transfer; HGT) ถึง 28 แห่งบนจีโนม. บางแห่งสามารถทำนายหน้าที่ได้จากการเปรียบเทียบความคล้ายของสาย DNA กับฐานข้อมูล เช่น ยีนที่เกี่ยวข้องกับการดื้อต่อโลหะหนัก, เมตาบอลิซึมและการดูดซึมธาตุเหล็ก, การสร้างฟิมบรี (Fimbriae เป็นพหูพจน์ของ Fimbria), กระบวนการที่เกี่ยวกับ autoinducer, และการสร้างผนังเซลล์และเยื่อหุ้มเซลล์ (Cell envelope). เอเลียนไอส์แลนด์ 4 แห่งในอย่างน้อย 6 แห่งยังไม่ทราบหน้าที่แต่ได้รับการยืนยันว่าเกี่ยวข้องกับความรุนแรงในการก่อโรคของแบคทีเรียเมื่อทดลองใน Caenorhabditis elegans และ Dictyostelium discoideum.
การดื้อยาต้านจุลชีพ (Antimicrobial resistance)[แก้]
การดื้อยาในกลุ่ม β-lactam[แก้]
การดื้อยาในกลุ่ม β-lactam จากเอนไซม์ β-lactamase[แก้]
- Cephalosporinase (AmpC) จากยีน blaampC ที่อยู่บนโครโมโซม
AmpC ถูกจำแนกด้วยลำดับนิวคลีโอไทด์และกรดอะมิโนให้เป็น Class C ของเอนไซม์ β-lactamase สามารถสลายยาในกลุ่ม Penicillin, Cephalosporin ที่มีฤทธิ์ขยาย (Extended-spectrum cephalosporin) ยกเว้น Cefepime, และ β-lactam ที่ผสมกับสารยับยั้ง β-lactamase (β-lactam-β-lactamase inhibitor combination). AmpC ของ Acinetobacter spp. (Acinetobacter-derived cephalosporinase; ADC) มีความหลากหลายไม่ต่ำกว่า 56 แบบจากความคล้ายกันของลำดับนิวคลีโอไทด์และความชอบสารตั้งต้นที่แตกต่างกันซึ่งใน A. baumannii มี ADC ที่แตกต่างกันไม่น้อยกว่า 25 แบบ. นอกจากนี้ อินเซอร์ชันซีเควน (Insertion sequence; IS) ISAba1 ซึ่งมีโปรโมเตอร์ (Promoter) อยู่ภายใน สามารถเพิ่มการแสดงออกของยีน blaampC ทำให้ดื้อต่อยาในกลุ่ม Cephalosporin ที่มีฤทธิ์ขยายเนื่องจาก ISAba1 อยู่ทางด้านต้นสายของ blaampC แต่ไม่ได้เปลี่ยนแปลงการดื้อต่อยาในกลุ่มเพนนิซิลลินให้เพิ่มขึ้นอย่างมีนัยสำคัญ
- Oxacillinase (OXA) จากยีน blaOXA
OXA ถูกจำแนกด้วยลำดับนิวคลีโอไทด์และกรดอะมิโนให้เป็น class D ของเอนไซม์ β-lactamase สามารถสลายยา Cloxacillin, Oxacillin, ยาบางตัวในกลุ่ม Oxyimino-β-lactam แต่ไม่ใช่ยาในกลุ่ม Carbapenem และอาจถูกยับยั้งด้วย Clavulanic acid แต่ OXA ของ Acinetobacter spp. สามารถสลายยาในกลุ่ม Carbapenem อย่าง Imipenem และ Meropenem ได้แต่ไม่ใช่ยาในกลุ่ม Cephalosporin ที่มีฤทธิ์ขยายและ Aztronam จึงมีชื่อเรียกว่า CHDL (Carbapenem-hydrolyzing class D β-lactamase) และมีกลุ่มเป็นของตนเองเมื่อจำแนกตามการทำงานของเอนไซม์เรียกว่า 2df. เอนไซม์ CHDL นี้โดยรวมมีการดำเนินไปของปฏิกิริยาที่ต่ำโดยเฉพาะในกรณีของ HGT แต่การมีอินเซอร์ชันซีเควนสามารถเพิ่มการแสดงออกของยีน blaOXA ได้. OXA ของ A. baumannii แบ่งออกเป็น 5 กลุ่มย่อยโดยใช้ Phylogenetics ได้แก่ OXA ในกลุ่มที่มีลำดับกรดอะมิโนคล้ายกับ OXA-51/69 ซึ่งมีอยู่แล้วตามธรรมชาติบนโครโมโซมแต่สามารถพบบนพลาสมิด (Plasmid) ได้, 3 กลุ่มที่สามารถพบได้ทั้งบนโครโมโซมและพลาสมิดคือ กลุ่มที่มีลำดับกรดอะมิโนคล้าย OXA-23, OXA-24/40, และ OXA-58 ซึ่ง OXA-58 พบได้เฉพาะใน Acinetobacter spp. เท่านั้น, และสุดท้ายคือกลุ่มที่มีลำดับกรดอะมิโนคล้าย OXA-143 ซึ่งพบบนพลาสมิดเท่านั้น. หมายเหตุไว้ว่าตัวเลขที่ตามหลัง OXA หรือเอนไซม์ β-lactamase อื่น ๆ หมายถึงอันดับการค้นพบรูปแบบของลำดับกรดอะมิโนเอนไซม์นั้น ๆ.
- Metallo-β-lactamase (MBL) จากยีน blaIMP, blaVIM, blaSIM, และ blaNDM
MBL ถูกจำแนกด้วยลำดับนิวคลีโอไทด์และกรดอะมิโนให้เป็น class B ของเอนไซม์ β-lactamase ซึ่งสามารถสลายกับสารตั้งต้นได้หลากหลาย (Broad substrate specificity) แต่ต้องอาศัยธาตุสังกะสีในการทำปฏิกิริยาจึงสามารถถูกยับยั้งได้โดย EDTA แต่ไม่ได้ถูกยับยั้งด้วย Clavulanic acid, Tazobactam, และ Sulbactam ซึ่งเป็นตัวยับยั้งของยาในกลุ่ม Carbapenem หรือ β-lactam. MBL สามารถสลายยาในกล่ม β-lactam ได้ทุกตัวยกเว้น Aztreonam และมีฤทธิ์ในการสลายยาในกลุ่ม Carbapenem ได้ดีกว่า class D ของเอนไซม์ β-lactamase ถึง 100-1,000 เท่า. MBL ที่ถูกพบแล้วใน A. baumannii ได้แก่ IMP, VIM, SIM, และ NDM ซึ่งยีน blaIMP, blaVIM, และ blaSIM เป็นยีนที่มักถูกพบบนอินทีกรอน Class 1 (Class 1 Integron) ซึ่งมียีนที่เกี่ยวข้องกับการดื้อยาในกลุ่ม Aminoglycoside อยู่ด้วย.
- IMP (Imipenemase) เป็นชื่อเอนไซม์ที่มาจากความสามารถในการสลายยา Imipenem ซึ่งถูกพบครั้งแรกใน P. aeruginosa จากประเทศญี่ปุ่น. IMP สามารถสลายสารตั้งต้นได้หลากหลายโดยเฉพาะยาในกลุ่ม Cephalosporin และ Carbapenem. IMP ที่ถูกค้นพบแล้วใน A. baumannii ได้แก่ IMP-1, -2, -4, -5, -6, -8, -11, และ -19.
- VIM (Veronese Imipenemase) เป็นชื่อเอนไซม์ที่มาจากความสามารถในการสลายยา Imipenem (Imipenemase) ซึ่งถูกพบครั้งแรกใน P. aeruginosa ที่แยกเชื้อได้จากเมืองเวโรนา (Verona) ประเทศอิตาลี. VIM มีคุณสมบัติคล้าย IMP แต่สามารถสลายยาในกลุ่ม Carbapenem ได้ดีเป็นพิเศษและมีความเหมือนของลำดับกรดอะมิโนน้อยกว่า 40% เมื่อเทียบกับ IMP. VIM ที่ถูกค้นพบแล้วใน A. baumannii ได้แก่ IMP-1, -2, -3, -4, และ -11.
- SIM-1 (Seoul Imipenemase) เป็นชื่อเอนไซม์ที่มาจากความสามารถในการสลายยา Imipenem (Imipenemase) ซึ่งถูกพบครั้งแรกใน A. baumannii ที่แยกเชื้อได้จากเมืองโซล (Seoul) ประเทศเกาหลี. SIM มีคุณสมบัติคล้าย IMP และ VIM จึงสามารถสลายยาในกลุ่ม Penicillin, Cephalosporin, และ Cephalosporin ที่มีฤทธิ์ขยาย, รวมถึง Carbapenem. SIM-1 มีความเหมือนของลำดับกรดอะมิโนอยู่ในช่วง 64-69% เมื่อเทียบกับ IMP.
- NDM-1 และ NDM-2 (New Delhi metallo-β-lactamase) เป็นชื่อที่มาจากเอนไซม์ Metallo-β-lactamase ที่ค้นพบครั้งแรกใน K. pneumoniae และ E. coli จากนักท่องเที่ยวชาวสวีเดนที่กลับจากเมืองนิวเดลี (New Delhi) ประเทศอินเดีย. NDM ทำให้ A. baumannii ดื้อต่อยาในกลุ่ม Penicillin ทั้งหมดยกเว้น Aztreonam. ยีน blaNDM-1 สามารถพบได้บนโครโมโซมและพลาสมิดส่วน ยีน blaNDM-2 ซึ่งลำดับต่างกันเพียงกรดอะมิโนเดียว ยังไม่ทราบแน่ชัดเกี่ยวกับตำแหน่งบนจีโนมแต่คาดว่าเป็นบนโครโมโซม.
- β-lactamase อื่น ๆ ที่มีความสำคัญ
- เอนไซม์ Serine β-lactamase ที่มีฤทธิ์แคบ (Narrow-spectrum Serine β-lactamase) ที่สามารถพบได้ใน A. baumannii ได้แก่ เอนไซม์ที่จัดอยู่ใน Class A ของเอนไซม์ β-lactamase ที่มักโดนคุณสมบัติของ AmpC หรือ OXA-51 บดบังเนื่องจากพบบ่อยมากกว่า อาทิ TEM-1, SCO-1, CARB-2, -4, และ -8 และเอนไซม์ที่จัดอยู่ใน Class D ของเอนไซม์ β-lactamase เช่น OXA-20, -21, และ -37.
- เอนไซม์ β-lactamase ที่มีฤทธิ์ขยาย (Extended-spectrum β-lactamase: ESBL) สามารถสลายยาในกลุ่ม Cephalosporin รุ่นที่ 4 (Fourth generation cephalosporin) แต่ไม่ใช่ Ceftazidime และ Cefotaxime. ESBL ที่สามารถพบได้ใน A. baumannii ได้แก่ เอนไซม์ที่จัดอยู่ใน Class A ของเอนไซม์ β-lactamase อาทิ PER-1, -2, -7, VEB-1, TEM-92, -116, -150, GES-11, -12, -14, CARB-10, SHV-2, -5, -12, CTX-M ที่สามารถส่งผ่านทางพลาสมิด ได้แก่ CTX-M-2, 15, และ 43 (CTX-M-2 และ -5 สามารถส่งผ่านทางทรานสโพซอน), และ KPC ต่าง ๆ และเอนไซม์ที่จัดอยู่ใน Class D ของเอนไซม์ β-lactamase เช่น OXA-2, และ -10.
การดื้อยาในกลุ่ม β-lactam ที่ไม่ได้เกิดจากเอนไซม์ β-lactamase[แก้]
- ความสามารถในการซึมผ่านเยื่อหุ้มเซลล์ (Membrane permeability)
- การดื้อยาในกลุ่ม β-lactamจากการขาดโปรตีน CarO (Carbapenem-associated Outer membrane protein) การแทรกยีน carO โดยอินเซอร์ชันซีเควนทำให้ยีนไม่สามารถทำงานได้ ส่งผลให้ A. baumannii ดื้อยาในกลุ่ม Carbapenem แม้ CarO เป็นโปรตีนช่องทางการขนส่งสารแบบไม่จำเพาะ. นอกจากนี้การลดการแสดงออกของโปรตีน CarO และ OprD-like porin ยังเกี่ยวข้องกับการลดลงของความรุนแรงในการก่อโรคของ A. baumannii สายพันธุ์ดื้อยาทุกขนาน (Pandrug-resistant A. baumannii) ซึ่งสันนิษฐานว่าเป็นสิ่งที่ต้องแลกเปลี่ยน (Fitness cost) เพื่อให้ได้คุณบัติการดื้อยา.
- การดื้อยาในกลุ่ม β-lactamจากการขาดหรือการลดการแสดงออกของโปรตีน OMP บางชนิด (22-23kDa, 33-36kDa, 37kDa, 43kDa, 44kDa, 47kDa, และ Heat-modifiable HMP-AB) การขาดโปรตีน OMP เหล่านี้ทำให้ A. baumannii สามารถดื้อต่อยาในกลุ่ม Carbapenem ได้เช่นกันโดยร่วมกับการเพิ่มการแสดงออกของเอนไซม์ β-lactamase ใน Class C หรือร่วมกับการรับยีนผลิตเอนไซม์ β-lactamase อย่าง OXA-23.
- การดื้อยาในกลุ่ม β-lactamจาก Efflux pump Resistance-nodulation-cell division (RND) efflux pump เฉพาะ AdeABC และ AdeIJK ทำให้ A. baumannii ดื้อต่อยาในกลุ่ม β-lactam แต่ไม่ทำให้ไวต่อยา Imipenem มากขึ้นเมื่อทดลองทำให้ยีน adeABC และ adeIJK ทำงานไม่ได้. นอกจากนี้เมื่อทดลองทำให้ยีน adeB ทำงานไม่ได้ทำให้ไวต่อยา Meropenem มากขึ้นแต่ไม่มีผลกับยา Imipenem เหมือนเดิม
- โปรตีนจับยาในกลุ่ม Penicillin (Penicillin-binding protein: PBP)
A. baumannii สามารถดื้อยาในกลุ่ม Carbapenem จากการเพิ่มการแสดงออกของยีนผลิต PBP ชนิดที่มีความจำเพาะกับยาต่ำหรือจากการลดการแสดงออกของยีนผลิต PBP ร่วมกับการสร้างเอนไซม์ β-lactamase หลายชนิดหรือร่วมกับการขาดโปรตีน OMP ที่มีขนาด 22.5 kDa. แต่ทั้งนี้ทั้งนั้นกลไกการดื้อที่เกี่ยวข้องกับ PBP นี้จำเป็นต้องอาศัยการเพิ่มการแสดงออกของ Efflux pump หรือการลดการแสดงออกของโปรตีน OMP แม้ว่ากลไกยังทราบแน่ชัด.
การดื้อยาในกลุ่ม Aminoglycoside[แก้]
- การดื้อยาในกลุ่ม Aminoglycoside ที่เกิดจาก Efflux pump (อยู่ในหัวข้อ การดื้อยาจาก Efflux pump)
- การดื้อยาในกลุ่ม Aminoglycoside ที่เกิดจากเอนไซม์ดัดแปลงโครงสร้างของยา (Aminoglycoside-modifying enzyme: AME)
เอนไซม์ Acetyltransferase และ Phosphotransferase สามารถดัดแปลงหมู่ Hydroxyl และ Amino ในโครงสร้างของยาในกลุ่ม Aminoglycoside ส่งผลให้ลดการจับและกับเป้าหมายของยาคือ 30s rRNA ซึ่งประกอบด้วย 16s และ 22s rRNA. เอนไซม์เหล่านี้สามารถปรากฏเป็นยีนที่อยู่บนโครโมโซมหรือพลาสมิดมากกว่า 1 ยีนเรียงกันหลายรูปแบบและเกี่ยวข้องกับอินทีกรอน Class I และรีซิสแตนซ์ไอส์แลนด์ซึ่งเน้นย้ำถึง HGT. AME สามารถถูกพบได้ใน A. baumannii เป็นยีน 2-5 ยีนเรียงตัวกันแตกต่างกันได้มากกว่า 15 รูปแบบและมักเกี่ยวข้องกับอินทีกรอน Class I เช่นกัน. นอกจากนี้ การเติมหมู่ Methyl ให้กับ 16s rRNA ซึ่งเป็นเป้าหมายของยา โดยเอนไซม์ Methyltransferase (16s rRNA methylation) จากยีน armA ทำให้ A. baumannii ดื้อต่อยาในกลุ่ม Aminoglycoside อย่าง Gentamicin, Tobramycin, และ Amikacin ในระดับสูงซึ่งมักพบร่วมกับยีน blaOXA23 อีกด้วย.
การดื้อยาในกลุ่ม Quinolone[แก้]
- การดื้อยาในกลุ่ม Quinolone ที่เกิดจาก Efflux pump (อยู่ในหัวข้อ การดื้อยาจาก Efflux pump)
- การดื้อยาในกลุ่ม Quinolone ที่เกิดจากการกลายพันธุ์ระดับนิวคลีโอไทด์ (Point mutation)
การกลายพันธุ์ระดับกรดนิวคลีโอไทด์แล้วเปลี่ยนลำดับกรดอะมิโน (amino acid substitution) บริเวณ QRDR (Quinolone-resistance determining region) ของยีน gyrA (DNA gyrase) และ parC (DNA topoisomerase IV) ทำให้ A. baumannii ดื้อต่อยาในกลุ่ม Fluoroquinolone. การเปลี่ยนแปลงลำดับกรดอะมิโนที่พบบ่อยได้แก่ S83L (กรดอะมิโน Serine ถูกเปลี่ยนเป็น Leucine ในลำดับกรดอะมิโนตำแหน่งที่ 83) ของยีน gyrA และ S80L ของยีน parC ซึ่งเมื่อพบการกลายพันธุ์ที่ยีน parC มักจะพบการกลายพันธุ์ที่ยีน gyrA ควบคู่กัน จึงเป็นนัยว่ายีน gyrA ถูกทำให้กลายพันธุ์ได้ดีกว่ายีน parC เพื่อการดื้อยาในกลุ่ม Fluoroquinolone ใน A. baumannii.
การดื้อยาในกลุ่ม Polymyxin[แก้]
- การดื้อยาในกลุ่ม Polymyxin ที่เกิดจากการดัดแปลง Lipid A ซึ่งเป็นเป้าหมายของยา
- การเติมหมู่ Phosphoethanolamine ที่หมู่ Phosphase ของ Lipid A โดยเอนไซม์ Phosphoethanolaminetransferase จากยีน pmrC. ยีน pmrC ถูกควบคุมการแสดงออกโดย pmrAB ซึ่งเป็น Two component sensor-regulator system แต่เมื่อเกิดการกลายพันธุ์ที่ pmrAB ซึงมักเกิดที่ pmrB (PmrB Sensor) ทำเกิด Autoregulation และทำให้ PmrA regulator พร้อมที่จะเป็น transcriptional factor โดยปราศจากสิ่งเร้า (Stimuli) สำหรับยีน pmrC จึงเป็นสาเหตุทำให้เพิ่มการแสดงออกของยีน pmrC ส่งผลให้ดื้อยาในกลุ่ม Polymyxin ใน A. baumannii
- การเติมหมู่ Galactosamine ที่หมู่ Phosphase ของ Lipid A สามารถเกิดขึ้นได้เช่นกัน ยีนที่เกี่ยวข้องได้แก่ naxD ซึ่งอยู่ในกระบวนการสังเคราะห์ Galactosamine และถูกควบคุมผ่านยีน pmrAB เช่นเดียวกับยีน pmrC
- การเติมหมู่ Acyl ของ Lipid A โดยเอนไซม์ Acyltransferase จากยีน lpxM สามารถทำให้เยื่อหุ้มเซลล์ทนต่อการแทรกตัวของยาในกลุ่ม Polymyxin เป็นเหตุให้ A. baumannii ดื้อยา.
- การดื้อยาในกลุ่ม Polymyxin ที่เกิดจากการกลายพันธุ์ในกลุ่มยีนในกระบวนการชีวสังเคราะห์ของ Lipid A
การกลายพันธุ์ในระดับกรดนิวคลีโอไทด์, การขาดหายบางส่วนหรือทั้งหมด, หรือการแทรกยีนโดยอินเซอร์ชั่นซีเควน ISAba11 ของยีน lpxA, lpxC, หรือ lpxD ซึ่งเป็นกลุ่มยีนในกระบวนการชีวสังเคราะห์ของ Lipid A ทำให้ A. baumannii ดื้อยาเนื่องจากไม่มี Lipid A ซึ่งเป็นเป้าหมายของยาในกลุ่ม Polymyxin บนเยื่อหุ้มเซลล์ชั้นนอก
นอกจากนี้ A. baumannii ที่ดื้อยาในกลุ่ม Polymyxin สามารถสูญเสียความสามารถ (Biological fitness) อย่างการเจริญเติบโตและลดความรุนแรงในการก่อโรคของแบคทีเรียลงได้ แต่การกลายพันธุ์ที่ช่วยบรรเทา Fitness cost (compensatory mutation) เพื่อช่วยให้ A. baumannii ที่ดื้อยายังคงมีความรุนแรงในการก่อโรคอยู่นั้นเกิดขึ้นอยู่เสมอ.
การดื้อยาจาก Efflux pump[แก้]
Efflux pump เป็นโปรตีนขนส่งสารจากภายในเซลล์ออกสู่ภายนอกเซลล์ซึ่งมักเกี่ยวข้องกับการขับยาต้านจุลชีพ ทำให้เกิดการดื้อยา. Efflux pump ในแบคทีเรียถูกแบ่งเป็น 5 family ตามความคล้ายของลำดับกรดอะมิโนได้แก่ 1. Adenosine triphosphate (ATP) -binding cassette (ABC) superfamily, 2. Multidug and toxic compound exclusion (MATE) family, 3. Small multidrug resistance (SMR) family, 4. Major facilitator superfamily (MFS), และ 5. Resistance-Nodulation-Cell Division (RND) family.
- RND family efflux pump เป็น Efflux pump ที่มีบทบาทมากที่สุดในการดื้อยาหลายขนานในแบคทีเรียแกรมลบและ A. baumannii. RND efflux pump ประกอบด้วยสามส่วน (เช่น AdeABC) คือ ส่วนที่เป็นโปรตีนขนส่ง (Transporter protein) ที่ฝังอยู่ในเยื่อหุ้มเซลล์ชั้นใน (AdeC), ช่อง OMP ที่อยู่บนเยื่อหุ้มเซลล์ชั้นนอก (AdeB), และโปรตีน (membrane fusion protein) ส่วนที่เชื่อมทั้งโปรตีนขนส่งและ OMP เข้าด้วยกันซึ่งอยู่บริเวณ Periplasmic space (AdeA). RND efflux pump ที่พบได้ใน A. baumannii มี 3 ชนิดได้แก่ AdeABC, AdeIJK, และ AdeFGH.
- AdeABC สามารถทำให้ดื้อต่อ Ethidium Bromide และดื้อต่อยา Meropenem, Erythromycin, Tetracycline, Tigecycline, Chloramphenicol, Trimethoprim, ยาในกลุ่ม Aminoglycoside (Kanamicin, Gentamicin, Tobramycin, Netilmicin, และ Amikacin), และยาในกลุ่ม Quinolone (Sparfloxacin, Ofloxacin, Perfloxacin, และ Norfloxacin). A. baumannii สายพันธุ์ทางคลิกนิกส่วนใหญ่ถูกตรวจพบ AdeABC (การตรวจยีน adeB) และมักอยู่ร่วมกับอินทีกรอน Class I โดยเฉพาะในสายพันธุ์ที่ดื้อยาซึ่งสนับสนุนข้อสันนิษฐานที่ว่า AdeABC อาจมาจาก HGT เนื่องจากพบ AdeSRABC ใน A. nosocomialis เช่นกัน.
- AdeIJK มีความเป็นพิษเมื่อถูกทำให้เพิ่มการแสดงออกมากเกินไปและถูกทดสอบว่าเกี่ยวข้องกับการดื้อยาในระดับต่ำจากภายใน (Intrinsic low-level resistance) ต่อยา Chloramphenicol, Erythromycin, Clindamycin, Tigecycline, ยาในกลุ่ม Tetracycline, และยาในกลุ่ม Fluoroquinolone คล้ายกับ AdeABC เนื่องจากความชอบสารตั้งต้นคล้ายกันแต่ไม่ใช่ยา Azithromycin และ Ethidium Bromide. นอกจากนี้ AdeIJK ค่อนข้างจำเพาะและพบได้ทุกสายพันธุ์ของ A. baumannii แต่อาจเป็น Efflux pump เดียวกับ AdeXYZ ของ A. pittii และ A. nosocomialis ซึ่งอยู่ใน A. calcoaceticus-A. baumannii complex เดียวกันเนื่องจากความเหมือนของลำดับนิวคลีโอไทด์และความคล้ายของลำดับกรดอะมิโนมีมากถึง 93 และ 99% ตามลำดับ. ยาในกลุ่ม Aminoglycoside ยังไม่ได้รับการทดสอบเนื่องจากใช้ในตัวบ่งชี้ของแบคทีเรียที่ถูกดัดแปลงพันธุกรรมเพื่อทดลองการดื้อยาดังกล่าว.
- AdeFGH ถูกทดสอบว่าเกี่ยวข้องกับการดื้อยาในระดับสูงต่อยา Chloramphenicol, Clindamycin, Trimethoprim, และยาในกลุ่ม Fluoroquinolone. นอกจากนี้ AdeFGH ทำให้เพิ่มการดื้อต่อยา Tetracycline-Tigecycline และยาในกลุ่ม Sulfonamide ยกเว้น Erythromycin, rifampin, และยาในกลุ่ม β-lactam. ยิ่งไปกว่านั้นการกลายพันธุ์ในยีน adeL ยังเกี่ยวข้องกับเพิ่มการแสดงออกของ AdeFGH เนื่องจากยีน adeL ซึ่งจะถูกแปลรหัสเป็นโปรตีน LysR-type transcriptional regulator ถูกพบอยู่ด้านต้นสายของยีน adeFGH ในทิศทางกลับ.ยาในกลุ่ม Aminoglycoside ยังไม่ได้รับการทดสอบเนื่องจากใช้ในตัวบ่งชี้ของแบคทีเรียที่ถูกดัดแปลงพันธุกรรมเพื่อทดลองการดื้อยาดังกล่าว.
- MFS efflux pump
- CraA จากยีน craA เป็น efflux pump ที่มีความจำเพาะสูงต่อยาในกลุ่ม Chloramphenicol และสามารถพบได้ทุกสายพันธุ์ของ A. baumannii จึงมีความเป็นไปได้สูงที่ที่ CraA เป็นกลไกที่ทำให้ดื้อต่อยาในกลุ่ม Chloramphenicol จากภายใน.
- AmvA จากยีน amvA เป็น efflux pump ที่เกี่ยวข้องกับนำออกของสารสี (Dye), สารฆ่าเชื้อ (Disinfectant), สารซักฟอก (Detergent) และยา erythromycin ซึ่งทำให้ลด MIC ลง 4 เท่า.
- Tet เป็น efflux pump ที่มาจากยีน tet ซึ่งรับมาจากภายนอก (HGT) โดยพลาสมิด, ทรานสโพซอน, หรือรีซิสแตนซ์ไอส์แลนด์. TetA และ TetB เป็น Tet efflux pump ที่พบได้มากที่สุดใน A. baumannii. TetA ทำให้ดื้อต่อยา Tetracycline แต่ TetB สามารถทำให้ดื้อได้ทั้ง Tetracycline และ Minocycline. ยีน tetA และ tetR (Transcriptional regulator) อยู่บนทรานสโพซอนในกลุ่มที่คล้ายกับ Tn1721 (Tn1721-like transposon) หรือรีซิสแตนซ์ไอส์แลนด์ที่มีขนาดใหญ่กว่า ในขณะที่ tetB อยู่บนพลาสมิดขนาดเล็ก (5k-9kDa) แต่พบได้บ่อยกว่าใน A. baumannii สายพันธุ์ที่ดื้อยาหลายขนาน. นอกจากนี้ยงมีรายงานเกี่ยวกับ TetM จากยีน tetM ซึ่งเกี่ยวกับการขัดขวางการจับกันระหว่างไรโบโซมและยา Tetracycline.
- MATE family efflux pump: AbeM จากยีน abeM เป็น efflux pump ที่พบได้ในทุกสายพันธุ์ของ A. baumannii ที่ขนส่งนำออกยา Chloramphenicol, Trimethoprim, ยาในกลุ่ม Aminoglycoside, ยาในกลุ่ม Fluoroquinolone, สารสี (Dye), และ Ethidium Bromide แต่ยังไม่แน่ชัดเกี่ยวกับการดื้อยาเนื่องจากยังไม่พบความสัมพันธ์กับยาเมื่อทำให้ AbeM แสดงออกมากกว่าปกติ.
- SMR family efflux pump: AbeS จากยีน abeS เป็น efflux pump ที่พบได้ในทุกสายพันธุ์ของ A. baumannii ทำให้ดื้อต่อยาหลายชนิดในระดับต่ำ (low-level resistance) เช่น Chlramphenicol, Erythromycin, Novobiocin, และยาในกลุ่ม Fluoroquinolone. นอกจากนี้ยังทำให้ดื้อต่อสารสี (Dye) และสารซักฟอก (Detergent) หลายชนิด.
ความยืดหยุ่นในการปรับแต่งจีโนม (Genome plasticity)[แก้]
A. baumannii สามารถปรับแต่งจีโนมเพื่อการอยู่รอดโดยรับ, สะสม, และแพร่กระจายยีนซึ่งมักเกี่ยวกับการทนต่อความแห้ง (desiccation), สารฆ่าเชื้อ (Disinfectant), หรือโดยเฉพาะอย่างยิ่งยาต้านจุลชีพ (Antimicrobial). ชิ้นส่วน DNA ที่เรียกว่า (Mobile) genetic element ได้แก่ อินเซอร์ชันซีเควน, ทรานสโพซอน, อินทีกรอน, พลาสมิด, และรีซิสแตนซ์ไอส์แลนด์ สามารถเป็นพาหะที่ใช้ปรับแต่งและแพร่กระจายยีนเหล่านั้น ทำให้จีโนมมีความยืดหยุ่นหรือเปลี่ยนแปลงตลอดเวลา.
อินเซอร์ชันซีเควน (Insertion sequence: IS)[แก้]
IS เป็น Mobile genetic element ที่เล็กที่สุด (<2.5Kb) ประกอบด้วยยีนเอนไซม์ Transposase สำหรับทรานสโพซิชันซึ่งขนาบข้างด้วย inverted repeat. IS จำนวนมากกว่า 30 แบบถูกพบใน A. baumannii โดยเฉพาะ ISAba1 และ ISAba125 ยกตัวอย่างเช่น A. baumannii สายพันธุ์ AYE มี ISAba1 อยู่ถึง 21 ตำแหน่งบนจีโนม. การปรากฏของ IS สามารถทำให้เกิดผลที่ตามมาได้หลายประการ. IS ที่ปรากฏทำให้เพิ่ม Promoter ให้กับยีนที่ปลายสายส่งผลให้ยีนเพิ่มการแสดงออกได้ เช่น ISAbaI ที่อยู่ต้นสายของยีน blaampC และ blaOXA-51-like ซึ่งทำให้ดื้อต่อยา Ceftazidime และยาในกลุ่ม Carbapenem ตามลำดับ. IS สามารถแทรกยีนทำสูญเสียหน้าที่ส่งผลให้ดื้อยาได้ เช่น ในกรณีของ ISAba11, การแทรกยีน lpxA หรือ lpxC ทำให้ A. baumannii ไม่สามารถสังเคราะห์ LPS ได้ส่งผลให้ไม่มีเป้าหมายของยาในกลุ่ม Polymyxin ก่อให้เกิดการดื้อยา. ยิ่งไปกว่านั้น, เมื่อ IS ที่ประกอบเป็นทรานสโพซอน (Composite transposon) สามารถเคลื่อนย้ายชุดของยีน (Gene cassette) ทั้งภายในโครโมโซม ระหว่างโครโมโซมกับพลาสมิด หรือแลกเปลี่ยนระหว่างสกุลของแบคทีเรียก็สามารถทำได้ซึ่งส่วนมากเป็นยีนดื้อยาต้านจุลชีพ เช่น ยีน ESBL blaPER-1 ที่ถูกขนาบข้างด้วย ISPa12 และ ISPa13 ประกอบกันเป็น Tn1213. แม้เพียง IS อย่างเดียวก็สามารถเคลื่อนย้ายยีนด้วยกลไก One-end transposition แม้จะพบได้ยากแต่เกิดขึ้นกับยีน CARB-10 โดย ISAba9. นอกจากนี้ IS ในกลุ่ม IS91 (รวมถึง ISCR1 และ ISCR2) สามารถย้ายตำแหน่งได้จากกลไก Rolling-cycle replication และย้ายตำแหน่งของยีนข้างเคียง (blaPER-7 สำหรับ ISCR1; blaVEB-1 สำหรับ ISCR2) เนื่องจาก Homologous recombination ระหว่าง IS.
IS ใน A. baumannii มักเกี่ยวข้องกับยีนดื้อยาต้านจุลชีพหลากหลายชนิด อาทิ
- ยีน blaOXA-23 ซึ่งถูกพบอยู่บน ISAba1 (2 ตำแหน่งภายใน Tn2006 และ Tn2009; 1 ตำแหน่งภายใน Tn2008) และ ISAba4 (1 ตำแหน่งภายใน Tn2007). blaOXA-23 ซึ่งพบอยู่บนพลาสมิดหรือโครโมโซมของ A. baumannii นี้ถูกสันนิษฐานว่ามาจากโครโมโซมของ Acinetobacter radioresistens ที่สามารถพบได้ในสิ่งแวดล้อมตามธรรมชาติ เนื่องจากพบอนุพันธุ์ (Variant) ของ blaOXA-23 ใน A. radioresistens หลายสายพันธุ์.
- ยีน blaOXA-58 ที่ถูกขนาบข้างด้วย IS ที่ต่างกันซึ่งต้นสายเป็น IS ที่เพิ่ม Promoter ให้กับยีนแต่หน้าที่สำหรับการเคลื่อนย้ายยีนยังไม่ทราบแน่ชัดแต่คาดว่าน่าจะส่งผ่านยีนทางพลาสมิดมากว่า เนื่องจาก ยีน blaOXA-58 มักปรากฏอยู่บนพลาสมิด ส่วนปลายสาย blaOXA-58 สามารถพบ ISAba3 ได้ถี่ที่สุดแต่ ISAba825, ISAba1, ISAba2, IS18, และ IS26 ก็สามารถพบได้. นอกจากนี้ยีน blaOXA-58 ที่มี ISAba3 ทั้งต้นสายและปลายสายก็สามารถพบได้เช่นกัน.
- ยีน blaCTX-M-15 ที่ขนาบข้างด้วย ISEcp1 และ IS26 ที่ไม่สมบูรณ์บนโครโมโซมแสดงถึงการส่งผ่านของยีนภายในวงศ์ Enterobacteriaceae.
- ยีน MBL blaNDM-1 และ blaNDM-2 ซึ่งพบ ISAba125 อยู่ต้นสายของ blaNDM-1 หรือขนาบข้างทั้ง blaNDM-1 และ blaNDM-2. Acinetobacter spp. อาจเป็นต้นกำเนิดของ blaNDM ที่พบในวงศ์ Enterobacteriaceae เนื่องจากมักพบ IS ที่ไม่สมบูรณ์รวมอยู่ด้วย. นอกจากนี้ ISAba125 ยังขนาบข้างยีน aphA6 ใน TnaphA6 ทำให้ดื้อต่อยาในกลุ่ม Aminoglycoside. SAba125 สามารถพบได้ทั้งบนพลาสมิดและโครโมโซม.
- ยีน tetA และ tetR ซึ่งเป็น Efflux pump ขอยาในกลุ่ม Tetracycline และ transcriptional regulator ตามลำดับ มักถูกพบภายในกลุ่มที่คล้ายกับ Tn1721 ซึ่งมักพบหลายตำแหน่งบนโครโมโซม.
- ยีน blaOXA-24/40 ที่ถูกขนาบข้างด้วย Inverted repeat ซึ่งแม้จะไม่ใช่ IS แต่ก็เป็นเป้าหมายให้เกิดการ recombination โดย XerD/XerC recombinase อย่างเจาะจง ถือว่าเป็นกลไกค่อนข้างใหม่ในการส่งผ่านยีน.
อินทีกรอน (Integron)[แก้]
อินทีกรอนโครงสร้างลำดับนิวคลีโอไทด์ที่สามารถสะสมและแลกเปลี่ยนยีนโดยใช้ Recombination อย่างเจาะจงแล้วสามารถทำให้ยีนแสดงออกได้โดยตรง. อินทีกรอนประกอบด้วยสามส่วนหลัก ได้แก่ intI เป็นบริเวณถอดรหัสเป็นเอนไซม์ Integrase สำหรับแทรก attC-gene cassette, Pc-Pint ซึ่ง Promoter Pint มีไว้สำหรับ intI ส่วน Promoter Pc มีไว้สำหรับ gene cassette และ attI ซึ่งเป็นบริเวณที่เกิดการ Recombination กับ attC และสะสมยีนต่อกันเป็น gene cassette. attC ที่ติดกับ gene cassette สามารถกลาย Circular DNA ที่เป็นอิสระจากอินทีกรอน สามารถเข้าแทรกหรือออกจากบริเวณที่เกิด recombination. อินทีกรอนจึงไม่ได้เป็น mobile genetic element โดยตรง. อินทีรอนแบ่งออกได้เป็นสองประเภทหลักตามร้อยละความเหมือนของเอนไซม์
อินทีกรอน ประเภทที่ 1 (Class 1 integron) ที่พบใน A. baumannii ส่วนใหญ่ปรากฏยีนดื้อยาในกลุ่ม Aminoglycoside, Sulfonamide, และ Antiseptic. นอกจากนี้ยังสามารถพบยีนพวก MBL ได้แก่ blaIMP, blaVIM, และ blaSIM และ Ambler class A β-lactamases บางชนิด เช่น CARB, GES, PER, VEB, และ Narrow spectrum OXA.
พลาสมิด (Plasmid)[แก้]
Conjugative plasmid เป็น Mobile genetic element ที่สามารถส่งต่อระหว่างสปีชีส์หรือระหว่างสายพันธุ์. แม้ว่า blaOXA-23 และ blaOXA-58 ใน A. baumannii จะส่งต่อทางพลาสมิดแต่ Replicon type ของพลาสมิดแตกต่างจากพลาสมิดในวงศ์ Enterbacteriaceae ซึ่งสอดคล้องกับที่ว่าแทบไม่พบยีนดื้อยาพวก ESBL หรือ KPC ปรากฏใน A. baumannii อีกทั้งยังมีกลุ่ม (2df) ของเอนไซม์ดื้อยาในกลุ่ม Carbapenem (Plasmid-borne carbapenem-hydrolyzing class D β-lactamase) เป็นของตนเองอีกด้วย.
รีซิสแตนซ์ไอส์แลนด์ (Resistance Island)[แก้]
รีซิสแตนซ์ไอส์แลนด์เป็นบริเวณหนึ่งของ DNA ซึ่งสะสมกลุ่มของยีนดื้อสารต่าง ๆ เช่น ยาปฏิชีวนะจากเหตุการณ์ HGT และมักจะสะสมที่เดิมซ้ำ ๆ บนโครโมโซมและเกี่ยวข้องกับอินเซอร์ชันซีเควน, ทรานสโพซอน, และอินทีกรอน. A. baumannii มีรีซิสแตนซ์ไอส์แลนด์มากกว่า 22 รูปแบบและเกือบทั้งหมดเกิดจากการแทรกภายในยีน comM. AbaR1 เป็นรีซิสแตนซ์ไอส์แลนด์แรกที่ถูกค้นพบใน A. baumannii (สายพันธุ์ดื้อยาหลายขนาน AYE) ที่มีความยาวถึง 86 กิโลเบสแทรกภายในยีน comM ซึ่งประกอบด้วยยีนดื้อต่อยาปฏิชีวนะ 45 ชนิดและยีนดื้อโลหะหนักและทั้งหมดถูกขนาบข้างด้วย directed repeat ของยีนทรานสโพซอนโดยสันนิษฐานซึ่งสื่อถึงเหตุการณ์ HGT. AbaR ถูกแยกเป็น 2 กลุ่มตามสายวิวัฒนาการของเชื้อ (lineage) ได้แก่ European clone I และ II. AbaR ของ European clone I อย่าง AbaR1 มียีนทรานสโพซอนโดยสันนิษฐานได้แก่ ยีน Arsenate resistance operon (arsH-BRC), Sulfate permease (sup) และ universal stress protein (uspA) และภายในยีน uspA ยังถูกแทรกด้วย Tn6018, Multiple antimicrobial resistance region (MARR), และ Tn6018 อีกซ้ำหนึ่งตามลำดับ ซึ่งยีน uspA ที่ถูกแทรกนี้เรียกรวมกันว่า Tn1069 และอาจเพิ่มอินทีกรอนประเภทที่ 1 และชุดยีนอีก 29 กิโลเบสอย่าง AbaR3 ได้ในขณะที่ European clone II ประกอบด้วย Tn6021 ตามด้วยอินทีกรอนประเภทที่ 1, Tn6021 อีกซ้ำหนึ่ง, และ Tn5395-like. Tn6021 มีความเกี่ยวข้องกับ Tn6018 เพราะมียีน uspA แต่ไม่ได้ถูกแทรกและไม่มี Tn6018 และ MARR. นอกจากนี้ยังมีข้อคิดเห็นเกี่ยวกับ AbaR ของ European clone I อาจมาจากระบบการใช้ยาช่วง ค.ศ. 1970-1989 แล้วจึงเพิ่มอินทีกรอนประเภทที่ 1 สำหรับการอยู่รอดของ A. baumannii จากระบบการใช้ยาในปัจจุบัน.
หนทางการรักษาในอนาคต[แก้]
- เนื่องจากกระบวนการผลิตยาใหม่ใช้เวลานานเป็นทศวรรษ การดัดแปลงโครงสร้างของยาต้านจุลชีพเพื่อแข่งขันกับการดื้อยาของแบคทีเรียจึงเป็นหนทางที่ง่ายกว่า เช่น UB-8902 (อนุพันธ์ของ Ciprofloxacin) ที่สามารถมีปฏิกิริยาที่ต่อ A. baumannii สายพันธุ์ดื้อยาหลายขนาน (MDR) แม้ว่ายีน gyrA กลายพันธุ์ทำให้ดื้อยาในกลุ่ม Fluoroquinolone
- การพัฒนาสารยับยั้งกลไกการดื้อยาเพื่อยืดอายุการใช้ยาต้านจุลชีพเดิมและอาจใช้ร่วมกับยาหลายชนิดในกลุ่มเดียวกัน เช่น BAL30072 ซึ่งจัดอยู่ในกลุ่ม Sulbactam ซึ่งมีปฏิกิริยาดีกว่า Meropenam และดียิ่งขึ้นเมื่อผสมกันต่อ A. baumannii สายพันธุ์ดื้อยาหลายขนาน
- การใช้ Antimicrobial peptide (AMP) แม้ว่าจะไม่เสถียรเนื่องจาก Protease ในเลือด (Blood) และน้ำเหลือง (Serum)
อ้างอิง[แก้]
- ↑ Rice, LB (Apr 15, 2008). "Federal funding for the study of antimicrobial resistance in nosocomial pathogens: no ESKAPE". The Journal of Infectious Diseases. 197 (8): 1079–81. doi:10.1086/533452. PMID 18419525.
- ↑ http://www.who.int/medicines/publications/WHO-PPL-Short_Summary_25Feb-ET_NM_WHO.pdf
- ↑ 3.0 3.1 McQueary, CN; Kirkup, BC; Si, Y; Barlow, M; Actis, LA; Craft, DW; Zurawski, DV (June 2012). "Extracellular stress and lipopolysaccharide modulate Acinetobacter baumannii surface-associated motility". Journal of Microbiology. 50 (3): 434–43. doi:10.1007/s12275-012-1555-1. PMID 22752907.
- ↑ Brisou, J., & Prevot, A. R. (1954, January). ETUDES DE SYSTEMATIQUE BACTERIENNE. 10. REVISION DES ESPECES REUNIES DANS LE GENRE ACHROMOBACTER. In Annales De L Institut Pasteur (Vol. 86, No. 6, pp. 722-728). 120 BLVD SAINT-GERMAIN, 75280 PARIS 06, FRANCE: MASSON EDITEUR.
- ↑ Bouvet, P. J., & Grimont, P. A. (1986). Taxonomy of the genus Acinetobacter with the recognition of Acinetobacter baumannii sp. nov., Acinetobacter haemolyticus sp. nov., Acinetobacter johnsonii sp. nov., and Acinetobacter junii sp. nov. and emended descriptions of Acinetobacter calcoaceticus and Acinetobacter lwoffii. International Journal of Systematic and Evolutionary Microbiology, 36 (2), 228-240.
- ↑ International Bulletin of Bacteriological Nomenclature and Taxonomy. Opinion No. 3.: The Gender of Generic Names Ending in -Bacter. Int J Syst Evol Microbiol. 1951;1 (2) :36-7.
- ↑ Ruggiero, M. A., Gordon, D. P., Orrell, T. M., Bailly, N., Bourgoin, T., Brusca, R. C., ... & Kirk, P. M. (2015). Correction: a higher level classification of all living organisms. Plos one, 10 (6), e0130114.
- ↑ Gerner-Smidt, P., Tjernberg, I., & Ursing, J. (1991). Reliability of phenotypic tests for identification of Acinetobacter species. Journal of clinical microbiology, 29 (2), 277-282.
- ↑ Cosgaya, C., Marí-Almirall, M., Van Assche, A., Fernández-Orth, D., Mosqueda, N., Telli, M., ... & Roca, I. (2016). Acinetobacter dijkshoorniae sp. nov., a member of the Acinetobacter calcoaceticus–Acinetobacter baumannii complex mainly recovered from clinical samples in different countries.International Journal of Systematic and Evolutionary Microbiology, 66 (10), 4105-4111.
- ↑ Roca I, Espinal P, Vila-Farrés X, Vila J. The Acinetobacter baumannii oxymoron: commensal hospital dweller turned pan-drug-resistant menace. Analyzing possible intersections in the resistome among human, animal and environment matrices. 2012 Apr 23:40.
- ↑ Bergogne-Berezin E, Towner KJ. Acinetobacter spp. as nosocomial pathogens: microbiological, clinical, and epidemiological features. Clinical microbiology reviews. 1996 Apr;9 (2) :148.
- ↑ Clemmer KM, Bonomo RA, Rather PN. Genetic analysis of surface motility in Acinetobacter baumannii. Microbiology. 2011 Sep 1;157 (9) :2534-44.
- ↑ Harding CM, Tracy EN, Carruthers MD, Rather PN, Actis LA, Munson RS. Acinetobacter baumannii strain M2 produces type IV pili which play a role in natural transformation and twitching motility but not surface-associated motility. MBio. 2013 Aug 30;4 (4) :e00360-13.
- ↑ Mattick JS. Type IV pili and twitching motility. Annual Reviews in Microbiology. 2002 Oct;56 (1) :289-314.
- ↑ Strom MS, Lory S. Structure-function and biogenesis of the type IV pili. Annual Reviews in Microbiology. 1993 Oct;47 (1) :565-96.
- ↑ Tomaras, Andrew P., et al. "Attachment to and biofilm formation on abiotic surfaces by Acinetobacter baumannii: involvement of a novel chaperone-usher pili assembly system." Microbiology 149.12 (2003) : 3473-3484.
- ↑ de Breij, Anna, et al. "CsuA/BABCDE-dependent pili are not involved in the adherence of Acinetobacter baumannii ATCC19606 T to human airway epithelial cells and their inflammatory response." Research in microbiology 160.3 (2009) : 213-218.
- ↑ Loehfelm, Thomas W., Nicole R. Luke, and Anthony A. Campagnari. "Identification and characterization of an Acinetobacter baumannii biofilm-associated protein." Journal of bacteriology 190.3 (2008) : 1036-1044.
- ↑ Russo, Thomas A., et al. "The K1 capsular polysaccharide of Acinetobacter baumannii strain 307-0294 is a major virulence factor." Infection and immunity 78.9 (2010) : 3993-4000.
- ↑ Choi, Alexis HK, et al. "The pgaABCD locus of Acinetobacter baumannii encodes the production of poly-β-1-6-N-acetylglucosamine, which is critical for biofilm formation." Journal of bacteriology 191.19 (2009) : 5953-5963.
- ↑ Knirel, Y. A., & Valvano, M. A. (Eds.). (2011). Bacterial lipopolysaccharides: structure, chemical synthesis, biogenesis and interaction with host cells. Springer Science & Business Media.
- ↑ GARCíA, A. P. O. L. I. N. A. R. I. A., SALGADO, F., SOLAR, H., GONZáLEZ, C. L., ZEMELMAN, R., & OñTATE, A. N. G. E. L. (1999). Some immunological properties of lipopolysaccharide from Acinetobacter baumannii. Journal of medical microbiology, 48 (5), 479-483.
- ↑ Erridge, C., Moncayo-Nieto, O. L., Morgan, R., Young, M., & Poxton, I. R. (2007). Acinetobacter baumannii lipopolysaccharides are potent stimulators of human monocyte activation via Toll-like receptor 4 signalling. Journal of medical microbiology, 56 (2), 165-171.
- ↑ Needham, B. D., & Trent, M. S. (2013). Fortifying the barrier: the impact of lipid A remodelling on bacterial pathogenesis. Nature Reviews Microbiology, 11 (7), 467-481.
- ↑ Vallenet, D., Nordmann, P., Barbe, V., Poirel, L., Mangenot, S., Bataille, E., ... & Oztas, S. (2008). Comparative analysis of Acinetobacters: three genomes for three lifestyles. PloS one, 3 (3), e1805.
- ↑ Kim, S. W., Choi, C. H., Moon, D. C., Jin, J. S., Lee, J. H., Shin, J. H., ... & Lee, J. C. (2009). Serum resistance of Acinetobacter baumannii through the binding of factor H to outer membrane proteins. FEMS microbiology letters,301 (2), 224-231.
- ↑ Choi, C. H., Lee, E. Y., Lee, Y. C., Park, T. I., Kim, H. J., Hyun, S. H., ... & Lee, J. C. (2005). Outer membrane protein 38 of Acinetobacter baumannii localizes to the mitochondria and induces apoptosis of epithelial cells. Cellular microbiology, 7 (8), 1127-1138.
- ↑ Gaddy, J. A., Tomaras, A. P., & Actis, L. A. (2009). The Acinetobacter baumannii 19606 OmpA protein plays a role in biofilm formation on abiotic surfaces and in the interaction of this pathogen with eukaryotic cells. Infection and immunity, 77 (8), 3150-3160.
- ↑ Kwon, S. O., Gho, Y. S., Lee, J. C., & Kim, S. I. (2009). Proteome analysis of outer membrane vesicles from a clinical Acinetobacter baumannii isolate.FEMS microbiology letters, 297 (2), 150-156.
- ↑ Jin, J. S., Kwon, S. O., Moon, D. C., Gurung, M., Lee, J. H., Kim, S. I., & Lee, J. C. (2011). Acinetobacter baumannii secretes cytotoxic outer membrane protein A via outer membrane vesicles. PloS one, 6 (2), e17027.
- ↑ Rumbo, C., Fernández-Moreira, E., Merino, M., Poza, M., Mendez, J. A., Soares, N. C., ... & Bou, G. (2011). Horizontal transfer of the OXA-24 carbapenemase gene via outer membrane vesicles: a new mechanism of dissemination of carbapenem resistance genes in Acinetobacter baumannii.Antimicrobial agents and chemotherapy, 55 (7), 3084-3090.
- ↑ Jacobs, A. C., Hood, I., Boyd, K. L., Olson, P. D., Morrison, J. M., Carson, S., ... & Dunman, P. M. (2010). Inactivation of phospholipase D diminishes Acinetobacter baumannii pathogenesis. Infection and immunity, 78 (5), 1952-1962.
- ↑ 33.0 33.1 Camarena, L., Bruno, V., Euskirchen, G., Poggio, S., & Snyder, M. (2010). Molecular mechanisms of ethanol-induced pathogenesis revealed by RNA-sequencing. PLoS Pathog, 6 (4), e1000834.
- ↑ 34.0 34.1 Dorsey, C. W., Tolmasky, M. E., Crosa, J. H., & Actis, L. A. (2003). Genetic organization of an Acinetobacter baumannii chromosomal region harbouring genes related to siderophore biosynthesis and transport. Microbiology, 149 (5), 1227-1238.
- ↑ Yamamoto, S., Okujo, N., & Sakakibara, Y. (1994). Isolation and structure elucidation of acinetobactin., a novel siderophore from Acinetobacter baumannii. Archives of microbiology, 162 (4), 249-254.
- ↑ 36.0 36.1 Zimbler, D. L., Penwell, W. F., Gaddy, J. A., Menke, S. M., Tomaras, A. P., Connerly, P. L., & Actis, L. A. (2009). Iron acquisition functions expressed by the human pathogen Acinetobacter baumannii. Biometals, 22 (1), 23-32.
- ↑ 37.0 37.1 37.2 Vallenet, D., Nordmann, P., Barbe, V., Poirel, L., Mangenot, S., Bataille, E., ... & Oztas, S. (2008). Comparative analysis of Acinetobacters: three genomes for three lifestyles. PloS one, 3 (3), e1805.
- ↑ 38.0 38.1 Antunes, L. C., Imperi, F., Towner, K. J., & Visca, P. (2011). Genome-assisted identification of putative iron-utilization genes in Acinetobacter baumannii and their distribution among a genotypically diverse collection of clinical isolates.Research in microbiology, 162 (3), 279-284.
- ↑ Mihara, K., Tanabe, T., Yamakawa, Y., Funahashi, T., Nakao, H., Narimatsu, S., & Yamamoto, S. (2004). Identification and transcriptional organization of a gene cluster involved in biosynthesis and transport of acinetobactin, a siderophore produced by Acinetobacter baumannii ATCC 19606T. Microbiology,150 (8), 2587-2597.
- ↑ 40.0 40.1 Whitehead, N. A., Barnard, A. M., Slater, H., Simpson, N. J., & Salmond, G. P. (2001). Quorum-sensing in Gram-negative bacteria. FEMS microbiology reviews, 25 (4), 365-404.
- ↑ Bhargava, N., Sharma, P., & Capalash, N. (2010). Quorum sensing in Acinetobacter: an emerging pathogen. Critical reviews in microbiology, 36 (4), 349-360.
- ↑ Niu, C., Clemmer, K. M., Bonomo, R. A., & Rather, P. N. (2008). Isolation and characterization of an autoinducer synthase from Acinetobacter baumannii.Journal of bacteriology, 190 (9), 3386-3392.
- ↑ Chan, K. G., Atkinson, S., Mathee, K., Sam, C. K., Chhabra, S. R., Cámara, M., ... & Williams, P. (2011). Characterization of N-acylhomoserine lactone-degrading bacteria associated with the Zingiber officinale (ginger) rhizosphere: co-existence of quorum quenching and quorum sensing in Acinetobacter and Burkholderia. BMC microbiology, 11 (1), 51.
- ↑ Rasko, D. A., & Sperandio, V. (2010). Anti-virulence strategies to combat bacteria-mediated disease. Nature reviews Drug discovery, 9 (2), 117-128.
- ↑ Smith, M. G., Des Etages, S. G., & Snyder, M. (2004). Microbial synergy via an ethanol-triggered pathway. Molecular and cellular biology, 24 (9), 3874-3884.
- ↑ Sauvage, E., Kerff, F., Terrak, M., Ayala, J. A., & Charlier, P. (2008). The penicillin-binding proteins: structure and role in peptidoglycan biosynthesis.FEMS microbiology reviews, 32 (2), 234-258.
- ↑ Russo, T. A., MacDonald, U., Beanan, J. M., Olson, R., MacDonald, I. J., Sauberan, S. L., ... & Umland, T. C. (2009). Penicillin-binding protein 7/8 contributes to the survival of Acinetobacter baumannii in vitro and in vivo.Journal of Infectious Diseases, 199 (4), 513-521.
- ↑ Smith, M. G., Gianoulis, T. A., Pukatzki, S., Mekalanos, J. J., Ornston, L. N., Gerstein, M., & Snyder, M. (2007). New insights into Acinetobacter baumannii pathogenesis revealed by high-density pyrosequencing and transposon mutagenesis. Genes & development, 21 (5), 601-614.
