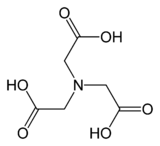
กรดไนตริโลไตรแอซีติก
| |
| ชื่อ | |
|---|---|
| Preferred IUPAC name
2,2′,2′′-Nitrilotriacetic acid[3] | |
| ชื่ออื่น | |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| 1710776 | |
| ChEBI | |
| เคมสไปเดอร์ | |
| ดรักแบงก์ | |
| ECHA InfoCard | 100.004.869 |
| EC Number |
|
| 3726 | |
| KEGG | |
| MeSH | Nitrilotriacetic+Acid |
ผับเคม CID
|
|
| RTECS number |
|
| UNII |
|
| UN number | 2811 |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| C6H9NO6 | |
| มวลโมเลกุล | 191.14 [4] |
| ลักษณะทางกายภาพ | White crystals |
| จุดหลอมเหลว | 246[4] องศาเซลเซียส (475 องศาฟาเรนไฮต์; 519 เคลวิน) |
| Insoluble. <0.01 g/100 mL at 23°C [4] | |
| อุณหเคมี | |
Std enthalpy of
formation (ΔfH⦵298) |
−1.3130–−1.3108 MJ mol−1 |
| ความอันตราย | |
| GHS labelling: | |
 
| |
| เตือน | |
| H302, H319, H351 | |
| P281, P305+P351+P338 | |
| จุดวาบไฟ | 100 องศาเซลเซียส (212 องศาฟาเรนไฮต์; 373 เคลวิน) |
| ปริมาณหรือความเข้มข้น (LD, LC): | |
LD50 (median dose)
|
1.1 g kg−1 (oral, rat) |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
alkanoic acidsที่เกี่ยวข้อง
|
|
สารประกอบที่เกี่ยวข้อง
|
|
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
กรดไนตริโลไตรแอซีติก (อังกฤษ: Nitrilotriacetic acid) เป็นกรดอะมิโนโพลีคาร์บอกซิลิกที่มีสูตร N (CH2CO2H) 3 เป็นสีที่เป็นของแข็งที่ถูกนำมาใช้เป็นตัวสารจับ ซึ่งเป็นรูปแบบสารประกอบโคออร์ดิเนชันด้วยไอออนโลหะ (คีเลต) เช่น Ca2+, Cu2+, และ Fe3+.[5]
การผลิตและใช้งาน
[แก้]สารประกอบนี้มีเชิงพาณิชย์เป็นกรดและในเกลือโซเดียม เป็นที่ผลิตจาก แอมโมเนีย, ฟอร์มาลดีไฮด์ และโซเดียมไซยาไนด์ หรือไฮโดรเจนไซยาไนด์ กำลังการผลิตทั่วโลกมีประมาณ 100,000 ตันต่อปี[6]
คุณสมบัติทางเคมีโคออร์ดิเนชัน และการประยุกต์ใช้
[แก้]การใช้ประโยชน์จาก NTA มีลักษณะที่คล้ายกับของ EDTA ทั้งสองเป็นตัวสารจับ ในทางตรงกันข้ามกับ EDTA NTA ย่อยสลายได้ง่ายและเกือบถูกเอาออกอย่างสมบูรณ์ในระหว่างการบำบัดน้ำเสีย มันจะใช้สำหรับน้ำและชะลอการทดแทนโซเดียม และโพแทสเซียมไตรฟอสเฟต ในผงซักฟอก และน้ำยาทำความสะอาด[6] NTA เป็น tripodal tetradentate trianionic ligand[7] ในห้องปฏิบัติการสารนี้จะใช้ในการไทเทรตปฏิกิริยาการเกิดสารเชิงซ้อน แตกต่างจาก NTA ที่ใช้สำหรับการแยกโปรตีนและการทำให้บริสุทธิ์ใน His-tag เมธอด การดัดแปลง NTA จะใช้ในการเคลื่อนนิกเกิลที่จะสนับสนุนให้แข็งแกร่ง ส่วนนี้จะช่วยให้การแยกของโปรตีนที่มี "แท็ก" ประกอบด้วยหกฮิสทิดีนตกค้างในปลายทางอย่างใดอย่างหนึ่ง[8]
- สารเชิงซ้อนของ NTA
-
โครงสร้าง [Ca (NTA) (H2O) 3]-.
อ้างอิง
[แก้]- ↑ "Nitrilotriacetic Acid - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information. 26 March 2005. Identification. สืบค้นเมื่อ 13 July 2012.
- ↑ Nitrilotriacetic acid
- ↑ Favre, Henri A.; Powell, Warren H. (2014). Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. pp. 21, 679. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ↑ 4.0 4.1 4.2 ChemBK Chemical Database http://www.chembk.com/en/chem/Nitrilotriacetic%20acid
- ↑ NITRILOTRIACETIC ACID AND ITS SALTS, International Agency for Research on Cancer (IARC)
- ↑ 6.0 6.1 Charalampos Gousetis, Hans-Joachim Opgenorth, "Nitrilotriacetic Acid", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a17_377
- ↑ B. L. Barnett, V. A. Uchtman "Structural investigations of calcium-binding molecules. 4. Calcium binding to aminocarboxylates. Crystal structures of Ca (CaEDTA).7H2O and Na (CaNTA) " Inorg. Chem., 1979, volume 18, pp 2674–2678. doi:10.1021/ic50200a007
- ↑ "qiaexpressionist" (PDF). คลังข้อมูลเก่าเก็บจากแหล่งเดิม (PDF)เมื่อ 2007-02-22. สืบค้นเมื่อ 2014-04-13.

![โครงสร้าง [Ca (NTA) (H2O) 3]-.](http://upload.wikimedia.org/wikipedia/commons/thumb/0/06/Calcium_complex_of_NTA_trianion.svg/252px-Calcium_complex_of_NTA_trianion.svg.png)