ซีนอนไดฟลูออไรด์

| |
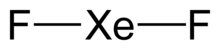
| |
| |

| |
| ชื่อ | |
|---|---|
| IUPAC names
Xenon difluoride
Xenon(II) fluoride | |
| เลขทะเบียน | |
3D model (JSmol)
|
|
| เคมสไปเดอร์ | |
| ECHA InfoCard | 100.033.850 |
ผับเคม CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| คุณสมบัติ | |
| F2Xe | |
| มวลโมเลกุล | 169.290 g·mol−1 |
| ลักษณะทางกายภาพ | ของแข็งสีขาว |
| ความหนาแน่น | 4.32 g/cm3, ของแข็ง |
| จุดหลอมเหลว | 128.6 องศาเซลเซียส (263.5 องศาฟาเรนไฮต์; 401.8 เคลวิน)[2] |
| 25 g/L (0 °C) | |
| ความดันไอ | 6.0×102 Pa[1] |
| โครงสร้าง | |
| parallel linear XeF2 units | |
| เส้นตรง | |
| 0 D | |
| อุณหเคมี | |
Std molar
entropy (S⦵298) |
254 J·mol−1·K−1[3] |
Std enthalpy of
formation (ΔfH⦵298) |
−108 kJ·mol−1[3] |
| ความอันตราย | |
| อาชีวอนามัยและความปลอดภัย (OHS/OSH): | |
อันตรายหลัก
|
กัดกร่อนเนื้อเยื่อที่สัมผัส ปล่อยสารพิษเมื่อสัมผัสกับความชื้น[5] |
| GHS labelling: | |
  
| |
| อันตราย | |
| H272, H301, H314, H330 | |
| P210, P220, P221, P260, P264, P270, P271, P280, P284, P301+P310+P330, P303+P361+P353, P304+P340+P310, P305+P351+P338, P331, P363, P370+P378, P403+P233, P405, P501[4] | |
| NFPA 704 (fire diamond) | |
| เอกสารข้อมูลความปลอดภัย (SDS) | PELCHEM MSDS |
| สารประกอบอื่นที่เกี่ยวข้องกัน | |
แอนไอออนอื่น ๆ
|
ซีนอน ไดคลอไรด์ ซีนอน ไดโบรไมด์ |
แคทไอออนอื่น ๆ
|
คริปทอนไดฟลูออไรด์ เรดอนไดฟลูออไรด์ |
สารประกอบที่เกี่ยวข้อง
|
ซีนอนเตตระฟลูออไรด์ ซีนอนเฮกซะฟลูออไรด์ |
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |
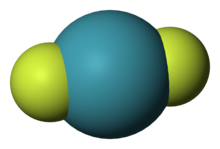
ซีนอนไดฟลูออไรด์ (อังกฤษ: Xenon difluoride) เป็นสารประกอบที่มีสูตรเคมี XeF
2 เป็นสารประกอบของซีนอนที่มีความเสถียรภาพมากที่สุดสารหนึ่ง เนื่องจากสารประกอบฟลูออไรด์อนินทรีย์ไม่สามารถใช้ร่วมกับโควาเลนต์อื่น ๆ ได้ จึงมีความไวต่อความชื้น และจะสลายตัวเมื่อสัมผัสกับแสงหรือไอน้ำ มีลักษณะเป็นผลึกแข็งสีขาวทึบ นอกจากนี้ยังมีกลิ่นเหม็นและความดันไอน้ำต่ำ[6]
อ้างอิง[แก้]
- ↑ Melita Tramšek; Boris Žemva (2006). "Synthesis, Properties and Chemistry of Xenon(II) Fluoride" (PDF). Acta Chim. Slov. 53 (2): 105–116. doi:10.1002/chin.200721209.
- ↑ Hindermann, D. K., Falconer, W. E. (1969). "Magnetic Shielding of 19F in XeF2". J. Chem. Phys. 50 (3): 1203. Bibcode:1969JChPh..50.1203H. doi:10.1063/1.1671178.
{{cite journal}}: CS1 maint: multiple names: authors list (ลิงก์) - ↑ 3.0 3.1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A23. ISBN 978-0-618-94690-7.
- ↑ "Sigma Aldrich Xenon Difluoride SDS". Sigma Aldrich. Millpore Sigma. สืบค้นเมื่อ 2 November 2022.
- ↑ "MSDS: xenon difluoride" (PDF). BOC Gases. สืบค้นเมื่อ 2010-06-01.
- ↑ James L. Weeks; Max S. Matheson (2007). Xenon Difluoride. Inorg. Synth. Inorganic Syntheses. Vol. 8. pp. 260–264. doi:10.1002/9780470132395.ch69. ISBN 9780470132395.
อ่านเพิ่ม[แก้]
- Greenwood, Norman Neill; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 894. ISBN 978-0-7506-3365-9.

