พันธะเพปไทด์
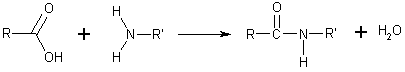


พันธะเพปไทด์ (อังกฤษ: peptide bond) หรือพันธะเอไมด์ (อังกฤษ: amide bond) เป็นพันธะเคมีชนิดพันธะโคเวเลนต์[1] ที่สร้างระหว่างหมู่คาร์บอกซิลของโมเลกุลหนึ่งกับหมู่อะมิโนของอีกโมเลกุลหนึ่ง และมีการปล่อยน้ำออกไปหนึ่งโมเลกุล จัดเป็นการสังเคราะห์แบบสูญเสียน้ำ (dehydration synthesis) และมักจะเกิดระหว่างกรดอะมิโน โมเลกุลที่เกิดใหม่เรียกว่าเอไมด์ C (=O) NH- หรือเพปไทด์
พอลิเพปไทด์และโปรตีนจะเป็นสายโซ่ของกรดอะมิโนที่เชื่อมต่อกันด้วยพันธะเพปไทด์ และเป็นองค์ประกอบหลักของพอลิเอไมด์ เช่นไนลอนและอะรามิดส์ ซึ่งเป็นพอลิเมอร์สังเคราะห์ที่มีพันธะเพปไทด์
พันธะเพปไทด์ถูกสลายได้ด้วยปฏิกิริยาเอไมด์ ไฮโดรไลซิส พันธะเพปไทด์ในโปรตีนมีความคงตัวปานกลาง หมายความว่าเมื่อมีน้ำอยู่จะสลายตัวได้ทันที ปล่อยพลังงานอิสระออกมา 10 kJ/mol แต่เกิดช้ามากในสิ่งมีชีวิต กระบวนการเกิดขึ้นด้วยการเร่งของเอนไซม์ที่ย่อยสลายพันธะเพปไทด์ ค่าการดูดกลืนแสงของเพปไทด์อยู่ที่ 190-230 nm
พันธะเพปไทด์สามารถเรียกอีกชื่อหนึ่งได้ว่า พันธะยูเพปไทด์ (eupeptide bond)[2] เพื่อให้แตกต่างจากพันธะไอโซเพปไทด์ (isopeptide bond) ที่เป็นพันธะเอไมด์อีกรูปแบบหนึ่ง ซึ่งสร้างขึ้นจากหมู่คาร์บอกซิลของกรดอะมิโนหนึ่ง กับหมู่อะมิโนของอีกโมเลกุลหนึ่ง
อ้างอิง[แก้]
- ↑ "Understanding the Types of Chemical Bonds in Proteins". ThoughtCo (ภาษาอังกฤษ). 17 Jul 2019. สืบค้นเมื่อ 21 Jun 2022.
{{cite web}}: CS1 maint: url-status (ลิงก์) - ↑ "Nomenclature and Symbolism for Amino Acids and Peptides. Recommendations 1983". European Journal of Biochemistry. 138 (1): 9–37. 1984. doi:10.1111/j.1432-1033.1984.tb07877.x. ISSN 0014-2956. PMID 6692818.
