มะเร็งเนื้อเยื่อเกี่ยวพัน
| มะเร็งเนื้อเยื่อเกี่ยวพัน Sarcoma | |
|---|---|
| ชื่ออื่น | Sarcomas, sarcomata |
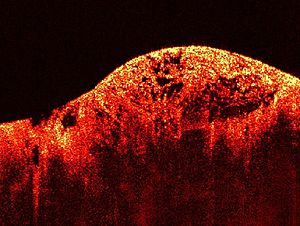 | |
| ภาพการตรวจวิเคราะห์จอประสาทตาด้วยเลเซอร์ (OCT) ของซาร์โคมา | |
| สาขาวิชา | วิทยามะเร็ง |
มะเร็งเนื้อเยื่อเกี่ยวพัน หรือ ซาร์โคมา (อังกฤษ: sarcoma) เป็นมะเร็งชนิดหนึ่งที่พัฒนามาจากเซลล์ต้นกำเนิดในเนื้อเยื่อมีเซนไคม์ (เนื้อเยื่อเกี่ยวพัน)[1][2] โดยคำว่าเนื้อเยื่อเกี่ยวพันเป็นคำที่กว้างซึ่งได้แก่ กระดูก กระดูกอ่อน เนื้อเยื่อไขมัน หลอดเลือด หรือเนื้อเยื่อของเซลล์เม็ดเลือด และซาร์โคมาสามารถพัฒนามาจากเนื้อเยื่อใด ๆ ก็ได้ดังที่กล่าวมา[2][3] เป็นผลให้ซาร์โคมามีหลายประเภท ซึ่งจะจำแนกประเภทโดยยึดหลักว่ามะเร็งนั้นมีต้นกำเนิดมาจากเนื้อเยื่อหรือเซลล์ชนิดใด[4] ซาร์โคมานั้นเป็นเนื้องอกเนื้อเยื่อเกี่ยวพันชนิดปฐมภูมิ หมายถึงพัฒนามาจากเนื้อเยื่อเกี่ยวพัน[2] แตกต่างจากเนื้องอกเนื้อเยื่อเกี่ยวพันชนิดทุตยภูมิ (หรือ "เนื้องอกที่แพร่กระจาย") ซึ่งเกิดขึ้นเมื่อมะเร็งจากที่อื่นในร่างกาย (เช่น ปอด เนื้อเยื่อเต้านม หรือต่อมลูกหมาก) แพร่กระจายมายังเนื้อเยื่อเกี่ยวพัน[5] คำว่าซาร์โคมามาจากคำของภาษากรีกโบราณ σάρκωμα sarkōma หมายถึง "เนื้อที่งอกออกมาอย่างผิดปกติ" โดย σάρξ sarx หมายถึง "เนื้อ"[6][7][8]
อ้างอิง[แก้]
- ↑ Yang J, Ren Z, Du X, Hao M, Zhou W (2014-10-27). "The role of mesenchymal stem/progenitor cells in sarcoma: update and dispute". Stem Cell Investigation. 1: 18. doi:10.3978/j.issn.2306-9759.2014.10.01. PMC 4923508. PMID 27358864.
- ↑ 2.0 2.1 2.2 Tobias J (2015). Cancer and its Management, Seventh Edition. Chichester, West Sussex, PO198SQ, UK: John Wiley & Sons, Ltd. p. 446. ISBN 9781118468753.
{{cite book}}: CS1 maint: location (ลิงก์) - ↑ DeVita Jr V (2015). DeVita, Hellman and Rosenberg's Cancer: Principles & Practice of Oncology (10th ed.). Philadelphia, PA 19103, USA: Wolters Kluwer Health. pp. 1241–1313. ISBN 978-1-4511-9294-0.
{{cite book}}: CS1 maint: location (ลิงก์) - ↑ Amin MB (2017). AJCC Cancer Staging Manual, Eight Edition. Chicago, IL 60611, USA: Springer International Publishing AG Switzerland. pp. 471–548. ISBN 978-3-319-40617-6.
{{cite book}}: CS1 maint: location (ลิงก์) - ↑ "Metastatic Cancer". National Cancer Institute (ภาษาอังกฤษ). 2015-05-12. สืบค้นเมื่อ 2019-03-22.
- ↑ σάρκωμα, σάρξ. Liddell, Henry George; Scott, Robert; A Greek–English Lexicon at Perseus Project.
- ↑ "Definition of SARCOMA". www.merriam-webster.com (ภาษาอังกฤษ). สืบค้นเมื่อ 2019-03-22.
- ↑ Harper, Douglas. "sarcoma". Online Etymology Dictionary.
แหล่งข้อมูลอื่น[แก้]
Sarcoma Cancer: Symptoms, Causes and Treatment
| การจำแนกโรค |
|---|
- Bone sarcoma at the National Cancer Institute
- มะเร็งเนื้อเยื่อเกี่ยวพัน ที่เว็บไซต์ Curlie
