ผลต่างระหว่างรุ่นของ "แบตเตอรี่"
ลไม่มีความย่อการแก้ไข |
ไม่มีความย่อการแก้ไข |
||
| บรรทัด 1: | บรรทัด 1: | ||
{{กล่องข้อมูล ชิ้นส่วนอิเล็กทรอนิกส์ |
|||
[[ไฟล์:Four AA batteries.jpg|thumb|right|250px|แบตเตอรี่แบบประจุได้ ขนาด AA]] |
|||
| name = แบตเตอรี่ |
|||
| image = File:Batteries.jpg |
|||
| image_size = 250 |
|||
| caption = รูปร่างของแบตเตอรี่แบบต่าง ๆ (บนซ้ายจนถึงล่างขวา) แบตเตอรี่แบบ AA 2 หน่วย, แบตเตอรี่แบบ D 1 หน่วย, แบตเตอรี่แบบหูหิ้ว 1 หน่วย, แบตเตอรี่แบบ 9 โวลท์ (PP3) 2 หน่วย, แบตเตอรี่แบบ AAA 2 หน่วย, แบตเตอรี่แบบ C 1 หน่วย, แบตเตอรี่ที่ใช้กับกล้องถ่ายวีดิโอ 1 หน่วย, แบตเตอรี่แบบใช้กับโทรศัพท์ในบ้าน 1 หน่วย |
|||
| type = [[แหล่งจ่ายไฟ]] |
|||
| working_principle = [[ปฏิกริยาไฟฟ้าเคมี]], [[แรงเคลื่อนไฟฟ้า]] |
|||
| invented = |
|||
| first_produced = 1800s |
|||
| symbol = [[File:Battery symbol2.svg|110px]] |
|||
| symbol_caption = สัญลักษณ์แบบอิเล็กทรอนิกส์สำหรับแบตเตอรี่ในแผนภาพวงจร |
|||
}} |
|||
'''แบตเตอรี่''' ({{lang-en|Battery}}) เป็นอุปกรณ์ที่ประกอบด้วย [[เซลล์ไฟฟ้าเคมี]] หนึ่งเซลล์หรือมากกว่า ที่มีการเชื่อมต่อภายนอกเพื่อให้กำลังงานกับอุปกรณ์ไฟฟ้า<ref>{{cite book|title=Battery Reference Book|edition=third|last=Crompton|first=T. R.|date=2000-03-20|publisher=Newnes|page=Glossary 3|isbn=0080499953|url=https://books.google.ca/books?id=QmVR7qiB5AUC&lpg=PA11&ots=ckHhIPVdcC&dq=battery%20one%20or%20more%20cells&pg=PA11#v=onepage&q&f=false|accessdate=2016-03-18}}</ref> แบตเตอรี่มี [[ขั้วบวก]] ({{lang-en|cathode}}) และ [[ขั้วลบ]] ({{lang-en|anode}}) ขั้วที่มีเครื่องหมายบวกจะมีพลังงานศักย์ไฟฟ้าสูงกว่าขั้วที่มีเครื่องหมายลบ ขั้วที่มีเครื่องหมายลบคือแหล่งที่มาของอิเล็กตรอนที่เมื่อเชื่อมต่อกับวงจรภายนอกแล้วอิเล็กตรอนเหล่านี้จะไหลและส่งมอบพลังงานให้กับอุปกรณ์ภายนอก เมื่อแบตเตอรี่เชื่อมต่อกับวงจรภายนอก สาร [[อิเล็กโทรไลต์]] มีความสามารถที่จะเคลื่อนที่โดยทำตัวเป็นไอออน ยอมให้ปฏิกิริยาทางเคมีทำงานแล้วเสร็จในขั้วไฟฟ้าที่อยู่ห่างกัน เป็นการส่งมอบพลังงานให้กับวงจรภายนอก การเคลื่อนไหวของไอออนเหล่านั้นที่อยู่ในแบตเตอรี่ที่ทำให้เกิดกระแสไหลออกจากแบตเตอรี่เพื่อปฏิบัติงาน<ref>{{cite web|url=http://www.merriam-webster.com/dictionary/battery|title=Battery - Definition of battery by Merriam-Webster|work=merriam-webster.com}}</ref> ในอดีตคำว่า "แบตเตอรี่" หมายถึงเฉพาะอุปกรณ์ที่ประกอบด้วยเซลล์หลายเซลล์ แต่การใช้งานได้มีการพัฒนาให้รวมถึงอุปกรณ์ที่ประกอบด้วยเซลล์เพียงเซลล์เดียว<ref>{{cite book|title=Batteries for Portable Devices|first=Gianfranco|last=Pistoia|date=2005-01-25|publisher=Elsevier|isbn=0080455565|page=1|url=https://books.google.ca/books?id=XMe1EnEMuMEC&lpg=PA1&dq=battery%20two%20or%20more%20cells&pg=PA1#v=onepage&q&f=false|accessdate=2016-03-18}}</ref> |
|||
แบตเตอรี่ปฐมภูมิจะถูกใช้เพียงครั้งเดียวหรือ "ใช้แล้วทิ้ง"; วัสดุที่ใช้ทำขั้วไฟฟ้าจะมีการเปลี่ยนแปลงอย่างถาวรในช่วงปล่อยประจุออก ({{lang-en|discharge}}) ตัวอย่างที่พบบ่อยก็คือ [[แบตเตอรี่อัลคาไลน์]] ที่ใช้สำหรับ [[ไฟฉาย]] และอีกหลายอุปกรณ์พกพา แบตเตอรี่ทุติยภูมิ ([[แบตเตอรี่ประจุใหม่ได้]]) สามารถดิสชาร์จและชาร์จใหม่ได้หลายครั้ง ในการนี้องค์ประกอบเดิมของขั้วไฟฟ้าสามารถเรียกคืนสภาพเดิมได้โดยกระแสย้อนกลับ ตัวอย่างเช่น [[แบตเตอรี่ตะกั่วกรด]] ที่ใช้ในยานพาหนะและแบตเตอรี่ [[ลิเธียมไอออน]] ที่ใช้สำหรับอุปกรณ์อิเล็กทรอนิกส์แบบเคลื่อนย้ายได้ |
|||
'''แบตเตอรี่''' ({{lang-en|battery}}) ในทาง[[วิทยาศาสตร์]]และ[[เทคโนโลยี]] หมายถึงอุปกรณ์อย่างหนึ่งที่ใช้เก็บ[[พลังงาน]] และนำมาใช้ได้ในรูปของ[[ไฟฟ้า]] แบตเตอรี่นั้นประกอบด้วยอุปกรณ์[[ไฟฟ้าเคมี]] เช่น [[เซลล์กัลวานิก]]หรือ[[เซลล์เชื้อเพลิง]] อย่างน้อยหนึ่งเซลล์ |
|||
แบตเตอรี่มาในหลายรูปทรงและหลายขนาด จากเซลล์ขนาดเล็กที่ให้พลังงานกับ [[เครื่องช่วยฟัง]] และนาฬิกาข้อมือ จนถึงแบตเตอรี่แบงค์ที่มีขนาดเท่าห้องที่ให้พลังงานเตรียมพร้อมสำหรับ [[ชุมสายโทรศัพท์]] และ [[ศูนย์ข้อมูล]] คอมพิวเตอร์ |
|||
เชื่อกันว่าหลักฐานชิ้นแรกสุดที่เป็นไปได้ว่าจะเป็นแบตเตอรี่ในประวัติศาสตร์โลก คือ วัตถุที่เรียกว่าแบตเตอรี่แบกแดด (Baghdad Battery) คาดว่ามีอายุในช่วง 250 ปีก่อนคริสตกาล ถึงคริสต์ศักราช 640 สำหรับพัฒนาการของแบตเตอรี่ในยุคใหม่นั้น เริ่มต้นที่ ที่พัฒนาขึ้นโดยนักฟิสิกส์ชาวอิตาลี นามว่า[[อาเลสซานโดร โวลตา]] เมื่อ [[ค.ศ. 1800]] ปัจจุบันนี้อุตสาหกรรมแบตเตอรี่ทั่วโลกสามารถสร้างรายได้จากการขายปีละ 4.8 หมื่นล้านดอลาร์สหรัฐเลยทีเดียว<ref>[http://www.dfj.com/cgi-bin/artman/publish/article_141.shtml (ประมาณการปี 2005 )]</ref> |
|||
ตามการคาดการณ์ในปี 2005 อุตสาหกรรมแบตเตอรี่ทั่วโลกสร้างมูลค่า US $48 พันล้าน ในการขายในแต่ละปี<ref>[http://www.dfj.com/cgi-bin/artman/publish/article_141.shtml Power Shift: DFJ on the lookout for more power source investments].''Draper Fisher Jurvetson''. Retrieved 20 November 2005.</ref> ด้วยการเจริญเติบโตประจำปี 6% |
|||
แบตเตอรี่มีค่า [[พลังงานเฉพาะ]] (พลังงานต่อหน่วยมวล) ต่ำกว่ามากเมื่อเทียบกับ [[เชื้อเพลิง]] ทั้งหลาย เช่นน้ำมัน แต่ก็สามารถชดเชยได้บ้างโดยประสิทธิภาพที่สูงของมอเตอร์ไฟฟ้าในการผลิตงานด้านกลไกเมื่อเทียบกับเครื่องยนต์สันดาป |
|||
== ประวัติความเป็นมา == |
|||
บทความหลัก: ประวัติความเป็นมาของแบตเตอรี่ |
|||
{{multiple image |
|||
| align = right |
|||
| direction = horizontal |
|||
| header = |
|||
| image1 = Pila di Volta.jpg |
|||
| caption1 = [[voltaic pile]] แบตเตอรี่ตัวแรก |
|||
| width1 = 90 |
|||
| image2 = Volta-and-napoleon.PNG |
|||
| caption2 = [[อาเลสซานโดร โวลตา]] กำลังสาธิตแบตเตอรี่ของเขาให้กับจักรพรรดิฝรั่งเศส [[จักรพรรดินโปเลียนที่ 3|นโปเลียน โบนาปาร์ต]] |
|||
| width2 = 195 |
|||
}} |
|||
การใช้ "แบตเตอรี่" เพื่ออธิบายกลุ่มของอุปกรณ์ไฟฟ้าสามารถย้อนหลังไปในสมัย [[เบนจามิน แฟรงคลิน]] ผู้ซึ่งในปี 1748 ได้อธิบายกลุ่มของ [[หม้อเลย์เดน]] โดยอุปมาว่าเป็น [[แบตเตอรี่ทางทหาร|แบตเตอรี่ของปืนใหญ่]]<ref>Bellis, Mary. [http://inventors.about.com/library/inventors/blbattery.htm History of the Electric Battery]. ''About.com''. Retrieved 11 August 2008.</ref> (เบนจามิน แฟรงคลิน ยืมคำว่า "แบตเตอรี่" จากกองทัพที่หมายถึงอาวุธที่ทำงานด้วยกัน<ref>{{cite web|url=http://environment.nationalgeographic.com/environment/energy/great-energy-challenge/battery-quiz/|title=Quiz: What You Don't Know About Batteries|author=National Geographic Society|work=National Geographic}}</ref>). |
|||
[[อาเลสซานโดร โวลตา]] ได้สร้างและได้อธิบายแบตเตอรี่ไฟฟ้าเคมีตัวแรก [[voltaic pile]] ในปี 1800.<ref>Bellis, Mary. [http://inventors.about.com/library/inventors/bl_Alessandro_Volta.htm Alessandro Volta – Biography of Alessandro Volta – Stored Electricity and the First Battery]. ''About.com''. Retrieved 7 August 2008.</ref> นี่เป็นชั้นซ้อนกันของแผ่นทองแดงและแผ่นสังกะสี คั่นโดยจานกระดาษชุ่มด้วยน้ำเกลือ มันสามารถผลิตกระแสที่คงที่ได้เป็นเวลานานทีเดียว โวลตาไม่ได้พอใจที่โวลเตจเกิดจากปฏิกริยาเคมี เขาคิดว่าเซลล์ของเขาเป็นแหล่งพลังงานที่ใช้ไม่หมด<ref>Stinner, Arthur. [http://home.cc.umanitoba.ca/~stinner/stinner/pdfs/2007-alessandro.pdf Alessandro Volta and Luigi Galvani] (PDF). Retrieved 11 August 2008.</ref> และการกัดกร่อนที่กระทบต่อขั้วไฟฟ้าทั้งสองเป็นเพียงสิ่งรบกวน มากกว่าจะเป็นผลตามมาที่ไม่อาจเลี่ยงได้ของการปฏิบัติงานของพวกมัน อย่างที่ [[ไมเคิล ฟาราเดย์]] แสดงให้เห็นในปี 1834.<ref>[http://www.ideafinder.com/history/inventions/battery.htm Electric Battery History – Invention of the Electric Battery]. ''The Great Idea Finder''. Retrieved 11 August 2008.</ref> |
|||
== หลักการทำงาน == |
|||
บทความหลัก: เซลล์ไฟฟ้าเคมี |
|||
[[ไฟล์:ElectrochemCell.png|thumb|เซลล์แบบโวลตา (เซลล์ที่สร้างแรงเคลื่อนไฟฟ้าโดยการแปลงที่ย้อนกลับไม่ได้จากพลังงานเคมีให้เป็นพลังงานไฟฟ้า ไม่สามารถประจุใหม่ได้) สำหรับวัตถุประสงค์เพื่อการสาธิต ในตัวอย่างนี้ครึ่ง-เซลล์สองตัวถูกเชื่อมเข้าด้วยกันโดยแผ่นคั่น [[สะพานเกลือ]] ที่ยอมให้มีการถ่ายโอนไอออนได้]] |
|||
แบตเตอรี่แปลงพลังงานเคมีให้เป็นพลังงานไฟฟ้าโดยตรง แบตเตอรี่ประกอบด้วยเซลล์แบบโวลตาได้มากกว่าหนึ่งเซลล์ แต่ละเซลล์ประกอบด้วยสอง [[ครึ่งเซลล์]] ที่เชื่อมต่อเรียงกันเป็นแถวโดยสารอิเล็กโทรไลต์ที่เป็นสื่อกระแสไฟฟ้าที่มีไอออนที่มีประจุลบ ({{lang-en|anion}}) และไอออนที่มีประจุบวก ({{lang-en|cation}}) ครึ่งเซลล์หนึ่งตัวจะมีอิเล็กโทรไลต์และขั้วลบ (อิเล็กโทรดที่แอนไอออนวิ่งเข้าหา); อีกครึ่งเซลล์หนึ่งจะมีอิเล็กโทรไลต์และขั้วบวก (อิเล็กโทรดที่แคทไอออนวิ่งเข้าหา [[Redox]] ปฏิกิริยา [[Redox]] เป็นตัวให้พลังงานกับแบตเตอรี่ แคทไอออนจะลดลง (อิเล็กตรอนมีการเพิ่ม) ที่แคโทดระหว่างการชาร์จประจุ ในขณะที่แอนไอออนจะถูกออกซิไดซ์ (อิเล็กตรอนจะถูกลบออก) ที่ขั้วบวกระหว่างการชาร์จ<ref>Dingrando 665.</ref> ในระหว่างการดีสชาร์จกระบวนการจะเป็นตรงกันข้าม ขั้วไฟฟ้าทั้งสองไม่ได้สัมผัสกัน แต่เชื่อมต่อทางไฟฟ้าโดย [[อิเล็กโทรไลต์]] เซลล์บางตัวใช้อิเล็กโทรไลต์แตกต่างกันสำหรับแต่ละครึ่งเซลล์ ตัวคั่นช่วยให้ไอออนไหลระหว่างครึ่งเซลล์ แต่จะช่วยป้องกันการผสมของอิเล็กโทรไลต์ทั้งสองด้าน |
|||
แต่ละครึ่งเซลล์มี [[แรงเคลื่อนไฟฟ้า]] (หรือ EMF) ที่กำหนดโดยความสามารถของมันในการขับกระแสไฟฟ้าจากภายในสู่ภายนอกของเซลล์ แรงเคลื่อนไฟฟ้าสุทธิของเซลล์คือความแตกต่างระหว่าง EMFs ของครึ่งเซลล์ของมัน<ref name="Saslow 338">Saslow 338.</ref> ดังนั้นหากขั้วไฟฟ้ามี EMFs = <math>\mathcal{E}_1</math> และ <math>\mathcal{E}_2</math> ดังนั้น EMF สุทธิจะเป็น <math>\mathcal{E}_{2}-\mathcal{E}_{1}</math>; พูดอีกอย่าง EMF สุทธิคือความแตกต่างระหว่าง [[Reduction potential]] ของ [[ครึ่งปฏิกิริยา]]<ref>Dingrando 666.</ref> |
|||
แรงขับไฟฟ้าหรือ <math>\displaystyle{\Delta V_{bat}}</math> ที่ตกคร่อม [[ขั้วแบตเตอรี่|ขั้ว]] ของเซลล์เรียกว่า ''แรงดันไฟฟ้า (แตกต่าง) ที่ขั้ว'' และถูกวัดเป็น [[โวลต์]]<ref name="pse943">Knight 943.</ref> แรงดันไฟฟ้าที่ขั้วของเซลล์ที่ไม่ใช่ทั้งกำลังชาร์จและดีสชาร์จเรียกว่า [[แรงดันไฟฟ้าวงจรเปิด]] และเท่ากับ emf ของเซลล์. ผลจากความต้านทานภายใน<ref name="pse976">Knight 976.</ref> แรงดันไฟฟ้าที่ขั้วของเซลล์ที่กำลังดีสชาร์จจึงมีขนาดเล็กกว่าแรงดันไฟฟ้าวงจรเปิด และแรงดันไฟฟ้าที่ขั้วของเซลล์ที่กำลังชาร์จก็จะมีมากเกินแรงดันไฟฟ้าวงจรเปิด<ref>[http://www.tiscali.co.uk/reference/encyclopaedia/hutchinson/m0030399.html Terminal Voltage – Tiscali Reference]. Originally from ''Hutchinson Encyclopaedia''. Retrieved 7 April 2007.</ref> |
|||
เซลล์ในอุดมคติจะมีความต้านทานภายในเล็กน้อยจนตัดทิ้งได้ ดังนั้นมันจึงจะรักษาระดับแรงดันที่ขั้วให้มีค่าคงที่ที่เท่ากับ <math>\mathcal{E}</math> จนหมดแรง แล้วลดลงไปอยู่ที่ศูนย์ ถ้าเซลล์ดังกล่าวสามารถรักษาระดับไว้ที่ 1.5 โวลต์และจัดเก็บประจุจำนวนหนึ่ง [[คูลอมบ์]] จากนั้นเมื่อมันดีสชาร์จอย่างสมบูรณ์ มันควรจะทำงานได้ 1.5 [[จูล]]<ref name=pse943 /> ในเซลล์ปกติ ความต้านทานภายในจะเพิ่มระหว่างการดีสชาร์จ<ref name="pse976" /> และแรงดันไฟฟ้าวงจรเปิดก็จะลดลงด้วยระหว่างการดีสชาร์จ ถ้าแรงดันไฟฟ้าและความต้านทานถูกวาดเป็นกราฟกับแกนเวลา รูปกราฟที่ได้มักจะเป็นเส้นโค้ง; รูปร่างของเส้นโค้งจะแปรไปตามคุณสมบัติทางเคมีและการจัดแจงภายใน |
|||
แรงดันไฟฟ้าที่พัฒนาขึ้นระหว่างขั้วไฟฟ้าของเซลล์จะขึ้นอยู่กับการปลดปล่อยพลังงานของปฏิกิริยาเคมีของขั้วไฟฟ้าและอิเล็กโทรไลต์ของมัน เซลล์แบบ [[แบตเตอรี่อัลคาไลน์|อัลคาไลน์]] และแบบ [[แบตเตอรี่สังกะสีคาร์บอน|สังกะสีคาร์บอน]] มีปฏิกริยาเคมีแตกต่างกัน แต่มี EMF ประมาณเดียวกันที่ 1.5 โวลต์; ในทำนองเดียวกัน เซลล์แบบ [[แบตเตอรี่นิกเกิลแคดเมียม|NiCd]] และแบบ [[แบตเตอรี่นิกเกิลโลหะไฮไดรด์|NiMH]] จะมีเคมีที่แตกต่างกัน แต่มี EMF ประมาณเดียวกันที่ 1.2 โวลต์<ref>Dingrando 674.</ref> การเปลี่ยนแปลงศักย์ไฟฟ้าเคมีที่สูงในปฏิกิริยาของสารประกอบ [[ลิเธียม]] จะเป็นผลให้เซลล์ลิเธียมมี EMF ที่ 3 โวลต์หรือมากกว่า<ref>Dingrando 677.</ref> |
|||
== ประเภทแบตเตอรี่สามัญ == |
== ประเภทแบตเตอรี่สามัญ == |
||
รุ่นแก้ไขเมื่อ 12:25, 23 มีนาคม 2559
 รูปร่างของแบตเตอรี่แบบต่าง ๆ (บนซ้ายจนถึงล่างขวา) แบตเตอรี่แบบ AA 2 หน่วย, แบตเตอรี่แบบ D 1 หน่วย, แบตเตอรี่แบบหูหิ้ว 1 หน่วย, แบตเตอรี่แบบ 9 โวลท์ (PP3) 2 หน่วย, แบตเตอรี่แบบ AAA 2 หน่วย, แบตเตอรี่แบบ C 1 หน่วย, แบตเตอรี่ที่ใช้กับกล้องถ่ายวีดิโอ 1 หน่วย, แบตเตอรี่แบบใช้กับโทรศัพท์ในบ้าน 1 หน่วย | |
| ชนิด | แหล่งจ่ายไฟ |
|---|---|
| หลักการทำงาน | ปฏิกริยาไฟฟ้าเคมี, แรงเคลื่อนไฟฟ้า |
| ผลิตครั้งแรก | 1800s |
| สัญลักษณ์ | |
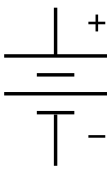 สัญลักษณ์แบบอิเล็กทรอนิกส์สำหรับแบตเตอรี่ในแผนภาพวงจร | |
แบตเตอรี่ (อังกฤษ: Battery) เป็นอุปกรณ์ที่ประกอบด้วย เซลล์ไฟฟ้าเคมี หนึ่งเซลล์หรือมากกว่า ที่มีการเชื่อมต่อภายนอกเพื่อให้กำลังงานกับอุปกรณ์ไฟฟ้า[1] แบตเตอรี่มี ขั้วบวก (อังกฤษ: cathode) และ ขั้วลบ (อังกฤษ: anode) ขั้วที่มีเครื่องหมายบวกจะมีพลังงานศักย์ไฟฟ้าสูงกว่าขั้วที่มีเครื่องหมายลบ ขั้วที่มีเครื่องหมายลบคือแหล่งที่มาของอิเล็กตรอนที่เมื่อเชื่อมต่อกับวงจรภายนอกแล้วอิเล็กตรอนเหล่านี้จะไหลและส่งมอบพลังงานให้กับอุปกรณ์ภายนอก เมื่อแบตเตอรี่เชื่อมต่อกับวงจรภายนอก สาร อิเล็กโทรไลต์ มีความสามารถที่จะเคลื่อนที่โดยทำตัวเป็นไอออน ยอมให้ปฏิกิริยาทางเคมีทำงานแล้วเสร็จในขั้วไฟฟ้าที่อยู่ห่างกัน เป็นการส่งมอบพลังงานให้กับวงจรภายนอก การเคลื่อนไหวของไอออนเหล่านั้นที่อยู่ในแบตเตอรี่ที่ทำให้เกิดกระแสไหลออกจากแบตเตอรี่เพื่อปฏิบัติงาน[2] ในอดีตคำว่า "แบตเตอรี่" หมายถึงเฉพาะอุปกรณ์ที่ประกอบด้วยเซลล์หลายเซลล์ แต่การใช้งานได้มีการพัฒนาให้รวมถึงอุปกรณ์ที่ประกอบด้วยเซลล์เพียงเซลล์เดียว[3]
แบตเตอรี่ปฐมภูมิจะถูกใช้เพียงครั้งเดียวหรือ "ใช้แล้วทิ้ง"; วัสดุที่ใช้ทำขั้วไฟฟ้าจะมีการเปลี่ยนแปลงอย่างถาวรในช่วงปล่อยประจุออก (อังกฤษ: discharge) ตัวอย่างที่พบบ่อยก็คือ แบตเตอรี่อัลคาไลน์ ที่ใช้สำหรับ ไฟฉาย และอีกหลายอุปกรณ์พกพา แบตเตอรี่ทุติยภูมิ (แบตเตอรี่ประจุใหม่ได้) สามารถดิสชาร์จและชาร์จใหม่ได้หลายครั้ง ในการนี้องค์ประกอบเดิมของขั้วไฟฟ้าสามารถเรียกคืนสภาพเดิมได้โดยกระแสย้อนกลับ ตัวอย่างเช่น แบตเตอรี่ตะกั่วกรด ที่ใช้ในยานพาหนะและแบตเตอรี่ ลิเธียมไอออน ที่ใช้สำหรับอุปกรณ์อิเล็กทรอนิกส์แบบเคลื่อนย้ายได้
แบตเตอรี่มาในหลายรูปทรงและหลายขนาด จากเซลล์ขนาดเล็กที่ให้พลังงานกับ เครื่องช่วยฟัง และนาฬิกาข้อมือ จนถึงแบตเตอรี่แบงค์ที่มีขนาดเท่าห้องที่ให้พลังงานเตรียมพร้อมสำหรับ ชุมสายโทรศัพท์ และ ศูนย์ข้อมูล คอมพิวเตอร์
ตามการคาดการณ์ในปี 2005 อุตสาหกรรมแบตเตอรี่ทั่วโลกสร้างมูลค่า US $48 พันล้าน ในการขายในแต่ละปี[4] ด้วยการเจริญเติบโตประจำปี 6%
แบตเตอรี่มีค่า พลังงานเฉพาะ (พลังงานต่อหน่วยมวล) ต่ำกว่ามากเมื่อเทียบกับ เชื้อเพลิง ทั้งหลาย เช่นน้ำมัน แต่ก็สามารถชดเชยได้บ้างโดยประสิทธิภาพที่สูงของมอเตอร์ไฟฟ้าในการผลิตงานด้านกลไกเมื่อเทียบกับเครื่องยนต์สันดาป
ประวัติความเป็นมา
บทความหลัก: ประวัติความเป็นมาของแบตเตอรี่
การใช้ "แบตเตอรี่" เพื่ออธิบายกลุ่มของอุปกรณ์ไฟฟ้าสามารถย้อนหลังไปในสมัย เบนจามิน แฟรงคลิน ผู้ซึ่งในปี 1748 ได้อธิบายกลุ่มของ หม้อเลย์เดน โดยอุปมาว่าเป็น แบตเตอรี่ของปืนใหญ่[5] (เบนจามิน แฟรงคลิน ยืมคำว่า "แบตเตอรี่" จากกองทัพที่หมายถึงอาวุธที่ทำงานด้วยกัน[6]).
อาเลสซานโดร โวลตา ได้สร้างและได้อธิบายแบตเตอรี่ไฟฟ้าเคมีตัวแรก voltaic pile ในปี 1800.[7] นี่เป็นชั้นซ้อนกันของแผ่นทองแดงและแผ่นสังกะสี คั่นโดยจานกระดาษชุ่มด้วยน้ำเกลือ มันสามารถผลิตกระแสที่คงที่ได้เป็นเวลานานทีเดียว โวลตาไม่ได้พอใจที่โวลเตจเกิดจากปฏิกริยาเคมี เขาคิดว่าเซลล์ของเขาเป็นแหล่งพลังงานที่ใช้ไม่หมด[8] และการกัดกร่อนที่กระทบต่อขั้วไฟฟ้าทั้งสองเป็นเพียงสิ่งรบกวน มากกว่าจะเป็นผลตามมาที่ไม่อาจเลี่ยงได้ของการปฏิบัติงานของพวกมัน อย่างที่ ไมเคิล ฟาราเดย์ แสดงให้เห็นในปี 1834.[9]
หลักการทำงาน
บทความหลัก: เซลล์ไฟฟ้าเคมี

แบตเตอรี่แปลงพลังงานเคมีให้เป็นพลังงานไฟฟ้าโดยตรง แบตเตอรี่ประกอบด้วยเซลล์แบบโวลตาได้มากกว่าหนึ่งเซลล์ แต่ละเซลล์ประกอบด้วยสอง ครึ่งเซลล์ ที่เชื่อมต่อเรียงกันเป็นแถวโดยสารอิเล็กโทรไลต์ที่เป็นสื่อกระแสไฟฟ้าที่มีไอออนที่มีประจุลบ (อังกฤษ: anion) และไอออนที่มีประจุบวก (อังกฤษ: cation) ครึ่งเซลล์หนึ่งตัวจะมีอิเล็กโทรไลต์และขั้วลบ (อิเล็กโทรดที่แอนไอออนวิ่งเข้าหา); อีกครึ่งเซลล์หนึ่งจะมีอิเล็กโทรไลต์และขั้วบวก (อิเล็กโทรดที่แคทไอออนวิ่งเข้าหา Redox ปฏิกิริยา Redox เป็นตัวให้พลังงานกับแบตเตอรี่ แคทไอออนจะลดลง (อิเล็กตรอนมีการเพิ่ม) ที่แคโทดระหว่างการชาร์จประจุ ในขณะที่แอนไอออนจะถูกออกซิไดซ์ (อิเล็กตรอนจะถูกลบออก) ที่ขั้วบวกระหว่างการชาร์จ[10] ในระหว่างการดีสชาร์จกระบวนการจะเป็นตรงกันข้าม ขั้วไฟฟ้าทั้งสองไม่ได้สัมผัสกัน แต่เชื่อมต่อทางไฟฟ้าโดย อิเล็กโทรไลต์ เซลล์บางตัวใช้อิเล็กโทรไลต์แตกต่างกันสำหรับแต่ละครึ่งเซลล์ ตัวคั่นช่วยให้ไอออนไหลระหว่างครึ่งเซลล์ แต่จะช่วยป้องกันการผสมของอิเล็กโทรไลต์ทั้งสองด้าน
แต่ละครึ่งเซลล์มี แรงเคลื่อนไฟฟ้า (หรือ EMF) ที่กำหนดโดยความสามารถของมันในการขับกระแสไฟฟ้าจากภายในสู่ภายนอกของเซลล์ แรงเคลื่อนไฟฟ้าสุทธิของเซลล์คือความแตกต่างระหว่าง EMFs ของครึ่งเซลล์ของมัน[11] ดังนั้นหากขั้วไฟฟ้ามี EMFs = และ ดังนั้น EMF สุทธิจะเป็น ; พูดอีกอย่าง EMF สุทธิคือความแตกต่างระหว่าง Reduction potential ของ ครึ่งปฏิกิริยา[12]
แรงขับไฟฟ้าหรือ ที่ตกคร่อม ขั้ว ของเซลล์เรียกว่า แรงดันไฟฟ้า (แตกต่าง) ที่ขั้ว และถูกวัดเป็น โวลต์[13] แรงดันไฟฟ้าที่ขั้วของเซลล์ที่ไม่ใช่ทั้งกำลังชาร์จและดีสชาร์จเรียกว่า แรงดันไฟฟ้าวงจรเปิด และเท่ากับ emf ของเซลล์. ผลจากความต้านทานภายใน[14] แรงดันไฟฟ้าที่ขั้วของเซลล์ที่กำลังดีสชาร์จจึงมีขนาดเล็กกว่าแรงดันไฟฟ้าวงจรเปิด และแรงดันไฟฟ้าที่ขั้วของเซลล์ที่กำลังชาร์จก็จะมีมากเกินแรงดันไฟฟ้าวงจรเปิด[15]
เซลล์ในอุดมคติจะมีความต้านทานภายในเล็กน้อยจนตัดทิ้งได้ ดังนั้นมันจึงจะรักษาระดับแรงดันที่ขั้วให้มีค่าคงที่ที่เท่ากับ จนหมดแรง แล้วลดลงไปอยู่ที่ศูนย์ ถ้าเซลล์ดังกล่าวสามารถรักษาระดับไว้ที่ 1.5 โวลต์และจัดเก็บประจุจำนวนหนึ่ง คูลอมบ์ จากนั้นเมื่อมันดีสชาร์จอย่างสมบูรณ์ มันควรจะทำงานได้ 1.5 จูล[13] ในเซลล์ปกติ ความต้านทานภายในจะเพิ่มระหว่างการดีสชาร์จ[14] และแรงดันไฟฟ้าวงจรเปิดก็จะลดลงด้วยระหว่างการดีสชาร์จ ถ้าแรงดันไฟฟ้าและความต้านทานถูกวาดเป็นกราฟกับแกนเวลา รูปกราฟที่ได้มักจะเป็นเส้นโค้ง; รูปร่างของเส้นโค้งจะแปรไปตามคุณสมบัติทางเคมีและการจัดแจงภายใน
แรงดันไฟฟ้าที่พัฒนาขึ้นระหว่างขั้วไฟฟ้าของเซลล์จะขึ้นอยู่กับการปลดปล่อยพลังงานของปฏิกิริยาเคมีของขั้วไฟฟ้าและอิเล็กโทรไลต์ของมัน เซลล์แบบ อัลคาไลน์ และแบบ สังกะสีคาร์บอน มีปฏิกริยาเคมีแตกต่างกัน แต่มี EMF ประมาณเดียวกันที่ 1.5 โวลต์; ในทำนองเดียวกัน เซลล์แบบ NiCd และแบบ NiMH จะมีเคมีที่แตกต่างกัน แต่มี EMF ประมาณเดียวกันที่ 1.2 โวลต์[16] การเปลี่ยนแปลงศักย์ไฟฟ้าเคมีที่สูงในปฏิกิริยาของสารประกอบ ลิเธียม จะเป็นผลให้เซลล์ลิเธียมมี EMF ที่ 3 โวลต์หรือมากกว่า[17]
ประเภทแบตเตอรี่สามัญ
แบตเตอรี่ชนิดประจุไฟฟ้าใหม่ได้ และชนิดใช้แล้วทิ้ง

จากมุมมองของผู้ใช้แบตเตอรี่แบ่งออกเป็น 2 กลุ่มใหญ่ๆ ดังนี้; แบตเตอรี่ชนิดประจุไฟฟ้าใหม่ได้ และ แบตเตอรี่ชนิดประจุไฟฟ้าใหม่ไม่ได้ (ใช้แล้วทิ้ง) ซึ่งนิยมใช้อย่างแพร่หลายทั้งสองชนิด
แบตเตอรี่ใช้แล้วทิ้งเรียกอีกอย่างว่า เซลล์ปฐมภูมิ ใช้ได้ครั้งเดียว เนื่องจากไฟฟ้าที่ได้เกิดจากการเปลี่ยนแปลงของสารเคมีเมื่อสารเคมีเปลี่ยนแปลงหมดไฟฟ้าก็จะหมดจากแบตเตอรี่ แบตเตอรี่เหล่านี้เหมาะสำหรับใช้ในอุปกรณ์ขนาดเล็กและสามารถเคลื่อนย้ายได้สะดวก ใช้ไฟน้อยหรือในที่ที่ห่างไกลจากพลังงานไฟฟ้ากระแสสลับ
ในทางตรงกันข้ามแบตเตอรี่ชนิดประจุไฟฟ้าใหม่ได้หรือ เซลล์ทุติยภูมิ สามารถประจุไฟฟ้าใหม่ได้หลังจากไฟหมดเนื่องจากสารเคมีที่ใช้ทำแบตเตอรี่ชนิดนี้สามารถทำให้กลับไปอยู่ในสภาพเดิมได้โดยการประจุไฟฟ้าเข้าไปใหม่ซึ่งอุปกรณ์ที่ใช้อัดไฟนี้เรียกว่า ชาร์เจอร์ หรือ รีชาร์เจอร์
แบตเตอรี่ชนิดประจุไฟฟ้าใหม่ได้ที่เก่าแก่ที่สุดซึ่งใช้อยู่จนกระทั่งปัจจุบันคือ "เซลล์เปียก" หรือแบตเตอรี่ตะกั่ว-กรด (lead-acid battery) แบตเตอรี่ชนิดนี้จะบรรจุในภาชนะที่ไม่ได้ปิดผนึก (unsealed container) ซึ่งแบตเตอรี่จะต้องอยู่ในตำแหน่งตั้งตลอดเวลาและต้องเป็นพื้นที่ที่ระบายอากาศได้เป็นอย่างดี เพื่อระบายก๊าซ ไฮโดรเจน ที่เกิดจากปฏิกิริยาและแบตเตอรี่ชนิดจะมีน้ำหนักมาก
รูปแบบสามัญของแบตเตอรี่ตะกั่ว-กรด คือแบตเตอรี่ รถยนต์ ซึ่งสามารถจะให้พลังงานไฟฟ้าได้ถึงประมาณ 10,000 วัตต์ในช่วงเวลาสั้นๆ และมีกระแสตั้งแต่ 450 ถึง 1100 แอมแปร์ สารละลายอิเล็กโตรไลต์ของแบตเตอรี่คือ กรดซัลฟิวริก ซึ่งสามารถเป็นอันตรายต่อผิวหนังและตาได้ แบตเตอรี่ตะกั่ว-กรดที่มีราคาแพงมากเรียกว่า แบตเตอรี่เจล (หรือ "เจลเซลล์") ภายในจะบรรจุอิเล็กโตรไลต์ประเภทเซมิ-โซลิด (semi-solid electrolyte) ที่ป้องกันการหกได้ดี และแบตเตอรี่ชนิดอัดไฟใหม่ได้ที่เคลื่อนย้ายได้สะดวกกว่าคือประเภท "เซลล์แห้ง" ที่นิยมใช้กันในโทรศัพท์มือถือและคอมพิวเตอร์โน้ตบุ๊ก เซลล์ของแบตเตอรี่ชนิดนี้คือ
- นิเกิล-แคดเมียม (NiCd) ,
- นิเกิลเมตทัลไฮไดรด์ (NiMH) ,
- ลิเทียม-ไอออน (Li-Ion)
ใช้แล้วทิ้ง
- Zinc-carbon battery
- Alkaline battery
- Silver-oxide battery
- Lithium battery
- Mercury battery
- Zinc-air battery
ชาร์จใหม่ได้
- Lead-acid battery
- lithium-ion battery
- lithium ion polymer battery
- NaS battery
- Nickel metal hydride battery
- Nickel-cadmium battery
- Sodium-metal chloride battery
- Nickel-zinc battery
ดูเพิ่ม
อ้างอิง
- ↑ Crompton, T. R. (2000-03-20). Battery Reference Book (third ed.). Newnes. p. Glossary 3. ISBN 0080499953. สืบค้นเมื่อ 2016-03-18.
- ↑ "Battery - Definition of battery by Merriam-Webster". merriam-webster.com.
- ↑ Pistoia, Gianfranco (2005-01-25). Batteries for Portable Devices. Elsevier. p. 1. ISBN 0080455565. สืบค้นเมื่อ 2016-03-18.
- ↑ Power Shift: DFJ on the lookout for more power source investments.Draper Fisher Jurvetson. Retrieved 20 November 2005.
- ↑ Bellis, Mary. History of the Electric Battery. About.com. Retrieved 11 August 2008.
- ↑ National Geographic Society. "Quiz: What You Don't Know About Batteries". National Geographic.
- ↑ Bellis, Mary. Alessandro Volta – Biography of Alessandro Volta – Stored Electricity and the First Battery. About.com. Retrieved 7 August 2008.
- ↑ Stinner, Arthur. Alessandro Volta and Luigi Galvani (PDF). Retrieved 11 August 2008.
- ↑ Electric Battery History – Invention of the Electric Battery. The Great Idea Finder. Retrieved 11 August 2008.
- ↑ Dingrando 665.
- ↑ Saslow 338.
- ↑ Dingrando 666.
- ↑ 13.0 13.1 Knight 943.
- ↑ 14.0 14.1 Knight 976.
- ↑ Terminal Voltage – Tiscali Reference. Originally from Hutchinson Encyclopaedia. Retrieved 7 April 2007.
- ↑ Dingrando 674.
- ↑ Dingrando 677.







