กลุ่มอาการกิลแลง-บาร์เร
| กลุ่มอาการกิลแลง-บาร์เร (Guillain-Barré syndrome) | |
|---|---|
| ชื่ออื่น | Guillain–Barré–Strohl syndrome, Landry's paralysis, postinfectious polyneuritis[1] |
 | |
| การออกเสียง |
|
| สาขาวิชา | ประสาทวิทยา |
| อาการ | กล้ามเนื้ออ่อนแรงเริ่มจากเท้าและมือ, มักจะมีอาการจากส่วนล่างขึ้นไปด้านบน[2] |
| ภาวะแทรกซ้อน | หายใจลำบาก, มีปัญหาเกี่ยวกับหัวใจและความดันโลหิต[1][2] |
| การตั้งต้น | เร็ว (ชั่วโมงถึงสัปดาห์)[2] |
| สาเหตุ | ไม่ทราบ[2] |
| วิธีวินิจฉัย | ขึ้นกับอาการ, ตรวจการชักนำกระแสประสาท, การเจาะเอว[2] |
| การรักษา | การดูแลแบบประคับประคอง, อิมมูโนโกลบูลินทางหลอดเลือดดำ, การแยกส่วนของน้ำเลือด |
| พยากรณ์โรค | ใช้เวลาสัปดาห์ถึงปีสำหรับการฟื้นฟู[2] |
| ความชุก | 2 ต่อ 100,000 ประชากรต่อปี[2][3] |
| การเสียชีวิต | 7.5% ของผู้ที่มีอาการ[1] |
กลุ่มอาการกิลแลง-บาร์เร[4] หรือ กลุ่มอาการกีแยง-บาร์เร[5] (อังกฤษ: Guillain–Barré syndrome) เป็นโรคแพ้ภูมิตัวเอง (autoimmune disorder) อย่างหนึ่งซึ่งเกิดกับระบบประสาทส่วนปลาย ส่วนใหญ่ถูกกระตุ้นโดยการอักเสบติดเชื้อเฉียบพลัน กลุ่มอาการนี้ตั้งชื่อตามแพทย์ชาวฝรั่งเศสชื่อ Guillain, Barré และ Strohl ซึ่งได้อธิบายกลุ่มอาการนี้ไว้ในปี ค.ศ. 1961 บางครั้งเรียกว่าอาการชาแบบแลนดรี (Landry's paralysis) ตามแพทย์ชาวฝรั่งเศสที่ได้อธิบายโรคคล้ายกันนี้ไว้ในปี ค.ศ. 1859 โรคนี้ถูกจัดอยู่ในกลุ่มพยาธิสภาพของเส้นประสาทส่วนปลาย (peripheral neuropathy) กลุ่มอาการกิลแลง-บาร์เรถูกแบ่งออกเป็นหลายประเภท แต่ส่วนใหญ่เมื่อกล่าวถึงกลุ่มอาการกิลแลง-บาร์เรจะหมายถึงประเภทที่พบบ่อยที่สุด คือประเภทที่มีพยาธิภาพของเส้นประสาทหลายเส้นแบบทำลายไมอิลินโดยการอักเสบเฉียบพลัน หรือเอไอดีพี (acute inflammatory demyelinating polyneuropathy, AIDP) กลุ่มอาการกิลแลง-บาร์เรเป็นโรคที่พบน้อยโดยมีอุบัติการณ์อยู่ที่ 1–2 ต่อ 100,000 ประชากร[6] ส่วนใหญ่อาการมักรุนแรงและปรากฏเป็นอาการอ่อนแรงแบบเป็นจากปลายมาหาต้น (ascending paralysis) โดยมีอาการอ่อนแรงของขา ค่อย ๆ ลามมายังแขนและใบหน้าพร้อมกับการหายไปของรีเฟลกซ์เอ็นลึก (deep tendon reflex) หากได้รับการรักษาอย่างทันท่วงทีด้วยการเปลี่ยนน้ำเลือด (plasmapheresis) หรือการให้อิมมูโนกลอบูลินทางหลอดเลือดดำ (intravenous immunoglobulin) ร่วมกับการรักษาประคับประคอง (supportive treatment) แล้วผู้ป่วยส่วนใหญ่สามารถกลับมาใช้ชีวิตได้ตามปกติ อย่างไรก็ดีหากมีภาวะแทรกซ้อนทางปอดรุนแรงหรือมีความผิดปกติของระบบประสาทอัตโนมัติแล้วอาจเสียชีวิตได้[7] กลุ่มอาการกิลแลง-บาร์เรเป็นหนึ่งในสาเหตุที่พบบ่อยที่สุดของการเป็นอัมพาตที่ไม่ได้เกิดจากการบาดเจ็บ
สาเหตุ[แก้]
กลุ่มอาการกิลแลง-บาร์เรทุกรูปแบบเกิดจากการตอบสนองของระบบภูมิคุ้มกันเพื่อต่อต้านแอนติเจนจากภายนอก (เช่น เชื้อโรค) แต่ภูมิคุ้มกันที่สร้างกลับไปทำลายเนื้อเยื่อประสาทของผู้ป่วยแทน ปรากฏการณ์นี้เรียกว่า "molecular mimicry" เป้าหมายที่ถูกระบบภูมิคุ้มกันทำลายเชื่อว่าเป็นสารประกอบที่พบได้เป็นปริมาณมากในเนื้อเยื่อประสาทส่วนปลายของมนุษย์ชื่อว่า แกงกลิโอไซด์ (ganglioside) เชื้อโรคที่ชักนำให้เกิดภาวะผิดปกติทางภูมิคุ้มกันดังกล่าวที่พบบ่อยที่สุดคือเชื้อแบคทีเรีย Campylobacter jejuni [8][9] รองลงมาคือเชื้อไซโตเมกาโลไวรัส (cytomegalovirus; CMV) [10] อย่างไรก็ตามมีจำนวนผู้ป่วยร้อยละ 60 ที่ไม่พบว่าเกิดจากการติดเชื้อใดนำมาก่อน ผู้ป่วยบางรายอาจเกิดการกระตุ้นจากการติดเชื้อไวรัสไข้หวัดใหญ่ หรือจากปฏิกิริยาทางภูมิคุ้มกันต่อเชื้อไวรัสไข้หวัดใหญ่[11] พบว่ามีอุบัติการณ์ของกลุ่มอาการกิลแลง-บาร์เรเพิ่มขึ้นหลังจากการให้วัคซีนไข้หวัดใหญ่ ในช่วงระหว่างการเกิดโรคไข้หวัดหมูระบาดทั่วในปี ค.ศ. 1976–1977[12] แต่จากการศึกษาทางระบาดวิทยาในภายหลังพบว่าการให้วัคซีนไข้หวัดใหญ่มีอัตราเสียงที่จะชักนำให้การเกิดกลุ่มอาการนี้เพิ่มขึ้นน้อยมาก (คือเพิ่มขึ้นน้อยกว่า 1 รายในการให้วัคซีน 1 ล้านคน) หรือแทบไม่มีความเสี่ยงเพิ่มขึ้นเลย[13][14]
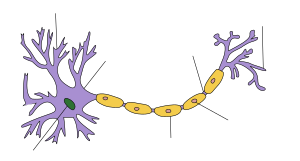
ผลจากการที่ระบบภูมิคุ้มกันเข้ามาทำลายเนื้อเยื่อประสาทส่วนปลาย ทำให้เยื่อไมอีลินซึ่งเป็นปลอกไขมันหุ้มรอบเส้นประสาทเสียหาย และทำให้การส่งกระแสประสาทถูกหยุดชะงัก และทำให้กล้ามเนื้อเป็นอัมพาต และอาจพบร่วมกับความรู้สึกสัมผัสและประสาทอัตโนมัติถูกรบกวน
ในรายที่เป็นไม่มาก แอกซอนของเส้นประสาท (ส่วนนำประสาทขาออกของเซลล์ประสาท) จะยังทำงานได้และกลับสู่สภาพปกติได้อย่างรวดเร็วถ้าเยื่อไมอีลินถูกซ่อมแซมได้เป็นปกติ ในรายที่มีอาการมากแอกซอนอาจเสียหาย และการฟื้นสภาพต้องขึ้นกับการซ่อมแซมของเยื่อไมอีลิน ประมาณร้อยละ 80 ของผู้ป่วยจะสูญเสียเยื่อไมอีลินไป อีกร้อยละ 20 จะสูญเสียแอกซอน
กลุ่มอาการกิลแลง-บาร์เรแตกต่างจากกลุ่มอาการอื่น ๆ เช่นโรคมัลติเพิล สเกลอโรซิส (multiple sclerosis; MS) หรือ อะไมโอโทรฟิก แลเทอรัล สเกลอโรซิส (Amyotrophic lateral sclerosis; ALS) ตรงที่กลุ่มอาการกิลแลง-บาร์เรเป็นโรคที่เกิดกับระบบประสาทส่วนปลาย และโดยทั่วไปแล้วจะไม่ทำความเสียหายต่อสมองหรือไขสันหลัง
ระบาดวิทยา[แก้]
อุบัติการณ์ของกลุ่มอาการกิลแลง-บาร์เรทั่วโลก ประมาณ 0.6–4 ต่อประชากร 100,000 คนต่อปี ผู้ชายเป็นมากกว่าผู้หญิง 1.5 เท่า อุบัติการณ์เพิ่มขึ้นตามอายุ ในผู้อายุต่ำกว่า 30 ปีพบประมาณ 1 รายต่อประชากร 100,000 คน และผู้อายุสูงกว่า 75 ปีพบประมาณ 4 รายต่อประชากร 100,000 คน[15] อุบัติการณ์ในระหว่างตั้งครรภ์ประมาณ 1.7 รายต่อประชากร 100,000 คน[16] มีรายงานผู้ป่วยกลุ่มอาการกิลแลง-บาร์เรแต่กำเนิดและในระยะแรกเกิด[17]
อ้างอิง[แก้]
- ↑ 1.0 1.1 1.2 Ferri FF (2016). Ferri's Clinical Advisor 2017: 5 Books in 1 (ภาษาอังกฤษ). Elsevier Health Sciences. p. 529. ISBN 9780323448383. เก็บจากแหล่งเดิมเมื่อ 2016-08-21.
- ↑ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 "Guillain–Barré Syndrome Fact Sheet". NIAMS. June 1, 2016. เก็บจากแหล่งเดิมเมื่อ 5 August 2016. สืบค้นเมื่อ 13 August 2016.
- ↑ Sejvar JJ, Baughman AL, Wise M, Morgan OW (2011). "Population incidence of Guillain-Barré syndrome: a systematic review and meta-analysis". Neuroepidemiology. 36 (2): 123–33. doi:10.1159/000324710. PMC 5703046. PMID 21422765.
- ↑ บัญชีจำแนกโรคระหว่างประเทศ ฉบับประเทศไทย (อังกฤษ-ไทย) ฉบับปี 2009. สำนักนโยบายและยุทธศาสตร์ สำนักงานปลัดกระทรวงสาธารณสุข, 2552.
- ↑ ศัพท์บัญญัติราชบัณฑิตยสถาน เก็บถาวร 2017-07-15 ที่ เวย์แบ็กแมชชีน ข้อมูลปรับปรุงวันที่ 6 สิงหาคม พ.ศ. 2544
- ↑ Mayo Clinic.com. GBS definition.. Retrieved 8-20-2009.
- ↑ U.S. National Library of Medicine. Medline Plus: "Guillain–Barré syndrome". Retrieved 8-28-2009.
- ↑ Yuki N (2008). "[Campylobacter genes responsible for the development and determinant of clinical features of Guillain-Barré syndrome]". Nippon Rinsho. Japanese Journal of Clinical Medicine (ภาษาญี่ปุ่น). 66 (6): 1205–10. PMID 18540372.
- ↑ Kuwabara S. (2004-08-10). "Does Campylobacter jejuni infection elicit "demyelinating" Guillain-Barré syndrome?". Neurology. Lippincott Williams & Wilkins. 63 (3): 529–33. PMID 15304587.
- ↑ Orlikowski D (2011). "Guillain–Barré Syndrome following Primary Cytomegalovirus Infection: A Prospective Cohort Study". Clin Infect Dis. (2011) 52 (7) : 837-844. 52 (7): 837–844. doi:10.1093/cid/cir074. PMID 21427390.
- ↑ Sivadon-Tardy V. (Jan 1, 2009). "Guillain-Barré syndrome and influenza virus infection". Clinical Infectious Diseases. The University of Chicago Press. 48 (1): 48–56. doi:10.1086/594124. PMID 19025491.
- ↑ Haber P (Nov 24, 2004). "Guillain-Barré syndrome following influenza vaccination". JAMA. 292 (20): 2478–81. PMID 15562126.
- ↑ Lehmann HC P (Sep 2010). "Guillain-Barré syndrome following influenza vaccination". Lancet Infect Dis. 10 (9): 643–51. PMID 20797646.
- ↑ Liang (2011). "Safety of Influenza A (H1N1) Vaccine in Postmarketing Surveillance in China". New England Journal of Medicine. 364: 638–647. doi:10.1056/NEJMoa1008553. PMID 21288090.
- ↑ Pithadia AB, Kakadia N. (2010). "Guillain-Barré syndrome (GBS)" (PDF). Pharmacol Rep. 62 (2): 220–32. PMID 20508277.
- ↑ Brooks, H; Christian AS; May AE (2000). "Pregnancy, anaesthesia and Guillain-Barré syndrome". Anaesthesia. 55 (9): 894–8. doi:10.1046/j.1365-2044.2000.01367.x. PMID 10947755.
- ↑ Iannello, S (2004). Guillain–Barré syndrome: Pathological, clinical and therapeutical aspects. Nova Publishers. ISBN 1594541701.
แหล่งข้อมูลอื่น[แก้]
- Mayo Clinic (2009). MayoClinic.com, Guillain-Barré
- GBS/CIDP Foundation International
- Guillain–Barré Syndrome Support Group (UK and Ireland)
- ข้อมูล เก็บถาวร 2008-08-24 ที่ เวย์แบ็กแมชชีนจากสมาคม GBS แหล่งนิวเซาท์เวลส์ (AU)
- NINDS Miller Fisher Syndrome Information Page เก็บถาวร 2010-02-27 ที่ เวย์แบ็กแมชชีน
| การจำแนกโรค | |
|---|---|
| ทรัพยากรภายนอก |
